布魯頓酪氨酸激酶抑制劑的合成的製作方法
2023-05-03 22:33:01
相關申請的交叉引用
本申請要求2015年1月14日提交的美國臨時申請號62/103,507的權益,該美國臨時申請以引用的方式整體併入本文。
背景技術:
布魯頓酪氨酸激酶(bruton′styrosinekinase,btk)是非受體酪氨酸激酶的tec家族的成員,是在除了t淋巴細胞和自然殺傷細胞之外的所有造血細胞類型中表達的一種關鍵的信號轉導酶。btk在使細胞表面b細胞受體(bcr)刺激與下遊細胞內反應相關聯的b細胞信號轉導通路中起必要的作用。
btk是b細胞發育、激活、信號轉導、以及存活的關鍵調節因子。此外,btk在許多其它造血細胞信號轉導通路中起作用,例如巨噬細胞中的toll樣受體(tlr)和細胞因子受體介導的tnf-α產生、肥大細胞中的ige受體(fcεri)信號轉導、對b譜系淋巴樣細胞中fas/apo-1細胞凋亡信號轉導的抑制、以及膠原刺激的血小板聚集。
1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼(ibrutinib))是布魯頓酪氨酸激酶(btk)抑制劑。1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮根據它的iupac名稱也被稱為1-{(3r)-3-[4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基]哌啶-1-基}丙-2-烯-1-酮或1-[(3r)-3-[4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基]-1-哌啶基-2-丙烯-1-酮,並且已經被給予usan名稱依魯替尼。對於依魯替尼所給予的各種名稱在本文可互換使用。
技術實現要素:
本文描述了btk抑制劑1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)(式(i))的合成:
在一個方面,提供了一種用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法,其中依魯替尼是式(i)的化合物,所述方法包括使式(ii)的化合物與式(iii)的化合物反應,其中x是滷素、硼酸或硼酸酯,如-b(or5)2,其中每一個r5獨立地是h或烴基,或兩個r5連同它們所連接的b原子和o原子一起形成環狀結構:
在本文所述的另一個實施方案中,使式(ii)的化合物與式(iii)的化合物在催化劑,如銅鹽存在下反應。可以利用的其它催化物質包括但不限於包含銅、鎳、鈦或鈀的催化劑,如銅、鎳、鈦或鈀的鹽、氧化物、以及絡合物。
在一些實施方案中,兩個r5一起形成亞烴基。
在一個方面,本文描述了一種用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法,其中依魯替尼是式(i)的化合物,所述方法包括使式(ii)的化合物與苯基硼酸反應:
在本文所述的另一個實施方案中,所述方法包括使式(ii)的化合物與苯基硼酸在催化劑(如銅鹽(例如乙酸銅(ii)))和鹼存在下反應。在一些實施方案中,所述鹼是無機鹼,如moh、m2co3(其中m選自鋰、鈉、鉀、以及銫)、caco3、二元磷酸鹽和三元磷酸鹽(例如m3po4、m2hpo4)或碳酸氫鹽(mhco3)。在一些實施方案中,所述鹼是有機鹼,如三取代的胺、吡啶或4-二甲基氨基吡啶。在一些實施方案中,所述鹼是nr1r2r3,其中r1、r2以及r3各自獨立地是c1-c6烴基,如三乙胺。
在另一個方面,本文描述了一種用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法,其中依魯替尼是式(i)的化合物,所述方法包括使式(ii)的化合物與式(iii)的化合物反應,其中x是滷素:
在本文所述的另一個實施方案中,所述方法包括使式(ii)的化合物與式(iii)的化合物在催化劑(如銅鹽(例如乙酸銅(ii)))和鹼存在下反應,其中x是滷素。在一些實施方案中,所述鹼是無機鹼,如moh、m2co3(其中m選自鋰、鈉、鉀、以及銫)、caco3、二元磷酸鹽和三元磷酸鹽(例如m3po4、m2hpo4)或碳酸氫鹽(mhco3)。在一些實施方案中,所述鹼是有機鹼,如三取代的胺、吡啶或4-二甲基氨基吡啶。在一些實施方案中,所述鹼是nr1r2r3,其中r1、r2以及r3各自獨立地是c1-c6烴基,如三乙胺。可以利用的其它催化物質包括但不限於銅、鎳、鈦或鈀的鹽、氧化物、以及絡合物。
在另一個方面,本文描述了一種用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法,其中依魯替尼是式(i)的化合物,所述方法包括使式(iv)的化合物與苯酚反應,其中x是滷素:
在本文所述的另一個實施方案中,所述方法包括使式(iv)的化合物與苯酚在催化劑(如銅鹽(例如乙酸銅(ii)))和鹼存在下反應,其中x是滷素。在一些實施方案中,所述鹼是無機鹼,如moh、m2co3(其中m選自鋰、鈉、鉀、以及銫)、caco3、二元磷酸鹽和三元磷酸鹽(例如m3po4、m2hpo4)或碳酸氫鹽(mhco3)。在一些實施方案中,所述鹼是有機鹼,如三取代的胺、吡啶或4-二甲基氨基吡啶。在一些實施方案中,所述鹼是nr1r2r3,其中r1、r2以及r3各自獨立地是c1-c6烴基,如三乙胺。可以利用的其它催化物質包括但不限於銅、鎳、鈦或鈀的鹽、氧化物、以及絡合物。
在另一個方面,本文描述了一種用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法,其中依魯替尼是式(i)的化合物,所述方法包括使式(v)的化合物與氨反應,其中l是離去基:
在一些實施方案中,l是滷素、羥基、烴氧基、-p(=o)r62(其中r6獨立地是oh、or7(r7是烴基)或滷代(例如cl))、甲烷磺酸酯基(甲磺酸酯基)或三氟甲烷磺酸酯基。在本文所述的另一個實施方案中,所述方法包括使式(v)的化合物與氨反應,其中l是滷素、羥基、烴氧基、或三氟甲烷磺酸酯基。在另一個實施方案中,l是二氯磷酸酯基(-p(=o)cl2)。
在另一個方面,本文描述了一種用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法,其中依魯替尼是式(i)的化合物,所述方法包括將式(vi)的化合物還原:
在本文所述的另一個實施方案中,所述方法包括通過催化氫化將式(vi)的化合物還原。
在另一個方面,本文描述了一種用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法,其中依魯替尼是式(i)的化合物,所述方法包括將式(vii)的化合物還原,其中z是滷素或三氟甲烷磺酸酯基:
在另一個方面,本文描述了一種用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法,其中依魯替尼是式(i)的化合物,所述方法包括將式(viii)的化合物還原,其中z是滷素或三氟甲烷磺酸酯基:
在另一個方面,本文描述了一種用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法,其中依魯替尼是式(i)的化合物,所述方法包括使其中x是滷素或磺酸酯基的式(ix)的化合物與其中y是烴基錫、硼酸或硼酸酯的式(x)的化合物反應:
在另一個方面,本文描述了一種用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法,其中依魯替尼是式(i)的化合物,所述方法包括使其中y是烴基錫、硼酸或硼酸酯的式(xi)的化合物與其中x是滷素或磺酸酯基的式(xii)的化合物反應:
在另一個方面,本文描述了一種用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法,其中依魯替尼是式(i)的化合物,所述方法包括使式(xia)的化合物,其中pg是h或保護基,如co-w,w是烴基、滷化烴基(如cf3)、烴氧基、二烴基氨基(nr1r2,其中r1和r2各自獨立地是c1-c6烴基);與式(xiia)的化合物反應,其中x是滷素或磺酸酯基、oso2r、b(or)2、n2+(重氮)、或so2r,其中r獨立地是c1-c6烴基、c1-c6滷代烴基、芳基或芳基烴基:
在另一個方面,本文描述了一種用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法,其中依魯替尼是式(i)的化合物,所述方法包括將式(xiii)的化合物還原:
在另一個方面,本文描述了一種用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法,其中依魯替尼是式(i)的化合物,所述方法包括將式(xiv)的化合物脫保護,其中pg是氨基保護基:
在本文所述的另一個實施方案中,所述方法包括將式(xiv)的化合物脫保護,其中pg是苯甲基、氨基甲酸苯甲酯、或氨基甲酸叔丁酯。
在另一個方面,本文描述了一種用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法,其中依魯替尼是式(i)的化合物,所述方法包括使式(xv)的化合物與式(xvi)的化合物反應,其中x是羥基、滷素、或磺酸酯基:
在另一個方面,本文描述了一種用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法,其中依魯替尼是式(i)的化合物,所述方法包括對式(xvii)的化合物進行β-消除,其中l是離去基:
在本文所述的另一個實施方案中,所述方法包括對式(xvii)的化合物進行β-消除,其中l是滷素、羥基、烴氧基、甲烷磺酸酯基、或三氟甲烷磺酸酯基。
在另一個方面,本文描述了一種用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法,其中依魯替尼是式(i)的化合物,所述方法包括對式(xviii)的化合物進行β-消除,其中l是離去基:
在本文所述的另一個實施方案中,所述方法包括對式(xviii)的化合物進行β-消除,其中l是滷素、羥基、烴氧基、甲烷磺酸酯基或三氟甲烷磺酸酯基。
在另一個方面,本文描述了一種用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法,其中依魯替尼是式(i)的化合物,所述方法包括使式(xix)的化合物與三苯基膦和甲醛反應,其中x是滷素:
在另一個方面,本文描述了一種用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法,其中依魯替尼是式(i)的化合物,所述方法包括使其中x是滷素的式(xx)的化合物與其中y是烴基錫、硼酸或硼酸酯的式(xxi)的化合物反應:
在另一個方面,本文描述了一種用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法,其中依魯替尼是式(i)的化合物,所述方法包括將式(xxii)的化合物氫化:
其中表示式(xxiia)-(xxiig)的化合物:
或其組合。
在另一個方面,本文描述了一種用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法,其中依魯替尼是式(i)的化合物,所述方法包括使式(xxiii)的化合物與甲醯胺、甲酸銨、原甲酸三甲酯和氨、或甲脒或其鹽,如鹽酸鹽或乙酸鹽縮合:
在另一個方面,本文描述了一種用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法,其中依魯替尼是式(i)的化合物,所述方法包括使式(xxiv)的化合物與式(xxv)的化合物反應,其中x是離去基:
在式(xxiv)的一些實施方案中,x是滷素、羥基、烴氧基、-p(=o)r6(其中r6獨立地是oh、or7(r7是烴基)或滷代(例如cl))、甲烷磺酸酯基或三氟甲烷磺酸酯基。在式(xxiv)的一些實施方案中,x是滷素、羥基、烴氧基、或三氟甲烷磺酸酯基。在式(xxiv)的一些實施方案中,x是滷素。在式(xxiv)的一些實施方案中,x是二氯磷酸酯基。
在另一個方面,本文描述了一種用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法,其中依魯替尼是式(i)的化合物,所述方法包括使式(xxvi)的化合物與丙烯醯胺反應,其中x是離去基,如滷素或磺酸酯基:
在式(xxvi)的一些實施方案中,x是滷素、羥基、烴氧基、-p(=o)r6(其中r6獨立地是oh、or7(r7是烴基)或滷代(例如cl))、甲烷磺酸酯基或三氟甲烷磺酸酯基。在式(xxvi)的一些實施方案中,x是滷素、羥基、烴氧基、或三氟甲烷磺酸酯基。在式(xxvi)的一些實施方案中,x是滷素。在式(xxvi)的一些實施方案中,x是二氯磷酸酯基。
在另一個方面,本文描述了一種用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法,其中依魯替尼是式(i)的化合物,所述方法包括使式(xxvii)的化合物與式(xxviii)的化合物反應,其中x是離去基,如羥基、烴氧基、滷素、磺酸酯基或二烴氧基-磷醯基(p(=o)(or4)2(每一個r4獨立地是烴基,例如me或et)):
在一些實施方案中,x不是cl。
在另一個方面,提供了用於上述方法中的任一種的中間體。
以引用的方式併入
本說明書中所提到的所有出版物和專利申請以引用的方式併入本文達到適用和相關的程度。
附圖說明
圖1描繪了化合物xvii-1的1hnmr。
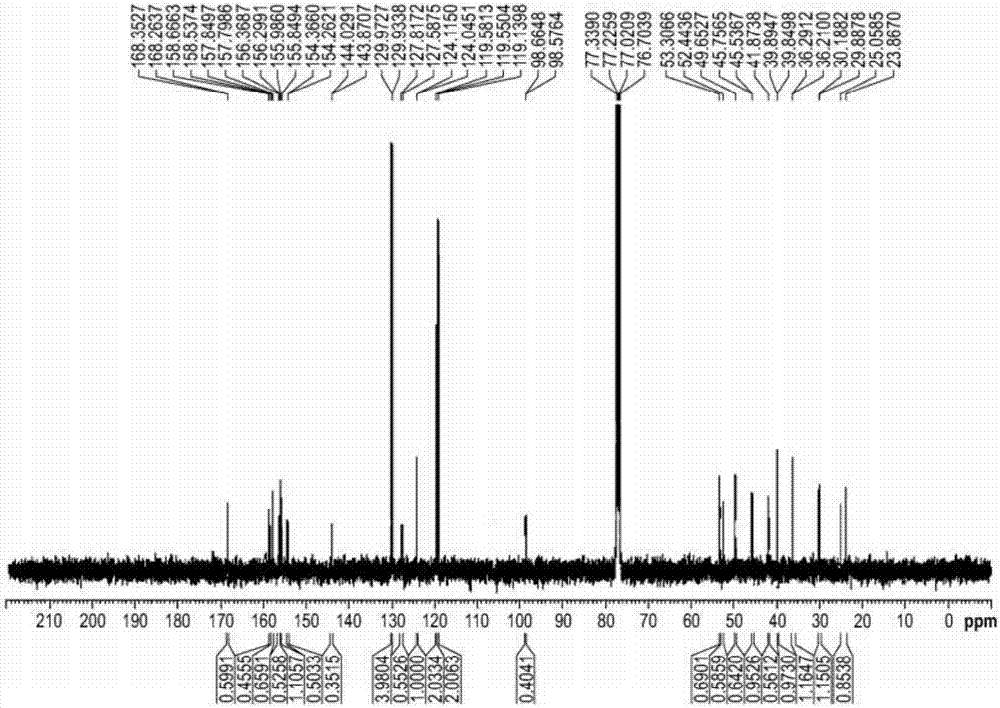
圖2描繪了化合物xvii-1的13cnmr。
圖3、圖4以及圖5描繪了化合物xvii-1的nmrnoe(核極化效應)。
圖6、圖7、圖8以及圖9描繪了化合物xvii-1的nmrhmbc(異核多鍵相關光譜學)。
具體實施方式
某些術語
除非另外定義,否則本文所用的所有技術術語和科學術語所具有的含義與要求保護的主題所屬領域的技術人員通常所了解的含義相同。應當理解的是,上述一般說明和以下詳細說明僅僅是示例性的和說明性的而不限制要求保護的任何主題。在本申請中,除非另外具體說明,否則使用單數時,包括複數。必須指出的是,除非上下文另外明確規定,否則如說明書和所附權利要求書中所用的單數形式「一個/種(a/an)」和「所述」包括複數指代對象。在本申請中,除非另外說明,否則使用「或」時,意指「和/或」。此外,術語「包括(including)」以及其它形式,如「包括(include)」、「包括(includes)」以及「包括(included)」的使用不具限制性。
本文所用的部分標題僅用於組織目的並且不應當被視為限制所述的主題。本申請中所引用的所有文件、或文件的部分,包括但不限於專利、專利申請、文章、書籍、手冊、以及論文在此明確地以引用的方式整體併入本文用於任何目的。
「烴基」指的是脂族烴基。烴基部分可以是「飽和烴基」,這意指它不含任何烯烴或炔烴部分。烴基部分也可以是「不飽和烴基」部分,這意指它含有至少一個烯烴或炔烴部分。「烯烴」部分指的是具有至少一個碳-碳雙鍵的基團,並且「炔烴」部分指的是具有至少一個碳-碳三鍵的基團。烴基部分,無論是飽和的還是不飽和的,均可以是支鏈的、直鏈的或環狀的。根據結構,烴基可以是單價基團或二價基團(即亞烴基)。烴基也可以是具有1個至6個碳原子的「低級烴基」。
如本文所用的c1-cx包括c1-c2、c1-c3……c1-cx。
「烴基」部分可以具有1個至10個碳原子(在它在本文出現時,諸如「1個至10個」的數值範圍指的是給定範圍內的每一個整數;例如「1個至10個碳原子」意指烴基可以具有1個碳原子、2個碳原子、3個碳原子等,最多並且包括10個碳原子,儘管本定義還涵蓋了其中沒有指定數值範圍的術語「烴基」的出現)。本文所述的化合物的烴基可以被命名為「c1-c4烴基」或類似的名稱。僅舉例來說,「c1-c4烴基」表示在烴基鏈中存在一個至四個碳原子,即所述烴基鏈選自甲基、乙基、丙基、異丙基、正丁基、異丁基、仲丁基、以及叔丁基。因此,c1-c4烴基包括c1-c2烴基和c1-c3烴基。烴基可以是取代的或未取代的。典型的烴基包括但決不限於甲基、乙基、丙基、異丙基、丁基、異丁基、叔丁基、戊基、己基、乙烯基、丙烯基、丁烯基、環丙基、環丁基、環戊基、環己基等。
「烴氧基」指的是(烴基)o-基團,其中烴基如本文所定義。
如本文所用的術語「芳基」指的是芳環,其中形成所述環的原子中的每一個均是碳原子。芳環可以由五個、六個、七個、八個、九個、或多於九個碳原子形成。芳基可以是任選取代的。芳基的實例包括但不限於苯基、萘基、菲基、蒽基、芴基、以及茚基。根據結構,芳基可以是單價基團或二價基團(即亞芳基)。
術語「滷代」或可替代地「滷素」或「滷基」意指氟、氯、溴以及碘。
「磺酸酯基」指的是-os(=o)2-r,其中r是任選取代的烴基或任選取代的芳基。
術語「任選取代的」或「取代的」意指所提到的基團可以被單獨地和獨立地選自以下各項的一個或多個另外的基團取代:烴基、環烴基、芳基、雜芳基、雜脂環、羥基、烴氧基、芳氧基、烴硫基、芳基硫基、烴基亞碸、芳基亞碸、烴基碸、芳基碸、氰基、滷代、醯基、硝基、滷代烴基、氟代烴基、氨基(包括單取代和二取代的氨基)、以及其受保護的衍生物。舉例來說,任選的取代基可以是lsrs,其中每一個ls獨立地選自化學鍵、-o-、-c(=o)-、-s-、-s(=o)-、-s(=o)2-、-nh-、-nhc(o)-、-c(o)nh-、s(=o)2nh-、-nhs(=o)2、-oc(o)nh-、-nhc(o)o-、-(取代或未取代的c1-c6烴基)、或-(取代或未取代的c2-c6烯基);並且每一個rs獨立地選自h、(取代或未取代的c1-c4烴基)、(取代或未取代的c3-c6環烴基)、雜芳基、或雜烴基。
術語「離去基」指的是在鍵斷裂中,例如在取代或消除反應中作為穩定物質攜帶成鍵電子離開的原子或化學部分。離去基一般是本領域已知的。離去基的實例包括但不限於,滷素,如cl、br、以及i;磺酸酯基,如甲苯磺酸酯基、甲烷磺酸酯基(甲磺酸酯基)、三氟甲烷磺酸酯基(三氟甲磺酸酯基)、羥基、烴氧基、磷酸酯基、取代的磷酸酯基、或二烴氧基-磷醯基。在一些實施方案中,離去基是oso2r、b(or)2、n2+(重氮)、或so2r,其中r獨立地是c1-c6烴基、c1-c6滷代烴基、芳基或芳基烴基。
如本文所用的術語「可接受的」或「藥學上可接受的」對於製劑、組合物或成分來說意指對接受治療的受試者的一般健康情況沒有持續的有害作用或不會消除化合物的生物活性或特性,並且是相對無毒的。
如本文所用的術語「布魯頓酪氨酸激酶」指的是來自智人的布魯頓酪氨酸激酶,如例如美國專利號6,326,469中所公開(基因庫登錄號np_000052)。
如本文所用的術語「分離」指的是從不關注的組分分離和取出所關注的組分。分離的物質可以呈乾燥或半乾的狀態,或呈溶液形式,包括但不限於水溶液。分離的組分可以呈均勻的狀態或分離的組分可以是藥物組合物的一部分,所述藥物組合物包含另外的藥學上可接受的載體和/或賦形劑。僅舉例來說,當核酸或蛋白質不含在天然狀態下與它締合的細胞組分中的至少一些或核酸或蛋白質已經被濃縮到大於它在體內或體外產生的濃度的水平時,這樣的核酸或蛋白質是「分離的」。此外,舉例來說,當與側接基因並且編碼除所關注的基因以外的蛋白質的開放閱讀框分離時,所述基因是分離的。
在本文提到時術語「基本上」例如在「基本上分離的形式」的背景下指的是大於50%,或在一個實施方案中,大於80%,如大於90%,或在另一個實施方案中,大於95%(例如大於98%)。舉例來說,在分離形式的背景下,這意指所分離的材料的大於50%(以重量計)含有所期望的材料,或在其它實施方案中,大於80%、90%、95%或98%(以重量計)。
合成途徑
在一些實施方案中,本文所述的方法是使用化學文獻中所述的手段、使用本文所述的方法、或通過其組合來實現的。此外,本文所提供的溶劑、溫度以及其它反應條件可以變化。
在其它實施方案中,用於合成本文所述的化合物的起始材料和試劑是合成的或從商業來源獲得的,諸如但不限於西格瑪-奧德裡奇公司(sigma-aldrich)、飛世爾科技公司(fischerscientific)(飛世爾化學品公司(fischerchemicals))、以及阿科斯有機品公司(acrosorganics)。
在另外的實施方案中,本文所述的方法使用本文所述的技術和材料以及本領域中公認的那些,如例如以下文獻中所述:《菲澤和菲澤的有機合成試劑(fieserandfieser′sreagentsfororganicsynthesis)》,第1-17卷(約翰·威利父子公司(johnwileyandsons),1991);《羅德的碳化合物化學(rodd′schemistryofcarboncompounds)》,第1-5卷和增刊(埃爾塞維爾科學出版公司(elseviersciencepublishers),1989);《有機反應(organicreactions)》,第1-40卷(約翰·威利父子公司,1991);《拉洛克的綜合有機轉化(larock′scomprehensiveorganictransformations)》,(vch出版公司,1989);march,《高等有機化學(advancedorganicchemistry)》,第4版(wiley1992);carey和sundberg,《高等有機化學(advancedorganicchemistry)》,第4版,a卷和b卷(plenum2000,2001);以及greene和wuts,《有機合成中的保護基(protectivegroupsinorganicsynthesis)》,第3版(wiley1999)(所有這些文獻以引用的方式併入本文用於這樣的公開)。用於製備如本文所公開的化合物的一般方法可以源自於反應並且所述反應可以通過使用適當的試劑和條件來改動以引入如本文所提供的化學式中存在的各種部分。
如果需要的話,可以使用常規技術來分離和純化反應的產物,所述技術包括但不限於過濾、蒸餾、結晶、色譜等。這些材料可以使用常規手段,包括物理常數和光譜數據來表徵。
本文所述的化合物可以使用本文所述的合成方法製備成單一異構體或異構體的混合物。
在一些實施方案中,本文所述的方法如以下方案中所概述。
在一個方面,提供了一種用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法,其中依魯替尼是式(i)的化合物,所述方法包括使式(ii)的化合物與式(iii)的化合物反應,其中x是滷素或-b(or5)2,其中每一個r5獨立地是h或烴基,或兩個r5連同它們所連接的b原子和o原子一起形成環狀結構:
在一些實施方案中,式(ii)的化合物是根據下文所述的方案1來製備的。
在本文所述的另一個實施方案中,使式(ii)的化合物與式(iii)的化合物在催化劑存在下反應。在一些實施方案中,所述催化劑包含銅、鎳、鈦或鈀,如銅、鎳、鈦或鈀的鹽、氧化物或絡合物。在一些實施方案中,x是滷素。在一些實施方案中,兩個r5一起形成亞烴基。
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)概述於方案1中:
方案1
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)包括:
a)使具有以下結構的化合物
其中pg是h或保護基,與草醯氯在二甲基甲醯胺(dmf)和溶劑存在下反應以產生具有以下結構的化合物
b)繼而使具有以下結構的化合物
與丙二腈在鹼和溶劑存在下反應以產生具有以下結構的化合物
c)繼而使具有以下結構的化合物
與硫酸二甲酯反應以產生具有以下結構的化合物
d)繼而使具有以下結構的化合物
與肼在溶劑存在下反應以產生具有以下結構的化合物
e)繼而使具有以下結構的化合物
與甲醯胺、甲酸銨、原甲酸三甲酯和氨、或甲脒或其鹽,如鹽酸鹽或乙酸鹽並且在加熱下反應以產生具有以下結構的化合物
f)繼而使具有以下結構的化合物
與(s)-3-羥基哌啶-1-甲酸叔丁酯、三苯膦、以及重氮二甲酸二異丙酯在溶劑存在下反應以產生具有以下結構的化合物
g)繼而使具有以下結構的化合物
與酸,然後與鹼在溶劑存在下反應以產生具有以下結構的化合物
h)繼而使具有以下結構的化合物
與鹼,然後與丙烯醯氯在溶劑存在下反應以產生具有式(ii)的結構的化合物
g)繼而使具有式(ii)的結構的化合物
與苯基硼酸在鹼、催化劑、以及溶劑存在下反應以產生具有式(i)的結構的化合物
在方案1的方法的一些實施方案中,pg是h。
在方案1的方法的一些實施方案中,pg是保護基,如苯甲基、叔丁基、烯丙基、三異丙基甲矽烷基或四氫吡喃基。在方案1的方法的一些實施方案中,pg是苯甲基。在方案1的方法的一些實施方案中,pg是叔丁基。在方案1的方法的一些實施方案中,pg是烯丙基。在方案1的方法的一些實施方案中,pg是三異丙基甲矽烷基。在方案1的方法的一些實施方案中,pg是四氫吡喃基。
在方案1的方法的一些實施方案中,所述鹼選自moh、m2co3、以及mhco3,其中m選自鋰、鈉、鉀、以及銫;1,8-二氮雜雙環[5.4.0]十一碳-7-烯(dbu)、r1r2r3n,其中r1、r2以及r3各自獨立地是c1-c6烴基。在方案1的方法的一些實施方案中,所述鹼是moh。在方案1的方法的一些實施方案中,所述鹼是naoh。在方案1的方法的一些實施方案中,所述鹼是koh。在方案1的方法的一些實施方案中,所述鹼是1,8-二氮雜雙環[5.4.0]十一碳-7-烯(dbu)。在方案1的方法的一些實施方案中,所述鹼是r1r2r3n,其中r1、r2以及r3各自獨立地是c1-c6烴基。在方案1的方法的一些實施方案中,所述鹼是r1r2r3n,其中r1、r2以及r3各自是乙基。在方案1的方法的一些實施方案中,所述鹼是r1r2r3n,其中r1和r2是異丙基並且r3是乙基。
在方案1的方法的一些實施方案中,所述酸是無機酸。在方案1的方法的一些實施方案中,所述酸是無機酸,其中所述無機酸是鹽酸、氫溴酸、硫酸、磷酸、或偏磷酸。在方案1的方法的一些實施方案中,所述酸是鹽酸。在方案1的方法的一些實施方案中,所述酸是氫溴酸。在方案1的方法的一些實施方案中,所述酸是硫酸。在方案1的方法的一些實施方案中,所述酸是磷酸。在方案1的方法的一些實施方案中,所述酸是偏磷酸。
在方案1的方法的一些實施方案中,所述酸是有機酸。在方案1的方法的一些實施方案中,所述酸是有機酸,其中所述有機酸是乙酸、丙酸、己酸、環戊烷丙酸、乙醇酸、丙酮酸、乳酸、丙二酸、丁二酸、蘋果酸、l-蘋果酸、順丁烯二酸、草酸、反丁烯二酸、三氟乙酸、酒石酸、l-酒石酸、檸檬酸、苯甲酸、3-(4-羥基苯甲醯基)苯甲酸、肉桂酸、扁桃酸、甲烷磺酸、乙烷磺酸、1,2-乙烷二磺酸、2-羥基乙烷磺酸、苯磺酸、甲苯磺酸、2-萘磺酸、4-甲基雙環[2.2.2]辛-2-烯-1-甲酸、葡庚糖酸、4,4′-亞甲基雙-(3-羥基-2-烯-1-甲酸)、3-苯丙酸、三甲基乙酸、叔丁基乙酸、月桂基硫酸、葡萄糖酸、穀氨酸、羥基萘甲酸、水楊酸、硬脂酸、粘康酸、丁酸、苯乙酸、苯丁酸、或丙戊酸。
在方案1的方法的一些實施方案中,所述溶劑選自水、c1-c6醇、四氫呋喃、2-甲基四氫呋喃、甲苯、二氯甲烷、二氯乙烷、以及其混合物。在方案1的方法的一些實施方案中,所述溶劑是水。在方案1的方法的一些實施方案中,所述溶劑是c1-c6醇。在方案1的方法的一些實施方案中,所述溶劑是甲醇。在方案1的方法的一些實施方案中,所述溶劑是異丙醇。在方案1的方法的一些實施方案中,所述溶劑是四氫呋喃。在方案1的方法的一些實施方案中,所述溶劑是2-甲基四氫呋喃。在方案1的方法的一些實施方案中,所述溶劑是甲苯。在方案1的方法的一些實施方案中,所述溶劑是二氯甲烷。在方案1的方法的一些實施方案中,所述溶劑是二氯乙烷。
在方案1的方法的一些實施方案中,所述催化劑包含金屬,如銅、鎳、鈦或鈀。在一些實施方案中,所述催化劑包含銅、鎳、鈦或鈀。在一些實施方案中,所述催化劑是銅、鎳、鈦或鈀的鹽、氧化物或絡合物。在一些實施方案中,所述催化劑是與鹼一起使用的銅鹽(例如乙酸銅(ii))。在一些實施方案中,所述鹼是無機鹼,如moh、m2co3(其中m選自鋰、鈉、鉀、以及銫)、caco3、二元磷酸鹽和三元磷酸鹽(例如m3po4、m2hpo4)或碳酸氫鹽(mhco3)。在一些實施方案中,所述鹼是有機鹼,如三取代的胺、吡啶或4-二甲基氨基吡啶。在一些實施方案中,所述鹼是nr1r2r3,其中r1、r2以及r3各自獨立地是c1-c6烴基,如三乙胺。
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)概述於方案2中:
方案2
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)包括:
使具有式(ii)的結構的化合物
與具有式(iii)的結構的化合物
其中x是滷素,
在催化劑存在下偶聯以產生具有式(i)的結構的化合物
在方案2的方法的一些實施方案中,x是cl。在方案2的方法的一些實施方案中,x是br。在方案2的方法的一些實施方案中,x是i。
在方案2的方法的一些實施方案中,所述催化劑包含金屬,如銅、鎳、鈦或鈀。在一些實施方案中,所述催化劑包含銅、鎳、鈦或鈀。在一些實施方案中,所述催化劑是銅、鎳、鈦或鈀的鹽、氧化物或絡合物。在一些實施方案中,所述催化劑是與鹼一起使用的銅鹽(例如乙酸銅(ii))。在一些實施方案中,所述鹼是無機鹼,如moh、m2co3(其中m選自鋰、鈉、鉀、以及銫)、caco3、二元磷酸鹽和三元磷酸鹽(例如m3po4、m2hpo4)或碳酸氫鹽(mhco3)。在一些實施方案中,所述鹼是有機鹼,如三取代的胺、吡啶或4-二甲基氨基吡啶。在一些實施方案中,所述鹼是nr1r2r3,其中r1、r2以及r3各自獨立地是c1-c6烴基,如三乙胺。
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)概述於方案3中:
方案3
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)包括:
使具有式(iv)的結構的化合物
其中x是滷素,與苯酚在銅鹽存在下偶聯以產生具有式(i)的結構的化合物
在方案3的方法的一些實施方案中,x是cl。在方案3的方法的一些實施方案中,x是br。在方案3的方法的一些實施方案中,x是i。
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)概述於方案4中:
方案4
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)包括:
使具有式(v)的結構的化合物
其中l是離去基,如滷素、羥基、烴氧基或三氟甲烷磺酸酯基,在氨存在下偶聯以產生具有式(i)的結構的化合物
在方案4的方法的一些實施方案中,l是滷素、羥基、烴氧基、-p(=o)r6(其中r6獨立地是oh、or7(r7是烴基)或滷代(例如cl)、甲烷磺酸酯基或三氟甲烷磺酸酯基。在方案4的方法的一些實施方案中,l是滷素。在方案4的方法的一些實施方案中,l是羥基。在方案4的方法的一些實施方案中,l是烴氧基。在方案4的方法的一些實施方案中,l是甲氧基。在方案4的方法的一些實施方案中,l是乙氧基。在方案4的方法的一些實施方案中,l是甲烷磺酸酯基。在方案4的方法的一些實施方案中,l是三氟甲烷磺酸酯基。在方案4的方法的一些實施方案中,l是二氯磷酸酯基。
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)概述於方案5中:
方案5
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)包括:
將具有式(vi)的結構的化合物還原
以產生具有式(i)的結構的化合物
在方案5的方法的一些實施方案中,所述還原過程是催化氫化。
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)概述於方案6中:
方案6
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)包括:
將具有式(vii)的結構的化合物還原
其中z是滷素或三氟甲烷磺酸酯基,以產生具有式(i)的結構的化合物
在方案6的方法的一些實施方案中,z是滷素。在方案6的方法的一些實施方案中,z是三氟甲烷磺酸酯基。
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)概述於方案7中:
方案7
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)包括:
將具有式(viii)的結構的化合物還原
其中z是滷素或三氟甲烷磺酸酯基,以產生具有式(i)的結構的化合物
在方案7的方法的一些實施方案中,z是滷素。在方案7的方法的一些實施方案中,z是三氟甲烷磺酸酯基。
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)概述於方案8中:
方案8
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)包括:
使具有式(ix)的結構的化合物
其中x是滷素或磺酸酯基,與具有式(x)的結構的化合物
其中y是烴基錫、硼酸、或硼酸酯,
偶聯以產生具有式(i)的結構的化合物
在方案8的方法的一些實施方案中,x是滷素。在方案8的方法的一些實施方案中,x是磺酸酯基。在方案8的方法的一些實施方案中,x是三氟甲烷磺酸酯基。在方案8的方法的一些實施方案中,y是烴基錫。在方案8的方法的一些實施方案中,y是硼酸。在方案8的方法的一些實施方案中,y是硼酸酯,如-b(or′r″),其中r′和r″各自獨立地是烴基或r′和r″一起形成亞烴基或取代的亞烴基。
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)概述於方案9中:
方案9
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)包括:
使具有式(xi)的結構的化合物
其中y是烴基錫、硼酸、或硼酸酯,
與具有式(xii)的結構的化合物
其中x是滷素或磺酸酯基,偶聯以產生具有式(i)的結構的化合物
在方案9的方法的一些實施方案中,x是滷素。在方案9的方法的一些實施方案中,x是磺酸酯基。在方案9的方法的一些實施方案中,x是三氟甲烷磺酸酯基。在方案9的方法的一些實施方案中,y是烴基錫。在方案9的方法的一些實施方案中,y是硼酸。在方案9的方法的一些實施方案中,y是硼酸酯,如-b(or′r″),其中r′和r″各自獨立地是烴基或r′和r″一起形成亞烴基或取代的亞烴基。
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)概述於方案10中:
方案10
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)包括:
將具有式(xiii)的結構的化合物還原
以產生具有式(i)的結構的化合物
在一些實施方案中,將具有式(xiii)的結構的化合物還原成具有式(i)的結構的化合物經由具有式(xiiia)的結構的中間化合物進行:
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)包括:
將具有式(xiiia)的結構的化合物還原
以產生具有式(i)的結構的化合物
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)概述於方案11中:
方案11
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)包括:
將具有式(xiv)的結構的化合物脫保護,
其中pg是保護基,以產生具有式(i)的結構的化合物
在方案11的方法的一些實施方案中,所述保護基是苯甲基、氨基甲酸苯甲酯、或氨基甲酸叔丁酯。在方案11的方法的一些實施方案中,所述保護基是苯甲基。在方案11的方法的一些實施方案中,所述保護基是氨基甲酸苯甲酯。在方案11的方法的一些實施方案中,所述保護基是氨基甲酸叔丁酯。
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)概述於方案12中:
方案12
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)包括:
使具有式(xv)的結構的化合物
與具有式(xvi)的結構的化合物
其中x是羥基、滷素或磺酸酯基,偶聯以產生具有式(i)的結構的化合物
在方案12的方法的一些實施方案中,x是羥基、滷素或磺酸酯基。在方案12的方法的一些實施方案中,x是滷素。在方案12的方法的一些實施方案中,x是磺酸酯基。在方案12的方法的一些實施方案中,x是甲烷磺酸酯基。在方案12的方法的一些實施方案中,x是三氟甲烷磺酸酯基。
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)概述於方案13中:
方案13
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)包括:
對具有式(xvii)的結構的化合物進行β-消除
其中l是離去基,以產生具有式(i)的結構的化合物
在方案13的方法的一些實施方案中,所述離去基是滷素、羥基、烴氧基、甲烷磺酸酯基或三氟甲烷磺酸酯基。在方案13的方法的一些實施方案中,所述離去基是滷素。在方案13的方法的一些實施方案中,所述離去基是羥基。在方案13的方法的一些實施方案中,所述離去基是烴氧基。在方案13的方法的一些實施方案中,所述離去基是三氟甲烷磺酸酯基。
在一些實施方案中,式(xvii)的化合物是式(xvii-1)的化合物,並且所述方法包括對式(xvii-1)的化合物
或其藥學上可接受的鹽進行β-消除。
包括對具有式(xvii)的結構的化合物,如具有式(xvii-1)的結構的化合物進行β-消除的方法可以被稱為「消除方法」。
在另一個實施方案中,還提供了式(xvii)的化合物,例如式(xvii-1)的化合物(原樣)或其藥學上可接受的鹽。具體來說,這樣的化合物呈基本上分離的形式和/或呈基本上純化的形式(例如hplc純度大於90%,例如大於95%)。
式(xvii)的化合物可以通過以下反應來製備:使式(xvii-a)的化合物
或其藥學上可接受的鹽
與l1-c(o)-ch2ch2l或其鹽反應,其中l1是離去基,如滷素或三氟甲烷磺酸酯基,所述方法也可以被稱為「醯化方法」。
在一些實施方案中,l和l1是相同的。在一些實施方案中,l和l1是不同的,前提條件是基團l1-c(o)比ch2l更具反應性。
在另一個實施方案中,式(xvii-1)的化合物可以通過以下反應來製備:使式(xvii-a)的化合物
或其藥學上可接受的鹽
與l1-c(o)-ch2ch2cl或其鹽反應,其中l1是離去基,如滷素或三氟甲烷磺酸酯基。在一些實施方案中,化合物l1-c(o)-ch2ch2cl是3-氯丙醯氯(即cl-c(o)-ch2ch2cl)。
在另一個實施方案中,提供了可通過所述醯化方法獲得的產物。
「消除方法」是消除反應,它優選地在鹼存在下進行。可以使用任何合適的鹼,例如有機鹼或無機鹼。它優選地是適用於消除反應的非親核鹼(即足夠強的鹼以促進消除;所述反應引起h+離子和cl-離子的產生,所述離子可以形成離子鍵以產生hcl)。在一個實施方案中,使用有機鹼。可以使用的這樣的鹼包括醇鹽鹼(例如叔丁醇鹽,如叔丁醇鉀)、胺鹼(例如三烴基胺,如三乙胺;二甲基氨基吡啶(dmap)、n-甲基嗎啉、1,4-二氮雜雙環[2.2.2]辛烷(dabco)、1,8-二氮雜雙環十一碳-7-烯(dbu)等)、醯胺鹼(例如lda或lihmds,即二異丙基氨基鋰或雙(三甲基甲矽烷基)氨基鋰)或其它合適的鹼(或鹼的混合物)。在一個實施方案中,所用的鹼是胺鹼,如dbu。
為了使消除方法有效地進行,需要至少1當量(與式xvii的化合物相比)的鹼。然而,在優選的實施方案中,使用過量的鹼當量(所述鹼可以是一種鹼或多於一種,例如兩種不同的鹼的混合物)。在一個實施方案中,存在至少約1.5當量,如約2當量的鹼(例如約2當量至約5當量)。在一個實施方案中,使用2當量、4當量或5當量的鹼(例如dbu)(與式xvii的化合物相比)。在一個優選的實施方案中,使用約1.5當量至2.5當量(例如約2當量)的dbu鹼。可以看出,不同的鹼可以引起所期望的產物的不同反應效率和/或不同產率和/或純度。
也可以使消除方法反應一段合適的時間。舉例來說,可以監測反應的進展(例如通過薄層色譜)並且持續時間可以是約1小時至約24小時的時間段。在其中使用約2當量的dbu的實施方案中,反應時間可以是約4小時至約24小時(優選地約4小時至10小時,如6小時至8小時,例如約7小時)。
在一個實施方案中,所述消除方法是在合適的溶劑,如極性非質子溶劑存在下進行的。合適的溶劑因此包括諸如thf(四氫呋喃)和etoac(乙酸乙酯)的溶劑。反應條件因此優選地在無水或惰性條件下進行,例如使用無水溶劑以及在惰性(例如n2)氣氛下進行。
消除方法的反應溫度優選地是約0℃至約80℃,但是取決於預期使用的鹼(例如對於氨基鋰鹼,需要諸如約0℃的低溫來避免鹼將溶劑去質子化)。當使用除氨基鋰(或有機鋰鹼)以外的類型的鹼時,則優選的溫度範圍是約室溫(例如約20℃至約25℃)至約65℃。當使用乙酸乙酯作為溶劑時,則優選的溫度可以是約室溫至約65℃。當使用thf時,反應的溫度優選地是約室溫(例如約20℃至25℃)。
所述消除方法還可以包括使用添加劑,例如可以促進方法反應的任何合適的添加劑。合適的添加劑可以包括三氟乙酸鈉(即cf3coona;它可以與三個水分子結合,從而形成例如cf3coona·3h2o)、乳酸鈉、ch3so3na、cf3so3na或cf3so3li(等,例如可以使用另一種合適的金屬離子代替na/li並且「酸」部分可以是另一種合適的酸)。在一個實施方案中,所述添加劑是三氟乙酸鈉(即cf3coona)。
在消除方法的一個實施方案中,優選的添加順序是添加式xvii的化合物(連同任選的溶劑一起),可以將所述化合物和溶劑混合在一起(例如經過10分鐘-15分鐘的過程)。在一個實施方案中,然後優選添加鹼(例如約2當量的dbu),優選地經過一段時間(例如10分鐘至4小時,例如約1小時或2小時)的過程。然後將反應物攪拌如本文所指定的時間段。
在一個實施方案中,將由消除方法獲得的混合物純化。這樣的純化可以在後處理階段中進行。舉例來說,可以例如在將反應混合物轉移到另一個容器中之後向消除方法的混合物中添加合適的鹼(例如碳酸鈉,例如na2co3,2當量5%的na2co3),並且攪拌一段時間(例如約5分鐘至4小時,如約30分鐘至2小時)。然後可以對反應混合物進行後處理。舉例來說,可以用水和/或檸檬酸洗滌有機相(特別是後一種洗滌劑可以有利於去除雜質)。然後可以用有機溶劑(例如乙酸乙酯)萃取(合併)水相併且合併有機相。然後可以根據需要對合併的有機相進行ph值調節,例如通過添加合適的鹼(例如na2co3)來實現,例如以將ph值調節到約6-7.5。
在醯化方法中,3-氯丙醯氯具有>50%的純度(例如通過hplc所測定)。因此,這不同於其中3-氯丙醯氯可能偶然作為雜質存在的情況。3-氯丙醯氯試劑因此以可以商購(例如從西格瑪-奧德裡奇公司商購)的形式/純度使用。
在一個實施方案中,在醯化方法中,以大量過量添加化合物l1-c(o)-ch2ch2l,如3-氯丙醯氯。舉例來說,首先可以將式(xvii-a)的化合物溶解在無水的適當溶劑(例如極性非質子溶劑,如thf、甲基-thf、乙酸乙酯等)中。這樣的反應可以在惰性氣氛下,例如在n2(或另一種惰性氣體)下進行。然後可以向式(xvii-a)的化合物和溶劑的混合物中首先添加合適的鹼。然後可以添加(例如逐滴以維持一定的反應溫度)l1-c(o)-ch2ch2l,如3-氯丙醯氯(例如1當量或更少,例如0.5當量至1當量,與式i的化合物相比)。可以用在所述方法的該步驟中使用的適當的溶劑(例如上述極性非質子溶劑)稀釋剩餘的l1-c(o)-ch2ch2l,如3-氯丙醯氯(考慮到在一個實施方案中,它可能以過量使用),並且也可以經過一段時間(例如10分鐘至2小時)的過程緩慢添加,這取決於維持反應溫度。所期望的材料的分離可以如下文所述來進行。
在醯化方法的一個實施方案中,除了所需的反應物之外,還可以使用添加劑,例如丁基化羥基甲苯(bht)。優選地在開始時將這樣的添加劑(例如bht)添加到反應混合物中(例如連同式(xvii-a)的化合物和溶劑一起)。
在醯化方法的一個實施方案中,可以在室溫或低於室溫,例如等於或低於約20℃至25℃的溫度下進行反應。在一個實施方案中,優選的是,它是在低於室溫(例如在約10℃)或在冰浴中進行的。在一個實施方案中,優選的是,以儘可能維持反應溫度恆定的速率進行3-氯丙醯氯的添加,例如本文所指定的持續時間(例如以將溫度維持在約10℃)。
可以用於醯化方法中的合適的鹼包括有機鹼和無機鹼。當使用無機鹼時,則可以使用肖滕-鮑曼條件(schotten-baumanncondition)(例如有機相和水相的混合物)。合適的無機鹼包括碳酸鹽和重碳酸鹽/碳酸氫鹽鹼(例如na2co3或nahco3)。
可以分離和/或純化通過醯化方法製備的式xvii的化合物。可以對醯化方法的混合物進行後處理,例如可以分離水相併且可以洗滌有機相(例如用碳酸氫鈉洗滌劑)。之後,可以使用兩種方法來分離和/或純化(如果確實這是意圖的話,即在一個實施方案中,式xvii的化合物不需要被離析/分離)以提供呈固體形式的式xvii的化合物。可以例如使用如可以在下文(例如在實施例中)所述的溶劑的混合物,例如使用極性非質子溶劑(例如可以用於本發明的第二種方法中的溶劑)和烷烴溶劑的混合物來進行結晶。可以提到的極性非質子溶劑包括me-thf和etoac(甲基四氫呋喃和乙酸乙酯)。可以提到的烷烴溶劑包括庚烷(例如正庚烷)。
在一個實施方案中,式xvii的化合物不需要從醯化方法中分離或離析,但是可以(例如在一個優選的實施方案中)直接用於消除方法中。這可以具有以下優勢,即它在整體上是更高效或更方便的方法。在這樣的一個實施方案中,可以用於醯化方法中的溶劑可以與該直接用於消除方法中的溶劑保持相同。或者,用於醯化方法中的溶劑可以在直接用於消除方法中之前被轉變成不同的溶劑。在這種背景下,「直接」指的是用於醯化方法中的式xvii的化合物在用於後續步驟,即消除方法中之前沒有經過分離、離析和/或純化。
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)概述於方案14中:
方案14
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)包括:
對具有式(xviii)的結構的化合物進行β-消除
其中l是離去基,以產生具有式(i)的結構的化合物
在方案14的方法的一些實施方案中,所述離去基是滷素、羥基、烴氧基、甲烷磺酸酯基或三氟甲烷磺酸酯基。在方案14的方法的一些實施方案中,所述離去基是滷素。在方案14的方法的一些實施方案中,所述離去基是羥基。在方案14的方法的一些實施方案中,所述離去基是烴氧基。在方案14的方法的一些實施方案中,所述離去基是三氟甲烷磺酸酯基。
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)概述於方案15中:
方案15
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)包括:
使具有式(xix)的結構的化合物
其中x是滷素,在三苯基膦和甲醛存在下偶聯以產生具有式(i)的結構的化合物
在方案15的方法的一些實施方案中,x是cl。在方案15的方法的一些實施方案中,x是br。
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)概述於方案16中:
方案16
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)包括:
使具有式(xx)的結構的化合物
其中x是滷素,與具有式(xxi)的結構的化合物
其中y是烴基錫、硼酸、或硼酸酯,偶聯以產生具有式(i)的結構的化合物
在方案16的方法的一些實施方案中,x是cl。在方案16的方法的一些實施方案中,y是烴基錫。在方案16的方法的一些實施方案中,y是硼酸。在方案16的方法的一些實施方案中,y是硼酸酯,如-b(or′r″),其中r′和r″各自獨立地是烴基或r′和r″一起形成亞烴基或取代的亞烴基。
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)概述於方案17中:
方案17
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)包括:
將具有式(xxii)的結構的化合物還原
以產生具有式(i)的結構的化合物
其中表示式(xxiia)-(xxiig)的化合物:
或其組合。
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)概述於方案18中:
方案18
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)包括:
使具有式(xxiii)的結構的化合物
與甲醯胺、甲酸銨、原甲酸三甲酯和氨、或甲脒或其鹽,如鹽酸鹽或乙酸鹽縮合以產生具有式(i)的結構的化合物
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)概述於方案19中:
方案19
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)包括:
使具有式(xxiv)的結構的化合物
其中x是離去基,如滷素,與具有式(xxv)的結構的化合物偶聯
以產生具有式(i)的結構的化合物
在式(xxiv)的一些實施方案中,x是滷素、磺酸酯基、磷酸酯基、羥基或烴氧基。在一些實施方案中,x是滷素。在一些實施方案中,x是-p(=o)r6(其中r6獨立地是oh、or7(r7是烴基)或滷代(例如cl))。在一些實施方案中,x是二氯磷酸酯基。
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)概述於方案20中:
方案20
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)包括:
a)使具有式(xv)的結構的化合物
與具有以下結構的化合物
其中x是滷素或磺酸酯基,偶聯以產生具有式(xxvi)的結構的化合物
b)繼而使具有式(xxvi)的結構的化合物
與丙烯醯胺反應以產生具有式(i)的結構的化合物
在方案20的方法的一些實施方案中,x是cl。在方案20的方法的一些實施方案中,x是br。在方案20的方法的一些實施方案中,x是三氟甲烷磺酸酯基。在方案20的方法的一些實施方案中,x是甲烷磺酸酯基。
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)概述於方案21中:
方案21
在本文所述的一些實施方案中,用於製備1-((r)-3-(4-氨基-3-(4-苯氧基苯基)-1h-吡唑並[3,4-d]嘧啶-1-基)哌啶-1-基)丙-2-烯-1-酮(依魯替尼)的方法(其中依魯替尼是式(i)的化合物)包括:
使具有式(xxvii)的結構的化合物
與具有式(xxviii)的結構的化合物
其中x是離去基,如羥基、烴氧基、br、磺酸酯基或二烴氧基-磷醯基(p(=o)(or4)2(每一個r4獨立地是烴基,例如me或et)),偶聯以產生具有式(i)的結構的化合物
在方案21的方法的一些實施方案中,x是羥基。在方案21的方法的一些實施方案中,x是烴氧基。在方案21的方法的一些實施方案中,x是br。在方案21的方法的一些實施方案中,x是三氟甲烷磺酸酯基。在方案21的方法的一些實施方案中,x是甲烷磺酸酯基。在方案21的方法的一些實施方案中,x是p(=o)(or4)2,如p(=o)(ome)2或p(=o)(oet)2。
一般來說,本文所述的方法可以具有以下優勢,即與現有技術中所公開的方法相比,所製備的化合物可以通過利用更少的試劑和/或溶劑和/或需要更少的反應步驟(例如不同/單獨的反應步驟)的方式而產生。
本發明的方法還可以具有以下優勢,即與現有技術中所公開的程序相比,所製備的一種或多種化合物是以更高的產率、更高的純度、更高的選擇性(例如更高的區域選擇性)、在更少的時間內、以更方便(即易於處理)的形式、由更方便(即易於處理)的前體、以更低的成本和/或在材料(包括試劑和溶劑)的使用和/或浪費更少的情況下而產生。此外,本發明的方法可以存在若干環境益處。
保護基的使用
在所述的反應中,可能需要保護反應性官能團,例如羥基、氨基、亞氨基、硫代或羧基,其中這些在最終產物中是所期望的,以避免它們不必要地參與反應。保護基用於阻隔一些或所有反應性部分並且防止這些基團參與化學反應直到保護基被去除為止。在一個實施方案中,每一個保護基可以是可通過不同的手段來去除的。在完全不同的反應條件下裂解的保護基滿足差異性去除的要求。保護基可以通過酸、鹼、以及氫解來去除。諸如三苯甲基、二甲氧基三苯甲基、縮醛以及叔丁基二甲基甲矽烷基的基團是酸不穩定的並且可以用於在受可通過氫解去除的cbz基團和鹼不穩定的fmoc基團保護的氨基存在下保護羧基和羥基反應性部分。羧酸和羥基反應性部分可以在被諸如氨基甲酸叔丁酯或氨基甲酸酯(這兩者均是酸和鹼穩定的,但是可水解去除)的酸不穩定基團阻隔的胺存在下用鹼不穩定基團,諸如但不限於甲基、乙基、以及乙醯基來阻隔。
羧酸和羥基反應性部分還可以用可水解去除的保護基,如苯甲基來阻隔,而能夠與酸進行氫鍵鍵合的胺基可以用鹼不穩定基團,如fmoc來阻隔。羧酸反應性部分可以通過轉化成如本文所舉例說明的簡單的酯化合物來保護,或它們可以用可氧化去除的保護基,如2,4-二甲氧基苯甲基來阻隔,而共同存在的氨基可以用氟化物不穩定的甲矽烷基氨基甲酸酯來阻隔。
烯丙基阻隔基在酸保護基和鹼保護基存在下是有用的,這是因為前者是穩定的並且可以隨後通過金屬或π酸催化劑來去除。舉例來說,烯丙基阻隔的羧酸可以用pd0催化的反應在酸不穩定的氨基甲酸叔丁酯或鹼不穩定的乙酸酯胺保護基存在下脫保護。又另一種形式的保護基是可以與化合物或中間體連接的樹脂。只要殘基與樹脂連接,該官能團就被阻隔並且不能反應。一旦從樹脂釋放,所述官能團就可供用於進行反應。
通常,阻隔基/保護基可以選自:
氨基保護基包括但不限於均三甲苯磺醯基(mts)、苯甲氧羰基(cbz或z)、2-氯苯甲氧羰基、叔丁氧羰基(boc)、叔丁基二甲基甲矽烷基(tbs或tbdms)、9-茀基甲氧羰基(fmoc)、甲苯磺醯基、苯磺醯基、2-吡啶基磺醯基、丁二醯亞胺、鄰苯二甲醯亞胺、對甲氧苯甲基(pmb)、或合適的光不穩定性保護基,如6-硝基藜蘆基氧基羰基(nvoc)、5-溴-7-硝基吲哚基、硝基苯甲基、α-,α-二甲基二甲氧基苯甲基氧羰基(ddz)、硝基胡椒基、芘基甲氧羰基等。易受酸介導的去除影響的氨基保護基包括但不限於boc和tbdms。能抵抗酸介導的去除並且易受氫介導的去除影響的氨基保護基包括但不限於烯丙氧羰基、cbz、硝基、以及2-氯苯甲氧羰基。能抵抗酸介導的去除並且易受鹼介導的去除影響的氨基保護基包括但不限於fmoc、(1,1-二氧代苯並[b]噻吩-2-基)甲氧基羰基(bsmoc)、2,7-二叔丁基-fmoc、2-氟-fmoc(fmoc(2f))、2-(4-硝基苯磺醯基)乙氧羰基(nsc)、(1,1-二氧代萘並[1,2-b]噻吩-2-基)甲氧基羰基(a-nsmoc)、1-(4,4-二甲基-2,6-二氧代環己-1-亞基)-3-甲基丁基(ivdde)、乙烷磺醯基乙氧羰基(esc)、以及2-[苯基(甲基)二氫硫基]乙氧基羰基四氟硼酸酯(pms)、四氯鄰苯二甲醯基(tcp)等。羥基保護基包括但不限於fmoc、tbs、光不穩定性保護基(如硝基藜蘆基氧甲醚(nvom))、mem(甲氧基乙氧基甲醚)、mom(甲氧基甲醚)、npeoc(4-硝基苯乙基氧羰基)以及npeom(4-硝基苯乙基氧甲基氧羰基)。
其它保護基加上適用於形成保護基和去除它們的技術的詳細說明描述於greene和wuts,《有機合成中的保護基(protectivegroupsinorganicsynthesis)》,第3版,紐約州紐約的約翰·威利父子公司(johnwiley&sons,newyork,ny),1999;以及kocienski,《保護基(protectinggroups)》,紐約州紐約的thiemeverlag公司(thiemeverlag,newyork,ny),1994,這些文獻以引用的方式整體併入本文。
式(i)的化合物、以及其藥學上可接受的鹽或組合物
本文所述的btk抑制劑化合物(即式(i)的化合物)對btk和在酪氨酸激酶的與btk中半胱氨酸481的胺基酸序列位置具有同源性的胺基酸序列位置上具有半胱氨酸殘基的激酶具有選擇性。btk抑制劑化合物可以與btk的cys481形成共價鍵(例如經由麥可反應(michaelreaction))。
多種藥學上可接受的鹽是由式(i)的化合物形成的並且包括:
-通過使式(i)的化合物與有機酸反應所形成的酸加成鹽,所述有機酸包括脂族一元羧酸和二羧酸、苯基取代的鏈烷酸、羥基鏈烷酸、鏈烷二酸、芳族酸、脂族和芳族磺酸、胺基酸等並且包括例如乙酸、三氟乙酸、丙酸、乙醇酸、丙酮酸、草酸、順丁烯二酸、丙二酸、丁二酸、反丁烯二酸、酒石酸、檸檬酸、苯甲酸、肉桂酸、扁桃酸、甲烷磺酸、乙烷磺酸、對甲苯磺酸、水楊酸等;
-通過使式(i)的化合物與無機酸反應所形成的酸加成鹽,所述無機酸包括鹽酸、氫溴酸、硫酸、硝酸、磷酸、氫碘酸、氫氟酸、亞磷酸等。
關於式(i)的化合物的術語「藥學上可接受的鹽」指的是式(i)的化合物的鹽,所述鹽不會對接受它的施用的哺乳動物引起顯著的刺激並且基本上不會消除化合物的生物活性和特性。
應當了解的是,提到藥學上可接受的鹽時,包括溶劑加成形式(溶劑化物)。溶劑化物含有化學計量或非化學計量的溶劑,並且是在產物形成或用藥學上可接受的溶劑分離的過程期間形成的,所述溶劑諸如水、乙醇、甲醇、甲基叔丁基醚(mtbe)、二異丙醚(dipe)、乙酸乙酯、乙酸異丙酯、異丙醇、甲基異丁基酮(mibk)、甲基乙基酮(mek)、丙酮、硝基甲烷、四氫呋喃(thf)、二氯甲烷(dcm)、二烷、庚烷、甲苯、苯甲醚、乙腈等。在一個方面,使用但不限於一種或多種第3類溶劑形成溶劑化物。溶劑的類別被定義於例如人用藥品註冊技術要求國際協調會議(internationalconferenceonharmonizationoftechnicalrequirementsforregistrationofpharmaceuticalsforhumanuse,ich),「雜質:殘留溶劑指南q3c(r3)(impurities:guidelinesforresidualsolvents,q3c(r3))」(2005年11月)中。在溶劑是水時,形成水合物,或在溶劑是醇時,形成醇化物。在一些實施方案中,式(i)的化合物或其藥學上可接受的鹽的溶劑化物在本文所述的方法期間方便地製備或形成。在一些實施方案中,式(i)的化合物的溶劑化物是無水的。在一些實施方案中,式(i)的化合物或其藥學上可接受的鹽以非溶劑化形式存在。在一些實施方案中,式(i)的化合物或其藥學上可接受的鹽以非溶劑化形式存在並且是無水的。
在另外的其它實施方案中,式(i)的化合物或其藥學上可接受的鹽被製備成各種形式,包括但不限於無定形相、結晶形式、研磨形式以及納米顆粒形式。在一些實施方案中,式(i)的化合物或其藥學上可接受的鹽是無定形的。在一些實施方案中,式(i)的化合物或其藥學上可接受的鹽是無定形的和無水的。在一些實施方案中,式(i)的化合物或其藥學上可接受的鹽是無定形的。在一些實施方案中,式(i)的化合物或其藥學上可接受的鹽是無定形的和無水的。
然後還提供了一種用於製備包含依魯替尼的藥物組合物的方法,所述方法包括使依魯替尼(或其藥學上可接受的鹽)與一種或多種藥學上可接受的賦形劑、佐劑、稀釋劑和/或載體締合,所述依魯替尼是根據本文所述的方法製備的。
合適的溶劑
可向諸如人類的哺乳動物施用的治療劑必須是通過遵循監管指南來製備的。這樣的政府監管的指南被稱為優良製造規範(goodmanufacturingpractice,gmp)。gmp指南概述了活性治療劑的可接受的汙染水平,例如像最終產品中殘留溶劑的量。優選的溶劑是適用於gmp設施中並且符合工業安全考慮的那些溶劑。溶劑的類別被定義於例如人用藥品註冊技術要求國際協調會議(ich),「雜質:殘留溶劑指南q3c(r3)(impurities:guidelinesforresidualsolvents,q3c(r3))」(2005年11月)中。
溶劑被分類為三個類別。第1類溶劑是有毒的並且應當被避免。第2類溶劑是在製造治療劑期間使用受限的溶劑。第3類溶劑是具有低毒性可能並且對人類健康有更低的風險的溶劑。第3類溶劑的數據表明它們在急性或短期研究中具有更低的毒性並且在遺傳毒性研究中呈陰性。
應當被避免的第1類溶劑包括:苯;四氯化碳;1,2-二氯乙烷;1,1-二氯乙烯;以及1,1,1-三氯乙烷。
第2類溶劑的實例是:乙腈、氯苯、氯仿、環己烷、1,2-二氯乙烯、二氯甲烷、1,2-二甲氧基乙烷、n,n-二甲基乙醯胺、n,n-二甲基甲醯胺、1,4-二烷、2-乙氧基乙醇、乙二醇、甲醯胺、己烷、甲醇、2-甲氧基乙醇、甲基丁基酮、甲基環己烷、n-甲基吡咯烷、硝基甲烷、吡啶、環丁碸、萘滿、甲苯、1,1,2-三氯乙烯、四氫呋喃以及二甲苯。
具有低毒性的第3類溶劑包括:乙酸、丙酮、苯甲醚、1-丁醇、2-丁醇、乙酸丁酯、叔丁基甲醚(mtbe)、異丙基苯、二甲亞碸、乙醇、乙酸乙酯、乙醚、甲酸乙酯、甲酸、庚烷、乙酸異丁酯、乙酸異丙酯、乙酸甲酯、3-甲基-1-丁醇、甲基乙基酮、甲基異丁基酮、2-甲基-1-丙醇、戊烷、1-戊醇、1-丙醇、2-丙醇、以及乙酸丙酯。
活性藥物成分(api)中殘留的溶劑源於api的製造。在一些情況下,溶劑沒有由實際的製造技術完全去除。用於合成api的溶劑的適當選擇可以提高產率或決定特徵,如晶形、純度、以及溶解度。因此,溶劑是合成方法中關鍵的參數。
在一些實施方案中,包含式(i)的化合物的組合物包含一種或多種有機溶劑。在一些實施方案中,包含式(i)的化合物的組合物包含殘留量的一種或多種有機溶劑。在一些實施方案中,包含式(i)的化合物的組合物包含殘留量的第3類溶劑。在一些實施方案中,所述有機溶劑是第3類溶劑。在一些實施方案中,第3類溶劑選自由以下各項組成的組:乙酸、丙酮、苯甲醚、1-丁醇、2-丁醇、乙酸丁酯、叔丁基甲醚、異丙基苯、二甲亞碸、乙醇、乙酸乙酯、乙醚、甲酸乙酯、甲酸、庚烷、乙酸異丁酯、乙酸異丙酯、乙酸甲酯、3-甲基-1-丁醇、甲基乙基酮、甲基異丁基酮、2-甲基-1-丙醇、戊烷、1-戊醇、1-丙醇、2-丙醇、以及乙酸丙酯。在一些實施方案中,第3類溶劑選自乙酸乙酯、乙酸異丙酯、叔丁基甲醚、庚烷、異丙醇、以及乙醇。
實施例
以下實施例意圖說明本發明並且不應當被視為對本發明的範圍的限制。
實施例1:化合物xvii-a到化合物xvii-1以及化合物xvii-1的分離
將化合物xvii-a(80g,0.207mol)、0.16g的bht(=丁基化羥基甲苯)以及me-thf(656.0g)添加到裝備有高架攪拌的2l夾套反應器中。在10℃攪拌20分鐘之後,添加7%nahco3水溶液(752g,0.627mol),然後在10℃在氮氣氣氛/保護下經過1小時經由滴液漏鬥緩慢添加3-氯丙醯氯(25.2g,0.198mol)。在10℃將反應混合物攪拌1小時之後,將另一部分的3-氯丙醯氯(2.61g,20.5mmol)用me-thf(32g,0.4×)稀釋,然後在10℃經過30分鐘緩慢添加到反應器中。在10℃攪拌30分鐘之後,分離出水相併且用7%nahco3(200g,0.167mol)洗滌含有化合物xvii-1的me-thf溶液。最終,獲得具有97.68%純度的化合物xvii-1的676.7g2-me-thf溶液(這在下文被稱為溶液a)。
存在分離出呈固體狀的化合物xvii-1的兩種方法:從me-thf/正庚烷中結晶以及從etoac/正庚烷中結晶。化合物xvii-1從me-thf/正庚烷和etoac/正庚烷中結晶的詳細說明匯總於下文中。
從me-thf/正庚烷中結晶:將化合物xvii-1的me-thf溶液(由20g的化合物xvii-a獲得,hplc純度:97.68%;即上文所提到的溶液a的四分之一)添加到具有機械攪拌的500ml夾套燒瓶中以進行共沸蒸餾。首先,將me-thf溶液在真空下濃縮到4v-5v(夾套溫度:28℃),然後添加新鮮和乾燥的me-thf(200ml)。將這一蒸餾循環重複兩次,然後蒸餾終點是4v-5v。然後在15℃經過2小時將反溶劑正庚烷(80ml)緩慢添加到反應器中。在15℃再攪拌1小時-2小時之後,過濾混合物並且用1v的me-thf/正庚烷(20ml,v/v=1/1)洗滌濾餅。在真空下在35℃將溼濾餅乾燥16小時之後,分離出呈白色固體狀的23.25g化合物xvii-1,hplc純度是98.36%,分離產率是88.7%。
從etoac/正庚烷中結晶:將化合物xvii-1的me-thf溶液(由20g的化合物xvii-a獲得,hplc純度:97.68%;即上文所提到的溶液a的四分之一)添加到具有機械攪拌的500ml夾套燒瓶中,然後在真空下將它濃縮到4v-5v(夾套溫度:28℃)。將etoac(200ml)添加到殘餘物中,然後將混合物再次濃縮到4v-5v。將這一蒸餾循環重複三次,然後大量白色固體沉澱出。然後在15℃經過2小時將反溶劑正庚烷(80ml)緩慢添加到反應器中。在15℃再攪拌1小時-2小時之後,過濾混合物並且用ea/正庚烷(20ml,v/v=4/4)洗滌濾餅。在真空下在35℃將溼濾餅乾燥16小時之後,分離出呈白色固體狀的21.7g化合物xvii-1,hplc純度是98.57%,分離產率是87.9%。
化合物xvii-1的表徵數據
可以獲得數據以對化合物xvii-1進行表徵,例如質譜數據、熔點和/或nmr(核磁共振)數據(例如質子)。在這種情況下,獲得情況以尤其通過nmr來對化合物xvii-1進行表徵,所述表徵數據如下參看於附圖中:
圖1:化合物xvii-1的1hnmr。
圖2:化合物xvii-1的13cnmr。
圖3、圖4以及圖5:化合物xvii-1的nmrnoe(核極化效應)。
圖6、圖7、圖8以及圖9:化合物xvii-1的nmrhmbc(異核多鍵相關光譜學)。
在提到noenmr的情況下,這是本領域技術人員已知的一種光譜方法。它是一種二維nmr光譜學方法。noe經由空間發生(因此,靠近的那些原子將顯示noe),而不是通過質子和碳nmr所看到的通常的自旋-自旋耦合效應。在提到hmbcnmr的情況下,這是也為本領域技術人員所知的一種特定的光譜方法。它也是一種二維nmr光譜學方法。它用於檢測約2個-4個鍵的更長範圍內的異核相關性。
進行篩選操作以在該方法反應中測試多種鹼,並且其中測量作為反應的結果的最終產物,即剩餘起始材料(化合物xvii-a)、所期望的產物(化合物xvii-1)以及作為副產物的化合物i(即依魯替尼)的百分比。
有機鹼的使用(3-cpc指的是3-氯丙醯氯):
無機鹼的使用:肖滕-鮑曼條件
實施例2:化合物xvii-1到化合物i(依魯替尼)以及化合物xvii-a到化合物i的「單步」方法
使用24.7g批量的化合物xvii-1來製備粗製化合物i(依魯替尼)。首先,將化合物xvii-1(呈固體形式)添加到12v的無水ea(乙酸乙酯)中,然後在20℃經過1小時添加2.5當量的dbu。在20℃攪拌24小時之後,所述溶液產生89%的所期望的產物。
分離的化合物xvii-1到化合物i(使用cf3coona)
程序:
將10g的化合物xvii-1加入到r1(反應容器1)中;
將115ml的ea(乙酸乙酯)加入到r1中;
將1.0當量的cf3coona加入到r1中,然後在15℃經過1小時將2.5當量的dbu逐滴添加到r1中;
用5mlea衝洗滴液漏鬥;
在15℃將r1攪拌5小時,並且獲取hplc讀數;
在0.5小時內將11×(2.0當量)5%na2co3逐滴添加到r1中,然後將r1攪拌1小時,然後分離各相;
用4.5×h2o洗滌有機相,將r1在20℃維持14小時;
分離各相;
用3.0×22%檸檬酸將有機物洗滌三次;
合併水相,然後將它用7vea萃取;
合併有機層;
用4.0×10%na2co3(ph值=6.10)洗滌有機相,然後用4.5×h2o將有機相洗滌兩次;
獲得143.36g的有機相;
在最終的後處理和結晶之後,以80.8%的產率分離出9.21g粗製化合物i。
從化合物xvii-a到化合物i,而不分離化合物xvii-1(在me-thf中進行消除)
程序:
1.將化合物xvii-1的me-thf溶液加入到r1中(基於化合物i的20g的量;如上文所提到的溶液a的四分之一)而不分離化合物xvii-1;
2.將溶液濃縮到5.5v,然後將4.5v的2-me-thf加入到r1中;
3.將溶液濃縮到5.5v,然後將4.5v的2-me-thf加入到r1中;
4.將溶液濃縮到5.5v,然後將4.5v的2-me-thf加入到r1中;
5.將溶液濃縮到5.5v,然後將4.5v的2-me-thf加入到r1中;
6.將溶液濃縮到5.5v,然後將6.5v的2-me-thf加入到r1中;
7.在22℃將2.5當量的dbu逐滴添加到r1中,持續1小時;
8.在22℃將r1攪拌22小時,將r1中的混合物轉移到r2中;
9.用1v的2-me-thf洗滌r1,然後轉移到r2中;
10.用3.0×22%檸檬酸洗滌一個或多個有機相,然後分離各相。用3.0×22%檸檬酸洗滌有機物,然後分離各相;
11.用3.0×22%檸檬酸洗滌有機物,然後分離各相。合併水相,然後將它用7v的2-me-thf萃取。測量一個或多個有機相的hplc純度;
12.合併水相併且獲得161.24g的水相;
13.合併有機層;
14.用8.4×10%na2co3(ph值=6-7.5)洗滌有機相;
15.用4.5×h2o將有機相洗滌兩次;
16.獲得343.23g的有機相;
17.在最終的後處理和結晶之後,以76.5%的產率分離出17.44g粗製化合物i。
在ea中從化合物xvii-a到化合物i,而不分離化合物xvii-1(不添加cf3coona)
程序:
將化合物xvii-1的me-thf溶液加入到r1中(基於化合物i的20g的量;如上文所提到的溶液a的四分之一)而不分離化合物xvii-1;
將溶液濃縮到5.5v,然後將4.5v的ea加入到r1中;
將溶液濃縮到5.5v,然後將4.5v的ea加入到r1中;
將溶液濃縮到5.5v,然後將4.5v的ea加入到r1中;
將溶液濃縮到5.5v,然後將4.5v的ea加入到r1中;
將溶液濃縮到5.5v,然後將6.5v的ea加入到r1中;
在22℃經過1小時將2.5當量的dbu逐滴添加到r1中;
在22℃將r1攪拌22小時,將r1中的混合物轉移到r2中;
用1v的ea洗滌r1,然後轉移到r2中;
用3.0×22%檸檬酸洗滌有機物,然後分離各相。用3.0×22%檸檬酸洗滌有機物,然後分離各相;
用3.0×22%檸檬酸洗滌有機物,然後分離各相。合併水相,然後將它用7vea萃取;
合併水相併且獲得190.59g的水相;
合併有機層;
用3.8×10%na2co3(ph值=6-7.5)洗滌有機相;
用4.5×h2o將有機相洗滌兩次;
獲得360.48g的有機相;
在最終的後處理和結晶之後,以73.2%的產率分離出16.70g粗製化合物i(母液的產率損失是6.3%)。
從化合物xvii-a到化合物i而不分離化合物xvii-1(添加cf3coona)
程序:
將化合物xvii-1的me-thf溶液加入到r1中(基於化合物i的20g的量;如上文所提到的溶液a的四分之一)而不分離化合物xvii-1;
將溶液濃縮到5.5v,然後將4.5v的ea加入到r1中;
將溶液濃縮到5.5v,然後將4.5v的ea加入到r1中;
將溶液濃縮到5.5v,然後將4.5v的ea加入到r1中;
將溶液濃縮到5.5v,然後將4.5v的ea加入到r1中;
將溶液濃縮到5.5v,然後將6.5.5v的ea加入到r1中;
將1.0當量的cf3coona(7.2g)加入到r1中;
在15℃經過1小時將2.5當量的dbu(19.6g)逐滴添加到r1中;
在15℃將r1攪拌3小時,並且將r1中的混合物轉移到r2中;
將r2中的混合物攪拌3小時;
經過0.5小時將2當量的5%na2co3逐滴添加到r1中;
將r1攪拌1小時;
分離r1中的混合物溶液;
用4.5×h2o洗滌有機相;
用3.0×22%檸檬酸將有機物洗滌三次,w=197g,測定是0.32%,損失產率是2.76%;
合併一個或多個水相併且將它用7v的ea萃取;
合併一個或多個有機相併且用10%na2co3(3.9×)將ph值調節到6-7.5;
用4.5×h2o將一個或多個有機相洗滌兩次。溶液產率是91.64%。
篩選消除步驟中的添加劑
化合物xvii-1(12v;乙酸乙酯)→1.0當量的添加劑→攪拌10分鐘-15分鐘→經過1小時逐滴添加2.5當量的dbu→在22℃攪拌(反應時間)→化合物i
篩選用於實現消除的鹼和條件
化合物xvii-1→鹼、溶劑、溫度、反應時間→化合物i
實施例:藥物製劑
可以使用標準程序將依魯替尼配製成藥學上可接受的製劑。
舉例來說,提供了一種用於製備包含依魯替尼或其衍生物的藥物製劑的方法,所述方法的特徵在於它包括如上文所限定的方法作為方法步驟。本領域技術人員將已知這樣的藥物製劑將包含什麼/由什麼組成(例如活性成分(即依魯替尼或其衍生物)和藥學上可接受的賦形劑、佐劑、稀釋劑和/或載體的混合物)。
還提供了一種用於製備包含依魯替尼(或其衍生物)的藥物製劑的方法,所述方法包括使依魯替尼或其藥學上可接受的鹽(其可以通過如上文所述的方法來形成)與一種或多種藥學上可接受的賦形劑、佐劑、稀釋劑和/或載體締合。
本文所述的實施例和實施方案具有說明性並且本領域技術人員所想到的各種改動方案或變化方案應當被包括在本公開內。
