分子內直接氨基化合成的吲哚並吡咯類化合物及合成方法與流程
2023-05-10 21:10:41 3
本發明屬於醫藥化工中間體及相關化學技術領域,具體涉及到多種吲哚並吡咯類化合物的綠色合成方法。
背景技術:
吲哚並吡咯類化合物廣泛應用於化學、醫藥領域,其化合物的骨架結構常可見於藥物,天然活性產物等分子結構中,例如,weidongding等人發現一種新的抗生素,其中吲哚並吡咯結構骨架就是其中不可或缺的一部分(thejournalofantibiotics1994,47,1250-1257);除此之外,飽和的吲哚並吡咯骨架結構,作為一種重要的藥效團結構,也常見於吲哚類生物鹼以及天然產物分子結構中,可見吲哚並吡咯類化合物的骨架具有廣闊的科研價值及市場前景。
文獻中報導過的合成吲哚並吡咯類化合物的方法非常罕見,只有一種通過疊氮類化合物氨基化反應(journalofthechemicalsociety,1984,1,2903-2909),但是此方法需要三步操作,存在原子經濟性不高,產物結構單一,適用性不廣,環境汙染等缺點。因此,如何通過更簡單的起始原料,較少的反應步驟,溫和的反應條件,以及使用廉價無汙染的催化劑或氧化劑來製備吲哚並吡咯類化合物的研究工作就十分必要。
技術實現要素:
本發明要解決的問題是提供一種高效的多取代吲哚並吡咯類化合物及其合成方法。
為達到上述目的,本發明的技術方案是這樣實現的:
一種吲哚並吡咯類化合物的合成方法,該方法包括將反應式(1)的化合物在催化劑、過氧化物、有機溶劑條件下反應,製得式(2)吲哚並吡咯類化合物,其反應通式如下:
其中r1為氫、甲基、甲氧基、羥基、氰基或滷素,其結合位置為4位或5位或6位;r2為氫、甲基、苄基或烯丙基;r3為氫、甲基、苄基或烯丙基;r4為甲基、乙基或苄基。
優選的,所述r1為滷素;r2為氫或苄基;r3為甲基;r4為苄基。
優選的,所述過氧化物為叔丁基過氧化氫、過氧化氫、過氧碳酸鈉、二叔丁基過氧化物、過氧化氫異丙苯、間氯過氧苯甲酸、過氧化苯甲酸叔丁酯、過硫酸氫鉀複合鹽、過硫酸鉀或醋酸碘苯中的一種。
優選的,所述過氧化物為叔丁基過氧化氫。
優選的,所述催化劑為含碘催化劑;更優選的,所述含碘催化劑為單質碘。
優選的,所述催化劑為含碘催化劑加鹼,其中,所述鹼為磷酸氫二鈉及其水合物、醋酸鈉、碳酸銫、三乙胺、碳酸鈉、碳酸鉀或氫氧化鈉中的一種。
優選的,所述鹼為磷酸氫二鈉水合物。
優選的,所述式(1)化合物、過氧化物、含碘催化劑和鹼的摩爾比為1:(1~2):(0.1~0.5):(1.5~5)。
優選的,所述有機溶劑為乙醇、甲醇、四氫呋喃、乙二醇二甲醚、乙酸乙酯或1,4-二氧六環中的一種;更優選的,所述有機溶劑為四氫呋喃或1,4-二氧六環;最優選的,所述有機溶劑為1,4-二氧六環。
優選的,所述有機溶劑的加入量為每0.5mmol式(1)化合物加入1~3ml溶劑。
優選的,所述反應溫度為30~90℃,反應時間為1~12小時;更優選的,所述反應溫度為80℃;反應時間為1.5小時。
本發明還提供了一種吲哚並吡咯類化合物,所述化合物具有式(2)所示的化學結構:
其中,r1為氫、甲基、甲氧基、羥基、氰基或滷素,其結合位置為4位或5位或6位;r2為氫、甲基、苄基或烯丙基;r3為氫、甲基、苄基或烯丙基;r4為甲基、乙基或苄基。
相對於現有技術,本發明所述的分子內直接氨基化來合成吲哚並吡咯類化合物的方法具有以下優勢:
本發明方法的合成路線短、起始原料簡單、反應條件溫和、過氧化物價廉無汙染,底物範圍廣,產物易分離,並且當擴大到克級的反應的時候,我們的反應也能得到很好的適用性。
附圖說明
構成本發明的一部分的附圖用來提供對本發明的進一步理解,本發明的示意性實施例及其說明用於解釋本發明,並不構成對本發明的不當限定。在附圖中:
圖1是實施例1-6化合物1a的1h核磁、13c核磁譜圖;圖2是實施例7化合物2a的1h核磁、13c核磁譜圖;圖3是實施例8化合物3a的1h核磁、13c核磁譜圖;圖4是實施例9化合物4a的1h核磁、13c核磁譜圖;圖5是實施例10化合物5a的1h核磁、13c核磁譜圖;圖6是實施例11化合物6a的1h核磁、13c核磁譜圖;圖7是實施例12化合物7a的1h核磁、13c核磁譜圖;圖8是實施例13化合物8a的1h核磁、13c核磁譜圖;圖9是實施例14化合物9a的1h核磁、13c核磁譜圖;圖10是實施例15化合物10a的1h核磁、13c核磁譜圖;圖11是實施例16化合物11a的1h核磁、13c核磁譜圖;圖12是實施例17化合物12a的1h核磁、13c核磁譜圖;圖13是實施例18化合物13a的1h核磁、13c核磁譜圖;圖14是實施例19化合物14a的1h核磁、13c核磁譜圖;圖15是實施例20化合物15a的1h核磁、13c核磁譜圖;圖16是實施例21化合物16a的1h核磁、13c核磁譜圖。
具體實施方式
除有定義外,以下實施例中所用的技術術語具有與本發明所屬領域技術人員普遍理解的相同含義。以下實施例中所用的試驗試劑,如無特殊說明,均為常規生化試劑;所述實驗方法,如無特殊說明,均為常規方法。
下面結合實施例來詳細說明本發明。
起初篩選反應是在色氨酸甲酯鹽酸鹽投的0.5mmol的條件下進行的,當我們將原料色氨酸甲酯鹽酸鹽投的量擴大到g級進行反應時,發現也取得了很高的產率。即在圓底燒瓶中加入色氨酸甲酯鹽酸鹽(10.0mmol,2.6g)、單質碘(3.0mmol,761.4mg)叔丁基過氧化氫(10.0mmol,1.4ml)、1,4-二氧六環40ml,封口,在80℃下攪拌反應4小時。冷卻至室溫,減壓除去溶劑後,通過柱層析分離純化(洗脫劑為石油醚/丙酮=5:1)得到methyl1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate1.3g,產率61%。
實施例1:methyl1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(1a)的合成
在反應器中加入色氨酸甲酯鹽酸鹽(0.5mmol,127.4mg)、單質碘(0.15mmol,38.1mg)、叔丁基過氧化氫(0.5mmol,75μl)、磷酸氫二鈉十二水合物(1.75mmol,626.8mg)、1,4-二氧六環2ml,封口,在80℃下攪拌反應1.5小時。冷卻至室溫,減壓除去溶劑後,通過柱層析分離純化(洗脫劑為石油醚/丙酮=5:1)得到methyl1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(1a)94.3mg,產率88%。
1hnmr(400mhz,dmso-d6):δ11.90(s,1h),11.11(s,1h),7.63(d,j=7.6hz,1h),7.33(d,j=7.9hz,1h),7.14–7.08(m,2h),7.02(t,j=7.4hz,1h),3.79(s,3h);13cnmr(101mhz,dmso-d6):δ162.0,142.9,141.8,121.9,121.2,120.1,119.5,119.2,112.2,109.7,107.4,51.3.
實施例2:methyl1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(1a)的合成
在反應器中加入色氨酸甲酯鹽酸鹽(0.5mmol,127.4mg)、單質碘(0.15mmol,38.1mg)、過氧碳酸鈉(0.5mmol,78.5mg)、磷酸氫二鈉十二水合物(1.75mmol,626.8mg)、1,4-二氧六環2ml,封口,在80℃下攪拌反應1.5小時。冷卻至室溫,減壓除去溶劑後,通過柱層析分離純化(洗脫劑為石油醚/丙酮=5:1)得到methyl1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(1a)63.1mg,產率59%。
實施例3:methyl1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(1a)的合成
在反應器中加入色氨酸甲酯鹽酸鹽(0.5mmol,127.4mg)、四丁基碘化銨(0.15mmol,55.4mg)、叔丁基過氧化氫(0.5mmol,75μl)、磷酸氫二鈉十二水合物(1.75mmol,626.8mg)、1,4-二氧六環2ml,封口,在80℃下攪拌反應1.5小時。冷卻至室溫,減壓除去溶劑後,通過柱層析分離純化(洗脫劑為石油醚/丙酮=5:1)得到methyl1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(1a)34.3mg,產率32%。
實施例4:methyl1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(1a)的合成
在反應器中加入色氨酸甲酯鹽酸鹽(0.5mmol,127.4mg)、單質碘(0.15mmol,38.1mg)、叔丁基過氧化氫(0.5mmol,75μl)、磷酸氫二鈉十二水合物(1.75mmol,626.8mg)、四氫呋喃2ml,封口,在80℃下攪拌反應1.5小時。冷卻至室溫,減壓除去溶劑後,通過柱層析分離純化(洗脫劑為石油醚/丙酮=5:1)得到methyl1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(1a)43.9mg,產率41%。
實施例5:methyl1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(1a)的合成
在反應器中加入色氨酸甲酯鹽酸鹽(0.5mmol,127.4mg)、單質碘(0.15mmol,38.1mg)、叔丁基過氧化氫(0.5mmol,75μl)、醋酸鈉(1.75mmol,143.6mg)、1,4-二氧六環2ml,封口,在80℃下攪拌反應1.5小時。冷卻至室溫,減壓除去溶劑後,通過柱層析分離純化(洗脫劑為石油醚/丙酮=5:1)得到methyl
1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(1a)69.6mg,產率65%。
實施例6:methyl1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(1a)的合成
在反應器中加入色氨酸甲酯鹽酸鹽(0.5mmol,127.4mg)、單質碘(0.15mmol,38.1mg)、叔丁基過氧化氫(0.5mmol,75μl)、磷酸氫二鈉十二水合物(1.75mmol,626.8mg)、1,4-二氧六環2ml,封口,在40℃下攪拌反應1.5小時。冷卻至室溫,減壓除去溶劑後,通過柱層析分離純化(洗脫劑為石油醚/丙酮=5:1)得到methyl1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(1a)77.3mg,產率72%。
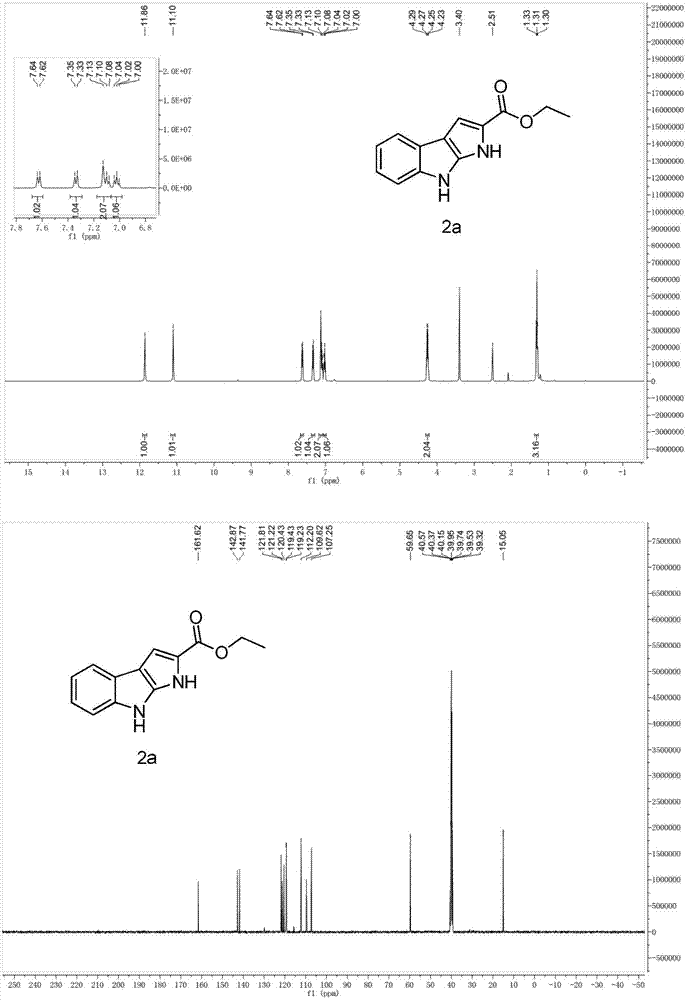
實施例7:methyl1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(2a)的合成
在反應器中加入色氨酸乙酯鹽酸鹽(0.5mmol,134.4mg)、單質碘(0.15mmol,38.1mg)、叔丁基過氧化氫(0.5mmol,75μl)、磷酸氫二鈉十二水合物(1.75mmol,626.8mg)、1,4-二氧六環2ml,封口,在80℃下攪拌反應1.5小時。冷卻至室溫,減壓除去溶劑後,通過柱層析分離純化(洗脫劑為石油醚/丙酮=5:1)得到ethyl1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(2a)106.5mg,產率93%。
1hnmr(400mhz,dmso-d6):11.86(s,1h),11.10(s,1h),7.63(d,j=7.6hz,1h),7.34(d,j=7.9hz,1h),7.13–7.08(m,2h),7.02(t,j=7.5hz,1h),4.26(q,j=6.8hz,2h),1.31(t,j=6.9hz,3h);13cnmr(101mhz,dmso-d6):δ161.6,142.9,141.8,121.8,121.2,120.4,119.4,119.2,112.2,109.6,107.2,59.7,15.0.
實施例8:methyl5-hydroxy-1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(3a)的合成
合成式(1)化合物的步驟:
將5-羥基色氨酸(198mg,0.9mmol)置於50ml圓底燒瓶中,在0℃下加入16ml甲醇,然後將hcl/meoh(1.25m)逐滴加入,直到溶液變澄清,繼續在該溫度下攪拌反應15min,減壓蒸餾旋幹並在高真空環境下乾燥1h;然後將其溶於無水甲醇中,在0℃下逐滴加入二甲基亞碸(0.66ml,9mmol),將其置於室溫下反應0.5h後回流3h,冷卻並減壓旋蒸,加入適量甲苯帶走多餘的二甲基亞碸(可多次加入旋幹直至形成固體產物);最後得到綠色的固體產物(234mg,產率96%),即為式(1)化合物5-羥基色氨酸甲酯鹽酸鹽,無需進一步純化。
合成式(2)化合物的步驟:
在反應器中加入5-羥基色氨酸甲酯鹽酸鹽(0.5mmol,135.4mg)、單質碘(0.15mmol,38.1mg)、叔丁基過氧化氫(0.5mmol,75μl)、磷酸氫二鈉十二水合物(1.75mmol,626.8mg)、1,4-二氧六環2ml,封口,在80℃下攪拌反應1.5小時。冷卻至室溫,減壓除去溶劑後,通過柱層析分離純化(洗脫劑為石油醚/丙酮=3:1)得到methyl5-hydroxy-1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(3a)42.0mg,產率37%。
1hnmr(400mhz,dmso-d6):δ11.74(s,1h),10.69(s,1h),8.75(s,1h),7.11–7.07(m,2h),7.00(s,1h),6.59(d,j=7.4hz,1h),3.77(s,3h);13cnmr(101mhz,dmso-d6):δ162.0,151.2,143.8,135.7,122.0,119.7,112.4,110.5,109.8,107.5,105.1,51.2.
實施例9:methyl5-methoxy-1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(4a)的合成
合成式(1)化合物的步驟:
將實施例8中的5-羥基色氨酸(198mg,0.9mmol)替換為5-甲氧基色氨酸(218mg,0.9mmol),其他方法及條件同實施例8,最後得到綠色的固體產物(248mg,產率97%),即為式(1)化合物5-甲氧基色氨酸甲酯鹽酸鹽。
合成式(2)化合物的步驟:
在反應器中加入5-甲氧基色氨酸甲酯鹽酸鹽(0.5mmol,142.4mg)、單質碘(0.15mmol,38.1mg)、叔丁基過氧化氫(0.5mmol,75μl)、磷酸氫二鈉十二水合物(1.75mmol,626.8mg)、1,4-二氧六環2ml,封口,在80℃下攪拌反應1.5小時。冷卻至室溫,減壓除去溶劑後,通過柱層析分離純化(洗脫劑為石油醚/丙酮=5:1)得到methyl5-methoxy-1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(1a)50.1mg,產率41%。
1hnmr(400mhz,dmso-d6):δ11.80(s,1h),10.84(s,1h),7.21–7.19(m,2h),7.09(s,1h),6.72(dd,j=8.8,2.5hz,1h),3.78(s,3h),3.77(s,3h);13cnmr(101mhz,dmso-d6):δ162.0,153.8,143.7,136.5,129.8,121.7,120.0,112.6,109.9,107.4,103.3,55.9,51.3.
實施例10:methyl4-methoxy-1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(5a)的合成
合成式(1)化合物的步驟:
將實施例8中的5-羥基色氨酸(198mg,0.9mmol)替換為4-甲氧基色氨酸(218mg,0.9mmol),其他方法及條件同實施例8,最後得到綠色的固體產物(248mg,產率97%),即為式(1)化合物4-甲氧基色氨酸甲酯鹽酸鹽。
合成式(2)化合物的步驟:
在反應器中加入4-甲氧基色氨酸甲酯鹽酸鹽(0.5mmol,142.4mg)、單質碘(0.15mmol,38.1mg)、叔丁基過氧化氫(0.5mmol,75μl)、磷酸氫二鈉十二水合物(1.75mmol,626.8mg)、1,4-二氧六環2ml,封口,在80℃下攪拌反應1.5小時。冷卻至室溫,減壓除去溶劑後,通過柱層析分離純化(洗脫劑為石油醚/丙酮=5:1)得到methylmethyl4-methoxy-1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(5a)71.0mg,產率63%。
1hnmr(400mhz,dmso-d6):δ11.90(s,1h),11.14(s,1h),7.06–7.01(m,2h),6.96(d,j=8.0hz,1h),6.61(d,j=7.9hz,1h),3.91(s,3h),3.78(s,3h);13cnmr(101mhz,dmso-d6):δ162.0,153.1,142.8,141.8,123.0,120.0,110.7,108.3,107.7,105.7,101.3,55.7,51.3.
實施例11:methyl5-methyl-1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(6a)的合成
合成式(1)化合物的步驟:
將實施例8中的5-羥基色氨酸(198mg,0.9mmol)替換為5-甲基色氨酸(200mg,0.9mmol),其他方法及條件同實施例8,最後得到白色的固體產物(237mg,產率98%),即為式(1)化合物5-甲基色氨酸甲酯鹽酸鹽。
合成式(2)化合物的步驟:
在反應器中加入5-甲基色氨酸甲酯鹽酸鹽(0.5mmol,134.4mg)、單質碘(0.15mmol,38.1mg)、叔丁基過氧化氫(0.5mmol,75μl)、磷酸氫二鈉十二水合物(1.75mmol,626.8mg)、1,4-二氧六環2ml,封口,在80℃下攪拌反應1.5小時。冷卻至室溫,減壓除去溶劑後,通過柱層析分離純化(洗脫劑為石油醚/丙酮=5:1)得到methyl5-methyl-1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(6a)85.5mg,產率75%。
1hnmr(400mhz,dmso-d6):δ11.85(s,1h),10.96(s,1h),7.42(s,1h),7.21(d,j=8.2hz,1h),7.10(s,1h),6.92(d,j=8.2hz,1h),3.78(s,3h),2.38(s,3h);13cnmr(101mhz,dmso-d6):δ162.0,143.3,140.0,128.0,123.0,121.3,119.9,119.4,111.9,109.6,107.3,51.3,21.6.
實施例12:methyl5-cyano-1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(7a)的合成
合成式(1)化合物的步驟:
將實施例8中的5-羥基色氨酸(198mg,0.9mmol)替換為5-氰基色氨酸(213mg,0.9mmol),其他方法及條件同實施例8,最後得到白色的固體產物(244mg,產率97%),即為式(1)化合物5-氰基色氨酸甲酯鹽酸鹽。
合成式(2)化合物的步驟:
在反應器中加入5-氰基色氨酸甲酯鹽酸鹽(0.5mmol,139.9mg)、單質碘(0.15mmol,38.1mg)、叔丁基過氧化氫(0.5mmol,75μl)、磷酸氫二鈉十二水合物(1.75mmol,626.8mg)、1,4-二氧六環2ml,封口,在80℃下攪拌反應1.5小時。冷卻至室溫,減壓除去溶劑後,通過柱層析分離純化(洗脫劑為石油醚/丙酮=3:1)得到methyl5-cyano-1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(7a)55.5mg,產率46%。
1hnmr(400mhz,dmso-d6):δ12.21(s,1h),11.85(s,1h),8.14(s,1h),7.49(s,2h),7.21(s,1h),3.81(s,3h);13cnmr(101mhz,dmso-d6):δ161.9,143.8,143.3,125.2,123.7,121.6,121.2,113.1,108.9,107.5,101.1,51.5.
實施例13:methyl5-fluoro-1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(8a)的合成
合成式(1)化合物的步驟:
將實施例8中的5-羥基色氨酸(198mg,0.9mmol)替換為5-氟色氨酸(210mg,0.9mmol),其他方法及條件同實施例8,最後得到黃色的固體產物(238mg,產率97%),即為式(1)化合物5-氟色氨酸甲酯鹽酸鹽。
合成式(2)化合物的步驟:
在反應器中加入5-氟色氨酸甲酯鹽酸鹽(0.5mmol,136.4mg)、單質碘(0.15mmol,38.1mg)、叔丁基過氧化氫(0.5mmol,75μl)、磷酸氫二鈉十二水合物(1.75mmol,626.8mg)、1,4-二氧六環2ml,封口,在80℃下攪拌反應1.5小時。冷卻至室溫,減壓除去溶劑後,通過柱層析分離純化(洗脫劑為石油醚/丙酮=5:1)得到methyl5-fluoro-1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(8a)70.5mg,產率61%。
1hnmr(400mhz,dmso-d6):δ11.95(s,1h),11.18(s,1h),7.43(dd,j=9.8,2.6hz,1h),7.31–7.27(m,1h),7.13(s,1h),6.92(td,j=9.2,2.7hz,1h),3.79(s,3h);13cnmr(101mhz,dmso-d6):δ162.0,158.4,156.1,144.0,138.2,121.7,121.6,120.6,112.7,112.6,109.6,109.6,108.9,108.7,107.5,105.2,104.9,51.4.
實施例14:methyl5-chloro-1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(9a)的合成
合成式(1)化合物的步驟:
將實施例8中的5-羥基色氨酸(198mg,0.9mmol)替換為5-氯色氨酸(221mg,0.9mmol),其他方法及條件同實施例8,最後得到白色的固體產物(247mg,產率95%),即為式(1)化合物5-氯色氨酸甲酯鹽酸鹽。
合成式(2)化合物的步驟:
在反應器中加入5-氯色氨酸甲酯鹽酸鹽(0.5mmol,144.6mg)、單質碘(0.15mmol,38.1mg)、叔丁基過氧化氫(0.5mmol,75μl)、磷酸氫二鈉十二水合物(1.75mmol,626.8mg)、1,4-二氧六環2ml,封口,在80℃下攪拌反應1.5小時。冷卻至室溫,減壓除去溶劑後,通過柱層析分離純化(洗脫劑為石油醚/丙酮=5:1)得到methyl5-chloro-1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(9a)90.1mg,產率72%。
1hnmr(400mhz,dmso-d6):δ12.01(s,1h),11.33(s,1h),7.70(s,1h),7.34(d,j=8.5hz,1h),7.16(s,1h),7.12(d,j=8.4hz,1h),3.81(s,3h);13cnmr(101mhz,dmso-d6):δ162.0,143.5,140.2,123.8,122.4,121.4,120.9,118.7,113.4,109.0,107.5,51.4.實施例15:methyl6-chloro-1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(10a)的合成
合成式(1)化合物的步驟:
將實施例8中的5-羥基色氨酸(198mg,0.9mmol)替換為6-氯色氨酸(221mg,0.9mmol),其他方法及條件同實施例8,最後得到白色的固體產物(247mg,產率95%),即為式(1)化合物6-氯色氨酸甲酯鹽酸鹽。
合成式(2)化合物的步驟:
在反應器中加入6-氯色氨酸甲酯鹽酸鹽(0.5mmol,144.6mg)、單質碘(0.15mmol,38.1mg)、叔丁基過氧化氫(0.5mmol,75μl)、磷酸氫二鈉十二水合物(1.75mmol,626.8mg)、1,4-二氧六環2ml,封口,在80℃下攪拌反應1.5小時。冷卻至室溫,減壓除去溶劑後,通過柱層析分離純化(洗脫劑為石油醚/丙酮=5:1)得到methyl6-chloro-1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(10a)79.8mg,產率64%。
1hnmr(400mhz,dmso-d6):δ12.05(s,1h),11.37(s,1h),7.66(d,j=8.3hz,1h),7.38(s,1h),7.18(s,1h),7.09(d,j=8.4hz,1h),3.83(s,3h);13cnmr(101mhz,dmso-d6):δ162.0,143.1,142.3,126.0,120.7,120.3,120.0,119.4,111.9,109.1,107.3,51.4.
實施例16:methyl5-bromo-1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(11a)的合成
合成式(1)化合物的步驟:
將實施例8中的5-羥基色氨酸(198mg,0.9mmol)替換為5-溴色氨酸(255mg,0.9mmol),其他方法及條件同實施例8,最後得到白色的固體產物(291mg,產率97%),即為式(1)化合物5-溴色氨酸甲酯鹽酸鹽。
合成式(2)化合物的步驟:
在反應器中加入5-溴色氨酸甲酯鹽酸鹽(0.5mmol,166.8mg)、單質碘(0.15mmol,38.1mg)、叔丁基過氧化氫(0.5mmol,75μl)、磷酸氫二鈉十二水合物(1.75mmol,626.8mg)、1,4-二氧六環2ml,封口,在80℃下攪拌反應1.5小時。冷卻至室溫,減壓除去溶劑後,通過柱層析分離純化(洗脫劑為石油醚/丙酮=5:1)得到methyl5-bromo-1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(11a)130.1mg,產率89%。
1hnmr(400mhz,dmso-d6):δ12.03(s,1h),11.37(s,1h),7.83(s,1h),7.29(d,j=8.5hz,1h),7.22(d,j=8.6hz,1h),7.15(s,1h),3.79(s,3h);13cnmr(101mhz,dmso-d6):δ161.9,143.3,140.4,124.0,123.0,121.6,120.9,114.0,111.6,108.9,107.5,51.4.
實施例17:methyl8-methyl-1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(12a)的合成
合成式(1)化合物的步驟:
將實施例8中的5-羥基色氨酸(198mg,0.9mmol)替換為n1-甲基色氨酸(200mg,0.9mmol),其他方法及條件同實施例8,最後得到白色的固體產物(237mg,產率98%),即為式(1)化合物n1-甲基色氨酸甲酯鹽酸鹽。
合成式(2)化合物的步驟:
在反應器中加入n1-甲基色氨酸甲酯鹽酸鹽(0.5mmol,134.4mg)、單質碘(0.15mmol,38.1mg)、叔丁基過氧化氫(0.5mmol,75μl)、磷酸氫二鈉十二水合物(1.75mmol,626.8mg)、1,4-二氧六環2ml,封口,在80℃下攪拌反應1.5小時。冷卻至室溫,減壓除去溶劑後,通過柱層析分離純化(洗脫劑為純二氯甲烷)得到methyl8-methyl-1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(12a)88.9mg,產率83%。
1hnmr(400mhz,dmso-d6):δ12.11(s,1h),7.66(d,j=7.4hz,1h),7.38(d,j=8.0hz,1h),7.20–7.17(m,2h),7.10–7.06(m,1h),3.81(s,3h),3.80(s,3h);13cnmr(101mhz,dmso-d6):δ162.0,144.3,142.2,121.9,120.9,120.3,119.7,119.5,110.1,108.4,107.8,51.4,30.3.
實施例18:methyl8-allyl-1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(13a)的合成
合成式(1)化合物的步驟:
在25ml圓底燒瓶中加入n-boc色氨酸甲酯(636.7mg,2mmol)和nah(120mg,2mmol),氮氣保護下加入4ml無水thf並將其置於-50℃攪拌反應30min,然後將烯丙基溴(296.3mg,2.4mmol)逐滴加入,室溫攪拌反應3h後,加入3ml水將其猝滅,用乙酸乙酯萃取,無水硫酸鈉乾燥,減壓旋幹後通過柱層析分離純化(洗脫劑為石油醚/乙酸乙酯=20:1)得到n1-烯丙基-n-boc色氨酸甲酯(400mg,56%)。高真空環境下乾燥3h後,將其溶於4.5ml無水甲醇中,並加入hcl/meoh(1.12ml,4m),然後回流反應2h,冷卻並減壓旋蒸,得到白色的固體產物(313.6mg,產率95%),即為式(1)化合物n1-烯丙基色氨酸甲酯鹽酸鹽。
合成式(2)化合物的步驟:
在反應器中加入n1-烯丙基色氨酸甲酯鹽酸鹽(0.5mmol,147.4mg)、單質碘(0.15mmol,38.1mg)、叔丁基過氧化氫(0.5mmol,75μl)、磷酸氫二鈉十二水合物(1.75mmol,626.8mg)、1,4-二氧六環2ml,封口,在80℃下攪拌反應1.5小時。冷卻至室溫,減壓除去溶劑後,通過柱層析分離純化(洗脫劑為石油醚/二氯甲烷=1:1)得到methyl8-allyl-1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(13a)100.0mg,產率79%。
1hnmr(400mhz,dmso-d6):δ12.09(s,1h),7.67(d,j=7.6hz,1h),7.37(d,j=8.0hz,1h),7.18–7.14(m,2h),7.08(t,j=7.6hz,1h),5.99–5.92(m,1h),5.12(d,j=10.3hz,1h),5.02(d,j=17.1hz,1h),4.94(s,2h),3.80(s,3h);13cnmr(101mhz,dmso-d6):δ162.0,143.6,141.4,133.6,122.0,121.1,120.4,119.8,119.6,117.2,110.6,108.6,107.7,51.4,45.8.
實施例19:methyl1-benzyl-1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(14a)的合成
合成式(1)化合物的步驟:
在25ml圓底燒瓶中加入色氨酸甲酯鹽酸鹽(509.42mg,2mmol),cs2co3(977.5mg,3mmol),[cu(oh)tmeda]2cl2(46.4mg,0.1mmol),氮氣保護下加入3ml無水乙腈,室溫下攪拌反應15min後,逐滴加入溴化苄(410.5mg,2.4mmol),繼續攪拌反應過夜,加入5ml水將其猝滅,並用乙酸乙酯萃取,無水硫酸鈉乾燥,減壓旋幹後通過柱層析分離純化(洗脫劑為石油醚/乙酸乙酯=3:1)得到白色固體產物,即為式(1)化合物n-苄基色氨酸甲酯(250mg,產率41%)。
合成式(2)化合物的步驟:
在反應器中加入n-苄基色氨酸甲酯(0.5mmol,154.2mg)、單質碘(0.15mmol,38.1mg)、叔丁基過氧化氫(0.5mmol,75μl)、磷酸氫二鈉十二水合物(1.75mmol,626.8mg)、1,4-二氧六環2ml,封口,在80℃下攪拌反應1.5小時。冷卻至室溫,減壓除去溶劑後,通過柱層析分離純化(洗脫劑為石油醚/乙酸乙酯=10:1)得到methyl1-benzyl-1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(14a)60.5mg,產率40%。
1hnmr(400mhz,cdcl3):δ7.70(s,1h),7.59(s,1h),7.38(s,1h),7.25(s,2h),7.13(d,j=16.2hz,5h),5.66(s,2h),3.77(s,3h);13cnmr(101mhz,cdcl3):δ162.5,144.2,140.8,136.9,129.0,127.8,126.9,122.3,121.8,120.6,120.3,119.6,111.7,110.0,108.9,51.1,49.3.
實施例20:methyl1-allyl-1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(15a)的合成
合成式(1)化合物的步驟:
將實施例19中的溴化苄(410.5mg,2.4mmol)替換為烯丙基溴(296.3mg,2.4mmol),其他方法及條件同實施例19,最後得到黃色固體產物(207mg,產率40%),即為式(1)化合物n-烯丙基色氨酸甲酯。
合成式(2)化合物的步驟:
在反應器中加入n-烯丙基色氨酸甲酯(0.5mmol,129.2mg)、單質碘(0.15mmol,38.1mg)、叔丁基過氧化氫(0.5mmol,75μl)、磷酸氫二鈉十二水合物(1.75mmol,626.8mg)、1,4-二氧六環2ml,封口,在80℃下攪拌反應1.5小時。冷卻至室溫,減壓除去溶劑後,通過柱層析分離純化(洗脫劑為石油醚/乙酸乙酯=10:1)得到methyl1-allyl-1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(15a)30.0mg,產率24%。
1hnmr(400mhz,cdcl3):δ7.92(s,1h),7.71–7.69(m,1h),7.34(s,1h),7.30–7.28(m,1h),7.20–7.16(m,2h),6.07–6.00(m,1h),5.20(d,j=10.3hz,1h),5.14(d,j=5.2hz,2h),5.06(d,j=17.1hz,1h),3.84(s,3h);13cnmr(101mhz,cdcl3):δ162.5,144.2,140.9,133.5,122.3,121.9,120.6,120.0,119.6,117.1,111.7,109.7,108.8,51.1,48.2.
實施例21:ethyl1-benzyl-1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(16a)的合成
合成式(1)化合物的步驟:
將實施例19中的色氨酸甲酯鹽酸鹽(509.42mg,2mmol)替換為色氨酸乙酯鹽酸鹽(537.5,2mmol),其他方法及條件同實施例19,最後得到淡黃色油狀產物(400mg,產率62%),即為式(1)化合物n-苄基色氨酸乙酯。
合成式(2)化合物的步驟:
在反應器中加入n-苄基色氨酸乙酯(0.5mmol,161.2mg)、單質碘(0.15mmol,38.1mg)、叔丁基過氧化氫(0.5mmol,75μl)、磷酸氫二鈉十二水合物(1.75mmol,626.8mg)、1,4-二氧六環2ml,封口,在80℃下攪拌反應1.5小時。冷卻至室溫,減壓除去溶劑後,通過柱層析分離純化(洗脫劑為石油醚/丙酮=5:1)得到ethyl1-benzyl-1,8-dihydropyrrolo[2,3-b]indole-2-carboxylate(16a)61.9mg,產率39%。
1hnmr(400mhz,cdcl3):δ7.70–7.68(m,2h),7.40(s,1h),7.23–7.22(m,2h),7.16–7.12(m,3h),7.10–7.07(m,2h),5.65(s,2h),4.22(q,j=7.1hz,2h),1.31(t,j=7.1hz,3h);13cnmr(101mhz,cdcl3):δ162.2,144.2,140.8,137.1,128.9,127.8,126.9,122.2,121.8,120.6,120.5,119.5,111.7,109.9,108.8,59.8,49.3,14.5.
以上所述僅為本發明的較佳實施例而已,並不用以限制本發明,凡在本發明的精神和原則之內,所作的任何修改等同替換改進等,均應包含在本發明的保護範圍之內。
