一種製備手性二氫1,4-苯並噁嗪類化合物的方法與流程
2023-11-01 03:16:52 1
本發明屬於有機合成領域,具體涉及一種由鄰氨基苯酚類化合物和炔丙基類化合物通過不對稱[4+2]環加成反應合成手性二氫1,4-苯並噁嗪類化合物的方法。
背景技術:
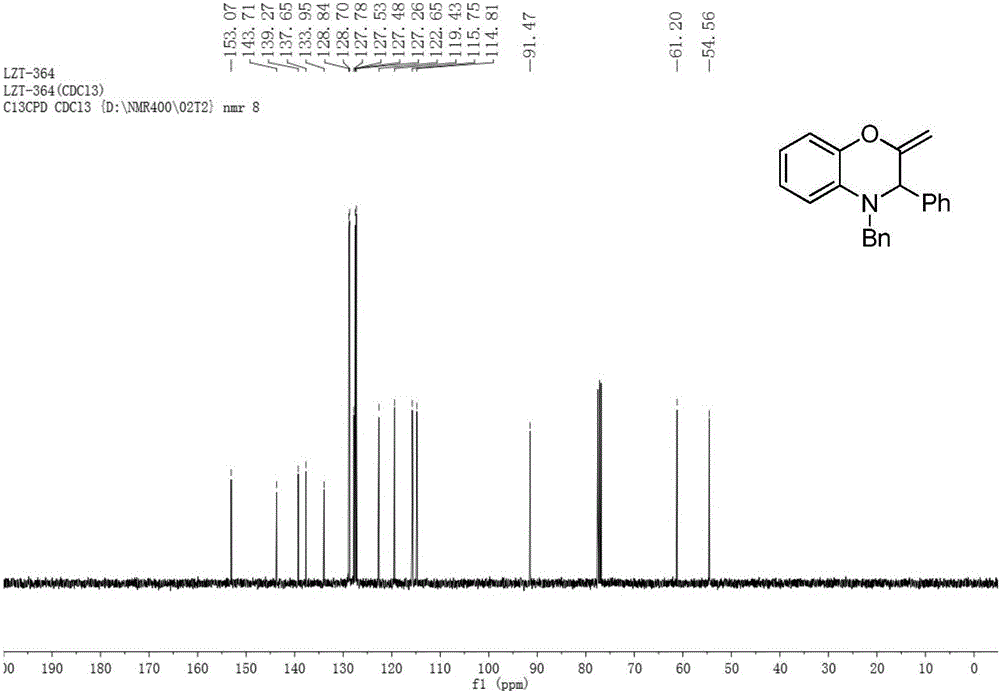
:許多1,4-苯並噁嗪類衍生物在臨床醫學和生物學上具有極其重要的生物活性,常見的有細胞內鈣拮抗物、風溼藥、鉀通道活化劑、神經抗氧化劑、降壓藥、抗菌劑、凝血酶阻聚劑、抗炎藥、抗生素C-1027等等[(a)Yamazaki,A.;Achiwa,I.;Achiwa,K.Tetrahedron:Asymmetry.1996,7,403.(b)J.;Jakopin,T.;Stegnar,M.;Kikelj,D.J.Med.Chem.2008,51,5617.(c)Otsuka,H.;Hirai,Y.Nagao,T.;Yamasaki,K.JournalofNaturalProducts1988,51,74.(d)Minami,Y.;Yoshida,K.;Azuma,R.;Saeki,M.;Otani,T.TetrahedronLett.1993,34,2633.(e)Touzeau,F.;Arrault,A.;Guillaumet,G.;Scalbert,E.;Pfeiffer,B.;Rettori,M.;Renard,P.;Mérour,J.-Y.J.Med.Chem.2003,46,1962.(f)Largeron,M.;Fleury,M.-B.TetrahedronLett.1998,39,8999.(g)Largeron,M.;Lockhart,B.;Pfeiffer,B.;Fleury,M.-B.J.Med.Chem.1999,42,5043.(h)Matsuoka,H.;Ohi,N.;Mihara,M.;Suzuki,H.;Miyamoto,K.;Maruyama,N.;Tsuji,K.;Kato,N.;Akimoto,T.;Takeda,Y.;Yano,K.;Kuroki,T.J.Med.Chem.1997,40,105–111.在這些具有藥物活性的二氫1,4-苯並噁嗪類化合物中,通常含有手性碳中心,即為手性二氫1,4-苯並噁嗪類化合物。因此發展不對稱合成方法來製備手性二氫1,4-苯並噁嗪類化合物具有重要的意義。二氫1,4-苯並噁嗪類化合物的製備,多以2-滷苯酚,2-氨基苯酚和2-硝基苯酚為起始底物,與合適底物進行環加成反應得到;也有通過環氧化物開環或者取代反應生成單取代產物,接著進行分子內環化反應得到目標產物。[(a)Albanese,D.;Landini,D.;Lupi,V.;Penso,M.Ind.Eng.Chem.Res.2003,42,680.(b)Kuroita,T.;Sakamori,M.;Kawakita,T.Chem.Pharm.Bull.1996,44,756.(c)Singh,S.K.;Bajpai,A.K.;Saini,R.TetrahedronLetters2013,54,7132.(d)Matsumoto,Y.;Tsuzuki,R.;Matsuhisa,A.;Takayama,K.;Yoden,T.;Uchida,W.;Asano,M.;Fujita,S.;Yanagisawa,I.;Fujikura,T.Chem.Pharm.Bull.1996,44,103.(e)Albanese,D.;Landini,D.;Lupi,V.;Penso,M.Ind.Eng.Chem.Res.2003,42,680.(f)Brahma,K.;Das,B.;Chowdhury,C.Tetrahedron2014,70,5863.(g)Rao,R.K.Naidu,A.B.;Sekar,G.Org.Lett.2009,11,1923.(h)Largeron,M.;Lockhart,B.;Pfeiffer,B.;Fleury,M.B.J.Med.Chem.1999,42,5043.(i)Ramesh,C.;Raju,B.R.;Kavala,V.;Kuo,C.-W.;Yao,C.-F.Tetrahedron2011,67,1187.(j)Sharifi,A.;Abaee,M.S.; Mokhtare,Z.;Mirzaei,M.EnvironmentalChemistryLetters2014,12,365.(k)Yu,G.;Zheng,Y.;Wu,J.;Dai,W.-M.Tetrahedron2013,69,10488.(l)Zidar,N.;Kikelj,D.Tetrahedron2008,64,5756.(m)Trost,B.M.;VanVranken,D.L.;Bingel,C.J.Am.Chem.Soc.1992,114,9327.(n)Feng,G.;Wu,J.;Dai,W.-M.Tetrahedron2006,62,4635.(o)Ramesh,C.;Raju,B.R.;Kavala,V.;Kuo,C.-W.;Yao,C.-F.Tetrahedron2011,67,1187.本專利利用手性銅催化劑催化鄰氨基苯酚類化合物與炔丙基類化合物進行[4+2]不對稱環加成反應,高收率和高對映選擇性地得到了手性二氫1,4-苯並噁嗪類化合物,為手性二氫1,4-苯並噁嗪類化合物提供了一條操作簡單,高收率,對映選擇性高的合成新路線。技術實現要素:本發明的目的是提供一種銅催化的鄰氨基苯酚類化合物與炔丙基類化合物通過[4+2]不對稱環加成反應來合成手性二氫1,4-苯並噁嗪類化合物的方法。本發明具有原料易得,操作簡單,反應條件溫和,對映選擇性高等特點。本發明提供了一種手性二氫1,4-苯並噁嗪類化合物的催化不對稱合成方法,在鹼添加劑的存在下,手性銅催化劑在反應介質中催化鄰氨基苯酚類化合物與炔丙基類化合物通過[4+2]不對稱環加成反應合成手性二氫1,4-苯並噁嗪類化合物,具體步驟為:(1)手性銅催化劑的製備:氮氣保護下,將銅鹽與手性P,N,N-配體按摩爾比1:0.1-1:10在反應介質中攪拌0.5-2小時製得手性銅催化劑;(2)手性二氫1,4-苯並噁嗪類化合物的製備:將鄰氨基苯酚類化合物、炔丙基類化合物和鹼添加劑溶於反應介質中,然後將該溶液在氮氣保護下加入到上述步驟(1)中製得的手性銅催化劑的溶液中,室溫攪拌反應1-24小時;反應完畢,減壓旋蒸,柱層析分離,得到手性二氫1,4-苯並噁嗪類化合物;上述步驟(2)中所述手性銅催化劑與炔丙基類化合物的摩爾比為0.001:1-1:1;所述鹼添加劑與炔丙基類化合物的摩爾比為0-10:1;所述鄰氨基苯酚類化合物與炔丙基類化合物的摩爾比為1:1-2:1。所述手性二氫1,4-苯並噁嗪類化合物具有以下兩種結構之一:I和II互為對映異構體,式中,R1,R2為C1-C40的烷基、C3-C12的環烷基、帶有取代基的C3-C12環烷基、苯基、取代苯基、苄基、取代苄基、含一個或二個以上氧、硫、氮原子的五元或六元雜環芳香基團或酯基中的 一種或兩種以上;上述C3-C12環烷基上的取代基、苯基上的取代基和苄基上的取代基為C1-C40烷基、C1-C40的烷氧基、滷素、硝基、酯基或氰基中的一種或兩種以上。所述反應介質為甲醇、乙醇、甲苯、苯、二甲苯、二氯甲烷、二氯乙烷、乙醚、四氫呋喃或乙酸乙酯中的一種或兩種以上。所述鄰氨基苯酚類化合物具有以下結構:式中:R1為C1-C40的烷基、C3-C12的環烷基、帶有取代基的C3-C12環烷基、苯基、取代苯基、苄基、取代苄基、含一個或二個以上氧、硫、氮原子的五元或六元雜環芳香基團或酯基中的一種或二種以上;上述C3-C12環烷基上的取代基、苯基上的取代基和苄基上的取代基為C1-C40烷基、C1-C40的烷氧基、滷素、硝基、酯基或氰基中的一種或兩種以上。所述炔丙基類化合物具有以下結構:式中:R2為C1-C40的烷基、C3-C12的環烷基、帶有取代基的C3-C12環烷基、苯基、取代苯基、苄基、取代苄基、含一個或二個以上氧、硫、氮原子的五元或六元雜環芳香基團或酯基中的一種或二種以上;上述C3-C12環烷基上的取代基、苯基上的取代基和苄基上的取代基為C1-C40烷基、C1-C40的烷氧基、滷素、硝基、酯基或氰基中的一種或兩種以上;X為氟、氯、溴、碘、烷基羧酸酯、烷基碳酸酯、烷基磺酸酯、烷基磷酸酯、苯基、取代苯基羧酸酯、苯基、取代苯基碳酸酯、苯基、取代苯基磺酸酯、苯基或取代苯基磷酸酯中的一種或兩種以上。所述銅鹽為Cu(OAc)2·H2O、CuSO4·H2O、Cu(OAc)2、CuSO4、Cu(OTf)2、CuCl2、CuOAc、CuCl、CuI、CuClO4、CuOTf·1/2C6H6、Cu(CH3CN)4BF4或Cu(CH3CN)4ClO4中的一種或兩種以上。所述手性P,N,N-配體具有以下結構特徵:式中:R3,R4為H、C1~C10內的烷基、C3~C8內的環烷基、苯基、取代苯基、苄基或取代苄基中的一種或兩種以上;R5,R6為H、滷素、烷基、環烷基、苯基、取代苯基、烷氧基、苯氧基、醯基或硝基中的一種或兩種以上;R7為烷基、環烷基、苯基、取代苯基、萘基、取代萘基、含一個或以上氧、硫、氮原子的五元或六元雜環芳香基團中的一種或兩種以上。所述鹼添加劑為各種無機鹼或有機鹼,為iPr2NEt、NEt3、tBuOK、KOH、NaOH、K2CO3、Na2CO3、或NaHCO3中的一種或兩種以上。所述步驟(2)催化反應條件優選為:溫度為-40℃;反應介質為甲醇;壓力為常壓;時間為24小時。所述手性銅催化劑與炔丙基類化合物的摩爾比優選為0.001:1-1:1;所述鹼添加劑與炔丙基類化合物的摩爾比優選為1.2:1;所述鄰氨基苯酚類化合物與炔丙基類化合物的摩爾比優選為1:1;所述銅鹽優選Cu(OAc)2·H2O、Cu(OTf)2、Cu(CH3CN)4BF4或Cu(CH3CN)4ClO4中的一種或兩種以上;所述反應介質優選甲醇、二氯甲烷中的一種或兩種。本發明的反應方程式為:本發明具有以下優點:1、起始原料廉價易得。2、手性配體合成簡便,催化劑廉價易得,用量少。3、反應活性好、立體選擇性高,反應條件易實現。4、與傳統方法相比較,該方法可以更方便地合成各種取代的手性二氫1,4-苯並噁嗪類化合物。附圖說明圖1為實施例1製備的手性二氫1,4-苯並噁嗪類環加成產物Ⅱ-1的核磁共振氫譜;圖2為實施例1製備的手性二氫1,4-苯並噁嗪類環加成產物Ⅱ-1的核磁共振碳譜;圖3為實施例11製備的產物Ⅱ-2的核磁共振氫譜;圖4為實施例11製備的產物Ⅱ-2的核磁共振碳譜;圖5為實施例12製備的產物Ⅱ-3的核磁共振氫譜;圖6為實施例12製備的產物Ⅱ-3的核磁共振碳譜;圖7為實施例13製備的產物Ⅱ-4的核磁共振氫譜;圖8為實施例13製備的產物Ⅱ-4的核磁共振碳譜;圖9為實施例14製備的產物Ⅱ-5的核磁共振氫譜;圖10為實施例14製備的產物Ⅱ-5的核磁共振碳譜;圖11為實施例15製備的產物Ⅱ-6的核磁共振氫譜;圖12為實施例15製備的產物Ⅱ-6的核磁共振碳譜;圖13為實施例16製備的產物Ⅱ-7的核磁共振氫譜;圖14為實施例16製備的產物Ⅱ-7的核磁共振碳譜。具體實施方式下面的實施例將對本發明予以進一步的說明,但並不因此而限制本發明。核磁共振是通過Bruker400核磁共振儀測定,高效液相色譜(HPLC)是通過Agilent1100系列高效液相色譜測定。實施例1:Cu(OTf)2和L-2-1絡合作為催化劑催化反應,生成手性二氫1,4-苯並噁嗪類環加成產物Ⅱ-1。在反應瓶中加入金屬前體Cu(OTf)2(0.015mmol,5mol%)及手性配體L-2-1(0.0165mmol,5.5mol%),氮氣保護下加入1.0mL無水甲醇,室溫攪拌1小時。然後將反應管移至-40℃的恆溫反應冷凍機中,將炔丙醇酯Ⅳ-1(0.3mmol,1equiv),N-苄基鄰氨基苯酚Ⅲ-1(0.3mmol,1equiv)和K2CO3(0.36mmol,1.2equiv)溶於2.0mL無水甲醇中,然後將該溶液在氮氣保護下加入到上述攪拌好的催化劑的溶液中,-40℃攪拌反應24h。反應完畢,減壓濃縮至無揮發性溶劑,矽膠柱層析分離(石油醚:乙酸乙酯=100:1),減壓濃縮至無揮發性溶劑,真空乾燥,得到化合物Ⅱ-1,無色油狀物,98%收率,95%ee.產物Ⅱ-1的核磁共振氫譜和核磁共振碳譜分別如圖1、圖2所示:1HNMR(400MHz,CDCl3)δ7.23–7.17(m,4H),7.16–7.04(m,6H),6.81–6.78(m,1H),6.75–6.71(m,1H),6.65–6.60(m,2H),4.71(s,1H),4.62(d,J=1.1Hz,1H),4.42(d,J=15.7Hz,1H),4.20(d,J=1.4Hz,1H),4.12(d,J=15.7Hz,1H).13CNMR(101MHz,CDCl3)δ153.1,143.7,139.3,137.7,134.0,128.8,128.7,127.8,127.5,127.5,127.3,122.7,119.4,115.8,114.8,91.5,61.2,54.6.HPLC(ChiralcelAD-H,n-hexane/i-PrOH=98/2,0.8mL/min,254nm,40℃):tR(major)=7.0min,tR(minor)=8.0min。Ⅲ-1,Ⅳ-1,Ⅱ-1,L-2-1的結構式如下:實施例2:L-1-1作為配體反應生成產物Ⅱ-1將實施例1中的配體L-2-1用配體L-1-1代替,Cu(OTf)2用Cu(OAc)2·H2O代替,反應溫度為0℃,其餘同實施例1。反應得到化合物Ⅱ-1,96%收率,69%ee。L-1-1的結構式如下:實施例3:L-2-2作為配體反應生成產物Ⅱ-1。將實施例1中的配體L-2-1用配體L-2-2代替,Cu(OTf)2用Cu(CH3CN)4BF4代替,反應溫度為0℃,其餘同實施例1。反應得到化合物Ⅱ-1,95%收率,80%ee。L-2-2的結構式如下:實施例4:L-3作為配體反應生成產物Ⅰ-1將實施例1中的配體L-2-1用配體L-3代替,反應溫度為0℃,其餘同實施例1。反應得到化合物Ⅰ-1,<5%收率。實施例5:Cu(OAc)2·H2O和L-2-1催化反應生成產物Ⅱ-1將實施例1中Cu(OTf)2用Cu(OAc)2·H2O代替,反應溫度為0℃,其餘同實施例1。得到化合物Ⅱ-1,88%收率,79%ee。實施例6:CuI和L-2-1催化反應生成產物Ⅱ-1將實施例1中的Cu(OTf)2用CuI代替,反應溫度為0℃,其餘同實施例1,得到化合物Ⅱ-1,79%收率,82%ee。實施例7:沒有鹼添加劑,無產物Ⅱ-1將實施例1中的K2CO3去掉,沒有得到產物Ⅱ-1。實施例8:N,N-iPr2NEt作為鹼添加劑反應生成產物Ⅱ-1將實施例1中的K2CO3替換為N,N-iPr2NEt,溫度為0℃,其餘同實施例1,得到化合物Ⅱ-1,75%收率,83%ee。實施例9:二氯甲烷作為溶劑反應生成產物Ⅱ-1將實施例1中的甲醇溶劑替換為二氯甲烷,其餘同實施例1,得到化合物Ⅱ-1,48%收率,35%ee。實施例10:甲苯作為溶劑反應生成產物Ⅱ-1將實施例1中的甲醇溶劑替換為甲苯,反應溫度為0℃,其餘同實施例1,得到化合物Ⅱ-1,26%收率,48%ee。實施例11:Ⅲ-2作為底物反應生成產物Ⅱ-2將實施例1中的N-苄基鄰氨基苯酚Ⅲ-1替換為Ⅲ-2,其餘同實施例1,得到化合物Ⅱ-2,94%收率,96%ee。產物Ⅱ-2的核磁共振氫譜和核磁共振碳譜分別如圖3、圖4所示:1HNMR(400MHz,CDCl3)δ7.35–7.31(m,2H),7.28–7.26(m,3H),7.25–7.21(m,3H),7.19–7.16(m,2H),6.86–6.79(m,2H),6.75–6.73(m,1H),4.81(s,1H),4.70(d,J=0.9Hz,1H),4.54(d,J=15.7Hz,1H),4.34(d,J=1.4Hz,1H),4.18(d,J=15.7Hz,1H).13CNMR(101MHz,CDCl3)δ152.5,142.5,138.8,136.7,135.2,128.9,128.8,128.0,127.7,127.5,127.0,121.6,117.0,116.4,114.9,91.8,60.6,53.7.HPLC(ChiralcelOJ-H,n-hexane/i-PrOH=95/5,0.8mL/min,254nm,40℃):tR(minor)=10.2min,tR(major)=15.5min.Ⅲ-2,Ⅱ-2的結構式如下:實施例12:Ⅲ-3作為底物反應生成產物Ⅱ-3將實施例1中的N-苄基鄰氨基苯酚Ⅲ-1替換為Ⅲ-3,其餘同實施例1,得到化合物Ⅱ-3,99%收率,97%ee。產物Ⅱ-3的核磁共振氫譜和核磁共振碳譜分別如圖5、圖6所示:1HNMR(400MHz,CDCl3)δ7.35–7.31(m,2H),7.29–7.20(m,6H),7.19–7.16(m,2H),6.81–6.79(m,1H),6.72–6.71(m,1H),6.68–6.65(m,1H),4.82(s,1H),4.70(d,J=1.3Hz,1H),4.54(d,J=15.8Hz,1H),4.34(d,J=1.6Hz,1H),4.19(d,J=15.8Hz,1H).13CNMR(101MHz,CDCl3)δ152.6,141.9,138.8,136.7,134.8,128.9,128.8,127.9,127.7,127.4,127.4,127.0,118.6,116.5,113.6,91.7,60.7,53.7.HPLC(ChiralcelOJ-H,n-hexane/i-PrOH=95/5,0.8mL/min,254nm,40℃):tR(minor)=10.5min,tR(major)=15.0min.Ⅲ-3,Ⅱ-3的結構式如下:實施例13:Ⅲ-4作為底物反應生成產物Ⅱ-4將實施例1中的N-苄基鄰氨基苯酚Ⅲ-1替換為Ⅲ-4,其餘同實施例1,得到化合物Ⅱ-4,92%收率,92%ee。產物Ⅱ-4的核磁共振氫譜和核磁共振碳譜分別如圖7、圖8所示:1HNMR(400MHz,CDCl3)δ7.25–7.22(m,4H),7.19–7.10(m,6H), 6.70–6.68(m,1H),6.51–6.44(m,2H),4.68(s,1H),4.61(d,J=0.9Hz,1H),4.45(d,J=15.6Hz,1H),4.20(d,J=1.3Hz,1H),4.12(d,J=15.6Hz,1H),2.12(s,3H).13CNMR(101MHz,CDCl3)δ153.0,141.7,139.3,137.7,133.6,131.9,128.7,128.6,127.7,127.6,127.4,127.2,120.0,115.4,115.4,91.1,60.9,54.5,21.2.HPLC(ChiralcelOJ-H,n-hexane/i-PrOH=95/5,0.8mL/min,254nm,40℃):tR(major)=9.6min,tR(minor)=12.9min.Ⅲ-4,Ⅱ-4的結構式如下:實施例14:Ⅳ-2作為底物反應生成產物Ⅱ-5將實施例1中的炔丙醇酯Ⅳ-1替換為Ⅳ-2,其餘同實施例1,得到化合物Ⅱ-5,91%收率,96%ee。產物Ⅱ-5的核磁共振氫譜和核磁共振碳譜分別如圖9、圖10所示:1HNMR(400MHz,CDCl3)δ7.23–7.20(m,4H),7.18–7.14(m,2H),7.07–7.01(m,3H),6.80–6.63(m,4H),4.67–4.64(m,2H),4.40(d,J=15.5Hz,1H),4.22(d,J=1.3Hz,1H),4.14(d,J=15.5Hz,1H).13CNMR(101MHz,CDCl3)δ151.9,143.9,141.3,137.3,134.5,133.5,129.9,128.9,127.9,127.7,127.6,127.5,125.3,122.8,120.1,115.9,115.9,92.2,60.5,55.4.HPLC(ChiralcelAD-H,n-hexane/i-PrOH=98/2,0.8mL/min,254nm,40℃):tR(major)=12.3min,tR(minor)=14.0min.Ⅳ-2,Ⅱ-5的結構式如下:實施例15:Ⅳ-3作為底物反應生成產物Ⅱ-6將實施例1中的炔丙醇酯Ⅳ-1替換為Ⅳ-3,其餘同實施例1,得到化合物Ⅱ-6,98%收率,93%ee。產物Ⅱ-6的核磁共振氫譜和核磁共振碳譜分別如圖11、圖12所示:1HNMR(400MHz,CDCl3)δ7.24–7.16(m,5H),7.03–7.01(m,2H),6.96–6.94(m,2H),6.81–6.79(m,1H),6.76–6.72(m,1H),6.65–6.63(m,2H),4.70(s,1H),4.61(s,1H),4.43(d,J=15.7Hz,1H),4.19(s,1H),4.12(d,J=15.7Hz,1H),2.17(s,3H).13CNMR(101MHz,CDCl3)δ153.4,143.6,137.7,137.4,136.2,134.0,129.4,128.8,127.5,127.4,127.1,122.5,119.3,115.7,114.6,91.2,60.9,54.3,21.2.HPLC(ChiralcelAD-H,n-hexane/i-PrOH=98/2,0.8mL/min,254nm,40℃):tR(major)=6.5min,tR(minor)=8.1min.Ⅳ-3,Ⅱ-6的結構式如下:實施例16:Ⅳ-4作為底物反應生成產物Ⅱ-7將實施例1中的炔丙醇酯Ⅳ-1替換為Ⅳ-4,其餘同實施例1,得到化合物Ⅱ-7,96%收率,91%ee。產物Ⅱ-7的核磁共振氫譜和核磁共振碳譜分別如圖13、圖14所示:1HNMR(400MHz,CDCl3)δ7.35–7.22(m,7H),7.12–7.10(m,2H),6.90–6.84(m,2H),6.81–6.74(m,2H),4.75(d,J=1.3Hz,1H),4.72(s,1H),4.49(d,J=15.4Hz,1H),4.30(d,J=1.4Hz,1H),4.23(d,J=15.4Hz,1H).13CNMR(101MHz,CDCl3)δ152.1,143.9,138.1,137.3,133.5,131.7,128.9,128.8,127.6,127.6,122.7,121.6,120.1,115.8,115.8,91.9,60.2,55.3.HPLC(ChiralcelAD-H,n-hexane/i-PrOH=98/2,0.8mL/min,254nm,40℃):tR(major)=8.7min,tR(minor)=11.4min.Ⅳ-4,Ⅱ-7的結構式如下:實施例17-30:反應底物適用性本發明具有廣泛的底物適用性,按照實施例1中的反應條件,許多底物能參與該反應,高收率、高立體選擇性地獲得手性二氫1,4-苯並噁嗪類化合物,反應式為:表1實施例R1R2產率(%)對映體過量(%)1HPh9794173-MePh9790185-MePh9094196-MePh9797205-ClPh9795214-NO2Ph9885224-SO2NH2Ph9791234-tBuPh737124H2-ClPh958025H4-ClPh969126H4-FPh979027H4-CF3Ph768428H2-萘基709329H甲基968030H苄基9194實施例裡17~30中,當R1和R2分別被替換,其產率和對映體過量值如上表1所示。當前第1頁1 2 3 
