海兔脯氨酸‑海兔異亮氨酸肽的衍生物的製作方法
2023-07-24 16:10:51 3
本文提供了海兔脯氨酸-海兔異亮氨酸(dolaproine-dolaisoleuine)肽類似物,包含這類化合物的藥物組合物,以及用這類化合物治療癌症的方法。
背景
癌症是僅次於冠狀動脈疾病的導致人類死亡的第二主要病因。在美國,癌症佔近四分之一的死亡。全球每年有上百萬人死於癌症。根據美國癌症協會(americancancersociety)所報導,僅在美國,癌症引起的死亡每年超過五十萬人,並且每年新增確診病例超過150萬。雖然由心臟病引起的死亡已顯著下降,但由癌症引起的死亡總體呈上升趨勢。除非發現新藥,預計到下世紀早期,癌症將成為主要死因。
全球有數種癌症明顯成為主要殺手。特別是肺癌、前列腺癌、乳腺癌、結腸癌、胰腺癌、卵巢癌和膀胱癌代表了癌症死亡的主要原因。鮮有例外,轉移性癌症是致命的。此外,即使那些患者最初在原發性癌中存活下來,但一般經驗表明他們的生活發生極大改變。許多癌症患者經歷由於顧慮到可能會復發或治療失敗導致的嚴重焦慮。許多患者在治療後經歷身體虛弱。此外,許多癌症患者會經歷復發。
有前景的新癌症療法包括尾海兔素和合成尾海兔素類似物如奧瑞他汀(美國專利號5,635,483、5,780,588、6,323,315、和6,884,869;shnyder等,(2007)int.j.oncol.31:353-360;otani,m.等,jpn.j.cancerres.2000,91,837-844;pct國際公開號wo01/18032a3、wo2005/039492、wo2006/132670、和wo2009/095447;fennell,b.j.等,j.antimicrob.chemther.2003,51,833-841)。尾海兔素和奧瑞他汀已顯示幹擾微管動力學,由此破壞細胞分裂(woyke等(2001)antimicrob.agentsandchemother.45(12):3580-3584)並具有抗癌(美國專利號5,663,149)和抗真菌活性(pettit等(1998)antimicrob.agentschemother.42∶2961-2965)。不幸的是,儘管初期熱度很高,但在ii期臨床試驗中作為單一試劑,尾海兔素10顯示不佳結果(shnyder(2007),同上)。奧瑞他汀家族中的某些化合物已經顯示作為具有比尾海兔素改善的功效和藥物特性的臨床候選物的更大前景(pettit等,(1995)anti-cancerdrugdes.10:529-544;pettit等,(1998)anti-cancerdrugdes.13:243-277;shnyder(2007),同上)。已經描述了這種結構類型的各種合成類似物(美國專利號6,569,834;美國專利號6,124,431;和pettit等,(2011)j.nat.prod.74:962-968)。
奧瑞他汀具有多種性質,使得它們對於藥物開發而言有吸引力。首先,這些化合物是效力極高。其次,由於肽支架,它們的製備是直接的。第三,它們與一般的肽,或者其他具體癌症藥物類別相比具有良好的藥物動力學和代謝概況。
儘管具有顯著的優勢,仍然需要具有所需藥物性質的新癌症療法。
概述
本文提供了新海兔脯氨酸-海兔異亮氨酸肽類似物。因此,本文提供了式(i)的化合物:
其中
r1和r2各自獨立地是-h或烷基;
x是-o-,-nrz-,-s-,或不存在;
其中rz是-h或烷基;
r3是下式基團:
其中r15和r16各自獨立地是-h、-oh、-nh2、-sh、-n3、烷基、烯基、炔基、-烷基-oh、-烷基-nh2、-烷基-sh、或-烷基-n3;
r4是下式基團:
其中r17和r18各自獨立地是-h、-oh、-nh2、-sh、-n3、-co2h、烷基、烯基、炔基、-烷基-oh、-烷基-nh2、-烷基-sh、-烷基-n3或-烷基-co2h
r5是仲丁基或異丁基;
r6是-h或烷基;
r7和r8各自獨立地是-h、烷基、-co2ra、conrbrc、取代或未取代的苯基、或取代或未取代的雜環;
其中ra是-h或烷基;
rb和rc各自獨立地是h或烷基;
r9是-h或烷基;或者r9與r4及它們連接的原子一起形成取代或未取代的雜環烷基環;
r10是-h或烷基;
r11是-h或烷基;
r12是-h或烷基;
r13是-h或烷基;並且
r14是-h、-oh或烷基;
前提是,當x不存在並且r15、r16、r17和r18各自是甲基時,r8不是取代或未取代的苯基、或取代或未取代的雜環;
或其藥學上可接受的鹽。
本文還提供了包含有效量的至少一種式(i)的化合物,或其藥學上可接受的鹽,和藥學上可接受的賦形劑的藥物組合物。
本文還提供了治療患有或診斷患有癌症的對象的方法,包括向需要這種治療的對象給予有效量的至少一種式(i)的化合物,或其藥學上可接受的鹽。
本文還提供了至少一種式(i)的化合物,或其藥學上可接受的鹽用於治療需要這種治療的對象中癌症的用途。
本文還提供了至少一種式(i)的化合物,或其藥學上可接受的鹽在製備用於治療需要這種治療的對象中癌症的藥物中的用途。
本文還提供了含有至少一種式(i)的化合物,或其藥學上可接受的鹽用於治療需要這種治療的對象中的癌症,以及使用說明的試劑盒。
本文還提供了包含至少一種式(i)的化合物,或其藥學上可接受的鹽的製品,其用於治療需要這種治療的對象中的癌症。
附圖的簡要說明
圖1顯示了用實施例2、實施例4和實施例6處理的微管蛋白的體外微管蛋白聚合數據。未處理的(緩衝劑)微管蛋白顯示基線水平的微管蛋白聚合。微管蛋白穩定劑(紫杉醇)和微管蛋白去穩定劑(對照)用作對照。所有的化合物以10μm的終濃度使用。
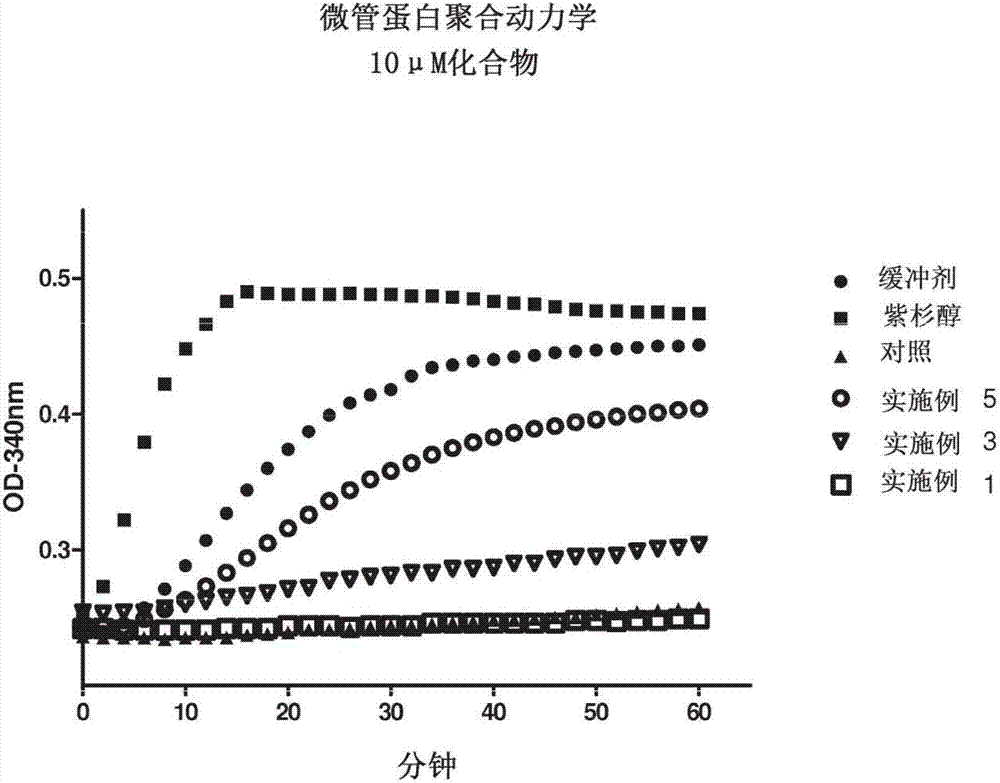
圖2顯示了用實施例1、實施例3和實施例5處理的微管蛋白的體外微管蛋白聚合數據。未處理的(緩衝劑)微管蛋白顯示基線水平的微管蛋白聚合。微管蛋白穩定劑(紫杉醇)和微管蛋白去穩定劑(對照)用作對照。所有的化合物以10μm的終濃度使用。
圖3顯示了用實施例8、實施例9和實施例12處理的微管蛋白的體外微管蛋白聚合數據。未處理的(緩衝劑)微管蛋白顯示基線水平的微管蛋白聚合。微管蛋白穩定劑(紫杉醇)和微管蛋白去穩定劑(對照)用作對照。所有的化合物以10μm的終濃度使用。
圖4顯示了用實施例7、實施例10和實施例11處理的微管蛋白的體外微管蛋白聚合數據。未處理的(緩衝劑)微管蛋白顯示基線水平的微管蛋白聚合。微管蛋白穩定劑(紫杉醇)和微管蛋白去穩定劑(對照)用作對照。所有的化合物以10μm的終濃度使用。
圖5顯示了用實施例19、實施例20和實施例21處理的微管蛋白的體外微管蛋白聚合數據。未處理的(緩衝劑)微管蛋白顯示基線水平的微管蛋白聚合。微管蛋白穩定劑(紫杉醇)和微管蛋白去穩定劑(對照)用作對照。所有的化合物以10μm的終濃度使用。
圖6顯示了用實施例13、實施例16和實施例22處理的微管蛋白的體外微管蛋白聚合數據。未處理的(緩衝劑)微管蛋白顯示基線水平的微管蛋白聚合。微管蛋白穩定劑(紫杉醇)和微管蛋白去穩定劑(對照)用作對照。所有的化合物以10μm的終濃度使用。
圖7顯示了用實施例14、實施例15、實施例18、實施例20和實施例23處理的微管蛋白的體外微管蛋白聚合數據。未處理的(緩衝劑)微管蛋白顯示基線水平的微管蛋白聚合。微管蛋白穩定劑(紫杉醇)和微管蛋白去穩定劑(對照)用作對照。所有的化合物以10μm的終濃度使用。
圖8顯示了用實施例17、實施例19、實施例25和實施例26處理的微管蛋白的體外微管蛋白聚合數據。未處理的(緩衝劑)微管蛋白顯示基線水平的微管蛋白聚合。微管蛋白穩定劑(紫杉醇)和微管蛋白去穩定劑(對照)用作對照。所有的化合物以10μm的終濃度使用。
圖9顯示了如實施例b1中所述,在使用pc3細胞的體外細胞毒性實驗中實施例1、2、3和紫杉醇的結果。數據繪製成與未處理的對照孔相比,存活百分比對比測試化合物濃度。
圖10顯示了如實施例b1中所述,在使用hct15細胞的體外細胞毒性實驗中實施例1、2、3和紫杉醇的結果。數據繪製成與未處理的對照孔相比,存活百分比對比測試化合物濃度。
圖11顯示了如實施例b1中所述,在使用hcc-1954細胞的體外細胞毒性實驗中實施例1、2、3和紫杉醇的結果。數據繪製成與未處理的對照孔相比,存活百分比對比測試化合物濃度。
圖12顯示了如實施例b1中所述,在使用pc3細胞的體外細胞毒性實驗中實施例4、5和6的結果。數據繪製成與未處理的對照孔相比,存活百分比對比測試化合物濃度。
圖13顯示了如實施例b1中所述,在使用hct15細胞的體外細胞毒性實驗中實施例4、5和6的結果。數據繪製成與未處理的對照孔相比,存活百分比對比測試化合物濃度。
圖14顯示了如實施例b1中所述,在使用hcc-1954細胞的體外細胞毒性實驗中實施例4、5和6的結果。數據繪製成與未處理的對照孔相比,存活百分比對比測試化合物濃度。
圖15顯示了如實施例b1中所述,在使用pc3細胞的體外細胞毒性實驗中實施例7、8和9的結果。數據繪製成與未處理的對照孔相比,存活百分比對比測試化合物濃度。
圖16顯示了如實施例b1中所述,在使用hct15細胞的體外細胞毒性實驗中實施例7、8和9的結果。數據繪製成與未處理的對照孔相比,存活百分比對比測試化合物濃度。
圖17顯示了如實施例b1中所述,在使用hcc-1954細胞的體外細胞毒性實驗中實施例7、8和9的結果。數據繪製成與未處理的對照孔相比,存活百分比對比測試化合物濃度。
圖18顯示了如實施例b1中所述,在使用pc3細胞的體外細胞毒性實驗中實施例10、11和12的結果。數據繪製成與未處理的對照孔相比,存活百分比對比測試化合物濃度。
圖19顯示了如實施例b1中所述,在使用hct15細胞的體外細胞毒性實驗中實施例10、11和12的結果。數據繪製成與未處理的對照孔相比,存活百分比對比測試化合物濃度。
圖20顯示了如實施例b1中所述,在使用hcc-1954細胞的體外細胞毒性實驗中實施例10、11和12的結果。數據繪製成與未處理的對照孔相比,存活百分比對比測試化合物濃度。
圖21顯示了如實施例b1中所述,在使用pc3細胞的體外細胞毒性實驗中實施例13、14和15的結果。數據繪製成與未處理的對照孔相比,存活百分比對比測試化合物濃度。
圖22顯示了如實施例b1中所述,在使用hcc-1954細胞的體外細胞毒性實驗中實施例13、14和15的結果。數據繪製成與未處理的對照孔相比,存活百分比對比測試化合物濃度。
圖23顯示了如實施例b1中所述,在使用pc3細胞的體外細胞毒性實驗中實施例16、21和22的結果。數據繪製成與未處理的對照孔相比,存活百分比對比測試化合物濃度。
圖24顯示了如實施例b1中所述,在使用hcc-1954細胞的體外細胞毒性實驗中實施例16、21和22的結果。數據繪製成與未處理的對照孔相比,存活百分比對比測試化合物濃度。
圖25顯示了如實施例b1中所述,在使用pc3細胞的體外細胞毒性實驗中實施例17、18和19的結果。數據繪製成與未處理的對照孔相比,存活百分比對比測試化合物濃度。
圖26顯示了如實施例b1中所述,在使用hcc-1954細胞的體外細胞毒性實驗中實施例17、18和19的結果。數據繪製成與未處理的對照孔相比,存活百分比對比測試化合物濃度。
圖27顯示了如實施例b1中所述,在使用pc3細胞的體外細胞毒性實驗中實施例20和23的結果。數據繪製成與未處理的對照孔相比,存活百分比對比測試化合物濃度。
圖28顯示了如實施例b1中所述,在使用hcc-1954細胞的體外細胞毒性實驗中實施例20和23的結果。數據繪製成與未處理的對照孔相比,存活百分比對比測試化合物濃度。
圖29顯示了如實施例b1中所述,在使用pc3細胞的體外細胞毒性實驗中實施例25和26的結果。數據繪製成與未處理的對照孔相比,存活百分比對比測試化合物濃度。
圖30顯示了如實施例b1中所述,在使用hcc-1954細胞的體外細胞毒性實驗中實施例25和26的結果。數據繪製成與未處理的對照孔相比,存活百分比對比測試化合物濃度。
發明詳述
為簡便起見,該說明書中引用的出版物的內容(包括專利)通過引用納入本文。
本文所用術語「包含」、「含有」和「包括」以其開放、非限定的含義使用。
為提供更簡明的描述,本文中的一些定量表達前不使用術語「約」。應理解無論是否明確地使用術語「約」,本文中的每個含量均表示實際給定的數值,且其還表示基於本領域普通技術所能合理推斷的給定數值的近似值,包括由於實驗和/或測量條件產生的這類給定數值的等同值和近似值。
術語「烷基」其本身或作為其他術語的部分,是指含有正、仲、叔或環碳原子的飽和c1-c12烴。具體的烷基是具有1-8個碳原子、1-6個碳原子、或1-4個碳原子的那些。烷基的示例包括但不限於,甲基(me)、乙基(et)、正丙基、異丙基、丁基、異丁基、仲丁基、叔丁基(tbu)、正戊基、異戊基、叔戊基、和正己基、異己基。在一些實施方式中,烷基具有正、仲、或叔碳原子並且沒有環碳原子。
術語「烯基」本身或作為其他術語的部分,是指含有正、仲、叔或環碳原子的c2-c12烴,其在至少一個位置不飽和,即碳-碳,sp2雙鍵。具體的烯基是具有2-8個碳原子、2-6個碳原子、或2-4個碳原子的那些。示例包括但不限於:乙烯基(-ch=ch2)、烯丙基(-ch2ch2=ch2)、環戊烯基(-c5h7)、和5-己烯基(-ch2ch2ch2ch2ch=ch2)。在一些實施方式中,烯基具有正、仲、或叔碳原子並且沒有環碳原子。
術語「炔基」本身或作為其他術語的部分,是指含有正、仲、叔或環碳原子的c2-c12烴,其具有至少一個不飽和位點,即碳-碳,sp三鍵。具體的炔基是具有2-8個碳原子、2-6個碳原子、或2-4個碳原子的那些。示例包括但不限於:乙炔基(-c≡ch)和2-丙炔基(-ch2c≡ch)。在一些實施方式中,炔基具有正、仲、或叔碳原子並且沒有環碳原子。
術語「烷氧基」是指-o-烷基,其中o是與分子的其他部分的連接點,並且烷基如上定義。
術語「雜環烷基」表示飽和或部分飽和的單環、或稠合、橋連、或螺環多環環結構且每個環結構含有3至12個選自碳原子和至多三個雜原子(選自氮、氧和硫)的環原子。特定雜環烷基是每個環結構具有3-8個環原子或5-7個環原子的那些。該環結構可任選地含有多至2個碳或硫環原子上的氧代基團。適當連接部分形式的示範性實體包括:
術語「雜芳基」表示單環、稠合雙環或稠合多環的芳族雜環(環結構含有選自碳原子和至多四個雜原子(選自氮、氧和硫)的環原子),每個雜環含有3至12個環原子。特定雜芳基是每個環結構具有3-8個環原子或5-7個環原子的那些。雜芳基基團的示範性示例包括以下實體(以適當連接部分的形式):
本文所用的術語「雜環」、「雜環的」或「雜環基」包括上述定義的「雜環烷基」和「雜芳基」基團。
本領域技術人員應認識到上文所列或所示的雜環基、雜芳基和雜環烷基的種類不是窮舉性的,也可選擇這些定義的術語範圍內的其他種類。
術語「滷素」指氯、氟、溴或碘。術語「滷代」指氯、氟、溴或碘。
術語「取代的」表示特定基團或部分帶有一個或多個取代基。術語「未取代的」表示特定基團不帶有取代基。術語「任選取代的」表示特定基團是未取代的或被一個或多個取代基取代。在使用術語「取代的」描述結構系統時,取代可發生在系統上任意價態允許的位置上。
本文所述的任何式旨在表示具有該結構式所示結構的化合物及某些變體或形式。具體地,任何本文所示的式的化合物可具有不對稱中心並且因此以不同的對映體形式存在。通式化合物的所有光學異構體和對映異構體,及其混合物均被認為在該式的範圍內。因此,本文所述的任何式旨在表示外消旋體,一種或多種對映體形式、一種或多種非對映異構體形式、一種或多種阻旋異構體形式,及其混合物。此外,某些結構可以幾何異構體(即,順式和反式異構體)、互變異構體、或阻旋異構體存在。另外,任何本文所示的式也旨在表示這類化合物的水合物、溶劑合物、以及無定形和多晶型形式中的任一種,及其混合物,即使這類形式沒有明確列出。在一些實施方式中,溶劑是水並且溶劑合物是水合物。
本文給出的任何化學式也旨在代表化合物的未標記的形式以及同位素標記形式。同位素標記的化合物具有本文給定化學式所描述的結構,不同之處在於一個或多個原子被具有選擇的原子質量或質量數的原子代替。可摻入本文所述化合物的同位素的示例包括氫、碳、氮、氧、磷、氟、氯和碘的同位素,分別例如2h、3h、11c、13c、14c、15n、18o、17o、31p、32p、35s、18f、36cl和125i。這類同位素標記的化合物可用於代謝研究(優選使用14c)、反應動力學研究(使用例如2h或3h)、包括檢測或成像技術(如正電子發射斷層成像術(pet)或單光子發射計算體層成像術(spect))的藥物或底物組織分布試驗、或對患者的放射性治療中。具體而言,18f或11c標記的化合物對於pet或spect研究是特別優選的。另外,用重同位素如氘(即2h)取代能提供因代謝穩定性較高(例如體內半衰期延長或劑量要求降低)而產生的某些治療優勢。本文所述同位素標記化合物及其前藥通常可通過進行下面方案或實施例和製備中公開的方法來製備,所述方法是用易於獲得的同位素標記的試劑取代非同位素標記的試劑。
當指代任何本文所示的式時,針對特定變量從可能物質中選擇特定部分並不旨在限定針對他處出現的變量選擇相同物質。換而言之,除非另有說明,在出現超過一種變量的情況中,從特定列表中選擇物質獨立於針對式中他處相同變量選擇物質。
在本文中對一類取代基使用時,命名法「ci-j」(其中j>i)表示獨立地實現從i至j(包括i和j)的每一個碳原子數目的本文所述任意組合物、用途或方法的實施方式。例如,術語c1-3獨立地表示含有一個碳原子(c1)的實施方式、含有兩個碳原子(c2)的實施方式和含有三個碳原子(c3)的實施方式。
術語cn-m烷基是指脂族鏈,無論是直鏈或支鏈,鏈中碳的總數n滿足n≤n≤m,其中m>n。
使用autonomtm軟體生成本文所列的化學名。如果化學結構和該結構所列名稱之間存在差異,則以結構為準。
根據對分配和命名的上述解釋性考慮,應理解本文明示引用組暗示,在化學上有意義並且除非另外說明,獨立引用該組的實施方式,並且引用明示的該組的亞組的可能實施方式中的每一個。
在一些實施方式中,r1和r2各自獨立地是-h或烷基,例如c1-6烷基。在一些實施方式中,r1和r2各自獨立地是-h或甲基。在一些實施方式中,r1和r2各自獨立地是烷基。在一些實施方式中,r1和r2都是甲基。在一些實施方式中,r1和r2都是-h。
在一些實施方式中,x是不存在。在其它實施方式中,x是-o-。在一些實施方式中,r1和r2各自獨立地是烷基,並且x不存在。在一些實施方式中,r1和r2都是甲基,並且x不存在。在其他實施方式中,r1和r2都是-h,並且x是-o-。在一些實施方式中,x是-nrz-,其中rz是-h或烷基。在一些實施方式中,rz是-h。在一些實施方式中,x是rz是烷基,例如c1-6烷基或甲基。
在某些實施方式中,r3是其中r15和r16各自獨立地是-h、-oh、-nh2、-sh、-n3、烷基、烯基、炔基、-烷基-oh、-烷基-nh2、-烷基-sh、或-烷基-n3。在其他實施方式中,r15和r16各自獨立地是-h、烷基、-(ch2)0-6c≡ch、-(ch2)0-6ch=ch2、-(ch2)0-6oh、-(ch2)0-6nh2、-(ch2)0-6sh、或-(ch2)0-6n3。在一些實施方式中,r15和r16各自獨立地是-h、-oh、或烷基。在一些實施方式中,r15和r16各自獨立地是-h、-oh、或甲基。在一些實施方式中,r15是-oh,且r16是氫。在一些實施方式中,r15是-oh,且r16是甲基。
在某些實施方式中,r3相對於分子的其他部分處於r立體化學構型。在其他實施方式中,r3相對於分子的其他部分處於s立體化學構型。在某些實施方式中,r3基團本身含有一個或多個手性中心,並且這些立體中心各自獨立地處於r或s構型。
在某些實施方式中,r4是其中r17和r18各自獨立地是-h、-oh、-nh2、-sh、-n3、-co2h、烷基、烯基、炔基、-烷基-oh、-烷基-nh2、-烷基-sh、-烷基-n3或-烷基-co2h。在其他實施方式中,r4是其中r17是-h、-oh、-nh2、-sh、-n3、-co2h、烷基、烯基、炔基、-烷基-oh、-烷基-nh2、-烷基-sh、-烷基-n3或-烷基-co2h,並且r18是-h、-oh、-nh2、-sh、-n3、-co2h、烯基、炔基、-烷基-oh、-烷基-nh2、-烷基-sh、-烷基-n3或-烷基-co2h。在其他實施方式中,r17和r18各自獨立地是-h、烷基、-(ch2)0-6c≡ch、-(ch2)0-6ch=ch2、-(ch2)0-6oh、-(ch2)0-6nh2、-(ch2)0-6sh、或-(ch2)0-6n3。在一些實施方式中,r17和r18各自獨立地是-h、-oh、-nh2、-sh、-n3、-co2h、烷基、-烷基-nh2,或-烷基-n3。在一些實施方式中,r17和r18各自獨立地是-h、-oh、-nh2、-sh、-n3、-co2h、甲基、-ch2nh2,或-ch2n3。
在某些實施方式中,r4與r9及它們連接的原子一起形成取代或未取代的雜環烷基環。在某些實施方式中,r4與r9及它們連接的原子一起形成5至7元雜環烷基環,其可以是未取代的或被一個或多個選自-oh、-nh2、-sh、和-n3的基團取代。在某些實施方式中,雜環烷基環是吡咯環,其可以是未取代的或被一個或多個選自-oh、-nh2、-sh和-n3的基團取代。
在某些實施方式中,r4相對於分子的其他部分處於r立體化學構型。在其他實施方式中,r4相對於分子的其他部分處於s立體化學構型。在某些實施方式中,r4基團本身含有一個或多個手性中心,並且這些立體中心各自獨立地處於r或s構型。
在某些實施方式中,r5是仲丁基。在其它實施方式中,r5是異丁基。在某些實施方式中,r5相對於分子的其他部分處於r立體化學構型。在其他實施方式中,r5相對於分子的其他部分處於s立體化學構型。在一些實施方式中,r5基團內的手性中心處於r構型,並且在其他實施方式中,該中心處於s構型。
在某些實施方式中,r6是-h。在其他實施方式中,r6是烷基,例如,c1-8烷基、c1-4烷基、甲基、或乙基。
在一些實施方式中,r7和r8各自獨立地是-h、烷基、-co2ra或-conrbrc;其中ra是-h或烷基,例如,c1-6烷基或甲基;並且rb和rc各自獨立地是-h或烷基,例如,c1-6烷基或甲基。
在某些實施方式中,r7和r8各自獨立地是取代或未取代的苯基或者取代或未取代的雜環,其中苯基或雜環可被一個或多個選自滷素、氧代、羥基、氨基、烷基和烷氧基的基團取代。在某些其他實施方式中,r7是未取代的3至8元雜環。在某些其他實施方式中,r7是取代的3至8元雜環。在某些其他實施方式中,r8是任選地被滷素取代的苯基。
在某些實施方式中,r7相對於分子的其他部分處於r立體化學構型。在其他實施方式中,r7相對於分子的其他部分處於s立體化學構型。
在某些實施方式中,r8相對於分子的其他部分處於r立體化學構型。在其他實施方式中,r8相對於分子的其他部分處於s立體化學構型。
在一些實施方式中,r7是-co2ra-conrbrc;四唑基或噻唑基,其中ra是-h或烷基,例如c1-6烷基或甲基;並且rb和rc各自獨立地是-h或烷基,例如,c1-6烷基或甲基;並且r8是任選地被滷素取代的苯基。
在一些實施方式中,r9是-h。在其他實施方式中,r9是烷基,例如,c1-8烷基、c1-4烷基、甲基、或乙基。在一些實施方式中,r9是-h或甲基。在一些實施方式中,r9是甲基。
在一些實施方式中,r10是-h。在其他實施方式中,r10是烷基,例如,c1-8烷基、c1-4烷基、甲基、或乙基。在一些實施方式中,r10是-h或甲基。在一些實施方式中,r10是甲基。
在一些實施方式中,r11是-h。在其他實施方式中,r11是烷基,例如,c1-8烷基、c1-4烷基、甲基、或乙基。在一些實施方式中,r11是-h或甲基。在一些實施方式中,r11是甲基。
在一些實施方式中,r12是-h。在其他實施方式中,r12是烷基,例如,c1-8烷基、c1-4烷基、甲基、或乙基。在一些實施方式中,r12是-h或甲基。在一些實施方式中,r12是甲基。
在一些實施方式中,r13是-h。在其他實施方式中,r13是烷基,例如,c1-8烷基、c1-4烷基、甲基或乙基。在一些實施方式中,r13是-h或甲基。在一些實施方式中,r13是甲基。
在一些實施方式中,r14是-h。在一些實施方式中,r14是烷基,例如,c1-6烷基、甲基、或乙基。在一些實施方式中,r14是-oh。
在某些實施方式中,r14相對於分子的其他部分處於r立體化學構型。在其他實施方式中,r14相對於分子的其他部分處於s立體化學構型。
在一些實施方式中,r7是-co2ra,其中ra是-h或烷基,例如c1-6烷基或甲基;r8是苯基;並且r14是-h。在一些實施方式中,r7是-conrbrc,其中rb和rc各自獨立地是-h或烷基,例如c1-6烷基或甲基;r8是苯基;並且r14是-h。在一些實施方式中,r7是烷基,例如c1-6烷基或甲基;r8是苯基;並且r14是-oh。在一些實施方式中,r7是甲基、r8是苯基,並且r14是-oh。在一些實施方式中,r7和r14都是-h,並且r8是吡啶基、哌啶基、未取代的苯基、或被滷素例如氟、氯或溴取代的苯基。在一些實施方式中,r7是-co2ra,其中ra是-h或烷基,例如,c1-6烷基或甲基;r8是-h或烷基,例如,c1-6烷基或甲基;並且r14是烷基,例如,c1-6烷基、甲基,或乙基。在一些實施方式中,r7是-co2ra,其中ra是-h或烷基,例如,c1-6烷基或甲基;r8是-h或烷基,例如,c1-6烷基或甲基;並且r14是-oh。
在某些實施方式中,
r1和r2各自獨立地是-h或c1-6烷基;
x是-o-,或不存在;
r3是其中r15和r16各自獨立地是-h、-oh、或c1-6烷基;
r4是其中r17是-oh、-nh2、-sh、-n3、-co2h、-c1-6烷基-nh2、炔基、烯基、或-c1-6烷基-n3;並且r18是-h或c1-6烷基;
r5是仲丁基;
r6是-h;
r7是-h、c1-6烷基、-co2ra、-conrbrc、四唑基或噻唑基;其中ra是-h或c1-6烷基;並且rb和rc各自是-h或c1-6烷基;
r8是-h、c1-6烷基、取代或未取代的苯基或者取代或未取代的雜環;
r9是-h;
r10、r11、r12、和r13各自獨立地是c1-6烷基;並且
r14是h、c1-6烷基或-oh。
在某些實施方式中,
r1和r2各自獨立地是-h或甲基;
x是-o-,或不存在;
r3是其中r15和r16各自獨立地是-h、-oh,或甲基;
r4是其中r17是-oh、-nh2、-sh、-n3、-co2h、氨基甲基、炔基、烯基、或疊氮甲基;並且r18是-h或甲基;
r5是仲丁基;
r6是-h;
r7是-h、甲基、-co2ra、或-conrbrc;其中ra是-h或甲基;並且rb和rc各自是-h或甲基;
r8是-h、甲基、乙基、吡啶基、哌啶基、未取代的苯基、被滷素取代的苯基;
r9是-h;
r10、r11、r12和r13各自是甲基;並且
r14是-h、甲基或-oh。
在某些實施方式中,
r1和r2各自獨立地是-h或c1-6烷基;
x不存在;
r3是其中r15和r16各自獨立地是-h、-oh或c1-6烷基;
r4是其中r17是-n3,並且r18是-h或甲基;
r5是仲丁基;
r6是-h;
r7是-h、c1-6烷基、-co2ra、-conrbrc、四唑基或噻唑基;其中ra是-h或c1-6烷基;並且rb和rc各自是-h或c1-6烷基;
r8是-h、c1-6烷基、取代或未取代的苯基或者取代或未取代的雜環;
r9是-h;
r10、r11、r12和r13各自獨立地是c1-6烷基;並且
r14是h、c1-6烷基或-oh。
在某些實施方式中,
r1和r2各自獨立地是-h或c1-6烷基;
x是-o-;
r3是其中r15和r16各自獨立地是-h、-oh或c1-6烷基;
r4是其中r17是-n3,並且r18是-h或甲基;
r5是仲丁基;
r6是-h;
r7是-h、c1-6烷基、-co2ra、-conrbrc、四唑基或噻唑基;其中ra是-h或c1-6烷基;並且rb和rc各自是-h或c1-6烷基;
r8是-h、c1-6烷基、取代或未取代的苯基或者取代或未取代的雜環;
r9是-h;
r10、r11、r12和r13各自獨立地是c1-6烷基;並且
r14是h、c1-6烷基或-oh。
在式(i)的一些實施方式中,其中,
r1和r2各自獨立是甲基;
x不存在;
r3是下式基團:
其中r15和r16各自是甲基;
r4是下式基團:
其中r17是-n3、-nh2、-oh、-sh,並且r18是-h或甲基;
r5是仲丁基;
r6是-h;
r7是-co2ra或conrbrc,
其中ra是-h或c1-6烷基;
rb和rc各自獨立地是h或c1-6烷基;
r8是苯基;
r9是-h;
r10、r11、r12和r13各自獨立地是甲基;並且
r14是-h。
在式(i)的一些實施方式中,其中,
r1和r2各自是-h;
x是-o-;
r3是下式基團:
其中r15和r16各自是甲基;
r4是下式基團:
其中r17是-n3,並且r18是-h或甲基;
r5是仲丁基;
r6是-h;
r7是-co2ra或conrbrc,
其中ra是-h或c1-6烷基;
rb和rc各自獨立地是h或c1-6烷基;
r8是苯基;
r9是-h;
r10、r11、r12和r13各自獨立地是甲基;並且
r14是-h。
應理解,本文提供的任意可變基團定義可與本文提供的任意其他可變基團定義組合使用,從而考慮化學上可行的本文提供的可變基團的所有可能組合和置換。
在某些實施方式中,所述式(i)的化合物選自下組:
(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-3-羥基-n-甲基丙醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯氨基)-3-苯基丙酸甲酯;
(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((2s,3r)-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-3-羥基-n-甲基丁醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯氨基)-3-苯基丙酸甲酯;
(s)-2-(二甲基氨基)-n-((s)-3-羥基-1-(((3r,4s,5s)-3-甲氧基-1-((s)-2-((1r,2r)-1-甲氧基-2-甲基-3-氧代-3-((2-(吡啶-2-基)乙基)氨基)丙基)吡咯烷-1-基)-5-甲基-1-氧代庚-4-基)(甲基)氨基)-1-氧代丙-2-基)-3-甲基丁醯胺;
(2s,3r)-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-3-羥基-n-((3r,4s5s)-3-甲氧基-1-((s)-2-((1r,2r)-1-甲氧基-2-甲基-3-氧代-3-((2-(吡啶-2-基)乙基)氨基)丙基)吡咯烷-1-基)-5-甲基-1-氧代庚-4-基)-n-甲基丁醯胺;
(2s)-2-(二甲基氨基)-n-((2s)-3-羥基-1-(((3r,4s5s)-3-甲氧基-1-((2s)-2-((1r,2r)-1-甲氧基-2-甲基-3-氧代-3-((2-(哌啶-2-基)乙基)氨基)丙基)吡咯烷-1-基)-5-甲基-1-氧代庚-4-基)(甲基)氨基)-1-氧代丙-2-基)-3-甲基丁醯胺;
(2s,3r)-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-3-羥基-n-((3r,4s5s)-3-甲氧基-1-((2s)-2-((1r,2r)-1-甲氧基-2-甲基-3-氧代-3-((2-(哌啶-2-基)乙基)氨基)丙基)吡咯烷-1-基)-5-甲基-1-氧代庚-4-基)-n-甲基丁醯胺;
(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((2s,3s)-3-疊氮基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丁醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯氨基)-3-苯基丙酸甲酯;
(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-3-氨基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丙醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯氨基)-3-苯基丙酸甲酯;
(s)-n-((s)-3-氨基-1-(((3r,4s,5s)-3-甲氧基-1-((s)-2-((1r,2r)-1-甲氧基-2-甲基-3-氧代-3-((2-(吡啶-2-基)乙基)氨基)丙基)吡咯烷-1-基)-5-甲基-1-氧代庚-4-基)(甲基)氨基)-1-氧代丙-2-基)-2-(二甲基氨基)-3-甲基丁醯胺;
(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-3-疊氮基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丙醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯氨基)-3-苯基丙酸甲酯;
(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-4-疊氮基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丁醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯氨基)-3-苯基丙酸甲酯;
(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-4-氨基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丁醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯氨基)-3-苯基丙酸甲酯;
(s)-2-((s)-2-(氨基氧基)-3-甲基丁醯氨基)-n-((3r,4s,5s)-3-甲氧基-1-((s)-2-((1r,2r)-1-甲氧基-2-甲基-3-氧代-3-((2-(吡啶-2-基)乙基)氨基)丙基)吡咯烷-1-基)-5-甲基-1-氧代庚-4-基)-n,3-二甲基丁醯胺;
((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-2-((s)-2-(二甲基氨基)-3-羥基丙醯氨基)-n,3-二甲基丁醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯基)-l-苯丙氨酸;
((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-2-((2s,3r)-2-(二甲基氨基)-3-羥基丁醯氨基)-n,3-二甲基丁醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯基)-l-苯丙氨酸;
(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((2s,3s)-3-疊氮基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丁醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯氨基)-3-苯基丙酸;
(s)-n-((3r,4s,5s)-1-((s)-2-((1r,2r)-3-(((s)-1-氨基-1-氧代-3-苯基丙-2-基)氨基)-1-甲氧基-2-甲基-3-氧代丙基)吡咯烷-1-基)-3-甲氧基-5-甲基-1-氧代庚-4-基)-2-((2s,3r)-2-(二甲基氨基)-3-羥基丁醯氨基)-n,3-二甲基丁醯胺;
(s)-n-((3r,4s,5s)-1-((s)-2-((1r,2r)-3-(((s)-1-氨基-1-氧代-3-苯基丙-2-基)氨基)-1-甲氧基-2-甲基-3-氧代丙基)吡咯烷-1-基)-3-甲氧基-5-甲基-1-氧代庚-4-基)-2-((s)-2-(二甲基氨基)-3-羥基丙醯氨基)-n,3-二甲基丁醯胺;
(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((r)-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-3-巰基-n-甲基丙醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯氨基)-3-苯基丙酸甲酯;
(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((r)-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-3-巰基-n-甲基丙醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯氨基)-3-苯基丙酸;
(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-3-羥基-n-甲基丙醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯氨基)-3-苯基丙酸;
(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((2s,3r)-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-3-羥基-n-甲基丁醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯氨基)-3-苯基丙酸;
(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-2-((s)-2-(二甲基氨基)-3-羥基丙醯氨基)-n,3-二甲基丁醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯氨基)-3-苯基丙酸甲酯;
(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-2-((2s,3r)-2-(二甲基氨基)-3-羥基丁醯氨基)-n,3-二甲基丁醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯氨基)-3-苯基丙酸甲酯;
(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((2s,3s)-3-氨基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丁醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯氨基)-3-苯基丙酸甲酯;
(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((2s,3s)-3-氨基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丁醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯氨基)-3-苯基丙酸;
(2s,3s)-3-疊氮基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-((3r,4s,5s)-3-甲氧基-1-((s)-2-((1r,2r)-1-甲氧基-2-甲基-3-氧代-3-(苯乙基氨基)丙基)吡咯烷-1-基)-5-甲基-1-氧代庚-4-基)-n-甲基丁醯胺;
(2s,3s)-3-疊氮基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-((3r,4s,5s)-1-((s)-2-((1r,2r)-3-(((1s,2r)-1-羥基-1-苯基丙-2-基)氨基)-1-甲氧基-2-甲基-3-氧代丙基)吡咯烷-1-基)-3-甲氧基-5-甲基-1-氧代庚-4-基)-n-甲基丁醯胺;
(2s,3s)-3-疊氮基-n-((3r,4s,5s)-1-((s)-2-((1r,2r)-3-((4-氯苯乙基)氨基)-1-甲氧基-2-甲基-3-氧代丙基)吡咯烷-1-基)-3-甲氧基-5-甲基-1-氧代庚-4-基)-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丁醯胺;
(2s,3s)-3-疊氮基-n-((3r,4s,5s)-1-((s)-2-((1r,2r)-3-((2-氯苯乙基)氨基)-1-甲氧基-2-甲基-3-氧代丙基)吡咯烷-1-基)-3-甲氧基-5-甲基-1-氧代庚-4-基)-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丁醯胺;
(2s,3s)-3-氨基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-((3r,4s,5s)-3-甲氧基-1-((s)-2-((1r,2r)-1-甲氧基-2-甲基-3-氧代-3-(苯乙基氨基)丙基)吡咯烷-1-基)-5-甲基-1-氧代庚-4-基)-n-甲基丁醯胺;
(2s,3s)-3-氨基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-((3r,4s,5s)-1-((s)-2-((1r,2r)-3-(((1s,2r)-1-羥基-1-苯基丙-2-基)氨基)-1-甲氧基-2-甲基-3-氧代丙基)吡咯烷-1-基)-3-甲氧基-5-甲基-1-氧代庚-4-基)-n-甲基丁醯胺;
(2s,3s)-3-氨基-n-((3r,4s,5s)-1-((s)-2-((1r,2r)-3-((4-氯苯乙基)氨基)-1-甲氧基-2-甲基-3-氧代丙基)吡咯烷-1-基)-3-甲氧基-5-甲基-1-氧代庚-4-基)-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丁醯胺;
(2s,3s)-3-氨基-n-((3r,4s,5s)-1-((s)-2-((1r,2r)-3-((2-氯苯乙基)氨基)-1-甲氧基-2-甲基-3-氧代丙基)吡咯烷-1-基)-3-甲氧基-5-甲基-1-氧代庚-4-基)-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丁醯胺;
(s)-4-氨基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-((3r,4s,5s)-3-甲氧基-1-((s)-2-((1r,2r)-1-甲氧基-2-甲基-3-氧代-3-(苯乙基氨基)丙基)吡咯烷-1-基)-5-甲基-1-氧代庚-4-基)-n-甲基丁醯胺;
(s)-4-氨基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-((3r,4s,5s)-1-((s)-2-((1r,2r)-3-(((1s,2r)-1-羥基-1-苯基丙-2-基)氨基)-1-甲氧基-2-甲基-3-氧代丙基)吡咯烷-1-基)-3-甲氧基-5-甲基-1-氧代庚-4-基)-n-甲基丁醯胺;
(s)-4-氨基-n-((3r,4s,5s)-1-((s)-2-((1r,2r)-3-((4-氯苯乙基)氨基)-1-甲氧基-2-甲基-3-氧代丙基)吡咯烷-1-基)-3-甲氧基-5-甲基-1-氧代庚-4-基)-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丁醯胺;
(s)-4-氨基-n-((3r,4s,5s)-1-((s)-2-((1r,2r)-3-((2-氯苯乙基)氨基)-1-甲氧基-2-甲基-3-氧代丙基)吡咯烷-1-基)-3-甲氧基-5-甲基-1-氧代庚-4-基)-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丁醯胺;
((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基戊-4-炔醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯基)-l-苯丙氨酸甲酯;
(2s,3s)-n-((3r,4s,5s)-1-((s)-2-((1r,2r)-3-(((s)-1-氨基-1-氧代-3-苯基丙-2-基)氨基)-1-甲氧基-2-甲基-3-氧代丙基)吡咯烷-1-基)-3-甲氧基-5-甲基-1-氧代庚-4-基)-3-疊氮基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丁醯胺;
(2s,3s)-3-疊氮基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-((3r,4s,5s)-3-甲氧基-1-((s)-2-((1r,2r)-1-甲氧基-2-甲基-3-氧代-3-((2-(吡啶-2-基)乙基)氨基)丙基)吡咯烷-1-基)-5-甲基-1-氧代庚-4-基)-n-甲基丁醯胺;
(2s,3s)-3-疊氮基-n-((3r,4s,5s)-1-((s)-2-((1r,2r)-3-(((s)-1-(叔丁基氨基)-1-氧代-3-苯基丙-2-基)氨基)-1-甲氧基-2-甲基-3-氧代丙基)吡咯烷-1-基)-3-甲氧基-5-甲基-1-氧代庚-4-基)-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丁醯胺;
((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((2s,3s)-3-疊氮基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丁醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯基)-l-纈氨酸甲酯;
((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-6-氨基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基己醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯基)-l-苯丙氨酸甲酯;
((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((2s,4s)-4-疊氮基-1-(二甲基-l-纈氨醯基)-n-甲基吡咯烷-2-甲醯胺基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯基)-l-苯丙氨酸甲酯;
(s)-3-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-4-(((3r,4s,5s)-3-甲氧基-1-((s)-2-((1r,2r)-1-甲氧基-3-(((s)-1-甲氧基-1-氧代-3-苯基丙-2-基)氨基)-2-甲基-3-氧代丙基)吡咯烷-1-基)-5-甲基-1-氧代庚-4-基)(甲基)氨基)-4-氧代丁酸;
(2s,3r)-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-3-羥基-n-((3r,4s,5s)-1-((s)-2-((1r,2r)-3-(((1s,2r)-1-羥基-1-苯基丙-2-基)氨基)-1-甲氧基-2-甲基-3-氧代丙基)吡咯烷-1-基)-3-甲氧基-5-甲基-1-氧代庚-4-基)-n-甲基丁醯胺;
((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n,3-二甲基丁醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯基)-l-絲氨酸甲酯;
((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((2s,3s)-3-疊氮基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丁醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯基)-l-異亮氨酸甲酯;
(2s,3s)-3-氨基-n-((3r,4s,5s)-1-((s)-2-((1r,2r)-3-(((s)-1-氨基-1-氧代-3-苯基丙-2-基)氨基)-1-甲氧基-2-甲基-3-氧代丙基)吡咯烷-1-基)-3-甲氧基-5-甲基-1-氧代庚-4-基)-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丁醯胺;
(2s,3s)-3-氨基-n-((3r,4s,5s)-1-((s)-2-((1r,2r)-3-(((s)-1-(叔丁基氨基)-1-氧代-3-苯基丙-2-基)氨基)-1-甲氧基-2-甲基-3-氧代丙基)吡咯烷-1-基)-3-甲氧基-5-甲基-1-氧代庚-4-基)-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丁醯胺;
((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-3-疊氮基-n-甲基-2-((s)-3-甲基-2-(甲基氨基)丁醯氨基)丙醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯基)-l-苯丙氨酸甲酯;
((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((2s,3s)-3-疊氮基-n-甲基-2-((s)-3-甲基-2-(甲基氨基)丁醯氨基)丁醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯基)-l-苯丙氨酸甲酯;
(2s,3s)-n-((3r,4s,5s)-1-((s)-2-((1r,2r)-3-(((s)-1-氨基-1-氧代-3-苯基丙-2-基)氨基)-1-甲氧基-2-甲基-3-氧代丙基)吡咯烷-1-基)-3-甲氧基-5-甲基-1-氧代庚-4-基)-3-疊氮基-n-甲基-2-((s)-3-甲基-2-(甲基氨基)丁醯氨基)丁醯胺;
((2s,3s)-3-疊氮基-n-((3r,4s,5s)-1-((s)-2-((1r,2r)-3-(((s)-1-(叔丁基氨基)-1-氧代-3-苯基丙-2-基)氨基)-1-甲氧基-2-甲基-3-氧代丙基)吡咯烷-1-基)-3-甲氧基-5-甲基-1-氧代庚-4-基)-n-甲基-2-((s)-3-甲基-2-(甲基氨基)丁醯氨基)丁醯胺;
((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((2s,3s)-3-疊氮基-n-甲基-2-((s)-3-甲基-2-(甲基氨基)丁醯氨基)丁醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯基)-l-苯丙氨酸叔丁酯;
((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((2s,3s)-3-疊氮基-n-甲基-2-((s)-3-甲基-2-(甲基氨基)丁醯氨基)丁醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯基)-l-苯丙氨酸;
((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((2s,3s)-3-疊氮基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丁醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯基)-l-苯丙氨酸叔丁酯;
(2s,3s)-3-疊氮基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-((3r,4s,5s)-3-甲氧基-1-((s)-2-((1r,2r)-1-甲氧基-2-甲基-3-氧代-3-(((s)-2-苯基-1-(1h-四唑-5-基)乙基)氨基)丙基)吡咯烷-1-基)-5-甲基-1-氧代庚-4-基)-n-甲基丁醯胺;
(2s,3s)-3-疊氮基-n-((3r,4s,5s)-3-甲氧基-1-((s)-2-((1r,2r)-1-甲氧基-2-甲基-3-氧代-3-(((s)-2-苯基-1-(1h-四唑-5-基)乙基)氨基)丙基)吡咯烷-1-基)-5-甲基-1-氧代庚-4-基)-n-甲基-2-((s)-3-甲基-2-(甲基氨基)丁醯氨基)丁醯胺;
(2s,3s)-3-疊氮基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-((3r,4s,5s)-3-甲氧基-1-((s)-2-((1r,2r)-1-甲氧基-2-甲基-3-氧代-3-(((s)-2-苯基-1-(噻唑-2-基)乙基)氨基)丙基)吡咯烷-1-基)-5-甲基-1-氧代庚-4-基)-n-甲基丁醯胺;
((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((2s,3s)-3-氨基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丁醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯基)-l-苯丙氨酸叔丁酯;
(2s,3s)-3-氨基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-((3r,4s,5s)-3-甲氧基-1-((s)-2-((1r,2r)-1-甲氧基-2-甲基-3-氧代-3-(((s)-2-苯基-1-(1h-四唑-5-基)乙基)氨基)丙基)吡咯烷-1-基)-5-甲基-1-氧代庚-4-基)-n-甲基丁醯胺;和
(2s,3s)-3-氨基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-((3r,4s,5s)-3-甲氧基-1-((s)-2-((1r,2r)-1-甲氧基-2-甲基-3-氧代-3-(((s)-2-苯基-1-(噻唑-2-基)乙基)氨基)丙基)吡咯烷-1-基)-5-甲基-1-氧代庚-4-基)-n-甲基丁醯胺;
及其藥學上可接受的鹽。
本發明還提供式(i)的化合物的藥學上可接受的鹽,優選上文所述的那些以及本文所示的特定化合物,以及包括所述鹽的藥學組合物,以及使用所述鹽的方法。
「藥學上可接受的鹽」旨在表示本文所示化合物的游離酸或鹼的鹽,其沒有毒性、生物學上可以容忍或者生物學上適於向對象給藥。通常參見,s.m.berge等,「pharmaceuticalsalts(《藥用鹽》)」j.pharm.sci.,1977,66,1-19。優選的藥學上可接受的鹽是藥學上有效並且適於接觸對象組織而沒有過多的毒性、刺激、或過敏反應的那些。本文所述的化合物可具有足夠酸性的基團、足夠鹼性的基團,或兩種類型的官能團,並且因此與多種無機或有機鹼,以及無機和有機酸反應以形成藥學上可接受的鹽。藥學上可接受的鹽的示例包括酸加成鹽如硫酸鹽、焦硫酸鹽、硫酸氫鹽、亞硫酸鹽、亞硫酸氫鹽、磷酸鹽、磷酸一氫鹽、磷酸二氫鹽、偏磷酸鹽、焦磷酸鹽、氯化物、溴化物、碘化物、乙酸鹽、丙酸鹽、癸酸鹽、辛酸鹽、丙烯酸鹽、甲酸鹽、異丁酸鹽、己酸鹽、庚酸鹽、丙炔酸鹽、草酸鹽、丙二酸鹽、琥珀酸鹽、辛二酸鹽、癸二酸鹽、富馬酸鹽、馬來酸鹽、1,4-丁炔二酸鹽、1,6-己炔二酸鹽、苯甲酸鹽、氯苯甲酸鹽、甲基苯甲酸鹽、二硝基苯甲酸鹽、羥基苯甲酸鹽、甲氧基苯甲酸鹽、鄰苯二甲酸鹽、磺酸鹽、甲基磺酸鹽、丙基磺酸鹽、苯磺酸鹽、二甲苯磺酸鹽、萘-1-磺酸鹽、萘-2-磺酸鹽、苯基乙酸鹽、苯基丙酸鹽、苯基丁酸鹽、檸檬酸鹽、乳酸鹽、γ-羥基丁酸鹽、乙醇酸鹽、酒石酸鹽、和扁桃酸鹽,以及與無機鹼如鈉、鉀、鎂、鈣、鋁等或有機鹼如甲基胺、乙基胺、乙醇胺、賴氨酸、鳥氨酸等的鹽,與各種胺基酸或胺基酸衍生物如乙醯基亮氨酸等的鹽,銨鹽等。
為治療目的,包括本文所述化合物的藥物組合物還可包括一種或多種藥學上可接受的賦形劑。藥學上可接受的賦形劑指沒有毒性且生物學上適於向對象給藥的物質。這類賦形劑促進本文所述化合物的配製和給藥過程且與活性成分相容。藥學上可接受的賦形劑的示例包括穩定劑、潤滑劑、表面活性劑、稀釋劑、抗氧化劑、粘結劑、著色劑、乳化劑或調味劑。在優選的實施方式中,藥物組合物是無菌組合物。
根據本領域中用於多種劑型製備的常規方法,本文所述藥物組合物可配製為適當藥物溶劑或載劑中的溶液劑、乳劑、混懸劑或分散劑,或者丸劑、片劑、錠劑、栓劑、用於重建的粉末劑或連同固態載劑的膠囊劑。對於局部使用,優選將本文所述的化合物配製為乳膏或軟膏或適用於局部給藥的類似載劑。本文所述的藥物組合物和化合物可在本發明的方法中通過合適的遞送途徑,例如,口服、經鼻、胃腸外、直腸、局部、眼部,或通過吸入給藥。
本文所用術語「治療」或「處理」旨在指代處於產生治療益處的目的向對象給予本文所述的化合物。治療包括逆轉、緩解、減輕、抑制疾病、紊亂或病症、或癌症的一種或多種症狀的發展,或降低其嚴重性。術語?對象?指需要該治療的哺乳動物患者,例如人。
在本文所述的治療方法中,「有效量」指足以使需要這類治療的對象獲得所需治療益處的量或劑量。本文所述的化合物的有效量或劑量可通過常規方法(如建模、劑量遞增或臨床試驗)確定,其中考慮常規因素,例如給藥或藥物遞送的模式或途徑、試劑的藥代動力學、感染的嚴重程度和過程、對象的健康狀態、病情和體重以及主治醫生的判斷。示例性劑量的範圍為每天每千克對象體重約1μg至2mg活性化合物,優選約0.05至100mg/kg/天、或約1至35mg/kg/天、或約0.1至10mg/kg/天。總劑量可以單個或分開的劑量單元(例如bid、tid、qid)給予。
本文所述的化合物可在藥物組合物或方法中與癌症治療中的其他活性成分聯用。其他活性成分可與本文所述的化合物分開給予或者可與本文所述的化合物一起包含在本文所述的藥物組合物中。例如,其他活性成分是已知或發現有效治療癌症,包括針對與癌症相關的其他靶標有活性的那些,諸如但不限於萬珂、利妥昔單抗、氨甲蝶呤、賀賽汀、長春新鹼、潑尼松、伊立替康等或其組合。這類組合可用於增加效力、減少一種或多種副作用或減少所需的本發明化合物劑量。
本文所述的化合物可與癌症治療中的其他活性成分聯用,用於藥物組合物或方法。其他活性成分可與本文所述的化合物分開給予或者可與本文所述的化合物一起包含在本文所述的藥物組合物中。例如,其他活性成分是已知或發現有效治療癌症,包括針對與癌症相關的其他靶標有活性的那些,諸如但不限於萬珂、利妥昔單抗、氨甲蝶呤、賀賽汀、長春新鹼、潑尼松、伊立替康等或其組合。這類組合可用於增加效力、減少一種或多種副作用或減少所需的本發明化合物劑量。
現在,通過參考用於本文中通用製備方法的示意性合成方案和之後的具體實施例來描述式(i)的化合物。本領域技術人員應認識到,為獲得本文中的多種化合物,可對起始材料進行適當選擇,從而通過適當地帶有或不帶有保護的反應方案使用最終所需的取代基以生成所需的產物。或者,可能需要或想要在最終所需的取代基位置上採用可通過反應方案攜帶並在適當時可被所需取代基替代的合適基團。另外,本領域技術人員將認識到,可使用保護基團來保護某些官能基團(氨基、羧基或側鏈基團)免於反應條件,並且可在合適時在標準條件下去除這類基團。方案a中描述的各反應均優選在約室溫至所用有機溶劑的回流溫度的溫度下進行。除非另有說明,變量如上文所定義,可參考式(i)。
方案a
參考方案a,式(i)的化合物的製備從海兔異亮氨酸(dil)標記的(a)的受保護酸形式開始(參見pettit等,(1994)j.org.chem.59∶1796-1800)。化合物(a)顯示帶有叔丁基酯保護基團,但本領域技術人員可選擇合適的替代方式。在標準肽偶聯條件下實現與氮保護的纈氨酸或異亮氨酸衍生物(b)偶聯,其中pg是合適的氨基保護基團,如boc(叔丁氧基羰基)或芴基甲氧羰基(fmoc)基團。例如,反應在氰基膦酸二乙酯(depc)、pybrop、pybop、bop、二異丙基碳二亞胺(dic)、二環己基碳二亞胺(dcc)、1-(3-二甲基氨基丙基)-3-乙基碳二亞胺鹽酸鹽(edci)、1-羥基苯並三唑(hobt)、1-羥基-7-氮雜-苯並三唑(hoat)、hbtu(o-苯並三唑-1-基-n,n,n』,n』-四甲基脲鎓六氟磷酸鹽)、hatu(o-(7-氮雜苯並三唑-1-基)-1,1,3,3-四甲基脲鎓六氟磷酸鹽)等或其組合存在下進行。反應一般在叔胺鹼,如二異丙基乙基胺存在下進行。合適的溶劑包括二氯甲烷、n,n-二甲基甲醯胺(dmf)、二甲亞碸(dmso)、乙酸乙酯等。通過在合適條件下的去保護去除所得二肽(c)上的氨基保護基團。例如,在pg是boc基團的情況中,用三氟乙酸處理化合物(c)以形成游離胺(d)。在pg是fmoc基團的情況中,用哌啶或二乙基胺處理化合物(c)以產生化合物(d)。在上述的肽偶聯條件下,化合物(d)然後偶聯至胺基酸衍生物(e)(如果需要,以保護形式)以生成三肽(f)。用酸處理去除羧基保護基團以提供游離酸(g)。
方案b
參考方案b,在上述肽偶聯條件下,命名為(h)的氨基保護海兔脯氨酸(dap)(參見pettit等,(1994)j.org.chem.59∶6287-6295)與胺(j)(其使用本領域已知的方法製備)偶聯。如方案a所述,所得的二肽(k)受保護以提供化合物(l)。
方案c
參考方案c,酸(g)和胺(l)在上述肽偶聯條件下偶聯以提供式(i)的化合物。在反應產物是式(i)的保護形式的情況中,採用合適的去保護條件以得到目標化合物。
實施例
提供以下實施例以顯示,但不限制本文提供的組合物、用途和方法。使用上述通用方法製備化合物。
在實施例中使用以下化學縮寫:dov(海兔纈氨酸);abu(2-氨基丁酸);dil(海兔異亮氨酸);dpr(2,3-二氨基丙酸);su(琥珀醯亞胺基);dab(2,4-二氨基丁酸);dap(海兔脯氨酸);bzl(苄基);和tr(三苯甲基)。
在40℃下使用以下方法之一(所示),在aquityuplcbehc81.7μm2.1x50mm柱上獲取lcms停留時間:
方法a:0-0.50分鐘:等度80水/10乙腈/10水中1%甲酸;0.50-3.50分鐘:線性梯度80水/10乙腈/10水中1%甲酸至0水/90乙腈/10水中1%甲酸;3.50-3.99分鐘等度0水/90乙腈/10水中1%甲酸;3.99-4.00分鐘線性梯度0水/90乙腈/10水中1%甲酸至80水/10乙腈/10水中1%甲酸。
方法b:0-0.50分鐘:等度85水/5乙腈/10水中1%甲酸;0.50-1.60分鐘:線性梯度85水/5乙腈/10水中1%甲酸至0水/98乙腈/2水中1%甲酸;1.60-1.80分鐘等度0水/98乙腈/2水中1%甲酸;1.80-1.90分鐘線性梯度0水/98乙腈/10水中1%甲酸至85水/10乙腈/5水中1%甲酸;1.90-2.00分鐘等度85水/5乙腈/10水中1%甲酸。
實施例1
(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-3-羥基-n-甲基丙醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯氨基)-3-苯基丙酸甲酯
向ch2cl2(20ml)中boc-dap-oh二環己基胺鹽(8.00g,17.1mmol)和h-phe-omehcl鹽(4.42g,20.5mmol)的攪拌的室溫懸液中添加二異丙基乙基胺(diea;9.13ml,51.3mmol),之後添加焦碳酸二乙酯(depc;5.15ml,34.2mmol)。10小時後,通過液相色譜/質譜(lcms)的分析顯示反應完成。使用ch2cl2中2%至10%meoh作為洗脫液,通過矽膠(矽膠40μm,3.0x17.0cm)上的快速色譜來分離boc-dap-phe-ome。獲得總共7.45g的boc-dap-phe-ome(16.61mmol,97%產率)。
向ch2cl2(10ml)中boc-dap-phe-ome(4.67g,10.4mmol)的攪拌的室溫溶液添加三氟乙酸(tfa;10ml)。10小時後,通過lcms的分析顯示反應完全。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共2.52g的h-dap-phe-ome的tfa鹽(6.23mmol,59%)。
向乙酸乙酯(etoac;15ml)中fmoc-ser(bzl)-oh(2.82g,6.76mmol)和h-dil-otbu鹽酸鹽(2.00g,6.76mmol)的攪拌的室溫溶液中添加diea(2.17ml,12.2mmol)。溶液冷卻至(0℃)並攪拌20分鐘。向反應混合物中添加diea(2.17ml,12.2mmol)。溶液冷卻至(0℃)並攪拌20分鐘。向反應混合物中添加2-氯-1-甲基碘化吡啶鎓(cmpi;2.76g,10.8mmol)並且使反應混合物達到室溫。12小時後,通過lcms的分析顯示反應完全。用0.1mhcl(150mlx2)洗滌粗反應。有機餾分在硫酸鎂墊上乾燥、過濾並真空濃縮。使用己烷中18%至90%etoac作為洗脫液,通過矽膠(矽膠40μm,3.0x17.0cm)上的快速色譜來分離fmoc-ser(bzl)-dil-otbu。獲得總共3.75g的fmoc-ser(bzl)-dil-otbu(5.69mmol,84%產率)。
向mecn(5ml)中fmoc-ser(bzl)-dil-otbu(1.79g,2.72mmol)的攪拌室溫溶液中添加哌啶(4ml)。5小時後,通過lcms的分析顯示反應完全。用己烷萃取粗反應混合物並且mecn層經真空濃縮以產生不需要進一步純化使用的粗h-ser(bzl)-dil-otbu。
向dmf(10ml)中粗h-ser(bzl)-dil-otbu和dov(0.790g,5.44mmol)的攪拌室溫懸液中添加diea(1.45ml,8.16mmol),之後添加hatu(2.07g,5.44mmol)。5小時後,通過lcms的分析顯示反應完全。粗反應混合物用飽和碳酸氫鈉(10ml)稀釋,並用etoac(40mlx2)萃取。合併的有機餾分用鹽水洗滌、在硫酸鎂墊上乾燥、過濾並真空濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共0.882g的dov-ser(bzl)-dil-otbu的tfa鹽(1.30mmol,48%)。
向ch2cl2(5ml)中dov-ser(bzl)-dil-otbu(0.288g,0.425mmol)的室溫溶液中添加tfa(4ml)。10小時後,通過lcms的分析顯示反應完全。揮發性有機物真空蒸發以產生不需要進一步純化使用的粗dov-ser(bzl)-dil-ohtfa鹽。
向dmf(10ml)中粗dov-ser(bzl)-dil-ohtfa鹽和h-dap-phe-ometfa鹽(0.163g,0.467mmol)的攪拌室溫懸液中添加diea(1.45ml,1.70mmol),之後添加hatu(0.323g,0.850mmol)。6小時後,通過lcms的分析顯示反應完全。粗反應混合物用飽和碳酸氫鈉(10ml)稀釋,並用etoac(40mlx2)萃取。合併的有機餾分用鹽水洗滌、在硫酸鎂墊上乾燥、過濾並真空濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共0.217g的dov-ser(bzl)-dil-dap-phe-ome的tfa鹽(0.228mmol,54%)。
在回流條件下,對meoh(5ml)中dov-ser(bzl)-dil-dap-phe-ometfa鹽(0.217g,0.228mmol)和活性炭載鈀(10%pd基,0.174g)的攪拌室溫懸液進行氫化。48小時後,通過lcms的分析顯示反應完全。粗反應混合物在硅藻土墊上過濾並且將濾液濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共0.104g的標題化合物的tfa鹽(0.121mmol,47%)。lcmsrt=2.32分鐘(方法a);esi-msm/z748.72[m+h]+;hrmsm/z748.4846[c39h65n5o9+h]+.
實施例2
(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((2s,3r)-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-3-羥基-n-甲基丁醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯氨基)-3-苯基丙酸甲酯
向etoac(15ml)中fmoc-thr(bzl)-oh(2.92g,6.76mmol)和h-dil-otbu鹽酸鹽(2.00g,6.76mmol)的攪拌室溫溶液中添加diea(2.17ml,12.2mmol)。溶液冷卻(0℃)並攪拌20分鐘。向反應混合物中添加diea(2.17ml,12.2mmol)。溶液冷卻(0℃)並攪拌20分鐘。向反應混合物中添加cmpi(2.76g,10.8mmol)並且使反應混合物達到室溫。12小時後,通過lcms的分析顯示反應完全。用0.1mhcl(100mlx2)洗滌粗反應。有機餾分在硫酸鎂墊上乾燥、過濾並真空濃縮。使用己烷中18%至90%etoac作為洗脫液,通過矽膠(矽膠40μm,3.0x17.0cm)上的快速色譜來分離fmoc-thr(bzl)-dil-otbu。獲得總共3.71g的fmoc-thr(bzl)-dil-otbu(5.51mmol,82%產率)。
向mecn(5ml)中fmoc-thr(bzl)-dil-otbu(3.71g,5.51mmol)的攪拌室溫溶液中添加哌啶(4ml)。5小時後,通過lcms的分析顯示反應完全。用己烷萃取粗反應混合物並且mecn層經真空濃縮以產生不需要進一步純化使用的粗h-thr(bzl)-dil-otbu。
向dmf(20ml)中粗h-thr(bzl)-dil-otbu和dov(1.60g,11.0mmol)的攪拌室溫懸液中添加diea(2.95ml,16.5mmol),之後添加hatu(4.19g,11.0mmol)。6小時後,通過lcms的分析顯示反應完全。粗反應混合物用飽和碳酸氫鈉(10ml)稀釋,並用etoac(40mlx2)萃取。合併的有機餾分用鹽水洗滌、在硫酸鎂墊上乾燥、過濾並真空濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共1.09g的dov-ser(bzl)-dil-otbu的tfa鹽(1.58mmol,29%)。
向ch2cl2(5ml)中dov-thr(bzl)-dil-otbutfa鹽(0.331g,0.478mmol)的室溫溶液中添加tfa(4ml)。10小時後,通過lcms的分析顯示反應完全。揮發性有機物真空蒸發以產生不需要進一步純化使用的粗dov-thr(bzl)-dil-ohtfa鹽。
向dmf(10ml)中粗dov-thr(bzl)-dil-ohtfa鹽和h-dap-phe-ometfa鹽(0.183g,0.526mmol)的攪拌室溫懸液中添加diea(0.341ml,1.92mmol),之後添加hatu(0.364g,0.957mmol)。24小時後,通過lcms的分析顯示反應完全。粗反應混合物用飽和碳酸氫鈉(10ml)稀釋,並用etoac(40mlx2)萃取。合併的有機餾分用鹽水洗滌、在硫酸鎂墊上乾燥、過濾並真空濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共0.290g的dov-thr(bzl)-dil-dap-phe-ome的tfa鹽(0.300mmol,63%)。
對meoh(5ml)中dov-thr(bzl)-dil-dap-phe-ometfa鹽(0.290g,0.300mmol)和活性炭載鈀(10%pd基,0.232g)的攪拌室溫懸液進行氫化。24小時後,通過lcms的分析顯示反應完全。粗反應混合物在硅藻土墊上過濾並且濾液經濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共0.129g的標題化合物的tfa鹽(0.147mmol,43%)。lcmsrt=2.40分鐘(方法a);esi-msm/z762.75[m+h]+;hrmsm/z762.5009[c40h67n5o9+h]+.
實施例3
(s)-2-(二甲基氨基)-n-((s)-3-羥基-1-(((3r,4s,5s)-3-甲氧基-1-((s)-2-((1r,2r)-1-甲氧基-2-甲基-3-氧代-3-((2-(吡啶-2-基)乙基)氨基)丙基)吡咯烷-1-基)-5-甲基-1-氧代庚-4-基)(甲基)氨基)-1-氧代丙-2-基)-3-甲基丁醯胺
向ch2cl2(20ml)中boc-dap-oh二環己基胺鹽(10.0g,21.4mmol)和2-(2-吡啶基)乙基胺(3.83ml,32.0mmol)的攪拌的室溫懸液中添加diea(11.4ml,64.1mmol),之後添加depc(4.83ml,32.0mmol)。過夜攪拌後,通過lcms的分析顯示反應完全。使用ch2cl2中2%至10%meoh/1%net3作為洗脫液,通過矽膠(矽膠40μm,3.0x17.0cm)上的快速色譜來分離boc-dap-2-(2-吡啶基)乙基胺。獲得總共7.42g的boc-dap-2-(2-吡啶基)乙基胺(19.0mmol,89%產率)。
向ch2cl2(10ml)中boc-dap-2-(2-吡啶基)乙基胺(7.42g,19.0mmol)的攪拌室溫溶液添加tfa(10ml)。過夜攪拌後,通過lcms的分析顯示反應完全。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共4.50g的h-dap-(2-吡啶基)乙基胺的tfa鹽(11.1mmol,59%)。
向ch2cl2(5ml)中dov-ser(bzl)-dil-otbu(0.287g,0.423mmol)的室溫溶液中添加tfa(4ml)。10小時後,通過lcms的分析顯示反應完全。揮發性有機物真空蒸發以產生不需要進一步純化使用的粗dov-ser(bzl)-dil-ohtfa鹽。
向dmf(10ml)中粗dov-ser(bzl)-dil-ohtfa鹽和h-dap-2-(2-吡啶基)乙基胺tfa鹽(0.136g,0.466mmol)的攪拌室溫懸液中添加diea(0.302ml,1.70mmol),之後添加hatu(0.322g,0.847mmol)。6小時後,通過lcms的分析顯示反應完全。粗反應混合物用飽和碳酸氫鈉(10ml)稀釋,並用etoac(40mlx2)萃取。合併的有機餾分用鹽水洗滌、在硫酸鎂墊上乾燥、過濾並真空濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共0.258g的dov-ser(bzl)-dil-dap-2-(2-吡啶基)乙基胺的tfa鹽(0.288mmol,68%)。
對meoh(5ml)中dov-ser(bzl)-dil-dap-2-(2-吡啶基)乙基胺tfa鹽(0.258g,0.330mmol)、甲酸銨(0.062g,0.991mmol)和活性炭載鈀(10%pd基,0.100g)的攪拌室溫懸液進行氫化。12小時後,通過lcms的分析顯示反應完全。粗反應混合物在硅藻土墊上過濾並且濾液經濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共0.014g的標題化合物的tfa鹽(0.017mmol,5%)。lcmsrt=1.76分鐘(方法a);esi-msm/z691.56[m+h]+;hrmsm/z691.4755[c36h62n6o7+h]+.
實施例4
(2s,3r)-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-3-羥基-n-((3r,4s,5s)-3-甲氧基-1-((s)-2-((1r,2r)-1-甲氧基-2-甲基-3-氧代-3-((2-(吡啶-2-基)乙基)氨基)丙基)吡咯烷-1-基)-5-甲基-1-氧代庚-4-基)-n-甲基丁醯胺
向ch2cl2(5ml)中dov-thr(bzl)-dil-otbu(0.357g,0.618mmol)的室溫溶液中添加tfa(4ml)。10小時後,通過lcms的分析顯示反應完全。揮發性有機物真空蒸發以產生不需要進一步純化使用的粗dov-thr(bzl)-dil-ohtfa鹽。
向dmf(10ml)中粗dov-thr(bzl)-dil-ohtfa鹽和h-dap-2-(2-吡啶基)乙基胺tfa鹽(0.198g,0.680mmol)的攪拌室溫懸液中添加diea(0.441ml,2.47mmol),之後添加hatu(0.470g,1.24mmol)和hobt(0.189g,1.24mmol)。6小時後,通過lcms的分析顯示反應完全。粗反應混合物用飽和碳酸氫鈉(10ml)稀釋,並用etoac(40mlx2)萃取。合併的有機餾分用鹽水洗滌、在硫酸鎂墊上乾燥、過濾並真空濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共0.356gdov-thr(bzl)-dil-dap-2-(2-吡啶基)乙基胺的tfa鹽(0.392mmol,63%)。
meoh(5ml)中dov-thr(bzl)-dil-dap-2-(2-吡啶基)乙基胺tfa鹽(0.356g,0.392mmol)、甲酸銨(0.085g,1.35mmol)和活性炭載鈀(10%pd基,0.175g)的攪拌室溫懸液經氫化。12小時後,通過lcms的分析顯示反應完全。粗反應混合物在硅藻土墊上過濾並且濾液經濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共0.010g的標題化合物的tfa鹽(0.012mmol,3%)。lcmsrt=1.72分鐘(方法a);esi-msm/z705.56[m+h]+;728.33[m+na]+;hrmsm/z705.4917[c37h64n6o7+h]+.
實施例5
(2s)-2-(二甲基氨基)-n-((2s)-3-羥基-1-(((3r,4s,5s)-3-甲氧基-1-((2s)-2-((1r,2r)-1-甲氧基-2-甲基-3-氧代-3-((2-(哌啶-2-基)乙基)氨基)丙基)吡咯烷-1-基)-5-甲基-1-氧代庚-4-基)(甲基)氨基)-1-氧代丙-2-基)-3-甲基丁醯胺
標題化合物作為實施例3中氫化反應的副產物獲得。獲得總共0.010g的標題化合物的tfa鹽(0.001mmol)。lcmsrt=1.83分鐘(方法a);esi-msm/z697.76[m+h]+;hrmsm/z697.5226[c36h68n6o7+h]+.
實施例6
(2s,3r)-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-3-羥基-n-((3r,4s,5s)-3-甲氧基-1-((2s)-2-((1r,2r)-1-甲氧基-2-甲基-3-氧代-3-((2-(哌啶-2-基)乙基)氨基)丙基)吡咯烷-1-基)-5-甲基-1-氧代庚-4-基)-n-甲基丁醯胺
標題化合物作為實施例4中氫化反應的副產物獲得。獲得總共0.010g的標題化合物的tfa鹽(0.012mmol)。lcmsrt=1.81分鐘(方法a);esi-msm/z711.43[m+h]+;hrmsm/z711.5389[c37h70n6o7+h]+.
實施例7
(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((2s,3s)-3-疊氮基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丁醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯氨基)-3-苯基丙酸甲酯
向etoac(10ml)中(2s,3s)-fmoc-abu(3-n3)-oh(1.00g,2.74mmol)和h-dil-otbu鹽酸鹽(0.810g,2.74mmol)的攪拌室溫溶液中添加diea(0.880ml,4.93mmol)。溶液冷卻(0℃)並攪拌20分鐘。向反應混合物中添加diea(0.880ml,4.93mmol)。溶液冷卻(0℃)並攪拌20分鐘。向反應混合物中添加cmpi(1.12g,4.38mmol)並且使反應混合物達到室溫。12小時後,通過lcms的分析顯示反應完全。用0.1mhcl(100mlx2),之後用鹽水(20mlx2)洗滌粗反應。有機餾分在硫酸鎂墊上乾燥、過濾並真空濃縮以產生不需要進一步純化使用的粗fmoc-abu(3-n3)-dil-otbu(1.12g,1.84mmol)。
向mecn(10ml)中fmoc-abu(3-n3)-dil-otbu(1.00g,1.65mmol)的攪拌室溫溶液中添加哌啶(2ml)。5小時後,通過lcms的分析顯示反應完全。用己烷萃取粗反應混合物並且mecn層經真空濃縮以產生不需要進一步純化使用的粗h-abu(3-n3)-dil-otbu。
向dmf(10ml)中粗h-abu(3-n3)-dil-otbu和dov(0.478g,3.29mmol)的攪拌室溫懸液中添加diea(0.880ml,4.94mmol),之後添加hatu(1.25g,3.29mmol)。6小時後,通過lcms的分析顯示反應完全。粗反應混合物用飽和碳酸氫鈉(10ml)稀釋,並用etoac(40mlx2)萃取。合併的有機餾分用鹽水洗滌、在硫酸鎂墊上乾燥、過濾並真空濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共0.670g的dov-abu(3-n3)-dil-otbu的tfa鹽(1.07mmol,65%)。
向ch2cl2(5ml)中dov-abu(3-n3)-dil-otbutfa鹽(0.289g,0.425mmol)的室溫溶液中添加tfa(5ml)。12小時後,通過lcms的分析顯示反應完全。揮發性有機物真空蒸發以產生不需要進一步純化使用的粗dov-abu(3-n3)-dil-ohtfa鹽。
向dmf(10ml)中粗dov-abu(3-n3)-dil-ohtfa鹽(1.04g,1.82mmol)和h-dap-phe-ometfa鹽(1.59g,3.44mmol)的攪拌室溫懸液中添加diea(1.18g,1.60ml,9.11mmol),之後添加hatu(1.74g,4.56mmol)。10小時後,通過lcms的分析顯示反應完全。粗反應混合物用飽和碳酸氫鈉(10ml)稀釋,並用etoac(20mlx3)萃取。合併的有機餾分用鹽水洗滌、在硫酸鎂墊上乾燥、過濾並真空濃縮。通過用phenomenexgemininx-c1810μ柱(150x30mm)的,使用0.1%水性甲酸中10%至90%mecn的製備型rp-hplc純化粗製油狀物。獲得總共935mg的標題化合物的甲酸鹽(1.12mmol,49%)。lcmsrt=1.09分鐘(方法a);esi-msm/z787.53[m+h]+;hrmsm/z787.5072[c40h66n8o8+h]+.
實施例8
(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-3-氨基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丙醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯氨基)-3-苯基丙酸甲酯
向etoac(10ml)中fmoc-dpr(boc)-oh(1.44g,3.38mmol)和h-dil-otbu鹽酸鹽(1.00g,3.38mmol)的攪拌室溫溶液中添加diea(1.08ml,6.08mmol)。溶液冷卻至(0℃)並攪拌20分鐘。向反應混合物中添加另外的diea(1.08ml,6.08mmol)並且0℃溶液攪拌20分鐘。向反應混合物中添加cmpi(1.38g,5.41mmol)並且使反應混合物升溫至室溫。12小時後,通過lcms的分析顯示反應完全。用0.1mhcl(100mlx2),之後用鹽水(20mlx2)洗滌粗反應。有機餾分在硫酸鎂墊上乾燥、過濾並真空濃縮。使用己烷中18%至90%etoac作為洗脫液,通過矽膠(矽膠40μm,3.0x17.0cm)上的快速色譜來分離fmoc-dpr(boc)-dil-otbu。獲得總共1.27g的fmoc-dpr(boc)-dil-otbu(1.90mmol,56%產率)。
向mecn(10ml)中fmoc-thr(bzl)-dil-otbu(1.27g,1.90mmol)的攪拌室溫溶液中添加哌啶(2ml)。5小時後,通過lcms的分析顯示反應完全。用己烷萃取粗反應混合物並且mecn層經真空濃縮以產生不需要進一步純化使用的粗h-dpr(boc)-dil-otbu。
向dmf(10ml)中粗h-dpr(boc)-dil-otbu和dov(0.552g,3.80mmol)的攪拌室溫懸液中添加diea(1.02ml,5.70mmol),之後添加hatu(1.45g,3.80mmol)。6小時後,通過lcms的分析顯示反應完全。粗反應混合物用飽和碳酸氫鈉(10ml)稀釋,並用etoac(40mlx2)萃取。合併的有機餾分用鹽水洗滌、在硫酸鎂墊上乾燥、過濾並真空濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共0.598g的dov-dpr(boc)-dil-otbu的tfa鹽(0.871mmol,46%)。
向ch2cl2(10ml)中dov-dpr(boc)-dil-otbutfa鹽(1.52g,2.65mmol)的室溫溶液中添加tfa(5ml)。10小時後,通過lcms的分析顯示反應完全。揮發性有機物真空蒸發以產生不需要進一步純化使用的粗dov-dpr-dil-ohtfa鹽。
向ch2cl2(10ml)中dov-dpr-dil-ohtfa鹽(1.00g,1.89mmol)和fmoc-osu(0.891g,2.64mmol)的攪拌室溫懸液中添加diea(0.460ml,2.64mmol)。12小時後,通過lcms的分析顯示反應完全。揮發性有機物真空蒸發。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.1%水性甲酸中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共1.49g的富集dov-dpr(fmoc)-dil-oh的甲酸鹽。
向dmf(10ml)中dov-dpr(fmoc)-dil-oh甲酸鹽(1.20g,1.75mmol)和h-dap-phe-ometfa鹽(0.982g,2.13mmol)的攪拌23℃懸液中添加diea(0.970g,1.30ml,7.514mmol),之後添加hatu(1.43g,3.76mmol)。10小時後,通過lcms的分析顯示反應完全。粗反應用飽和碳酸氫鈉(10ml)稀釋,並用etoac(20mlx3)萃取。合併的有機餾分用鹽水洗滌、在硫酸鎂墊上乾燥、過濾並真空濃縮。通過用phenomenexgemininx-c1810μ柱(150x30mm)的,使用0.1%水性nh4oh中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共1.01g的dov-dpr(fmoc)-dil-dap-phe-ome(1.04mmol,56%)。
向乙腈(10ml)中dov-dpr(fmoc)-dil-dap-phe-ome(1.01g,1.04mmol)的攪拌23℃溶液中添加哌啶(5ml)。3小時後,通過lcms的分析顯示反應完全。向粗反應溶液中添加己烷。乙腈層經真空濃縮。通過用phenomenexgemininx-c1810μ柱(150x30mm)的,使用0.1%水性甲酸中5%至95%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共413g的標題化合物的甲酸鹽(0.521mmol,50%)。lcmsrt=2.10分鐘(方法a);esi-msm/z747.84[m+h]+;hrmsm/z747.5008[c39h66n6o8+h]+.
實施例9
(s)-n-((s)-3-氨基-1-(((3r,4s,5s)-3-甲氧基-1-((s)-2-((1r,2r)-1-甲氧基-2-甲基-3-氧代-3-((2-(吡啶-2-基)乙基)氨基)丙基)吡咯烷-1-基)-5-甲基-1-氧代庚-4-基)(甲基)氨基)-1-氧代丙-2-基)-2-(二甲基氨基)-3-甲基丁醯胺
向dmf(10ml)中粗dov-dpr(fmoc)-dil-oh和h-dap-2-(2-吡啶基)乙基胺tfa鹽(0.230g,0.789mmol)的攪拌室溫懸液中添加diea(0.511ml,2.87mmol),之後添加hatu(0.545g,1.43mmol)。6小時後,通過lcms的分析顯示反應完全。粗反應混合物用飽和碳酸氫鈉(10ml)稀釋,並用etoac(25mlx3)萃取。合併的有機餾分用鹽水洗滌、在硫酸鎂墊上乾燥、過濾並真空濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共0.150gdov-dpr(fmoc)-dil-dap-2-(2-吡啶基)乙基胺的tfa鹽(0.146mmol,20%)。
向mecn(10ml)中dov-dpr(fmoc)-dil-dap-2-(2-吡啶基)乙基胺tfa鹽(0.150g,0.146mmol)的攪拌室溫溶液中添加哌啶(2ml)。5小時後,通過lcms的分析顯示反應完全。用己烷萃取粗反應混合物並且mecn層經真空濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共0.089g的標題化合物的tfa鹽(0.111mmol,75%)。lcmsrt=1.52分鐘(方法a);esi-msm/z690.67[m+h]+;hrmsm/z690.4917[c36h63n7o6+h]+.
實施例10
(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-3-疊氮基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丙醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯氨基)-3-苯基丙酸甲酯
向etoac(10ml)中n-boc-4-疊氮基-丙氨酸二環己基胺鹽(1.02g,2.47mmol)和h-dil-otbu鹽酸鹽(0.730g,2.74mmol)的攪拌室溫溶液中添加diea(0.792ml,4.44mmol)。溶液冷卻(0℃)並攪拌20分鐘。向反應混合物中添加diea(0.792ml,4.44mmol)。溶液冷卻(0℃)並攪拌20分鐘。向反應混合物中添加cmpi(1.01g,3.95mmol)並且使反應混合物達到室溫。12小時後,通過lcms的分析顯示反應完全。用0.1mhcl(100mlx2),之後用鹽水(20mlx2)洗滌粗反應。有機餾分在硫酸鎂墊上乾燥、過濾並真空濃縮以產生不需要進一步純化使用的粗n-boc-4-疊氮基-ala-dil-otbu(1.08g,2.29mmol)。
向ch2cl2(5ml)中n-boc-4-疊氮基-ala-dil-otbu(1.08g,2.29mmol)的室溫溶液中添加tfa(3ml)。10小時後,通過lcms的分析顯示反應完全。揮發性有機物真空蒸發以產生不需要進一步純化使用的粗h-4-疊氮基-ala-dil-ohtfa鹽。
向dmf(10ml)中dov(0.739g,5.09mmol)的攪拌室溫懸液中添加diea(1.36ml,7.63mmol),之後添加hatu(1.95g,5.09mmol)。在10分鐘後,向反應混合物中添加粗h-4-疊氮基-ala-dil-oh。6小時後,通過lcms的分析顯示反應完全。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共0.130gdov-4-疊氮基-ala-dil-oh的tfa鹽(0.261mmol,10%)。
向dmf(10ml)中粗dov-4-疊氮基-ala-dil-ohtfa鹽(0.130g,0.261)和h-dap-phe-ometfa鹽(0.205g,0.588mmol)的攪拌室溫懸液中添加diea(0.140ml,0.783mmol),之後添加hatu(0.198g,0.522mmol)。6小時後,通過lcms的分析顯示反應完全。粗反應混合物用飽和碳酸氫鈉(10ml)稀釋,並用etoac(40mlx2)萃取。合併的有機餾分用鹽水洗滌、在硫酸鎂墊上乾燥、過濾並真空濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共0.015g的標題化合物的tfa鹽(0.017mmol,7%)。lcmsrt=2.36分鐘(方法a);esi-msm/z773.48[m+h]+;hrmsm/z773.4916[c39h64n8o8+h]+.
實施例11
(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-4-疊氮基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丁醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯氨基)-3-苯基丙酸甲酯
向etoac(10ml)中n-boc-4-疊氮基-高丙氨酸二環己基胺鹽(1.01g,2.37mmol)和h-dil-otbu鹽酸鹽(0.700g,2.37mmol)的攪拌室溫溶液中添加diea(0.759ml,4.26mmol)。溶液冷卻(0℃)並攪拌20分鐘。向反應混合物中添加diea(0.759ml,4.26mmol)。溶液冷卻(0℃)並攪拌20分鐘。向反應混合物中添加cmpi(0.967g,3.79mmol)並且使反應混合物達到室溫。12小時後,通過lcms的分析顯示反應完全。用0.1mhcl(100mlx2),之後用鹽水(20mlx2)洗滌粗反應。有機餾分在硫酸鎂墊上乾燥、過濾並真空濃縮以產生不需要進一步純化使用的粗n-boc-4-疊氮基-高ala-dil-otbu(1.09g,2.25mmol)。
向ch2cl2(5ml)中n-boc-4-疊氮基-高ala-dil-otbu(1.09g,2.25mmol)的室溫溶液中添加tfa(3ml)。10小時後,通過lcms的分析顯示反應完全。揮發性有機物真空蒸發以產生不需要進一步純化使用的粗h-4-疊氮基-高ala-dil-ohtfa鹽。
向dmf(10ml)中dov(0.652g,4.49mmol)的攪拌室溫懸液中添加diea(1.20ml,6.73mmol),之後添加hatu(1.71g,4.49mmol)。在10分鐘後,向反應混合物中添加粗h-4-疊氮基-高ala-dil-ohtfa鹽。6小時後,通過lcms的分析顯示反應完全。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共0.127g的dov-4-疊氮基-高ala-dil-oh的tfa鹽(0.223mmol,10%)。
向dmf(10ml)中粗dov-4-疊氮基-高ala-dil-ohtfa鹽(0.127g,0.223)和h-dap-phe-ometfa鹽(0.198mmol,0.568mmol)的攪拌室溫懸液中添加diea(0.140ml,0.783mmol),之後添加hatu(0.198g,0.522mmol)。6小時後,通過lcms的分析顯示反應完全。粗反應混合物用飽和碳酸氫鈉(10ml)稀釋,並用etoac(40mlx2)萃取。合併的有機餾分用鹽水洗滌、在硫酸鎂墊上乾燥、過濾並真空濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共0.015g的標題化合物的tfa鹽(0.017mmol,7%)。lcmsrt=2.38分鐘(方法a);esi-msm/z787.49[m+h]+;hrmsm/z787.5078[c40h66n8o8+h]+.
實施例12
(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-4-氨基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丁醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯氨基)-3-苯基丙酸甲酯
向etoac(10ml)中fmoc-dab(boc)-oh(1.54g,3.38mmol)和h-dil-otbu鹽酸鹽(1.00g,3.38mmol)的攪拌室溫溶液中添加diea(1.08ml,6.08mmol)。溶液冷卻(0℃)並攪拌20分鐘。向反應混合物中添加另外的diea(1.08ml,6.08mmol)並且0℃溶液攪拌20分鐘。然後,向反應混合物中添加cmpi(1.38g,5.41mmol)並且使反應混合物升溫至室溫。12小時後,通過lcms的分析顯示反應完全。用0.1mhcl(100mlx2),之後用鹽水(20mlx2)洗滌粗反應。有機餾分在硫酸鎂墊上乾燥、過濾並真空濃縮。使用己烷中18%至90%etoac作為洗脫液,通過矽膠(矽膠40μm,3.0x17.0cm)上的快速色譜來分離fmoc-dab(boc)-dil-otbu。獲得總共1.18g的fmoc-dpr(boc)-dil-otbu(1.73mmol,51%產率)。
向mecn(10ml)中fmoc-dab(boc)-dil-otbu(1.18g,1.73mmol)的攪拌室溫溶液中添加哌啶(2ml)。5小時後,通過lcms的分析顯示反應完全。用己烷萃取粗反應混合物並且mecn層經真空濃縮以產生不需要進一步純化使用的粗h-dab(boc)-dil-otbu。
向dmf(10ml)中粗h-dab(boc)-dil-otbu和dov(0.502g,3.46mmol)的攪拌室溫懸液中添加diea(0.925ml,5.19mmol),之後添加hatu(1.32g,3.46mmol)。6小時後,通過lcms的分析顯示反應完全。粗反應混合物用飽和碳酸氫鈉(10ml)稀釋,並用etoac(40mlx2)萃取。合併的有機餾分用鹽水洗滌、在硫酸鎂墊上乾燥、過濾並真空濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共0.410g的dov-dab(boc)-dil-otbu的tfa鹽(0.583mmol,34%)。
向ch2cl2(10ml)中dov-dab(boc)-dil-otbutfa鹽(0.240g,0.419mmol)的室溫溶液中添加tfa(2ml)。10小時後,通過lcms的分析顯示反應完全。揮發性有機物真空蒸發以產生不需要進一步純化使用的粗dov-dab-dil-ohtfa鹽。
向ch2cl2(5ml)中dov-dab-dil-ohtfa鹽(0.175g,0.406mmol)和fmoc-osu(0.151g,0.447mmol)的攪拌室溫懸液中添加diea(0.080ml,0.447mmol)。12小時後,通過lcms的分析顯示反應完全。揮發性有機物真空蒸發。粗反應混合物溶於etoac並用0.1mhcl(100mlx2),之後用鹽水(20mlx2)洗滌。有機餾分在硫酸鎂墊上乾燥、過濾並真空濃縮以產生不需要進一步純化使用的粗dov-dab(fmoc)-dil-oh。
向dmf(10ml)中粗dov-dab(fmoc)-dil-oh(0.363g,0.556mmol)和h-dap-phe-ometfa鹽(0.194g,0.420mmol)的攪拌室溫懸液中添加diea(0.291ml,1.67mmol),之後添加hatu(0.424g,1.11mmol)。10小時後,通過lcms的分析顯示反應完全。粗反應混合物用飽和碳酸氫鈉(10ml)稀釋,並用etoac(30mlx2)萃取。合併的有機餾分用鹽水洗滌、在硫酸鎂墊上乾燥、過濾並真空濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.2%水性甲酸中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共449mg的富集dov-dab(fmoc)-dil-dap-phe-ome的甲酸鹽。
向mecn(10ml)中dov-dab(fmoc)-dil-dap-phe-ome甲酸鹽(0.449g)的攪拌室溫溶液中添加哌啶(5ml)。10小時後,通過lcms的分析顯示反應完全。用己烷萃取粗反應混合物並且mecn層經真空濃縮。通過用phenomenexgemininxc1810μmax-rp柱(150x30mm)的,使用0.1%水性甲酸中10%至90%mecn作為洗脫液的rp-hplc純化粗製油狀物。獲得總共43.0g的標題化合物的甲酸鹽(0.053mmol,13%)。lcmsrt=1.24分鐘(方法b);esi-msm/z761.57[m+h]+;hrmsm/z761.5165[c40h68n6o8+h]+.
實施例13
(s)-2-((s)-2-(氨基氧基)-3-甲基丁醯氧基)-n-((3r,4s,5s)-3-甲氧基-1-((s)-2-((1r,2r)-1-甲氧基-2-甲基-3-氧代-3-((2-(吡啶-2-基)乙基)氨基)丙基)吡咯烷-1-基)-5-甲基-1-氧代庚-4-基)-n,3-二甲基丁醯胺
向在etoac(3ml)中攪拌的h-dil-otbu鹽酸鹽(0.60g。2.03mmol)和fmoc-val-oh(0.829g,2.44mmol)的溶液中添加diea(0.65ml,3.7mmol)。反應冷卻至0℃並攪拌20分鐘,之後添加diea(0.65ml,3.7mmol)。反應混合物再冷卻(0℃)20分鐘,之後添加cmpi(0.83g,3.7mmol)。8小時後,通過lcms的分析顯示反應完全。用1mhcl(150mlx2)和鹽水(50ml)洗滌反應混合物。有機相在na2so4上乾燥,過濾並真空濃縮。使用己烷中18%至90%etoac作為洗脫液,通過矽膠(矽膠40μm,3.0x17.0cm)上的快速色譜來分離fmoc-val-dil-otbu。獲得總共1.1g的fmoc-val-dil-otbu(1.9mmol,93%產率)。
向ch2cl2(10ml)中fmoc-val-dil-otbu(0.883g,1.52mmol)和boc-dap-2-(2-吡啶基)乙基胺(0.451g,1.52mmol)的攪拌室溫懸液添加tfa(5ml)。8小時後,通過lcms的分析顯示反應完全。揮發性有機物真空蒸發以產生粗fmoc-val-dil-oh和h-dap-2-(2-吡啶基)乙基胺tfa鹽,其使用不需要進一步純化。
向etoac(2ml)中粗h-dap-2-(2-吡啶基)乙基胺tfa鹽和fmoc-val-dil-oh的攪拌室溫懸液中添加diea(1.10ml,6.08mmol),之後添加depc(0.92ml,6.08mmol)。15小時後,通過lcms的分析顯示反應完全。反應用飽和nahco3溶液(50ml),之後用水(50mlx2)洗滌。有機餾分在硫酸鎂墊上過濾並真空濃縮。使用ch2cl2中5%至10%meoh作為洗脫液,痛過矽膠(矽膠40μm,23x123mm)上的快速色譜來純化所得粘稠油狀物。獲得總共0.888g的fmoc-val-dil-dap-2-(2-吡啶基)乙基胺(1.11mmol,73%產率)。
向ch2cl2(5ml)中fmoc-val-dil-dap-2-(2-吡啶基)乙基胺(1.75g,2.19mmol)的攪拌室溫溶液添加哌啶(5ml)。8小時後,通過lcms的分析顯示反應完全。揮發性有機物真空蒸發以產生粗h-val-dil-dap-2-(2-吡啶基)乙基胺,其使用不需要進一步純化。
向dmf(5ml)中粗h-val-dil-dap-2-(2-吡啶基)乙基胺和n-boc-n-羥基val-oh(0.390g,1.67mmol)的攪拌室溫懸液中添加diea(0.797ml,5.02mmol),之後添加hatu(1.28g,3.34mmol)。8小時後,通過lcms的分析顯示反應完全。粗反應混合物用飽和碳酸氫鈉(10ml)稀釋,並用etoac(50mlx3)萃取。合併的有機餾分用鹽水洗滌,在硫酸鎂墊上乾燥,過濾並真空濃縮以產生0.563g的粗n-boc-n-羥基val-val-dil-dap-2-(2-吡啶基)乙基胺(0.712mmol,43%),其使用不需要進一步純化。
向dmf(2ml)中n-boc-n-羥基val-val-dil-dap-2-(2-吡啶基)乙基胺(0.563g,0.712mmol)的室溫溶液添加tfa(2ml)。2小時後,通過lcms的分析顯示反應完全。揮發性有機物真空蒸發。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共0.209g的標題化合物的tfa鹽(0.302mmol,43%)。lcmsrt=1.70分鐘(方法a);esi-msm/z691.53[m+h]+;hrmsm/z691.4755[c36h62n6o7+h]+.
實施例14
((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-2-((s)-2-(二甲基氨基)-3-羥基丙醯氨基)-n,3-二甲基丁醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯基)-l-苯丙氨酸
向meoh(10ml)中h-ser(bzl)-oh(0.500g,2.56mmol)和多聚甲醛(1.15g,38.4mmol)的攪拌室溫溶液中添加hco2nh4(0.808g,12.8mmol)和活性炭載鈀(10%pd基,0.250g)。72小時後,通過lcms的分析顯示反應完全。粗反應混合物在硅藻土墊上過濾並且濾液經濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共0.168g的n,n-二甲基ser(bzl)-oh的tfa鹽(0.498mmol,19%)。
向ch2cl2(20ml)中fmoc-val-dil-otbu(13.3g,22.8mmol)的攪拌室溫溶液中添加哌啶(15ml)。8小時後,通過lcms的分析顯示反應完全。揮發性有機物真空蒸發以產生不需要進一步純化使用的粗h-val-dil-otbu。
向dmf(10ml)中粗h-val-dil-otbu和n,n-二甲基ser(bzl)-ohtfa鹽(0.780g,3.49mmol)的攪拌室溫懸液中添加diea(1.25ml,6.99mmol),之後添加hatu(1.77g,4.66mmol)。6小時後,通過lcms的分析顯示反應完全。粗反應混合物用飽和碳酸氫鈉(10ml)稀釋,並用etoac(40mlx2)萃取。合併的有機餾分用鹽水洗滌、在硫酸鎂墊上乾燥、過濾並真空濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共0.220g的n,n-二甲基ser(bzl)-val-dil-otbu的tfa鹽(0.325mmol,14%)。
向ch2cl2(5ml)中n,n-二甲基ser(bzl)-val-dil-otbutfa鹽(0.220g,0.325mmol)的室溫溶液中添加tfa(2ml)。10小時後,通過lcms的分析顯示反應完全。揮發性有機物真空蒸發以產生不需要進一步純化使用的粗n,n-二甲基ser(bzl)-val-dil-ohtfa鹽。
向dmf(5ml)中粗n,n-二甲基ser(bzl)-val-dil-ohtfa鹽(0.166g,0.477mmol)的攪拌室溫懸液中添加diea(0.207ml,1.30mmol),之後添加hatu(0.330g,0.868mmol)。4小時後,通過lcms的分析顯示反應完全。粗反應混合物用飽和碳酸氫鈉(10ml)稀釋,並用etoac(40mlx2)萃取。合併的有機餾分用鹽水洗滌、在硫酸鎂墊上乾燥、過濾並真空濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共0.201g的n,n-二甲基ser(bzl)-val-dil-dap-phe-ome的tfa鹽(0.211mmol,49%)。
向meoh(6ml)和水(1.0ml)中n,n-二甲基ser(bzl)-val-dil-dap-phe-ometfa鹽(0.201g,0.211mmol)和nh4hco2(2.00g,31.7mmol)的攪拌室溫懸液中添加10%pd/c(10mg)。在室溫下劇烈攪拌該溶液。10小時後,通過lcms分析顯示反應完全,和苯丙氨酸甲酯的水解。反應混合物在硅藻土墊上過濾並且濾液經濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共63.0mg的標題化合物的tfa鹽(0.074mmol,31%)。lcmsrt=2.01分鐘(方法a);esi-msm/z734.61[m+h]+;hrmsm/z734.4715[c38h63n5o9+h]+.
實施例15
((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-2-((2s,3r)-2-(二甲基氨基)-3-羥基丁醯氨基)-n,3-二甲基丁醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯基)-l-苯丙氨酸
向meoh(40ml)中h-thr(bzl)-oh(2.00g,9.56mmol)和多聚甲醛(9.87g,95.6mmol)的攪拌室溫溶液中添加hco2nh4(3.01g,47.8mmol)和活性炭載鈀(10%pd基,1.00g)。72小時後,通過lcms的分析顯示反應完全。粗反應混合物在硅藻土墊上過濾並且濾液經濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共1.54g的n,n-二甲基thr(bzl)-oh的tfa鹽(4.38mmol,19%)。
向dmf(20ml)中粗h-val-dil-otbu和n,n-二甲基thr(bzl)-ohtfa鹽(1.21g,5.10mmol)的攪拌室溫懸液中添加diea(1.82ml,10.2mmol),之後添加hatu(2.59g,6.80mmol)。6小時後,通過lcms的分析顯示反應完全。粗反應混合物用飽和碳酸氫鈉(15ml)稀釋,並用etoac(40mlx2)萃取。合併的有機餾分用鹽水洗滌、在硫酸鎂墊上乾燥、過濾並真空濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共0.161g的n,n-二甲基thr(bzl)-val-dil-otbu的tfa鹽(0.234mmol,7%)。
向ch2cl2(5ml)中n,n-二甲基thr(bzl)-val-dil-otbutfa鹽(0.220g,0.325mmol)的室溫溶液中添加tfa(2ml)。10小時後,通過lcms的分析顯示反應完全。揮發性有機物真空蒸發以產生不需要進一步純化使用的粗n,n-二甲基thr(bzl)-val-dil-ohtfa鹽。
向dmf(5ml)中粗n,n-二甲基thr(bzl)-val-dil-ohtfa鹽(0.118g,0.339mmol)的攪拌室溫懸液中添加diea(0.147ml,0.927mmol),之後添加hatu(0.235g,0.618mmol)。4小時後,通過lcms的分析顯示反應完全。粗反應混合物用飽和碳酸氫鈉(10ml)稀釋,並用etoac(40mlx2)萃取。合併的有機餾分用鹽水洗滌、在硫酸鎂墊上乾燥、過濾並真空濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共0.186g的n,n-二甲基thr(bzl)-val-dil-dap-phe-ome的tfa鹽(0.193mmol,62%)。
向meoh(6ml)和水(1.0ml)中n,n-二甲基thr(bzl)-val-dil-dap-phe-ometfa鹽(0.186g,0.193mmol)和nh4hco2(2.00g,31.7mmol)的攪拌室溫懸液中添加10%pd/c(100mg)。在室溫下劇烈攪拌該溶液。72小時後,通過lcms分析顯示反應完全,和苯丙氨酸甲酯的水解。反應混合物在硅藻土墊上過濾並且濾液經濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共63.0mg的標題化合物的tfa鹽(0.073mmol,38%)。lcmsrt=2.04分鐘(方法a);esi-msm/z748.58[m+h]+;hrmsm/z748.4854[c39h65n5o9+h]+.
實施例16
(s)-2-((2r,3r)-3-((s)-1-((3r,4s,55)-4-((2s,3s)-3-疊氮基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丁醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯氨基)-3-苯基丙酸
向meoh(0.1ml)和thf(0.1ml)中dov-abu(3-n3)-dil-dap-phe-ometfa鹽(60mg,0.067mmol)的攪拌室溫溶液中添加水(0.1ml)中一水合氫氧化鋰(9.6mg,0.229mmol)。12小時後,通過lcms的分析顯示反應完全。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共55.0mg的標題化合物的tfa鹽(0.062mmol,93%)。lcmsrt=2.25分鐘(方法a);esi-msm/z773.45[m+h]+;hrmsm/z773.49119[c39h64n8o8+h]+.
實施例17
(s)-n-((3r,4s,5s)-1-((s)-2-((1r,2r)-3-(((s)-1-氨基-1-氧代-3-苯基丙-2-基)氨基)-1-甲氧基-2-甲基-3-氧代丙基)吡咯烷-1-基)-3-甲氧基-5-甲基-1-氧代庚-4-基)-2-((2s,3r)-2-(二甲基氨基)-3-羥基丁醯氨基)-n,3-二甲基丁醯胺
向ch2cl2(10ml)中n,n-二甲基thr-val-dil-dap-phe-ohtfa鹽(40mg,0.053mmol)的攪拌室溫溶液中加入氯化銨(5.72mg,0.107mmol)、diea(28.6μl,0.160mmol)和edci(30.3mg,0.107mmol)。12小時後,通過lcms的分析顯示反應完全。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共28.0mg的標題化合物的tfa鹽(0.037mmol,70%)。lcmsrt=2.14分鐘(方法a);esi-msm/z747.61[m+h]+;hrmsm/z747.5017[c39h66n6o8+h]+.
實施例18
(s)-n-((3r,4s,5s)-1-((s)-2-((1r,2r)-3-(((s)-1-氨基-1-氧代-3-苯基丙-2-基)氨基)-1-甲氧基-2-甲基-3-氧代丙基)吡咯烷-1-基)-3-甲氧基-5-甲基-1-氧代庚-4-基)-2-((s)-2-(二甲基氨基)-3-羥基丙醯氨基)-n,3-二甲基丁醯胺
向ch2cl2(10ml)中n,n-二甲基ser-val-dil-dap-phe-ohtfa鹽(12mg,0.016mmol)的攪拌室溫溶液中加入氯化銨(1.00mg,0.019mmol)、diea(3.21μl,0.018mmol)和edci(5.09mg,0.018mmol)。12小時後,通過lcms的分析顯示反應完全。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共10.0mg的標題化合物的tfa鹽(0.014mmol,83%)。lcmsrt=2.07分鐘(方法a);esi-msm/z733.63[m+h]+;hrmsm/z733.4866[c38h64n6o8+h]+.
實施例19
(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((r)-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-3-巰基-n-甲基丙醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯氨基)-3-苯基丙酸甲酯
向etoac(15ml)中fmoc-cys(trt)-oh(3.96g,6.76mmol)和h-dil-otbu鹽酸鹽(2.00g,6.76mmol)的攪拌室溫溶液中添加diea(2.17ml,12.2mmol)。溶液冷卻(0℃)並攪拌20分鐘。向反應混合物中添加另外的diea(2.17ml,12.2mmol)並且0℃溶液攪拌20分鐘。然後向反應混合物中添加cmpi(2.76g,10.8mmol)並且使反應混合物達到室溫。12小時後,通過lcms的分析顯示反應完全。用0.1mhcl(100mlx2),之後用鹽水(20mlx2)洗滌粗反應。有機餾分在硫酸鎂墊上乾燥、過濾並真空濃縮。使用己烷中18%至90%etoac作為洗脫液,通過矽膠(矽膠40μm,3.0x17.0cm)上的快速色譜來分離fmoc-cys(trt)-dil-otbu。獲得總共4.73g的fmoc-cys(trt)-dil-otbu(5.72mmol,85%產率)。
向mecn(10ml)中fmoc-cys(trt)-dil-otbu(2.61g,3.16mmol)的攪拌室溫溶液中添加哌啶(5ml)。5小時後,通過lcms的分析顯示反應完全。用己烷萃取粗反應混合物並且mecn層經真空濃縮以產生不需要進一步純化使用的粗h-cys(trt)-dil-otbu。
向dmf(15ml)中粗h-cys(trt)-dil-otbu和dov(0.916g,6.31mmol)的攪拌室溫懸液中添加diea(1.69ml,9.47mmol),之後添加hatu(2.40g,6.31mmol)。8小時後,通過lcms的分析顯示反應完全。粗反應混合物用飽和碳酸氫鈉(10ml)稀釋,並用etoac(40mlx2)萃取。合併的有機餾分用鹽水洗滌、在硫酸鎂墊上乾燥、過濾並真空濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共1.40gdov-cys(trt)-dil-otbu的tfa鹽(1.66mmol,52%)。
向ch2cl2(10ml)中dov-cys(trt)-dil-otbutfa鹽(1.40g,1.66mmol)的室溫溶液中添加tfa(5ml)。10小時後,通過lcms的分析顯示反應完全。揮發性有機物真空蒸發以產生不需要進一步純化使用的粗dov-cys(trt)-dil-ohtfa鹽。
向dmf(10ml)中dov-cys(trt)-dil-ohtfa鹽(0.225g,285mmol)和h-dap-phe-ometfa鹽(0.139mmol,0.301mmol)的攪拌室溫懸液中添加diea(0.237ml,1.33mmol),之後添加hobt(0.102g,0.666mmol)和hatu(0.253g,0.666mmol)。過夜攪拌後,通過lcms的分析顯示反應完全。粗反應混合物用飽和碳酸氫鈉(10ml)稀釋,並用etoac(50mlx3)萃取。合併的有機餾分用鹽水洗滌、在硫酸鎂墊上乾燥、過濾並真空濃縮,並且使用不需要進一步純化。
向dov-cys(trt)-dil-dap-phe-ometfa鹽(0.568g,0.507mmol)的室溫溶液中添加tfa(10ml)。60℃下12小時後,通過lcms的分析顯示反應完全。揮發性有機物真空蒸發。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共10.0mg的標題化合物的二硫橋二聚體tfa鹽(0.011mmol,3%)。lcmsrt=2.50分鐘(方法a);esi-msm/z764.60[m+h]+;hrmsm/z763.4547z=2.
實施例20
(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((r)-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-3-巰基-n-甲基丙醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯氨基)-3-苯基丙酸
向dcm(20ml)中boc-dap-oh二環己基胺鹽(6.47g,13.8mmol)和h-phe-otbuhcl鹽(3.91g,15.2mmol)的攪拌室溫溶液中添加diea(8.78ml,55.2mmol),之後添加depc(3.12ml,20.7mmol)。8小時後,通過lcms的分析顯示反應完全。揮發性有機物經真空蒸發以得到不需要進一步純化使用的粗產物。
向ch2cl2(10ml)中boc-dap-phe-otbu(5.25g,10.7mmol)的攪拌室溫溶液添加tfa(10ml)。12小時後,通過lcms分析顯示反應完全,其是游離苯丙氨酸羧酸和tbu酯的混合物。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得2.85g的h-dap-phe-otbutfa鹽的琥珀色油狀物(5.65mmol)並且獲得總共2.01g的h-dap-phe-ohtfa鹽的黃色油狀物(4.49mmol)。
向dmf(10ml)中粗dov-cys(trt)-dil-ohtfa鹽(0.208g)和h-dap-phe-ometfa鹽(0.144g,0.369mmol)的攪拌室溫懸液中添加diea(0.219ml,1.23mmol),之後添加hatu(0.234g,0.615mmol)。10小時後,通過lcms的分析顯示反應完全。粗反應混合物用飽和碳酸氫鈉(10ml)稀釋,並用etoac(40mlx2)萃取。合併的有機餾分用鹽水洗滌、在硫酸鎂墊上乾燥、過濾並真空濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共0.509g的富集dov-cys(trt)-dil-dap-phe-otbu的tfa鹽。
向富集dov-cys(trt)-dil-dap-phe-otbutfa鹽(0.509)的室溫溶液中添加tfa(5ml)。溶液加熱至60℃並攪拌24小時。24小時後,通過lcms的分析顯示反應完全。揮發性有機物真空蒸發。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共56.0mg的標題化合物的tfa鹽(0.065mmol,25%)。lcmsrt=2.32分鐘(方法a);esi-msm/z750.60[m+h]+;hrmsm/z750.4460[c38h63n5o8s+h]+.
實施例21
(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-3-羥基-n-甲基丙醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯氨基)-3-苯基丙酸
向dmf(10ml)中粗dov-ser(bzl)-dil-ohtfa鹽(0.232g)和h-dap-phe-otbutfa鹽(0.196g,0.389mmol)的攪拌室溫懸液中添加diea(0.326ml,1.83mmol),之後添加hatu(0.348,0.914mmol)。6小時後,通過lcms的分析顯示反應完全。粗反應混合物用飽和碳酸氫鈉(10ml)稀釋,並用etoac(40mlx2)萃取。合併的有機餾分用鹽水洗滌、在硫酸鎂墊上乾燥、過濾並真空濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共0.378gdov-ser(bzl)-dil-dap-phe-otbu的tfa鹽(0.380mmol,98%)。
向ch2cl2(5ml)中dov-ser(bzl)-dil-dap-phe-otbutfa鹽(0.455g,0.517mmol)的室溫溶液中添加tfa(2ml)。12小時後,通過lcms的分析顯示反應完全。揮發性有機物真空蒸發以產生不需要進一步純化使用的粗dov-ser(bzl)-dil-dap-phe-ohtfa鹽。
meoh(10ml)中粗dov-ser(bzl)-dil-dap-phe-ohtfa鹽和活性炭載鈀(10%pd基,10.0mg)的攪拌室溫懸液經氫化。12小時後,通過lcms的分析顯示反應完全。粗反應混合物在硅藻土墊上過濾並且濾液經濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共0.115g的標題化合物的tfa鹽(0.136mmol,28%)。lcmsrt=2.10分鐘(方法a);esi-msm/z734.61[m+h]+;hrmsm/z734.4708[c38h63n5o9+h]+.
實施例22
(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((2s,3r)-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-3-羥基-n-甲基丁醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯氨基)-3-苯基丙酸
向dmf(10ml)中粗dov-thr(bzl)-dil-ohtfa鹽(0.180g)和h-dap-phe-otbutfa鹽(0.148g,0.294mmol)的攪拌室溫懸液中添加diea(0.246ml,1.38mmol),之後添加hatu(0.262,0.690mmol)。6小時後,通過lcms的分析顯示反應完全。粗反應混合物用飽和碳酸氫鈉(10ml)稀釋,並用etoac(40mlx2)萃取。合併的有機餾分用鹽水洗滌、在硫酸鎂墊上乾燥、過濾並真空濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共0.298gdov-thr(bzl)-dil-dap-phe-otbu的tfa鹽(0.296mmol,78%)。
向ch2cl2(5ml)中dov-thr(bzl)-dil-dap-phe-otbutfa鹽(0.298g,0.296mmol)的室溫溶液中添加tfa(2ml)。10小時後,通過lcms的分析顯示反應完全。揮發性有機物真空蒸發以產生不需要進一步純化使用的粗dov-thr(bzl)-dil-dap-phe-ohtfa鹽。
meoh(10ml)中粗dov-thr(bzl)-dil-dap-phe-ohtfa鹽和活性炭載鈀(10%pd基,10.0mg)的攪拌室溫懸液經氫化。12小時後,通過lcms的分析顯示反應完全。粗反應混合物在硅藻土墊上過濾並且濾液經濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共0.120g的標題化合物的tfa鹽(0.139mmol,47%)。lcmsrt=2.22分鐘(方法a);esi-msm/z748.62[m+h]+;hrmsm/z748.4842[c39h65n5o9+h]+.
實施例23
(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-2-((s)-2-(二甲基氨基)-3-羥基丙醯氨基)-n,3-二甲基丁醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯氨基)-3-苯基丙酸甲酯
meoh(10ml)中n,n-二甲基ser(bzl)-val-dil-dap-phe-ometfa鹽(50.0mg,0.053mmol)和活性炭載鈀(10%pd基,10mg)的攪拌室溫懸液經氫化。10小時後,通過lcms的分析顯示反應完全。粗反應混合物在硅藻土墊上過濾並且濾液經濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共8.00mg的標題化合物的tfa鹽(0.009mmol,18%)。lcmsrt=2.38分鐘(方法a);esi-msm/z748.57[m+h]+;hrmsm/z748.4849[c39h65n5o9+h]+.
實施例24
(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-2-((2s,3r)-2-(二甲基氨基)-3-羥基丁醯氨基)-n,3-二甲基丁醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯氨基)-3-苯基丙酸甲酯
使用與通用合成方案和實施例中所述的那些方法類似的方法製備標題化合物。
實施例25
(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((2s,3s)-3-氨基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丁醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯氨基)-3-苯基丙酸甲酯
向thf(0.10ml)中dov-abu(3-n3)-dil-dap-phe-ometfa鹽(10mg,0.011mmol)的攪拌室溫溶液中添加thf中三甲基膦(1m,0.022ml,0.022mmol)。4小時後,通過lcms的分析顯示反應完全並且向反應混合物中添加h2o(0.05ml)。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗反應混合物。獲得總共6.00mg的標題化合物的tfa鹽(0.007mmol,62%)。lcmsrt=2.12分鐘(方法a);esi-msm/z761.63[m+h]+;hrmsm/z761.5159[c40h68n6o8+h]+.
實施例26
(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((2s,3s)-3-氨基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丁醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯氨基)-3-苯基丙酸
向thf(0.10ml)中dov-abu(3-n3)-dil-dap-phe-ohtfa鹽(10mg,0.011mmol)的攪拌室溫溶液中添加thf中三甲基膦(1m,0.022ml,0.022mmol)。4小時後,通過lcms的分析顯示反應完全並且向反應混合物中添加h2o(0.05ml)。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗反應混合物。獲得總共2.00mg的標題化合物的tfa鹽(0.002mmol,21%)。lcmsrt=2.02分鐘(方法a);esi-msm/z747.65[m+h]+;hrmsm/z747.5008[c39h66n6o8+h]+.
實施例27
(2s,3s)-3-疊氮基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-((3r,4s,5s)-3-甲氧基-1-((s)-2-((1r,2r)-1-甲氧基-2-甲基-3-氧代-3-(苯乙基氨基)丙基)吡咯烷-1-基)-5-甲基-1-氧代庚-4-基)-n-甲基丁醯胺
向ch2cl2(20ml)中boc-dap-oh二環己基胺鹽(6.47g,13.8mmol)和苯乙胺(3.914g,15.19mmol)的攪拌25℃溶液中添加diea(8.76ml,55.2mmol),之後添加depc(3.12ml,20.7mmol)。8小時後,通過lcms的分析顯示反應完全。揮發性有機物經真空蒸發以得到不需要進一步純化使用的粗產物。獲得總共4.04g的boc-dap-苯乙胺(10.3mmol)。lcmsrt=3.00分鐘(方法a);esi-msm/z391.37[m+h]+.
向ch2cl2(15.0ml)中boc-dap-苯乙胺(4.04g,10.3mmol)的攪拌25℃溶液添加tfa(15.0ml)。14小時後,通過lcms的分析顯示反應完全。揮發性有機物經真空蒸發並且通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共2.51g的h-dap-苯乙胺的tfa鹽(6.21mmol)。lcmsrt=1.72分鐘(方法a);esi-msm/z291.29[m+h]+.
向dmf(10ml)中dov-abu(3-n3)-dil-ohtfa鹽(0.300g,0.526mmol)和h-dap-苯乙胺tfa鹽(0.191g,0.471mmol)的攪拌室溫溶液中添加diea(0.343ml,1.97mmol),之後添加hatu(0.501g,1.31mmol)。10小時後,通過lcms的分析顯示反應完全。粗反應用飽和碳酸氫鈉(10ml)稀釋,並用etoac(20mlx2)萃取。合併的有機餾分用鹽水洗滌、用硫酸鎂乾燥、過濾並真空濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共196mg的標題化合物的tfa鹽(0.233mmol,49%)。lcmsrt=2.45分鐘(方法a);esi-msm/z729.55[m+h]+;hrmsm/z729.5030[c38h64n8o6+h]+.
實施例28
(2s,3s)-3-疊氮基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-((3r,4s,5s)-1-((s)-2-((1r,2r)-3-(((1s,2r)-1-羥基-1-苯基丙-2-基)氨基)-1-甲氧基-2-甲基-3-氧代丙基)吡咯烷-1-基)-3-甲氧基-5-甲基-1-氧代庚-4-基)-n-甲基丁醯胺
向ch2cl2(20ml)中boc-dap-oh二環己基胺鹽(10.0g,0.021mol)和(1r,2s)-(-)-降麻黃鹼(3.87g,0.026mol)的攪拌室溫溶液中添加diea(11.4ml,0.064mol)和depc(6.44ml,0.043mol)。14小時後,通過lcms的分析顯示反應完全。向粗反應混合物中添加0.1mhcl(20.0ml)。有機層經分離、在硫酸鎂墊上乾燥、過濾並真空濃縮以產生粗產物。獲得總共7.92g的boc-dap-(1r,2s)-(-)-降麻黃鹼(18.8mmol,88%)。lcmsrt=2.25分鐘(方法a);esi-msm/z421.31[m+h]+.
向ch2cl2(10ml)中boc-dap-(1r,2s)-(-)-降麻黃鹼(7.92g,18.8mmol)的攪拌室溫溶液添加tfa(10ml)。10小時後,通過lcms的分析顯示反應完全。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。製備總共5.00g的h-dap-(1r,2s)-(-)-降麻黃鹼的tfa鹽(11.5mmol,61%)。lcmsrt=1.10分鐘(方法a);esi-msm/z321.33[m+h]+.
向dmf(5ml)中dov-abu(3-n3)-dil-ohtfa鹽(0.300g,0.526mmol)和h-dap-(1r,2s)-(-)-降麻黃鹼tfa鹽(0.211g,0.486mmol)的攪拌室溫溶液中添加diea(0.351ml,1.97mmol),之後添加hatu(0.501g,1.31mmol)。10小時後,通過lcms的分析顯示反應完全。粗反應用飽和碳酸氫鈉(10ml)稀釋,並用etoac(20mlx2)萃取。合併的有機餾分用鹽水洗滌、用硫酸鎂乾燥、過濾並真空濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共128mg的標題化合物的tfa鹽(0.147mmol,30%)。lcmsrt=1.95分鐘(方法a);esi-msm/z759.65[m+h]+;hrmsm/z759.5121[c39h66n8o7+h]+.
實施例29
(2s,3s)-3-疊氮基-n-((3r,4s,5s)-1-((s)-2-((1r,2r)-3-((4-氯苯乙基)氨基)-1-甲氧基-2-甲基-3-氧代丙基)吡咯烷-1-基)-3-甲氧基-5-甲基-1-氧代庚-4-基)-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丁醯胺
向ch2cl2(20ml)中boc-dap-oh二環己基胺鹽(5.00g,10.7mmol)和2-(4-氯苯基)乙基胺(1.85g,11.7mmol)的攪拌室溫溶液中添加diea(6.78ml,42.7mmol)和depc(2.41ml,16.0mmol)。10小時後,通過lcms的分析顯示反應完全。揮發性有機物經真空蒸發以得到不需要進一步純化使用的粗產物。獲得總共4.25g的boc-dap-2-(4-氯苯基)乙基胺(10.0mmol,94%)。lcmsrt=3.10分鐘(方法a);esi-msm/z425.32[m+h]+.
向ch2cl2(15ml)中boc-dap-2-(4-氯苯基)乙基胺(4.25g,10.0mmol)的攪拌室溫溶液添加tfa(15ml)。10小時後,通過lcms的分析顯示反應完全。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。製備總共2.27g的h-dap-2-(4-氯苯基)乙基胺的tfa鹽(5.18mmol,52%)。lcmsrt=2.05分鐘(方法a);esi-msm/z325.24[m+h]+.
向dmf(10ml)中dov-abu(3-n3)-dil-ohtfa鹽(0.526g,0.923mmol)和h-dap-2-(4-氯苯基)乙基胺tfa鹽(0.347g,0.792mmol)的攪拌室溫溶液中添加diea(0.602ml,3.46mmol),之後添加hatu(0.878g,2.30mmol)。10小時後,通過lcms的分析顯示反應完全。粗反應用飽和碳酸氫鈉(10ml)稀釋,並用etoac(20mlx2)萃取。合併的有機餾分用鹽水洗滌、用硫酸鎂乾燥、過濾並真空濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共596mg的標題化合物的tfa鹽(0.680mmol,85%)。lcmsrt=2.38分鐘(方法a);esi-msm/z763.71[m+h]+;hrmsm/z763.4633[c38h63n8o6cl+h]+.
實施例30
(2s,3s)-3-疊氮基-n-((3r,4s,5s)-1-((s)-2-((1r,2r)-3-((2-氯苯乙基)氨基)-1-甲氧基-2-甲基-3-氧代丙基)吡咯烷-1-基)-3-甲氧基-5-甲基-1-氧代庚-4-基)-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丁醯胺
向ch2cl2(10ml)中boc-dap-oh二環己基胺鹽(5.00g,10.7mmol)和2-(2-氯苯基)乙基胺(1.85g,11.7mmol)的攪拌室溫溶液中添加diea(4.76ml,26.7mmol)和depc(2.41ml,16.0mmol)。10小時後,通過lcms的分析顯示反應完全。揮發性有機物經真空蒸發以得到不需要進一步純化使用的粗產物。獲得總共3.98g的boc-dap-2-(2-氯苯基)乙基胺(9.37mmol,88%)。lcmsrt=3.04分鐘(方法a);esi-msm/z425.23[m+h]+.
向ch2cl2(5ml)中boc-dap-2-(2-氯苯基)乙基胺(3.98g,9.37mmol)的攪拌室溫溶液添加tfa(5ml)。10小時後,通過lcms的分析顯示反應完全。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。製備總共2.87g的h-dap-2-(2-氯苯基)乙基胺的tfa鹽(6.55mmol,70%)。lcmsrt=1.83分鐘(方法a);esi-msm/z325.22[m+h]+.
向dmf(10ml)中dov-abu(3-n3)-dil-ohtfa鹽(0.450g,0.789mmol)和h-dap-2-(2-氯苯基)乙基胺tfa鹽(0.320g,0.731mmol)的攪拌室溫溶液中添加diea(0.515ml,2.96mmol),之後添加hatu(0.751g,1.97mmol)。10小時後,通過lcms的分析顯示反應完全。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗反應混合物。獲得總共253mg的標題化合物的tfa鹽(0.289mmol,32%,基於rsm)。lcmsrt=1.26分鐘(方法b);esi-msm/z763.60[m+h]+;hrmsm/z763.4632[c38h63n8o6cl+h]+.
實施例31
(2s,3s)-3-氨基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-((3r,4s,5s)-3-甲氧基-1-((s)-2-((1r,2r)-1-甲氧基-2-甲基-3-氧代-3-(苯乙基氧基)丙基)吡咯烷-1-基)-5-甲基-1-氧代庚-4-基)-n-甲基丁醯胺
向thf(0.5ml)中dov-abu(3-n3)-dil-dap-petfa鹽(25mg,0.030mmol)的攪拌室溫溶液中添加thf中三甲基膦(1m,0.045ml,0.045mmol)。1小時後,通過lcms的分析顯示反應完全。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.1%水性甲酸中5%至95%mecn作為洗脫液的製備型rp-hplc純化粗反應混合物。獲得總共9.0mg的標題化合物的甲酸鹽(0.012mmol,41%)。lcmsrt=1.02分鐘(方法b);esi-msm/z703.71[m+h]+;hrmsm/z703.5117[c38h66n6o6+h]+.
實施例32
(2s,3s)-3-氨基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-((3r,4s,5s)-1-((s)-2-((1r,2r)-3-(((1s,2r)-1-羥基-1-苯基丙-2-基)氨基)-1-甲氧基-2-甲基-3-氧代丙基)吡咯烷-1-基)-3-甲氧基-5-甲基-1-氧代庚-4-基)-n-甲基丁醯胺
向thf(0.3ml)中dov-abu(3-n3)-dil-dap-降麻黃鹼tfa鹽(27mg,0.031mmol)的攪拌室溫溶液中添加thf中三甲基膦(1m,0.046ml,0.046mmol)。2小時後,通過lcms的分析顯示反應完全。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性三氟乙酸中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗反應混合物。獲得總共6.8mg的標題化合物的tfa鹽(0.008mmol,26%)。lcmsrt=1.95分鐘(方法b);esi-msm/z733.72[m+h]+;hrmsm/z733.5227[c39h68n6o7+h]+.
實施例33
(2s,3s)-3-氨基-n-((3r,4s,5s)-1-((s)-2-((1r,2r)-3-((4-氯苯乙基)氨基)-1-甲氧基-2-甲基-3-氧代丙基)吡咯烷-1-基)-3-甲氧基-5-甲基-1-氧代庚-4-基)-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丁醯胺
向thf(0.3ml)中dov-abu(3-n3)-dil-dap-2-(4-氯苯基)乙基胺tfa鹽(117mg,0.133mmol)的攪拌室溫溶液中添加thf中三甲基膦(1m,0.2ml,0.2mmol)。2小時後,通過lcms的分析顯示反應完全。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.1%水性甲酸中5%至95%mecn作為洗脫液的製備型rp-hplc純化粗反應混合物。獲得總共9.0mg的標題化合物的甲酸鹽(0.011mmol,9%)。lcmsrt=0.97分鐘(方法b);esi-msm/z737.51[m+h]+;hrmsm/z737.4731[c38h65n6o6cl+h]+.
實施例34
(2s,3s)-3-氨基-n-((3r,4s,5s)-1-((s)-2-((1r,2r)-3-((2-氯苯乙基)氨基)-1-甲氧基-2-甲基-3-氧代丙基)吡咯烷-1-基)-3-甲氧基-5-甲基-1-氧代庚-4-基)-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丁醯胺
向thf(1.0ml)中dov-abu(3-n3)-dil-dap-2-(2-氯苯基)乙基胺甲酸鹽(46mg,0.057mmol)的攪拌室溫溶液中添加thf中三甲基膦(1m,0.085ml,0.085mmol)。1小時後,通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.1%水性甲酸中5%至95%mecn作為洗脫液的製備型rp-hplc純化粗反應混合物。獲得總共13.6mg的標題化合物的甲酸鹽(0.017mmol,30%)。lcmsrt=1.03分鐘(方法b);esi-msm/z737.57[m+h]+;hrmsm/z737.4731[c38h65n6o6cl+h]+.
實施例35
(s)-4-氨基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-((3r,4s,5s)-3-甲氧基-1-((s)-2-((1r,2r)-1-甲氧基-2-甲基-3-氧代-3-(苯乙基氨基)丙基)吡咯烷-1-基)-5-甲基-1-氧代庚-4-基)-n-甲基丁醯胺
向dmf(15ml)中dov-dab(fmoc)-dil-ohtfa鹽(0.450g,0.587mmol)和h-dap-苯乙胺tfa鹽(0.200g,0.495mmol)的攪拌室溫溶液中添加diea(0.360ml,2.07mmol),之後添加hatu(0.526g,1.38mmol)。10小時後,通過lcms的分析顯示反應完全。粗反應混合物用飽和碳酸氫鈉(10ml)稀釋,並用etoac(20mlx2)萃取。合併的有機餾分用鹽水洗滌、用硫酸鎂乾燥、過濾並真空濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.1%水性甲酸中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共276mg的富集dov-dab(fmoc)-dil-dap-苯乙胺的甲酸鹽(0.266mmol,54%)。lcmsrt=1.37分鐘(方法b);esi-msm/z925.48[m+h]+.
向乙腈(10ml)中dov-dpr(fmoc)-dil-dap-苯乙胺(0.276g,0.266mmol)的攪拌室溫溶液中添加哌啶(5ml)。10小時後,通過lcms的分析顯示反應完全。向粗反應混合物中添加己烷。乙腈層經真空濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.1%水性甲酸中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共98.0mg的標題化合物的甲酸鹽(0.120mmol,45%)。lcmsrt=1.02分鐘(方法b);esi-msm/z703.78[m+h]+;hrmsm/z703.5117[c38h66n6o6+h]+.
實施例36
(s)-4-氨基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-((3r,4s,5s)-1-((s)-2-((1r,2r)-3-(((1s,2r)-1-羥基-1-苯基丙-2-基)氨基)-1-甲氧基-2-甲基-3-氧代丙基)吡咯烷-1-基)-3-甲氧基-5-甲基-1-氧代庚-4-基)-n-甲基丁醯胺
向dmf(15ml)中dov-dab(fmoc)-dil-ohtfa鹽(0.459g,0.599mmol)和h-dap-(1r,2s)-(-)-降麻黃鹼tfa鹽(0.225g,0.518mmol)的攪拌室溫溶液中添加diea(0.376ml,2.11mmol),之後添加hatu(0.536g,1.41mmol)。10小時後,通過lcms的分析顯示反應完全。粗反應混合物用飽和碳酸氫鈉(10ml)稀釋,並用etoac(20mlx2)萃取。合併的有機餾分用鹽水洗滌、用硫酸鎂乾燥、過濾並真空濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.1%水性甲酸中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共449mg的富集dov-dab(fmoc)-dil-dap-(1r,2s)-(-)-降麻黃鹼的甲酸鹽(0.420mmol,81%)。lcmsrt=1.35分鐘(方法b);esi-msm/z955.74[m+h]+.
向乙腈(10ml)中dov-dab(fmoc)-dil-dap-(1r,2s)-(-)-降麻黃鹼甲酸鹽(0.449g,0.420mmol)的攪拌室溫溶液中添加哌啶(5ml)。10小時後,通過lcms的分析顯示反應完全。向粗反應混合物中添加己烷。乙腈層經真空濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.1%水性甲酸中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共53.0mg的標題化合物的甲酸鹽(0.068mmol,14%)。lcmsrt=0.79分鐘(方法b);esi-msm/z733.71[m+h]+;hrmsm/z733.5227[c39h68n6o7+h]+.
實施例37
(s)-4-氨基-n-((3r,4s,5s)-1-((s)-2-((1r,2r)-3-((4-氯苯乙基)氨基)-1-甲氧基-2-甲基-3-氧代丙基)吡咯烷-1-基)-3-甲氧基-5-甲基-1-氧代庚-4-基)-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丁醯胺
向dmf(10ml)中dov-dab(fmoc)-dil-ohtfa鹽(0.255g,0.333mmol)和h-dap-2-(4-氯苯基)乙基胺tfa鹽(0.127g,0.290mmol)的攪拌室溫溶液中添加diea(0.204ml,1.17mmol),之後添加hatu(0.298g,0.781mmol)。10小時後,通過lcms的分析顯示反應完全。粗反應混合物用飽和碳酸氫鈉(10ml)稀釋,並用etoac(20mlx2)萃取。合併的有機餾分用鹽水洗滌、用硫酸鎂乾燥、過濾並真空濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.1%水性甲酸中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共190mg的dov-dab(fmoc)-dil-dap-2-(4-氯苯基)乙基胺的甲酸鹽(0.177mmol,61%)。lcmsrt=1.49分鐘(方法b);esi-msm/z959.62[m+h]+.
向乙腈(5ml)中dov-dab(fmoc)-dil-dap-2-(4-氯苯基)乙基胺甲酸鹽(0.190g,0.177mmol)的攪拌室溫溶液中添加哌啶(5ml)。10小時後,通過lcms的分析顯示反應完全。向粗反應混合物中添加己烷。乙腈層經真空濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.1%水性甲酸中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共118mg的標題化合物的甲酸鹽(0.151mmol,85%)。lcmsrt=1.06分鐘(方法b);esi-msm/z737.55[m+h]+;hrmsm/z737.4729[c38h65n6o6cl+h]+.
實施例38
(s)-4-氨基-n-((3r,4s,5s)-1-((s)-2-((1r,2r)-3-((2-氯苯乙基)氨基)-1-甲氧基-2-甲基-3-氧代丙基)吡咯烷-1-基)-3-甲氧基-5-甲基-1-氧代庚-4-基)-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丁醯胺
向dmf(5ml)中dov-dab(fmoc)-dil-ohtfa鹽(0.306g,0.399mmol)和h-dap-2-(2-氯苯基)乙基胺tfa鹽(0.170g,0.388mmol)的攪拌室溫溶液中添加diea(0.300g,400μl,2.29mmol),之後添加hatu(360mg,0.944mmol)。10小時後,通過lcms的分析顯示反應完全。粗反應用飽和碳酸氫鈉(10ml)稀釋,並用etoac(10mlx3)萃取。合併的有機餾分用鹽水洗滌、在硫酸鎂墊上乾燥、過濾並真空濃縮。通過用phenomenexgemini10μmax-rp柱(150x30mm)的,使用0.1%水性nh4oh中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共115mg的dov-dab(fmoc)-dil-dap-2-(2-氯苯基)乙基胺的白色固體(0.120mmol,26%)。lcmsrt=1.40分鐘(方法b);esi-msm/z959.75[m+h]+.
向乙腈(10ml)中dov-dab(fmoc)-dil-dap-2-(2-氯苯基)乙基胺(0.115g,0.120mmol)的攪拌室溫溶液中添加哌啶(2ml)。3小時後,通過lcms的分析顯示反應完全。向粗反應混合物中添加己烷。乙腈層經真空濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.1%水性nh4oh中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共30.0mg的標題化合物的白色固體(0.041mmol,34%)。lcmsrt=1.15分鐘(方法b);esi-msm/z737.68[m+h]+;hrmsm/z737.4729[c38h65n6o6cl+h]+.
實施例39
((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基戊-4-炔醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯基)-l-苯丙氨酸甲酯
向etoac(10ml)中boc-炔丙基gly-oh(1.00g,4.69mmol)和h-dil-otbu鹽酸鹽(1.15g,3.90mmol)的攪拌25℃溶液中添加diea(1.49ml,9.38mmol)。溶液冷卻至(0℃)並且攪拌20分鐘,並且添加額外部分的diea(1.49ml,9.38mmol)並且反應混合物在0℃下攪拌20分鐘。然後向反應混合物中添加cmpi(1.80g,7.04mmol),其升溫至室溫並且攪拌12小時。用0.1mhcl(20mlx2),之後用鹽水(20mlx2)洗滌粗反應混合物。有機餾分在無水硫酸鎂上乾燥,過濾,並真空濃縮以得到粗產物。獲得總共2.05g的boc-炔丙基gly-dil-otbu(4.50mmol,96%)。lcmsrt=3.46分鐘(方法a);esi-msm/z455.42[m+h]+.
向ch2cl2(6ml)中boc-炔丙基gly-dil-otbu(2.05g,4.50mmol)的攪拌25℃溶液添加tfa(6ml)。14小時後,通過lcms的分析顯示反應完全。揮發性有機物經真空濃縮以得到不需要進一步純化使用的粗產物。獲得總共1.30gh-炔丙基gly-dil-oh的tfa鹽(3.16mmol,70%)。
向dmf(10ml)中dov(1.27g,8.71mmol)的攪拌25℃溶液中添加diea(2.33ml,13.1mmol),之後添加hatu(3.32g,8.71mmol)。10分鐘後,向反應中添加dmf中h-炔丙基gly-dil-ohtfa鹽(1.30g,3.16mmol)的溶液。8小時後,通過lcms的分析顯示反應完全。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共455mg的dov-炔丙基gly-dil-oh的tfa鹽(0.844mmol,27%產率)。lcmsrt=1.65分鐘(方法a);esi-msm/z425.95[m+h]+.
向dmf(15ml)中dov-炔丙基gly-dil-ohtfa鹽(0.198g,0.367mmol)和h-dap-phe-ometfa鹽(0.156g,0.338)的攪拌室溫溶液中添加diea(0.222ml,1.40mmol),之後添加hatu(0.355g,0.931mmol)。10小時後,通過lcms的分析顯示反應完全。粗反應用飽和碳酸氫鈉(10ml)稀釋,並用etoac(20mlx2)萃取。合併的有機餾分用鹽水洗滌、用硫酸鎂乾燥、過濾並真空濃縮。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共10.0mg的標題化合物的tfa鹽(0.012mmol,3%)。lcmsrt=2.50分鐘(方法a);esi-msm/z756.44[m+h]+;hrmsm/z756.4902[c41h65n5o8+h]+.
實施例40
(2s,3s)-n-((3r,4s,5s)-1-((s)-2-((1r,2r)-3-(((s)-1-氨基-1-氧代-3-苯基丙-2-基)氨基)-1-甲氧基-2-甲基-3-氧代丙基)吡咯烷-1-基)-3-甲氧基-5-甲基-1-氧代庚-4-基)-3-疊氮基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丁醯胺
向dmf(0.2ml)中dov-abu(3-n3)-dil-dap-phe-oh甲酸鹽(42.1mg,0.051mmol)、氯化銨(7.9mg,0.148mmol)、tbtu(52.5mg,0.163mmol)的攪拌室溫溶液中添加胡尼鹼(0.045ml,0.258mmol)。16小時後,通過lcms的分析顯示反應完全。通過用phenomenexgemini-nx10μc-18柱(150x30mm)的使用0.1%水性氫氧化銨中5%至95%mecn作為洗脫液的製備型rp-hplc純化粗反應混合物。獲得總共13.4mg的標題化合物(0.017mmol,33%)。lcmsrt=1.05分鐘(方法b);esi-msm/z772.61[m+h]+;hrmsm/z772.5078[c39h65n9o7+h]+.
實施例41
(2s,3s)-3-疊氮基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-((3r,4s,5s)-3-甲氧基-1-((s)-2-((1r,2r)-1-甲氧基-2-甲基-3-氧代-3-((2-(吡啶-2-基)乙基)氨基)丙基)吡咯烷-1-基)-5-甲基-1-氧代庚-4-基)-n-甲基丁醯胺
向dmf(10ml)中dov-abu(3-n3)-dil-ohtfa鹽(0.300g,0.526mmol)和h-dap-2-(2-吡啶基)乙基胺tfa鹽(0.287g,0.709mmol)的攪拌23℃溶液中添加diea(343μl,1.97mmol),之後添加hatu(0.501g,1.31mmol)。10小時後,通過lcms的分析顯示反應完全。粗反應用飽和碳酸氫鈉(10ml)稀釋,並用etoac(20mlx2)萃取。合併的有機餾分用鹽水洗滌、在硫酸鎂墊上乾燥、過濾並真空濃縮。通過用phenomenexgemini-nx10μc-18柱(150x30mm)的,使用0.1%水性nh4oh中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共139mg的標題化合物(0.190mmol,29%)。lcmsrt=0.916分鐘(方法b);esi-msm/z730.64[m+h]+;hrmsm/z730.4985[c37h63n9o6+h]+.
實施例42
(2s,3s)-3-疊氮基-n-((3r,4s,5s)-1-((s)-2-((1r,2r)-3-(((s)-1-(叔丁基氨基)-1-氧代-3-苯基丙-2-基)氨基)-1-甲氧基-2-甲基-3-氧代丙基)吡咯烷-1-基)-3-甲氧基-5-甲基-1-氧代庚-4-基)-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丁醯胺
向dmf(0.2ml)中dov-abu(3-n3)-dil-dap-phe-oh甲酸鹽(24.0mg,0.029mmol)、叔丁基胺鹽酸鹽(7.9mg,0.072mmol)、hatu(24.5mg,0.064mmol)的攪拌室溫溶液中添加胡尼鹼(0.022ml,0.124mmol)。18小時後,通過lcms的分析顯示反應完全。通過用phenomenexgemini-nx10μc-18柱(150x30mm)的,使用0.1%水性氫氧化銨中5%至95%mecn作為洗脫液的製備型rp-hplc純化粗反應混合物。獲得總共15.4mg的標題化合物(0.017mmol,59%)。lcmsrt=1.27分鐘(方法b);esi-msm/z828.8[m+h]+;hrmsm/z828.5671[c39h66n6o8+h]+.
實施例43
((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((2s,3s)-3-疊氮基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丁醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯基)-l-纈氨酸甲酯
向ch2cl2(20ml)中boc-dap-oh二環己基胺鹽(4.00g,8.54mmol)和h-val-omehcl鹽(1.80g,10.7mmol)的攪拌23℃懸液中添加diea(4.44g,6.00ml,34.4mmol),之後添加hatu(2.15g,2.00ml,0.013mol)。10小時後,通過lcms的分析顯示反應完全。揮發性有機物經真空蒸發以得到不需要進一步純化使用的粗產物。獲得總共6.80g的無色油狀物的boc-dap-val-ome(17.0mmol,80%)。lcmsrt=1.33分鐘(方法b);esi-msm/z401.6[m+h]+.
攪拌二噁烷(20ml)中4.0mhcl中boc-dap-val-ome(6.80g,17.0mmol)的23℃懸液。4小時後,通過lcms的分析顯示反應完全。揮發性有機物經真空蒸發以得到不需要進一步純化使用的粗產物。獲得總共4.57g的h-dap-val-ome的鹽酸鹽(13.6mmol,80%)。lcmsrt=0.726分鐘(方法b);esi-msm/z301.45[m+h]+.
向dmf(10ml)中dov-abu(3-n3)-dil-ohtfa鹽(0.144g,0.253mmol)和h-dap-val-omehcl鹽(0.332g,0.985mmol)的攪拌23℃懸液中添加diea(0.222g,0.300ml,1.72mmol),之後添加hatu(0.240g,0.631mmol)。10小時後,通過lcms的分析顯示反應完全。粗反應用飽和碳酸氫鈉(10ml)稀釋,並用etoac(20mlx3)萃取。合併的有機餾分用鹽水洗滌、在硫酸鎂墊上乾燥、過濾並真空濃縮。通過用phenomenexgemini-nx10μc-18柱(150x30mm)的,使用0.1%水性nh4oh中5%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共129mg的淡黃色固體的標題化合物(0.175mmol,55%)。lcmsrt=1.15分鐘(方法b);esi-msm/z739.75[m+h]+;hrmsm/z739.5074[c36h66n8o8+h]+.
實施例44
((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-6-氨基-2-((s)-2-(二甲基氨基)1-3-甲基丁醯氨基)-n-甲基己醯氨基1-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯基)-l-苯丙氨酸甲酯
向etoac(20ml)中boc-lys(fmoc)-oh(5.60g,12.0mmol)和h-dil-otbu鹽酸鹽(3.06g,10.9mmol)的攪拌23℃溶液中添加diea(4.44g,6.00ml,34.4mmol)。溶液冷卻至0℃並攪拌0.5小時。0.5小時後,向反應混合物中添加其他diea(4.44g,6.00ml,34.4mmol)並且0℃反應攪拌0.5小時。然後向反應混合物中添加cmpi(4.20g,16.4mmol),其緩慢升溫至室溫並且攪拌10小時。用1mhcl(30mlx2),之後用鹽水(25mlx2)洗滌粗反應。有機餾分在硫酸鎂墊上乾燥、過濾並真空濃縮。獲得總共7.38g的淡黃色固體的boc-lys(fmoc)-dil-otbu(10.4mmol,86%)。lcmsrt=1.85分鐘(方法b);esi-msm/z710.1[m+h]+.
攪拌二嗯烷(10.0ml)中4.0mhcl中boc-lys(fmoc)-dil-otbu(7.38g,10.4mmol)的23℃懸液。10小時後,通過lcms的分析顯示反應完全。揮發性有機物經真空蒸發以得到不需要進一步純化使用的粗產物。獲得總共7.05g的淡黃色的h-lys(fmoc)一dil-oh的hcl鹽(0.012mol,89%)。lcmsrt=1.20分鐘(方法b);esi-msm/z554.54[m+h]+.
向dmf(20ml)中dov-oh(2.50g,17.2mmol)的攪拌23。℃懸液中添加diea(4.44g,6.00ml,0.034mol),之後添加hatu(4.82g,12.6mmol)。5分鐘後,向反應混合物中添加h-lys(fmoc)-dil-ohhcl鹽(7.05g,0.012mol)。4小時後,通過lcms的分析顯示反應完全。粗反應混合物用飽和碳酸氫鈉(10ml)稀釋,並用etoac(20mlx2)萃取。合併的有機餾分用鹽水洗滌、在硫酸鎂墊上乾燥、過濾並真空濃縮。通過用phenomenexgemininx-c1810u柱(150x30mm)的,使用0.1%水性nh4oh中5%至95%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共4.45g的淡黃色固體的dov-lys(fmoc)-dil-oh(6.54mmol,78%)。lcmsrt=1.21分鐘(方法b);esi-msm/z681.68[m+h]+.
向dmf(10ml)中dov-lys(fmoc)-dil-oh(2.17g,3.19mmol)和h-dap-ometfa鹽(1.78g,3.85mmol)的攪拌23℃懸液中添加diea(1.65g,2.20ml,12.7mmol),之後添加hatu(1.94g,5.10mmol)。10小時後,通過lcms的分析顯示反應完全。粗反應用飽和碳酸氫鈉(10ml)稀釋,並用etoac(20mlx3)萃取。合併的有機餾分用鹽水洗滌、在硫酸鎂墊上乾燥、過濾並真空濃縮。通過用phenomenexgemini10μmax-rp柱(150x30mm)的,使用0.1%水性nh4oh中5%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共2.25g的淡黃色固體的dov-lys(fmoc)-dil-dap-phe-ome(2.23mmol,70%)。lcmsrt=1.29分鐘(方法b);esi-msm/z1011.77[m+h]+.
向乙腈(20ml)中dov-lys(fmoc)-dil-dap-phe-ome(2.25g,2.23mmol)的攪拌23℃懸液中添加哌啶(5ml)。2小時後,通過lcms的分析顯示反應完全。向粗反應溶液中添加己烷。乙腈層經真空濃縮。通過用phenomenexgemininx-c1810μ柱(150x30mm)的使用0.1%水性nh4oh中5%至95%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共898mg的白色固體的標題化合物(1.14mmol,51%)。lcmsrt=0.840分鐘(方法b);esi-msm/z789.5[m+h]+;hrmsm/z789.5482[c42h72n6o8+h]+.
實施例45
((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((2s,4s)-4-疊氮基-1-(二甲基-l-纈氨醯基)-n-甲基吡咯烷-2-甲醯胺基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯基)-l-苯丙氨酸甲酯
向etoac(20ml)中順式-fmoc-pro(4-n3)-oh(2.00g,5.27mmol)和h-dil-otbuhcl(1.49g,5.27mmol)的攪拌23℃懸液中添加diea(2.22g,3.0ml,17.2mmol)。溶液冷卻至0℃並攪拌0.5小時。向冷卻的反應混合物中添加額外的diea(2.22g,3.0ml,17.2mmol)並且0℃反應混合物攪拌0.5小時。然後向反應混合物中添加cmpi(2.03g,7.93mmol),其緩慢升溫至室溫並且攪拌10小時。用1mhcl(30mlx2),之後用鹽水(25mlx2)洗滌粗反應。有機餾分在硫酸鎂墊上乾燥、過濾並真空濃縮。該粗產物無需進一步純化即可使用。獲得總共3.13g的黃色油狀物的順式-fmoc-pro(4-n3)-dil-otbu(5.05mmol,76%)。lcmsrt=1.73分鐘(方法b);esi-msm/z621.46[m+h]+.
向乙腈(20ml)中順式-fmoc-pro(4-n3)-dil-otbu(3.13g,4.04mmol)的攪拌23℃溶液中添加哌啶(10ml)。10小時後,通過lcms的分析顯示反應完全。向粗反應混合物中添加己烷。乙腈層經真空濃縮,並且不需要進一步純化使用粗產物。獲得總共1.57g的澄清油的h-pro(4-n3)-dil-otbu(3.95mmol,88%)。lcmsrt=1.19分鐘(方法b);esi-msm/z398.50[m+h]+.
向dmf(10ml)中dov-oh(1.03g,7.12mmol)和h-pro(4-n3)-dil-otbu(1.57g,3.56mmol)的攪拌23℃懸液中添加diea(1.84g,2.50ml,0.014mol),之後添加hatu(2.03g,5.33mmol)。3小時後,通過lcms的分析顯示反應完全。粗反應用飽和碳酸氫鈉(10ml)稀釋,並用etoac(20mlx2)萃取。合併的有機餾分用鹽水洗滌、在硫酸鎂墊上乾燥、過濾並真空濃縮。通過用phenomenexgemininx-c1810μ柱(150x30mm)的,使用0.1%水性nh4oh中5%至95%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共817mg的白色固體的dov-pro(4-n3)-dil-otbu(1.56mmol,44%)。lcmsrt=1.21分鐘(方法b);esi-msm/z525.28[m+h]+.
攪拌3.0hcl中dov-pro(4-n3)-dil-otbu(0.817g,1.56mmol)的23℃懸液。10小時後,通過lcms的分析顯示反應完全。揮發性有機物經真空蒸發以得到不需要進一步純化使用的粗產物。獲得總共704mg的dov-pro(4-n3)-dil-oh的hcl鹽(1.39mmol,89%)。lcmsrt=0.676分鐘(方法b);esi-msm/z469.44[m+h]+.
向dmf(10ml)中dov-pro(4-n3)-dil-ohhcl鹽(0.120g,0.256mmol)和h-dap-phe-ometfa鹽(0.143g,0.310mmol)的攪拌23℃懸液中添加diea(0.132g,0.200ml,1.02mmol),之後添加hatu(0.156g,0.410mmol)。10小時後,通過lcms的分析顯示反應完全。粗反應用飽和碳酸氫鈉(10ml)稀釋,並用etoac(20mlx3)萃取。合併的有機餾分用鹽水洗滌、在硫酸鎂墊上乾燥、過濾並真空濃縮。通過用phenomenexgemininx-c1810μ柱(150x30mm)的,使用0.1%水性nh4oh中5%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共37.0mg的黃色固體的標題化合物(0.046mmol,18%)。lcmsrt=1.13分鐘(方法b);esi-msm/z799.43[m+h]+;hrmsm/z799.5064[c41h66n8o8+h]+.
實施例46
(s)-3-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-4-(((3r,4s,5s)-3-甲氧基-1-((s)-2-((1r,2r)-1-甲氧基-3-(((s)-1-甲氧基-1-氧代-3-苯基丙-2-基)氨基)-2-甲基-3-氧代丙基)吡咯烷-1-基)-5-甲基-1-氧代庚-4-基)(甲基)氨基-4-氧代丁酸
向etoac(20ml)中boc-asp(obzl)-oh(5.00g,15.5mmol)和h-dil-otbutfa鹽(4.36g,15.5mmol)的攪拌23℃溶液中添加diea(6.00g,8.10ml,46.41mmol)。反應混合物冷卻至0℃並攪拌0.5小時。0.5小時後,向反應混合物中添加其他diea(6.00g,8.01ml,46.4mmol)並且攪拌0.5小時。然後向反應混合物中添加cmpi(5.93g,23.2mmol),其緩慢升溫至室溫並且攪拌10小時。用1mhcl(30mlx2),之後用鹽水(25mlx2)洗滌粗反應。有機餾分在無水硫酸鈉上乾燥,過濾並真空濃縮。該粗產物無需進一步純化即可使用。獲得總共7.85g的棕色油狀物的boc-asp(obzl)-dil-otbu(13.9mmol,90%)。lcmsrt=1.72分鐘(方法b);esi-msm/z565.3[m+h]+.
攪拌二噁烷(20ml)中4.0mhcl中boc-asp(obzl)-dil-otbu(7.85g,13.9mmol)的23℃溶液。10小時後,通過lcms的分析顯示反應完全。揮發性有機物經真空蒸發以得到不需要進一步純化使用的粗產物。獲得總共7.85g的富集h-asp(obzl)-dil-oh的鹽酸鹽。lcmsrt=0.951分鐘(方法b);esi-msm/z409.40[m+h]+.
向dmf(20ml)中dov-oh(3.00g,20.7mmol)的攪拌23℃懸液中添加diea(6.96g,9.40ml,0.054mol)和hatu(7.60g,19.9mmol),之後添加富集h-asp(obzl)-dil-ohhcl鹽(7.85g)。4小時後,通過lcms的分析顯示反應完全。粗反應用飽和碳酸氫鈉(10ml)稀釋,並用etoac(20mlx2)萃取。合併的有機餾分用鹽水洗滌、在硫酸鎂墊上乾燥、過濾並真空濃縮。通過用phenomenexgemininx-c1810μ柱(150x30mm)的,使用0.1%水性nh4oh中5%至95%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共2.00g的白色固體的dov-asp(obzl)-dil-oh(3.74mmol,28%)。lcmsrt=1.10分鐘(方法b);esi-msm/z536.5[m+h]+.
向dmf(10ml)中dov-asp(obzl)-dil-oh(1.00g,1.87mmol)和h-dap-phe-ometfa鹽(1.04g,2.25mmol)的攪拌23℃懸液中添加diea(0.970g,1.30ml,7.47mmol),之後添加hatu(1.14g,2.99mmol)。10小時後,通過lcms的分析顯示反應完全。粗反應用飽和碳酸氫鈉(10ml)稀釋,並用etoac(20mlx3)萃取。合併的有機餾分用鹽水洗滌、在硫酸鎂墊上乾燥、過濾並真空濃縮。通過用phenomenexgemininx-c1810μ柱(150x30mm)的,使用0.1%水性nh4oh中5%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共1.25g的橙色固體的dov-asp(obzl)-dil-dap-phe-ome(1.44mmol,77%)。lcmsrt=1.21分鐘(方法b);esi-msm/z866.6[m+h]+.
向meoh(10ml)中dov-asp(obzl)-dil-dap-phe-ome(0.525g,0.606mmol)的攪拌23℃懸液中添加10%pd/c(50mg),之後添加氫氣氛。5小時後,通過lcms的分析顯示反應完全。粗反應混合物在硅藻土墊上過濾,之後蒸發揮發性有機物。通過用phenomenexgemininx-c1810μ柱(150x30mm)的,使用0.1%水性nh4oh中5%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共6.00mg的白色固體的標題化合物(0.008mmol,1%)。lcmsrt=1.04分鐘(方法b);esi-msm/z776.43[m+h]+;hrmsm/z776.4794[c40h65n5o10+h]+.
實施例47
(2s,3r)-2-((s)-2-(二甲基氨基)-3-甲基丁醯氧基)-3-羥基-n-((3r,4s,5s)-1-((s)-2-((1r,2r)-3-(((1s,2r)-1-羥基-1-苯基丙-2-基)氨基)-1-甲氧基-2-甲基-3-氧代丙基)吡咯烷-1-基)-3-甲氧基-5-甲基-1-氧代庚-4-基)-n-甲基丁醯胺
向dmf(20ml)中dov-dab(fmoc)-dil-ohtfa鹽(561mg,0.883mmol)和h-dap-(1r,2s)-(-)-降麻黃鹼tfa鹽(345mg,0.794mmol)的攪拌23℃溶液中添加diea(417mg,562μl,3.23mmol),之後添加hatu(820mg,2.15mmol)。8小時後,通過lcms的分析顯示反應完全。粗反應用飽和碳酸氫鈉(10ml)稀釋,並用etoac(20mlx2)萃取。合併的有機餾分用鹽水洗滌、在硫酸鎂墊上乾燥、過濾並真空濃縮。通過用phenomenexgemininx-c1810μ柱(150x30mm)的使用0.1%水性nh4oh中5%至95%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共326mg的白色固體的dov-thr(bzl)-dil-dap-(1r,2s)-(-)-降麻黃鹼(0.396mmol,37%)。lcmsrt=1.20分鐘(方法b);esi-msm/z824.76[m+h]+.
將meoh(10ml)中dov-thr(bzl)-dil-dap-(1r,2s)-(-)-降麻黃鹼(326mg,0.396mmol)的攪拌23℃懸液加載到使用rani(catcart)以及升高的溫度(120℃)和壓力(80巴)的連續流氫化反應器中。洗脫後,通過lcms的分析顯示反應完全。揮發性有機物經真空蒸發以得到粗產物,其通過用phenomenexgemininx-c1810μ柱(150x30mm)的,使用0.1%水性nh4oh中5%至95%mecn作為洗脫液的製備型rp-hplc純化。獲得總共15mg的白色固體的標題化合物(0.020mmol,5%)。lcmsrt=1.17分鐘(方法b);esi-msm/z734.5[m+h]+;hrmsm/z734.5053[c39h67n5o8+h]+.
實施例48
((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n,3-二甲基丁醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯基)-l-絲氨酸甲酯
向dmf(10ml)中dov-val-dil-ohtfa鹽(583mg,1.07mmol)和h-dap-ser-ometfa鹽(783mg,1.97mmol)的攪拌23℃懸液中添加diea(223mg,0.324ml,1.72mmol),之後添加hatu(1.03g,2.71mmol)。10小時後,通過lcms的分析顯示反應完全。粗反應用飽和碳酸氫鈉(10ml)稀釋,並用etoac(20mlx3)萃取。合併的有機餾分用鹽水洗滌、在硫酸鎂墊上乾燥、過濾並真空濃縮。通過用phenomenexgemininx-c1810μ柱(150x30mm)的,使用0.1%水性nh4oh中5%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共704mg的淡黃色固體的標題化合物(1.01mmol,74%)。lcmsrt=0.917分鐘(方法b);esi-msm/z700.43[m+h]+;hrmsm/z700.4843[c35h65n5o9+h]+.
實施例49
((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((2s,3s)-3-疊氮基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丁醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯基)-l-異亮氨酸甲酯
向ch2cl2(20ml)中boc-dap-oh二環己基胺鹽(6.62g,14.1mmol)和h-ile-ome(3.08g,21.2mmol)的攪拌23℃懸液中添加diea(7.30g,9.90ml,56.5mmol),之後添加hatu(3.44g,3.20ml,0.021mol)。10小時後,通過lcms的分析顯示反應完全。揮發性有機物經真空蒸發以得到不需要進一步純化使用的粗產物。獲得總共8.56g的棕色油狀物的boc-dap-ile-ome(20.7mmol,88%)。lcmsrt=1.51分鐘(方法b);esi-msm/z415.16[m+h]+.
向ch2cl2(20ml)中boc-dap-ile-ome(6.62g,16.0mmol)的攪拌23℃懸液添加tfa(10ml)。10小時後,通過lcms的分析顯示反應完全。揮發性有機物真空蒸發。通過用phenomenexgemininx-c1810μ柱(150x30mm)的,使用0.1%水性nh4oh中5%至95%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共3.55g的黃色固體的h-dap-ile-ome(8.29mmol,52%)。lcmsrt=0.691分鐘(方法b);esi-msm/z315.16[m+h]+.
向dmf(10ml)中dov-abu(3-n3)-dil-ohtfa鹽(150mg,0.329mmol)和h-dap-ile-ome(207mg,0.657mmol)的攪拌23℃懸液中添加diea(170mg,0.220ml,1.31mmol),之後添加hatu(251mg,0.657mmol)。10小時後,通過lcms的分析顯示反應完全。粗反應用飽和碳酸氫鈉(10ml)稀釋,並用etoac(20mlx3)萃取。合併的有機餾分用鹽水洗滌、在硫酸鎂墊上乾燥、過濾並真空濃縮。通過用phenomenexgemininx-c1810μ柱(150x30mm)的,使用0.1%水性nh4oh中5%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共148mg的淡黃色固體的標題化合物(0.197mmol,60%)。lcmsrt=1.43分鐘(方法b);esi-msm/z753.48[m+h]+;hrmsm/z753.5224[c37h68n8o8+h]+.
實施例50
(2s,3s)-3-氨基-n-((3r,4s,5s)-1-((s)-2-((1r,2r)-3-(((s)-1-氨基-1-氧代-3-苯基丙-2-基)氨基)-1-甲氧基-2-甲基-3-氧代丙基)吡咯烷-1-基)-3-甲氧基-5-甲基-1-氧代庚-4-基)-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丁醯胺
向thf(0.1ml)中dov-abu(3-n3)-dil-dap-phe-nh2(13.4mg,0.017mmol)的攪拌室溫溶液中添加thf中三甲基膦(1m,0.035ml,0.035mmol)。3小時後,添加額外的三甲基膦(1m,0.020ml,0.020mmol)。另外1小時後,通過lcms的分析顯示反應完全。溶液用水和dmf稀釋並放置30分鐘。通過用phenomenexgemini-nx10μc18,柱(150x30mm)的,使用0.1%水性氫氧化銨中5%至95%mecn作為洗脫液的製備型rp-hplc純化粗反應混合物。獲得總共5.8mg的標題化合物(0.008mmol,45%)。lcmsrt=0.85分鐘(方法b);esi-msm/z746.6[m+h]+;hrmsm/z746.5173[c39h67n7o7+h]+.
實施例51
(2s,3s)-3-氨基-n-((3r,4s,5s)-1-((s)-2-((1r,2r)-3-(((s)-1-(叔丁基氨基)-1-氧代-3-苯基丙-2-基)氨基)-1-甲氧基-2-甲基-3-氧代丙基)吡咯烷-1-基)-3-甲氧基-5-甲基-1-氧代庚-4-基)-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丁醯胺
向thf(0.1ml)中dov-abu(3-n3)-dil-dap-phe-nht-bu(15.4mg,0.019mmol)的攪拌室溫溶液中添加thf中三甲基膦(1m,0.037ml,0.037mmol)。3小時後,添加額外的三甲基膦(1m,0.020ml,0.020mmol)。另外1小時後,通過lcms的分析顯示反應完全。反應溶液用水和dmf稀釋並放置30分鐘。通過用phenomenexgemini-nx10μc-18,柱(150x30mm)的,使用0.1%水性氫氧化銨中5%至95%mecn作為洗脫液的製備型rp-hplc純化粗反應混合物。獲得總共2.7mg的標題化合物(0.003mmol,18%)。lcmsrt=0.85分鐘(方法b);esi-msm/z746.6[m+h]+;hrmsm/z802.5799[c43h75n7o7+h]+.
實施例52
((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-3-疊氮基-n-甲基-2-((s)-3-甲基-2-(甲基氨基)丁醯氨基)丙醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯基)-l-苯丙氨酸甲酯
向dmf(10ml)中fmoc-meval-oh(1.03g,2.90mmol)的攪拌23℃懸液中添加diea(1.35ml,7.74mmol),之後添加hatu(1.11g,2.90mmol)。在5分鐘後,向反應混合物中添加h-4-疊氮基-ala-dil-oh(0.610g,2.90mmol)。10小時後,通過lcms的分析顯示反應完全。粗反應用飽和碳酸氫鈉(15ml)稀釋,並用etoac(40mlx2)萃取。合併的有機餾分用鹽水洗滌、在硫酸鎂墊上乾燥、過濾並真空濃縮。通過用phenomenexgemininx-c1810μ柱(150x30mm)的,使用0.1%水性nh4oh中5%至95%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共348mgfmoc-meval-4-疊氮基-ala-dil-oh的黃色油狀物(0.535mmol,28%)。lcmsrt=1.80分鐘(方法b);esi-msm/z651.3[m+h]+.
向dmf(10ml)中fmoc-meval-4-疊氮基-ala-dil-oh(348.00mg,0.535mmol)和h-dap-phe-ome(372.66mg,1.07mmol)的攪拌23℃懸液中添加diea(276mg,0.400ml,2.14mmol),之後添加hatu(408mg,1.07mmol)。10小時後,通過lcms分析顯示反應完全,同時出現fmoc基團去保護。粗反應用飽和碳酸氫鈉(10ml)稀釋,並用etoac(20mlx3)萃取。合併的有機餾分用鹽水洗滌、在硫酸鎂墊上乾燥、過濾並真空濃縮。通過用phenomenexgemininx-c1810μ柱(150x30mm)的,使用0.1%水性甲酸中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共5.00mg的標題化合物(0.006mmol,1%)。lcmsrt=1.08分鐘(方法b);esi-msm/z759.5[m+h]+;hrmsm/z759.4753[c38h62n8o8+h]+.
實施例53
((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((2s,3s)-3-疊氮基-n-甲基-2-((s)-3-甲基-2-(甲基氨基)丁醯氨基)丁醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯基)-l-苯丙氨酸甲酯
向dmf(10ml)中fmoc-meval-oh(2.46g,6.96mmol)和h-abu(3-n3)-dil-otbu(2.46g,6.38mmol)的攪拌23℃懸液中添加diea(3.30g,4.5ml,25.5mmol),之後添加hatu(3.65g,9.57mmol)。6小時後,通過lcms的分析顯示反應完全。通過用phenomenexgemininx-c1810μ柱(150x30mm)的,使用0.1%水性甲酸中5%至95%mecn作為洗脫液的製備型rp-hplc純化粗反應混合物。獲得總共3.16g的fmoc-meval-abu(3-n3)-dil-otbu的甲酸鹽(4.12mmol,65%)。lcmsrt=2.08分鐘(方法a);esi-msm/z722.7[m+h]+.
向ch2cl2(5.0ml)中fmoc-meval-abu(3-n3)-dil-otbu甲酸鹽(3.16g,4.12mmol)的攪拌23℃懸液中添加tfa(10.0ml)。14小時後,通過lcms的分析顯示反應完全。揮發性有機物經真空蒸發得到油。通過用phenomenexgemininx-c1810μ柱(150x30mm)的,使用0.1%水性tfa中5%至95%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共2.26g的fmoc-meval-abu(3-n3)-dil-oh的tfa鹽(2.90mmol,66%)。lcmsrt=1.80分鐘(方法b);esi-msm/z665.3[m+h]+.
向dmf(2ml)中fmoc-meval-abu(3-n3)-dil-ohtfa鹽(80.0mg,0.103mmol)和h-dap-phe-ometfa鹽(83.9mg,0.182mmol)的攪拌23℃懸液中添加diea(0.083mmol,0.481mmol),之後添加hatu(91.8mg,0.241mmol)。12小時後,通過lcms的分析顯示反應完全。粗反應混合物用dmf稀釋並通過用phenomenexgemininx-c1810μ柱(150x30mm)的,使用0.1%水性甲酸中10%至90%mecn作為洗脫液的製備型rp-hplc純化。獲得總共97.0mg的fmoc-meval-abu(3-n3)-dil-dap-phe-ome的甲酸鹽(0.093mmol,77%)。lcmsrt=1.90分鐘(方法b);esi-msm/z995.6[m+h]+.
向乙腈(10ml)中fmoc-meval-abu(3-n3)-dil-dap-phe-ome(97.0mg,0.093mmol)的攪拌23℃溶液中添加哌啶(5ml)。5小時後,通過lcms的分析顯示反應完全。向粗反應溶液中添加己烷(25mlx3)以萃取非極性副產物。乙腈層經真空濃縮並且通過用phenomenexgemininx-c1810μ柱(150x30mm)的,使用0.1%水性nh4oh中5%至95%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共74.0mg的白色固體的標題化合物(0.096mmol,103%)。lcmsrt=1.09分鐘(方法b);esi-msm/z773.5[m+h]+;hrmsm/z773.4911[c39h64n8o8+h]+.
實施例54
(2s,3s)-n-((3r,4s,5s)-1-((s)-2-((1r,2r)-3-(((s)-1-氨基-1-氧代-3-苯基丙-2-基)氨基)-1-甲氧基-2-甲基-3-氧代丙基)吡咯烷-1-基)-3-甲氧基-5-甲基-1-氧代庚-4-基)-3-疊氮基-n-甲基-2-((s)-3-甲基-2-(甲基氨基)丁醯氨基)丁醯胺
向ch2cl2(20.0ml)中bod-dap-oh二環己基胺鹽(10.0g,21.3mmol)和h-phe-nh2hcl鹽(6.42g,32.0mmol)的攪拌23℃懸液中添加diea(11.0g,14.9ml,85.3mmol),之後添加depc(5.19g,4.80ml,0.032mol)。10小時後,通過lcms的分析顯示反應完全。用h2o(25mlx2),之後用鹽水(25mlx2)洗滌粗反應。有機餾分在硫酸鎂墊上乾燥、過濾並真空濃縮。使用ch2cl2中2%至10%甲醇作為洗脫劑,通過快速色譜(矽膠40μm,尺寸)純化粗製橙色油狀物。獲得總共7.25g的boc-dap-phe-nh2的黃色油(16.7mmol,78%)。lcmsrt=1.28分鐘(方法b);esi-msm/z434.19[m+h]+.
向ch2cl2(10ml)中boc-dap-phe-nh2(7.25g,16.7mmol)的攪拌23℃懸液添加tfa(10ml)。5小時後,通過lcms的分析顯示反應完全。揮發性有機物經真空蒸發以得到不需要進一步純化使用的粗產物。獲得總共6.00g的黃色固體的h-dap-phe-nh2(13.4mmol,80%)。lcmsrt=0.691分鐘(方法b);esi-msm/z334.17[m+h]+.
向dmf(10ml)中fmoc-meval-abu(3-n3)-dil-ohtfa鹽(456mg,0.586mmol)和h-dap-phe-nh2tfa鹽(457mg,1.02mmol)的攪拌23℃懸液中添加diea(0.350g,0.500ml,2.74mmol),之後添加hatu(0.520g,1.37mmol)。10小時後,通過lcms的分析顯示反應完全。通過用phenomenexgemininx-c1810μ柱(150x30mm)的,使用0.1%水性甲酸中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗反應。獲得總共526mg的fmoc-meval-abu(3-n3)-dil-dap-phe-nh2的甲酸鹽(0.513mmol,75%)。lcmsrt=1.81分鐘(方法b);esi-msm/z980.39[m+h]+.
向乙腈(10ml)中fmoc-meval-abu(3-n3)-dil-dap-phe-nh2(525mg,0.513mmol)的攪拌23℃溶液中添加哌啶(5ml)。2小時後,通過lcms的分析顯示反應完全。向粗反應中添加己烷(15mlx3)。乙腈層經真空濃縮。通過用phenomenexgemininx-c1810μ柱(150x30mm)的,使用0.1%水性tfa中5%至95%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共354mg的標題化合物的tfa鹽(0.406mmol,79%)。lcmsrt=1.15分鐘(方法b);esi-msm/z758.24[m+h]+;hrmsm/z758.4915[c38h63n9o7+h]+.
實施例55
((2s,3s)-3-疊氮基-n-((3r,4s,5s)-1-((s)-2-((1r,2r)-3-(((s)-1-(叔丁基氨基)-1-氧代-3-苯基丙-2-基)氨基)-1-甲氧基-2-甲基-3-氧代丙基)吡咯烷-1-基)-3-甲氧基-5-甲基-1-氧代庚-4-基)-n-甲基-2-((s)-3-甲基-2-(甲基氨基)丁醯氨基)丁醯胺
向dmf(1.0ml)中fmoc-meval-abu(3-n3)-dil-dap-phe-oh(111mg,0.113mmol)、叔丁基胺鹽酸鹽(31.5mg,0.287mmol)、hatu(92.0mg,0.242mmol)的攪拌室溫溶液中添加胡尼鹼(0.079ml,0.454mmol)。1小時後,通過lcms的分析顯示反應完全。用乙酸乙酯稀釋粗反應混合物並且用1nhcl和鹽水洗滌有機餾分。有機餾分在硫酸鎂上乾燥,過濾,並減壓濃縮。粗製黃色油狀物溶於哌啶(2.0ml)和乙腈(5.0ml)。1小時後,通過lcms的分析顯示反應完全。乙腈層用乙烷(2x)萃取並且乙腈層經減壓濃縮。通過用phenomenexgemini-nx10μc-18,柱(150x30mm)的,使用0.1%水性氫氧化銨中5%至95%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共50.3mg的標題化合物(0.062mmol,55%)。lcmsrt=1.29分鐘(方法b);esi-msm/z814.1[m+h]+;hrmsm/z814.5541[c42h71n9o7+h]+.
實施例56
((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((2s,3s)-3-疊氮基-n-甲基-2-((s)-3-甲基-2-(甲基氨基)丁醯氨基)丁醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯基)-l-苯丙氨酸叔丁酯
向dcm(20ml)中boc-dap-oh二環己基胺鹽(6.47g,13.8mmol)和h-phe-otbu(3.91g,15.2mmol)的攪拌25℃溶液中添加diea(8.76ml,55.2mmol),之後添加depc(3.12ml,20.7mmol)。8小時後,通過lcms的分析顯示反應完全。揮發性有機物經真空蒸發以得到不需要進一步純化使用的粗產物。獲得總共5.35g的boc-dap-phe-otbu(10.9mmol,79%)。lcmsrt=2.89分鐘(方法a);esi-msm/z491.48[m+h]+.
向ch2cl2(10.0ml)中boc-dap-phe-otbu(5.25g,10.7mmol)的攪拌室溫溶液添加tfa(10.0ml)。12小時後,通過lcms的分析顯示反應完全。通過用phenomenexsynergi10μmax-rp柱(150x30mm)的,使用0.05%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共2.85g的h-dap-phe-otbu的tfa鹽(5.65mmol,68%)。lcmsrt=1.82分鐘(方法a);esi-msm/z391.02[m+h]+.
向dmf(10ml)中fmoc-meval-abu(3-n3)-dil-ohtfa鹽(410mg,0.527mmol)和h-dap-phe-otbutfa鹽(482mg,0.956mmol)的攪拌23℃懸液中添加diea(319mg,430μl,2.47mmol),之後添加hatu(470mg,1.23mmol)。10小時後,通過lcms分析顯示反應完全,同時去除10%的fmoc基團。通過用phenomenexgemininx-c1810μ柱(150x30mm)的,使用0.1%水性甲酸中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗反應混合物。獲得總共26.0mg的標題化合物的白色甲酸鹽(0.030mmol,5%)。lcmsrt=1.41分鐘(方法b);esi-msm/z815.33[m+h]+;hrmsm/z815.5383[c42h70n8o8+h]+.
實施例57
((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((2s,3s)-3-疊氮基-n-甲基-2-((s)-3-甲基-2-(甲基氨基)丁醯氨基)丁醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯基)-l-苯丙氨酸
向dmf(10ml)中fmoc-meval-abu(3-n3)-dil-ohtfa鹽(410mg,0.527mmol)和h-dap-phe-otbutfa鹽(482mg,0.956mmol)的攪拌23℃懸液中添加diea(319mg,430μl,2.47mmol),之後添加hatu(470mg,1.23mmol)。10小時後,通過lcms的分析顯示反應完全。通過用phenomenexgemininx-c1810μ柱(150x30mm)的,使用0.1%水性甲酸中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗反應混合物。獲得總共648mg的fmoc-meval-abu(3-n3)-dil-dap-phe-otbu的白色甲酸鹽(0.598mmol,97%)。lcmsrt=1.41分鐘(方法b);esi-msm/z1037.41[m+h]+.
向ch2cl2(5.00ml)中fmoc-meval-abu(3-n3)-dil-dap-phe-otbu甲酸鹽(648mg,0.598mmol)的攪拌23℃懸液中添加tfa(5.00ml)。2小時後,通過lcms的分析顯示反應完全。揮發性有機物經真空蒸發得到棕色油狀物。通過用phenomenexgemininx-c1810μ柱(150x30mm)的,使用0.1%水性tfa中5%至95%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共502mg的fmoc-meval-abu(3-n3)-dil-dap-phe-oh的tfa鹽(0.458mmol,77%)。lcmsrt=1.81分鐘(方法b);esi-msm/z981.22[m+h]+.
向乙腈(10ml)中fmoc-meval-abu(3-n3)-dil-dap-phe-ohtfa鹽(392mg,0.382mmol)的攪拌23℃溶液中添加哌啶(5ml)。2小時後,通過lcms的分析顯示反應完全。向粗反應中添加己烷(15mlx3)。乙腈層經真空濃縮。通過用phenomenexgemininx-c1810μ柱(150x30mm)的,使用0.1%水性tfa中5%至95%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共360mg的標題化合物的tfa鹽。lcmsrt=1.19分鐘(方法b);esi-msm/z759.13[m+h]+;hrmsm/z759.4755[c38h62n8o8+h]+.
實施例58
((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((2s,3s)-3-疊氮基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丁醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯基)-l-苯丙氨酸叔丁酯
向dmf(10ml)中dov-abu(3-n3)-dil-ohtfa鹽(327mg,0.574mmol)和h-dap-phe-otbutfa鹽(0.340g,0.675mmol)的攪拌23℃懸液中添加diea(0.370g,0.500ml,2.87mmol),之後添加hatu(0.550g,1.43mmol)。10小時後,通過lcms的分析顯示反應完全。通過用phenomenexgemininx-c1810μ柱(150x30mm)的,使用0.1%水性甲酸中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗反應。獲得總共453mg的標題化合物的甲酸鹽(0.518mmol,72%)。lcmsrt=1.42分鐘(方法b);esi-msm/z828.94[m+h]+;hrmsm/z829.5536[c43h72n8o8+h]+.
實施例59
(2s,3s)-3-疊氮基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-((3r,4s,5s)-3-甲氧基-1-((s)-2-((1r,2r)-1-甲氧基-2-甲基-3-氧代-3-(((s)-2-苯基-1-(1h-四唑-5-基)乙基)氨基)丙基)吡咯烷-1-基)-5-甲基-1-氧代庚-4-基)-n-甲基丁醯胺
向ch2cl2(20.0ml)中boc-dap-oh二環己基胺鹽(2.48g,5.29mmol)和(s)-2-苯基-1-(1h-四唑-5-基)乙基胺(1.00g,5.29mmol)的攪拌23℃懸液中添加diea(2.73g,3.7ml,21.1mmol),之後添加depc(1.29g,1.20ml,7.93mmol)。10小時後,通過lcms的分析顯示反應完全。揮發性有機物真空蒸發。通過用phenomenexgemininx-c1810μ柱(150x30mm)的,使用0.1%水性甲酸中5%至95%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共2.52g的boc-dap-(s)-2-苯基-1-(1h-四唑-5-基)乙基胺的甲酸鹽(4.99mmol,94%)。lcmsrt=1.35分鐘(方法b);esi-msm/z459.2[m+h]+.
向ch2cl2(10ml)中boc-dap-(s)-2-苯基-1-(1h-四唑-5-基)乙基胺(2.52g,4.99mmol)的攪拌23℃懸液添加tfa(5.00ml)。5小時後,通過lcms的分析顯示反應完全。揮發性有機物經真空蒸發以得到不需要進一步純化使用的粗產物。獲得總共2.43g的h-dap-(s)-2-苯基-1-(1h-四唑-5-基)乙基胺的tfa鹽(5.14mmol,84%)。lcmsrt=0.575分鐘(方法b);esi-msm/z359.2[m+h]+.
向dmf(10ml)中dov-abu(3-n3)-dil-ohtfa鹽(305mg,0.668mmol)和h-dap-(s)-2-苯基-1-(1h-四唑-5-基)乙基胺tfa鹽(0.36g,1.002mmol)的攪拌23℃懸液中添加diea(0.35g,0.5ml,2.67mmol),之後添加hatu(509mg,1.34mmol)。10小時後,通過lcms的分析顯示反應完全。粗反應用飽和碳酸氫鈉(10ml)稀釋,並用etoac(20mlx3)萃取。合併的有機餾分用鹽水洗滌、在硫酸鎂墊上乾燥、過濾並真空濃縮。通過用phenomenexgemininx-c1810μ柱(150x30mm)的,使用0.1%水性甲酸中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共47.0mg的標題化合物的甲酸鹽(0.056mmol,8%)。lcmsrt=1.24分鐘(方法b);esi-msm/z797.3[m+h]+;hrmsm/z797.5139[c39h64n12o6+h]+.
實施例60
(2s,3s)-3-疊氮基-n-((3r,4s,s)-3-甲氧基-1-((s)-2-((1r,2r)-1-甲氧基-2-甲基-3-氧代-3-(((s)-2-苯基-1-(1h-四唑-5-基)乙基)氨基)丙基)吡咯烷-1-基)-5-甲基-1-氧代庚-4-基)-n-甲基-2-((s)-3-甲基-2-(甲基氨基)丁醯氨基)丁醯胺
同dmf(10ml)中fmoc-meval-abu(3-n3)-dil-ohtfa鹽(0.491g,0.631mmol)和h-dap-(s)-2-苯基-1-(1h-四唑-5-基)乙基胺tfa鹽(0.532g,1.13mmol)的攪拌23℃懸液中添加diea(0.381g,0.500ml,2.97mmol),之後添加hatu(0.57g,1.486mmol)。10小時後,通過lcms的分析顯示反應完全。粗反應用飽和碳酸氫鈉(10ml)稀釋,並用etoac(20mlx3)萃取。合併的有機餾分用鹽水洗滌、在硫酸鎂墊上乾燥、過濾並真空濃縮。通過用phenomenexgemininx-c1810μ柱(150x30mm)的,使用0.1%水性甲酸中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共125mg的fmoc-meval-abu(3-n3)-dil-dap-(s)-2-苯基-1-(1h-四唑-5-基)乙基胺的甲酸鹽(0.119mmol,16%)。lcmsrt=1.94分鐘(方法b);esi-msm/z1005.35[m+h]+.
向乙腈(10ml)中fmoc-meval-abu(3-n3)-dil-dap-(s)-2-苯基-1-(1h-四唑-5-基)乙基胺(525mg,0.499mmol)的攪拌23℃溶液中添加哌啶(5ml)。2小時後,通過lcms的分析顯示反應完全。向粗反應溶液中添加己烷(x3)。乙腈層經真空濃縮。通過用phenomenexgemininx-c1810μ柱(150x30mm)的,使用0.1%水性tfa中5%至95%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共20.0mg的標題化合物的tfa鹽(0.022mmol,5%)。lcmsrt=1.37分鐘(方法b);esi-msm/z783.42[m+h]+;hrmsm/z783.4979[c38h62n12o6+h]+.
實施例61
(2s,3s)-3-疊氮基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-((3r,4s,5s)-3-甲氧基-1-((s)-2-((1r,2r)-1-甲氧基-2-甲基-3-氧代-3-(((s)-2-苯基-1-(噻唑-2-基)乙基)氨基)丙基)吡咯烷-1-基)-5-甲基-1-氧代庚-4-基)-n-甲基丁醯胺
向ch2cl2(20.0ml)中boc-dap-oh二環己基胺鹽(1.95g,4.154mmol)和(s)-2-苯基-1-(2-四唑2-基)乙基胺(1.00g,4.154mmol)的攪拌23℃懸液中添加diea(2.15g,2.9ml,16.615mmol),之後添加depc(1.01g,0.9ml,0.006mol)。10小時後,通過lcms的分析顯示反應完全。用h2o(25mlx2),之後用鹽水(25mlx2)洗滌粗反應混合物。有機餾分在mgso4墊上乾燥、過濾並真空濃縮。獲得總共1.65g的黃色油狀物的boc-dap-(s)-2-苯基-1-(噻唑-2-基)乙基胺(3.48mmol,84%)。lcmsrt=1.59分鐘(方法b);esi-msm/z475.2[m+h]+.
向ch2cl2(10.0ml)中boc-dap-(s)-2-苯基-1-(噻唑-2-基)乙基胺(1.65g,3.49mmol)的攪拌23℃懸液添加tfa(10.0ml)。4小時後,通過lcms的分析顯示反應完全。揮發性有機物真空蒸發。粗製油狀物溶於dmf(5ml)和三乙基胺(1ml)以實現ph8。通過用phenomenexgemininx-c1810μ柱(150x30mm)的,使用0.1%水性tfa中5%至95%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共935mg的h-dap-(s)-2-苯基-1-(噻唑-2-基)乙基胺的tfa鹽(1.92mmol,55%)。lcmsrt=1.04分鐘(方法b);esi-msm/z375.0[m+h]+.
向dmf(10ml)中dov-abu(3-n3)-dil-ohtfa鹽(302mg,0.661mmol)和h-dap-(s)-2-苯基-1-(噻唑-2-基)乙基胺tfa鹽(247mg,0.661mmol)的攪拌23℃懸液中添加diea(0.34g,0.5ml,2.65mmol),之後添加hatu(504mg,1.32mmol)。10小時後,通過lcms的分析顯示反應完全。粗反應混合物用飽和碳酸氫鈉(10ml)稀釋,並用etoac(20mlx3)萃取。合併的有機餾分用鹽水洗滌、在硫酸鎂墊上乾燥、過濾並真空濃縮。通過用phenomenexgemininx-c1810μ柱(150x30mm)的,使用0.1%水性tfa中10%至90%mecn作為洗脫液的製備型rp-hplc純化粗製油狀物。獲得總共111mg的標題化合物的tfa鹽(0.120mmol,18%)。lcmsrt=1.33分鐘(方法b);esi-msm/z812.2[m+h]+;hrmsm/z812.4835[c41h65n9o6s+h]+.
實施例62
((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((2s,3s)-3-氨基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-甲基丁醯氨基)-3-甲氧基-5-甲基庚醯基)吡咯烷-2-基)-3-甲氧基-2-甲基丙醯基)-l-苯丙氨酸叔丁酯
向dmf(1.0ml)中dov-abu(3-n3)-dil-dap-phe-ot-bu甲酸鹽(102.5mg,0.117mmol)的攪拌室溫溶液中添加thf中三甲基膦(1m,0.350ml,0.350mmol)。2小時後,通過lcms的分析顯示反應完全。通過用phenomenexgemini-nx10μc-18,柱(150x30mm)的,使用0.1%水性甲酸中5%至95%mecn作為洗脫液的製備型rp-hplc純化粗反應混合物。獲得總共70.1mg的標題化合物的甲酸鹽(0.083mmol,70%)。lcmsrt=1.22分鐘(方法b);esi-msm/z803.3[m+h]+;hrmsm/z803.5642[c43h74n6o8+h]+.
實施例63
(2s,3s)-3-氨基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-((3r,4s,5s)-3-甲氧基-1-((s)-2-((1r,2r)-1-甲氧基-2-甲基-3-氧代-3-(((s)-2-苯基-1-(1h-四唑-5-基)乙基)氨基)丙基)吡咯烷-1-基)-5-甲基-1-氧代庚-4-基)-n-甲基丁醯胺
向dmf(0.2ml)中dov-abu(3-n3)-dil-dap-phe-四唑甲酸鹽(19.4mg,0.023mmol)的攪拌室溫溶液中添加thf中三甲基膦(1m,0.068ml,0.068mmol)。2小時後,通過lcms的分析顯示反應完全。通過用phenomenexgemini-nx10μc-18,柱(150x30mm)的,使用0.1%水性甲酸中5%至95%mecn作為洗脫液的製備型rp-hplc純化粗反應混合物。獲得總共9.9mg的標題化合物的甲酸鹽(0.012mmol,53%)。lcmsrt=1.07分鐘(方法b);esi-msm/z771.2[m+h]+;hrmsm/z771.5233[c39h66n10o8+h]+.
實施例64
(2s,3s)-3-氨基-2-((s)-2-(二甲基氨基)-3-甲基丁醯氨基)-n-((3r,4s,5s)-3-甲氧基-1-((s)-2-((1r,2r)-1-甲氧基-2-甲基-3-氧代-3-(((s)-2-苯基-1-(噻唑-2-基)乙基)氨基)丙基)吡咯烷-1-基)-5-甲基-1-氧代庚-4-基)-n-甲基丁醯胺
向dmf(0.2ml)中dov-abu(3-n3)-dil-dap-phe-噻唑甲酸鹽(37.2mg,0.043mmol)的攪拌室溫溶液中添加thf中三甲基膦(1m,0.090ml,0.090mmol)。1小時後,通過lcms的分析顯示反應完全。通過用phenomenexgemini-nx10μc-18,柱(150x30mm)的,使用0.1%水性甲酸中5%至95%mecn作為洗脫液的製備型rp-hplc純化粗反應混合物。獲得總共16.8mg的標題化合物的甲酸鹽(0.020mmol,47%)。lcmsrt=1.15分鐘(方法b);esi-msm/z786.2[m+h]+;hrmsm/z786.4940[c41h67n7o6s+h]+.
實施例b1
體外細胞毒性實驗
通過評價化合物對各種癌細胞系的細胞毒性活性測量它們的體外效力。在用透明組織培養處理的96-孔板中進行該試驗。使用的細胞系是pc3(人前列腺癌)、hcc-1954(人乳腺導管癌)、和hct15(人結直腸腺癌,pgp-表達)。細胞以約1,000-1,500個細胞/孔接種到50μl的生長培養基(rpmi-1640+10%熱滅活胎牛血清)中並在37℃和5%co2下過夜孵育使它們貼壁。第二天,一式三份向各孔中添加50μl的載劑對照(dmso)的2x母液或不同濃度的化合物。另外,使用沒有細胞或僅未處理細胞的對照孔。在添加化合物之後,板在37℃下5%co2的加溼組織培養孵育器中孵育4-6天以測量細胞毒性。在4-6天後,每孔添加20μl的prestobluetm細胞活力試劑(生命技術公司(lifetechnologies)#a13261)。板在37℃下孵育1-2小時。使用bioteksynergytmh4酶標儀記錄540ex/590em下的螢光。代表性數據繪製為與未處理的對照孔相比的存活百分比。該試驗中測試的化合物的數據繪製為與未處理的對照孔相比的存活百比分,如圖9-30所示。
實施例b2
微管蛋白聚合的測定
在牛腦微管蛋白上評價本文所述的化合物對微管蛋白聚合的抑制。為了評價化合物的活性,以約400μg/孔在100μl通用微管蛋白緩衝液中接種微管蛋白,然後在試驗開始時一式兩份用10μm終濃度的化合物處理。在添加測試化合物之後,通常在37℃下進行微管蛋白聚合試驗持續60分鐘。通過利用340nm處的光學密度值的吸光度光譜分析確定微管蛋白聚合。為了測試聚合的微管蛋白的量,在添加測試化合物之後,獲取每分鐘的340nm處的光學密度值。對於分析,化合物處理的微管蛋白的微管蛋白聚合程度與對照的程度相比,對照是緩衝液處理的微管蛋白。具體地,使用hts-微管蛋白聚合試驗試劑盒(細胞骨架公司(cytoskeletoninc.);目錄號bk004p)進行微管蛋白抑制研究,採用以下取樣方案:
1.在試驗開始之前,預熱光度計和96-孔板至37℃持續30分鐘。熱板對於高聚合活性和可重複結果而言是必要的。
2.輸入所有的酶標儀參數(340nm處吸光度,37℃,每分鐘一個讀數)使光度計備用。一旦微管蛋白分裝到37℃孔中,必須立即開始讀取。
3.使500μl的通用微管蛋白緩衝液升溫至室溫。微管蛋白配體稀釋需要溫熱緩衝液。
4.包括紫杉醇作為對照。使用10μl的紫杉醇/孔,其使終濃度最終達到10μm。
5.製備冷試驗緩衝液:通用微管蛋白緩衝液,1mmgtp,10%甘油。
6.用1ml的冷試驗緩衝液重懸4mg的微管蛋白以使最終蛋白質濃度達到4mg/ml。將管放在冰上並且使蛋白質完全重懸3分鐘。
7.在試驗緩衝液中製備10x濃度的選擇化合物。
8.移取10μl的10x濃縮化合物到預熱板的所需數量的孔中。在37℃下孵育板2分鐘。
9.移取10μl的僅試驗緩衝液到2的對照孔中(緩衝液處理的微管蛋白)。
10.移取100μl的微管蛋白到所需數量的孔中(2個孔應該是零化合物對照,其經緩衝液處理)。
11.立即將板放入37℃的光度計中,並且開始讀取每分鐘的340nm處的光密度。340nm處增加的光密度等同於增加的微管蛋白聚合。
該試驗中測試的化合物的數據如圖1-8所示。
實施例b3
測試化合物體外效力的測定:在icrscid小鼠中植入的皮下建立的人膀胱癌細胞系sw780中的效力評價
對於動物體內研究,用20mm組氨酸,5%蔗糖,ph6和15%dmso稀釋測試化合物。雄性icrscid小鼠(紐約州哈德遜的塔科尼農場(taconicfarm,hudson,ny))飼養在標準嚙齒類微隔離器籠中。動物室的環境控制設為維持溫度20-24℃,相對溼度30%至70%,和大約12小鼠光/12小時黑暗循環。自由提供水和食物。在72小時順應後,用在與pbs(吉布可公司(gibco))混合的50%完全培養混合物(艾美捷(trevigen,inc.))中懸浮的sw780人膀胱癌細胞(2x106個細胞/小鼠)植入小鼠,並且監測腫瘤生長速率。當平均腫瘤體積達到約200mm3時,腫瘤經尺寸匹配並且小鼠隨機分成治療組(n=8或10)。在qw劑量方案上用2或4mg/kg(mpk)的測試化合物或載劑靜脈內處理荷瘤小鼠持續3周。使用卡尺測量腫瘤體積,每周2次。
雖然本發明中所述的化合物、用途和方法使本領域普通技術人員能夠製備並使用本文所述的化合物、用途和方法,本領域普通技術人員會理解並認同存在本文的具體實施方式、方法和實施例的變化、組合和等同方式。因此,本文提供的化合物、用途和方法不應受到上述實施方式、方法或實施例的限制,而是包括本文提供的化合物、用途和方法的範圍和精神內的所有實施方式和方法。
