染色體基因引物對和探針組合以及染色體核酸檢測試劑盒的製作方法
2023-12-01 07:28:16 3
本發明涉及一種基因引物與探針的組合以及包含該組合的試劑盒。更確切的說,是一種染色體基因引物對和探針組合以及染色體核酸檢測試劑盒。屬於醫用檢測領域。
背景技術:
目前檢測染色體一般採用原位雜交技術(fish),其缺點:自身雜交物的幹擾,不穩定、時間長、操作較繁瑣等,特別是在應用較短的cdna探針時效率明顯下降。使測試結果造成錯誤,正確率難以保證。針對有效游離dna保存、提取鑑定方法,日益引起廣大醫學家的關注。現有技術中,缺少有效鑑定游離dna、dna保存效果,及游離dna、dna提取效果的技術和檢測試劑盒。
為此,需要設計一種染色體基因引物對和探針組合以及染色體核酸檢測試劑盒,具有適用於無創基因管游離dna保存效果鑑定、游離dna提取效果鑑定、單細胞dna提取效果鑑定、法醫鑑定。
技術實現要素:
本發明的目的是為了解決現有技術中缺少有效鑑定游離dna、dna保存效果及游離dna、dna提取效果的技術和相關檢測試劑盒的問題;提供一種染色體基因引物對和探針組合以及染色體核酸檢測試劑盒通過探針與染色體基因引物對的組合適用於無創基因管游離dna保存效果鑑定、游離dna提取效果鑑定、單細胞dna提取效果鑑定、法醫鑑定。
本發明通過如下技術方案達到:
一種染色體基因引物對和探針組合,包括一個探針、一對染色體基因引物,其結構特點是:所述探針為taqman探針,所述一對染色體基因引物為一對基因序列反向的引物;
所述探針的序列為:acgcggctggtggatcagtgct;
所述第一引物對中的正向引物的序列為ttatgagcgcgaagcaaacg;
所述第一引物對中的反向引物的序列為:ccgtgggtggtctttaccg。
一種染色體核酸檢測試劑盒,包括chromosome反應混合液、dna提取液i;
所述chrmosome反應混合液包括taq酶系、dntp緩衝液混合物終濃度1×加量25μl、如權利要求1所述的正向引物25pmol/μl終濃度30~900nm加量1μl、如權利要求1所述的反向引物25pmol/μl終濃度30~900nm加量1μl、如權利要求1所述的探針25pmol/μl終濃度200nm加量0.5μl、無菌去離子水加量20.5μl。
所述dna提取液i包括na0h100mmol/l、edta1.5mmol/l、tristonx-10050mmol/l、1%np-40、ph=8.0的tris-hc150mmol/l。
本發明有益效果
本發明適用於無創基因管游離dna保存效果鑑定、游離dna提取效果鑑定、單細胞dna提取效果鑑定、法醫鑑定,檢測精確,避免了漏檢。
【附圖說明】
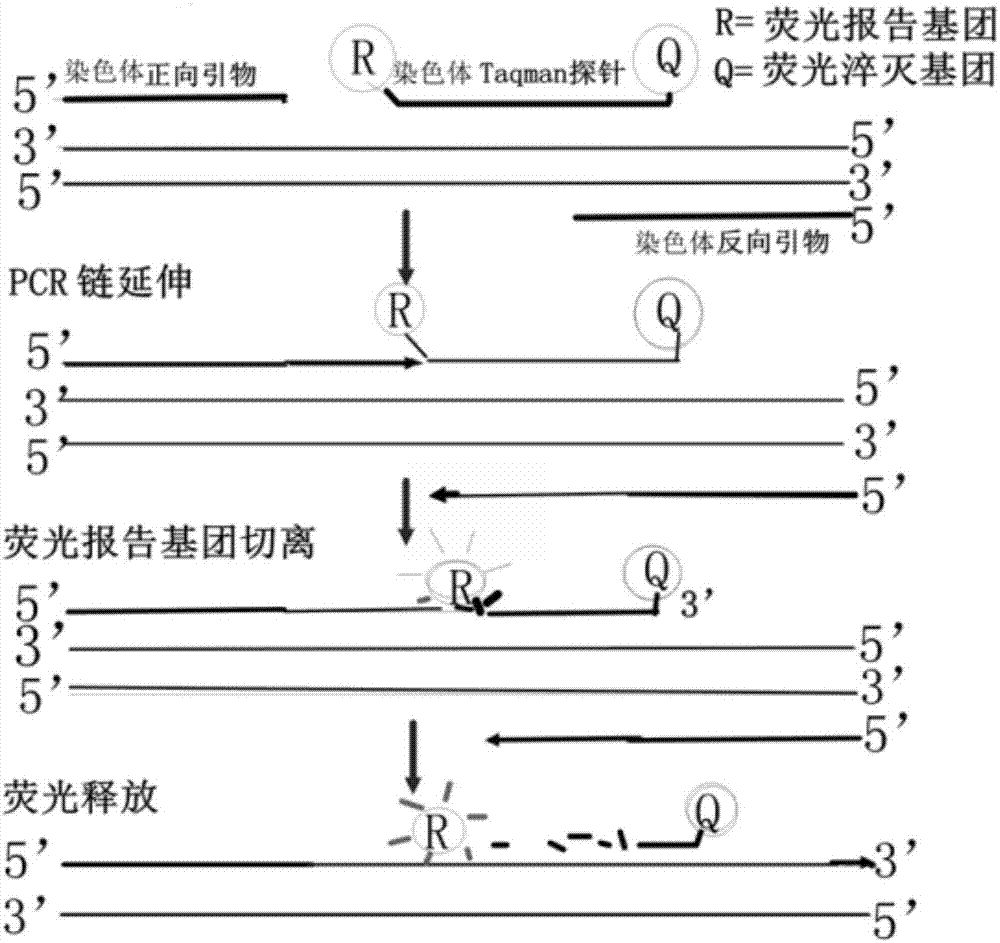
圖1為第一引物對和探針pcr螢光擴增原理圖;
圖2為核酸擴增螢光檢測結果分析陰性圖;
圖3為核酸擴增螢光檢測結果分析陽性圖。
具體實施例
以下本實施例結合附圖具體闡述本發明:
一種染色體基因引物對和探針組合,包括一個探針、一對染色體基因引物,其結構特點是:所述探針為taqman探針,所述一對染色體基因引物為一對基因序列反向的引物;
所述探針的序列為:acgcggctggtggatcagtgct;
所述第一引物對中的正向引物的序列為ttatgagcgcgaagcaaacg;
所述第一引物對中的反向引物的序列為:ccgtgggtggtctttaccg。
一種染色體核酸檢測試劑盒,包括chromosome反應混合液、dna提取液i;
所述chrmosome反應混合液包括taq酶系、dntp緩衝液混合物終濃度1×加量25μl、如權利要求1所述的正向引物25pmol/μl終濃度30~900nm加量1μl、如權利要求1所述的反向引物25pmol/μl終濃度30~900nm加量1μl、如權利要求1所述的探針25pmol/μl終濃度200nm加量0.5μl、無菌去離子水加量20.5μl。
所述dna提取液i包括na0h100mmol/l、edta1.5mmol/l、tristonx-10050mmol/l、1%np-40、ph=8.0的tris-hc150mmol/l。
使用該染色體核酸檢測試劑盒,實驗證明:100例樣本,用單細胞基因序列提取液提取單細胞dna產物30例,樣本編號d160501-d160530使用該染色體核酸擴增螢光檢測試劑盒來鑑定提取效果,染色體基因陽性,其平均濃度為(560000.00±50.00)拷貝/毫升。
如使用現有技術的上海醫脈賽科技有限公司提供的核酸提取試劑盒的磁珠法,血漿游離dna提取試劑盒提取無創基因管保存3天的40名孕婦游離dna,樣本編號c160531-c160570,染色體基因陽性,其平均濃度為(570.00±80.00)拷貝/毫升;其它試管保存3天的30名孕婦游離dna,樣本編號e160971-e1609100均為陰性。
結論用染色體核酸檢測試劑盒鑑定提取、保存效果有效,即呈陽性時游離dna、dna提取成功或保存有效;呈陰性時游離dna、dna提取或保存失敗。
樣本數據顯示如下:
參照附圖1至3,以上表格表示呈陽性時游離dna、dna提取成功或保存有效;呈陰性時游離dna、dna提取或保存失敗。廣泛應用於無創基因管游離dna保存效果鑑定、游離dna提取效果鑑定、單細胞dna提取效果鑑定、法醫鑑定等。
實時螢光定量pcr技術,是指在pcr反應體系中加入螢光基團,利用螢光信號積累實時監測整個pcr進程,最後通過標準曲線對未知模板進行定量分析的方法。
以下為檢測原理:
ct值的定義:
在螢光定量pcr技術中,c代表cycle,t代表threshold,ct值的含義是:每個反應管內的螢光信號到達設定的域值時所經歷的循環數螢光域值(threshold)的設定pcr反應的前10個循環的螢光信號作為螢光本底信號,螢光域值的預設設置是3-10個循環的螢光信號的標準偏差的10倍,即:threshold=10′sdcycle6-10
ct值與起始模板的關係
研究表明,每個模板的ct值與該模板的起始拷貝數的對數存在線性關係即起始拷貝數越多,ct值越小。只要獲得未知樣品的ct值,即可從標準曲線上計算出該樣品的起始拷貝數。
螢光定量pcr所使用的螢光化學現將其原理簡述如下:
taqman螢光探針:pcr擴增時在加入一對引物的同時加入一個特異性的螢光探針,該探針為一寡核苷酸,兩端分別標記一個報告螢光基團和一個淬滅螢光基團。探針完整時,報告基團發射的螢光信號被淬滅基團吸收;pcr擴增時,taq酶的5'-3'外切酶活性將探針酶切降解,使報告螢光基團和淬滅螢光基團分離,從而螢光監測系統可接收到螢光信號,即每擴增一條dna鏈,就有一個螢光分子形成,實現了螢光信號的累積與pcr產物形成完全同步。
現有技術中上海醫脈賽科技有限公司提供的核酸提取試劑盒---磁珠法,該試劑盒適合於從血漿等無細胞組織液中提取游離dna(circulatingfreedna,cfdna)片段。該試劑盒中的提取過程,具體操作步驟請按照該試劑盒說明書指引進行。
染色體核酸檢測試劑盒:
【檢驗原理】
本試劑盒利用螢光pcr技術,以chromosome基因組中相對保守區為靶區域,設計特異性引物及螢光探針,在樣本核酸純化之後,通過pcr對chromosomedna進行快速檢測。使用本試劑盒提供的核酸提取試劑對臨床樣本進行處理和核酸提取,以試劑盒中提供的pcr檢測試劑配製成pcr反應管,將提取的核酸加入pcr反應管,使用螢光定量pcr儀進行pcr擴增,並檢測螢光信號,儀器軟體自動繪製出實時擴增曲線,根據閾循環值(ct值)實現對未知樣本的定性檢測。
【儲存條件及有效期】
經包裝後的試劑盒(包含核酸提取試劑、質控品組分、pcr檢測試劑組分)保存於—20±5℃環境下,有效期6個月。
避免反覆凍融。凍融次數不超過4次。試劑開瓶後,在室溫條件下放置時間不應超過8小時。運輸採用乾冰(或者冰袋)保持低溫,運輸時間不應超過4天。
【適用儀器】abiprism7300abiprism7500,lightcycler480,da7600
【樣本要求】
1適用標本類型:血清、血漿、體液或組織。
2標本採集:
2.1血清一用一次性無菌注射器抽取受檢者靜脈血2毫升,注入無菌的乾燥試管,室溫放置血標本可自發安完全凝集析出血清,或直接使用水平離心機,1500轉離心5min:吸取上層血清,轉移至1.5ml滅菌離心管。
2.2血漿用一次性無菌注射器抽取受檢者靜脈血2毫升,注入含乙二胺四乙酸二鉀
(edta-2k)或無創基因管,立即輕輕顛倒試管混合10次,充分混勻,後即可分離出血漿,轉移至1.5ml滅菌離心管。
3標本保存和運送:所採集的標本可立即用於測試,也可以保存於-20℃,可存期為6個月。標本運送採用0℃冰壺,無創基因管的標本常溫運送。
【檢驗方法】
1dna提取(樣本製備區)
將待測樣本、陽性定量參考品、陰性質控品、chromosome強陽性臨界陽性質控品進行同步處理。
1.12次離心的方法分離血漿:4℃,1,600轉離心10min分離血漿勿觸動白膜層;4℃,16,000轉離心10min仔細吸取上清50μ1樣品,加入100μ1dna提取液i,用振蕩器劇烈振蕩混勻10秒,8000轉離心數秒。100℃恆溫處理10±1min;
1.212,000轉離心5min,備用。
2pcr試劑準備(試劑準備區)
直接使用chromosome反應混合液管。
3加樣(樣本製備區)
往上述chromosome反應管中用帶濾芯吸嘴分別加入提取後的待測樣本核酸、chromosome陰性質控品、chromosome強陽性質控品、chromosome臨界陽性質控品和陽性定量參考品的上清各5μl。蓋緊管蓋,8,000轉離心數秒後轉移至擴增檢測區。
4pcr擴增(擴增和產物分析區)
4.1abiprism7500儀器設置(7300參照此操作)
4.1.1打開「setup」窗口,按樣本對應順序設置陰性質控(ntc)、陽性質控以及未知樣本(unknow)、陽性定量參考品(standard),並在「samplename」一欄中設置樣本名稱;探針檢測模式設置為:reporterdyel:fam,quencherdyel:none;reporterdye2:vic,quencherdye2:none;passivereference:rox。
4.1.2打開instrument窗口,設置循環條件如下:94℃2min,93℃45秒→55℃60秒→10個循環,93℃40秒→55℃55秒→30個循環,保存檔,運行。
4.2lightcycler480儀器設置
4.2.1打開軟體後,選擇「newexperiment」,設置檢測模式為「multicolorhydrolysisprobe」,檢測通首為fam,vic。
4.2.2設置循環條件:
4.2.3選擇「sampleeditor」,設定樣品的名稱、類型,在「standardconcentration」框中輸入陽性定量參考品濃度,設置完成後,保存文件,運行程序。
4.3da7600儀器設置
4.3.1打開軟體後,在設置程序參數接口中,設置擴增程序和溫度設置,條件如下:
4.3.2點擊樣本參數接口,按樣本對應順序設置陰性質控(ntc)、陽性質控以及未知樣本(unk),並在「樣本名稱」一欄中設置樣本名稱:陽性定量參考品在「樣品類型」中選擇「標準」,「標準濃度」中輸入濃度。探針染料類型選擇:fam和hex。
4.3.3設置完成後,保存文件,運行程序。
5結果分析
反應結束後自動保存結果,根據分析後圖像調節baseline的start值、end值以及threshold值(使用者可根據實際情況自行調整,start值可以在end值可設在在log圖譜窗口設置threshold的value值,使基線位於擴增曲線指數期,設置陰性質控品的擴增曲線平直或低於閾值線),點擊analysis自動獲得分析結果,在report接口察看結果,記錄未知樣本數值(c)。
6質量控制
陰性質控品:全部陰性
陽性質控品:全部陽性,弱陽性質控品檢測值允許範圍1×102~5.0×102copy/ml;
陽性定量參考品:均為陽性,且0.97≤|r|≤1(correlation數值即為r)
以上要求需在同一實驗中同時滿足,否則,本次實驗無效,全部實驗應重新進行。
7結果判斷
7.1如果在fam檢測信道擴增曲線無明顯對數增長期或ct值等於30,在vic檢測信道擴增曲線有對數增長期,則判樣品的chromosomedna濃度小於檢測靈敏度。
7.2如果在fam檢測信道擴增曲線有對數增長期且ct值<30,則按以下方法判斷:
若樣品的c<100,則該樣品的chromosomedna濃度<100copy/ml;
若樣品的100≤c≤1.00×108,則該樣品的chromosomedna濃度=ccopy/ml;
若樣品的c>1.00×108,則該樣品的chromosomedna濃度>5×106copy/ml。如果需要精確定量結果,可將樣品陰性質控品稀釋到線性範圍後再檢測。則該樣品的chromosomedna濃度=(c×稀釋倍數)copy/ml。
8檢驗結果的解釋
1每次實驗均需檢測陰性質控品,chromosome強陽性質控品,chromosome臨界陽性質控品,質控品結果滿足質量控制要求時方可進行檢測結果的判定。
2陽性結果判定標準:在fam檢測信道擴增曲線有對數增長期且ct值<30。
3陰性結果判定標準:在fam檢測通首擴增曲線無明顯對數增長期或ct值等於30,在vic檢測信道擴增曲線有對數增長期。
9檢驗方法的局限性
1樣本檢測結果和樣本收集、處理、運送及保存質量有關,其中任務失誤都將會導致假陰性結果。如果樣本處理時沒有控制好交叉汙染,可能出現假陽性結果。
3臨床實驗室應嚴格按照《臨床基因擴增實驗室工作規範》配備設備及操作人員,應嚴格按照說明書要求進行操作。
4本試劑盒檢測僅限於規定的樣本類型及適用機型。
10產品性能
根據臨床試驗結果顯示,本試劑盒的靈敏度為1×102copy/ml,線性範圍為本試劑盒與對照試劑的總符合率為100%;對血清和血漿兩種類型樣本檢測結果無差異。
11注意事項
1試劑盒的內質控品等組分,雖已經通過了hiv1/2-ab、hbs-ag和hcv-ab等項止的檢測,但截止目前,沒有任務一項檢測可以確保絕對安全,故仍應將這些組份作為潛在傳染源對待。為了避免樣本中任何潛在的生物危險,檢測樣本應視為具有傳染性物質,避免接觸到皮膚和黏膜;樣本的處理建議在可防止氣霧外流的生物安全櫃中操作,樣本製備區所用過的試管、吸頭需打入盛有消毒劑的容器,並與廢棄物一起滅菌後方可丟棄;樣本操作和處理均需符合相關法規要求:衛生部《微生物生物醫學實驗室生物安全通用準則》和《醫療廢物管理條例》。
1試劑盒中組分需在效期內使用,不使用本試劑盒提供的組分進行實驗將可能導致錯誤結果。
2實驗室管理應嚴格按照pcr基因擴增實驗室的管理規範,實驗人員必進行專業培訓,實驗過程嚴格分區進行(試劑準備區、樣本製備區、擴增和產物分析區,所用的消耗品應滅菌後一次性使用,實驗操作的每個階段使用專用的儀器和設備,各區各階段用品不能交叉使用。
3使用經高壓滅菌的一次性離心管和吸頭或購買無dna酶、rna酶的離心管和吸頭。
4pcr檢測試劑使用前要完全解凍,8,000轉離心數秒後使用,但應避免反覆凍融。
5完成樣本核酸提取後,建議馬上進行下一步實驗,否則請保存於—20℃待用(24h內)。
6如果在標本處理中沒有控制好交叉汙染,可能出現假陽性。
7對每次實驗進行質量控制。
8實驗完畢用10%次氯酸或75%酒精處理工作檯和移液器,然後用紫外線燈照射30min。
11本試劑盒內的陽性質控品和檢測樣本均應視為具有傳染性物質,因此標本操作和處理均需符合相關法規要求:衛生部《微生物生物醫學實驗室生物安全通用準則》和《醫療廢物管理條例》。
以上內容僅為優選下的實施例方案,不因此而限制本發明的保護範圍,凡是利用本發明說明書內容所作的等效結構變換,或直接或間接運用附屬在其他相關產品的技術領域,均同理包括在本發明的專利保護範圍內。
sequencelisting
胡松
一種染色體基因引物對和探針組合以及染色體核酸檢測試劑盒
3
patentinversion3.3
1
22
dna
人工序列
1
acgcggctggtggatcagtgct22
2
20
dna
人工序列
2
ttatgagcgcgaagcaaacg20
3
19
dna
人工序列
3
ccgtgggtggtctttaccg19
