一種用於可見光降解水中抗生素的磁性複合材料的製作方法
2023-05-09 19:59:26 2
本發明屬於水處理領域,具體涉及一種用於可見光降解水中抗生素的磁性複合材料及其製備方法與應用。
背景技術:
抗生素是由生物(包括微生物和高等動植物)在生活過程中所生產的具有抗病原體或其它活性的一類次級代謝產物,是能干擾其他生活細胞發育功能的有機物質。抗生素因被人類發現了其巨大功能,如抑制和殺滅細菌、黴菌、支原體等其他致病微生物,而開始被廣泛地研究和應用。目前,抗生素不僅被用來治療人類臨床的各種疾病,如殺菌、消炎;而且也在畜牧業醫療救治中發揮了巨大的作用,如作為動物飼料添加劑和動物生長促進劑。但是,由於抗生素類藥物具有穩定性、持久性等特點,以及其本身對細菌有較強的抑制作用,難於通過自然生物降解去除,容易產生積累,排放到環境中的抗生素有的會隨著水進入土壤和沉積物中。抗生素過量積累會導致微生物抗藥基因的產生,即使是在微量水平上的抗生素長期暴露,也會對生態環境和人體健康造成危害,與此同時,含抗生素的廢水大量排放,會導致水體環境受到嚴重危害。
在各種環境淨化方法中,光催化技術具有可以直接利用太陽光、在常溫下反應、無二次汙染等優點備受關注。近年來,AgBr分散在於Ag3PO4表面形成複合物AgBr-Ag3PO4光催化材料引起了大家的廣泛關注,Ag3PO4的導帶和價帶電勢低於AgBr導帶和價帶的電勢,有利於光生電子和空穴對的有效分離,使得該類光催化材料對可見光具有很好的響應。
為了實現光催化材料的回收利用,研究人員將光催化材料與磁性納米粒子(磁基體)結合製備磁性光催化材料,使其在保持較高的催化活性下,又具有一定的磁性,實現在外加磁場作用下的簡單分離。而對於磁性光催化材料的研究通常是將具有光催化活性的組分分散於Fe3O4、Fe2O3及各種鐵氧體(MFe2O4,其中M=Zn、Co、Ni、Ba、Sr等)上,但是這些磁基體的比表面積較小,因而所能結合的活性組分的量受到限制,磁基體表面的光催化活性組分也較易發生團聚,同時由於這些磁基體對水中的有機汙染物的親和力較弱,使得當有機汙染物濃度較低時,活性組分與有機汙染物的碰撞頻率較低,限制了光催化反應的速率。因此,需要尋求一種更優異的磁基體用於製備磁性光催化材料,該類磁基體必須擁有發達的孔隙及較大的比表面積。
MIL-101(Cr)是由鉻金屬離子和有機配體對苯二甲酸組裝而成的一種金屬有機骨架材料,其不僅擁有較大的比表面積、孔徑尺寸和孔體積,同時也對可見光具有一定的響應,並且該材料在水相中具有非比尋常的穩定性,使得其在水相中的應用及發展擁有巨大的潛力。因此若能獲得磁性Fe3O4@MIL-101(Cr)材料,便可以滿足上述對磁基體的要求。然而磁性Fe3O4@MIL-101(Cr)材料的製備面臨著巨大的挑戰,這主要是由於傳統的MIL-101(Cr)是以氫氟酸作為礦化劑,在220℃、pH<2條件下合成的,而HF具有強的腐蝕性,將會對添加的Fe3O4形成破壞。
技術實現要素:
為了解決上述存在的難題,本發明的目的在於提供一種用於可見光降解水中抗生素的磁性複合材料及其製備方法與應用。本發明製備方法簡單,所得磁性複合材料兼具磁性納米粒子的磁特性及優異的可見光催化降解汙染物的能力,可作為光催化材料應用於水相中抗生素的光降解去除,並可採用外加磁場實現光催化材料的簡單回收再利用。
為實現上述目的,本發明採用如下技術方案:
一種用於可見光降解水中抗生素的磁性複合材料,其為Fe3O4@MIL-101(Cr)@AgBr-Ag3PO4。
所述磁性複合材料是先採用巰基乙酸對Fe3O4磁性納米粒子進行改性,然後將改性的Fe3O4磁性納米粒子加入到MIL-101(Cr)前驅體溶液中,得到磁性Fe3O4@MIL-101(Cr),再在避光條件下,將所得磁性Fe3O4@MIL-101(Cr)與硝酸銀、磷酸二氫鉀、十六烷基三甲基溴化銨進行共沉澱反應,使AgBr、Ag3PO4共同負載在磁性Fe3O4@MIL-101(Cr)上製備而成;其製備具體步驟如下:
(1)改性Fe3O4磁性納米粒子的製備
將2.5 mmol氯化鐵溶解於40 mL乙二醇中形成清液,然後加入1.8 g無水乙酸鈉、0.5 g聚乙二醇,攪拌溶解後轉移至高壓反應釜中,於200℃下反應8 h,利用磁鐵分離反應產物並用無水乙醇和去離子水交替洗滌3~6次,60℃下真空乾燥6~8 h,製得Fe3O4磁性納米粒子;將1.25 g所得Fe3O4磁性納米粒子加入到250 mL濃度為0.29 mmol/L的巰基乙酸乙醇溶液中攪拌24 h,產物採用磁鐵分離並用去離子水和無水乙醇交替洗滌3~6次,60℃下真空乾燥8~10 h,即得到巰基乙酸改性的Fe3O4磁性納米粒子;
(2)磁性Fe3O4@MIL-101(Cr)的製備
將5 mmol硝酸鉻、5 mmol對苯二甲酸溶於25 mL去離子水中,然後加入1.29 mmol四甲基氫氧化銨,攪拌溶解20 min,再加入0.12~1.2 g步驟(1)得到的巰基乙酸改性的Fe3O4磁性納米粒子進行超聲混合,將混合物移入高壓反應釜中,在180℃下反應18~24 h,產物利用磁鐵進行分離,然後依次用N,N-二甲基甲醯胺、無水乙醇和去離子水分別於110℃、60℃、80℃回流純化產物,再於100℃下真空乾燥18~24 h,即獲得磁性Fe3O4@MIL-101(Cr);
(3)Fe3O4@MIL-101(Cr)@AgBr-Ag3PO4磁性複合材料的製備
將0.4 g步驟(2)所得磁性Fe3O4@MIL-101(Cr)溶於蒸餾水中並通過超聲使其分散均勻,加入1.85~5.55 mmol硝酸銀,在避光條件下攪拌1 h,然後逐滴加入0.46~1.39 mmol磷酸二氫鉀,於避光條件下繼續混合攪拌3 h,最後逐滴加入十六烷基三甲基溴化銨0.27~0.84 mmol,於避光條件下繼續攪拌3 h,反應產物分別用去離子水、無水乙醇交替洗滌3~6次,經磁鐵分離後於60℃下乾燥12 h,即獲得Fe3O4@MIL-101(Cr)@AgBr-Ag3PO4磁性複合材料。
所述磁性複合材料兼具磁性納米粒子的磁特性及優異的可見光催化降解汙染物的能力,可用於可見光催化降解水中抗生素。
本發明的優點及技術效果在於:
本發明首先採用溶劑熱法合成Fe3O4納米粒子並利用巰基乙酸對其表面進行改性,然後將改性的Fe3O4磁性納米粒子添加到鹼性MIL-101(Cr)前驅體溶液中,通過簡單的水熱法原位製備磁性金屬有機骨架材料Fe3O4@MIL-101(Cr),再採用共沉澱法將AgBr-Ag3PO4分散於Fe3O4@MIL-101(Cr)上,得到具有可見光響應的磁性光催化複合材料Fe3O4@MIL-101(Cr)@AgBr-Ag3PO4。該複合材料兼具磁性納米粒子的磁特性及優異的可見光催化降解汙染物的能力,在降解水中抗生素後可採用外加磁場實現光催化材料的簡單回收再利用。
附圖說明
圖1為Fe3O4、MIL-101(Cr)、Fe3O4@MIL-101(Cr)和Fe3O4@MIL-101(Cr)@AgBr-Ag3PO4和AgBr-Ag3PO4的XRD圖。
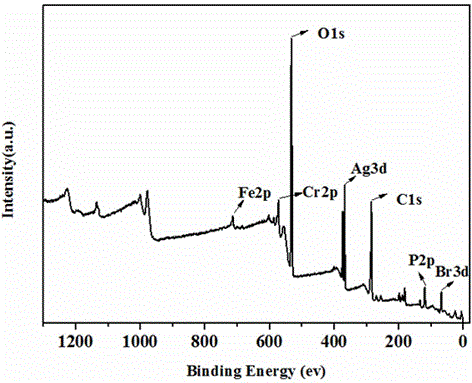
圖2為Fe3O4@MIL-101(Cr)@AgBr-Ag3PO4的XPS圖。
圖3為Fe3O4@MIL-101(Cr)@AgBr-Ag3PO4的TEM圖。
圖4為Fe3O4、AgBr-Ag3PO4和Fe3O4@MIL-101(Cr)@AgBr-Ag3PO4的UV-Vis DRS圖。
圖5為Fe3O4@MIL-101(Cr)@AgBr-Ag3PO4的磁滯回曲線圖(A)和磁分離效果圖(B)。
圖6為Fe3O4@MIL-101(Cr)@AgBr-Ag3PO4在不同pH下對土黴素的降解效果圖。
圖7為Fe3O4@MIL-101(Cr)@AgBr-Ag3PO4在不同pH下對氧氟沙星的降解效果圖。
圖8為Fe3O4@MIL-101(Cr)@AgBr-Ag3PO4對土黴素降解效果的高效液相色譜圖。
圖9為Fe3O4@MIL-101(Cr)@AgBr-Ag3PO4對氧氟沙星降解效果的高效液相色譜圖。
具體實施方式
為了使本發明所述的內容更加便於理解,下面結合具體實施方式對本發明所述的技術方案做進一步的說明,但是本發明不僅限於此。
實施例1:磁性複合材料Fe3O4@MIL-101(Cr)@AgBr-Ag3PO4的製備,包括如下步驟:
(1)改性Fe3O4磁性納米粒子的製備
將0.675 g氯化鐵(Fe3Cl3·6H2O)溶解於40 mL乙二醇中形成清液,然後加入1.8 g無水乙酸鈉、0.5 g聚乙二醇,攪拌溶解後轉移至高壓反應釜中,於200℃下反應8 h,利用磁鐵分離反應產物並用無水乙醇和去離子水交替洗滌5次,60℃下真空乾燥8 h,製得Fe3O4磁性納米粒子;將1.25 g Fe3O4磁性納米粒子加入到250 mL濃度為0.29 mmol/L的巰基乙酸乙醇溶液中攪拌24h,產物採用磁鐵分離並用去離子水和無水乙醇交替洗滌3次,60℃下真空乾燥8 h,即得到巰基乙酸改性的Fe3O4磁性納米粒子;
(2)磁性Fe3O4@MIL-101(Cr)的製備
將2.0 g硝酸鉻(Cr(NO3)3·9H2O)、0.832 g對苯二甲酸(H2BDC)溶於25 mL去離子水中,然後加入1.29 mmol四甲基氫氧化銨(TMAOH),攪拌溶解20 min,再加入0.232 g步驟(1)得到的巰基乙酸改性的Fe3O4磁性納米粒子進行超聲混合,將混合物移入高壓反應釜中,在180℃下反應24 h,產物利用磁鐵進行分離,然後依次用N,N-二甲基甲醯胺、無水乙醇和去離子水分別於110℃、60℃、80℃回流純化產物,再於100℃下真空乾燥24 h,即獲得磁性Fe3O4@MIL-101(Cr);
(3)Fe3O4@MIL-101(Cr)@AgBr-Ag3PO4 磁性複合材料的製備
將0.4 g步驟(2)所得磁性Fe3O4@MIL-101(Cr)溶於20 mL蒸餾水中並通過超聲使其分散均勻,加入0.6296 g硝酸銀(AgNO3),在避光條件下攪拌1 h,然後逐滴加入25 mL濃度為37 mmoL/L磷酸二氫鉀溶液,於避光條件下繼續混合攪拌3 h,最後逐滴加入40 mL濃度為13.875 mmoL/L的十六烷基三甲基溴化銨(CTAB)溶液,於避光條件下繼續攪拌3 h,反應產物分別用去離子水、無水乙醇交替洗滌6次,經磁鐵分離後於60℃下乾燥12 h,即獲得Fe3O4@MIL-101(Cr)@AgBr-Ag3PO4磁性複合材料。
實施例2:MIL-101(Cr)材料的製備
其製備方法同實施例1步驟(2)所述,但不加入Fe3O4磁性納米粒子。
圖1為Fe3O4、MIL-101(Cr)、Fe3O4@MIL-101(Cr)和Fe3O4@MIL-101(Cr)@AgBr-Ag3PO4和AgBr-Ag3PO4的XRD圖。由圖1可知,所製備的Fe3O4@MIL-101(Cr)的XRD圖譜上兼具Fe3O4和MIL-101(Cr)的特徵峰,說明在鹼性條件下成功合成了Fe3O4@MIL-101(Cr)材料,水熱過程不會造成Fe3O4晶體的破壞;而Fe3O4@MIL-101(Cr)@AgBr-Ag3PO4的XRD圖譜上具有Fe3O4、MIL-101(Cr)和AgBr-Ag3PO4三種成分的特徵峰,說明Fe3O4@MIL-101(Cr)@AgBr-Ag3PO4複合材料由這三種材料組成,AgBr-Ag3PO4的負載過程並未引起金屬有機骨架結構的變化。
圖2為Fe3O4@MIL-101(Cr)@AgBr-Ag3PO4的XPS圖。由圖2可以看出,所製備的Fe3O4@MIL-101(Cr)@AgBr-Ag3PO4的X射線光電子能譜(XPS)能檢測到Fe、Cr、O、Ag、C、P和Br等元素。
圖3為Fe3O4@MIL-101(Cr)@AgBr-Ag3PO4的TEM圖。由圖3可以看出,尺寸為300 nm左右的Fe3O4磁性粒子包裹在材料中心,MIL-101(Cr)均勻的生長在其外,AgBr-Ag3PO4分散負載於MIL-101(Cr)上。
圖4為Fe3O4、AgBr-Ag3PO4和Fe3O4@MIL-101(Cr)@AgBr-Ag3PO4的UV-Vis DRS圖。由圖4可以看出,所製備的Fe3O4@MIL-101(Cr)@AgBr-Ag3PO4的可見光響應範圍明顯得到拓寬。
圖5為Fe3O4@MIL-101(Cr)@AgBr-Ag3PO4的磁滯回曲線圖(A)和磁分離效果圖(B)。由圖5(A)可以看出,所製備的Fe3O4@MIL-101(Cr)@AgBr-Ag3PO4顯示了明顯的磁滯回特性;由圖5(B)可以看出,所製備的Fe3O4@MIL-101(Cr)@AgBr-Ag3PO4可均勻分散於水相中,而通過外加磁鐵處理可實現其與水相的分離。
實施例3:不同pH對磁性複合材料催化降解土黴素效果的影響
(1)取100 mL濃度為30 mg/L的土黴素溶液置於燒杯中,分別用0.1 mol/L的NaOH和HCl調節土黴素溶液的pH,使其pH值分別為3、5、7和9。加入100 mg實施例1中製備的磁性複合材料,在黑暗條件下攪拌反應12 h,使其達到吸附平衡,然後將溶液置於氙燈下,打開氙燈(300 W,濾光片波長大於400 nm),在室溫下照射反應30 min,每隔一定時間取樣3 mL,樣品經離心後取上清液經0.45 μm濾膜過濾後於液相色譜儀中分析測定其濃度。
(2)測定條件:色譜柱:Agilent C18反向色譜柱(250 mm×4.5 mm I.d.,5 μm)。檢測波長355 nm,柱溫為30℃。流動相為乙腈:水=80:20(其中水的pH=2)。流動相流速為1.0 mL/min,進樣量為20 μL,保留時間為10 min。
圖6為Fe3O4@MIL-101(Cr)@AgBr-Ag3PO4在不同pH下對土黴素的降解效果圖。由圖6可知,在酸性條件下(pH=3、5),土黴素的降解效率得到抑制,而在中性和鹼性的環境中,Fe3O4@MIL-101(Cr)@AgBr-Ag3PO4對土黴素能夠發揮最好的降解效率。
實施例4:不同pH對磁性複合材料催化降解氧氟沙星效果的影響
(1)取100 mL濃度為30 mg/L的氧氟沙星溶液置於燒杯中,分別用0.1 mol/L的NaOH和HCl調節氧氟沙星溶液的pH,使其pH值分別為3、5、7和9。加入100 mg實施例1中製備的磁性複合材料,在黑暗條件下攪拌反應12 h,使其達到吸附平衡,然後將溶液置於氙燈下,打開氙燈(300 W,濾光片波長大於400 nm),在室溫下照射反應30 min,每隔一定時間取樣3 mL,樣品經離心後取上清液經0.45 μm濾膜過濾後於液相色譜儀中分析測定其濃度。
(2)測定條件:色譜柱:Agilent C18反向色譜柱(250 mm×4.5 mm I.d.,5 μm)。檢測波長290 nm,柱溫為25℃。流動相為乙腈:水=15:85(其中磷酸的體積為水的1%)。流動相流速為1.5 mL/min,進樣量為20 μL,保留時間為6 min。
圖7為Fe3O4@MIL-101(Cr)@AgBr-Ag3PO4在不同pH下對氧氟沙星的降解效果圖。由圖7可知,在酸性條件下(pH=3、5),氧氟沙星的降解效率得到抑制,而在中性和鹼性的環境中,e3O4@MIL-101(Cr)@AgBr-Ag3PO4對氧氟沙星能夠發揮最好的降解效率。
實施例5:Fe3O4@MIL-101(Cr)@AgBr-Ag3PO4對土黴素的降解試驗
(1)取100 mL濃度為30 mg/L的土黴素溶液置於燒杯中,將其pH調節至7~9,然後加入100 mg實施例1中製備的磁性複合材料,在黑暗條件下攪拌反應12 h,使其達到吸附平衡,然後將溶液置於氙燈下,打開氙燈(300 W,濾光片波長大於400 nm),在室溫下照射反應30 min,每隔一定時間取樣3 mL,樣品經離心後取上清液經0.45 μm濾膜過濾後於液相色譜儀中分析測定其濃度。
(2)測定條件:色譜柱:Agilent C18反向色譜柱(250 mm×4.5 mm I.d.,5 μm)。檢測波長355 nm,柱溫為30℃。流動相為乙腈:水=80:20(其中水的pH=2)。流動相流速為1.0 mL/min,進樣量為20 μL,保留時間為10 min。
圖8為Fe3O4@MIL-101(Cr)@AgBr-Ag3PO4降解土黴素效果的高效液相色譜圖。由圖8可以看出,經過30 min分鐘的可見光降解,在出峰時間t=2.5 min的特徵峰已經非常小,說明土黴素幾乎完全降解,降解率高達97.0%。
實施例6:Fe3O4@MIL-101(Cr)@AgBr-Ag3PO4對氧氟沙星的降解試驗
(1)取100 mL濃度為20 mg/L的氧氟沙星溶液置於燒杯中,將其pH調節至7~9,然後加入100 mg實施例1中製備的磁性複合材料,在黑暗條件下攪拌反應12 h,使其達到吸附平衡,然後將溶液置於氙燈下,打開氙燈(300 W,濾光片波長大於400 nm),在室溫下照射反應40 min,每隔一定時間取樣3 mL,樣品經離心後取上清液再經0.45 μm濾膜過濾後於液相色譜儀中分析測定其濃度。
(2)測定條件:色譜柱:Agilent C18反向色譜柱(250 mm×4.5 mm I.d.,5 μm)。檢測波長290 nm,柱溫為25℃。流動相為乙腈:水=15:85(其中磷酸的體積為水的1%)。流動相流速為1.5 mL/min,進樣量為20 μL,保留時間為6 min。
圖9為Fe3O4@MIL-101(Cr)@AgBr-Ag3PO4對氧氟沙星降解效果的高效液相色譜圖。由圖9可以看出,經過40 min分鐘的可見光降解,在出峰時間t=4.1 min的特徵峰已經非常小,說明氧氟沙星幾乎完全降解,降解率高達98.1%。
以上所述僅為本發明的較佳實施例,凡依本發明申請專利範圍所做的均等變化與修飾,皆應屬本發明的涵蓋範圍。
