miR‑10b在體外促進間充質幹細胞分化為成骨細胞和抑制其分化為成脂細胞的用途的製作方法
2023-05-28 19:17:18 1
本發明涉及再生醫學的領域,具體而言本發明涉及miR-10b在體外促進間充質幹細胞分化為成骨細胞和在體外抑制間充質幹細胞分化為成脂細胞中的用途。
背景技術:
間充質幹細胞(MSC)具有自我更新和多譜系分化潛能,在一定的誘導條件下能夠分化為成骨細胞、軟骨細胞、脂肪細胞、肌肉細胞和內皮細胞等[1-3]。成骨細胞和脂肪細胞起源於MSC,MSC向成脂細胞分化和成骨細胞分化是機體普遍存在的兩種重要的生理過程,參與了多種組織代謝與平衡的維持[4]。MSC向成脂分化和成骨分化的平衡失調,會引起多種疾病的發生,如骨質疏鬆症、肥胖症、動脈粥樣硬化等,揭示MSC向成脂和成骨分化平衡的調控機制對上述脂肪和骨分化失衡相關疾病的治療具有重要的指導意義。
microRNA(miRNA)是一類長22nt左右的非編碼單鏈RNA的總稱,能夠識別特定的靶標mRNA,使之降解或抑制其蛋白質合成,從而發揮調控基因表達的作用[5,6]。miRNA具有靶基因調控的廣泛性和功能的多效性,一個miRNA可調控數百個不同的靶基因,單個編碼基因的表達也可能受多個miRNA的調控[7]。越來越多的證據表明miRNA能夠調控細胞分化和命運決定[8]。據報導,miR-2861、miR-3960、miR-196a、miR-29b、miR-335-5p和miR-216a等可以增強MSC的成骨分化[9-12],而miR-26a、miR-133、miR-135、miR-141、miR-200a和miR-23a等具有抑制成骨分化的作用[13-16]。miR-143、miR-24、miR-31、miR-30c和miR-642a-3p等則被報導可以調控MSC的脂肪生成[17-20],少數miRNA被發現參與了MSC成骨和成脂分化平衡的調控,例如miR-204、miR-637、miR-22、miR-17-5p、miR-106a和let-7等[21-26]。這些研究結果提示,miRNA在MSC的成骨和成脂分化調控中可能扮演非常重要的角色。
技術實現要素:
一方面,本發明提供了一種體外誘導間充質幹細胞分化為成骨細胞的方法,所述方法包括以下步驟:
i)在適合脂肪源間充質幹細胞生長的培養基中培養所述脂肪源間充質幹細胞;
ii)向步驟i)的所述脂肪源間充質幹細胞內轉染miR-10b後,繼續培養24小時;
iii)在步驟ii)中培養的間充質幹細胞至亞融合狀態時,向培養基中添加10%FBS、10nM地塞米松、0.2mM抗壞血酸和10mMβ-甘油磷酸鈉;
iv)繼續培養0~12天後,收集並鑑定獲得的成骨細胞。
根據本發明所述的方法,其中所述miR-10b促進間充質幹細胞向成骨分化,抑制其向成脂分化。
根據本發明所述的方法,其中所述間充質幹細胞是脂肪源間充質幹細胞;優選地,所述間充質幹細胞是成人脂肪源間充質幹細胞。
根據本發明所述的方法,其中miR-10b的轉染濃度為10~200nmol/L。
根據本發明所述的方法,其中miR-10b的序列如SEQ ID No.1所示。SEQ ID No.1為UACCCUGUAGAACCGAAUUUGUG,其登錄號為miRbase Accession number MIMAT0000254。
根據本發明所述的方法,其中用Lipofectamine 2000將miR-10b轉染至間充質幹細胞,但不限於Lipofectamine 2000。
另一方面,本發明還提供了miR-10b在製備用於體外促進間充質幹細胞分化為成骨細胞和抑制所述間充質幹細胞分化為脂肪細胞試劑中的用途。
根據本發明的用途,其中所述間充質幹細胞是脂肪源間充質幹細胞;優選地,所述間充質幹細胞是成人脂肪源間充質幹細胞。
附圖說明
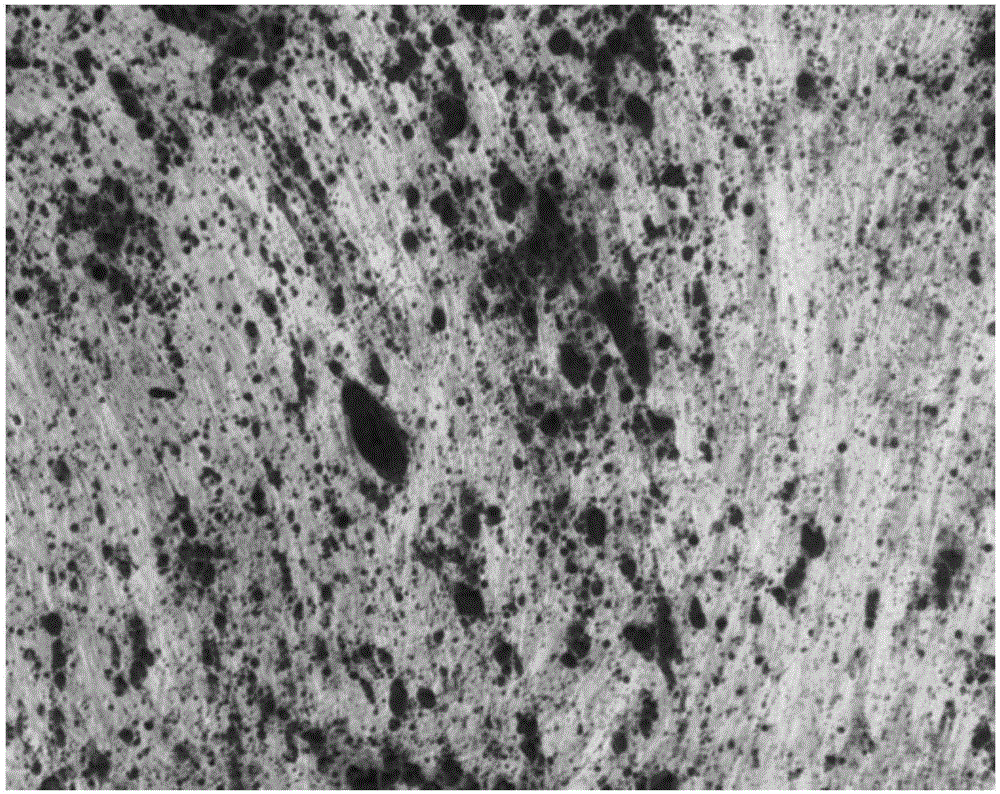
圖1:MSC經成骨誘導培養基誘導3天的ALP染色。
圖2:MSC經成骨誘導培養基誘導12天的茜素紅染色。
圖3A:MSC轉染NC對照後,經成骨誘導培養基誘導3天的ALP染色。
圖3B:MSC轉染miR-10b後,經成骨誘導培養基誘導3天的ALP染色。
圖4A:MSC轉染NC對照後,經成骨誘導培養基誘導12天的茜素紅染色。
圖4B:MSC轉染miR-10b後,經成骨誘導培養基誘導12天的茜素紅染色。
圖5:成骨誘導後細胞的鹼性磷酸酶活性。NC:轉染NC的、經過成骨誘導的細胞;miR-10b:轉染有miR-10b的、經過成骨誘導的細胞。
圖6:MSC經成脂誘導培養基誘導10天的油紅O染色。
圖7A:MSC轉染NC對照後,經成脂誘導培養基誘導10天的細胞的油紅O染色。
圖7B:MSC轉染miR-10b後,經成脂誘導培養基誘導10天的細胞的油紅O染色。
圖8:成脂誘導後油紅O萃取定量分析。NC:轉染有NC對照的、經過成脂誘導的細胞;miR-10b:轉染有miR-10b的、經過成脂誘導的細胞。
具體實施方式
以下提供了本發明實施方式中所使用的具體材料及其來源。但是,應當理解的是,這些僅僅是示例性的,並不意圖限制本發明,與如下組織、細胞、試劑和儀器的類型、型號、品質、性質或功能相同或相似的材料均可以用於實施本發明。
實施例1:成人脂肪源間充質幹細胞(hADSCs)的分離和鑑定
1.成人脂肪組織取自吸脂手術患者(中國醫學科學院整形醫院),因取材不對患者造成額外傷害,亦不洩露患者的個人信息,已經由中國醫學科學院基礎醫學研究所倫理委員會批准免除知情同意。捐獻者均為25~35歲的健康女性。
2.從脂肪組織中分離hADSCs的方法簡述如下:
吸脂術採集出來的脂肪組織用D-Hanks洗去血細胞和麻醉藥,0.2g/100ml膠原酶P(購自:美國Life Technologies公司)消化1h,之後用D-Hanks洗滌2遍以除去膠原酶。
離心收集細胞,細胞以2×106/ml的密度接種於含58%(v/v)DMEM/F12+40%(v/v)MCDB-201、2%(v/v)胎牛血清、10ng/ml EGF、10ng/ml PDGF、1×胰島素-轉鐵蛋白-亞硒酸(ITS)、l×亞油酸-牛血清白蛋白、50μMβ-巰基乙醇、2mM L-穀氨醯胺、l00μg/m1青黴素和100U/ml硫酸鏈黴素的幹細胞培養液,37℃、5%CO2、95%溼度的培養箱培養。
兩天後換液,棄去未貼壁的細胞,以後每3天半量換液。
當細胞達70%~80%匯合度時,0.25g/100ml胰酶(Gibco)常規消化,細胞按照l:3進行傳代。
3.hADSCs的表型:
收集第三代細胞,PBS洗3次;
加0.1%皂素室溫破膜1h,PBA洗3次(若檢測細胞內抗原,則進行本步驟;若檢測細胞表面抗原,則直接進行下一步);
加一抗(CD29、CD44、CD105、CD31、CD34、CD106、HLA-DR、FLK-1單抗,購自:BD公司),4℃孵育30min;
加PBS洗3次,加FITC標記二抗(兔抗鼠,購自中杉金橋生物技術有限公司),4℃孵育30min;
加PBS洗3次,4%多聚甲醛固定,300μl PBS重懸;
流式細胞儀Accuri C6(BD)檢測細胞。經鑑定,細胞呈現典型的hADSCs表型:CD29+、CD44+、CD105+、FLK-1+;CD31-、CD34-、CD106-、HLA-DR-。
實施例2:miRNA的轉染
1.試劑:
(1)轉染試劑為Lipofectamine 2000(Invitrogen);
(2)待轉染的miRNA:
miR-10b模擬物為美國Life Technologies公司合成;
採用公知技術合成與miR-10b長度相似的無關RNA對照(SEQ ID No.2:正義:5』-UUCUCCGAACGUGUCACGUTT-3』,反義:5』-ACGUGACACGUUCGGAGAATT-3』)作為陰性對照(negative control,NC)。
2.待轉染的miRNA儲備液配置:
將裝有待轉染的miRNA的管低速離心5min,按照Lipofectamine2000(Invitrogen)說明書加入Opti-MEM溶解miRNA,震蕩並瞬時離心配成20μM的儲備液。
3.細胞準備:
取第3代對數生長期、70%~80%匯合的hADSCs進行轉染。
4.轉染過程:
用Opti-MEM分別稀釋待轉染的miRNA和Lipofectamine 2000,輕輕混勻後室溫放置5min;
將Lipofectamine 2000稀釋液緩慢逐滴加入待轉染的miRNA稀釋液中,輕輕混勻獲得miRNA和Lipofectamine 2000混合液,室溫孵育20min;
從培養箱取出待轉染細胞,吸出培養液,用DPBS液洗3遍,吸淨洗液後每孔加入1.5ml Opti-MEM;
將孵育好的miRNA-Lipofectamine 2000混合液緩慢逐滴加入培養皿中。轉染量:miRNA終濃度為10~200nmol/L,輕搖混勻後放培養箱繼續培養;
轉染6h後,去除轉染工作液,用DPBS洗3遍;
更換幹細胞培養液,24h後,去除幹細胞培養基,用DPBS洗3遍,隨後可更換成骨或成脂誘導培養基。
實施例3:hADSCs向成骨誘導分化
分別取第3代的hADSCs(未經轉染)、實施例2所獲得的細胞(轉染有miR-10b、或轉染有NC對照)以2×104細胞/cm2的密度接種於T25培養瓶,貼壁過夜後,觀察細胞達70%~80%匯合後,更換成骨誘導培養基(H-DMEM培養基中加入10%FBS、10nM地塞米松、0.2mM抗壞血酸和10mMβ-甘油磷酸鈉)繼續培養,每隔兩天半量換液一次。
分別於誘導後的第0、3、6、9天取樣,用qRT-PCR和western blot檢測成骨表型標誌基因在mRNA和蛋白水平的表達變化。
分別於誘導後3天和12天時,用鹼性磷酸酶染色和茜素紅染色鑑定鈣化情況。
實施例4:hADSCs向成骨分化的鑑定
1.鹼性磷酸酶染色
1.1實驗原理:細胞內鹼性磷酸酶在pH 9.4~9.6條件下水解磷酸萘酚AS-MX產生萘酚,後者被重氮鹽捕獲,生成不溶性藍色沉澱。
1.2操作步驟:
使用天津血液學研究所鹼性磷酸酶染色試劑盒進行鹼性磷酸酶染色。
向成骨誘導的培養皿中滴加數滴1號液,室溫固定1min,流水漂洗2min;
取2號儲備液10ml,加3號液200μl,再加4號粉劑10mg,振搖速溶,用濾紙立即過濾,濾液即工作液:
滴加工作液數滴,置溼盒內於37℃孵育2h,流水衝洗2min;
甘油封片,顯微鏡下觀察照相。
2.茜素紅染色
2.1實驗原理:茜素紅可與鈣離子以螯合方式形成複合物。用來識別組織細胞的鈣鹽成分。通過茜素紅染色,產生桔紅色沉積(即鈣結節),在細胞外基質中被染成橘紅色。細胞本身被染成粉紅色。鈣鹽變化是骨細胞增殖分化和骨組織成骨潛能的標誌之一。
2.2操作步驟:
培養皿用PBS衝洗2次,95%乙醇固定10min,去離子水衝洗3次;
0.1%茜素紅S(Tris-HCl,pH 8.3)37℃孵育30min;
蒸餾水衝洗;
甘油封片,顯微鏡下觀察照相。
3.鹼性磷酸酶(ALP)活性測定
3.1實驗原理:ALP與底物pNPP反應,生成黃色物質,通過測定405nm處的吸光度可以反應ALP活性。
3.2操作步驟:
培養細胞去除培養基,冷PBS洗2遍,加適量蛋白裂解液(RIPA裂解液(中),碧雲天生物技術研究所),冰上裂解30min,收集細胞裂解液;
12000rpm在4℃離心15min;
取5μl細胞裂解液,加入96孔酶標板;
加200μl的鹼性磷酸酶底物pNPP(sigma公司);
37℃孵育30min;
405nm檢測吸光值;
計算ALP活性,ALP的活性以細胞裂解液的總蛋白濃度為標準化。
實施例5:hADSCs向成脂誘導分化
分別取第3代的hADSCs(未經轉染)、實施例2所獲得的細胞(轉染有miR-10b、或轉染有NC對照)以2×104細胞/cm2的密度接種於T25培養瓶,貼壁過夜後,觀察細胞達80%~90%匯合後,更換成脂誘導培養基(H-DMEM培養基中加入10%FBS、10μM地塞米松、50μg/ml抗壞血酸和100μg/ml 1-甲基-3-異丁基-黃嘌呤)繼續培養,每隔兩天半量換液一次。
分別於誘導後的第0、3、6、9天取樣,用qRT-PCR和western blot檢測成脂表型標誌基因在mRNA和蛋白水平的表達變化。
於誘導後10天時,用油紅O染色測定脂滴的產生。
實施例6:hADSCs向成脂誘導分化的鑑定
1.油紅 2染色#
1.1實驗原理:脂肪主要存積於脂肪組織中,並以油滴狀的微粒存在脂肪細胞漿內,脂肪被油紅O染色,染料被脂肪溶解吸附而呈現染料的顏色。利用染料易溶於脂質的特性證明組織脂質含量的多少。
1.2操作步驟:
油紅O原液的配製:用異丙醇配成1mg/ml,避光可長期保存;
工作液的配製:60%的油紅O原液加40%去離子水,顛倒混勻,室溫靜置30min後過濾,現配現用。
1.3染色步驟:
培養皿用D-Hanks洗2次,用中性甲醛室溫固定10min;
蒸餾水衝洗2次,每孔加適量油紅O工作液,室溫染色1h;
蒸餾水衝洗;
顯微鏡下觀察並拍照。
結果:
1.hADSCs(未經轉染)經過成骨誘導培養基的誘導,3天後ALP染色呈陽性(圖1),12天後出現茜素紅染色陽性的鈣結節(圖2)。該結果表明,hADSCs在成骨誘導培養條件下,具有成骨分化的能力。
2.miR-10b促進hADSCs成骨分化
(1)圖3為ALP染色的結果(圖3A為NC對照組、圖3B為miR-10b組)。具體而言,從圖3A中可見,僅有較少比例的細胞呈ALP染色陽性,圖3B顯示大部分細胞呈ALP染色陽性。這種差異表明miR-10b與NC相比,可以促進hADSCs成骨分化。
(2)圖4為茜素紅染色的結果(圖4A為NC對照組、圖4B為miR-10b組)。具體而言,從圖4A中可見,少部分細胞呈茜素紅染色陽性,圖4B顯示大部分細胞呈茜素紅染色陽性。這種結果再次證明miR-10b可以促進hADSCs的成骨分化。
(3)經過成骨誘導後,轉染有miR-10b的hADSCs ALP活性明顯高於轉染有NC對照的經過相同時間成骨誘導的hADSCs(圖5)。這一結果表明miR-10b與NC相比,可以促進hADSCs成骨分化。
以上結果證實,轉染miR-10b後,hADSCs的成骨能力增加。
3.hADSCs(未經轉染)經過成脂誘導培養基的誘導,10天後油紅O染色呈陽性(圖6)。該結果表明,hADSCs在成脂誘導培養條件下,具有成脂分化的能力。
4.miR-10b抑制hADSCs成脂分化
(1)圖7為油紅O染色的結果(圖7A為NC對照組、圖7B為miR-10b組)。具體而言,圖7A中的被染上橘紅色脂滴的細胞數明顯多於圖7B中的被染上橘紅色脂滴的細胞數。這種差異表明miR-10b與NC相比,可以抑制hADSCs成脂分化。
(2)經過成脂誘導後,轉染有miR-10b的hADSCs油紅O萃取活性明顯低於轉染有NC對照的經過相同時間成脂誘導的hADSCs(圖8)。這一結果表明miR-10b與NC相比,可以抑制hADSCs成脂分化。
以上結果證實,轉染miR-10b後,hADSCs的成脂能力減弱。
綜上結果證實,miR-10b具有促進hADSCs成骨分化而抑制其成脂分化的作用。
參考文獻:
1.Friedenstein,A.J.,Chailakhyan R.K.,Gerasimov U.V.,Bone marrow osteogenic stem cells:in vitro cultivation and transplantation in diffusion chambers.Cell and tissue kinetics,1987.20(3):p.263-272.
2.Grigoriadis,A.E.,Heersche,J.N.M.,Aubin,J.E.Differentiation of muscle,fat,cartilage,and bone from progenitor cells present in a bone-derived clonal cell population effect of dexamethasone.Journal of cell biology,1988.106(6):p.2139-2151.
3.Planat-Benard,V.,et al.Plasticity of human adipose lineage cells toward endothelial cells-Physiological and therapeutic perspectives.Circulation,2004.109(5):p.656-663.
4.Pittenger,M.F.,Mackay,A.M.,Beck,S.C.,Jaiswal,R.K.,Douglas,R.,Mosca,J.D.,Moorman,M.A.,Simonetti,D.W.,Craig,S.,Marshak.D.R.(1999)Science 284,143–147.
5.Ambros,V.The functions of animal microRNA.Nature 2004;431:350-355.
6.Bartel,DP.MicroRNA:genomics,biogenesis,mechanism,and function.Cell 2004;116:281-297.
7.Miranda,K.C.,et al.,A pattern-based method for the identification of microRNA binding sites and their corresponding heteroduplexes.Cell,2006.126(6):p.1203-1217.
8.Ivey,KN and D Srivastava.MicroRNA as regulators of differentiation and cell fate decisions.Cell Stem Cell 2010;7:36-41.
9.Hu,R.,et al.,A Runx2/miR-3960/miR-2861 regulatory feedback loop during mouse osteoblast differentiation.Journal of Biological Chemistry,2011.286(14).
10.Kim,Y.J.,et al.,miR-196a Regulates proliferation and osteogenic differentiation in mesenchymal stem cells derived from human adipose tissue.Journal of Bone and Mineral Research,2009.24(5):p.816-825.
11.Li,Z.Y.,et al.,Biological functions of miR-29b contribute to positive regulation of osteoblast differentiation.Journal of Biological Chemistry,2009.284(23):p.15676-15684.
12.Zhang,J.,et al.,Effects of miR-335-5p in modulating osteogenic differentiation by specifically downregulating Wnt antagonist DKK1.Journal of Bone and Mineral Research,2011.26(8):p.1953-1963.
13.Li,Z.,et al.,A microRNA signature for a BMP2-induced osteoblast lineage commitment program.Proceedings of the National Academy of Sciences of the United States of America,2008.105(37):p.13906-13911.
14.Itoh,T.,Y.Nozawa,and Y.Akao,MicroRNA-141 and-200a Are Involved in Bone Morphogenetic Protein-2-induced Mouse Pre-osteoblast Differentiation by Targeting Distal-less Homeobox 5.Journal of Biological Chemistry,2009.284(29):p.19272-19279.
15.Luzi,E.,et al.,Osteogenic differentiation of human adipose tissue-derived stem cells is modulated by the miR-26a targeting of the SMAD1 transcription factor.Journal of Bone and Mineral Research,2008.23(2):p.287-295.
16.Li,T.,et al.,microRNA-23a inhibits osteogenic differentiation of human bone marrow-derived mesenchymal stem cells by targeting LRP5.International Journal of Biochemistry&Cell Biology,2016.72:p.55-62.
17.Esau,C.,et al.,MicroRNA-143 regulates adipocyte differentiation.Journal of Biological Chemistry,2004.279(50):p.52361-52365.
18.Sun,F.Y.,et al.,Characterization of function and regulation of miR-24-1 and miR-31.Biochemical and Biophysical Research Communications,2009.380(3):p.660-665.
19.Yang,Z.,et al.,MicroRNA hsa-miR-138 inhibits adipogenic differentiation of human adipose tissue-derived mesenchymal stem cells through adenovirus EID-1.Stem Cells and Development,2011.20(2):p.259-267.
20.Zaragosi,L.E.,et al.,Small RNA sequencing reveals miR-642a-3p as a novel adipocyte-specific microRNA and miR-30 as a key regulator of human adipogenesis.Genome Biology,2011.12(7).
21.Eskildsen,T.,et al.,MicroRNA-138 regulates osteogenic differentiation of human stromal(mesenchymal)stem cells in vivo.Proceedings of the National Academy of Sciences of the United States of America,2011.108(15):p.6139-6144.
22.Huang,J.,et al.,MicroRNA-204 regulates Runx2 protein expression and mesenchymal progenitor cell differentiation.Stem Cells,2010.28(2):p.357-364.
23.Zhang,J.F.,et al.,MiR-637 maintains the balance between adipocytes and osteoblasts by directly targeting Osterix.Molecular Biology of the Cell,2011.22(21):p.3955-3961.
24.Huang,S.,et al.,Upregulation of miR-22 promotes osteogenic differentiation and inhibits adipogenic differentiation of human adipose tissue-derived mesenchymal stem cells by repressing HDAC6 protein expression.Stem Cells and Development,2012.21(13):p.2531-2540.
25.Li,H.L.,et al.,miR-17-5p and miR-106a are involved in the balance between osteogenic and adipogenic differentiation of adipose-derived mesenchymal stem cells.Stem Cell Research,2013.10(3):p.313-324.
26.Wei,J.F.,et al.,let-7 enhances osteogenesis and bone formation while repressing adipogenesis of human stromal/mesenchymal stem cells by regulating HMGA2.Stem Cells and Development,2014.23(13):p.1452-1463.
序列表
中國醫學科學院基礎醫學研究所
miR-10b在體外促進間充質幹細胞分化為成骨細胞和抑制其分化為成脂細胞的用途
360234CG
3
PatentIn version 3.3
1
23
RNA
miRNA-10b
1
uacccuguag aaccgaauuu gug 23
2
21
DNA
人工序列
對照RNA
2
uucuccgaac gugucacgut t 21
3
21
DNA
人工序列
對照RNA
3
acgugacacg uucggagaat t 21
