對於穩定含有蛋白質的製劑有用的組合物和方法與流程
2023-05-26 11:39:16 2
本申請為2011年3月21日提交的、發明名稱為「對於穩定含有蛋白質的製劑有用的組合物和方法」的pct申請pct/us2011/029206的分案申請,所述pct申請進入中國國家階段的日期為2012年9月24日,申請號為201180018192.3。
相關申請
本申請是基於37cfr1.53(b)(1)提交的非臨時申請,基於35usc119(e)要求於2010年3月22日提交的臨時申請號61/316326的優先權,其內容通過引用整合到本文中。
發明領域
本發明涉及非表面活性劑化合物(包括例如聚氧乙烯(poe)山梨聚糖和聚乙二醇(peg))用於穩定含有蛋白質的製劑和用於防止此類製劑中的蛋白質聚集的用途。
發明背景
當需要蛋白質製劑的穩定劑以保護蛋白質免受振蕩、攪拌、剪切作用和凍融,或在界面上的靜止狀態而造成的變性時,通常使用非離子去垢劑(即,表面活性劑)(參見例如,美國專利號5,183,746)。作為示例的是在許多含有蛋白質的產品中聚山梨酸酯的用途。例如,聚山梨酸酯20和80(20和80)用於生物治療性產品的製劑中,用於防止表面吸附和作為抵抗蛋白質聚集的穩定劑(kerwin,j.pharm.sci.97(8):2924-2936(2008))。聚山梨酸酯是兩親性的、非離子型表面活性劑,由聚氧乙烯(poe)山梨聚糖的脂肪酸酯組成,聚山梨酸酯20是聚氧乙烯山梨聚糖單月桂酸酯,而聚山梨酸酯80是聚氧乙烯山梨聚糖單油酸酯。
然而不幸的是,聚山梨酸酯可以通過氧化或水解進行降解。當聚山梨酸酯分子降解時,產生多種降解副產物,包括例如脂肪酸、poe山梨聚糖、peg、peg酯和烷基酸。聚山梨酸酯降解的這類副產物中的某些(包括游離的脂肪酸)可以導致含有蛋白質的製劑中增加的濁度和蛋白質聚集。因此,雖然聚山梨酸酯通常作為蛋白質穩定劑使用,但隨時間從聚山梨酸酯降解中釋放的脂肪酸和其他降解副產物可以不利地影響聚山梨酸酯在含有蛋白質的製劑中表現出的保護效果。
因此,需要對於防止蛋白質在含有蛋白質的水性製劑中聚集的有用的額外的組合物。
發明概述
本發明基於這樣的新發現,即,以某些濃度存在於水性製劑中的聚氧乙烯(poe)山梨聚糖和聚乙二醇(peg)對於穩定含有蛋白質或含有肽的製劑,和對於防止蛋白質在此類製劑中的聚集是有用的。
因此,在一個方面,本發明涉及包含抗體或其他蛋白質或肽,和poe山梨聚糖的物質組合物。在一個實施方案中,聚氧乙烯山梨聚糖以從約20ppm至約100,000ppm的濃度存在。在另一個實施方案中,包含抗體或其他蛋白質或肽和poe山梨聚糖的物質組合物不合非離子型表面活性劑,例如,不含聚山梨酸酯。任選地,物質組合物還可以不含凍幹保護劑(lyoprotectant),例如糖、游離胺基酸及其變體等。在某些實施方案中,物質組合物可以是水性的或固體的形式。
在另一個方面,本發明涉及包含抗體或其他蛋白質或肽和聚乙二醇的物質組合物。在某些實施方案中,聚乙二醇在所述物質組合物中以低於約10,000ppm的濃度存在,優選在約20ppm至約10,000ppm之間。在另一個實施方案中,物質組合物任選地包含至少一種poe山梨聚糖,所述poe山梨聚糖任選地以從約20ppm至約100,000ppm的濃度存在於所述物質組合物中。物質組合物還可以任選地不含非離子型表面活性劑,例如,不含聚山梨酸酯。任選地,物質組合物還可以不合凍幹保護劑(lyoprotectant),例如糖、游離胺基酸及其變體等。在某些實施方案中,物質組合物可以是水性的或固體的形式。
在另一個方面,本發明涉及包含裝有任何本文描述的物質組合物的容器的製品。
在另一個方面,提供了用於製備含有抗體(或其他蛋白質或肽)的穩定組合物方法,通過共同混合抗體或其他蛋白質與poe山梨聚糖或peg。
在另一個方面,本發明涉及增加抗體或其他蛋白質或肽在水性製劑中的穩定性的方法,包括混合抗體或其他蛋白質或肽與起穩定作用的量的poe山梨聚糖,其中poe山梨聚糖增加抗體或其他蛋白質或肽的穩定性。在一個實施方案中,poe山梨聚糖以從約20ppm至約100,000ppm的濃度存在,可任選地不含非離子型表面活性劑(例如,不含聚山梨酸酯),或凍幹保護劑,例如糖、游離胺基酸及其變體等。
在另一個方面,本發明涉及增加抗體或其他蛋白質或肽在水性製劑中的穩定性的方法,包括混合抗體或其他蛋白質或肽與起穩定作用的量的聚乙二醇,其中聚乙二醇增加抗體或其他蛋白質或肽的穩定性。在一個實施方案中,聚乙二醇以低於約10,000ppm,優選地在約20ppm至約10,000ppm之間的濃度存在。在另一個實施方案中,物質組合物任選地包含至少一種poe山梨聚糖,所述poe山梨聚糖可任選地以從約20ppm至約100,000ppm的濃度存在,並且可以任選地不合非離子型表面活性劑(例如,不含聚山梨酸酯),或凍幹保護劑,例如糖、游離胺基酸及其變體等。
在另一個方面,本發明涉及防止或降低抗體或其他蛋白質或肽在水性製劑中聚集的方法,包括混合抗體或其他蛋白質或肽與poe山梨聚糖。在一個實施方案中,poe山梨聚糖以從約20ppm至約100,000ppm的濃度存在。水性製劑任選地不含非離子型表面活性劑(例如,不含聚山梨酸酯),或凍幹保護劑,例如糖、游離氫基酸及其變體等。在另一個實施方案中,抗體或其他蛋白質的聚集是由攪拌水性溶液誘導的。
在另一個方面,本發明涉及防止或降低抗體或其他蛋白質或肽在水性製劑中聚集的方法,包括混合抗體或其他蛋白質或肽與聚乙二醇。在一個實施方案中,聚乙二醇以低於約10,000ppm,優選地在約20ppm至約10,000ppm之間的濃度存在。在另一個實施方案中,水性製劑任選地包含至少一種poe山梨聚糖,所述poe山梨聚糖任選地以從約20ppm至約100,000ppm的濃度存在,並且可以任選地不含非離子型表面活性劑(例如,不含聚山梨酸酯),或凍幹保護劑,例如糖、游離氫基酸及其變體等。另一個實施方案中,抗體或其他蛋白質的聚集是由攪拌水性溶液誘導的。
在從重組細胞蛋白質或其他汙染性蛋白質中純化蛋白質、肽或抗體的方法中,本發明的實施方案涉及這樣的改良,所述改良包括在純化過程中向蛋白質、肽或抗體添加poe山梨聚糖或聚乙二醇。
本發明的另一個方面是通過在包含自我聚集型抗體或其他蛋白質或肽的水性溶液中混合至少一種poe山梨聚糖或聚乙二醇,然後濃縮所述水性溶液,來製造另外的自我聚集型抗體或其他蛋白質或肽的非聚集型水性溶液的方法。
根據下文詳細的說明和實例,本發明的其他特徵和優點是顯而易見的,但所述說明和實例不應被視為限制。本申請全文引用的所有參考文獻、專利和公開的專利申請的內容都明確的通過引用整合到本文中。
附圖簡介
圖1顯示了從抗il13抗體與多種添加物組合的濁度分析中獲得的結果,所述添加物包括聚山梨酸酯20(ps)、月桂酸(la)或poe山梨聚糖20(poe)。
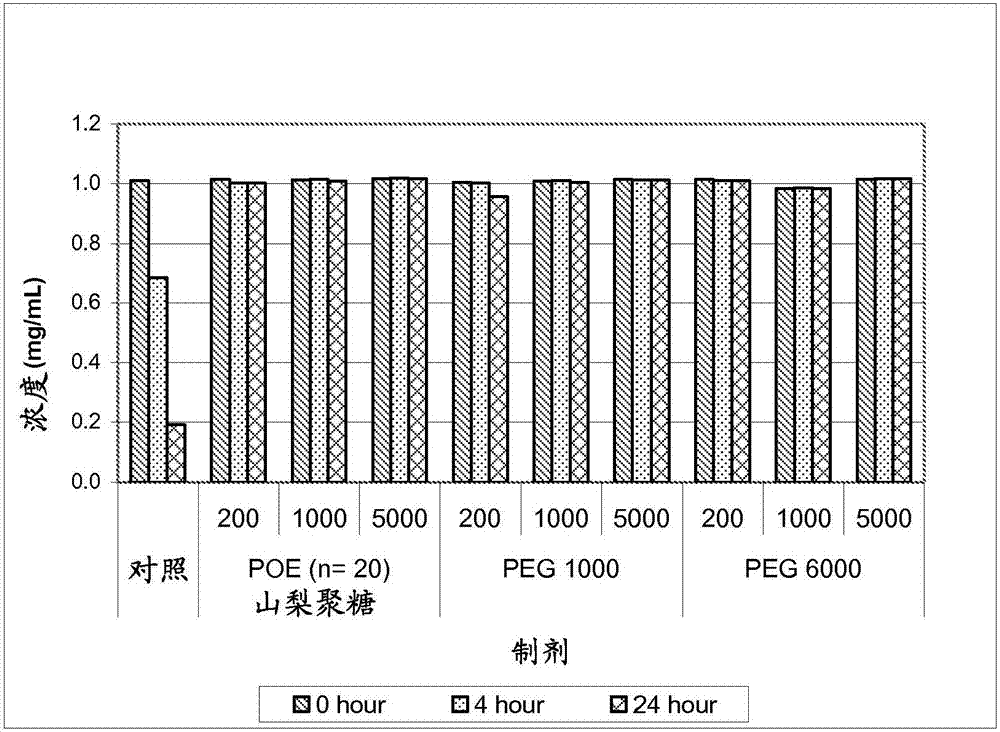
圖2顯示了從抗il13抗體與多種添加物組合的蛋白質濃度分析中獲得的結果,所述添加物包括poe山梨聚糖20、peg1000或peg6000,都具有多種濃度。
圖3顯示了從抗ige抗體與多種添加物組合的蛋白質濃度分析中獲得的結果,所述添加物包括poe山梨聚糖20、peg1000或peg6000,都具有多種濃度。
圖4顯示了從抗il13抗體與多種添加物組合的濁度分析中獲得的結果,所述添加物包括poe山梨聚糖20、peg1000或peg6000,都具有多種濃度。
圖5顯示了從抗ige抗體與多種添加物組合的濁度分析中獲得的結果,所述添加物包括poe山梨聚糖20、peg1000或peg6000,都具有多種濃度。
圖6顯示了從抗il13抗體與多種添加物組合的顆粒大小分析(大於2μm的顆粒)中獲得的結果,所述添加物包括poe山梨聚糖20、peg1000或peg6000,都具有多種濃度。
圖7顯示了從抗ige抗體與多種添加物組合的顆粒大小分析(大於2μm的顆粒)中獲得的結果,所述添加物包括poe山梨聚糖20、peg1000或peg6000,都具有多種濃度。
圖8顯示了從抗il13抗體與多種添加物組合的顆粒大小分析(大於10μm的顆粒)中獲得的結果,所述添加物包括poe山梨聚糖20、peg1000或peg6000,都具有多種濃度。
圖9顯示了從抗ige抗體與多種添加物組合的顆粒大小分析(大於10μm的顆粒)中獲得的結果,所述添加物包括poe山梨聚糖20、peg1000或peg6000,都具有多種濃度。
圖10顯示了從抗il13抗體與多種添加物組合的顆粒大小分析(大於50μm的顆粒)中獲得的結果,所述添加物包括poe山梨聚糖20、peg1000或peg6000,都具有多種濃度。
圖11顯示了從抗ige抗體與多種添加物組合的顆粒大小分析(大於50μm的顆粒)中獲得的結果,所述添加物包括poe山梨聚糖20、peg1000或peg6000,都具有多種濃度。
優選實施方案的詳細描述
通過參考下列對具體實施方案和本文囊括的實施例的詳細說明,可以更容易地理解本發明。
除非另外定義,本文中使用的所有技術和科學術語都具有與發明所屬領域的普通技術人員通常理解的相同含義。雖然任何與本文所述相似或等價的方法和材料也可用於實踐或測試本發明,但本文描述了優選的方法和材料。本文提及的所有出版物都通過引用以其整體整合到本文中。
抗體和其他蛋白質的聚集主要是由疏水性相互作用導致的,最終導致變性。當部分或完全未摺疊的蛋白質的疏水區暴露在水中時,由於通常包埋著的疏水性內部現在暴露在親水性的水性環境中,導致熱力學不利的情況。因此,來自圍繞疏水區的結構性水分子的熵減少驅使變性的蛋白質聚集,聚集主要通過已暴露的疏水區。因此,也危及了蛋白質的溶解度。在一些情況下,蛋白質亞基可在某些條件下發生自我關聯(不論是天然的或錯誤的摺疊),這可能導致沉澱和活性喪失。
影響溶液中的蛋白質聚集的因素一般包括蛋白質濃度、ph、溫度、其他賦形劑和機械脅迫。在純化、配合、生產、儲藏和使用過程中,一些因素(例如,溫度)比其他因素(例如,機械脅迫)更易於控制。製劑研究將指定對ph和賦形劑的恰當選擇,所述選擇不誘導聚集和/或實際上幫助防止聚集。蛋白質濃度由所需治療劑量指定,並根據該濃度的多少將決定是否存在更高關聯狀態(二聚體、四聚體等)的可能性,這可以導致溶液中的聚集。在製劑開發過程中必須進行仔細的研究,以確定何種因素影響蛋白質聚集,以及之後可以如何消除或控制這些因素。
需要鑑別用於腸道外的或其他施用中的抗體或其他蛋白質的穩定溶液製品,該需求可以導致開發用於評估多種添加物對物理穩定性的影響的測試方法。基於已知的影響蛋白質聚集的因素和對此類應用的要求,可以使用涉及攪拌或旋轉蛋白質溶液的機械方法來評估物理穩定性。用於鑑別多種添加物防止聚集的能力的物理脅迫測試方法可以涉及暴露於水平面上的振蕩或攪拌,或者距離以nrev/min在垂直面旋轉的輪軸xcm的旋轉。由聚集導致的濁度通常由視覺觀察或光散射分析確定為時間的函數。備選地,可以通過hplc測定,將由於沉澱造成的可溶性蛋白質含量的降低定量為時間的函數。
本發明是基於這樣的新發現,即在液體製劑中存在的某些濃度的聚氧乙烯(poe)山梨聚糖和聚乙二醇(peg)對於穩定含有蛋白質的製劑,和用於防止此類製劑中的蛋白質聚集是有用的。
因此,在一個方面,本發明描述了包含不論高或低濃度的抗體或其他蛋白質以及poe山梨聚糖的物質組合物。如本文中使用的,「聚氧乙烯山梨聚糖」或「poe山梨聚糖」指具有下列化學結構的非表面活性劑化合物:
其中a+b+c+d優選是從約6至約80,更優選是從約8至約60,更優選是從約10至約40,和更優選是從約10至約20。如上述,本領域技術人員應理解化合物(例如本文描述的poe山梨聚糖)的化學合成導致化合物的一定程度的異源混合物,而非完全同源的製品。由此可見,當本文中描述a+b+c+d是例如優選從約6至約80時,應理解所述定義是指由其化學合成獲得的異源混合物的主要組分。
poe山梨聚糖可以單個地用作抗體或其他蛋白質的穩定劑,或者可以與其他poe山梨聚糖組合使用,用於穩定水性溶液中的抗體或其他蛋白質。在濃度範圍廣泛的水性溶液中,poe山梨聚糖可用作抗體或其他蛋白質的穩定(或抗聚集)劑。在本發明的某些實施方案中,在含有抗體或其他蛋白質的水性製劑中,poe山梨聚糖(如果用作單個穩定劑)或poe山梨聚糖(如果組合使用)能以從約20ppm至約100,000ppm,更優選以從100ppm至約50,000ppm,更優選以從150ppm至約10,000ppm,更優選以從200ppm至約5,000ppm,更優選以從200ppm至約1,000ppm的濃度存在。
在另一個方面,本發明描述了包含不論是高濃度或低濃度的抗體或其他蛋白質,以及聚乙二醇的物質組合物。
如本文中使用的,「聚乙二醇」、「peg」及相似的術語意在涵蓋聚乙二醇及其多種衍生物,例如甲氧基-peg-胺、二胺-peg等。更具體而言,在本發明的某些實施方案中,術語「聚乙二醇」或「peg」指具有下列化學結構的非表面活性劑化合物:
其中n是從約5至約240,並可以任選地含有一定程度的不飽和。涵蓋在本發明的用途中的peg可以是支化的或線性的,優選線性的。如上述,本領域技術人員應理解化合物(例如本文描述的peg)的化學合成導致化合物的一定程度的異源混合物,而非完全同源的製品。由此可見,當本文中描述n優選從約5至240時,應理解所述定義是指由其化學合成獲得的異源混合物的主要組分。
peg可以單個地用作抗體或其他蛋白質的穩定劑,或者可以與其他peg組合使用,用於穩定水性溶液中的抗體或其他蛋白質。在濃度範圍廣泛的水性溶液中,peg可用作抗體或其他蛋白質的穩定(或抗聚集)劑。在本發明的某些實施方案中,在含有抗體或其他蛋白質的水性製劑中,peg(如果用作單個穩定劑)或peg(如果組合使用)能以少於約10,000ppm,優選從約20ppm至約10,000ppm,更優選從約200ppm至約10,000ppm,更優選從約200ppm至約5,000ppm,更優選從約200ppm至約1,000ppm,更優選從約200ppm至約500ppm的濃度存在。
優選的peg包括分子量約200至12,000的聚合物,但更高分子量的聚合物也落入本發明的範圍內。peg包括線性和支化的聚合物,星形分子和通過偶聯至少兩種不同的peg聚合物以形成更高分子量的聚合物而形成的peg嵌段共聚物,這些都是本領域普遍已知的。
「多肽」或「蛋白質」意指這樣的胺基酸序列,所述序列的鏈長度足以產生更高水平的三級和/或四級結構。因此,蛋白質不同於「肽」,後者也是基於胺基酸的分子,但不具有此類結構。一般地,本文使用的蛋白質具有至少約5-20kd,備選地至少約15-20kd,優選至少約20kd的分子量。「肽」意指這樣的胺基酸序列,所述序列一般不表現出更高水平的三級和/或四級結構。肽一般具有少於約5kd的分子量。
涵蓋在本文定義內的多肽實例包括哺乳動物蛋白質,例如腎素;生長激素,包括人生長激素和牛生長激素;生長激素釋放因子;甲狀旁腺激素;甲狀腺刺激激素;脂蛋白;α-1-抗胰蛋白酶;胰島素a鏈;胰島素b鏈;胰島素原;卵泡刺激激素;降鈣素;黃體生成素;胰高血糖素;凝固因子如因子viiic、因子ix、組織因子和vonwillebrands因子;抗凝固因子如蛋白c;心房鈉尿因子;肺表面活性物質;纖溶酶原活化因子,例如尿激酶或人尿或組織類纖溶酶原活化因子(t-pa);鈴蟾素;凝血酶;造血生長因子;腫瘤壞死因子-α和-β;腦啡肽酶;rantes(通過活化調控的由正常t細胞表達分泌);人巨噬細胞炎性蛋白(mip-1-α);血清白蛋例如人血清白蛋白;muellerian抑制性物質;鬆弛素a鏈;鬆弛素b鏈;prorelaxin;小鼠促性腺激素相關肽;微生物蛋白,例如β-內醯胺酶;dna酶;ige;細胞毒性t淋巴細胞相關抗原(ctla),例如ctla-4;抑制素;活化素;血管內皮細胞生長因子(vegf);激素或生長因子的受體;蛋白a或d;類風溼因子;神經營養因子例如骨源性神經營養因子(bdnf),神經營養因子-3、-4、-5,或-6(nt-3、nt-4、nt-5,或nt-6),或神經生長因子例如ngf-β;血小板源性生長因子(pdgf);成纖維細胞生長因子如afgf和bfgf;表皮生長因子(egf);轉化生長因子(tgf),例如tgf-α和tgf-β,包括tgf-β1、tgf-β2、tgf-β3、tgf-β4或tgf-β5;胰島素樣生長因子-i和ii(igf-i和igf-ii);des(1-3)-igf-i(腦igf-i)、胰島素樣生長因子結合蛋白(igfbp);cd蛋白,如cd3、cd4、cd8、cd19和cd20;紅細胞生成素;骨誘導性因子;免疫毒素;骨形態發生蛋白(bmp);幹擾素如幹擾素α、β和γ;集落刺激因子(csf),例如m-csf、gm-csf和g-csf;白介素(il),例如il-1至il-10;超氧化物歧化酶;t-細胞受體;表面膜蛋白;衰變加速因子;病毒抗原,如,例如aids包膜的部分;運輸蛋白;歸巢受體;地址素;調控蛋白;整聯蛋白如cd11a、cd11b、cd11c、cd18、icam、vla-4和vcam;腫瘤相關抗原如ca125(卵巢癌抗原)或her2、her3或her4受體;免疫粘附素;和任意上述列舉的蛋白質的片段和/或變體,以及與任意上述列舉的蛋白質結合的抗體,包括抗體片段。
配製的蛋白質優選是基本純的,且理想地是基本同質的(即,不含汙染蛋白質)。「基本純的」蛋白質意指基於組合物的總重量,包含按重量計至少約90%,優選按重量計至少約95%的蛋白質的組合物。「基本同質的」蛋白質意指基於組合物的總重量,包含按蛋白質重量計至少約99%的組合物。
在某些實施方案中,蛋白質是抗體。抗體在本文中是針對目標「抗原」的。優選地,抗原是生物學重要的蛋白質,將抗體施用給患疾病或病症的哺乳動物可以在哺乳動物中導致治療益處。然而,還考慮針對非蛋白質抗原(例如,腫瘤相關的糖脂抗原;參見美國專利5,091,178)的抗體。當抗原是蛋白質時,其可以是跨膜分子(例如,受體)或配體,如生長因子。示例性的抗原包括上述蛋白質。本發明涵蓋的抗體的優選的分子靶包括cd多肽,如cd3、cd4、cd8、cdl9、cd20和cd34;her受體家族成員,如egf受體(her1)、her2、her3或her4受體;細胞粘附分子,如lfa-1、mac1、p150、95、vla-4、icam-1、vcam和av/b3整聯蛋白(包括其a或b亞基)(例如,抗cd11a、抗cd18或抗cd11b抗體);生長因子如vegf;ige;血型抗原;flk2/flt3受體;肥胖症(ob)受體;mpl受體;ctla-4;多肽c等。任選地與其他分子綴合的可溶性抗原或其片段可用作生成抗體的免疫原。對於跨膜分子,如受體,其片段(例如,受體的胞外結構域)可用作免疫原。備選地,表達跨膜分子的細胞可用作免疫原。此類細胞可源自天然來源(例如,癌細胞系),或者可以是通過重組技術轉化來表達跨膜分子的細胞。
本文中待純化的抗體實例包括但不限於:her2抗體,包括曲妥珠單抗(trastuzumab)(carter等人,proc.natl.acad.sci.usa,89:4285-4289(1992),美國專利號5,725,856)和培妥珠單抗(pertuzumab)(omnitargtm)(wo01/00245);cd20抗體(見下文);il-8抗體(stjohn等人,chest,103:932(1993),和國際公開號wo95/23865);vegf或vegf受體抗體,包括人源化和/或親和性成熟的vegf抗體,如人源化vegf抗體hua4.6.1貝伐珠單抗(bevacizumab)和雷珠單抗(ranibizumab)(kim等人,growthfactors,7:53-64(1992);wo96/30046和1998年10月15日公開的國際公開號wo98/45331);psca抗體(wo01/40309);cd11a抗體,包括依法珠單抗(efalizumab)(美國專利號6,037,454、美國專利號5,622,700、wo98/23761、stoppa等人,transplantintl.4:3-7(1991)和hourmant等人,transplantation58:377-380(1994));結合ige的抗體,包括奧馬珠單抗(omalizumab)(presta等人,j.immunol.151:2623-2632(1993)和國際公開號wo95/19181;1998年2月3日公布的美國專利號5,714,338或1992年2月25日公布的美國專利號5,091,313;1993年3月4日公開的wo93/04173或1998年6月30日公開的國際申請號pct/us98/13410;美國專利號5,714,338);cd18抗體(1997年4月22日公布的美國專利號5,622,700,或1997年7月31日公開的wo97/26912);apo-2受體抗體抗體(1998年11月19日公開的wo98/51793);組織因子(tf)抗體(1994年11月9日授權的歐洲專利號0420937b1);α4-α7整聯蛋白抗體(1998年2月19日公開的wo98/06248);egfr抗體(例如,嵌合的或人源化的225抗體、西妥昔單抗(cetuximab),如1996年12月19日公開的wo96/40210中的);cd3抗體,如okt3(1985年5月7日公布的美國專利號4,515,893);cd25或tac抗體,如chi-621和(參見1997年12月2日公布的美國專利號5,693,762);cd4抗體,如cm-7412抗體(choy等人,arthritisrheum39(1):52-56(1996));cd52抗體,例如campath-1h(ilex/berlex)(riechmann等人,nature332:323-337(1988));fc受體抗體,如針對fcγri的m22抗體(如graziano等人,j.immunol.155(10):4996-5002(1995)中的ri);癌胚抗原(cea)抗體,如hmn-14(sharkey等人,cancerres.55(23suppl):5935s-5945s(1995));針對乳腺上皮細胞的抗體(包括hubre-3、hu-mc3和chl6)(ceriani等人,cancerres.55(23):5852s-5856s(1995);和richman等人,cancerres.55(23supp):5916s-5920s(1995));結合結腸癌細胞的抗體如c242(litton等人,eurj.immunol.26(1):l-9(1996));cd38抗體,例如at13/5(ellis等人,j.immunol.155(2):925-937(1995));cd33抗體,如hum195(jurcic等人,cancerres55(23suppl):5908s-5910s(1995))和cma-676或cdp771;epcam抗體,如17-1a;gpiib/iiia抗體,如阿昔單抗(abciximab)或c7e3fab;rsv抗體,如medi-493;cmv抗體,如;hiv抗體,如pro542;肝炎抗體,如hepb抗體;ca125抗體,包括抗muc16(wo2007/001851;yin,bwt和lloyd,ko,j.biol.chem.276:27371-27375(2001))和ovarex;獨特型gd3表位抗體bec2;αvβ3抗體(例如,;medimmune);人腎細胞癌抗體,如ch-g250;ing-1;抗人17-1an抗體(3622w94);抗人結腸直腸腫瘤抗體(a33);針對gd3神經節苷脂的抗人黑素瘤抗體r24;抗人鱗狀細胞癌(sf-25);人白細胞抗原(hla)抗體,如smartid10和抗hladr抗體oncolym(lym-1);cd37抗體,如tru016(trubion);il-21抗體(zymogenetics/novonordisk);抗b細胞抗體(impheron);b細胞靶向mab(immunogen/aventis);1d09c3(morphosys/gpc);lymphorad131(hgs);lym-1抗體,如lym-1y-90(usc)或抗lym-1oncolym(usc/peregrine);lif226(enhancedlifesci.);baff抗體(例如,wo03/33658);baff受體抗體(參見例如,wo02/24909);br3抗體;blys抗體,如貝利木單抗(belimumab);lymphostat-btm;isf154(ucsd/roche/tragen);gomilixima(idec152;biogenidec);il-6受體抗體,如atlizumab(actemratm;chugai/roche);il-15抗體,如humax-il-15(genmab/amgen);趨化因子受體抗體,如ccr2抗體(例如,mln1202;millieneum);抗補體抗體,如c5抗體(例如,依庫珠單抗(eculizumab)、5g1.1;alexion);人免疫球蛋白的口服製劑(例如,igpo;proteintherapeutics);il-12抗體,如abt-874(cat/abbott);替奈昔單抗(teneliximab)(bms-224818;bms);cd40抗體,包括s2c6及其人源化變體(wo00/75348)和tnx100(chiron/tanox);tnf-α抗體,包括ca2英利昔單抗(infliximab)、cdp571、mak-195、阿達木單抗(adalimumab)(humiratm)、聚乙二醇化的tnf-α抗體片段,如cdp-870(celltech)、d2e7(knoll)、抗tnf-α多克隆抗體(例如,passtnf;verigen);cd22抗體,如ll2或依帕珠單抗(epratuzumab)(;immunomedics),包括依帕珠單抗y-90和依帕珠單抗i-131,abiogen的cd22抗體(abiogen,義大利)、cmc544(wyeth/celltech)、combotox(utsoutwestern)、bl22(nih)和lymposcantc99(immunomedics)。
cd20抗體的實例包括:「c2b8」,現在被稱為「利妥昔單抗」(美國專利號5,736,137);釔-[90]-標記的2b8鼠抗體,被稱為「y2b8」或「替伊莫單抗(ibritumomabtiuxetan)」,可自idecpharmaceuticals,inc.商業購買(美國專利號5,736,137;以atcc登錄號hb11388於1993年6月22日儲藏的2b8);鼠igg2a「b1」,也被稱為「託西莫單抗(tositumomab)」,任選地用131i標記,生成可自corixa商業購買的「131i-b1」或「碘i131託西莫單抗」抗體(bexxartm)(還參見美國專利號5,595,721);鼠單克隆抗體「1f5」(press等人,blood69(2):584-591(1987))及其包括「框架補丁」在內的變體或人源化1f5(wo2003/002607,leung,s.;atcc保藏號hb-96450);鼠2h7和嵌合的2h7抗體(美國專利號5,677,180);人源化2h7(wo2004/056312,lowman等人);2f2(humax-cd20),靶向b細胞的細胞膜中的cd20分子的完整的人高親和力抗體(genmab,denmark;參見例如glennie和vandewinkel,drugdiscoverytoday8:503-510(2003)和cragg等人,blood101:1045-1052(2003);wo2004/035607;us2004/0167319);wo2004/035607和us2004/0167319中示出的人單克隆抗體(teeling等人);us2004/0093621中描述的具有與fc區結合的複合n-糖苷連接的糖鏈的抗體(shitara等人);結合cd20的單克隆抗體和抗原結合片段(wo2005/000901,tedder等人),如hb20-3、hb20-4、hb20-25和mb20-11;cd20結合分子,如ame系列抗體,例如wo2004/103404和us2005/0025764中示出的ame33抗體(watkins等人,elililly/appliedmolecularevolution,ame);cd20結合分子,如us2005/0025764中描述的那些(watkins等人);a20抗體或其變體,如嵌合的或人源化的a20抗體(分別是ca20、ha20)或immu-106(us2003/0219433,immunomedics);cd20-結合抗體,包括表位缺失的leu-16、1h4或2b8,任選地與il-2綴合,如us2005/0069545a1和wo2005/16969(carr等人);結合cd22和cd20的雙特異性抗體,例如,hll2xha20(wo2005/14618,chang等人);可獲得自internationalleukocytetypingworkshop的單克隆抗體l27、g28-2、93-1b3、b-c1或nu-b2(valentine等人,在leukocytetypingiii(mcmichael編著,第440頁,oxforduniversitypress(1987))中;1h4(haisma等人,blood92:184(1998));抗cd20auristatine綴合物(seattlegenetics);抗cd20-il2(emd/biovation/cityofhope);抗cd20mab療法(epicyte);抗cd20抗體tru015(trubion)。
術語「抗體」在本文中包括單克隆抗體(包括具有免疫球蛋白fc區的全長抗體)、具有多表位特異性的抗體組合物、多特異性抗體(例如,雙特異性抗體、雙抗體和單鏈分子,以及抗體片段(例如,fab、f(ab′)2和fv)。術語「免疫球蛋白」(ig)在本文中與「抗體」可互換使用。
基礎的4條鏈的抗體單位是由2條相同的輕鏈(l)和2條相同的重鏈(h)組成的異源四聚體糖蛋白。igm抗體由5個基礎的異源四聚體單位和被稱為j鏈的額外多肽組成,並且含有10個抗原結合位點;而iga抗體包括從2-5個基礎的4條鏈單位,其可以多聚化與j鏈組合形成多價裝配物。在igg的情況下,4條鏈單位一般是約150,000道爾頓。每條l鏈通過1個共價二硫鍵與h鏈連接,而2條h鏈通過一個或多個(取決於h鏈的同種型)二硫鍵彼此連接。每條h和l鏈也具有規律間隔的鏈內二硫橋。每條h鏈在n端具有可變結構域(vh),對於α和γ鏈而言,vh後有3個恆定結構域(ch),而對於μ和ε同種型而言,vh後有4個ch結構域。每條l鏈在n端具有可變結構域(vl),在其另一端後有恆定結構域。vl與vh配對,而cl與重鏈的第一恆定結構域(ch1)配對。特定的胺基酸殘基被認為在輕鏈和重鏈可變結構域之間形成接觸面。成對的vh和vl一起形成單個抗原結合位點。關於不同類的抗體的結構和性質,參見例如basicandclinicalimmunology,第8版,danielp.sties,abbai.terr和tristramg.parsolw(編著),appleton&lange,norwalk,conn.,1994,第71頁和第6章。
基於其恆定結構域的胺基酸序列,來自任何脊椎動物物種的l鏈都可歸入2個明確不同類型中的一種,稱為κ和λ。取決於其重鏈恆定結構域(ch)的胺基酸序列,免疫球蛋白可歸入不同類或同種型。存在5類免疫球蛋白:iga、igd、ige、igg和igm,分別具有名為α、δ、ε、γ和μ的重鏈。基於ch序列和功能中的相對細微的差異,γ和α類進一步分為亞類,例如,人表達下列亞類:igg1、igg2、igg3、igg4、iga1和iga2。
術語「可變的「指這樣的事實,即可變結構域的某些片段的序列在抗體之間顯著不同。v結構域介導抗原結合,定義特定抗體與其特定抗原的特異性。然而,可變性並非均勻地分布在整個可變結構域的範圍中。相反,v區由約15-30個胺基酸殘基的、被稱為框架區(fr)的相對不變的幾段序列組成,其被每個長度約9-12個胺基酸殘基的、被稱為「高變區」或有時被稱為「互補決定區」(cdr)的極度可變的較短區域分隔開。每個天然重鏈和輕鏈的可變結構域包含4個fr,大部分採用β-片層構象,由3個高變區連接,形成環狀連接,在一些情況下形成β-片層結構的一部分。每條鏈中的高變區由fr緊密相鄰地結合在一起,並且與來自其他鏈的高變區一起對抗體的抗原結合位點的形成起作用(參見kabat等人,sequencesofproteinsofimmunologicalinterest,第5版,publichealthservice,nationalinstitutesofhealth,bethesda,md.(1991)。恆定結構域不直接參與抗體與抗原的結合,但表現出多種效應子功能,例如參與抗體依賴性細胞的細胞毒性(adcc)。
術語「高變區」(也被稱為「互補決定區」或cdr)在本文中指免疫球蛋白v區結構域中的抗體胺基酸殘基(通常是3或4個具有高度序列可變性的短區域),其形成抗原結合位點,是抗原特異性的主要決定簇。有至少兩種方法用於鑑別cdr殘基:(1)基於跨物種序列可變性的方法(即,kabat等人,sequencesofproteinsofimmunologicalinterest(nationalinstituteofhealth,bethesda,ms1991));和(2)基於抗原-抗體複合物的晶體學研究的方法(chothia,c.等人,j.mol.biol.196:901-917(1987))。但是,兩種殘基鑑別技術定義重疊的區域而非相同區域,可以將它們組合來定義雜交cdr。
如本文中使用的,術語「單克隆抗體」指從基本均質的抗體群體中獲得的抗體,即,除可能天然存在的突變和/或可能以少量存在的翻譯後修飾(例如,異構化、醯胺化)外,包括相同群體的單種抗體。單克隆抗體是高度特異性的,針對單種抗原性位點。此外,與通常包括針對不同決定簇(表位)的不同抗體的常規的(多克隆)抗體製品相反,每種單克隆抗體都針對抗原上的單種決定簇。除特異性外,單克隆抗體的優點還在於它們是通過雜交瘤培養物合成的,不被其他免疫球蛋白汙染。修飾語「單克隆」表示抗體的特徵是從基本均質的抗體群體中獲得的,而不被視為要求通過任何特定的方法生產抗體。例如,可以通過由kohler等人,nature,256:495(1975)首次描述的雜交瘤方法,或者可以通過重組dna方法(參見例如,美國專利號4,816,567),製備根據本發明的待使用的單克隆抗體。還可以使用例如clackson等人,nature,352:624-628(1991)和marks等人,j.mol.biol.,222:581-597(1991)中描述的技術,從噬菌體抗體文庫中分離「單克隆抗體」。
單克隆抗體在本文中具體包括「嵌合」抗體(免疫球蛋白)以及此類抗體的片段(只要所述片段表現出所需的生物學活性),其中重鏈和/或輕鏈的一部分與源自特定物種或者屬於特定的抗體類型或亞類的抗體中的相應序列相同或同源,而鏈的剩餘部分與源自另一種物種或者屬於另一種抗體類型或亞類的抗體中的相應序列相同或同源(美國專利號4,816,567;morrison等人,proc.natl.acad.sci.usa,81:6851-6855(1984))。本文中的目標嵌合抗體包括「靈長化(primitized)」抗體,其包含源自非人靈長類(例如,舊世界猴子、猿等)的可變結構域抗原結合序列和人恆定區序列。
「完整的」抗體是這樣的抗體,其包含抗原結合位點和cl,以及至少包含重鏈結構域ch1、ch2和ch3。恆定結構域可以是天然序列恆定結構域(例如,人天然序列恆定結構域)或其胺基酸序列變體。優選地,完整的抗體具有一種或多種效應子功能。
抗體片段包括完整抗體的一部分,優選地是完整抗體的抗原結合和/或可變區。抗體片段的實例包括fab、fab′、f(ab』)2和fv片段;雙抗體;線性抗體(參見美國專利號5,641,870,實施例2;zapata等人,proteineng.8(10):1057-1062[1995]);從抗體片段形成的單鏈抗體分子和多特異性抗體。
木瓜蛋白酶消化抗體產生2個相同的、被稱為「fab」片段的抗原結合片段,和殘餘的「fc」片段,該名稱反映了易於結晶的能力。fab片段由完整的l鏈、h鏈的可變區結構域(vh)和一條重鏈的第一恆定結構域(ch1)組成。對於抗原結合而言,每個fab片段都是單價的,即,其具有單個抗原結合位點。胃蛋白酶處理抗體產生單個大的f(ab』)2片段,所述f(ab』)2片段大致對應於2個由二硫化物連接的、具有不同抗原結合活性的fab片段,且仍然能夠交聯抗原。fab′片段不同於fab片段,其在ch1結構域的羧基端具有若干個額外殘基,包括一個或多個來自抗體鉸鏈區的半胱氨酸。fab′-sh在本文中是這樣的fab′的名稱,其中恆定結構域的半胱氨酸殘基具有游離的巰基。f(ab』)2抗體片段最初被生產為之間具有鉸鏈半胱氨酸的fab′片段對。抗體片段的其他化學偶聯也是已知的。
fc片段包含由二硫化物結合在一起的兩條h鏈的羧基端部分。抗體的效應子功能是由fc區的序列決定的,該區域也被可見於某些細胞類型上的fc受體(fcr)識別。
「fv」是含有完全的抗原識別和結合位點的最小抗體片段。該片段由緊密的、非共價關聯的一條重鏈和一條輕鏈可變區結構域的二聚體組成。這兩個結構域的摺疊發出了6個高變環(來自h鏈和l鏈各3個環),提供了用於抗原結合的胺基酸殘基,並且賦予抗體抗原結合特異性。然而,即使是單個可變結構域(或者進包括抗原特異性的3個cdr的一半fv)也具有識別和結合抗原的能力,雖然比完整結合位點的親和力低。
「單鏈fv」,也縮寫為「sfv」或「scfv」,是包含連接成單條多肽鏈的vh和vl抗體結構域的抗體片段。優選地,sfv多肽進一步包含在vh和vl結構域之間的多肽接頭,所述多肽接頭使sfv能夠形成抗原結合所需的結構。關於sfv的綜述,參見pluckthuninthepharmacologyofmonoclonalantibodies,第113卷,rosenburg和moore編著,springer-verlag,newyork,第269-315頁(1994)。
術語「雙抗體」指通過構建在vh和vl結構域之間具有短接頭(約5-10個殘基)的sfv片段(參見前述章節)製備的小抗體片段,如此使得形成鏈間而非鏈內的v結構域配對,從而獲得二價片段,即,具有2個抗原結合位點的片段。雙特異性的雙抗體是兩個「交換」sfv片段的異二聚體,其中兩個抗體的vh和vl結構域存在於不同的多肽鏈上。雙抗體詳細描述在例如ep404,097;wo93/11161;hollinger等人,proc.natl.acad.sci.usa90:6444-6448(1993)中。
「特異性結合」特定多肽或特定多肽上的表位或對於特定多肽或特定多肽上的表位「特異性」的抗體是這樣的抗體,所述抗體結合特定多肽或特定多肽上的表位,而基本不結合任何其他多肽或多肽表位。
術語「固相」描述了本發明的抗體可以附著的非水性基質。涵蓋在本文中的固相的實例包括部分地或完全地由玻璃(例如,可控孔度的玻璃)、多糖(例如,瓊脂糖)、聚丙烯醯胺、聚苯乙烯、聚乙烯醇和聚矽氧烷形成的固相。在某些實施方案中,根據上下文,固相可以包含測定平板的孔;在其他情況下,其是純化柱(例如,親和層析柱)。該術語也包括分散顆粒的不連續固相,例如美國專利號4,275,149中描述的那些。
非人(例如,鼠)抗體的「人源化」形式是大部分是人序列的嵌合免疫球蛋白、免疫球蛋白鏈或其片段(如fv、fab、fab′、f(ab』)2或抗體的其他抗原結合亞序列),其含有源自非人免疫球蛋白的最小序列。大部分情況下,人源化抗體是人免疫球蛋白(受體抗體),其中來自受體的高變區(也是cdr)的殘基被來自具有所需的特異性、親和力和能力的非人物種(供體抗體)(如,小鼠、大鼠或兔)的高變區的殘基取代。在一些情況下,人免疫球蛋白的fv框架區(fr)殘基被相應的非人殘基取代。此外,本文中使用的「人源化抗體」還包含既不存在於受體抗體也不存在於供體抗體中的殘基。進行這些修飾以進一步改善和優化抗體性能。人源化抗體任選地還包括至少一部分免疫球蛋白恆定區(fc),通常是人免疫球蛋白的恆定區。關於其他細節,參見jones等人,nature,321:522-525(1986);reichmann等人,nature,332:323-329(1988);和presta,curr.op.struct.biol.,2:593-596(1992)。
「物種依賴性抗體」,例如,哺乳動物抗人ige抗體是這樣的抗體,其對來自第一種哺乳動物物種的抗原的結合親和力比對來自第二種哺乳動物物種的該抗原的同源物的結合親和力更強。一般而言,物種依賴性抗體「特異性地結合」人抗原(即,具有不多於約1x10-7m、備選地不多於約1x10-8m、備選地不多於約1x10-9m的結合親和力(kd)值),但對來自第二種非人哺乳動物物種的抗原同源物的結合親和力比其與非人抗原的結合親和力弱至少約50倍,至少約500倍,或者至少約1000倍。物種依賴性抗體可以是上述多種抗體類型中的任一種,但優選是人源化抗體或人抗體。
抗體的「效應子功能」指歸因於抗體的fc區(天然序列fc區或胺基酸序列變體fc區)的生物學活性,並且隨抗體同種型而改變。抗體的效應子功能的實例包括:c1q結合和補體依賴性的細胞毒性;fc受體結合;抗體依賴性細胞介導的細胞毒性(adcc);吞噬作用;細胞表面受體(例如,b細胞受體)下調;和b細胞活化。
「抗體依賴性細胞介導的細胞毒性」或adcc指細胞毒性的形式,其中分泌的ig結合到存在於某些細胞毒性細胞(例如,天然殺傷細胞(nk)、嗜中性粒細胞和巨噬細胞)上的fc受體(fcr)上,使這些細胞毒性效應子細胞能夠特異性地結合具有抗原的靶細胞,並且之後用細胞毒素殺死靶細胞。抗體「武裝」細胞毒性細胞,並且是通過該機制殺死靶細胞所必需的。介導adcc的初級細胞,nk細胞,僅表達fcγriii,而單核細胞表達fcγri、fcγrii和fcγriii。ravetch和kinet,annu.rev.immunol.9:457-92(1991)的第464頁的表3中總結了造血細胞上的fc表達。為了評估目標分子的adcc活性,可以實施體外acdd測定,如美國專利號5,500,362或5,821,337中描述的。對於此類測定有用的效應子細胞包括外周血單核細胞(pbmc)和天然殺傷細胞(nk)。備選地,或額外地,可以在體內評估目標分子的adcc活性,例如,在如clynes等人,pnasusa95:652-656(1998)中公布的動物模型中。
「fc受體」或「fer」描述了結合抗體的fc區的受體。優選的fcr是天然序列的人fcr。此外,優選的fcr是結合igg抗體(γ受體)的,並包括fcγri、fcγrii和fcγriii亞類的fcr,包括等位變體和備選地這些受體的剪切形式,fcγrii受體包括fcγriia(「活化型受體」)和fcγriib(「抑制型受體」),具有相似的胺基酸序列,主要在其胞質結構域中有差別。活化型受體fcγriia在其胞質結構域中含有基於免疫受體酪氨酸的活化基序(itam)。抑制型受體fcγriib在其胞質結構域中含有基於免疫受體酪氨酸的抑制基序(itim)(參見,m.daeron,annu.rev.immunol.15:203-234(1997))。ravetch和kinet,annu.rev.immunol.9:457-92(1991);capel等人,immunomethods4:25-34(1994);和dehaas等人,j.lab.clin.med.126:330-41(1995)中綜述了fcr。其他fcr,包括待在將來鑑別的那些,都涵蓋在本文的術語「fcr」中。術語還包括新生兒受體fcrn,其負責將母體的igg轉移到胎兒中。guyer等人,j.immunol.117:587(1976)和kim等人,j.immunol.24:249(1994)。
「人效應子細胞」是表達一種或多種fcr並發揮效應子功能的白細胞。優選地,細胞至少表達fcriii,並發揮效應子功能。介導adcc的人白細胞的實例包括外周血單核細胞(pbmc)、天然殺傷細胞(nk)、單核細胞、細胞毒性t細胞和嗜中性粒細胞,其中pbmc和mnk細胞是優選的。效應子細胞可以從天然源(例如血液)分離。
「補體依賴性細胞毒性」或「cdc」指在存在補體的條件下裂解靶細胞。經典補體途徑的活化是由補體系統的第一個組分(c1q)與結合其關聯抗原的(恰當亞類的)抗體的結合而起始的。為了評估補體活化,可以實施例如,如gazzano-santoro等人,j.immunol.methods202:163(1996)中描述的cdc測定。
當使用「分離的」來描述本文公布的多種多肽和抗體時,意味著多肽或抗體已經從它的生產環境的組分中鑑別、分離和/或回收。優選地,分離的多肽不與來自它的生產環境中的所有其他組分相關聯。它的生產環境的汙染性組分,例如由重組的轉染細胞造成的汙染性組分,是通常幹擾多肽的診斷或治療用途的材料,並且可包括酶、激素和其他蛋白質的或非蛋白質的溶質。在優選的實施方案中,多肽將被純化至(1)通過使用旋杯式測序儀足以獲得n端或內部胺基酸序列的至少15個殘基的程度,或(2)均質(使用考馬斯藍或優選銀染法,在非還原或還原條件下,通過sds-page)。然而,一般地,分離的多肽或抗體是通過至少一個純化步驟製備的。
編碼本文中的多肽和抗體的「分離的」核酸分子是這樣的核酸分子,所述核酸分子是從在它的生產環境中與其通常相關聯的至少一種汙染性核酸分子中鑑別和分離的。優選地,分離的核酸不與和生產環境相關聯的所有組分關聯。編碼本文中的多肽和抗體的分離的核酸分子處於非其被自然發現時的形式或環境的形式。因此,分離的核酸分子不同於編碼本文中天然存在於細胞中的的多肽和抗體的核酸。
術語「控制序列」指在特定的宿主生物體中表達有效連接的編碼序列所必需的dna序列。適合原核生物的控制序列包括例如啟動子,任選地包括操縱子序列,和核糖體結合位點。已知真核細胞利用啟動子、多聚腺苷酸信號和增強子。
當核酸位於與另一種核酸序列的功能性關係中時,所述核酸是「有效連接的」。例如,如果前序列或分泌前導的dna作為參與多肽分泌的前蛋白表達,則其與多肽的dna是有效連接的;如果啟動子或增強子影響序列轉錄,則其與編碼序列是有效連接的;或者如果核糖體結合位點的放置促進了翻譯,則它與編碼序列是有效連接的。一般而言,「有效連接的」意味著連接的dna序列是連續的,並且在分泌前導序列的情況下,是連續且處於閱讀相(readingphase)中的。然而,增強子不必連續。連接是通過在方便的限制性位點連接而實現的。如果不存在此類位點,則根據常規實踐,使用合成的寡核苷酸銜接子或接頭。
術語「已附加表位的」用於本文中指包含與「標籤多肽」融合的本文所述多肽或抗體的嵌合多肽。標籤多肽具有足夠的殘基來提供針對其製備抗體的表位,然而又足夠短使得不幹擾與其融合的多肽的活性。優選地,標籤多肽是相當足夠獨特的,使得抗體基本不與其他表位交叉反應。合適的標籤多肽一般具有至少6個胺基酸殘基,並且通常在約8和50個胺基酸殘基之間(優選在約10和20個胺基酸殘基之間)。
如本文中使用的,術語「免疫粘附素」表示這樣的抗體樣分子,所述分子組合了異源蛋白質(「粘附素」)的結合特異性與免疫球蛋白恆定結構域的效應子功能。在結構上,免疫粘附素包含與抗體的抗原識別位點和結合位點不同的(即,「異源的」)、具有所需的結合特異性的胺基酸序列和免疫球蛋白恆定結構域序列的融合體。免疫粘附素分子的粘附部分通常是至少包含受體或配體的結合位點的、連續的胺基酸序列。免疫粘附素中的免疫球蛋白恆定結構域序列可以獲得自任何免疫球蛋白,如igg-1、igg-2、igg-3或igg-4亞型、iga(包括iga-1和iga-2)、ige、igd或igm。ig融合體優選的包括用本文描述的多肽或抗體的結構域替代ig分子內的至少一個可變區。在特別優選的實施方案中,免疫球蛋白融合體包括igg1分子的鉸鏈區、ch2和ch3,或鉸鏈區、ch1、ch2和ch3區。關於免疫球蛋白融合體的生產,還參見1995年6月7目公布的美國專利號5,428,130。
術語「藥物製劑」指這樣的製品,所述製品的形式允許活性成分的生物學活性生效,並且不含有對施用製劑的對象不可接受的毒性的其他組分。
如果在給定的時間時抗體的生物學活性是製備藥物製劑時表現出的生物學活性的約10%以內(在測定的誤差內),則抗體在藥物製劑中具有「生物學活性」,這首根據抗體在體外或體內與抗原結合的能力和所導致的可測量的生物學應答來確定的。
「穩定的」或「穩定化」製劑是這樣的製劑,其中的蛋白質在儲藏後基本保留了它的生理學和/或化學穩定性。可以在選定的溫度下,測量選定的時間段的穩定性。優選地,製劑在室溫(~30℃)下或者在40℃下穩定至少1個月,和/或在約2-8℃下穩定至少1年,優選至少2年。例如,在儲藏過程中的聚集程度可用作蛋白質穩定性的標誌。因此,「穩定的」製劑可以是這樣的製劑,其中少於約10%,並且優選少於約5%的蛋白質在製劑中以聚集物的形式存在。用於測量蛋白質穩定性的多種分析技術是本領域可獲得的,綜述在例如,在peptideandproteindrugdelivery,247-301,vincentlee編著,marceldekker,inc.,newyork,n.y.,pubs.(1991)和jones,a.adv.drugdeliveryrev.10:29-90(1993)中。
增加含有蛋白質的製劑的「穩定性」指降低(相比未處理過的含蛋白質的製劑)或防止製劑中形成蛋白質聚集物。
術語「水性溶液」指這樣的溶液,其中水是溶解基質或溶劑。當物質溶解在液體中時,混合物被稱為溶液。溶解的物質是溶質,實施溶解的液體是溶劑(在此情況下是水)。
術語「穩定化試劑」或「穩定劑」在本文中是向溶液和混合物或懸浮液或組合物或治療性組合物中添加的,以維持其處於穩定或不變狀態的化學品或化合物;或者是因為其產生涉及原子或分子的改變,導致更穩定的或不變的狀態所以使用的化學品或化合物。
術語「聚集物」或「聚集」在本文中意指聚攏到一起,或集合成團或成整體,例如,如在肽、多肽、抗體或其變體的聚集中。聚集物可以自我聚集,或由於其他因素而聚集,例如聚集劑,沉澱劑、攪拌或其他手段和方法,從而導致肽、多肽、抗體或其變體聚攏到一起。
攪拌誘導的聚集是在含有蛋白質的溶液中由攪拌誘導的聚集物形成,其中攪拌是由振蕩或攪動引發的運動。
「易於聚集」的抗體是被觀察到與其他抗體分子聚集的抗體,尤其是在攪拌的條件下。
「抑制」由攪拌誘導的聚集意指防止、降低或減少由攪拌誘導的聚集的量,是通過比較在包含至少一種攪拌誘導的聚集的抑制劑的含有蛋白質的溶液中存在的聚集物的量,和不包含至少一種攪拌誘導的聚集的抑制劑的含有蛋白質的溶液中存在的聚集物的量來測量的。
攪拌誘導的聚集的抑制量是抑制攪拌誘導的聚集的量。
可用於本發明中用於測量攪拌誘導的聚集的方法包括凝膠電泳、等電聚焦、毛細管電泳、層析如尺寸排阻層析、離子交換層析和逆向高性能液相層析、肽作圖、寡糖作圖、質譜、紫外吸收光譜學、螢光光譜學、圓二色光譜學、等溫滴定量熱法、差示掃描量熱法、分析超速離心、動態光散射、蛋白水解和交聯、濁度測量、過濾阻滯測定、免疫測定、螢光染料結合測定、蛋白質染色測定、顯微術和通過elisa或其他結合測定檢測聚集。
「等滲」製劑是具有與人血液基本相同的滲透壓的製劑。等滲製劑一般具有從約250至350mosm的滲透壓。術語「低滲」描述了具有低於人血液的滲透壓的滲透壓的製劑。相應地,術語「高滲」用於描述具有高於人血液的滲透壓的滲透壓的製劑。例如可以使用蒸汽壓或冰凍型滲壓計測量等滲性。由於添加鹽和/或緩衝液的結果,本發明的製劑是高滲的。
「重構的」製劑是通過在稀釋劑中溶解凍幹的蛋白質或抗體製劑使得所述蛋白質分散在重構的製劑中而製備的製劑。重構的製劑適合向待用目標蛋白質治療的患者施用(例如,腸胃外施用),在本發明的某些實施方案中,可以是適合皮下施用的重構的製劑。
「表面活性劑」是可以在固體-固體、固體-液體、液體-液體和液體-氣體的表面發揮效果的表面活性試劑,因為它們的化學組成含有親水性和疏水性基團。這些材料降低處於空氣-水和/或水固體界面處的稀釋的溶液中的蛋白質濃度,蛋白質可以吸附在所述界面處並可能聚集。表面活性劑可以結合到蛋白質製劑中的疏水界面上。由於蛋白質單層的解摺疊和之後的聚集,特別地當攪拌時水表面上的蛋白質將聚集。
「表面活性劑」可以使蛋白質變性,但也可以使其對於表面變性穩定。一般而言,離子型表面活性劑可以使蛋白質變性。然而,即使在相對高濃度(1%w/v)的條件下,非離子型表面活性劑一般不使蛋白質變性。大部分親代可接受的非離子型表面活性劑來自聚山梨酸酯或聚醚類。聚山梨酸酯20和80是上市的蛋白質製劑中的當代的表面活性劑穩定劑。然而,蛋白質製劑中使用的其他表面活性劑包括pluronicf-68和「brij」類的成員。非離子型表面活性劑可以是基於糖的。基於糖的表面活性劑可以是烷基糖苷類。烷基糖苷的一般結構是r1-o-(ch2)x-r,其中r獨立地是ch3或環己基(c6h11),r1獨立地是葡萄糖或麥芽糖。示例性的烷基糖苷類包括這樣的烷基糖苷,其中r1是葡萄糖,r是ch3,並且x是5(n-己基-β-d-吡喃葡萄糖苷)、x是6(n-庚基-β-d-吡喃葡萄糖苷)、x是7(n-辛基-β-d-吡喃葡萄糖苷)、x是8(n-壬基-β-d-吡喃葡萄糖苷)、x是9(n-癸基-β-d-吡喃葡萄糖苷)和x是11(n-十二烷基-β-d-吡喃葡萄糖苷)。有時吡喃葡萄糖苷被稱為葡萄糖苷。示例性的烷基糖苷類還包括這樣的烷基糖苷,其中r1是麥芽糖,r是ch3,並且x是5(n-己基-β-d-吡喃麥芽糖苷)、x是7(n-辛基-β-d-吡喃麥芽糖苷)、x是8(n-壬基-β-d-吡喃麥芽糖苷)、x是9(n-癸基-β-d-吡喃麥芽糖苷)、x是10(n-十一烷基-β-d-吡喃麥芽糖苷)、x是11(n-十二烷基-β-d-吡喃麥芽糖苷)、x是12(n-十三烷基-β-d-吡喃麥芽糖苷)、x是13(n-十四烷基-β-d-吡喃麥芽糖苷),和x是15(n-十六烷基-β-d-吡喃麥芽糖苷)。有時吡喃麥芽糖苷被稱為麥芽糖苷。示例性的烷基糖苷類還包括這樣的烷基糖苷,其中r1是葡萄糖,x是3,並且r是環己基(3-環己基-1-丙基-β-d-葡萄糖苷);其中r1是麥芽糖,x是4,和r是環己基(4-環己基-1-丁基-β-d-麥芽糖苷)。
「可藥用的酸」包括在配製的濃度和方式下無毒的無機酸和有機酸。例如,合適的無機酸包括鹽酸、高氯酸、氫溴酸、氫碘酸、硝酸、硫酸、磺酸、亞磺酸、磺胺酸、磷酸、碳酸等。合適的有機酸包括直鏈和支鏈的烷烴的、芳香烴的、環烴的、脂環族的、芳香脂肪族的、雜環的、飽和的、不飽和的、單、二和三羧酸,包括例如甲酸、乙酸、2-羥基乙酸、三氟乙酸、苯乙酸、三甲基乙酸、t-丁基乙酸、氨基苯甲酸、丙酸、2-羥基丙酸、2-氧基丙酸、丙二酸、環戊基丙酸、環戊基丙酸、3-苯基丙酸、丁酸、丁二酸、苯甲酸、3-(4-羥基苯甲醯基)苯甲酸、2-乙醯氧基-苯甲酸、抗壞血酸、肉桂酸、十二烷基硫酸、硬脂酸、粘康酸、苦杏仁酸、琥珀酸、撲酸(embonicacid)、反丁烯二酸、蘋果酸、馬來酸、羥基馬來酸、丙二酸、乳酸、檸檬酸、酒石酸、乙醇酸、葡萄糖酸、葡糖酸、丙酮酸、乙醛酸、草酸、甲磺酸、琥珀酸、水楊酸、鄰苯二甲酸、palmoic、palmeic、硫氰酸、甲磺酸、乙磺酸、1,2-二乙磺酸、2-羥基乙磺酸、苯磺酸、4-氯苯磺酸、萘-2-磺酸、對甲基苯磺酸、樟腦磺酸、4-甲基雙環[2.2.2]-辛-2-烯-1-羧基、葡庚糖酸、4,4′-亞甲基雙-3-(羥基-2-烯-1-羧酸)、羥基萘甲酸。
「可藥用的鹼」包括在配製的濃度和方式下無毒的無機鹼和有機鹼。例如,合適的鹼包括從形成無機鹼的金屬所形成的鹼,例如鋰、鈉、鉀、鎂、鈣、銨、鐵、鋅、銅、錳、鋁、n-甲基葡糖胺、嗎啉、哌啶,以及有機無毒鹼包括伯胺、仲銨和叔胺、取代胺、環胺和鹼性離子交換樹脂(例如,n(r′)4+【其中r′獨立地是h或c1-4烷基,例如銨、tris)】,例如異丙胺、三甲胺、二乙胺、三乙胺、三丙胺、乙醇胺、2-二乙氨基乙醇、trimethamine、二環己胺、賴氨酸、精氨酸、組氨酸、咖啡鹼、普魯卡因、,hydrabamine、膽鹼、甜菜鹼、乙二胺、葡糖胺、甲基葡糖胺、可可鹼、嘌呤類、哌嗪、哌啶、n-乙基哌啶、聚胺樹脂等。特別優選的有機無毒鹼是異丙胺、二乙胺、乙醇胺、trimethamine,雙環己胺、膽鹼和咖啡鹼。
可用於本發明的其他可藥用的酸和鹼包括源自胺基酸(例如組氨酸、甘氨酸、苯丙氨酸、天冬氨酸、穀氨酸、賴氨酸和天冬醯胺)的酸和鹼。
「可藥用的」緩衝液和鹽包括源自上述酸和鹼的酸和鹼加成鹽的。特定的緩衝液和/或鹽包括組氨酸、琥珀酸鹽和乙酸鹽。
「凍幹保護劑」是這樣的分子,當所述分子與目標蛋白組合時,顯著防止或降低蛋白質在凍幹和後續儲藏時的物理化學不穩定性。示例性的凍幹保護劑包括糖及其相應的糖醇;胺基酸,例如穀氨酸一鈉或組氨酸;甲胺,例如甜菜鹼;易溶鹽,例如硫酸鎂;多元醇,例如三羥的或更高分子量的糖醇,例如甘油、葡聚糖、赤蘚糖醇、丙三醇、阿拉伯糖醇、木糖醇、山梨糖醇和甘露糖醇;丙二醇;聚乙二醇;;及其組合。其他示例性的凍幹保護劑包括丙三醇和明膠,以及糖類蜜二糖、松三糖、棉子糖、甘露三糖和水蘇糖。還原性糖的實例包括葡萄糖、麥芽糖、乳糖、麥芽酮糖、異麥芽酮糖和乳果糖。非還原性糖的實例包括選自糖醇和其他直鏈多元醇的多羥基化合物的非還原性糖苷。優選的糖醇是單糖苷,尤其是通過還原二糖(例如乳糖、麥芽糖、乳果糖和麥芽酮糖)獲得的化合物。糖苷的側鏈基團可以是葡萄糖苷或半乳糖苷。糖醇的其他實例是葡萄糖醇、麥芽糖醇、乳糖醇和異麥芽酮糖。優選的凍幹保護劑是非還原性糖海藻糖或蔗糖。
以「凍幹保護的量」將凍幹保護劑加入到預凍幹的製劑中,這意味著,在存在凍幹保護量的凍幹保護劑的條件下凍幹蛋白質後,在凍幹和儲藏時,蛋白質基本保持了它的物理化學穩定性。
「可藥用的糖」是這樣的分子,當其與目標蛋白組合時,顯著防止或降低蛋白質在儲藏時的物理化學不穩定性。當打算將製劑凍幹並然後重構時,「可藥用的糖」也被稱為「凍幹保護劑」。示例性的糖及其相應的糖醇包括:胺基酸,例如穀氨酸鈉或組氨酸;甲胺,例如甜菜鹼;易溶鹽,例如硫酸鎂;多元醇,例如三羥的或更高分子量的糖醇,例如甘油、葡聚糖、赤蘚糖醇、丙三醇、阿拉伯糖醇、木糖醇、山梨糖醇和甘露糖醇;丙二醇;聚乙二醇;;及其組合。其他示例性的凍幹保護劑包括丙三醇和明膠,以及糖類蜜二糖、松三糖、棉子糖、甘露三糖和水蘇糖。還原性糖的實例包括葡萄糖、麥芽糖、乳糖、麥芽酮糖、異麥芽酮糖和乳果糖。非還原性糖的實例包括選自糖醇和其他直鏈多元醇的多羥基化合物的非還原性糖苷。優選的糖醇是單糖苷,尤其是通過還原二糖(例如乳糖、麥芽糖、乳果糖和麥芽酮糖)獲得的化合物。糖苷的側鏈基團可以是葡萄糖苷或半乳糖苷。糖醇的其他實例是葡萄糖醇、麥芽糖醇、乳糖醇和異麥芽酮糖。優選的凍幹保護劑是非還原性糖海藻糖或蔗糖。
以「保護量」將可藥用的糖加入到(例如,預凍幹)製劑中,意味著在儲藏過程中(例如,重構和儲藏後),蛋白質基本保持了它的物理化學穩定性。
本文中的目標「稀釋劑」是可藥用的(對於施用給人是安全無毒的),並且對於製備液體製劑(例如凍幹後重構的製劑)是有用的。示例性的稀釋劑包括無菌水、注射用抑菌水(bwfi)、ph緩衝溶液(例如,磷酸鹽緩衝的鹽水)、無菌鹽溶液、ringer溶液或葡萄糖[溶液。在備選的實施方案中,稀釋劑可包括鹽的水性溶液和/或緩衝液。
「防腐劑」是能夠添加到本文的製劑中以降低細菌活性的化合物。例如,添加防腐劑可以促進多次使用(多劑量)製劑的生產。潛在的防腐劑的實例包括十八烷基二甲基苄基氯化銨、氯化六甲銨、氯化苯甲烷銨(烷基苄基二甲基氯化銨的混合物,其中烷基是長鏈化合物)和苯索氯銨。其他類型的防腐劑包括芳香醇,例如苯酚、丁醇和苯甲醇,烷基對羥基苯甲酸酯類如甲基或丙基對羥基苯甲酸酯、兒茶酚、雷瑣酚、環己醇、3-戊醇和間甲酚。本文中最優選的防腐劑是苯甲醇。
「治療」指療法性治療和預防性或防止性措施。需要治療的包括已患疾病的,以及需要防止病症的。
用於治療目的的「哺乳動物」指任何分類為哺乳動物的動物,包括人,馴養的和農場動物,以及動物園、體育運動或寵物動物,如狗、馬、兔、牛、豬、倉鼠、沙鼠、小鼠、雪貂、大鼠、貓等。優選地,哺乳動物是人。
「病症」是受益於用蛋白質治療的任何病況。包括慢性和急性病症或疾病,包括那些誘使哺乳動物患所討論的病症的病理學病況。本文治療的病症的非限制性實例包括癌症和炎症。
「治療有效量」是產生對特定的病症的可測量的改善或防止特定的病症至少所需的最低濃度。已知蛋白質的治療有效量是本領域普遍已知的,而後文發現的蛋白質的治療有效量可以通過本領域技術人員(例如普通醫生)普遍已知的標準技術確定。
按本文所述配製的抗體(包括與毒素綴合的抗體)和其他蛋白質的製備方法是本領域普遍已知的,詳細描述在例如wo2007/001851中。
可以按照本發明以水性或凍幹的形式配製抗體和其他蛋白質,所述凍幹的形式能夠重構為水性的形式。
本文描述的製劑可以製備為重構的凍幹製劑。將本文描述的蛋白質或抗體凍幹,然後重構以生產本發明的液體製劑。在該特別的實施方案中,在如上所述製備目標蛋白後,生產了「預凍幹的」製劑。考慮所需的劑量體積、施用模式等,測定存在於預凍幹的製劑中的蛋白質的量。例如,完整抗體的起始濃度可以是從約2mg/ml至約50mg/ml,優選從約5mg/ml至約40mg/ml並且最優選從約20-30mg/ml。
待配製的蛋白質一般存在於溶液中。例如,在本發明的液體製劑中,蛋白質可以存在於ph從約4-8,並且優選約5-7的ph緩衝溶液中。緩衝液濃度可以是從約1mm至約20mm,備選地從約3mm至約15mm,取決於例如緩衝液和製劑的(例如,重構製劑的)所需的滲漲度(tonicity)。示例性的緩衝液和/或鹽是可藥用的,並且可以由合適的酸、鹼及其鹽產生,例如在「可藥用的」酸、鹼或緩衝液下定義的那些。
在一個實施方案中,向預凍幹的製劑中添加凍幹保護劑。預凍幹的製劑中的凍幹保護劑的量一般使重構後所獲得的製劑是等滲的。然而,高滲的重構製劑也可能是合適的。此外,凍幹保護劑的量不能太低,使得在凍幹時發生不可接受的量的蛋白質降解/聚集。然而,在預凍幹製劑中的示例性凍幹保護劑濃度是從約10mm至約400mm,備選地從約30mm至約300mm,備選地從約50mm至約100mm。示例性的凍幹保護劑包括糖和糖醇,例如蔗糖、甘露糖、海藻糖、葡萄糖、山梨糖醇、甘露糖醇。然而,在特定環境下,某些凍幹保護劑也可以對增加製劑的粘度有作用。因此,需要小心選擇特定的凍幹保護劑,其使該效果最小化或中和該效果。在上文的「凍幹保護劑」的定義中描述了其他的凍幹保護劑,其在本文中也被稱為「可藥用的糖」。
對於每種特定的蛋白質或抗體和凍幹保護劑的組合而言,蛋白質與凍幹保護劑的比例可以變化。在選擇抗體作為蛋白質和糖(例如,蔗糖或海藻糖)作為凍幹保護劑,用於生成具有高蛋白質濃度的等滲重構的製劑的情況下,凍幹保護劑與抗體的摩爾比可以是從約100至約1500摩爾凍幹保護劑比1摩爾抗體,和優選地從約200至約1000摩爾凍幹保護劑比1摩爾抗體,例如從約200至約600摩爾凍幹保護劑比1摩爾抗體。
凍幹保護劑(例如,蔗糖或海藻糖)和增量劑(例如,甘露糖醇或甘油)的混合物可用於製備預凍幹製劑。增量劑可以允許生產均勻的凍幹餅,其中不含過多的孔穴等。其他可藥用的載體、賦形劑或穩定劑,例如remington′spharmaceuticalsciences第16版,osol,a.編著(1980)中所述,也可以包括在預凍幹的製劑(和/或凍幹的製劑和/或重構的製劑)中,只要它們不對製劑的所需特徵產生不利影響。可接受的載體、賦形劑或穩定劑在所使用的劑量和濃度下對受體是無毒的,包括:其他緩衝劑;防腐劑;共溶劑;抗氧化劑,包括抗壞血酸和甲硫氨酸;螯合劑如edta;金屬複合物(例如,zn-蛋白質複合物);可生物降解的聚合物,如聚酯;和/或成鹽的抗衡離子,例如鈉。
本文中的製劑還可以含有多於一種的、治療特別指徵所必需的蛋白質,優選地具有對其他蛋白質沒有不利影響的互補活性的蛋白質。例如,在單個製劑中提供結合所需的靶(例如,受體或抗原)的兩種或多種抗體是理想的。此類蛋白質以對預期目的有效的量合適地組合存在。
體內施用所使用的製劑必需是無菌的。可以通過在凍幹和重構之前或之後無菌濾膜過濾,來方便的實現。備選地,可以通過例如將除蛋白質以外的成分在約120℃高壓滅菌約30分鐘,實現對整個混合物的滅菌。
在將蛋白質、任選的凍幹保護劑和其他任選的組分一起混合後,將製劑凍幹。有多種不同的凍幹機可用於該目的,例如hull50tm(hull,美國)或gt20tm(leybold-heraeus,德國)凍幹機。凍幹是通過冷凍製劑,並且隨後在適合初步乾燥的溫度下使冰從冰凍內含物中升華來實現的。在該條件下,產品溫度低於製劑的共晶點或塌陷溫度。通常,在合適的壓力下(通常是從約50-250mtorr),初步乾燥的貯存溫度(shelftemperature)範圍是從約-30至25℃(條件是產物在初步乾燥的過程中保持冷凍)。製劑、裝有樣品的容器(例如,玻璃瓶)的大小和類型,以及液體的體積,將主要決定乾燥所需的時間,所述時間範圍從若干小時至若干天(例如,40-60hrs)。任選地,取決於產品中所需的剩餘溼度水平,還可以實施次級乾燥階段。實施次級乾燥的溫度是在約0-40℃的範圍,主要取決於容器的類型和大小,和所使用的蛋白質的類型。例如,凍幹的整個除水階段的貯存溫度可以是從約15-30℃(例如,約20℃)。次級乾燥所需的時間和壓力是生產合適的凍幹餅的時間和壓力,取決於例如溫度和其他的參數。次級乾燥的時間由產物中所需的剩餘溼度水平決定,通常需要至少約5小時(例如,10-15小時)。壓力可以與初級乾燥步驟過程中使用的壓力相同。根據製劑和瓶大小,冷凍乾燥條件可以變化。
在向患者施用前,用可藥用的稀釋劑重構凍幹的製劑,使重構的製劑中的蛋白質濃度是至少約50mg/ml,例如從約50mg/ml至約400mg/ml,備選地從約80mg/ml至約300mg/ml,備選地從約90mg/ml至約150mg/ml。當需要皮下遞送重構的製劑時,重構的製劑中的此類高蛋白質濃度被認為是特別有用的。然而,對於其他施用途徑,例如靜脈內施用,重構的製劑中較低的蛋白質濃度可為理想的(例如,在重構的製劑中從約5-50mg/ml,或從約10-40mg/ml蛋白質)。在某些實施方案中,重構的製劑中的蛋白質濃度顯著高於預凍幹的製劑中的蛋白質濃度。例如,重構的製劑中的蛋白質濃度可以是預凍幹的製劑中的濃度的約2-40倍,備選地3-10倍,備選地3-6倍(例如,至少3倍或至少4倍)。
重構一般發生在約25℃的溫度下,以保證充分水合,但需要時也可以使用其他溫度。重構所需的時間取決於例如稀釋劑的類型、賦形劑和蛋白質的量。示例性的稀釋劑包括無菌水、注射用抑菌水(bwf)、ph緩衝溶液(例如,磷酸鹽緩衝鹽水)、無菌鹽溶液、ringer溶液或葡萄糖溶液。稀釋劑任選地含有防腐劑。示例性的防腐劑如上所述,優選的防腐劑是芳香醇,例如苯甲醇或酚醇。所使用的防腐劑的量通過評估不同防腐劑濃度與蛋白質的相容性和防腐效力測試來決定。例如,如果防腐劑是芳香醇(例如,苯甲醇),它可以以從約0.1-2.0%,並且優選地從約0.5-1.5%,但最優選地從約1.0-1.2%的量存在。
優選的,每小瓶重構的製劑具有少於6000個、大小≥10μm的顆粒。
通過混合具有所需的純度的活性成分和任選的可藥用的載體、賦形劑或穩定劑,製備用於儲藏的治療性製劑(remington′spharmaceuticalsciences,第18版,mackpublishingco.,easton,pa.18042[1990])。可接受的載體、賦形劑或穩定劑在所使用的劑量和濃度下,對受體是無毒的,並包括緩衝劑;抗氧化劑,包括抗壞血酸、甲硫氨酸、維生素e、偏亞硫酸氫鈉、防腐劑、isotonicifier、穩定劑、金屬複合物(例如,zn-蛋白質複合物),和/或螯合劑,例如edta。
當治療劑是抗體片段時,特異性結合靶蛋白的結合結構域的最小片段是優選的。例如,基於抗體的可變區序列,可以設計保留結合靶蛋白序列的能力的抗體片段,或者甚至肽分子。此類肽可以是化學合成的和/或通過重組dna技術生產的(參見例如,marasco等人,proc.natl.acad.sci.usa90:7889-7893[1993])。
緩衝液用於控制ph在優化治療效果的範圍內,尤其是當穩定性是ph依賴性的情況下。緩衝液優選以從約50mm至約250mm的濃度存在。用於本發明的合適的緩衝劑包括有機酸和無機酸,及其鹽。例如,檸檬酸、磷酸、琥珀酸、酒石酸、延胡索酸、葡萄糖酸、草酸、乳酸、乙酸。此外,緩衝液可以由組氨酸和三甲基胺鹽如tris組成。
添加防腐劑以延緩微生物生長,通常以從0.2%-1.0%(w/v)的範圍存在。用於本發明的合適的防腐劑包括十八烷基二甲基苄基氯化銨、氯化六甲銨、苯甲烴銨滷化物(例如氯、溴、碘)、苯索氯銨、硫柳汞、苯酚、丁醇或苯甲醇;烷基對羥基苯甲酸酯類例如甲基或丙基對羥基苯甲酸酯;兒茶酚、雷瑣酚、環己醇、3-戊醇和間甲苯酚。
存在滲漲度劑,有時被稱為「穩定劑」,用於調節或維持液體組合物的滲透壓。當與大的帶電生物分子(例如蛋白質和抗體)使用時,通常被稱為「穩定劑」是因為它們可以與胺基酸側鏈的帶電基團相互作用,從而減少分子間和分子內相互作用的可能性。考慮其他成分的相對量,滲漲度劑存在的量可以是按重量計在0.1%至25%之間的任何量,優選1至5%。優選的滲漲度劑包括多羥基糖醇,優選三羥基或更多的糖醇,例如甘油、赤蘚糖醇、阿拉伯糖醇、木糖醇、山梨糖醇和甘露糖醇。
其他賦形劑包括可用作一種或多種下列物質的活性劑:(1)增量劑,(2)溶解性增強劑,(3)穩定劑和(4)防止變性或吸附到容器壁上的活性劑。此類賦形劑包括:多羥基糖醇(以上枚舉的);胺基酸,如丙氨酸、甘氨酸、穀氨醯胺、天冬醯胺、組氨酸、精氨酸、賴氨酸、鳥氨酸、亮氨酸、2-苯丙氨酸、穀氨酸、蘇氨酸等;有機糖或糖醇,如蔗糖、乳糖、乳糖醇、海藻糖、水蘇糖、甘露糖、山梨糖、木糖、核糖、核糖醇、myoinisitose、myoinisitol、半乳糖、半乳糖醇、甘油、環多醇(例如,肌醇)聚乙二醇;含有硫的還原劑,例如尿素、穀胱甘肽、硫辛酸、巰基乙酸鈉、硫代甘油、α-單硫代甘油和硫代硫酸鈉;低分子量蛋白,如人血清白蛋白、牛血清白蛋白、明膠或其他免疫球蛋白;親水聚合物如聚乙烯吡咯烷酮;單糖(例如,木糖、甘露糖、果糖、葡萄糖;二糖(例如,乳糖、麥芽糖、蔗糖);三糖例如棉子糖;和多糖例如糊精或葡聚糖。
為了體外施用製劑,其必須是無菌的。可以通過無菌濾膜過濾使製劑無菌。本文中的治療性組合物一般放在具有無菌進入口的容器中,例如靜脈內輸液袋或具有可以用皮下注射針頭穿刺的瓶塞的小瓶。
施用途徑是根據已知的和可接受的方法的,如,通過單次或多次大丸劑或以合適的方式在較長時間段灌注,例如,通過皮下、靜脈內、腹膜內、肌肉內、動脈內、損害內或關節內的途徑注射或灌注、局部施用、吸入、持續釋放或緩釋的方式。
本文中的製劑還可以含有一種以上的、治療特定指徵必需的活性化合物,優選具有互補活性的、不彼此不利地影響的那些化合物。備選地或額外地,組合物可以包含細胞毒性劑、細胞因子或生長抑制劑。此類分子以對預期目的有效的量合適地組合存在。
活性成分還可以包載在通過例如凝聚技術或界面聚合所製備的微膠囊,例如羥甲基纖維素或明膠微膠囊和多聚(甲基丙烯酸甲酯)微膠囊,分別在膠體藥物遞送系統(例如,脂質體、白蛋白微球、微乳劑、納米顆粒和納米膠囊)或粗乳劑中。此類技術公布在remington′spharmaceuticalsciences,第18版中,見上文。
可以製備持續釋放的製品。持續釋放的製品的合適實例包括含有抗體的固體疏水聚合物的半滲透性基質,所述基質為成形製品的形式,例如膜狀或微膠囊狀。持續釋放的基質的實例包括聚酯、水凝膠(例如,聚(2-羥乙基-甲基丙烯酸),或聚(乙烯醇))、聚乳酸(美國專利號3,773,919)、l-穀氨酸和γ-乙基-l-穀氨酸酯的共聚物、不可降解的乙烯-醋酸乙烯酯、可降解的乳酸-乙醇酸共聚物,如luprondepottm(由乳酸-乙醇酸共聚物和亮氨醯脯氨酸醋酸鹽組成的可注射微球)和聚-d-(-)-3-羥基丁酸。已經用人生長激素(rhgh)、幹擾素-(rhifn-)、白介素-2和mnrpg120成功地實施了重組蛋白的微膠囊化,用於持續釋放。johnson等人,nat.med.2:795-799(1996);yasuda等人,biomed.ther.27:1221-1223(1993);hora等人,bio/technology8:755-758(1990);cleland,″designandproductionofsingleimmunizationvaccinesusingpolylactidepolyglycolidemicrospheresystems,″invaccinedesign:thesubunitandadjuvantapproach,powell和newman編著(plenumpress:newyork,1995),第439-462頁;wo97/03692;wo96/40072;wo96/07399;和美國專利號5,654,010。
由於其生物相容性和廣泛的生物可降解的性質,可以使用聚乳酸-羥基乙酸共聚物(plga)聚合物開發這些蛋白質的持續釋放的製劑。plga的降解產物——乳酸和羥基乙酸,可以在人體內快速清除。此外,可以根據其分子量和組成,從數月至數年調節該聚合物的可降解性。lewis,″controlledreleaseofbioactiveagentsfromlactide/glycolidepolymer″,在biodegradablepolymersasdrugdeliverysystems(marceldekker;newyork,1990),m.chasin和r.langer(編著)第1-41頁。
聚合物(如乙烯-醋酸乙烯酯和乳酸-羥基乙酸)使得分子能夠在100天的時間釋放,而某些水凝膠則在較短的時間段釋放蛋白質。當膠囊化的抗體在體內長時間存留時,它們可能由於暴露在37℃的溼度下而變性或聚集,導致喪失生物學活性,並可能改變免疫原性。可以根據所涉及的機制來設計理性的對策用於穩定化。例如,如果發現聚集機制是通過二硫鍵交換而形成分子間s-s鍵,則可以通過修飾巰基殘基、從酸性溶液凍幹、控制含溼量、使用恰當的添加劑和開發特定的聚合物基質組合物,來實現穩定化。
脂質體或類蛋白質組合物還可用於配製本文公布的蛋白質或抗體。參見美國專利號4,925,673和5,013,556。
可以通過使用無毒的「水溶性多價金屬鹽」增強本文描述的蛋白質和抗體的穩定性。實例包括ca2+、mg2+、zn2+、fe2+、fe3+、cu2+、sn2+、sn3+、al2+和al3+。可以與上述多價金屬陽離子形成水溶性鹽的陰離子實例包括從無機酸和/或有機酸形成的陰離子。此類水溶性鹽在水中(20℃時)具有至少約20mg/ml,備選地至少約100mg/ml,備選地至少約200mg/ml的溶解度。
可用於形成「水溶性多價金屬鹽」的合適的無機酸包括鹽酸、醋酸、硫酸、硝酸、硫氰酸和磷酸。可以使用的合適有機酸包括脂肪族羧酸和芳香族酸。該定義內的脂肪族酸可被定義為飽和的或不飽和的c2-9羧酸(例如,脂肪族單羧酸、二羧酸和三羧酸)。例如,該定義內的單羧酸包括飽和的c2-9單羧酸乙酸、丙酸、丁酸、戊酸、己酸、庚酸、辛酸、壬酸和capryonic,而不飽和的c2-9單羧酸丙烯酸、propriolic甲基丙烯酸、丁烯酸和異丁烯酸。示例性的二羧酸包括飽和的c2-9二羧酸丙二酸、琥珀酸、戊二酸、己二酸和庚二酸,而不飽和的c2-9二羧酸包括馬來酸、延胡索酸、檸康酸和甲基延胡索酸。示例性的三羧酸包括飽和的c2-9三羧酸丙三羧酸和1,2,3-丁三羧酸。此外,該定義的羧酸還可以含有一個或兩個羥基,形成羥基羧酸。示例性的羥基羧酸包括乙醇酸、乳酸、甘油酸、羥基丙二酸、蘋果酸、酒石酸和檸檬酸。該定義內的芳香酸包括苯甲酸和水楊酸。
可用於幫助穩定本發明的膠囊化的多肽的常用水溶性多價金屬鹽包括例如:(1)無機酸金屬鹽滷化物(例如,氯化鋅、氯化鈣)、硫酸鹽、硝酸鹽、磷酸鹽和硫氰酸鹽;(2)脂肪族羧酸金屬鹽(例如,醋酸鈣、醋酸鋅、丙酸鈣、乳酸鋅和酒石酸鋅);和(3)苯甲酸鹽的芳香族羧酸金屬鹽(例如,苯甲酸鋅)和水楊酸鹽。
為了預防或治療疾病,活性劑的恰當劑量取決於如上所定義的的待治療的疾病的類型、疾病的嚴重程度和病程、是出於預防還是治療目的施用活性劑、先前的療法、患者的臨床史和對活性劑的應答,以及主治醫生的自主裁量。適合以一次或在系列治療中對患者施用活性劑。
本發明的方法可與治療病症的已知方法組合,作為組合的或額外的治療步驟,或者作為療法製劑的額外組分。
本發明的藥物組合物的劑量和所需的藥物濃度可以取決於預期的特定用途而改變。確定恰當的劑量或施用途徑為本領域普通技術人員所知曉。動物實驗提供了用於確定人類療法的有效劑量的可靠指導。可以遵循mordenti,j.和chappell,w.″theuseofinterspeciesscalingintoxicokinetics,″intoxicokineticsandnewdrugdevelopment,yacobi等人編著,pergamonpress,newyork1989,第42-46頁設置的規則,實施有效劑量的種間類推(interspeciesscaling)。
當體內施用本文所述多肽或抗體時,普通劑量可以是每天從約10ng/kg哺乳動物體重多至約100mg/kg哺乳動物體重或更多,優選約1mg/kg/天至10mg/kg/天,取決於施用途徑。文獻中提供了對特定劑量和遞送方法的指導;參見例如美國專利號4,657,760;5,206,344或5,225,212。以下內容也落入本發明的範圍內,即,不同的製劑對於不同的治療和不同的病症是有效的,且預期用來治療特定器官或組織的施藥可能需要以不同於對另一種器官或組織的施藥方式的方式來遞送。此外,可以通過一次或多次分開的施用或通過連續灌注來施用劑量。對於在若干天或更久的時間的重複施藥,根據病況,持續治療直到出現對疾病症狀的理想抑制作用。然而,其他劑量方案也可以是有用的。通過常規技術和測定,可以方便地監控該療法的進展。
根據已知的方法,向需要用蛋白質治療的哺乳動物(優選人)施用本發明的製劑(包括但不限於重構的製劑),如作為大丸劑或通過連續灌注一段時間靜脈內施用,通過肌肉內、腹膜內、腦脊髓內、皮下、動脈內、滑膜腔內、鞘膜內、口服、局部或吸入的途徑。
在優選的實施方案中,製劑通過皮下(即,皮膚下)施用給哺乳動物。出於此類目的,可以使用注射器注射製劑。然而,用於施用製劑的其他裝置也是可獲得的,例如注射裝置(例如,inject-easetm和genjecttm裝置);注射筆(例如genpentm);自動注射裝置、無針裝置(例如,medijectortm和biojectortm);和皮下膜片(patch)遞送系統。
在具體的實施方案中,本發明涉及用於單劑量施藥單元的試劑盒。此類試劑盒包含治療性蛋白質或抗體的水性製劑的容器,包括單室或多室的預填充注射器。示例性的預填充注射器可獲得自vettergmbh,ravensburg,德國。
蛋白質的恰當劑量(「療法有效量」)取決於,例如,待治療的病況,病況的嚴重程度和病程,蛋白質是出於預防還是治療目的施用的,先前療法,患者的臨床史和對蛋白質的應答性,所使用的蛋白質類型,和主治醫生的自由裁量。以一次或經過系列治療對患者合適地施用蛋白質,而且可以在診斷後任何的時間對患者施用蛋白質。蛋白質可以作為唯一治療施用,或者與對於治療考慮的病況有用的其他藥物或療法聯合施用。
當所選擇的蛋白質是抗體時,對患者施用的初始候選劑量是從約0.1-20mg/kg,例如,通過一次或多次分開的施用。然而,其他劑量方案也可以是有用的。通過常規技術可以方便地監控該療法的進展。
在本發明的另一個實施方案中,提供了含有製劑、並且優選地提供了關於其使用說明書的製品。製品包含容器。合適的容器包括例如瓶、小瓶(例如,雙室小瓶)、注射器(例如,單室或雙室注射器)和試管。容器可以由多種材料形成,例如玻璃或塑料。裝有製劑的容器上或與容器相關聯的標籤可以指明重構或使用的說明。標籤還可以表明製劑是用於皮下施用或預期用於皮下施用的。裝有製劑的容器可以是多次使用的小瓶,其允許重複施用(例如,2-6次施用)重構的製劑。製品還可以包含第二個容器,其包含合適的稀釋劑(例如,bwfi)。在混合稀釋劑和凍幹的製劑後,重構的製劑中的蛋白質終濃度一般是至少50mg/ml。製品還可以包含基於商業和用戶的立場所需要的其他材料,包括其他緩衝液、稀釋劑、過濾器、針頭、注射器和具有使用說明的包裝說明書。
通過下列實施例將更全面的理解本發明。但其不應被視為對本發明範圍的限制。本公開內容全文的所有引用都明確地通過引用整合到本文中。
實施例1:對脂肪酸、聚山梨酸酯和poe山梨聚糖對蛋白質聚集的作用的研究
本實施例說明了聚山梨酸酯、脂肪酸和poe山梨聚糖如何影響水性溶液中的蛋白質聚集。
使用攪拌誘導的蛋白質聚集分析,評價poe山梨聚糖針對溶液中攪拌誘導的抗il13單克隆抗體的聚集的保護性作用。具體而言,在該研究中,製備與下列潛在的穩定化添加物組合的、含有1mg/ml抗il13單克隆抗體的緩衝溶液(20mmhis-oac,ph5.7):
(i)無添加物,對照;
(ii)月桂酸(29ppm);
(iii)月桂酸(29ppm)和聚山梨酸酯20(24ppm);
(iv)poe山梨聚糖20「(a+b+c+d=20)」(150ppm);
(v)poe山梨聚糖20「(a+b+c+d=20)」(150ppm)和聚山梨酸酯20(24ppm);
(vi)poe山梨聚糖20「(a+b+c+d=20)」(150ppm)和月桂酸(29ppm);
(vii)poe山梨聚糖20「(a+b+c+d=20)」(150ppm),月桂酸(29ppm)和聚山梨酸酯20(24ppm);
(viii)聚山梨酸酯20(24ppm)。
將9ml含有單克隆抗體的製劑存放到分開的15mlformavitrium小瓶(一式三份)中,密封小瓶,然後允許在臺式振蕩器上在室溫攪拌(70rpm)0小時、4小時或24小時。完成時,立即對每個小瓶的內含物進行uv光譜測定法分析(340-360nm),測量溶液的濁度。使用1cm路徑長度室和agilent8453uv分光光度計在25℃下獲得濁度。將在沒有蛋白質製劑生色團吸光的340、345、350、355和360nm處的吸光值進行平均,並可以測定不可溶的蛋白質聚集物的散射作用。在上述波長下的平均吸收值代表樣品的濁度。在這方面,本領域普遍已知含有蛋白質的溶液的濁度與溶液中蛋白質聚集的量直接且定量地相關(例如參見,dani等人,j.pharm.sci.,96(6):1504-1517(2007))。這些分析的結果顯示在圖1中。
圖1中顯示的數據表明,某些聚山梨酸酯降解物(包括脂肪酸、月桂酸)對水性溶液中的蛋白質穩定性具有不利的作用,並且在攪拌時引起蛋白質聚集。相反,向含有抗體的水性溶液中添加poe山梨聚糖防止了在攪拌時蛋白質聚集物的形成。因此,這些數據表明了poe山梨聚糖具有在攪拌時防止蛋白質聚集的作用,因此增強了溶液中的治療性蛋白質的穩定性。
實施例2:對poe山梨聚糖和peg對蛋白質聚集的作用的研究
本實施例說明了poe山梨聚糖和peg作為防止或降低蛋白質聚集的穩定劑的用途。
使用攪拌誘導蛋白質聚集分析,評價多種poe山梨聚糖和peg針對溶液中攪拌誘導的兩種單克隆抗體(抗il13和抗ige抗體)的聚集的保護性作用。
在這組研究中,製備含有1mg/ml抗il13抗體(20mmhis-oac,ph5.7)或抗ige抗體(his-hiscl,ph6.0)的緩衝溶液,其中具有下列添加物:
(i)無添加物,對照;
(ii)濃度為200ppm的poe山梨聚糖20「(a+b+c+d=20)」;
(iii)濃度為1000ppm的poe山梨聚糖20「(a+b+c+d=20)」;
(iv)濃度為5000ppm的poe山梨聚糖20「(a+b+c+d=20)」;
(v)濃度為200ppm的peg1000;
(vi)濃度為1000ppm的peg1000;
(vii)濃度為5000ppm的peg1000;
(viii)濃度為200ppm的peg6000;
(ix)濃度為1000ppm的peg6000;
(x)濃度為5000ppm的peg6000。
將9ml含有單克隆抗體的每種製劑存放到分開的15mlformavitrium小瓶(一式三份)中,密封小瓶,然後允許在臺式振蕩器上在室溫攪拌(70rpm)0小時、4小時或24小時。完成時,立即對每個小瓶的內含物進行下列分析,(a)uv光譜測定法分析,以測量過濾後的蛋白質濃度,(b)uv光譜測定法分析(340-360nm),以測量溶液的濁度,和(c)不透光度(lightobscuration)分析,用於測定蛋白質顆粒大小和分布。
a.uv光譜測定法測量蛋白質濃度
在如上所述進行振蕩後,立即過濾含有蛋白質的溶液,以移除蛋白質聚集物,然後通過uv光譜測定法確定濾液中的蛋白質濃度。蛋白質濃度數據是使用0.5或1cm路徑長度室和agilent8453uv分光光度計在25℃獲得的。在278nm處使用的消光係數e為1.45和1.60mlmg-1cm-1,來測定通過0.2μm注射器式濾器過濾後的抗體濃度。從在278nm處的吸光值中減去在320nm處的吸光值,來計算散射作用。在這方面,本領域普遍已知可以使用uv吸收分析定量地測量含有蛋白質的溶液中的蛋白質濃度(例如參見,liu等人,j.pharm.sci.,94(9):1928-1940(2005))。對於抗il13抗體和抗ige抗體獲得的數據的結果分別顯示在圖2和3中。
圖2和3中的數據表明,攪拌未處理的對照抗體製劑誘導可測量的並且顯著的聚集以及在過濾時的蛋白質損失。相反,添加全部測試的多種濃度的poe山梨聚糖或peg都防止攪拌誘導的蛋白質聚集物形成,並因此防止過濾時的蛋白質損失。這些數據表明,poe山梨聚糖和聚乙二醇通過防止或降低溶液中的蛋白質聚集物形成,而在水性溶液中作為有效的蛋白質穩定劑發揮功能。
b.uv光譜測定法測量溶液濁度
如上所述,在340-360nm處的uv光譜測定法提供了定量地測定溶液中存在的蛋白質聚集物的量的有效手段,其中濁度與存在的聚集的蛋白質的量直接相關。從抗il13抗體和抗ige抗體的濁度分析獲得的結果分別顯示在圖4和5中。
圖4和5中的數據表明,攪拌未處理的對照抗體製劑誘導其中可測量的和顯著的抗體聚集。相反,添加全部測試的多種濃度的poe山梨聚糖或peg都防止和/或降低了攪拌誘導的蛋白質聚集物形成。這些數據表明,poe山梨聚糖和聚乙二醇通過防止或降低溶液中的蛋白質聚集物形成,而在水性溶液中作為有效的蛋白質穩定劑發揮功能。
c.測定顆粒大小分布
還分析上述含有抗體的水性溶液,以測定其中含有的蛋白質的顆粒大小分布。具體而言,使用與hiac/royco3000a液體注射器採樣儀、hrld-150傳感器相連的hiac/royco9703液體顆粒計數器,在室溫下測量在2至50μm之間的不可溶的顆粒的數量和大小,並使用pacificspec2.0版軟體進行分析。檢測的上限是~18000顆粒/ml,並且超過該閾值的樣品經過恰當稀釋後進行測量。以每次注射1.0ml體積,測量每個樣品4次。丟棄第1次注射,從最後3次注射獲得平均值。在每次樣品分析之間,用注射用水清洗系統,至儀器的2μm顆粒計數<10。≥2、5、10、15、25、35和50μm的亞可見(sub-visible)的顆粒表示為每ml的累積計數。
從這些分析獲得的結果分別顯示在圖6-11中。圖6-11中的數據表明,攪拌未處理的對照抗體製劑誘導其中可測量的和顯著的抗體聚集。相反,添加全部測試的多種濃度的poe山梨聚糖或peg都防止和/或降低了攪拌誘導的蛋白質聚集物形成。這些數據表明,poe山梨聚糖和聚乙二醇通過防止或降低溶液中的蛋白質聚集物形成,而在水性溶液中作為有效的蛋白質穩定劑發揮功能。
