作為TRKA激酶抑制劑的1‑((3S,4R)‑4‑(3‑氟苯基)‑1‑(2‑甲氧基乙基)吡咯烷‑3‑基)‑3‑(4‑甲基‑3‑(2‑甲基嘧啶‑5‑基)‑1‑苯基‑1H‑吡唑‑5‑基)脲的製作方法
2023-05-23 02:50:01 2
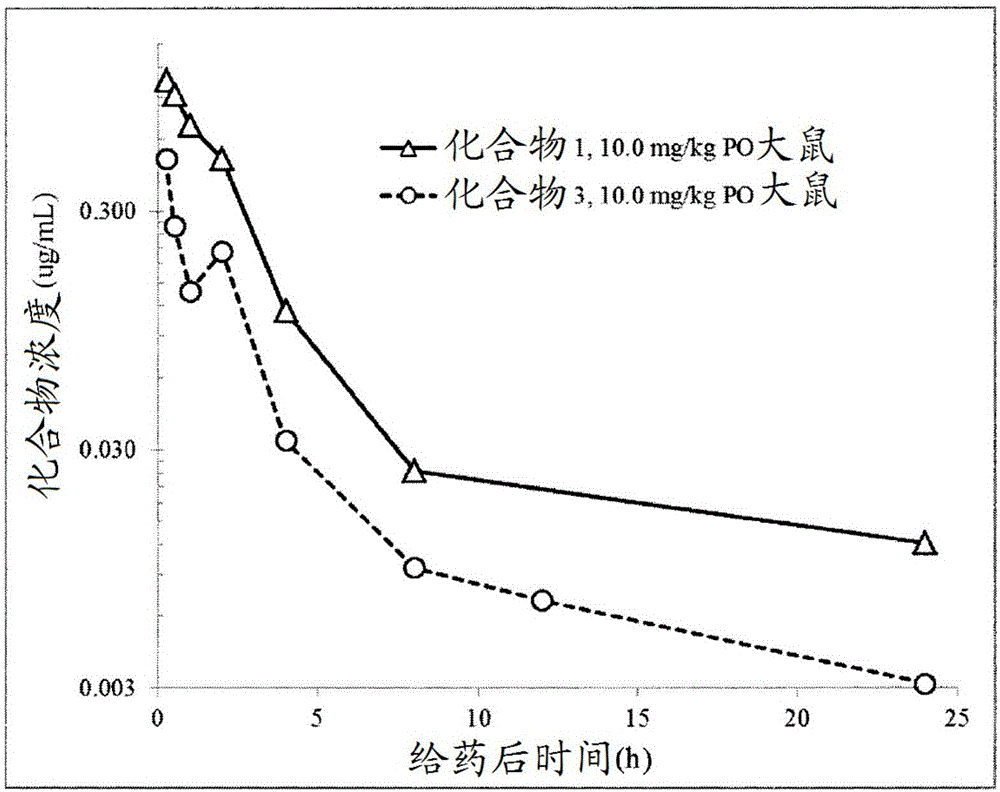
本發明涉及新型化合物、包含所述化合物的藥物組合物、用於製備所述化合物的方法和中間體以及所述化合物在療法中的用途。更具體地說,其涉及1-((3S,4R)-4-(3-氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-基)-3-(4-甲基-3-(2-甲基嘧啶-5-基)-1-苯基-1H-吡唑-5-基)脲或其藥學上可接受的鹽,其顯示出TrkA激酶抑制並且可用於治療疼痛、癌症、炎症/炎性疾病、神經變性疾病、某些感染性疾病、舍格倫氏症候群、子宮內膜異位、糖尿病性周圍神經病變、前列腺炎、盆腔疼痛症候群、與骨重塑調節失衡相關的疾病以及由結締組織生長因子異常信號傳導引起的疾病。用於疼痛疾患的現有治療方案利用若干類別的化合物。鴉片類(諸如嗎啡)具有若干缺點,包括催吐作用、便秘作用和負呼吸作用、以及成癮的可能性。非甾體抗炎止痛劑(NSAID,諸如COX-1或COX-2型)也具有包括治療劇痛功效不佳在內的缺點。另外,COX-1抑制劑可引起黏膜潰瘍。因此,持續需要用於減輕疼痛、特別是慢性疼痛的新型且更有效的治療。Trk′s類為由一組可溶性生長因子(稱為神經營養因子(NT))活化的高親和力受體酪氨酸激酶。Trk受體家族具有三個成員:TrkA、TrkB和TrkC。神經營養因子為(i)活化TrkA的神經生長因子(NGF)、(ii)活化TrkB的腦源性神經生長因子(BDNF)和NT-4/5和(iii)活化TrkC的NT3。Trk′s在神經元組織中廣泛表達並且涉及神經元細胞的維持、信號傳導和存活(Patapoutian,A.等,CurrentOpinioninNeurobiology,2001,11,272-280)。已證實Trk/神經營養因子途徑的抑制劑在許多疼痛的臨床前動物模型中是有效的。例如,已顯示拮抗性NGF和TrkA抗體諸如RN-624在炎性和神經性疼痛動物模型(Woolf,C.J.等,(1994)Neuroscience62,327-331;Zahn,P.K.等,(2004)J.Pain5,157-163;McMahon,S.B.等,(1995)Nat.Med.1,774-780;Ma,Q.P.和Woolf,C.J.(1997)NeuroReport8,807-810;Shelton,D.L.等,(2005)Pain116,8-16;Delafoy,L.等,(2003)Pain105,489-497;Lamb,K.等,(2003)Neurogastroenterol.Motil.15,355-361;Jaggar,S.I.等,(1999)Br.J.Anaesth.83,442-448)和神經性疼痛動物模型(Ramer,M.S.和Bisby,M.A.(1999)Eur.J.Neurosci.11,837-846;Ro,L.S.等(1999)Pain79,265-274;Herzberg,U.等,(1997)Neuroreport8,1613-1618;Theodosiou,M.等,(1999)Pain81,245-255;Li,L.等,(2003)Mol.Cell.Neurosci.23,232-250;Gwak,Y.S.等,(2003)Neurosci.Lett.336,117-120)中是有效的。還已顯示由腫瘤細胞和腫瘤侵入巨噬細胞分泌的NGF直接刺激位於周圍疼痛纖維上的TrkA。使用小鼠和大鼠中的各種腫瘤模型,已證實用單克隆抗體中和NGF抑制癌症相關疼痛至類似於或超過嗎啡最高耐受劑量的程度。因為TrkA激酶可充當NGF驅動性生物反應的中介物,所以TrkA和/或其他Trk激酶的抑制劑可提供一種用於慢性疼痛狀態和癌症相關疼痛的有效治療。最新文獻還已顯示Trk激酶的過度表達、活化、擴增和/或突變與許多癌症有關,所述癌症包括成神經細胞癌(Brodeur,G.M.,Nat.Rev.Cancer2003,3,203-216)、卵巢癌(Davidson.B.等,Clin.CancerRes.2003,9,2248-2259)、結腸直腸癌(Bardelli,A.,Science2003,300,949)、黑色素瘤(Truzzi,F.等,Dermato-Endocrinology2011,3(1),第32-36頁)、頭頸癌(Yilmaz,T.等,CancerBiologyandTherapy2010,10(6),第644-653頁)、胃癌(Du,J.等,WorldJournalofGastroenterology2003,9(7),第1431-1434頁)、肺癌(RicciA.等,AmericanJournalofRespiratoryCellandMolecularBiology25(4),第439-446頁)、乳腺癌(Jin,W.等,Carcinogenesis2010,31(11),第1939-1947頁)、分泌性乳腺癌(Euthus,D.M.,等,CancerCell2002,2(5),第347-348頁)、成膠質細胞瘤(Wadhwa,S.等,JournalofBiosciences2003,28(2),第181-188頁)、成神經管細胞瘤(Gruber-Olipitz,M.等,JournalofProteomeResearch2008,7(5),第1932-1944頁)、唾液腺癌(Li,Y.-G.等,ChineseJournalofCancerPreventionandTreatment2009,16(6),第428-430頁)、乳頭狀甲狀腺癌(Greco,A.等,MolecularandCellularEndocrinology2010,321(1),第44-49頁)以及成人骨髓性白血病(Eguchi,M.等,Blood1999,93(4),第1355-1363頁)。在癌症的臨床前模型中,TrkA、B和C的非選擇性小分子抑制劑可有效抑制腫瘤生長並阻止腫瘤轉移(Nakagawara,A.(2001)CancerLetters169:107-114;Meyer,J.等,(2007)Leukemia,21(10):2171-2180;Pierottia,M.A.和GrecoA.,(2006)CancerLetters232:90-98;EricAdriaenssens,E.等,CancerRes(2008)68:(2)346-351)。這些數據支持使用Trk抑制劑治療癌症的基本原理。另外,已顯示神經營養因子/Trk途徑的抑制可有效用NGF抗體或非選擇性小分子TrkA抑制劑治療炎性疾病的臨床前模型。例如,神經營養因子/Trk途徑的抑制已涉及以下疾病的臨床前模型:炎性肺病,包括哮喘(Freund-Michel,V;Frossard,N.,Pharmacology&Therapeutics(2008)117(1),52-76);間質性膀胱炎(Hu,VivianY等,TheJournalofUrology(2005),173(3),1016-21);膀胱疼痛症候群(Liu,H.-T.等,(2010)BJUInternational,106(11),第1681-1685頁);炎性腸病,包括潰瘍性結腸炎和克羅恩氏病(Crohn’sdisease)(DiMola,F.F等,Gut(2000)46(5),670-678);以及炎性皮膚病,諸如過敏性皮膚炎(Dou,Y.-C.等,ArchivesofDermatologicalResearch(2006)298(1),31-37)、溼疹和銀屑病(Raychaudhuri,S.P.等,J.InvestigativeDermatology(2004)122(3),812-819)。這些數據支持使用Trk抑制劑治療炎性疾病的基本原理。TrkA受體還被認為對於克氏錐蟲在人宿主中的寄生蟲感染(美洲錐蟲病)的疾病過程是關鍵的(deMelo-Jorge,M.等,CellHost&Microbe(2007)1(4),251-261)。Trk抑制劑還發現可用於治療與骨重塑調節失衡有關的疾病,諸如骨質疏鬆症、類風溼性關節炎以及骨轉移。骨轉移為常見的癌症併發症,在多至70%患有晚期乳腺癌或前列腺癌的患者中發生並且在約15%至30%患有肺癌、結腸癌、胃癌、膀胱癌、子宮癌、直腸癌、甲狀腺癌或腎癌的患者中發生。溶骨性轉移可引起劇痛、病理性骨折、威脅生命的血鈣過多症、脊髓壓迫以及其他神經壓迫症候群。出於這些原因,骨轉移為一種嚴重且昂貴的癌症併發症。因此,可誘導增殖性成骨細胞發生細胞凋亡的藥劑將為高度有利的。已在小鼠骨折模型中的骨形成區域內觀察到TrkA受體的表達(K.Asaumi等,Bone(2000)26(6)625-633)。另外,在幾乎所有的骨形成細胞中觀察到NGF的定位(K.Asaumi等,Bone(2000)26(6)625-633)。最近,已證實Trk抑制劑抑制了由結合至人hFOB成骨細胞中的所有三種Trk受體的神經營養因子活化的信號傳導(J.Pinski等,CancerResearch(2002)62,986-989)。這些數據支持使用Trk抑制劑治療骨重塑疾病諸如癌症患者中的骨轉移的基本原理。Trk抑制劑還可發現可用於治療疾病和病症,諸如舍格倫氏症候群(Sjogren’ssyndrome)(Fauchais,A.L.等,(2009)ScandinavianJournalofRheumatology,38(1),第50-57頁)、子宮內膜異位(BarcenaDeArellano,M.L.等,(2011)ReproductiveSciences,18(12),第1202-1210頁;BarcenaDeArellano等,(2011)FertilityandSterility,95(3),第1123-1126頁;Cattaneo,A.,(2010)CurrentOpinioninMolecularTherapeutics,12(1),第94-106頁)、糖尿病性周圍神經病變(Kim,H.C.等,(2009)DiabeticMedicine,26(12),第1228-1234頁;Siniscalco,D.等,(2011)CurrentNeuropharmacology,9(4),第523-529頁;Ossipov,M.H.,(2011)CurrentPainandHeadacheReports,15(3),第185-192頁)、以及前列腺炎和盆腔疼痛症候群(Watanabe,T.等,(2011)BJUInternational,108(2),第248-251頁;以及Miller,L.J.等,(2002)Urology,59(4),第603-608頁)。TrkA抑制劑還可用於治療由結締組織生長因子(CTGF,也稱為CCN2)異常信號傳導引起的疾病,例如涉及組織重塑和纖維化的疾病。CTGF為組織重塑和纖維化的重要中介物(Lipson,K.E.等,(2012),Fibrogenesis&TissueRepair2012,5(增刊1):S24)並且減少CTGF信號傳導的療法已證明作為纖維化的治療是有效的(Li,G.等,J.GeneMed.,2006,8:889-900)。CTGF與TrkA相互作用並活化所述TrkA(Wahab,N.A.,(2005)J.Am.Soc.Nephrol.16:340-351)並且TrkA抑制劑對此途徑的抑制可證明可用於治療各種纖維化疾病諸如雷諾氏症候群(Raynaud’sSyndrome)、特發性肺纖維化、瘢痕(肥大型、瘢痕瘤型和其他形式)、硬化、心內膜心肌纖維化、心房纖維化、骨髓纖維化、進行性塊狀纖維化(肺)、腎源性系統性纖維化、硬皮病、系統性硬化、關節纖維化以及眼部纖維化。已知據稱可用於治療疼痛或癌症的幾種類別的小分子Trk激酶抑制劑(Wang,T等,ExpertOpin.Ther.Patents(2009)19(3),305-319;McCarthyC.和WalkerE.,ExpertOpin.Ther.Patents2014,24(7):731-744)。國際申請公布No.WO2010/032856描述了由以下式表示的化合物其中環B為芳族環,環D為芳族環,並且L為NR3、NR3C(R4aR4b)、O或OC(R4aR4b),所述化合物被視為速激肽受體拮抗劑。國際申請公布No.WO2012/158413公開了一個亞類的作為TrkA抑制劑的具有以下通式的吡咯烷基脲化合物:其中:Y為一個鍵、-O-或-OCH2-;X為O、S或NH;R1為(1-3C烷氧基)(1-6C)烷基、(三氟甲氧基)(1-6C)烷基、(1-3C硫烷基)(1-6C)烷基、單氟(1-6C)烷基、二氟(1-6C)烷基、三氟(1-6C)烷基、四氟(2-6C)烷基、五氟(2-6C)烷基、氰基(1-6C)烷基、氨基羰基(1-6C)烷基、羥基(1-6C)烷基、二羥基(2-6C)烷基、(1-6C)烷基、(1-3C烷基氨基)(1-3C)烷基、(1-4C烷氧基羰基)(1-6C)烷基、氨基(1-6C)烷基、羥基(1-3C烷氧基)(1-6C)烷基、二(1-3C烷氧基)(1-6C)烷基、(1-3C烷氧基)三氟(1-6C)烷基、羥基三氟(1-6C)烷基、(1-4C烷氧基羰基)(1-3C烷氧基)(1-6C)烷基、羥基羰基(1-3C烷氧基)(1-6C)烷基、hetAr5(CH2)0-1或Ar5(CH2)0-1;hetAr5為具有1-3個獨立地選自N、O或S的環雜原子的5-6元雜芳基環,其中所述環任選地被一個或多個獨立地選自滷素、(1-6C)烷基、(1-6C)烷氧基和CF3的取代基取代;Ar5為任選地被一個或多個獨立地選自滷素、(1-6C)烷基、(1-6C)烷氧基、CF3O-、(1-4C)烷氧基羰基和氨基羰基的基團取代的苯基;B為任選地被一個或多個獨立地選自滷素、CF3、CF3O-、(1-4C)烷氧基、羥基(1-4C)烷基、(1-6C)烷基和CN的取代基取代的苯基;具有1-3個獨立地選自N、S和O的環雜原子並任選地被1-2個獨立地選自(1-6C)烷基、滷素、OH、CF3、NH2和羥基(1-2C)烷基的基團取代的5-6元雜芳基;1-6C烷基;或(1-6C)烷氧基;並且環C為式C-1、C-2或C-3:在WO2012/158413中此類化合物的實例包括實施例511中具有以下結構的化合物:其也被稱為1-((3S,4R)-4-(3,4-二氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-基)-3-(4-甲基-3-(2-甲基嘧啶-5-基)-1-苯基-1H-吡唑-5-基)脲(在下文中為「化合物2」),以及具有以下結構的實施例441的化合物:其也被稱為1-(1′,4-二甲基-1-苯基-1H,1′H-[3,4′-二吡唑]-5-基)-3-((3S,4R)-4-(4-氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-基)脲(在下文中為「化合物3」)。現在已發現具有出乎意料的且特別需要的特徵的化合物可通過選擇2-甲基嘧啶-5-基作為R4基團並選擇3-氟苯基作為B基團來獲得。發明概述本文提供了化合物1:或其藥學上可接受的鹽,所述化合物為TrkA的抑制劑。所述化合物還可由化學名1-((3S,4R)-4-(3-氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-基)-3-(4-甲基-3-(2-甲基嘧啶-5-基)-1-苯基-1H-吡唑-5-基)脲描述。已出乎意料地發現化合物1相對於化合物2和化合物3在大鼠中具有顯著更低的預測的人IV(靜脈內)清除率。還出乎意料地發現化合物1相對於化合物2和化合物3在大鼠中在經口給藥10mg/kg之後實現更高的經口AUC(血漿藥物濃度-時間曲線下面積)。還出乎意料地發現化合物1相對於化合物2和化合物3在大鼠中在經口給藥10mg/kg之後實現更高的C最大值(在血漿藥物濃度-時間曲線中實現的最大濃度)。還出乎意料地發現化合物1相對於化合物2和化合物3在大鼠中在經口給藥10mg/kg之後實現更高的谷濃度(在血漿藥物濃度-時間曲線中實現的最小濃度)。還出乎意料地發現化合物1相對於化合物2和化合物3具有更高的估算的TrkA抑制。化合物1相對於化合物2具有出乎意料地提高的外周至中樞神經系統分布,如通過在大鼠中經口給藥之後較高的血漿與腦內的比率證明的。化合物1相對於化合物2還具有出乎意料地減小的hERG(人Ether-à-go-go-相關基因)通道的抑制活性。本文還提供了治療由TrkA調節的疾病或病症的方法,其包括向需要此治療的哺乳動物施用有效量的化合物1或其藥學上可接受的鹽。本文還提供了治療慢性和急性疼痛的方法,所述疼痛包括但不限於炎性疼痛、神經性疼痛、以及與癌症、手術或骨折有關的疼痛,所述方法包括向需要此治療的哺乳動物施用有效量的化合物1或其藥學上可接受的鹽。本文還提供了治療癌症的方法,其包括向需要此治療的哺乳動物施用有效量的化合物1或其藥學上可接受的鹽。本文還提供了治療炎症或炎性疾病的方法,其包括向需要此治療的哺乳動物施用有效量的化合物1或其藥學上可接受的鹽。本文還提供了治療神經變性疾病的方法,其包括向需要此治療的哺乳動物施用有效量的化合物1或其藥學上可接受的鹽。本文還提供了治療前列腺炎或盆腔疼痛症候群的方法,其包括向需要此治療的哺乳動物施用有效量的化合物1或其藥學上可接受的鹽。本文還提供了治療與骨重塑調節失衡相關的疾病的方法,所述疾病諸如骨質疏鬆症、類風溼性關節炎以及骨轉移,所述方法包括向需要此治療的哺乳動物施用有效量的化合物1或其藥學上可接受的鹽。本文還提供了治療選自某些感染性疾病、舍格倫氏症候群、子宮內膜異位和糖尿病性周圍神經病變的疾病和病症的方法,其包括向需要此治療的哺乳動物施用有效量的化合物1或其藥學上可接受的鹽。本文還提供了治療由結締組織生長因子異常信號傳導引起的疾病的方法,其包括向需要此治療的哺乳動物施用有效量的化合物1或其藥學上可接受的鹽。在一個實施方案中,任何以上治療包括向需要此治療的哺乳動物施用有效量的化合物1或其藥學上可接受的鹽與另一種治療劑的組合。本文還提供了一種包含化合物1或其藥學上可接受的鹽的藥物組合物。本文還提供了化合物1或其藥學上可接受的鹽以供用於治療。本文還提供了化合物1或其藥學上可接受的鹽以供用於治療慢性和急性疼痛,包括但不限於炎性疼痛、神經性疼痛、以及與癌症、手術或骨折有關的疼痛。本文還提供了化合物1或其藥學上可接受的鹽以供用於治療癌症。本文還提供了化合物1或其藥學上可接受的鹽以供用於治療炎症或炎性疾病。本文還提供了化合物1或其藥學上可接受的鹽以供用於治療神經變性疾病。本文還提供了化合物1或其藥學上可接受的鹽以供用於治療前列腺炎或盆腔疼痛症候群。本文還提供了化合物1或其藥學上可接受的鹽以供用於治療與骨重塑調節失衡相關的疾病,諸如骨質疏鬆症、類風溼性關節炎和骨轉移。本文還提供了化合物1或其藥學上可接受的鹽以供用於治療某些感染性疾病、舍格倫氏症候群、子宮內膜異位和糖尿病性周圍神經病變。本文還提供了化合物1或其藥學上可接受的鹽以供用於治療由結締組織生長因子異常信號傳導引起的疾病。本文還提供了化合物1或其藥學上可接受的鹽在製造用於治療諸如慢性和急性疼痛的疾病和病症的藥物中的用途,所述疼痛包括但不限於炎性疼痛、神經性疼痛、以及與癌症、手術或骨折有關的疼痛本文還提供了化合物1或其藥學上可接受的鹽在製造用於治療選自以下各項的疾病和病症的藥物中的用途:癌症、炎症或炎性疾病、神經變性疾病、某些感染性疾病、合格倫氏症候群、子宮內膜異位、糖尿病性周圍神經病變、前列腺炎、盆腔疼痛症候群以及與骨重塑調節失衡相關的疾病(諸如骨質疏鬆症、類風溼性關節炎和骨轉移)。本文還提供了化合物1或其藥學上可接受的鹽在製造用於治療由結締組織生長因子異常信號傳導引起的疾病的藥物中的用途。本文還提供了可用於製備TrkA抑制性化合物諸如化合物1的中間體和製備此類中間體的方法。本文還提供了化合物1或其藥學上可接受的鹽的製備方法、分離方法和純化方法。附圖簡述圖1為比較化合物1(三角形)和化合物2(正方形)在大鼠中經口給藥10mg/kg之後血漿藥物濃度(μg/mL)對比時間(小時)的圖。圖2為比較化合物1(三角形)和化合物3(圓形)在大鼠中經口給藥10mg/kg之後血漿藥物濃度(μg/mL)對比時間(小時)的圖。圖3為比較化合物1(三角形)和化合物2(正方形)在大鼠中經口給藥10mg/kg之後估算的TrkA抑制百分比對比時間(小時)的比較。圖4為比較化合物1(三角形)和化合物3(圓形)在大鼠中經口給藥10mg/kg之後估算的TrkA抑制百分比對比時間(小時)的比較。發明詳述本文提供了化合物1或其藥學上可接受的鹽,所述化合物為TrkA的抑制劑。所述化合物還可由化學名1-((3S,4R)-4-(3-氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-基)-3-(4-甲基-3-(2-甲基嘧啶-5-基)-1-苯基-1H-吡唑-5-基)脲描述。已發現化合物1具有特別意外且希望的特徵。化合物1特別有利的特徵為其預測的人IV清除率,所述清除率相對於化合物2和化合物3的預測的IV清除率顯著更低,如表1所示。表1*不可用**針對臨床前物種觀察到的平均校正分數用於預測人的IV清除率。***所有測試物種的臨床前平均校正因子在表1中,預測的人IV清除率由在靜脈內(IV)給藥1mg/kg之後從臨床前物種(小鼠、大鼠、狗和猴)中收集的血漿中的化合物濃度對比時間數據計算。血漿中的化合物濃度通過LC-MS(液相色譜法-質譜法)測量。個別Cp/t曲線(在任何時間t時血漿中的藥物濃度)的AUCinf值(從時間0外推至無限時間的給藥間隔的血漿濃度-時間曲線下面積)使用線性-梯形積分法和來自Cp/t曲線終點的一級外推法來確定,並且清除率(CL)使用劑量/AUCinf計算。預測的肝清除率(CLh)值通過使用表2中列出且以下等式中所採用的身體和生理標度因子測量關於化合物在肝微粒體中的穩定性的體外半衰期(t1/2)來計算(1mg/mL;20分鐘),所述標度因子用於預測內在清除率(CLint)和肝清除率(CLhep):其中D為每份質量的肝的細胞色素P450-相關蛋白的量,W為每份重量的動物存在的平均肝質量,C為肝微粒體濃度,並且Q為物種依賴性肝血流量。表2物種WaQbDc小鼠87.09050大鼠45.07045兔30.87178狗32.03555猴32.04460人25.72053a)W=每份質量的動物(kg)的平均肝質量(g)。b)Q=平均肝血流量(mL/min/kg)。c)D(微粒體)=每份質量的肝(g)的細胞色素P450-相關蛋白的量(mg)。體內/體外校正因子然後通過用IVCL值除以微粒體CLh值來測定。每種化合物的臨床前校正因子的算術平均值用於由測量的人微粒體CLh預測人IV清除率(CLh/校正因子)。另外,化合物1相對於化合物2和化合物3在經口給藥(10mg/kg)之後實現更高的經口AUC(血漿藥物濃度-時間曲線下面積)、更高的C最大值(在血漿藥物濃度-時間曲線中實現的最大濃度)、以及更高的谷濃度(在血漿藥物濃度-時間曲線中實現的最小濃度),如由其大鼠藥代動力學曲線舉例說明的,如圖1和圖2所示並且如表3中所總結的。表3大鼠PK參數化合物1化合物2化合物3AUC(μg-hr/mL)2.570.9251.06C最大值(μg/mL)1.060.4200.498谷濃度(μg/mL)0.001340.0004460.00044圖3和圖4分別示出了化合物1相對於化合物2在大鼠中在經口給藥10mg/kg之後估算的TrkA抑制和化合物1相對於化合物3的TrkA抑制。圖3和圖4中的曲線使用以下等式來計算:其中I最小值和I最大值分別為最小和最大可能的靶標抑制,IC50為靶標被抑制50%時的濃度,C為抑制劑的濃度,並且n為Hill斜率。如圖3和圖4所示的,化合物1估算的TrkA抑制比化合物2和化合物3更高。化合物1的較低清除率、較高AUC、較高C最大值和較高谷濃度在向患者施用化合物1之後的一整天內引起與化合物2和化合物3相比更大的TrkA受體抑制。這轉換成化合物1相對於化合物2和化合物3的更大治療功效。實現提高的治療功效的能力在治療罹患例如中度至重度疼痛、某些炎症疾患或癌症(包括由異常TrkA信號傳導驅動的癌症)的患者中是重要的。另外,化合物1的較低清除率在施用之後引起相對於化合物2和化合物3更長的半衰期,從而在經口、靜脈內或皮下施用所述化合物之後引起更持久的TrkA受體抑制。增加的半衰期具有提供更持久的功效和/或減少的藥物給藥頻率的益處。此外,化合物1的較低人清除率和較高經口AUC有益之處在於相對於化合物2和化合物3僅需要更低劑量的化合物1來有效抑制TrkA受體並提供給定治療功效。功效所需要的化合物劑量降低轉換成了通過給藥方案改進藥物耐受性、治療成本和患者順應性。化合物1相對於化合物2具有出乎意料地提高的外周至中樞神經系統分布,如通過在大鼠中經口給藥之後較高的血漿與腦內的比率證明的,如表4中所示的。維持低腦暴露具有降低中樞神經系統相關副作用的風險的益處,所述副作用諸如與認知或運動受損有關的副作用。中樞神經系統暴露減少有益之處在於在患者中對於給定治療作用發生較少或減少的副作用並且/或者在觀察到任何劑量限制性副作用之前實現較大治療作用。化合物1相對於化合物2還具有出乎意料地減小的針對hERG(人Ether-à-go-go-相關基因)通道的抑制活性。hERG通道功能的抑制可導致嚴重的藥物誘導性(獲得性)長QT症候群副作用,所述副作用可產生伴隨的猝死風險。由於此副作用的嚴重性質,具有針對hERG的減小的抑制活性是希望的。表4化合物1相對於化合物2的上述意外特徵可能不能合理地預期來自這些化合物之間的微小結構差異。化合物1對比化合物2的僅有結構差異為去除了單個氟原子。然而,在本領域中已證實從化合物中去除單個氟原子通常不能提供在預測的人清除率中具有改進的變化的化合物,所述變化為對於化合物1相對於化合物2觀察到的。實際上,在本領域中存在具有藥物繼續的許多實例,它們證實具有更多氟原子的類似物相對於其具有更少氟原子的類似物傾向於具有更低的體內清除率(參見,例如,Barker,A.J.等,Bioorg.Med.Chem.Lett.11(2001)1911-1914;Rosenblum,S.B.等,J.Med.Chem.,41,(1998)973-980;Brown,M.F.等,Bioorg.Med.Chem.Lett.14(2004)2175-2179)。相比之下,單氟化合物1相對於二氟化合物2具有預測的更低的人清除率。類似地,化合物1相對於化合物2更高C最大值、更高AUC、更高谷暴露和更高TrkA靶敲除的藥代動力學(PK)優點(如通過臨床前大鼠PK證實的)對於此小結構變化為相當顯著且出乎意料的。另外,化合物1和化合物3的PK參數的比較證實化合物1的提高的藥代動力學不是所有單氟類似物的一般現象。實際上,儘管具有單氟取代的苯基,但是化合物3與化合物1相比顯示一個更差的投射的人清除率和就C最大值、AUC、谷暴露和TrkA靶標敲除而言的較差PK。在化合物1中甲基嘧啶基與單氟取代的苯基部分的獨特組合出乎意料地提供以上所列出的優異特徵。本文還提供化合物1的藥學上可接受的鹽。具體是鹽為鹽酸鹽。在一個實施方案中,本文提供了一種化合物1的單鹽酸鹽。在一個實施方案中,本文提供了一種化合物1的二鹽酸鹽。在一個實施方案中,本文提供了化合物1的游離鹼形式。在一個實施方案中,化合物1或其鹽可以溶劑化物形式分離,並且因此其任何此類溶劑化物被包括在本發明的範圍內。例如,化合物1或其鹽可以非溶劑化形式以及與藥學上可接受的溶劑諸如水、乙醇等溶劑化的形式存在。術語「藥學上可接受的」是指物質或組合物為在化學上和/或毒理學上與構成製劑的其他成分、和/或用它治療的哺乳動物相容的。本文還提供了一種用於製備化合物1或其藥學上可接受的鹽的方法,所述方法包括:(a)使具有以下式II-A的化合物與具有以下式III的化合物在羰基二咪唑或三光氣和鹼存在下反應;或者(b)使具有以下式II-A的化合物與具有以下式IV的化合物其中L1為離去基團,在鹼存在下反應;或者(c)使具有以下式V的化合物其中L2為離去基團,與具有以下式III的化合物在鹼存在下反應;或者(d)使具有以下式VI的化合物與二苯基磷醯基疊氮反應以形成一種中間體,接著使所述中間體與具有以下式III的化合物在鹼存在下反應;或者(e)使具有以下式II-A的化合物與具有以下式VII的化合物在鹼存在下反應;並且去除保護基團(如果存在的話)並任選地製備其藥學上可接受的鹽。參考方法(a),所述鹼可為胺鹼,諸如三乙胺或二異丙基胺。適合的溶劑包括二氯甲烷、二氯乙烷、THF、DMA以及DMF。所述反應合宜地在環境溫度下進行。參考方法(b),所述離去基團可為例如苯氧基或4-硝基苯氧基。所述鹼可為胺鹼,諸如三乙胺或二異丙基胺。適合的溶劑包括DMA、DMF和DCE。所述反應合宜地在環境溫度下進行。參考方法(c),所述離去基團可為例如苯氧基或4-硝基苯氧基。所述鹼可為胺鹼,諸如三乙胺或二異丙基胺。適合的溶劑包括DCE、DMA和DMF。所述反應合宜地在環境溫度下進行。參考方法(d),所述鹼可為胺鹼,諸如三乙胺或二異丙基胺。適合的溶劑包括甲苯和DMF。所述反應合宜地在高溫下進行,所述高溫例如溶劑的回流溫度。參考方法(e),所述鹼可為胺鹼,諸如三乙胺或二異丙基胺。適合的溶劑包括DCM、DCE、DMF和THF。所述反應合宜地在約0℃與環境溫度之間的溫度下進行。本文還提供了一種用於製備式II化合物的外消旋混合物的方法其中B環和NH2部分處於反式構型中。式II化合物(諸如式II-A化合物)可用於製備諸如TrkA抑制性化合物諸如化合物1的化合物。因此,本文提供了一種用於製備式II化合物的外消旋混合物的方法其中:環B為Ar1或hetAr1;Ar1為任選地被一個或多個獨立地選自以下各項的取代基取代的苯基:滷素、CF3、CF3O-、(1-4C)烷氧基、羥基(1-4C)烷基、(1-6C)烷基以及CN;並且hetAr1為具有1-3個獨立地選自N、S和O的環雜原子並且任選地被1-2個獨立地選自(1-6C)烷基、滷素、OH、CF3、NH2和羥基(1-2C)烷基的基團取代的5-6元雜芳基,所述方法包括:(a)使以下式(a)化合物其中環B為針對式II所定義的,與具有以下式的2-甲氧基-N-(甲氧基甲基)-N-((三甲基甲矽烷基)甲基)乙胺在催化量的酸存在下反應,以提供以下式(b)化合物其中環B為針對式II所定義的;(b)使所述式(b)化合物與羰基二咪唑在催化量的咪唑鹽酸鹽存在下反應,接著用氨處理,以提供具有以下式(c)的化合物其中環B為針對式II所定義的;以及(c)使所述式(c)化合物與次氯酸鈉反應,接著用KOH處理,然後用HCl處理,以提供作為反式式II外消旋混合物的所述式II化合物。參考步驟(a),所述酸可為有機酸,諸如三氟乙酸。在用於製備式II化合物的外消旋混合物的以上方法的一個實施方案中,環B為任選地被一個或多個獨立地選自以下各項的取代基取代的苯基:滷素、CF3、CF3O-、(1-4C)烷氧基、羥基(1-4C)烷基、(1-6C)烷基以及CN。在用於製備式II化合物的外消旋混合物的以上方法的一個實施方案中,環B為任選地被一個或多個獨立地選自滷素的取代基取代的苯基。在用於製備式II化合物的外消旋混合物的以上方法的一個實施方案中,環B為任選地被一個或多個氟取代的苯基。在用於製備式II化合物的外消旋混合物的以上方法的一個實施方案中,環B為3-氟苯基。在用於製備式II化合物的外消旋混合物的以上方法的一個實施方案中,環B為3,4-二氟苯基。在用於製備式II化合物的外消旋混合物的以上方法的一個實施方案中,環B為具有1-3個獨立地選自N、S和O的環雜原子並且任選地被1-2個獨立地選自(1-6C)烷基、滷素、OH、CF3、NH2和羥基(1-2C)烷基的基團取代的5-6元雜芳基。在以上方法的一個實施方案中,環B為任選地被1-2個獨立地選自以下各項的基團取代的吡啶基環、苯硫基環、噻唑基環、噁唑基環或異噁唑基環:(1-6C)烷基、滷素、OH、CF3、NH2以及羥基(1-2C)烷基。在用於製備式II化合物的外消旋混合物的以上方法的一個實施方案中,環B為任選地被1-2個獨立地選自滷素和(1-6C)烷基的基團取代的吡啶基環、苯硫基環、噻唑基環、噁唑基環或異噁唑基環。在用於製備式II化合物的外消旋混合物的以上方法的一個實施方案中,具有以下式的2-甲氧基-N-(甲氧基甲基)-N-((三甲基甲矽烷基)甲基)乙胺可通過包括以下各項的方法來製備:(i)使(氯甲基)三甲基矽烷與2-甲氧基乙胺反應,以提供具有以下結構的(2-甲氧基-N-((三甲基甲矽烷基)甲基)乙胺以及(ii)用甲醇中的甲醛處理所述(2-甲氧基-N-((三甲基甲矽烷基)甲基)乙胺,以提供所述2-甲氧基-N-(甲氧基甲基)-N-((三甲基甲矽烷基)甲基)乙胺。本文還提供了一種用於分離反式式II作為游離鹼或作為二-對-甲苯醯基-D-酒石酸鹽的對映體1的方法,其包括:用二-對-甲苯醯基-D-酒石酸處理外消旋反式式II以提供外消旋反式II的二-對-甲苯醯基-D-酒石酸鹽;使反式II的二-對-甲苯醯基-D-酒石酸鹽重結晶,以提供反式II的對映體1的二-對-甲苯醯基-D-酒石酸鹽;以及任選地用無機鹼處理反式II的對映體1的二-對-甲苯醯基-D-酒石酸鹽,以提供具有如下所示絕對構型的反式式II的對映體1的游離鹼:在一個實施方案中,反式II的對映體1的二-對-甲苯醯基-D-酒石酸鹽用於製備諸如TrkA抑制劑化合物諸如化合物1的化合物。例如,在一個實施方案中,反式式II的對映體1的二-對-甲苯醯基-D-酒石酸鹽用於在Shotten-Baumann條件下製備諸如TrkA抑制劑化合物諸如化合物1的化合物,在所述條件中反式式II的對映體1的二-對-甲苯醯基-D-酒石酸鹽在由水和有機溶劑(諸如二氯甲烷)組成的兩相溶劑系統下在諸如氫氧化鈉的鹼存在下生成,並且與具有式IV的化合物反應。在一個實施方案中,反式式II的對映體1的游離鹼用於製備諸如TrkA抑制劑化合物諸如化合物1的化合物。在用於分離反式式II的對映體1的以上方法的一個實施方案中,環B為任選地被一個或多個獨立地選自以下各項的取代基取代的苯基:滷素、CF3、CF3O-、(1-4C)烷氧基、羥基(1-4C)烷基、(1-6C)烷基以及CN。在用於分離反式式II的對映體1的以上方法的一個實施方案中,環B為任選地被一個或多個獨立地選自滷素的取代基取代的苯基。在用於分離反式式II的對映體1的以上方法的一個實施方案中,環B為任選地被一個或多個氟取代的苯基。在用於分離反式式II的對映體1的以上方法的一個實施方案中,環B為3-氟苯基。在用於分離反式式II的對映體1的以上方法的一個實施方案中,環B為3,4-二氟苯基。在一個實施方案中,用於分離反式式II的對映體1的以上方法提供了一種用於製備(3S,4R)-4-(3,4-二氟苯基)-1-(2-甲氧基甲基)吡咯烷-3-胺的方法。在用於分離反式式II的對映體1的以上方法的一個實施方案中,環B為具有1-3個獨立地選自N、S和O的環雜原子並且任選地被1-2個獨立地選自(1-6C)烷基、滷素、OH、CF3、NH2和羥基(1-2C)烷基的基團取代的5-6元雜芳基。在用於分離反式式II的對映體1的以上方法的一個實施方案中,環B為任選地被1-2個獨立地選自以下各項的基團取代的吡啶基、苯硫基、噻唑基、噁唑基或異噁唑基環:(1-6C)烷基、滷素、OH、CF3、NH2以及羥基(1-2C)烷基。在用於分離反式式II的對映體1的以上方法的一個實施方案中,環B為任選地被1-2個獨立地選自滷素和(1-6C)烷基的基團取代的吡啶基、苯硫基、噻唑基、噁唑基或異噁唑基環。用於製備式II化合物的外消旋混合物的以上方法與國際申請公布號WO2012/158413中所述的方法相比具有若干優點。例如,WO2012/158413中所述的方法包括苯甲醛試劑與硝基甲烷之間的Nitro-Aldol反應。然後通過在高壓下加氫來還原所得2-硝基乙烯基苯中間體。這兩個反應步驟不適合用於大規模合成,因為Nitro-Aldol反應和由其衍生的硝基中間體不穩定並且可能有危險。相比之下,用於製備式II化合物的外消旋混合物的以上方法並不使用任何高危害的化學劑並且避免了含硝基中間體和加氫作用。另外,在用於製備式II化合物的外消旋混合物的以上方法中使用的所有條件均處於用於大規模合成的試驗工廠中通常可見的標準運行參數內,例如所述方法不使用極端溫度並且不需要高壓容器。化合物1或其藥學上可接受的鹽充當TrkA抑制劑的能力已通過實施例A和實施例B中所述的試驗來證實。化合物1或其藥學上可接受的鹽可用於治療疾病和病症,包括但不限於疼痛、癌症、炎症/炎性疾病、神經變性疾病、某些感染性疾病、合格倫氏症候群、子宮內膜異位、糖尿病性周圍神經病變、前列腺炎、盆腔疼痛症候群、與骨重塑調節失衡相關的疾病、以及由結締組織生長因子異常信號傳導引起的疾病。如本文所用的,術語「治療(treat/treatment)」是指治療性或緩解性措施。有利的或希望的臨床結果包括但不限於與病症或疾患有關的症狀完全或部分緩解、疾病程度減輕、疾病處於穩定(即未惡化)狀態、疾病進展延遲或減慢、疾病狀態改善或緩和、以及緩解(無論是部分還是總體),無論這些結果是可檢測的還是不可檢測的。「治療」還意味著與未接受治療時的預期存活時間相比延長的存活時間。在某些實施方案中,化合物1或其藥學上可接受的鹽可用於預防本文所定義的疾病和病症。如本文所用的術語「預防」意指整體或部分預防本文所述的疾病或疾患或其症狀的發作、復發或傳播,並且包括在症狀發作前施用化合物1或其藥學上可接受的鹽。化合物1或其藥學上可接受的鹽可與一種或多種另外的治療劑組合使用,所述另外的治療劑通過相同或不同的作用機制起作用。如本文所用的術語「藥物組合」是指通過將超過一種活性成分混合或組合產生的藥物治療劑並且包括固定和不固定的活性成分組合。術語「固定組合」意指化合物1或其藥學上可接受的鹽和至少一種另外的治療劑二者同時以單一實體或劑量形式向患者施用。術語「非固定組合」意指化合物1或其藥學上可接受的鹽和至少一種另外的治療劑作為單獨的實體同時或以可變幹預時限依次向患者施用,其中此施用在患者身體中提供有效水平的兩種或更多種化合物。這些也可用於混合療法(cocktailtherapy),例如施用三種或更多種活性成分。如本文所用的,「共同施用」意指包括向單一患者施用所選擇的治療劑,並且旨在包括其中所述藥劑通過相同或不同施用途徑或在相同或不同時間施用的治療方案。此術語包括向哺乳動物施用兩種或更多種藥劑以使得兩種藥劑和/或其代謝物同時存在於哺乳動物中。它包括以單獨的組合物同時施用、以單獨的組合物在不同時間施用和/或以其中存在兩種藥劑的組合物施用。在一個實施方案中,本發明的化合物和其他治療劑以單一組合物施用。在一個實施方案中,化合物1或其藥學上可接受的鹽和其他藥劑在所述組合物中混合。在一個實施方案中,化合物1或其藥學上可接受的鹽可用於治療疼痛,包括慢性和急性疼痛。例如,化合物1或其藥學上可接受的鹽可用於治療多種類型的疼痛,包括炎性疼痛、神經性疼痛、背痛、以及與癌症、手術或骨折有關的疼痛。在一個實施方案中,化合物1或其藥學上可接受的鹽可用於治療急性疼痛。如國際疼痛研究協會(InternationalAssociationfortheStudyofPain)定義的急性疼痛由疾病、炎症或組織損傷所引起。這種類型的疼痛通常例如在創傷或手術之後突然發作,並且可能伴隨有焦慮或緊張,並且局限於給定的時間段和嚴重性。在一些情況下,它可變成慢性的。在一個實施方案中,化合物1或其藥學上可接受的鹽可用於治療慢性疼痛。如國際疼痛研究協會定義的慢性疼痛被廣泛地認為代表疾病本身。它可能因環境和生理因素而惡化。慢性疼痛持續比急性疼痛更長的時間段並且對大部分醫學治療抵抗,通常持續3個月或更長時間。它可以並常常引起患者的嚴重問題。因此,本文提供了一種治療哺乳動物中的疼痛的方法,其包括向有需要的所述哺乳動物施用有效於治療所述疼痛的量的化合物1或其藥學上可接受的鹽。在一個實施方案中,所述疼痛為急性疼痛。在一個實施方案中,所述疼痛為慢性疼痛。在一個實施方案中,所述疼痛為慢性背痛。在一個實施方案中,所述疼痛為神經性疼痛,諸如與糖尿病性周圍神經病變或非糖尿病性(例如化學治療誘導的)周圍神經變性有關的疼痛。在一個實施方案中,所述疼痛為炎性疼痛,諸如與骨關節炎有關的疼痛。在一個實施方案中,所述疼痛為與癌症有關的疼痛。在一個實施方案中,所述疼痛為與手術有關的疼痛。在一個實施方案中,所述疼痛為與骨折有關的疼痛。本文還提供了一種預防哺乳動物的疼痛的方法,其包括向有需要的所述哺乳動物施用有效於預防所述疼痛的量的化合物1或其藥學上可接受的鹽在一個實施方案中,所述疼痛為急性疼痛。在一個實施方案中,所述疼痛為慢性疼痛。在一個實施方案中,所述疼痛為慢性背痛。在一個實施方案中,所述疼痛為神經性疼痛,諸如與糖尿病性周圍神經病變或非糖尿病性(例如化學治療誘導的)周圍神經變性有關的疼痛。在一個實施方案中,所述疼痛為炎性疼痛,諸如與骨關節炎有關的疼痛。在一個實施方案中,所述疼痛為與癌症有關的疼痛。在一個實施方案中,所述疼痛為與手術有關的疼痛。在一個實施方案中,所述疼痛為與骨折有關的疼痛。本文還提供了一種治療哺乳動物中的疼痛的方法,其包括向有需要的哺乳動物共同施用有效量的:(a)化合物1或其藥學上可接受的鹽;以及(b)至少一種選自選自以下各項的另外的治療劑:抗炎化合物、類固醇(例如,地塞米松、可的松和氟替卡松)、止痛劑諸如NSAID(例如,阿司匹林、布洛芬、消炎痛和酮洛芬)、阿片類(諸如嗎啡)、降鈣素基因相關肽受體拮抗劑、亞型選擇性離子通道調節劑、抗驚厥藥(例如普瑞巴林和加巴噴丁)、雙重血清素-去甲腎上腺素再吸收抑制劑(例如度洛西汀、文拉法辛和米那普侖)、JAK家族激酶抑制劑(例如,魯索利替尼或託法替尼)、以及三環抗抑鬱藥(諸如阿米替林,去甲阿米替林和脫甲丙咪嗪)。這些另外的治療劑可與化合物1或其藥學上可接受的鹽作為相同或單獨劑型的一部分,經由相同或不同施用途徑並按照根據本領域技術人員已知的標準藥物實踐的相同或不同施用方案施用。因此,本文還提供了一種包含有效量的以下各項的藥物組合:(a)化合物1或其藥學上可接受的鹽和(b)至少一種選自以下各項的另外的治療劑:抗炎化合物、類固醇(例如,地塞米松、可的松和氟替卡松)、止痛劑諸如NSAID(例如,阿司匹林、布洛芬、消炎痛和酮洛芬)、以及阿片類(諸如嗎啡),以用於治療哺乳動物中的疼痛,其中(a)和(b)可處於單獨的劑型中或處於相同的劑型中。在一個實施方案中,本文提供了一種包含以下各項的藥物組合:(a)有效量的化合物1或其藥學上可接受的鹽和(b)有效量的止痛劑諸如NSAID(例如,阿司匹林、布洛芬、消炎痛和酮洛芬)。化合物1或其藥學上可接受的鹽也可用於治療癌症。具體實例包括成神經細胞瘤、卵巢癌、胰腺癌、結腸直腸癌以及前列腺癌。因此,本文還提供了一種治療哺乳動物中的癌症的方法,其包括向有需要的所述哺乳動物施用有效於治療所述癌症的量的化合物1或其藥學上可接受的鹽。化合物1或其藥學上可接受的鹽也可用於治療具有TrkA調節異常的癌症。因此,本文還提供一種用於治療診斷患有具有TrkA調節異常的癌症的患者的方法,其包括向所述患者施用治療有效量的化合物1或其藥學上可接受的鹽。在一個實施方案中,TrkA調節異常包括野生型TrkA過度表達(自分泌/旁分泌活化)。在一個實施方案中,TrkA調節異常包括引起TrkA基因融合物的基因擴增或一個或多個染色體易位或倒位。在一個實施方案中,所述調節異常為基因易位的結果,其中所表達的蛋白質為含有來自非-TrkA蛋白和TrkA蛋白的殘基的融合蛋白,並且最少為TrkA激酶結構域。在一個實施方案中,TrkA融合蛋白為LMNA-TrkA、TFG-TrkA、TPM3-TrkA、CD74-TrkA、NFASC-TrkA、MPRIP-TrkA、BCAN-TrkA、或TPR-TrkA。在一個實施方案中,TrkA融合蛋白為LMNA-TrkA、TFG-TrkA、TPM3-TrkA、CD74-TrkA、NFASC-TrkA、MPRIP-TrkA、BCAN-TrkA、TP53-TrkA、RNF213-TrkA、RABGAP1L-TrkA、IRF2BP2-TrkA、SQSTM1-TrkA、SSBP2-TrkA、或TPR-TrkA,其中:LMNA=前層蛋白-A/C;TFG=TRK-融合基因蛋白TPM3=原肌球蛋白α-3;CD74=HLAII類組織相容性抗原γ鏈;NFASC=神經束蛋白;MPRIP=MPRIP蛋白;BCAN=短小蛋白聚糖(Brevican)核心蛋白;並且TP53=細胞腫瘤抗原p53RNF213=E3泛素-蛋白連接酶RNF213RABGAP1L=RabGTP酶活化蛋白1-樣IRF2BP2=幹擾素調節因子2-結合蛋白2SQSTM1=Sequestosome-lSSBP2=單鏈DNA-結合蛋白2TPR=核蛋白TPR在一個實施方案中,TrkA調節異常包括TrkA蛋白質中的一個或多個缺失、插入或突變。在一個實施方案中,所述調節異常包括來自TrkA蛋白的一個或多個殘基的缺失,從而產生TrkA激酶的組成型活性。在一個實施方案中,所述缺失包括TrkA同種型2中的殘基303-377的缺失。在一個實施方案中,TrkA調節異常包括拼接變化,其中所表達的蛋白質可選地為具有一個或多個缺失的殘基的TrkA的拼接變體,從而產生TrkA激酶的組成型活性。在一個實施方案中,具有組成型活性的TrkA的替代性拼接形式具有外顯子8、9和11的缺失,從而導致表達的蛋白質相對於TrkA同種型2失去殘基192-284和393-398。已鑑別為具有TrkA調節異常的癌症(參見以下參考文獻;還參見www.cancer.gov和www.nccn.org)包括:(A)類癌症,其中TrkA調節異常包括引起TrkA基因融合物的基因擴增或一個或多個染色體易位或倒位,所述癌症包括:(B)類癌症,其中TrkA調節異常包括TrkA蛋白質中的一個或多個缺失、插入或突變,所述癌症包括:(C)類癌症,其由野生型TrkA的過度表達(自分泌活化)所驅動,所述癌症包括:在一個實施方案中,本文提供了一種用於治療診斷患有帶有TrkA調節異常的癌症的患者的方法,其包括向患者施用化合物1或其藥學上可接受的鹽以治療所述癌症,其中所述癌症選自非小細胞肺癌、乳頭狀甲狀腺癌、多形性成膠質細胞瘤、急性骨髓性白血病、結腸直腸癌、大細胞神經內分泌癌、前列腺癌、成神經細胞瘤、胰腺癌、黑色素瘤、頭頸鱗狀細胞癌以及胃癌。在一個實施方案中,本文提供了一種用於治療診斷患有具有TrkA調節異常的癌症的患者的方法,其包括向患者施用化合物1或其藥學上可接受的鹽以治療所述癌症,其中所述癌症選自非小細胞肺癌、乳頭狀甲狀腺癌、多形性成膠質細胞瘤、急性骨髓性白血病、結腸直腸癌、大細胞神經內分泌癌、前列腺癌、成神經細胞瘤、胰腺癌、黑色素瘤、頭頸鱗狀細胞癌、胃癌、膽管癌以及肉瘤。還提供了一種用於治療在有需要的哺乳動物中的癌症的方法,所述方法包括:(a)確定所述癌症是否與TrkA激酶調節異常有關;以及(b)如果確定癌症與TrkA激酶調節異常有關,則向所述哺乳動物施用治療有效量的化合物1或其藥學上可接受的鹽。在一個實施方案中,化合物1為二鹽酸鹽。在一個實施方案中,TrkA調節異常包括引起TrkA基因融合物的一個或多個染色體易位或倒位。在一個實施方案中,TrkA基因融合物為LMNA-TrkA、TFG-TrkA、TPM3-TrkA、CD74-TrkA、NFASC-TrkA、MPRIP-TrkA、BCAN-TrkA、TP53-TrkA、RNF213-TrkA、RABGAP1L-TrkA、IRF2BP2-TrkA、SQSTM1-TrkA、SSBP2-TrkA、或TPR-TrkA。在一個實施方案中,所述癌症為非小細胞肺癌、乳頭狀甲狀腺癌、多形性成膠質細胞瘤、結腸直腸癌、黑色素瘤、膽管癌、或肉瘤。在一個實施方案中,TrkA調節異常包括TrkA蛋白質中的一個或多個缺失、插入或突變。在一個實施方案中,所述癌症為急性骨髓性白血病、大細胞神經內分泌癌、或成神經細胞瘤。在一個實施方案中,TrkA調節異常為野生型TrkA過度表達(自分泌活化)。在一個實施方案中,所述癌症為前列腺癌、成神經細胞瘤、胰腺癌、黑色素瘤、頭頸鱗狀細胞癌、或胃癌。在一個實施方案中,任何以上用於治療有需要的哺乳動物中的癌症的方法還包括施用有效量的化合物1或其藥學上可接受的鹽與有效量的至少一種選自以下的另外的治療劑的組合:一種或多種另外的療法或化學治療劑。在一個實施方案中,任何以上用於治療有需要的哺乳動物中的癌症的方法包括向有需要的所述哺乳動物施用有效量的化合物1或其藥學上可接受的鹽與有效量的一種或多種另外的化學治療劑的組合。在一個實施方案中,另外的化學治療劑選自受體酪氨酸激酶靶向治療劑,包括卡博替尼(cabozantinib)、克唑替尼、埃羅替尼、吉非替尼、伊馬替尼、拉帕替尼、尼羅替尼、帕唑帕尼、培妥珠單抗、瑞格菲尼、舒尼替尼、以及曲妥珠單抗。在一個實施方案中,另外的化學治療劑選自信號轉導途徑抑制劑,包括Ras-Raf-MEK-ERK途徑抑制劑(例如比尼替尼(binimetinib)、司美替尼(selumetinib)、恩可非尼(encorafinib)、索拉非尼、曲美替尼、維羅非尼)、PI3K-Akt-mTOR-S6K途徑抑制劑(例如依維莫司、雷帕黴素、哌立福辛、坦羅莫司)以及細胞凋亡途徑的調節劑(例如奧巴克拉(obataclax))。在一個實施方案中,另外的化學治療劑選自細胞毒性化學治療劑,包括三氧化二砷、博來黴素、卡巴他塞、卡培他濱、卡鉑、順鉑、環磷醯胺、阿糖胞苷、達卡巴嗪、柔紅黴素、多西他賽、阿黴素、依託泊苷、氟尿嘧啶、吉西他濱、伊立替康、洛莫司汀、甲氨蝶呤、絲裂黴素C、奧沙利鉑、紫杉醇、培美曲塞、替莫唑胺、以及長春新鹼。在一個實施方案中,另外的化學治療劑選自血管發生靶向治療劑,包括阿柏西普和貝伐單抗。在一個實施方案中,另外的化學治療劑選自免疫靶向藥劑,包括阿地白介素、伊匹木單抗、拉姆單抗(lambrolizumab)、納武單抗(nivolumab)、西普魯塞-T。在一個實施方案中,另外的化學治療劑選自具有針對TrkA途徑的活性的藥劑,包括NGF-靶向生物藥劑諸如NGF抗體和panTrk抑制劑。在一個實施方案中,另外的化學治療劑或治療為放射療法,包括放射性碘療法、外部射線束放射和鐳223療法。在一個實施方案中,另外的化學治療劑包括作為癌症標準護理的以上所列出的治療或治療劑中的任一種,其中所述癌症具有TrkA調節異常。在一個實施方案中,本文提供了一種治療有需要的患者中的癌症的方法,其包括向所述患者施用化合物1或其藥學上可接受的鹽與至少一種選自以下各項的另外的治療或治療劑的組合:放射療法(例如放射性碘療法、外部射線束放射、鐳223療法)、細胞毒性化學治療劑(例如三氧化二砷、博來黴素、卡巴他塞、卡培他濱、卡鉑、順鉑、環磷醯胺、阿糖胞苷、達卡巴嗪、柔紅黴素、多西他賽、阿黴素、依託泊苷、氟尿嘧啶、吉西他濱、伊立替康、洛莫司汀、甲氨蝶呤、絲裂黴素C、奧沙利鉑、紫杉醇、培美曲塞、替莫唑胺、長春新鹼)、酪氨酸激酶靶向治療劑(例如阿法替尼(afatinib)、卡博替尼、西妥昔單抗、克唑替尼、達拉菲尼、埃羅替尼、吉非替尼、伊馬替尼、拉帕替尼、尼羅替尼、帕唑帕尼、帕木單抗、培妥珠單抗、瑞格菲尼、舒尼替尼、曲妥珠單抗)、細胞凋亡調節劑和信號轉導抑制劑(例如依維莫司、哌立福辛、雷帕黴素、比尼替尼、司美替尼、恩可非尼、索拉非尼、坦羅莫司、曲美替尼、維羅非尼)、免疫靶向療法(例如阿地白介素、幹擾素α-2b、伊匹木單抗、派姆單抗、納武單抗、潑尼松、西普魯塞-T)以及血管生成靶向療法(例如阿柏西普、貝伐單抗),其中所述化合物1或其藥學上可接受的鹽與另外的治療或治療劑組合的量有效於治療所述癌症。這些另外的治療劑可與化合物1或其藥學上可接受的鹽作為相同或單獨劑型的一部分,經由相同或不同施用途徑並按照根據本領域技術人員已知的標準藥物實踐的相同或不同施用方案施用。本文還提供了(i)一種用於治療有需要的患者中的癌症的藥物組合,其包含(a)化合物1或其藥學上可接受的鹽、(b)另外的治療劑和(c)任選地至少一種藥學上可接受的載體,以用於同時、單獨或依次用於治療癌症,其中所述化合物1或其藥學上可接受的鹽和所述另外的治療劑的量一起有效於治療所述癌症;(ii)一種包含此組合的藥物組合物;(iii)此組合用於製備治療癌症的藥物的用途;以及(iv)一種包含此組合作為用於同時、單獨或依次使用的組合製劑的商業包裝或產品;以及一種治療有需要的患者的癌症的方法。在一個實施方案中,組合治療是用於治療選自以下各項的癌症:非小細胞肺癌、乳頭狀甲狀腺癌、多形性成膠質細胞瘤、急性骨髓性白血病、結腸直腸癌、大細胞神經內分泌癌、前列腺癌、成神經細胞瘤、胰腺癌、黑色素瘤、頭頸鱗狀細胞癌以及胃癌。在一個實施方案中,組合治療是用於治療選自以下各項的癌症:非小細胞肺癌、乳頭狀甲狀腺癌、多形性成膠質細胞瘤、急性骨髓性白血病、結腸直腸癌、大細胞神經內分泌癌、前列腺癌、成神經細胞瘤、胰腺癌、黑色素瘤、頭頸鱗狀細胞癌、胃癌、膽管癌以及肉瘤。化合物1或其藥學上可接受的鹽還可用於治療炎症或炎性疾病或病症。因此,本文提供了一種治療哺乳動物中的炎症或炎性疾病或病症的方法,其包括向有需要的所述哺乳動物施用有效於治療所述炎症的量的化合物1或其藥學上可接受的鹽。在一個實施方案中,所述炎性疾病選自炎性肺病(諸如哮喘)、間質性膀胱炎(IC)、痛性膀胱症候群(PBS)、炎性腸疾病(包括潰瘍性結腸炎和克羅恩氏病)、以及炎性皮膚病諸如特異性皮炎和銀屑病。在一個實施方案中,治療炎症或炎性疾病或病症的方法包括向有需要的哺乳動物施用化合物1或其藥學上可接受的鹽與一種或多種另外的藥劑的組合。另外的藥劑的實例包括抗-TNF劑(例如單克隆抗體,諸如英利昔單抗(類克(Remicade))、阿達木單抗(修美樂(Humira))、聚乙二醇化賽妥珠單抗(Cimzia)以及戈利木單抗(辛普尼(Simponi)),或循環受體融合蛋白,諸如依那西普(恩博(Enbrel)))、抗代謝藥和抗葉酸藥(例如甲氨蝶呤)、或靶向激酶抑制劑(例如JAK家族抑制劑,諸如魯索利替尼、託法替尼、CYT387、來他替尼(Lestaurtinib)、帕克替尼(Pacritinib)以及TG101348)。這些另外的治療劑可與化合物1或其藥學上可接受的鹽作為相同或單獨劑型的一部分,經由相同或不同施用途徑並按照根據本領域技術人員已知的標準藥物實踐的相同或不同施用方案施用。化合物1或其藥學上可接受的鹽還可用於治療哺乳動物中的神經變性疾病。在一個實施方案中,化合物1或其藥學上可接受的鹽還可用於通過經由阻斷Sp35-TrkA相互作用來促進髓鞘形成、神經元存活和少突膠質細胞分化以治療脫髓鞘和髓鞘形成障礙。因此,本文還提供了一種治療哺乳動物中的神經變性疾病的方法,其包括向有需要的所述哺乳動物施用有效於治療所述神經變性疾病的量的化合物1或其藥學上可接受的鹽。在一個實施方案中,所述神經變性疾病為多發性硬化。在一個實施方案中,所述神經變性疾病為帕金森病。在一個實施方案中,所述神經變性疾病為阿爾茲海默病。本文還提供了一種治療哺乳動物中的某些感染性疾病諸如克氏錐蟲感染的方法,其包括向有需要的所述哺乳動物施用有效於治療所述克氏錐蟲感染的量的化合物1或其藥學上可接受的鹽。本文還提供了一種治療哺乳動物中的合格倫氏症候群的方法,其包括向有需要的所述哺乳動物施用有效於治療所述症候群的量的化合物1或其藥學上可接受的鹽。本文還提供了一種治療哺乳動物中的子宮內膜異位的方法,其包括向有需要的所述哺乳動物施用有效於治療所述子宮內膜異位的量的化合物1或其藥學上可接受的鹽。本文還提供了一種治療哺乳動物中的糖尿病性周圍神經病變的方法,其包括向有需要的所述哺乳動物施用有效於治療所述糖尿病性周圍神經病變的量的化合物1或其藥學上可接受的鹽。本文還提供了一種治療哺乳動物中的前列腺炎的方法,其包括向有需要的所述哺乳動物施用有效於治療所述前列腺炎的量的化合物1或其藥學上可接受的鹽。本文還提供了一種治療哺乳動物中的盆腔疼痛症候群的方法,其包括向有需要的所述哺乳動物施用有效於治療所述盆腔疼痛症候群的量的化合物1或其藥學上可接受的鹽。本文還提供了一種治療哺乳動物中與骨重塑調節失衡相關的疾病的方法,其包括向有需要的所述哺乳動物施用有效於治療所述疾病的量的化合物1或其藥學上可接受的鹽。在一個實施方案中,所述疾病為骨質疏鬆症、類風溼性關節炎或骨轉移。在一個實施方案中,用於治療有需要的哺乳動物中與骨重塑調節失衡相關的疾病的方法包括施用化合物1或其藥學上可接受的鹽與一種或多種另外的治療劑或治療的組合。另外的治療劑或治療的實例包括抗-TNF治療(例如單克隆抗體,諸如英利昔單抗(類克)、阿達木單抗(修美樂)、聚乙二醇化賽妥珠單抗(Cimzia)以及戈利木單抗(辛普尼),或使用循環受體融合蛋白,諸如依那西普(恩博))、抗代謝藥和抗葉酸藥(例如甲氨蝶呤)、或靶向激酶抑制劑(例如JAK家族抑制劑魯索利替尼、託法替尼、CYT387、來他替尼、帕克替尼以及TG101348)。這些另外的治療劑可與化合物1或其藥學上可接受的鹽作為相同或單獨劑型的一部分,經由相同或不同施用途徑並按照根據本領域技術人員已知的標準藥物實踐的相同或不同施用方案施用。本文還提供了一種治療有需要的哺乳動物中由結締組織生長因子異常信號傳導引起的疾病的方法,其包括向所述哺乳動物施用有效於治療所述疾病的量的化合物1或其藥學上可接受的鹽。在一個實施方案中,由結締組織生長因子異常信號傳導引起的疾病為雷諾氏症候群、特發性肺纖維化、瘢痕(肥大型、瘢痕瘤型和其他形式)、硬化、心內膜心肌纖維化、心房纖維化、骨髓纖維化、進行性塊狀纖維化(肺)、腎源性系統性纖維化、硬皮病、系統性硬化、關節纖維化或眼部纖維化。如本文所用的,「有效量」意指化合物當向需要此治療的哺乳動物施用時足以(i)治療可用化合物1或其藥學上可接受的鹽治療的特定疾病、疾患或病症,或者(ii)減輕、改善或消除本文所述特定疾病、疾患或病症的一種或多種症狀的量。化合物1將與此量對應的量將根據各種因素改變,所述因素諸如疾病疾患及其嚴重性和需要治療的哺乳動物的特性(例如,體重),但也可由本領域技術人員常規測定。如本文所用的,術語「哺乳動物」是指具有發展本文所述的疾病的風險或處於所述風險下的溫血動物並且包括但不限於,豚鼠、狗、貓、大鼠、小鼠、倉鼠、以及靈長類(包括人類)。化合物1或其藥學上可接受的鹽可通過任何常規路徑施用到例如胃腸道(例如經直腸地或經口地)、鼻、肺、肌肉系統或脈管系統、創口灌洗、或經皮地或經真皮地。化合物1或其藥學上可接受的鹽可以任何常規施用形式施用,所述施用形式例如片劑、散劑、膠囊、溶液、分散劑、懸浮劑、糖漿劑、噴霧劑、栓劑、凝膠劑、乳劑、貼劑等。此類組合物可含有藥物製劑中常見的組分,例如稀釋劑、載體、pH調節劑、甜味劑、膨脹劑、以及其他活性劑。如果希望胃腸外施用,則所述組合物將為無菌的並且為可用於注射或輸注的溶液或懸浮液形式。此類組合物構成本發明的另一個方面。另一種製劑可通過將化合物1或其藥學上可接受的鹽和載體或賦形劑混合來製備。適合的載體和賦形劑為本領域技術人員所熟知的。所述製劑還可包含一種或多種緩衝劑、穩定劑、表面活性劑、潤溼劑、潤滑劑、乳化劑、助懸劑、防腐劑、抗氧化劑、遮光劑、助流劑、加工助劑、著色劑、甜味劑、芳香劑、調味劑、稀釋劑以及提供藥物(即本文所述的化合物或其藥物組合物)高雅外觀或有助於製造藥物產品(即藥品)的其他已知添加劑。因此,本文還提供了一種藥物組合物,其包含化合物1或其藥學上可接受的鹽和藥學上可接受的稀釋劑或載體。在一個實施方案中,配製一種包含化合物1或其藥學上可接受的鹽的藥物組合物以用於經口施用。在一個實施方案中,配製用於經口施用的一種包含化合物1或其藥學上可接受的鹽的藥物組合物為片劑或膠囊形式。本文還提供了化合物1或其藥學上可接受的鹽以供用於治療哺乳動物中的疼痛。在一個實施方案中,所述疼痛為慢性疼痛。在一個實施方案中,所述疼痛為急性疼痛。在一個實施方案中,所述疼痛為慢性背痛、炎性疼痛、神經性疼痛或與癌症、手術或骨折有關的疼痛。本文還提供了化合物1或其藥學上可接受的鹽以供用於治療哺乳動物中的癌症。在一個實施方案中,所述癌症選自非小細胞肺癌、乳頭狀甲狀腺癌、多形性成膠質細胞瘤、急性骨髓性白血病、結腸直腸癌、大細胞神經內分泌癌、前列腺癌、成神經細胞瘤、胰腺癌、黑色素瘤、頭頸鱗狀細胞癌、胃癌、膽管癌以及肉瘤。本文還提供了化合物1或其藥學上可接受的鹽以供用於治療哺乳動物中的炎症或炎性疾病或病症。在一個實施方案中,所述炎性疾病為炎性肺病(諸如哮喘)、間質性膀胱炎、膀胱疼痛症候群、炎性腸疾病(包括潰瘍性結腸炎和克羅恩氏病)、以及炎性皮膚病諸如特異性皮炎。本文還提供了化合物1或其藥學上可接受的鹽以供用於治療哺乳動物中的感染性疾病,例如克氏錐蟲感染。本文還提供了化合物1或其藥學上可接受的鹽以供用於治療哺乳動物中的合格倫氏症候群。本文還提供了化合物1或其藥學上可接受的鹽以供用於治療哺乳動物中的子宮內膜異位。本文還提供了化合物1或其藥學上可接受的鹽以供用於治療哺乳動物中的糖尿病性周圍神經病變。本文還提供了化合物1或其藥學上可接受的鹽以供用於治療哺乳動物中的前列腺炎。本文還提供了化合物1或其藥學上可接受的鹽以供用於治療哺乳動物中的盆腔疼痛症候群。本文還提供了化合物1或其藥學上可接受的鹽以供用於治療哺乳動物中的神經變性疾病。本文還提供了化合物1或其藥學上可接受的鹽以供用於治療與骨重塑調節失衡相關的疾病。本文還提供了化合物1或其藥學上可接受的鹽以供用於治療由結締組織生長因子異常信號傳導引起的疾病。本文還提供了化合物1或其藥學上可接受的鹽在製造用於治療選自以下各項的疾患的藥物中的用途:疼痛、癌症、炎症、神經變性疾病、克氏錐蟲感染、以及由結締組織生長因子異常信號傳導引起的疾病。在一個實施方案中,所述疾患為慢性疼痛。在一個實施方案中,所述疾患為急性疼痛。在一個實施方案中,所述疼痛為慢性背痛。在一個實施方案中,所述疼痛為炎性疼痛、神經性疼痛或與癌症、手術或骨折有關的疼痛。在一個實施方案中,所述疾患為癌症。在一個實施方案中,所述疾患為炎症。在一個實施方案中,所述疾患為神經變性疾病。在一個實施方案中,所述疾患為克氏錐蟲感染。在一個實施方案中,所述疾患為舍格倫氏症候群。在一個實施方案中,所述疾患為子宮內膜異位。在一個實施方案中,所述疾患為糖尿病性周圍神經病變。在一個實施方案中,所述疾患為前列腺炎。在一個實施方案中,所述疾患為盆腔疼痛症候群。在一個實施方案中,所述疾病為與骨重塑調節失衡相關的疾病。在一個實施方案中,所述疾病為由結締組織生長因子異常信號傳導引起的疾病。本文還提供了一種藥品,其包含用於治療哺乳動物中的疼痛的化合物1或其藥學上可接受的鹽與選自以下各項的另一種治療劑的組合:抗炎化合物、類固醇(例如,地塞米松、可的松和氟替卡松)、止痛劑諸如NSAID(例如,阿司匹林、布洛芬、消炎痛和酮洛芬)、阿片類(諸如嗎啡)、降鈣素基因相關肽受體拮抗劑、亞型選擇性離子通道調節劑、抗驚厥藥(例如普瑞巴林和加巴噴丁)、雙重血清素-去甲腎上腺素再吸收抑制劑(例如度洛西汀、文拉法辛和米那普侖)、JAK家族激酶抑制劑(諸如,魯索利替尼或託法替尼)、以及三環抗抑鬱藥(諸如阿米替林,去甲阿米替林和脫甲丙咪嗪)。在一個實施方案中,本文提供了一種藥品,其包含用於治療哺乳動物中的疼痛的化合物1或其藥學上可接受的鹽與NSAID的組合。本文還提供了一種藥品,其包含用於治療哺乳動物中的疼痛的選自以下各項的治療劑與化合物1或其藥學上可接受的鹽的組合:抗炎化合物、類固醇(例如,地塞米松、可的松和氟替卡松)、止痛劑諸如NSAID(例如,阿司匹林、布洛芬、消炎痛和酮洛芬)和阿片類(諸如嗎啡)。實施例合成中間體的製備製備A(3S,4R)-4-(3-氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-胺二鹽酸鹽步驟A:(3S,4R)-4-(3-氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-基氨基甲酸叔丁酯的製備:將(3S,4R)-4-(3-氟苯基)吡咯烷-3-基氨基甲酸叔丁酯(250mg,0.89mmol,商購獲得)、DIEA(0.48mL,2.68mmol)和1-溴-2-甲氧基乙烷(149mg,1.07mmol)於DMF(3mL)中的溶液在環境溫度下攪拌2小時,然後加熱至60℃持續4小時,隨後經16小時冷卻至環境溫度。在分配於EtOAc與飽和NaHCO3(各自10mL)之間之後,將有機層用水和鹽水(各自2x10mL)洗滌,經Na2SO4乾燥,過濾並濃縮,以獲得呈粘稠橙色油狀物的(3S,4R)-4-(3-氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-基氨基甲酸叔丁酯(250mg,83%產率)。LCMS(apci)m/z=339.1(M+H)。步驟B:(3S,4R)-4-(3-氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-胺二鹽酸鹽的製備:將5-6NHCl中的(3S,4R)-4-(3-氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-基氨基甲酸叔丁酯(250mg,0.74mmol)於異丙醇(14.8mL,73.9mmol)中的溶液在環境溫度下攪拌1小時。在真空下濃縮混合物並用Et2O研磨以獲得呈米色固體的標題化合物(230mg,100%產率)。LCMS(apci)m/z=239.1(M+H)。製備B4-甲基-3-(2-甲基嘧啶-5-基)-1-苯基-1H-吡唑-5-胺步驟A:5-氨基-4-甲基-1-苯基-1H-吡唑-3(2H)-酮的製備:將2-氰基丙酸乙酯(50.5g,397.2mmol)和苯肼(39mL,397.2mmol)於二噁烷(100mL)中的混合物在110℃下加熱5天。將冷卻的混合物濃縮至1/2體積並且隨後在冰中冷卻並用冷Et2O研磨。過濾所得固體,用Et2O充分洗滌並在真空下乾燥,以獲得呈蓬鬆白色粉末的5-氨基-4-甲基-1-苯基-1H-吡唑-3(2H)-酮(34.69g,46%產率)。MS(apci)m/z=190.1(M+H)。步驟B:5-氨基-4-甲基-1-苯基-1H-吡唑-3-基三氟甲烷磺酸酯的製備:用DIEA(37.9mL,217.5mmol)處理5-氨基-4-甲基-1-苯基-1H-吡唑-3(2H)-酮(13.72g,72.5mmol)和N-苯基雙(三氟甲基磺醯胺)(27.2g,76.1mmol)於DMF(100mL)中的懸浮液並且將混合物在環境溫度下攪拌16小時。使所述混合物分配在飽和NaHCO3(400mL)與EtOAc(200mL)之間並且用EtOAc(2x200mL)萃取水層。用水(5x50mL)和鹽水(50mL)洗滌合併的有機相,然後經Na2SO4乾燥,過濾並真空濃縮。通過用4∶1己烷/EtOAc洗脫的矽膠柱色譜法純化殘餘物,以獲得呈淡黃色固體的5-氨基-4-甲基-1-苯基-1H-吡唑-3-基三氟甲烷磺酸酯(23.1g,99%產率)。MS(apci)m/z=322.0(M+H)。步驟C:4-甲基-3-(2-甲基嘧啶-5-基)-1-苯基-1H-吡唑-5-胺:將5-氨基-4-甲基-1-苯基-1H-吡唑-3-基三氟甲烷磺酸酯(900mg,2.8mmol)、2-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧雜硼雜戊烷-2-基)嘧啶(925mg,4.2mmol)、K2CO3(1.55g,11.2mmol)和Pd(PPh3)4(324mg,0.28mmol)合併在甲苯(10mL)、水(5mL)和EtOH(2.5mL)中並在密封管中升溫至95℃,持續16小時。將冷卻的混合物過濾並使濾液分配在水(50mL)與EtOAc(50mL)之間。用EtOAc(2x30mL)萃取水層並用鹽水(30mL)洗滌合併的有機相,經Na2SO4乾燥、過濾並在真空下濃縮。通過用2%MeOH/DCM洗脫的矽膠柱色譜法純化殘餘物,以獲得呈粉色固體的標題化合物(533mg,72%產率)。MS(apci)m/z=266.1(M+H)。製備C2-甲氧基-N-(甲氧基甲基)-N-((三甲基甲矽烷基)甲基)乙胺步驟A:2-甲氧基-N-((三甲基甲矽烷基)甲基)乙胺的製備:在40分鐘內在90℃下通過加料漏鬥向2-甲氧基乙胺(14.2mL,163mmol)的DMSO溶液(15mL)中添加(氯甲基)三甲基矽烷(11.4mL,81.5mmol)的DMSO(10mL)溶液。將混合物在90℃下加熱3.5小時,然後冷卻至環境溫度。然後用H2O(150mL)稀釋混合物並且用EtOAc(2×150mL)萃取。用鹽水(150mL)洗滌合併的有機萃取物,用MgSO4乾燥,過濾並濃縮,以獲得呈黃色油狀物的2-甲氧基-N-((三甲基甲矽烷基)甲基)乙胺(8.14g,62%產率)。MS(apci)m/z=162.0(M+H)。步驟B:2-甲氧基-N-(甲氧基甲基)-N-((三甲基甲矽烷基)甲基)乙胺的製備:將甲醛(37%水溶液,4.91g,60.6mmol)的MeOH(2.45mL)溶液冷卻至0℃,並通過逐滴添加2-甲氧基-N-((三甲基甲矽烷基)甲基)乙胺(8.14g,50.5mmol)來處理。將雙相混合物在0℃下攪拌3小時,然後添加K2CO3(6.97g,50.5mmol)並在0℃下攪拌1小時。將黃色油狀物傾析到K2CO3(2.00g,14.4mmol)上,並且將混合物在環境溫度下攪拌2小時。在傾析黃色油狀物之後,用Et2O(2×10mL)洗滌固體K2CO3,並且將Et2O洗滌物與傾析的黃色油狀物合併並在旋轉蒸發器上濃縮,以產生呈黃色油狀物的標題化合物(9.92g,96%產率)。1HNMR(CDCl3)δ4.00(s,2H),3.37-3.43(m,2H),3.29(s,3H),3.19(s,3H),2.77-2.82(m,2H),2.18(s,2H),0.00(s,9H)ppm。製備D(3S,4R)-4-(3-氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-胺步驟A:(反式)-4-(3-氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-羧酸的製備:依次用EtOAc(75mL)和庚烷(75mL)處理(E)-3-(3-氟苯基)丙烯酸(25.20g,151.7mmol),隨後用TFA(1.17mL,15.17mmol)處理。將混合物置於冷水浴(內部溫度15℃)中,並在20分鐘內從加料漏鬥中逐滴添加2-甲氧基-N-(甲氧基甲基)-N-((三甲基甲矽烷基)甲基)乙胺[製備C](69.82g,197.2mmol),加冰到水浴中,以使內部溫度在添加過程中維持在13℃-19℃。移除冰浴並將混合物在環境溫度下攪拌18小時,然後冷卻(內部溫度13℃),並且在6分鐘內從加料漏鬥中逐滴添加另外的2-甲氧基-N-(甲氧基甲基)-N-((三甲基甲矽烷基)甲基)乙胺(製備C;34g)。移除水浴並在環境溫度下再攪拌4小時之後,將混合物濃縮至一半體積。加入庚烷(100mL)並部分濃縮混合物,除去約150mL溶劑。將此步驟重複兩次,每次除去100mL溶劑。將殘餘漿液用庚烷(50mL)衝洗到燒瓶底部內,然後密封並在環境溫度下攪拌64小時。將固體過濾,用庚烷(2x50mL)衝洗並在真空下乾燥,以獲得呈淡黃色固體的(反式)-4-(3-氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-羧酸(44.99g,111%產率),其直接用於下一個步驟,假定100%產率。MS(apci)m/z=268.1(M+H)。步驟B:(反式)-4-(3-氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-甲醯胺的製備:向(反式)-4-(3-氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-羧酸(40.54g,151.7mmol)於THF(440mL)中的懸浮液添加CDI(31.97g,197.2mmol),接著添加咪唑鹽酸鹽(3.171g,30.33mmol)。將反應混合物在環境溫度下攪拌16小時,並隨後在30分鐘內通過加料漏鬥添加氨(135.0mL,2M於iPrOH中,270.0mmol)。在再攪拌3小時之後,過濾所得固體,用EtOAc洗滌並濃縮濾液。將殘餘物溶解於EtOAc(200mL)中並用25/75水∶鹽水(2x200mL)洗滌。經MgSO4乾燥有機相,將其過濾,濃縮並在真空下乾燥,以得到呈黃色固體的(反式)-4-(3-氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-甲醯胺(54.97g,136%產率),其可使用,假定100%產率。MS(apci)m/z=267.2(M+H)。步驟C:(反式)-4-(3-氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-胺的製備:在20分鐘內通過加料漏鬥向配有溫度計、在冰浴中冷卻的3頸1-L圓底燒瓶中的(反式)-4-(3-氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-甲醯胺(29.33g,85.90mmol)於MeOH(345mL)中的溶液添加NaOCl(10%-15%可用的Cl,水溶液)(116.3mL,189.0mmol)[內部溫度為7℃-13℃]。去除冰浴並將不均勻混合物在環境溫度下攪拌90分鐘,然後在55℃下攪拌3小時。添加KOH(67.48g,1203mmol)於H2O(225.9mL,12,542mmol)中的溶液並將所述溶液在75℃下攪拌19小時。將混合物冷卻至0℃並且在30分鐘內緩慢添加濃HCl(147.1mL,4,802mmol)。通過添加K3PO4水溶液(30重量%,155mL)將pH調節至6,並且將混合物部分濃縮以去除有機溶劑。添加水性K3PO4(30重量%,280mL)直到pH10,並且用EtOAc(2x450mL)萃取所述混合物。將合併的有機萃取物濃縮並在真空下乾燥,以獲得呈深琥珀色漿液的(反式)-4-(3-氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-胺(28.08g,91%產率)。MS(apci)m/z=239.2(M+H)。步驟D:(3S,4R)-4-(3-氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-胺(2S,3S)-2,3-雙((4-甲基苯甲醯基)氧基)琥珀酸酯的製備:將(反式)-4-(3-氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-胺(125mg,0.52mmol)和(2S,3S)-2,3-雙((4-甲基苯甲醯基)氧基)琥珀酸(222.9mg,0.58mmol)稱量到4mL小瓶中,然後用MeOH(1.57mL)處理,接著用水(0.175mL)處理。將小瓶加蓋並將反應混合物在50℃下攪拌5分鐘,然後經17小時使其緩慢冷卻至環境溫度。將所得的固體過濾,用Et2O(4x0.2mL)洗滌並在真空下乾燥,以獲得呈白色固體的(3S,4R)-4-(3-氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-胺(2S,3S)-2,3-雙((4-甲基苯甲醯基)氧基)琥珀酸酯(131.6mg,40%產率)。游離鹼性樣品的手性SFC分析指示>95%對映體過量(ee)。在以下步驟中將此物質用作晶種:將(反式)-4-(3-氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-胺(7.39g,18.61mmol)溶解於MeOH(52.7mL)中並用(2S,3S)-2,3-雙((4-甲基苯甲醯基)氧基)琥珀酸(10.78g,27.91mmol)、接著用H2O(9.3mL)處理。將混合物在50℃下攪拌5分鐘。將晶種(90mg)添加到溶液中,並經16小時使所述混合物緩慢升溫至環境溫度。將所得固體過濾,用Et2O(4x5mL)衝洗並在真空下乾燥。使殘餘物在MeOH(15mL)和H2O(2.7mL)中漿化,在50℃下攪拌15分鐘,然後經19小時使其緩慢冷卻至環境溫度。將固體過濾,用Et2O(3x5mL)洗滌並在真空下乾燥,以獲得呈白色固體的(3S,4R)-4-(3-氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-胺(2S,3S)-2,3-雙((4-甲基苯甲醯基)氧基)琥珀酸酯(3.12g,27%產率)。游離鹼性樣品的手性分析指示>99.7%對映體過量。步驟E:(3S,4R)-4-(3-氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-胺的製備:用1M水性NaOH(2x15mL)洗滌(3S,4R)-4-(3-氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-胺(2S,3S)-2,3-雙((4-甲基苯甲醯基)氧基)琥珀酸酯(2.89g,4.63mmol)於DCM(25mL)中的懸浮液。用DCM(25mL)萃取合併的水相,並用鹽水(30mL)洗滌合併的有機萃取物,經Na2SO4乾燥、過濾、濃縮並在真空下乾燥,以獲得呈淺褐色油狀物(3S,4R)-4-(3-氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-胺(998mg,90%產率)、MS(apci)m/z=239.2(M+H)。合成實施例實施例11-((3S,4R)-4-(3-氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-基)-3-(4-甲基-3-(2-甲基嘧啶-5-基)-1-苯基-1H-吡唑-5-基)脲二鹽酸鹽步驟A:1-((3S,4R)-4-(3-氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-基)-3-(4-甲基-3-(2-甲基嘧啶-5-基)-1-苯基-1H-吡唑-5-基)脲的製備:向4-甲基-3-(2-甲基嘧啶-5-基)-1-苯基-1H-吡唑-5-胺(製備B;61mg,0.16mmol)於DCM(2mL)中的溶液添加三光氣(24mg,0.08mmol),接著添加DIEA(84μL,0.48mmol)。將混合物在環境溫度下攪拌15分鐘,然後用(3S,4R)-4-(3-氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-胺二鹽酸鹽(製備A;50mg,0.16mmol)和DIEA(84μL,0.48mmol)處理。將反應混合物攪拌16小時。使所述混合物分配在水(10mL)與DCM(10mL)之間並且用DCM(2x10mL)萃取水層。用鹽水(10mL)洗滌合併的有機相,經Na2SO4乾燥,過濾並濃縮。通過用2.5%-5%MeOH/DCM洗脫的矽膠柱色譜法純化殘餘物。通過反相HPLC(5%-95%ACN/水/0.1%TFA)純化含有所述產物的級分,以在鹼性水性後處理之後獲得呈白色固體的標題化合物(28mg,33%產率)。MS(apci)m/z=530.3(M+H)。步驟B:1-((3S,4R)-4-(3-氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-基)-3-(4-甲基-3-(2-甲基嘧啶-5-基)-1-苯基-1H-吡唑-5-基)脲二鹽酸鹽的製備:向冷卻至0℃的4-甲基-3-(2-甲基嘧啶-5-基)-1-苯基-1H-吡唑-5-胺(製備B;2.56g,9.64mmol)於DCM(96mL)中的溶液一次性添加三光氣(1.72g,5.78mmol),接著逐滴添加DIEA(8.40mL,48.20mmol)。將混合物在0℃下攪拌1小時。在10分鐘內將(3S,4R)-4-(3-氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-胺二鹽酸鹽(製備A;3.0g,9.64mmol)分小批添加到混合物中。將反應混合物在環境溫度下攪拌40分鐘,然後將其倒入到水(100mL)中。在相分離之後,用DCM(2x100mL)萃取水層。用鹽水(100mL)洗滌合併的有機相、過濾並濃縮。通過反相色譜法(SNAP120gC18,具有0.1%HCl的5%至75%MeOH/水)純化殘餘物並在真空下乾燥,以獲得呈奶油色泡沫的標題化合物(3.33g,57%產率)。MS(apci)m/z=530.3(M+H)。實施例21-((3S,4R)-4-(3-氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-基)-3-(4-甲基-3-(2-甲基嘧啶-5-基)-1-苯基-1H-吡唑-5-基)脲向4-甲基-3-(2-甲基嘧啶-5-基)-1-苯基-1H-吡唑-5-胺(製備B;800mg,3.02mmol)於DCM(15mL)中的懸浮液添加三乙胺(2.1mg,15.1mmol),接著添加CDI(587mg,3.62mmol)。將混合物在N2下密封並在環境溫度下攪拌22小時,然後用DCM(4mL)中的(3S,4R)-4-(3-氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-胺(製備D;826mg,3.47mmol)處理。繼續攪拌100分鐘。使所述混合物分配在DCM(60mL)與水(100mL)之間。在相分離之後,用0.5NHCl(50mL)萃取DCM層,然後用0.2NHCl(2x25mL)萃取。將酸性萃取物合併,將其傾析到乾淨燒瓶中,將其置於室溫水浴中並用6NNaOH(水溶液)、隨後用1NNaOH(水溶液)鹼化至pH9-10,同時攪拌。將懸浮液在冰浴中攪拌5分鐘。將所得固體過濾,用水和醚(各自3x20mL)衝洗並在真空下乾燥,以獲得呈白色固體的標題化合物(1.44g,90%產率)。MS(apci)m/z=530.3(M+H)。實施例3(3S,4R)-4-(3,4-二氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-胺(2S,3S)-2,3-雙((4-甲基苯甲醯基)氧基)琥珀酸酯的製備步驟A:(2-甲氧基-N-((三甲基甲矽烷基)甲基)乙胺的製備:將(氯甲基)三甲基矽烷(3300.0g,1.0當量)、乙腈(5.28L)和2-甲氧基乙胺(4041.0g,2.0當量)裝到燒瓶中。將反應混合物在74℃下攪拌16小時,然後使反應物冷卻至25℃。添加戊烷(16L)並將反應混合物攪拌1分鐘。分離各層。將底層(乙腈層)添加回到分液漏鬥中並將戊烷(16L)添加到分液漏鬥中。在攪動之後分離各層。重複用戊烷(16L)進行萃取。將合併的戊烷層添加到分液漏鬥中並加入水(3.3L)。在攪動之後分離各層。將MeOH(3.0L)添加到裝有機械攪拌的蒸汽冷凝器、J-Kem溫度探頭和加料漏鬥的22L反應器中。在25℃-45℃下進行溶劑常壓蒸餾。在蒸餾期間,將戊烷溶液通過加料漏鬥以一定速率添加到蒸餾燒瓶中,所述速率使體積保持約6.6L,直到所有戊烷溶液均在蒸餾燒瓶中。繼續蒸餾直到燒瓶中的總體積為約6.6L。將反應混合物冷卻至25℃並在環境溫度下在氮氣氛下攪拌,以提供(2-甲氧基-N-((三甲基甲矽烷基)甲基)乙胺(72%產率)。步驟B:2-甲氧基-N-(甲氧基甲基)-N-((三甲基甲矽烷基)甲基)乙胺的製備:將(2-甲氧基-N-((三甲基甲矽烷基)甲基)乙胺(380.0g,1.0當量)、甲醇(332mL)和戊烷(193mL)裝入到燒瓶中。將反應混合物在低於5℃的冷水浴中攪拌。將37%甲醛水溶液(97.9mL,1.2當量)以使內部溫度保持低於10℃的速率添加到反應混合物,並且將反應混合物在低於10℃的溫度下攪拌2小時。將叔丁基甲基醚(700mL,5.2當量)和水(300.0mL)添加到反應混合物,並且將所述混合物在環境溫度下攪拌約1分鐘。分離各層,並將有機層添加回到分液漏鬥中。將鹽水(300mL)添加到分液漏鬥。將混合物攪動並分離各層。將碳酸鉀K2CO3(10.0g)添加到有機層,並且在混合之後將有機層經濾紙過濾。用叔丁基甲基醚衝洗濾餅。將合併的有機層濃縮,以提供呈油狀物的2-甲氧基-N-(甲氧基甲基)-N-((三甲基甲矽烷基)甲基)乙胺(75%產率)。步驟C:反式-4-(3,4-二氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-羧酸的製備:將(E)-3-(3,4-二氟苯基)丙烯酸(57.0g,1.0當量)、乙酸乙酯(143mL和庚烷(143mL)裝入燒瓶中並攪動混合物。加入三氟乙酸(2.4mL,0.1當量)並將反應混合物冷卻至低於20℃。通過加料漏鬥以使內部溫度保持在20℃-25℃的速率添加2-甲氧基-N-(甲氧基甲基)-N-((三甲基甲矽烷基)甲基)乙胺,並且將反應混合物在20℃下攪拌2小時。將反應混合物在減壓下在10℃至27℃的溫度下濃縮。將乙酸乙酯(200mL)加入到殘餘物中,並且在減壓下濃縮混合物。將殘餘物在20℃下攪動過夜。通過真空蒸餾經由分批加入庚烷進行雜質的共沸去除(總體積:1200mL)。將所得漿液在20℃下靜置過夜,然後在濾紙上過濾。用庚烷衝洗濾餅並在真空烘箱中在45℃下乾燥約4小時,以提供反式-4-(3,4-二氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-羧酸(90%產率)。步驟D:反式-4-(3,4-二氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-甲醯胺的製備:將反式-4-(3,4-二氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-羧酸(98.3g,1.0當量)、羰基二咪唑(69.8g,1.3當量)、HCl咪唑(7.2g,0.2當量)和四氫呋喃(1000mL)裝入燒瓶中。將反應混合物在25℃下攪拌1小時,然後在環境溫度(約20℃)下在氮氣下過夜。在15分鐘內將氨(2.0M於異丙醇中)(307mL,1.8當量)加入到反應混合物中。將反應混合物在25℃下攪拌約30分鐘。將反應混合物經濾紙過濾並用EtOAc(200mL)衝洗過濾的固體。在減壓下在37℃下濃縮合併的有機層。將乙酸乙酯(200mL)加入到所得粗油狀物中並且在減壓下在37℃下濃縮混合物。將乙酸乙酯(200mL)、水(500mL)和NaCl(82.0g,4.1當量)加入到殘餘物並將混合物在環境溫度下攪拌約2分鐘。分離各層,並在減壓下在37℃下濃縮合併的有機層,以提供反式-4-(3,4-二氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-甲醯胺(99%產率)。步驟E:反式-4-(3,4-二氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-胺的製備:將反式-4-(3,4-二氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-甲醯胺(96.8g,1.0當量)和甲醇(1450mL)裝入燒瓶中並將反應混合物冷卻至5℃。通過加料漏鬥以使內部溫度保持低於20℃的速率加入10%次氯酸鈉溶液(462.2mL,2.2當量)。將反應混合物在20℃下攪拌1小時,然後在55℃下攪拌1小時。在5分鐘內將氫氧化鉀(314.6g,14.0當量)作為水溶液(100mL)加入到反應混合物中,並將反應混合物在72℃-75℃下攪拌12小時。將反應混合物冷卻至55℃,並且在10分鐘內加入37重量%HCl(583.8mL,55.9當量)以將pH調節為低於2。加入三元K3PO4(30重量%,100.0mL),以將反應混合物的pH調節至6與7之間。在減壓下在37℃下濃縮反應混合物。將所得水性混合物轉移到分液漏鬥中,並且加入30重量%三元K3PO4(540.0mL)和37重量%三元K3PO4(50.0mL)以將pH調節至≥10。加入EtOAc(1000mL)並將混合物在環境溫度下攪拌約2分鐘。分離各層,並將水層添加回到分液漏鬥中。將EtOAc(500mL)加入到分液漏鬥中,並攪動混合物。分離各層,並在減壓下濃縮合併的有機層,以提供反式-4-(3,4-二氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-胺(99%產率)。步驟F:(3S,4R)-4-(3,4-二氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-胺(2S,3S)-2,3-雙((4-甲基苯甲醯基)氧基)琥珀酸酯的製備:將反式-4-(3,4-二氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-胺(123.3g,1.0當量)和甲醇(1603mL)裝入燒瓶中。將混合物在環境溫度下攪拌。加入(2S,3S)-2,3-雙((4-甲基苯甲醯基)氧基)琥珀酸(145.0g,1.5當量)和水(295mL),並且將反應混合物加熱至65℃。用(3S,4R)-4-(3,4-二氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-胺(2S,3S)-2,3-雙((4-甲基苯甲醯基)氧基)琥珀酸酯(0.5g,0.7當量)接種反應混合物(通過小規模地進行反應來製備晶種,所述反應提供了呈固體的產物),並且將反應混合物經16小時緩慢冷卻至25℃。在濾紙上過濾漿液。用叔丁基甲基醚(700mL)衝洗濾餅,然後在真空烘箱中在45℃下乾燥約4小時,以提供(3S,4R)-4-(3,4-二氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-胺(2S,3S)-2,3-雙((4-甲基苯甲醯基)氧基)琥珀酸酯(2個步驟有35%產率)。生物測定在生物測定中,化合物1是指1-((3S,4R)-4-(3-氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-基)-3-(4-甲基-3-(2-甲基嘧啶-5-基)-1-苯基-1H-吡唑-5-基)脲;化合物2是指1-((3S,4R)-4-(3,4-二氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-基)-3-(4-甲基-3-(2-甲基嘧啶-5-基)-1-苯基-1H-吡唑-5-基)脲(在WO2012/158413中公開);並且化合物3是指1-(1′,4-二甲基-1-苯基-1H,1′H-[3,4′-二吡唑]-5-基)-3-((3S,4R)-4-(4-氟苯基)-1-(2-甲氧基乙基)吡咯烷-3-基)脲(在WO2012/158413中公開)。實施例ATrkA激酶結合測定在TrkALanthaScreenTMEu激酶結合測定中測定TrkA結合活性。在緩衝液(25mMMOPS,pH7.5,5mMMgCl2,0.005%TritonX-100)中用4nMAlexa-示蹤劑236(Invitrogen目錄號PV5592)、2nM生物素化抗-His(Invitrogen目錄號PV6090)和2nM銪標記的鏈黴親和素(Invitrogen目錄號PV5899)孵育5nMHis-標記的重組人TrkA(來自Invitrogen的6HIS標記的胞質域,目錄號PV3144)。加入化合物1、化合物2或化合物3在DMSO中的三倍連續稀釋液,以使最終百分比為2%DMSO。在22℃下孵育60分鐘之後,使用EnVision多模式讀板儀(PerkinElmer)通過在615nM和665nM下進行TR-FRET雙波長檢測來測量反應物。使用比率測量排放係數計算對照百分比。通過將四參數模型擬合至對照數據百分比來確定IC50值。化合物1當在實施例A的測定中測試時具有1.1nM的平均IC50值。化合物2當在實施例A的測定中測試時具有1.5nM的平均IC50值。化合物3當在實施例A的測定中測試時具有1.7nM的平均IC50值。實施例BTrkA細胞測定將用人野生型TrkA轉染的CHO-K1細胞以3x105個細胞/孔接種在96孔平底板中的含10%FBS的完全DMEM培養基中並且在37℃、5%CO2下使細胞附著24小時。然後用完全無血清測定培養基替換培養基並使細胞在37℃,5%CO2下飢餓1小時。使用化合物1、2或3利用最終濃度範圍為1μM至152pM的1∶3連續稀釋液處理細胞。將化合物在細胞上在37℃、5%CO2下孵育1小時。然後在37℃、5%CO2下將細胞用最終濃度30ng/mL的人NGF刺激7分鐘。去除培養基並用含有磷酸酶和蛋白酶抑制劑的裂解緩衝液裂解細胞。通過ELISA(R&D目錄號DYC2578)測量磷酸-TrkA。ELISA捕獲全部的TrkA並且檢測總磷-酪氨酸。使用Versamax讀取器在450nm波長下測量每個孔的光密度。通過將四參數模型擬合至對照數據百分比來確定IC50值。化合物1當在實施例B的測定中測試時具有1.9nM的平均IC50值。化合物2當在實施例B的測定中測試時具有1.3nM的平均IC50值。化合物3當在實施例B的測定中測試時具有6.1nM的平均IC50值。實施例C化合物1、2和3的人微粒體清除率和人肝細胞清除率肝微粒體孵育如下製備100mM磷酸鉀測定緩衝溶液(KPB)。將KH2PO4和K2HPO4二者單獨溶解於試劑級水中,以得到最終濃度100mM。製備K2HPO4∶KH2PO4的75∶25混合物v/v並且用稀HCl或稀NaOH溶液將溶液的pH調節至7.4。製備化合物1、化合物2和化合物3於DMSO中的的10mM(活性化合物)原液。在使用前立即用KPB溶液稀釋原液至2.5μM,以形成工作標準物。通過在室溫下目視檢查確定所有測試化合物均完全溶解於DMSO中。在分析那天通過用一個體積的78mg/mL葡萄糖-6-磷酸(二者均於KPB中製備,pH7.4)和7.9個體積的20mMMgCl2稀釋一個體積的17mg/mLNADP+來製備NADPH-再生溶液(NRS)。NADP+和葡萄糖-6-磷酸的最終濃度分別為1.7mg/mL和7.8mg/mL。就在使用前,通過每mLNRS原液加入10μL葡萄糖-6-磷酸脫氫酶(KPB中的150個單位/mL,pH7.4)來活化NRS。將肝微粒體用KPB稀釋至2.5mg蛋白質/mL。對於化合物1、化合物2和化合物3以及各種陽性對照(即,右美沙芬、地西泮、地爾硫卓、非那西汀、甲苯磺丁脲以及維拉帕米),將20μL2.5μM測試化合物的工作標準溶液和20μL微粒體(2.5mg蛋白質/mL)一式兩份加入96-孔聚丙烯板(Costar,VWR,WestChester,PA)的每個孔中。將所述板置於37℃的孵育箱5分鐘,之後加入起始溶液。將10-μL等份的NRS溶液加入每個初始孔中,以啟動代謝。測試化合物在孵育開始時的濃度為1μM。對每個時間點(即0和20分鐘)製備一個孵育板。在37℃和100%相對溼度下進行孵育。在每個時間點,從孵育箱中取出適當的孵育板,並將含有內部標準物(150μL,60%乙腈中的0.25μM拉貝洛爾)的溶液加入到每個孔中。立即在室溫下利用Allegra臺式離心機(BeckmanCoulter,Fullerton,CA)將所述板在離心機中以2,095xg離心7分鐘。將200-μL等份的上清液從每個孔中轉移到96-孔淺層板(Costar)中。利用可再用板墊密封所述板。肝細胞孵育製備化合物1、化合物2和化合物3於DMSO中的10mM(活性化合物)原液。在肝細胞存在下如下評估化合物1、化合物2和化合物3(1μM)的體外穩定性。將低溫保存的肝細胞解凍,從運輸培養基中分離並根據供應商指南利用杜氏改良伊格爾培養基(Dulbecco’sModifiedEagleMedium),1X,高葡萄糖(DMEM,Invitrogen,Carlsbad,CA)稀釋至1x106個活細胞/mL的密度。通過臺盼藍排除法利用血球計數器(3500Hausser,VWR,WestChester,PA)測定存活力。利用補充的DMEM稀釋化合物1、化合物2和化合物3的10mM原液至2μM,以形成工作標準物。將20-μL等份的測試化合物或對照(即,安替比林、地西泮、地爾硫卓、蘿拉西泮、普萘洛爾、維拉帕米以及7-乙基-10-羥基喜樹鹼[SN-38])加入96-孔聚丙烯板(Costar,VWR,WestChester,PA)的每個測試孔中,接著立即加入20μL肝細胞懸浮液。對每個時間點(即0、60和120分鐘)製備一個孵育板,其中樣品一式兩份地製備。在37℃和100%相對溼度下進行孵育。在每個時間點,從孵育箱中取出適當的孵育板,並將含有IS(200μL,60%乙腈中的0.25μM拉貝洛爾)的溶液加入到每個孔中。在平板振蕩器(IKAMTS2/4DigitalMicrotiterShaker,VWR)上將板以700rpm混合1分鐘並且立即在室溫下利用Allegra臺式離心機(BeckmanCoulter,Fullerton,CA)在離心機中以2,095xg離心10分鐘。將200-μL等份上清液從每個孔中轉移到96孔淺層板(Costar)中。利用可再用板墊密封所述板。計算使用BioAssayEnterprise進行所有計算。通過對化合物1、化合物2、化合物3以及每種樣品的內部標準物的峰面積比率(n=2)取平均值來計算平均峰面積比率。通過測定每個時間點的峰面積比率與零時樣品的峰面積比率的比率來計算剩餘物的百分比。通過使-ln(f(t))對比時間線性回歸來測定測試化合物損失率(km)。所述回歸利用形式「y=mx」,因此模型迫使截取100%剩餘物並且假定代謝遵循一級動力學。將ln(2)除以km來確定t1/2。通過使用表5所列出且以下等式中所採用的物理和生理標度因子測量化合物1、化合物2和化合物3各自穩定性的體外半衰期來計算預測的內在清除率(CLint):其中D為特定物種每份質量的肝的肝細胞數目。W為每份重量的動物存在的平均肝質量,並且C為在孵育期間每單位體積存在的肝細胞數目。利用表5中所列出且以下等式所採用的物理和生理標度因子計算預測的肝清除率(CLh):其中Q為物種依賴性肝血流量。對於測試化合物的未結合份數(fu)無需調整。通過計算預測的CLh與肝血流量的比率確定預測的肝萃取率(ER)。表5物種WaQbD(mic.)cD(hep.)d小鼠87.090501.20E+08大鼠45.070451.35E+08兔30.871781.20E+08狗32.035551.20E+08猴32.044601.20E+08人25.720531.20E+08a)W=每份質量的動物(kg)的平均肝質量(g)。b)Q=平均肝血流量(mL/min/kg)。c)D(mic.)=每份質量的肝(g)的細胞色素P450-相關蛋白的量(mg)。d)D(hep.)=每份質量的肝臟(g)的肝細胞數目。實施例D雄性SpragueDawlev大鼠藥代動力學通過將化合物(乾燥)加入20%(羥丙基β環糊精;CDT,Inc.)(水溶液)pH5.0中並渦旋作用直到獲得均勻懸浮液(PO)或溶液(IV)來配製化合物1、化合物2和化合物3中的每一種。對於靜脈內給藥,用以O2平衡的3%異氟烷麻醉動物。向側尾靜脈施用1mL/kg劑量體積的1mg/kg化合物1、化合物2和化合物3。當動物處於麻醉狀態(以O2平衡的3%異氟烷,0.2mL/時間點)時在以下時間點從對側尾靜脈抽血到NaEDTA管(1.5%v/v)中:1、5、15、30分鐘以及1、2、4、8和24小時,並且徹底混合。對於經口給藥,大鼠在過夜禁食之後接受單次經口給藥。當動物用以O2平衡的3%異氟烷(0.2mL/時間點)麻醉後在以下時間點從側尾靜脈抽血到NaEDTA管(1.5%v/v)中:5、15和30分鐘,以及1、2、4、8、24和26小時,並且徹底混合。在24小時血液採集後,重新向動物經口給藥,並在給藥後2小時採集血漿和腦,以進行化合物分析。在去除之前用鹽水灌注腦,稱量,並且將其速凍在液氮中,直到通過LCMS/MS進行分析。通過在14,000rpm下離心10分鐘來分離血漿並且將血漿樣品轉移到具有橡皮帽的96孔板管內並保存在-20℃±5℃,直到分析。血漿分析通過首先連續稀釋(3-倍)化合物1、化合物2和化合物3於DMSO中的40-μg/mL原液以提供標準溶液,從而製備單個12點校準曲線。然後將血漿(20μL)加入到萃取板中,並將2.5μL各標準溶液加入到天然血漿中。隨後將內部標準物的原液(10.0μL於乙腈中的2.5μg/mL)加入到各標準物和樣品溶液中。通過加入317.5μL乙腈以使總體積為350μL來從20μL血漿中沉澱出蛋白物質。將樣品渦旋混合5分鐘並在AllegraX-12R離心機(BeckmanCoulter,Fullerton,CA)中在約1,500xg下在4℃下離心15分鐘。經由550μL個人移液管(PersonalPipettor)(ApricotDesigns,Monrovia,CA)將100-μL等份的各上清液轉移到96-孔板中並用HPLC級水1∶1稀釋。用板墊密封所得板並通過LC-MS/MS分析化合物在血漿中的量。LC-MS/MS系統由HTC-PAL自動進樣器(LeapTechnologies,Inc.,Carrboro,NC)、HP1100HPLC(AgilentTechnologiesInc.,SantaClara,CA)和API4000三重四極杆質譜儀(AppliedBiosystems,FosterCity,CA)組成。使用Synergi4uHydro-RP80A柱(2.1x30mm,4μm粒徑;Phenomenex,Torrance,CA)結合採用流動相A(0.1%甲酸水溶液和1%異丙醇中的10mM乙酸銨)和B(89.9%乙腈、10%甲醇、0.1%甲酸中的10mM乙酸銨)的梯度條件實現分析物和內部標準物的色譜滯留。單次注射的包括再平衡時間的總運行時間為3.5分鐘並且流速為0.8mL/分鐘。將溶劑B在1.0分鐘內從5%增加至95%,在95%下保持1.0分鐘,然後在0.1分鐘內降低至5%。時間(min)流動相A(%)流動相B(%)0.009550.259551.255952.255952.359553.50955腦分析通過首先連續稀釋(3-倍)化合物1、化合物2和化合物3各自於DMSO中的40-μg/mL原液來製備單個12點校準曲線。通過將5.0mL水加入到含有腦的50mL錐形管中來製備腦勻漿物。將管內容物用Omni-PrepMultiSampleHomogenizer(Kennesaw,GA)在22,000RPM下均質化180秒。然後將勻漿物(100μL)加入到萃取板中,並將2.5μL各標準溶液加入到天然腦勻漿物中。隨後將內部標準物的原液(10.0μL乙腈中的2.5μg/mL)加入到各標準物和樣品溶液中。通過加入237.5μL乙腈以使總體積為350μL來從100μL小鼠腫瘤均漿物中沉澱蛋白物質。將樣品渦旋混合5分鐘並在AllegraX-12R離心機(BeckmanCoulter,Fullerton,CA)中在約1,500xg下在4℃下離心15分鐘。經由550μL個人移液管(PersonalPipettor)(ApricotDesigns,Monrovia,CA)將100-μL等份的各上清液轉移到96-孔板中並用HPLC級水1∶1稀釋。用板墊密封所得板並通過LC-MS/MS分析化合物1n在腦中的量。LC-MS/MS系統由HTC-PAL自動進樣器(LeapTechnologies,Inc.,Carrboro,NC)、HP1100HPLC(AgilentTechnologiesInc.,SantaClara,CA)和API4000三重四極杆質譜儀(AppliedBiosystems,FosterCity,CA)組成。使用Synergi4μHydro-RP80A柱(2.1x30mm,4μm粒徑;Phenomenex,Torrance,CA)結合採用流動相A(0.1%甲酸水溶液和1%異丙醇中的10mM乙酸銨)和B(89.9%乙腈、10%甲醇、0.1%甲酸中的10mM乙酸銨)的梯度條件實現分析物和內部標準物的色譜滯留。時間(min)流動相A(%)流動相B(%)0.009550.259551.255952.255952.359553.50955單次注射的包括再平衡時間的總運行時間為3.5分鐘並且流速為0.8mL/分鐘。將溶劑B在1.0分鐘內從5%增加至95%,在95%下保持1.0分鐘,然後在0.1分鐘內降低至5%。使用ESI+離子化模式實現分析物的質譜檢測。在化合物1、化合物2和化合物3的原液輸注期間優化離子電流。通過多重反應檢測(MRM)每種化合物所特有的躍遷來測量分析物反應。通過使用內部專有軟體(SherlockVersion2.1)建立的非房室建模來計算藥代動力學參數。使用線性梯形求積法計算AUC。實施例E狗藥代動力學如下製備用於以1mL/kg劑量體積遞送1mg/kg的IV給藥製劑。用於配製的媒介物為水中的20%(羥丙基β環糊精;CDT,Inc.)(水溶液)。將最終體積的媒介物加入到各化合物1、化合物2和化合物3(作為無水化合物)並且攪拌混合物直到獲得均勻溶液為止。最終溶液的pH為7。用0.2μM過濾器過濾溶液,之後遞送至動物。雄性Beagle狗在過夜禁食之後接受單次靜脈內給藥。在給藥後的以下時間點在K2EDTA血液採集管中採集血液/血漿(1.5mL/時間點):0、1、5、15和30分鐘以及1、2、4、8、12、24和48小時,並且徹底混合。從清醒動物的頸靜脈、頭靜脈或隱靜脈採集血液樣品。將血液樣品保持在冰上,直到加工獲得血漿為止。將血液樣品在3200RPM下在約5℃下離心10分鐘。將血漿樣品直接轉移到96孔板管(MatrixTech,0.75mL)。將可注射橡膠帽置於96孔板管上。將血漿樣品保存在-20℃±5℃,直到分析。血漿分析通過首先連續稀釋(3-倍)化合物1、化合物2和化合物3於DMSO中的40-μg/mL原液以提供標準溶液,從而製備單個12點校準曲線。然後將血漿(20μL)加入到萃取板中,並將2.5μL各標準溶液加入到天然血漿中。隨後將內部標準物的原液(10.0μL乙腈中的2.5μg/mL)加入到各標準物和樣品溶液中。通過加入317.5μL乙腈以使總體積為350μL來從20μL血漿中沉澱出蛋白物質。將樣品渦旋混合5分鐘並在AllegraX-12R離心機(BeckmanCoulter,Fullerton,CA)中在約1,500xg下在4℃下離心15分鐘。通過550μL個人移液管(ApricotDesigns,Monrovia,CA)將100-μL等份的各上清液轉移到96-孔板中並用HPLC級水1∶1稀釋。用板墊密封所得板並通過LC-MS/MS分析化合物在血漿中的量。LC-MS/MS系統由HTC-PAL自動進樣器(LeapTechnologies,Inc.,Carrboro,NC)、HP1100HPLC(AgilentTechnologiesInc.,SantaClara,CA)和API4000三重四極杆質譜儀(AppliedBiosystems,FosterCity,CA)組成。使用Synergi4μHydro-RP80A柱(2.1x30mm,4μm粒徑;Phenomenex,Torrance,CA)結合採用流動相A(0.1%甲酸水溶液和1%異丙醇中的10mM乙酸銨)和B(89.9%乙腈、10%甲醇、0.1%甲酸中的10mM乙酸銨)的梯度條件實現分析物和內部標準物的色譜滯留。單次注射的包括再平衡時間的總運行時間為3.5分鐘並且流速為0.8mL/分鐘。將溶劑B在1.0分鐘內從5%增加至95%,在95%下保持1.0分鐘,然後在0.1分鐘內降低至5%。時間(min)流動相A(%)流動相B(%)0.009550.259551.255952.255952.359553.50955使用ESI+離子化模式實現分析物的質譜檢測。在化合物1、化合物2和化合物3的原液輸注期間優化離子電流。通過多重反應檢測(MRM)每種化合物所特有的躍遷來測量分析物反應。通過使用內部專有軟體(Sherlock2.1版)建立的非房室建模來計算藥代動力學參數。使用線性梯形求積法計算AUC。實施例FhERG測定此測定用於測量化合物1、化合物2和化合物3對人胚腎細胞(HEK293)中表達的克隆的hERG鉀通道的作用。在室溫下使用自動平行膜片鉗系統QPatch(SophionBioscienceA/S,Denmark)評估化合物1、化合物2和化合物3對哺乳動物細胞中表達的hERG(人ether-à-go-go-相關基因)鉀通道電流(IKr的替代物,快速活化的心臟延遲整流鉀電流)的體外作用。在0.3、1、3、10、30以及100μM下評估測試品,在三種或更多種細胞(n≥3)中測試各濃度。暴露於每種測試品濃度的持續時間為3分鐘。陽性對照確認了測試系統對hERG抑制的靈敏度。實施例Gp38激酶結合測定在p38αLanthaScreenTMEu激酶結合測定中測定化合物1的p38α結合活性。在緩衝液(25mM[Na+]HEPESpH7.3,10mMMgCl2,100μMNaVO4)中用5nMAlexa-示蹤劑199(Invitrogen目錄號PV5830)和2nM銪標記的抗-GST抗體(Invitrogen目錄號PV5594)孵育5nM無活性的GST-標記的重組人p38α(來自Invitrogen的GST-標記的胞質域,目錄號PV3305)。加入化合物1在DMSO中的三倍連續稀釋液,以使最終百分比為2%DMSO。在22℃下孵育60分鐘之後,使用EnVision多模式讀板儀(PerkinElmer)通過在615nM和665nM下進行TR-FRET雙波長檢測來測量反應物。使用比率測量排放係數計算對照百分比。通過將四參數模型擬合至對照數據百分比來確定IC50值。發現化合物1對TrkA比對p38α有效1000倍。實施例H脫靶激酶圖譜表徵通過Millipore,Inc.的KinaseProfilerTM業務測試在10μM濃度下化合物1針對其全部激酶板上可獲得的所有激酶的脫靶激酶活性。根據Millipore說明書在接近每種單獨激酶的Km的ATP濃度下一式兩份地運行化合物1。結果顯示在以下表中。數據被報導為對照百分比(POC)並且為兩次重複的平均值。在KinaseProfilerTM中,化合物1相對於板中的其他激酶顯示對抑制TrkA有顯著且出乎意料的選擇性。事實上,化合物1在10μM濃度下對脫靶激酶為大部分無活性的,並且因此並不預期在哺乳動物中以治療劑量抑制脫靶激酶。化合物1選擇性抑制Trk途徑而不抑制其他脫靶激酶的能力可轉變成基本上不具有與脫靶激酶抑制相關的副作用的藥物特性。此類藥物特性可代表一種比先前已報導的方法更安全的治療疼痛、炎症、癌症和某些皮膚疾病的方法。當前第1頁1 2 3 
