人源化二肽基肽酶IV(DPP4)動物的製作方法
2023-05-22 20:28:31 1
本申請要求2014年5月30日提交的美國臨時專利申請No.62/005,476、2014年9月17日提交的美國臨時專利申請No.62/051,626、以及2014年10月30日提交的美國臨時專利申請No.62/072,692的優先權,每一專利申請的公開內容均以引用方式全文併入本文。
技術領域:
本發明涉及包含編碼二肽基肽酶IV(DPP4)蛋白的核酸序列的非人動物,所述二肽基肽酶IV(DPP4)蛋白包含人序列。本發明涉及包含DPP4基因的轉基因非人動物,所述DPP4基因全部或部分是人的。本發明涉及表達人DPP4蛋白或人源化DPP4蛋白的非人動物。本發明還涉及產生和使用包含人DPP4核酸序列或人源化DPP4核酸序列的非人動物的方法。
背景技術:
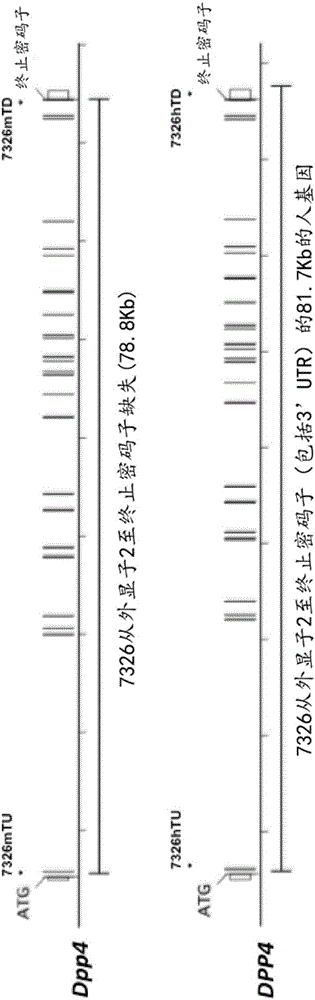
:二肽基肽酶IV(DPP4)是治療多種人類疾病、障礙和病症的治療靶標,所述疾病、障礙和病症包括例如高血糖症(參見例如,Gerich(2013)PathogenesisandManagementofPostpandrialHyperglycemia:RoleofIncretin-BasedTherapies,Intl.J.Gen.Med.6:877-895(Gerich,2013年,「餐後高血糖的發病機理和管理:基於腸降血糖素的療法的作用」,《國際全科醫學雜誌》,第6卷,第877-895頁))和中東呼吸症候群冠狀病毒(MERS-CoV)感染(參見例如,Rajetal.(2013)DipeptidylPeptidase4isaFunctionalReceptorfortheEmergingHumanCoronovirus-EMC,Nature495(7440):251-254(Raj等人,2013年,「二肽基肽酶4是新興的人冠狀病毒-EMC的功能受體」,《自然》,第495卷,第7440期,第251-254頁))。對特異性靶向人DPP4蛋白的治療性分子的藥代動力學(PK)和藥效動力學(PD)的評價通常在非人動物如齧齒動物(例如小鼠或大鼠)中進行。然而,在某些非人動物中如果這些治療性分子也不靶向內源Dpp4蛋白,則在不能適當地確定此類分子的PD。而且,在其中物種特異性拮抗劑不與內源Dpp4蛋白相互作用的某些非人動物中,在疾病的非人動物模型中評價人DPP4特異性小分子、肽或蛋白質(即,生物)拮抗劑的體內治療功效是有問題的。此外,在其中治療靶分子本身不與內源Dpp4蛋白相互作用的某些非人動物中,評價靶向與人DPP4蛋白特異性相互作用的分子的小分子、肽或蛋白質(即,生物)拮抗劑的體內治療功效也是有問題的。因此,存在對包含人DPP4基因或人源化DPP4基因的非人動物如齧齒動物(例如小鼠或大鼠)的需要。例如,存在對其中非人動物的Dpp4基因全部或部分人源化或用包含編碼人DPP4蛋白或人源化DPP4蛋白的序列的人DPP4基因置換(例如,在內源非人基因座處置換)的非人動物如齧齒動物(例如小鼠或大鼠)的需要。也存在對這樣的包含DPP4基因(例如,人DPP4基因或人源化DPP4基因)的非人動物的需要:其中所述DPP4基因在非人調控元件(例如,內源調控元件)的控制下,例如DPP4基因的5』側翼區中的調控元件(例如,啟動子和一個或多個增強子)或3』非翻譯區中的調控元件。也存在對這樣的包含DPP4基因(例如,人DPP4基因或人源化DPP4基因)的非人動物的需要:其中所述DPP4基因在人調控元件的控制下,例如人DPP4基因的5』側翼區中的調控元件(例如,啟動子或一個或多個增強子)或3』非翻譯區中的調控元件。還存在對這樣的人源化非人動物的需要:所述人源化非人動物在免疫細胞(例如T細胞)表面上,和/或在一種或多種組織(例如胎盤、腎、肺、肝、骨骼肌、心臟、腦和/或胰腺)中的細胞表面上表達人DPP4蛋白或人源化DPP4蛋白,表達水平類似於表達功能性Dpp4蛋白但不包含人DPP4基因或人源化DPP4基因的年齡匹配的非人動物的免疫細胞(例如T細胞)表面上,和/或一種或多種組織(例如胎盤、腎、肺、肝、骨骼肌、心臟、腦和/或胰腺)中的細胞表面上的Dpp4蛋白表達水平。此外,存在對這樣的人源化非人動物的需要:所述人源化非人動物在免疫細胞(例如T細胞)表面上,和/或在一種或多種組織(例如胎盤、腎、肺、肝、骨骼肌、心臟、腦和/或胰腺)中細胞表面上表達人DPP4蛋白或人源化DPP4蛋白,表達水平高於或低於表達功能性Dpp4蛋白但不包含人DPP4基因或人源化DPP4基因的年齡匹配的非人動物的免疫細胞(例如T細胞)表面上,和/或一種或多種組織(例如胎盤、腎、肺、肝、骨骼肌、心臟、腦和/或胰腺)中的細胞表面上的Dpp4蛋白的水平。在本說明書通篇中,引用了各種專利、專利申請和其他類型的出版物(例如,期刊論文、電子資料庫條目等)。本文所引用的所有專利、專利申請和其他出版物的公開內容,出於所有目的,均據此以引用方式全文併入本文。技術實現要素:本發明提供了包含編碼DPP4蛋白的核酸序列的非人動物,所述DPP4蛋白包含人序列。本發明提供了包含DPP4基因的轉基因非人動物,所述DPP4基因全部或部分是人的。本發明提供了表達人DPP4蛋白或人源化DPP4蛋白的非人動物。本發明提供了內源非人動物Dpp4基因被置換(全部或部分置換)的非人動物。本發明提供了在內源非人Dpp4基因座處包含DPP4人源化(全部或部分人源化)的非人動物。本發明提供了具有人DPP4基因或人源化DPP4基因的非人動物,其中所述非人動物不表達內源Dpp4蛋白,並且其中所述非人動物在免疫細胞(例如T細胞)表面上,和/或在一種或多種組織(包括胎盤、腎、肺、肝、骨骼肌、心臟、腦和/或胰腺)中的細胞表面上表達人DPP4蛋白或人源化DPP4蛋白,表達水平類似於表達功能性內源Dpp4蛋白但不包含置換的年齡匹配的非人動物的免疫細胞(例如T細胞)表面上,和/或一種或多種組織(包括胎盤、腎、肺、肝、骨骼肌、心臟、腦和/或胰腺)中的細胞表面上存在的Dpp4蛋白的水平。在一個方面,本發明提供了包含人DPP4核酸序列或人源化DPP4核酸序列的非人動物。在一個方面,本發明提供了經遺傳修飾的非人動物,該非人動物在內源Dpp4基因座處用編碼人DPP4蛋白或人源化DPP4蛋白的基因對編碼內源Dpp4基因的基因進行了置換。本發明提供了在內源Dpp4基因座處用人Dpp4基因置換內源Dpp4基因的齧齒動物,例如小鼠或大鼠。在一個實施例中,齧齒動物對於在內源Dpp4基因座處用編碼人DPP4蛋白或人源化DPP4蛋白的基因置換內源Dpp4基因而言是雜合的。在一個實施例中,齧齒動物對於在內源Dpp4基因座處用編碼人DPP4蛋白或人源化DPP4蛋白的基因置換內源Dpp4基因而言是純合的。在一個實施例中,齧齒動物是小鼠。在一個實施例中,齧齒動物是大鼠。在一個方面,提供了包含內源齧齒動物Dpp4基因的人源化的經遺傳修飾的齧齒動物(例如小鼠或大鼠),其中該人源化包括在內源齧齒動物Dpp4基因座處用編碼人DPP4基因的至少一個外顯子的核酸序列置換編碼Dpp4基因的外顯子的齧齒動物基因以形成經修飾的DPP4基因,其中所述經修飾的DPP4基因的表達處於內源齧齒動物Dpp4基因座處的齧齒動物調控元件的控制下。在一個實施例中,齧齒動物對於編碼人DPP4基因的至少一個外顯子的核酸序列是雜合的以形成經修飾的DPP4基因。在一個實施例中,齧齒動物對於編碼人DPP4基因的至少一個外顯子的核酸序列是純合的以形成經修飾的DPP4基因。在一個實施例中,齧齒動物是小鼠或大鼠。在一個實施例中,齧齒動物是小鼠。在一個實施例中,齧齒動物是大鼠。在一個實施例中,編碼人DPP4蛋白或人源化DPP4蛋白的人DPP4基因包含人DPP4基因的外顯子2至外顯子26。在一個實施例中,人源化DPP4蛋白包含人DPP4蛋白的細胞外結構域。在一個實施例中,人源化DPP4蛋白包含小鼠Dpp4蛋白的跨膜結構域和胞質結構域。在一個實施例中,齧齒動物是不能夠表達小鼠Dpp4蛋白的小鼠。在一個實施例中,齧齒動物是小鼠,其中用編碼人DPP4的外顯子2至外顯子26的人DPP4序列的毗鄰基因組片段置換編碼小鼠Dpp4的外顯子2至外顯子26的小鼠Dpp4序列的毗鄰基因組片段。在一個方面,提供表達人DPP4蛋白或人源化DPP4蛋白的經遺傳修飾的齧齒動物(例如小鼠或大鼠),其中該表達人DPP4蛋白或人源化DPP4蛋白的齧齒動物包含正常的免疫系統,即,表達人DPP4蛋白或人源化DPP4蛋白的齧齒動物的血液、血漿或血清中的免疫細胞(例如T細胞)的數量類似於表達功能性內源Dpp4蛋白的齧齒動物的血液、血漿或血清中的免疫細胞(例如T細胞)的數量。在一個實施例中,齧齒動物是小鼠。在一個實施例中,齧齒動物是大鼠。在一個實施例中,表達人DPP4蛋白或人源化DPP4蛋白的齧齒動物的血液具有與表達功能性內源Dpp4蛋白的齧齒動物(例如野生型小鼠或大鼠)大約相同數量的免疫細胞(例如T細胞)。在一個實施例中,齧齒動物是小鼠。在一個實施例中,齧齒動物是大鼠。在一個實施例中,在T細胞的表面上表達人DPP4或人源化DPP4的小鼠的血液中存在的T細胞量是表達功能性內源Dpp4蛋白但在內源小鼠Dpp4基因座處不用人DPP4基因置換內源Dpp4基因的年齡匹配的小鼠的血液中存在的T細胞量的至少約20%、30%、40%、50%、60%、70%、80%、90%、100%、110%、120%、130%、140%、150%、160%、170%、180%、190%或200%。在一個實施例中,在T細胞的表面上表達人DPP4蛋白或人源化DPP4蛋白的小鼠的血液中的T細胞量是表達功能性內源Dpp4蛋白但在內源小鼠Dpp4基因座處不用人DPP4基因置換內源Dpp4基因的年齡匹配的小鼠血液中存在的T細胞量的在約20%與約200%之間、約40%與約160%之間或約80%與約120%之間。在一個方面,提供了表達人DPP4蛋白或人源化DPP4蛋白的經遺傳修飾的齧齒動物(例如小鼠或大鼠),其中該齧齒動物在表達功能性內源Dpp4蛋白且年齡匹配的齧齒動物的免疫細胞(例如T細胞)表面上,和/或一種或多種組織(例如胎盤、腎、肺、肝、骨骼肌、心臟、腦和/或胰腺)中的細胞的表面上表達人DPP4蛋白或人源化DPP4蛋白。在一個實施例中,齧齒動物是小鼠。在一個實施例中,齧齒動物是大鼠。在一個實施例中,表達人DPP4蛋白或人源化DPP4蛋白的齧齒動物的免疫細胞(例如T細胞)在其表面上具有與表達功能性內源Dpp4蛋白的齧齒動物(例如野生型小鼠或大鼠)的免疫細胞(例如T細胞)大約相同水平的DPP4蛋白。在一個實施例中,齧齒動物是小鼠。在一個實施例中,齧齒動物是大鼠。在一個實施例中,該小鼠在免疫細胞(例如T細胞)表面上表達人DPP4蛋白或人源化DPP4蛋白,表達水平為表達功能性內源Dpp4蛋白但在內源小鼠Dpp4基因座處不用人DPP4基因置換內源Dpp4基因的年齡匹配的小鼠的免疫細胞(例如T細胞)表面上的Dpp4蛋白水平的至少約20%、30%、40%、50%、60%、70%、80%、90%、100%、110%、120%、130%、140%、150%、160%、170%、180%、190%或200%。在一個實施例中,該小鼠在免疫細胞(例如T細胞)表面上表達人DPP4蛋白或人源化DPP4蛋白,表達水平為表達功能性內源Dpp4蛋白但在內源小鼠Dpp4基因座處不用人DPP4基因置換內源Dpp4基因的年齡匹配的小鼠的免疫細胞(例如T細胞)表面上存在的小鼠Dpp4蛋白水平的約20%與約200%之間、約40%與約160%之間或約80%至約120%之間。在一個實施例中,表達人DPP4蛋白或人源化DPP4蛋白的齧齒動物的一種或多種組織(例如胎盤、腎、肺、肝、骨骼肌、心臟、腦和/或胰腺)中的細胞在其表面上具有與表達功能性內源Dpp4蛋白的齧齒動物(例如野生型小鼠或大鼠)的一種或多種組織(例如胎盤、腎、肺、肝、骨骼肌、心臟、腦和/或胰腺)中的細胞大約相同水平的DPP4蛋白。在一個實施例中,齧齒動物是小鼠。在一個實施例中,齧齒動物是大鼠。在一個實施例中,該小鼠在一種或多種組織(例如胎盤、腎、肺、肝、骨骼肌、心臟、腦和/或胰腺)中的細胞表面上表達人DPP4蛋白或人源化DPP4蛋白,表達水平為表達功能性內源Dpp4蛋白但在內源小鼠Dpp4基因座處不用人DPP4基因置換內源Dpp4基因的年齡匹配的小鼠的一種或多種組織(例如胎盤、腎、肺、肝、骨骼肌、心臟、腦和/或胰腺)中的細胞表面上的Dpp4蛋白水平的至少約20%、30%、40%、50%、60%、70%、80%、90%、100%、110%、120%、130%、140%、150%、160%、170%、180%、190%或200%。在一個實施例中,該小鼠在一種或多種組織(例如胎盤、腎、肺、肝、骨骼肌、心臟、腦和/或胰腺)中的細胞表面上表達人DPP4蛋白或人源化DPP4蛋白,表達水平為表達功能性內源Dpp4蛋白但在內源小鼠Dpp4基因座處不用人DPP4基因置換內源Dpp4基因的年齡匹配的小鼠的一種或多種組織(例如胎盤、腎、肺、肝、骨骼肌、心臟、腦和/或胰腺)中的細胞表面上存在的小鼠Dpp4蛋白水平的約20%與約200%之間、約40%與約160%之間或約80%與約120%之間。在一個方面,提供包含人源化DPP4基因的經遺傳修飾的齧齒動物,所述人源化DPP4基因包含用人DPP4細胞外結構域編碼序列對齧齒動物Dpp4細胞外結構域編碼序列的置換,其中該人源化DPP4基因包含齧齒動物Dpp4跨膜序列和齧齒動物Dpp4胞質序列,其中該人源化DPP4基因處於內源Dpp4基因座處的內源齧齒動物Dpp4調控元件的控制下。在一個實施例中,齧齒動物對於人源化DPP4基因是雜合的。在一個實施例中,齧齒動物對於人源化DPP4基因是純合的。在一個實施例中,齧齒動物是小鼠或大鼠。在一個實施例中,齧齒動物是小鼠。在一個實施例中,齧齒動物是大鼠。在一個實施例中,小鼠不能夠表達小鼠Dpp4蛋白。在一個實施例中,內源齧齒動物Dpp4基因座處的齧齒動物調控元件或序列來自小鼠或大鼠。在一個實施例中,齧齒動物調控元件或序列是齧齒動物Dpp4基因座處的內源齧齒動物調控元件或序列並且來自小鼠或大鼠。在一個方面,提供表達人DPP4蛋白或人源化DPP4蛋白的非人動物如齧齒動物(例如小鼠或大鼠),其中所述非人動物表達來自內源非人Dpp4基因座的人DPP4蛋白或人源化DPP4蛋白。在一個實施例中,非人動物是齧齒動物。在一個實施例中,齧齒動物是小鼠。在一個實施例中,齧齒動物是大鼠。在一個實施例中,齧齒動物對於表達人DPP4蛋白或人源化DPP4蛋白的內源非人Dpp4基因座是雜合的。在一個實施例中,齧齒動物對於表達人DPP4蛋白或人源化DPP4蛋白的內源非人Dpp4基因座是純合的。在一個方面,提供表達來自內源小鼠Dpp4基因座的人DPP4蛋白或人源化DPP4蛋白的經遺傳修飾的小鼠,其中已用人DPP4基因完全或部分置換了內源小鼠Dpp4基因。在一個實施例中,內源小鼠Dpp4基因座處包括外顯子2至外顯子26中的終止密碼子在內的約78.8kb被缺失,並用包含人DPP4基因的外顯子2至外顯子26以及3′非翻譯序列的一部分的約81.8kb人DPP4基因序列置換。在一個具體的實施例中,該人DPP4基因包含人BACRP11-68L22的人DPP4基因的外顯子2至外顯子26以及3′非翻譯序列的一部分。在一個具體的實施例中,該DPP4基因包含小鼠Dpp4基因5』調控元件、小鼠Dpp4外顯子1(包括小鼠Dpp4蛋白的前兩個胺基酸Met和Lys以及小鼠Dpp43』調控元件(例如,3』非翻譯區))以及人DPP4基因外顯子2至外顯子26,即,除了來源於小鼠Dpp4外顯子1的前兩個胺基酸外的人DPP4蛋白編碼序列。在一個方面,提供包含編碼人DPP4蛋白或人源化DPP4蛋白的核苷酸序列的經遺傳修飾的小鼠,其中編碼人DPP4蛋白或人源化DPP4蛋白的核苷酸序列全部或部分置換編碼內源小鼠Dpp4蛋白的內源核苷酸序列。在一個實施例中,小鼠對於編碼人DPP4蛋白或人源化DPP4蛋白的核苷酸序列是雜合的。在一個實施例中,小鼠對於編碼人DPP4蛋白或人源化DPP4蛋白的核苷酸序列是純合的。在一個方面,提供用於產生人源化DPP4齧齒動物的方法,包括用包含編碼人DPP4蛋白或人源化DPP4蛋白的人DPP4基因序列的一個或多個外顯子的人DPP4基因序列置換編碼齧齒動物Dpp4蛋白的齧齒動物Dpp4基因序列,其中所述置換發生在內源齧齒動物Dpp4基因座處,並且包含編碼人DPP4蛋白或人源化DPP4蛋白的人DPP4基因序列的一個或多個外顯子的人DPP4基因序列有效地連接至內源齧齒動物Dpp4基因座處的齧齒動物調控元件或序列。在一個實施例中,齧齒動物對於編碼人DPP4蛋白或人源化DPP4蛋白的核苷酸序列是雜合的。在一個實施例中,齧齒動物對於編碼人DPP4蛋白或人源化DPP4蛋白的核苷酸序列是純合的。在一個實施例中,齧齒動物是小鼠或大鼠。在一個實施例中,齧齒動物是小鼠。在一個實施例中,齧齒動物是大鼠。在一個實施例中,齧齒動物調控元件或序列來自小鼠。在一個實施例中,齧齒動物調控元件或序列來自大鼠。在一個實施例中,齧齒動物調控元件或序列是齧齒動物Dpp4基因座處的內源齧齒動物調控元件或序列。在一個實施例中,齧齒動物是小鼠。在一個實施例中,齧齒動物是大鼠。在一個實施例中,置換齧齒動物Dpp4基因序列的人DPP4基因序列包含人DPP4基因序列的至少一個外顯子。在其他實施例中,置換齧齒動物Dpp4基因序列的人DPP4基因序列包含人DPP4基因序列的至少2個、至少3個、至少4個、至少5個、至少6個、至少7個、至少8個、至少9個、至少10個、至少11個、至少12個、至少13個、至少14個、至少15個、至少16個、至少17個、至少18個、至少19個、至少20個、至少21個、至少22個、至少23個、至少24個或至少25個外顯子。在一個實施例中,置換齧齒動物Dpp4基因序列的人DPP4基因序列包含人DPP4基因序列的所有26個外顯子。在一個實施例中,齧齒動物是小鼠。在一個實施例中,齧齒動物是大鼠。在一個實施例中,置換齧齒動物Dpp4基因序列的人Dpp4基因序列或人源化Dpp4基因序列編碼的蛋白質與人DPP4具有約85%、90%、95%、96%、97%、98%或約99%同一性。在一個實施例中,置換齧齒動物Dpp4基因序列的人Dpp4基因序列或人源化Dpp4基因序列包含編碼人DPP4蛋白的細胞外結構域的至少一個人DPP4基因序列外顯子。在其他實施例中,置換齧齒動物Dpp4基因序列的人DPP4基因序列包含編碼人DPP4蛋白的細胞外結構域的至少2個、至少3個、至少4個、至少5個、至少6個、至少7個、至少8個、至少9個、至少10個、至少11個、至少12個、至少13個、至少14個、至少15個、至少16個、至少17個、至少18個、至少19個、至少20個、至少21個、至少22個或至少23個人DPP4基因序列外顯子。在一個實施例中,置換齧齒動物Dpp4基因序列的人DPP4基因序列包含編碼人DPP4蛋白的細胞外結構域的所有24個人DPP4基因序列外顯子。在一個實施例中,齧齒動物是小鼠。在一個實施例中,齧齒動物是大鼠。在一個實施例中,置換齧齒動物Dpp4基因序列的人Dpp4基因序列或人源化Dpp4基因序列編碼的DPP4蛋白的細胞外結構域與人DPP4蛋白的細胞外結構域具有約85%、90%、95%、96%、97%、98%或約99%同一性。在一個實施例中,置換發生在內源齧齒動物Dpp4基因座處,並且包含編碼人DPP4蛋白或人源化DPP4蛋白的人DPP4基因序列的一個或多個外顯子的人DPP4基因序列有效連接至內源齧齒動物Dpp4基因座處的內源齧齒動物調控元件或序列。在一個方面,提供產生人源化DPP4小鼠的方法,包括用編碼人DPP4蛋白或人源化DPP4蛋白的人DPP4基因序列置換編碼小鼠Dpp4蛋白的小鼠Dpp4基因序列。在一個實施例中,置換發生在內源小鼠Dpp4基因座處,並且編碼人DPP4蛋白或人源化DPP4蛋白的人DPP4基因有效連接至內源小鼠Dpp4基因座處的小鼠調控元件或序列。在一個實施例中,置換發生在內源小鼠Dpp4基因座處,並且編碼人DPP4蛋白或人源化DPP4蛋白的人DPP4基因有效連接至內源小鼠Dpp4基因座處的內源小鼠調控元件或序列。在多個方面,本文所述的經遺傳修飾的非人動物如齧齒動物(例如小鼠或大鼠)包含在其種系中的遺傳修飾。在一個方面,提供包含如本文所述的遺傳修飾的非人動物如齧齒動物(例如小鼠或大鼠)胚胎。在一個方面,提供包含供體細胞的非人動物如齧齒動物(例如小鼠或大鼠)宿主胚胎,所述供體細胞包含如本文所述的遺傳修飾。在一個方面,提供包含如本文所述的遺傳修飾的多能或全能非人動物如齧齒動物(例如小鼠或大鼠)細胞。在一個實施例中,細胞是齧齒動物細胞。在一個實施例中,細胞是小鼠細胞。在一個實施例中,細胞是齧齒動物胚胎幹(ES)細胞。在一個實施例中,細胞是小鼠ES細胞。在一個方面,提供非人動物如齧齒動物(例如小鼠或大鼠)卵,其中所述非人動物卵包含異位非人動物染色體,其中所述異位非人動物染色體包含如本文所述的遺傳修飾。在一個實施例中,非人動物是齧齒動物。在一個實施例中,齧齒動物是小鼠。在一個實施例中,齧齒動物是大鼠。在一個方面,經遺傳修飾以包含人DPP4基因的小鼠胚胎、卵或細胞是C57BL品系小鼠的,所述品系選自C57BL/A、C57BL/An、C57BL/GrFa、C57BL/KaLwN、C57BL/6、C57BL/6J、C57BL/6ByJ、C57BL/6NJ、C57BL/10、C57BL/10ScSn、C57BL/10Cr和C57BL/Ola。在另一個實施例中,小鼠是129品系,選自為129P1、129P2、129P3、129X1、129S1(例如,129S1/SV、129S1/Svlm)、129S2、129S4、129S5、129S9/SvEvH、129S6(129/SvEvTac)、129S7、129S8、129T1、129T2的品系(參見例如,Festingetal.(1999)Revisednomenclatureforstrain129mice,MammalianGenome10:836(Festing等人,1999年,品系129小鼠的修訂命名),還參見Auerbachetal(2000)EstablishmentandChimeraAnalysisof129/SvEv-andC57BL/6-DerivedMouseEmbryonicStemCellLines(Auerbach等人,2000年,129/SvEv來源和C57BL/6來源的小鼠胚胎幹細胞系的建立和嵌合體分析))。在一個具體的實施例中,經遺傳修飾的小鼠是前述129品系和前述C57BL/6品系的雜種。在另一個具體的實施例中,小鼠是前述129品系的雜種,或前述BL/6品系的雜種。在一個具體的實施例中,所述雜種的129品系是129S6(129/SvEvTac)品系。在另一個實施例中,小鼠是BALB品系,例如BALB/c品系。在另一個實施例中,小鼠是BALB品系和另一前述品系的雜種。在一個實施例中,小鼠是Swiss或SwissWebster小鼠。在各個方面,包含人DPP4核酸序列或人源化DPP4核酸序列的非人動物選自哺乳動物和鳥類。在一個實施例中,非人動物是哺乳動物。在一個實施例中,哺乳動物是齧齒動物。在一個實施例中,齧齒動物是小鼠或大鼠。在一個方面,提供包含具有人DPP4基因或其片段的核酸序列的齧齒動物,其中所述人DPP4基因或其片段包含人DPP4基因的至少一個外顯子,並且其中人DPP4基因或其片段編碼人DPP4蛋白或人源化DPP4蛋白。在一個實施例中,人DPP4基因或其片段包含人DPP4基因的至少2個、3個、4個、5個、6個、7個、8個、9個、10個、11個、12個、13個、14個、15個、16個、17個、18個、18個、20個、21個、22個、23個、24個或25個外顯子。在一個實施例中,人DPP4基因或其片段包含人DPP4基因的所有26個外顯子。在一個實施例中,核酸序列還包含人DPP4基因的5』側翼區。在一個實施例中,人DPP4基因或其片段有效連接至人DPP4基因的5』側翼區。在一個實施例中,人DPP4基因的5』側翼區包含至少1kb的長度(例如,至少1、2、3、4、5、10、20、30、40、50kb或更大的長度)。在一個實施例中,人DPP4基因的5』側翼區包含至少10kb的長度。在一個實施例中,人DPP4基因的5』側翼區包含至少40kb的長度。在一個實施例中,人DPP4基因或其片段的表達處於人DPP4基因的5』側翼區的控制下。在一個實施例中,人DPP4蛋白或人源化DPP4蛋白包含SEQIDNO:24的胺基酸序列或其片段。在一個實施例中,齧齒動物在T細胞表面上表達人DPP4蛋白或人源化DPP4蛋白,表達水平為表達功能性內源齧齒動物Dpp4蛋白但不包含人DPP4基因或其片段且年齡匹配的齧齒動物的T細胞表面上存在的齧齒動物Dpp4蛋白水平的至少約20%(例如,至少約20%、30%、40%、50%、60%、70%、80%、90%、95%、98%、99%或更大)。在一個實施例中,齧齒動物在選自胎盤、腎、肺、肝、骨骼肌、心臟、腦和胰腺的一種或多種組織中的細胞表面上表達人DPP4蛋白或人源化DPP4蛋白,表達水平為表達功能性內源齧齒動物Dpp4蛋白但不包含人DPP4基因或其片段且年齡匹配的齧齒動物的一種或多種組織的表面上存在的齧齒動物Dpp4蛋白水平的至少約20%(例如,至少約20%、30%、40%、50%、60%、70%、80%、90%、95%、98%、99%或更大)。在一個實施例中,齧齒動物表達功能性內源齧齒動物Dpp4蛋白。在一個實施例中,齧齒動物是小鼠或大鼠。在一個方面,本文提供用於產生人源化轉基因齧齒動物的方法,包括將包含人DPP4基因序列的一個或多個外顯子的核酸序列整合進齧齒動物的染色體,其中所述人DPP4基因序列的一個或多個外顯子編碼人DPP4蛋白或人源化DPP4蛋白。在一個實施例中,人DPP4基因或其片段包含人DPP4基因的至少2個、3個、4個、5個、6個、7個、8個、9個、10個、11個、12個、13個、14個、15個、16個、17個、18個、18個、20個、21個、22個、23個、24個或25個外顯子。在一個實施例中,人DPP4基因或其片段包含人DPP4基因的所有26個外顯子。在一個實施例中,核酸序列還包含人DPP4基因的5』側翼區。在一個實施例中,人DPP4基因序列有效連接至人DPP4基因的5』側翼區。在一個實施例中,人DPP4蛋白或人源化DPP4蛋白包含SEQIDNO:24的胺基酸序列或其片段。在一個實施例中,齧齒動物是小鼠或大鼠。在另外的方面,提供了用於確定人特異性DPP4拮抗劑在本文所述的任何人源化DPP4齧齒動物中的體內治療功效的方法,所述方法包括向所述齧齒動物施用DPP4拮抗劑,其中所述齧齒動物感染有中東呼吸症候群冠狀病毒(MERS-CoV);以及與未施用所述DPP4拮抗劑的感染有MERS-CoV的對照齧齒動物相比,確定所述DPP4拮抗劑是否治療或預防MERS-CoV感染的一種或多種症狀。在一個實施例中,DPP4拮抗劑選自小分子、肽和抗體。在一個實施例中,DPP4拮抗劑是MERS-CoV蛋白的抗體。在一個實施例中,MERS-CoV蛋白是MERS-CoV刺突蛋白。在一個實施例中,齧齒動物感染有MERS-CoV的一個或多個毒株,所述毒株選自:Al-Hasa_1、Al-Hasa_2、Al-Hasa_3、Al-Hasa_4、Al-Hasa_12、Al-Hasa_15、Al-Hasa_16、Al-Hasa_17、Al-Hasa_18、Al-Hasa_19、Al-Hasa_21、Al-Hasa_25、Buraidah_1、EMC/2012、FRA/UAE、Hafr-Al-Batin_1、Hafr-Al-Batin_2、Hafr-Al-Batin_6、Jeddah_1、Jordan-N3/2012、Munich、Riyadh_3、Riyadh_4、Riyadh_5、Riyadh_14、Taif_1、Wadi-Ad-Dawasir_1、Riyadh_9、KFU-HKU1、KFU-HKU13、Qatar3、Qatar4、England1、England-Qatar/2012、Bisha_1、Riyadh_1和Riyadh_2。在一個實施例中,在MERS-CoV感染之前施用拮抗劑。在一個實施例中,在MERS-CoV感染之後施用拮抗劑。在一個實施例中,與MERS-CoV感染同時施用拮抗劑。在一個實施例中,MERS-CoV感染的症狀是病毒滴度或RNA水平。在一個實施例中,通過一種或多種選自以下的方法測定病毒滴度或RNA水平:qPCR、RNA印跡、噬菌斑測定和原位雜交。在一個實施例中,MERS-CoV感染的症狀是肺部炎症。在一個實施例中,通過組織化學方法評估肺部炎症。在一個實施例中,MERS-CoV感染的症狀是體重減輕。在一個實施例中,齧齒動物是小鼠或大鼠。在一個實施例中,齧齒動物是小鼠。在一個實施例中,齧齒動物是大鼠。除非從實施例或方面的上下文中明確或明顯排除,否則本文所述的每個方面和實施例能夠一起使用。附圖說明圖1A至圖1B提供用於人源化Dpp4基因座的策略的圖示,未按比例繪製。圖1A是示出跨越外顯子2至外顯子26中的終止密碼子的78.8kb小鼠Dpp4基因(上圖)被缺失,並用跨越外顯子2至外顯子26以及3′非翻譯區的一部分的81.7kb人DPP4基因(下圖)置換的示意圖,如圖所示。圖1B是示出人源化DPP4小鼠包含(i)小鼠Dpp4基因5』側翼區(包括調控序列,例如啟動子和轉錄起始位點)和外顯子1(包括起始ATG密碼子),(ii)跨越外顯子2至外顯子26的人DPP4基因(包括終止密碼子)以及3′非翻譯區的一部分(包括loxP位點),和(iii)剛好從3′開始到終止密碼子的小鼠Dpp4基因3』非翻譯區的示意圖,如圖所示。圖2示出在人源化DPP4小鼠中表達的人源化DPP4蛋白的胺基酸序列(SEQIDNO:17)。圖3示出感染後4天,對從模擬(PBS)感染或MERS-CoV(Jordan毒株)感染的F0人源化DPP4小鼠的肺組織獲得的RNA進行實時PCR的結果。圖4示出感染後4天,來自模擬(PBS)感染或MERS-CoV(Jordan毒株)感染的F0人源化DPP4小鼠的肺的氣道(10倍放大和40倍放大)和肺泡(40倍放大)的H&E染色。圖5是小鼠Dpp4(mDpp4)胺基酸序列(SEQIDNO:25)與由轉基因MAID7326/7327小鼠編碼的人DPP4(hDPP4)蛋白(SEQIDNO:26)的序列比對。序列之間不同的非同源殘基以下劃線標出,序列之間不同的同源殘基用粗體和斜體表示,並且空位用連字符示出。兩個序列之間相同的殘基用無格式的文本示出。圖6是展示人DPP4的基因、序列和染色體信息的表。圖7是示出BAC(BACRP11-345J9和BACRP11-68L22)每一者的人DPP4基因和側翼基因組序列的覆蓋度的示意圖。還示出人DPP4內的位置和人TaqManTM引物-探針組退火所在的啟動子區域(對上遊組是7333hTU,且對下遊組是7333hTD)。圖8是展示用於人TaqManTM等位基因獲得測定法的引物-探針組的表,其中7333hTU指上遊組,並且7333hTD指下遊組。圖9是由轉基因MAID7333和7334小鼠編碼的人源化DPP4蛋白的胺基酸序列(SEQIDNO:24)。圖10A是示出感染後2天和4天(dpi),感染小鼠中MERS-CoV基因組(UpERNA)的定量PCR測量結果的柱形圖。圖10B是示出在感染後2和4天,感染小鼠中MERS-CoVmRNA轉錄物(前導RNA)的定量PCR測量結果的柱形圖。圖10C是在感染後2天和4天,定量受感染的小鼠肺的MERS-CoV病毒滴度的柱形圖。均質化的小鼠肺中的MERS-CoV水平通過半數組織培養感染劑量(TCID50)測定法來定量並表示為每mL的菌斑形成單位(pfu)。圖10D是來自MERS-CoV感染小鼠的肺的用蘇木精和伊紅染色的組織學圖像的圖。示出了PBS處理小鼠、感染後2天和感染後4天的小鼠的氣道(10X)、脈管系統(10X)和間質(40X)。圖11A是示出病毒感染前用抗MERS-CoV刺突蛋白抗體(Ab2或Ab4)預處理小鼠的肺,對來自該肺的MERS-CoV基因組(UpERNA)進行定量PCR測量所得結果的柱形圖。圖11B是示出病毒感染前用抗MERS-CoV刺突蛋白抗體預處理小鼠的肺,對來自該肺的MERS-CoVmRNA轉錄物(前導RNA)進行定量PCR測量所得結果的柱形圖。RNA使用針對MERS-CoV基因組的引物進行定量,並且與hIgG1同種型對照處理的小鼠進行比較。將所有樣品與設定為100%的hIgG1對照進行比較。圖11C是示出病毒感染前用抗MERS-CoV刺突蛋白抗體預處理的小鼠的肺中的病毒滴度的柱形圖。病毒滴度通過噬菌斑測定法進行定量並記錄為pfu/mL。圖12A是使用抗MERS-CoV刺突蛋白抗體(Ab2或Ab4)預處理的感染MERS-CoV的B6/hDPP4小鼠的肺的組織學圖像的分圖。小鼠肺的蘇木精和伊紅染色的切片顯示出來自各組的代表性小鼠的氣道、脈管系統和間質。圖12B是示出圖12A中所示的小鼠肺的組織學評分的柱形圖。所述分值是每個試驗組和時間點中所有小鼠的平均分值。圖13A是示出來自受感染的肺的MERS-CoV基因組(UpERNA)的定量PCR測量結果的柱形圖。比較病毒感染前一天或病毒感染後一天注射的抗MERS-CoV刺突蛋白抗體(Ab2或Ab4)的效果。圖13B是示出來自受感染的肺的MERS-CoVmRNA轉錄物(前導RNA)的定量PCR測量結果的柱形圖。比較病毒感染前一天或病毒感染後一天注射的抗MERS-CoV刺突蛋白抗體(Ab2或Ab4)的效果。對於圖13A至圖13B,RNA使用針對MERS-CoV基因組的引物進行定量,並且與hIgG1同種型對照處理的小鼠進行比較。將所有樣品與設定為100%的hIgG1對照進行比較。圖13C是示出病毒感染後用抗MERS-CoV刺突蛋白抗體(Ab2或Ab4)處理的小鼠的肺中的病毒滴度的柱形圖。病毒滴度通過噬菌斑測定進行定量並記錄為pfu/mL肺。比較病毒感染前一天或病毒感染後一天注射的抗體的效果。圖14A是感染後1天,使用抗MERS-CoV刺突蛋白Ab2抗體處理的感染MERS-CoV的B6/hDPP4小鼠的肺的組織學圖像的圖。小鼠肺的蘇木精和伊紅染色的切片顯示出來自各組的代表性小鼠的氣道、脈管系統和間質。圖14B是示出圖14A的小鼠肺的組織學評分的柱形圖。圖15示出在人源化DPP4小鼠中,重量隨用MERS-CoV感染後的時間變化的劑量響應研究。每組使用4-5隻小鼠。圖16示出在雜合和純合人源化DPP4小鼠中,重量隨用MERS-CoV(1×106pfu/小鼠;每組4-5隻小鼠)感染後的時間變化的劑量響應研究。圖17示出相對於經PBS處理的對照,在暴露於高劑量的病毒(1×106pfu/小鼠)的人源化DPP4小鼠中在第7天通過組織學檢查所看到的病變(炎症)。具體實施方式DPP4基因和蛋白DPP4基因編碼II型跨膜蛋白三肽基肽酶IV(DPP4)(也稱為CD26、腺苷脫氨酶複合蛋白-2(ADCP2)、腺苷脫氨酶結合蛋白(ADABP)和TP103),其具有絲氨酸外肽酶活性,並且在T細胞的激活以及在若干其他細胞類型中的細胞內信號傳導級聯中發揮重要作用。人DPP4.NCBI基因ID:1803;主要來源:HGNC:3009;RefSeq轉錄物:NM_001935.3;UniProtID:P27487;基因組裝配:GRCh38;位置:chr2:162,848,755-162,931,052-鏈。(參見圖6)。人DPP4基因位於染色體2,在2q24.3。人DPP4基因具有26個外顯子並編碼長度為766個胺基酸的II型跨膜多肽,包括N端6個胺基酸的胞質結構域、22個胺基酸的跨膜結構域和C端738個胺基酸的細胞外結構域。人DPP4蛋白的細胞外結構域(即,胞外域)由人DPP4基因的編碼外顯子3至26編碼。小鼠Dpp44.NCBI基因ID:13482;主要來源:MGI:94919;RefSeq轉錄物:NM_010074.3;UniProtID:P28843;基因組裝配:GRCh38;位置:chr2:62,330,073-62,412,591-鏈。小鼠DPP4基因位於染色體2,在235.85cM。小鼠Dpp4基因具有26個外顯子並編碼長度為760個胺基酸的II型跨膜多肽,包括N端6個胺基酸的胞質結構域、22個胺基酸的跨膜結構域和C端732個胺基酸的細胞外結構域。小鼠Dpp4蛋白的細胞外結構域(即,胞外域)由小鼠DPP4基因的編碼外顯子3至26編碼。DPP4蛋白的物種特異性如以下實例2中所述,人DPP4蛋白而不是小鼠DPP4蛋白是中東呼吸症候群冠狀病毒(MERS-CoV)感染的功能性受體。通常在非人動物如齧齒動物(例如小鼠或大鼠)中針對藥代動力學(PK)和藥效動力學(PD),對以物種特異性方式靶向人DPP4蛋白,或以物種特異性方式靶向分子(諸如與人DPP4蛋白相互作用的MERS-CoV)的候選治療性分子進行評價。還在其中DPP4發揮作用的人疾病、障礙和病症的非人動物如齧齒動物(例如小鼠或大鼠)模型中測試這種治療性分子的體內治療功效。然而,不能在齧齒動物(具體為小鼠)中適當地評價對人DPP4蛋白具有特異性的治療性分子(例如,人特異性DPP4抑制劑)的藥效動力學和/或體內治療功效,因為這些治療性分子的靶標缺失。而且,不能在齧齒動物(具體為小鼠)中適當地評價對與人DPP4蛋白特異性相互作用的靶標(例如,人DPP4特異性MERS-CoV)具有特異性的治療性分子的體內治療功效,因為這些治療性靶分子的靶標(例如,受體、相互作用配偶體)缺失。因此,在多個實施例中,為在非人動物如齧齒動物(例如小鼠或大鼠)中評估人特異性DPP4蛋白拮抗劑或抑制劑的藥效動力學和/或體內治療功效,需要用人DPP4蛋白或人源化DPP4蛋白置換內源Dpp4蛋白。在多個實施例中,為在非人動物如齧齒動物(例如小鼠或大鼠)中評估與人DPP4蛋白特異性相互作用的靶分子的小分子、肽或生物拮抗劑或抑制劑的體內治療功效,需要用人DPP4蛋白或人源化DPP4蛋白置換內源Dpp4蛋白。另外,在多個實施例中,為了避免其中內源Dpp4蛋白不正常表達的細胞和組織中人DPP4蛋白或人源化DPP4蛋白的過表達或低表達,和/或人DPP4蛋白或人源化DPP4蛋白的不適當表達的潛在問題,可取的是將人DPP4基因全部或部分插入非人動物如齧齒動物(例如小鼠或大鼠)的基因組的內源DPP4基因座,並且至少部分地在內源Dpp4調控元件的控制下在非人動物如齧齒動物(例如小鼠或大鼠)中表達人DPP4蛋白或人源化DPP4蛋白。在一些實施例中,可取的是用人DPP4基因或其片段靶向置換內源(例如,小鼠或大鼠)Dpp4基因。在其他實施例中,將人DPP4基因或其片段隨機插入齧齒動物(例如,小鼠或大鼠)基因組中而不是用人DPP4基因或其片段置換內源Dpp4基因。在一些實施例中,在其中人DPP4基因或其片段已隨機插入基因組的齧齒動物(例如小鼠或大鼠)中,內源齧齒動物Dpp4的表達得以保持。本文提供了在內源Dpp4基因座中或在一個或多個其他基因座中包含人DPP4基因或其片段(即,包含置換內源Dpp4基因座中或在一個或多個其他基因座的人DPP4基因或其片段)的非人動物如齧齒動物(例如小鼠或大鼠)。本文還提供了在內源Dpp4基因座中和在一個或多個另外的基因座二者中包含人DPP4基因或其片段(即包含置換內源Dpp4基因座和一個或多個另外的基因座的人DPP4基因或其片段)的非人動物如齧齒動物(例如小鼠或大鼠)。在一些實施例中,人DPP4基因的片段含有200千鹼基(kb)或更少的核苷酸,例如180kb、160kb、140kb、120kb、100kb、80kb、70kb、60kb、50kb、40kb、30kb、20kb、10kb、5kb、2.5kb、1kb或更少的核苷酸,例如,1000個、800個、600個、400個、200個或更少的核苷酸。具有人DPP4的細胞和非人動物的產生為了用人DPP4基因或片段靶向置換內源非人Dpp4基因或片段,生成了靶向構建體。參見,例如Valenzuelaetal.NatureBiotech,21.6(2003):652-659(Valenzuela等人,《自然生物技術》,第21卷,第6期,2003年,第652-659頁)、US6,586,251和US8,759,105。例如,靶向構建體包含側接置換用人DPP4基因或其片段的同源臂。在一些實施例中,該置換用人DPP4基因或其片段包含整個人DPP4基因。在其他實施例中,該置換用人DPP4基因或其片段包含人DPP4基因的一部分。例如,該置換用人DPP4基因或其片段包含人DPP4基因的一個或多個外顯子,例如人DPP4基因的1個、2個、3個、4個、5個、6個、7個、8個、9個、10個、11個、12個、13個、14個、15個、16個、17個、18個、19個、20個、21個、22個、23個、24個、25個或26個外顯子。例如,該置換用人DPP4基因或其片段包含人DPP4基因的外顯子1至26。在其他實施例中,該置換用人DPP4基因或其片段包含人DPP4基因的外顯子2至26。例如,該置換用人DPP4基因或其片段包含人DPP4基因的外顯子2上遊的內含子1至外顯子26。在一些實施例中,該置換用人DPP4基因或其片段還包含人調控元件,例如人DPP4基因下遊的人3』非翻譯區(UTR)的一部分,例如下遊區的至少1kb(例如,至少1Kb、2Kb、3Kb、4Kb、5Kb、10Kb、20Kb、30Kb、40Kb或更多),和/或人DPP4基因上遊的人啟動子或增強子區,例如上遊區的至少10kb(例如,至少10Kb、20kb、30kb、40kb、50kb或更多)。同源臂是與側接所需的遺傳修飾/置換,例如側接待置換的內源Dpp4基因或片段的內源染色體核酸序列同源的序列。同源核酸序列可以是兩個或更多個核酸序列,所述核酸序列或相同或足夠相似以便它們能夠彼此雜交或進行分子間交換。由於同源臂與相應的內源序列之間的同源性,同源臂使得靶向構建體指向基因組內的特定染色體位置,例如內源Dpp4基因座。參見,例如Valenzuelaetal.NatureBiotech,21.6(2003):652-659(Valenzuela等人,《自然生物技術》,第21卷,第6期,2003年,第652-659頁)、US6,586,251和US8,759,105。任選地,靶向構建體還包含,例如在兩個同源臂之間的選擇標記。示例性的選擇標記包括抗生素抗性標記(例如,新黴素或卡那黴素)和螢光蛋白。在一些實施例中,選擇標記被敲入(floxed),即側接在兩個loxP位點之間。可通過添加Cre重組酶移除敲入的選擇標記,所述Cre重組酶催化敲入區段(例如包括選擇標記)的切除。載體/構建體可通過使用各種載體和/或構建體產生本發明的轉基因非人動物(如齧齒動物,例如小鼠或大鼠)。在一些實施例中,靶向構建體是一段環狀雙鏈DNA,例如細菌人工染色體(BAC)、質粒或源自P1的人工染色體(PAC)的形式。為產生內源Dpp4基因座被靶向置換的非人細胞,將含有本文所述的人DPP4基因或片段的靶向構建體引入到非人(如齧齒動物,例如小鼠或大鼠)細胞,例如胚胎幹(ES)細胞。為產生包含隨機插入到基因組中的人DPP4基因或片段的非人細胞,將包含人DPP4基因或其片段的環狀DNA構建體(例如BAC)引入進非人(如齧齒動物,例如小鼠或大鼠)細胞,例如ES細胞中。在一些情況下,環狀DNA構建體(例如BAC)還含有人DPP4調控元件,例如人DPP4基因的上遊和/或下遊的人啟動子或增強子區。例如,環狀DNA構建體含有人DPP4基因的ATG起始密碼子上遊的啟動子/增強子區的至少10kb(例如,至少10kb、20kb、30kb、40kb、50kb或更多)。此外或作為另外一種選擇,環狀DNA構建體含有人DPP4基因下遊的非翻譯區的至少1kb(例如,至少1kb、2kb、3kb、4kb、5kb、10kb、20kb、30kb、40kb或更多)。例如,人DPP4基因或片段有效連接至人DPP4調控元件。在一些實施例中,環狀DNA構建體(例如BAC)中的人DPP4基因或其片段包含整個人DPP4基因。在其他實施例中,人DPP4基因或其片段包含人DPP4基因的一部分。例如,人DPP4基因或其片段包含人DPP4基因的一個或多個外顯子,例如人DPP4基因的1個、2個、3個、4個、5個、6個、7個、8個、9個、10個、11個、12個、13個、14個、15個、16個、17個、18個、19個、20個、21個、22個、23個、24個、25個或26個外顯子。例如,人DPP4基因或其片段包含人DPP4基因的外顯子1至26。在其他實施例中,人DPP4基因或其片段包含人DPP4基因的外顯子2至26。例如,人DPP4基因或其片段包含人DPP4基因的外顯子2上遊的內含子1至外顯子26。例如,通過電穿孔或脂質介導的轉染完成引入進細胞的步驟。任選地,在引入進細胞中之前,使環狀DNA構建體(例如BAC)線性化。例如,用稀切限制酶(例如SgrDI、SfiI、NotI、PacI或Swal)進行線性化。在靶向構建體包含抗生素選擇標記(例如新黴素)的情況下,任選在含有新黴素/G418的培養基中選擇已吸收靶向構建體的細胞。選擇在含有新黴素/G418的培養基中存活和/或增殖的細胞,該細胞對於靶向構建體呈陽性。在一些實施例中,針對已將人DPP4基因或其片段併入到它們的基因組中(例如隨機插入到基因組中或(例如,通過靶向構建體)靶向至內源Dpp4基因座)的那些細胞對細胞群進行篩選。用於篩選的方法包括定量PCR和螢光原位雜交。參見,例如US6,586,251B2和US8,759,105B2。例如,篩選的方法包括檢測人DPP4基因或片段的存在。在一些實施例中,篩選的方法包括檢測內源Dpp4基因或片段拷貝數的丟失和/或人DPP4基因或片段的拷貝數的獲得。用於篩選的示例性方法描述於實例1和3中。在其中靶向構建體包含敲入的選擇標記的一些實施例中,任選還用Cre-表達載體(例如瞬時表達Cre重組酶)電穿孔被正確靶向的細胞,以移除敲入的選擇標記。為產生轉基因動物,將含有人DPP4基因或其片段的陽性ES細胞克隆(例如不帶有敲入的選擇標記)引入到齧齒動物胚胎中,例如小鼠或大鼠胚胎,諸如8-細胞期小鼠胚胎。例如通過囊胚注射技術、聚集技術、核移植和克隆和/或方法完成該引入步驟。參見,例如US8,759,105B2、US7,294,754、US7,576,259和US7,659,442。例如,ES細胞克隆是對ES細胞群體引入DNA並進行後續選擇之後,從其單個細胞衍生得到的細胞亞群。在一些情況下,對來自轉基因非人動物的DNA以如上所述的相似方式進行篩選以確認人DPP4基因/片段通過種系的遺傳性(transmittance)。在一些實施例中,本文所述的人源化DPP4齧齒動物對人DPP4等位基因是雜合的。正因為如此,這些齧齒動物具有一個人DPP4等位基因和一個野生型齧齒動物DPP4等位基因。在其他實施例中,人源化DPP4齧齒動物對人DPP4等位基因是純合的。人源化DPP4齧齒動物的用途人源化DPP4齧齒動物(例如小鼠或大鼠)可用於評價用於治療高血糖症的人特異性DPP4拮抗劑(例如小分子抑制劑、肽抑制劑或生物抑制劑)的藥效動力學(PD)。可根據本領域已知的標準程序在人源化DPP4齧齒動物(例如小鼠或大鼠)中進行藥代動力學(PK)和PD測定。人源化DPP4齧齒動物(例如小鼠或大鼠)可用於評價人特異性DPP4拮抗劑(例如小分子抑制劑、肽抑制劑或生物抑制劑)在治療高血糖症方面的體內治療功效。人源化DPP4齧齒動物(例如小鼠或大鼠)可用於測試在MERS-CoV感染的治療或預防(或防治)中對與人DPP4特異性相互作用的靶分子如MERS-CoV(例如MERS-CoV的刺突蛋白(S),例如MERS-CoV的刺突蛋白的受體結合結構域)具有特異性的拮抗劑(例如小分子抑制劑、肽抑制劑或生物抑制劑,例如中和抗體)的治療功效。在一些實施例中,對於人DPP4等位基因是雜合的齧齒動物用於測試一種或多種拮抗劑在MERS-CoV感染的治療或預防(或防治)中的體內治療功效。在其他實施例中,對於人DPP4等位基因是純合的DPP4齧齒動物用於測試一種或多種拮抗劑在MERS-CoV感染的治療或預防(或防治)中的體內治療功效。示例性MERS-CoV毒株包括MERS-CoVJordan毒株(GenBank登錄號KC776174.1,MERS-CoV-Hu/Jordan-N3/2012)和MERS-CoVEMC/2012毒株(GenBank登錄號JX869059.2)。在一些實施例中,本文所述的MERS-CoV病毒包含MERS-CoV臨床分離株。在其他實施例中,本文所述的MERS-CoV病毒包含與本文所述的臨床分離株具有相同刺突蛋白受體結合結構域(RBD)序列的毒株。示例性臨床分離株在下表中示出。該表示出了在若干MERS-CoV臨床分離株的刺突蛋白的受體結合結構域(RBD)中的胺基酸序列變異。對美國國家生物技術信息中心(NCBI)保藏的MERS-CoV臨床分離株序列在第367-606位胺基酸處進行比對,並且與EMC/2012毒株的該序列進行比較。帶有A431P、S457G、S460F、A482V、L506F、D509G和V534A置換(其中數字之前的胺基酸(單字母名稱)是EMC/2012毒株的胺基酸,並且數字之後的胺基酸(單字母名稱)是臨床分離株的胺基酸)的臨床分離株在表中示出。表I在一些實施例中,在齧齒動物MERS-CoV感染前(例如,至少1小時、2小時、4小時、6小時、12小時、24小時、48小時、2天、3天、4天、5天、6天、7天或更早以前)施用拮抗劑。在其他實施例中,在齧齒動物MERS-CoV感染後(例如至少1小時、2小時、4小時、6小時、12小時、24小時、48小時、2天、3天、4天、5天、6天、7天或更久以後)施用拮抗劑。在一些實施例中,其中在MERS-CoV感染後給齧齒動物施用拮抗劑,施用拮抗劑後齧齒動物中相較於對照水平的較低病毒滴度或RNA水平(例如病毒UpE或前導序列RNA水平),例如降低至少5倍(例如至少5倍、10倍、50倍、100倍、500倍、1000倍、104倍、105倍、106倍、107倍或更多倍),表明拮抗劑可有效用於治療MERS-CoV感染。例如,對照水平是在施用拮抗劑前齧齒動物中的病毒滴度或RNA水平。在其他例子中,對照水平是未用拮抗劑處理的受病毒感染齧齒動物中的病毒滴度或RNA水平。在一些實施例中,其中在MERS-CoV感染之前給齧齒動物施用拮抗劑,施用拮抗劑後齧齒動物中相較於對照水平的較低病毒滴度或RNA水平(例如病毒UpE或前導序列RNA水平),例如降低至少5倍(例如至少5倍、10倍、50倍、100倍、500倍、1000倍、104倍、105倍、106倍、107倍或更多倍),表明拮抗劑可有效用於預防MERS-CoV感染。例如,對照水平是未用拮抗劑處理的受MERS-CoV感染齧齒動物中的病毒滴度或RNA水平。在一些實施例中,可通過在含有苯酚的溶液,例如含有苯酚和異硫氰酸胍的溶液(例如(生命技術公司(LifeTechnologies,Inc)))中均質化,通過從齧齒動物肺中提取RNA來確定齧齒動物肺中的病毒RNA水平。例如,可按照製造商使用說明使用Magnalyzer(羅氏公司(Roche))將肺均質化。在一些實施例中,可使用定量PCR(qPCR)評估MERS-CoVRNA的水平,所述qPCR使用靶向MERS-CoV基因組的引物和/或靶向MERS-CoVmRNA轉錄物的引物。例如,快速病毒一步母液混合液(Fastvirusone-stepmastermix)(美國應用生物系統公司(AppliedBiosystems))可按照製造商使用說明通過使用獲自生命技術公司的引物的雙鏈體而用於qPCR中,所述引物雙鏈體靶向包膜基因上遊基因組區(UpE)或核殼信使RNA的前導序列(前導引物),並與內源對照諸如齧齒動物(例如大鼠)18SrRNA相比較。例如,可在7500DX快速實時定量PCR儀(7500fastDXreal-timePCRinstrument)(美國應用生物系統公司(AppliedBiosystems))上讀取快速光學反應板(fastopticalreactionplate)(美國應用生物系統公司)中的qPCR反應。在一些例子中,可使用ΔCt方法分析qPCR數據,其中未感染對照設定為1。例如,在拮抗劑是抗MERS-CoV的抗體的情況下,可相對於用對照拮抗劑(例如同種型匹配的對照抗體)處理的受感染小鼠中的RNA檢測水平表示檢測到的MERS-CoVRNA百分比。在一些實施例中,齧齒動物肺中的病毒滴度可通過這樣來測定:將齧齒動物肺在緩衝液(例如磷酸鹽緩衝鹽水(PBS))中均質化,離心(例如以10,000rpm)。可通過在哺乳動物細胞諸如Vero細胞(例如VeroE6細胞)上進行噬菌斑測定來分析上清液,從而定量在用拮抗劑處理後殘留的病毒水平。可使用標準的噬菌斑測定法,例如在Pageetal.(2012)Inductionofalternativelyactivatedmacrophagesenhancespathogenesisduringsevereacuterespiratorysyndromecoronavirusinfection,JVirol86:13334–13349(Page等人,2012年,「嚴重急性呼吸症候群冠狀病毒感染過程中誘導替代性活化巨噬細胞可增強發病」,《病毒學雜誌》,第86卷,第13334–13349頁)中描述的噬菌斑測定。在一些例子中,可通過靜置板3天等待噬菌斑出現的方式改進Page等人所述的噬菌斑測定法。在一些實施例中,與對照肺樣本相比,在MERS-CoV感染之前或之後用拮抗劑處理的齧齒動物的肺樣品中有較少炎症(例如間質炎症或血管周圍炎症)、較少炎性細胞和/或較少細支氣管呈袖套徵(例如通過組織學分析確定的),可表明拮抗劑對治療或預防MERS-CoV感染有效。例如,對照肺樣品可來自未經拮抗劑處理的(例如感染之前和/或之後未處理的)受MERS-CoV感染的齧齒動物。本文所述的齧齒動物可用於有效測試針對MERS-CoV的藥物和疫苗,例如用以在人體臨床試驗前證明安全性和功效。它們使得能例如在測試的數周內快速鑑定和/或驗證治療劑/預防劑。定義同源胺基酸殘基是共有相似特徵或特性的殘基。胺基酸殘基的特徵或特性基於例如多肽主鏈的結構(例如,片層或螺旋構型)、殘基的電荷或疏水性和/或側鏈的體積。例如,同源殘基在側鏈特性(例如,極性、電荷、大小、芳香性和/或疏水性)方面相似。術語「約」指設定值加上或減去另一量;從而確立值的範圍。在某些實施例中,「約」指相對於基準(或核心或參照)值或量加上或減去最多15%、14%、13%、12%、11%、10%、9%、8%、7%、6%、5%、4%、3%、2%、1%,0.75%、0.5%、0.25%或0.1%的範圍。例如,約指所引用數字,例如核苷酸鹼基的數量之下和之上+/-5%的範圍。如本文所用,術語「有效連接」指所述的組分(例如核苷酸序列)的位置處於允許其以其預期方式發揮作用的關係。如本文所用,術語「蛋白質」包括多肽、肽、多肽的片段和融合多肽。如本文所用,「核酸」指兩個或多個脫氧核糖核苷酸和/或核糖核苷酸以單鏈或雙鏈的形式共價連接在一起。關於基因置換的術語「置換」指將外源遺傳物質置於內源基因座處,從而用直系同源或同源核酸序列置換內源基因的全部或一部分。在一個實例中,用相應的人基因或其片段置換內源非人基因或其片段。相應的人基因或其片段是作為被置換的內源非人基因或其片段的直系同源物或同系物,或在結構和/或功能上與被置換的內源非人基因或其片段基本上同一或相同的人基因或片段。如本文所用,術語「齧齒動物」指齧齒目的任何成員。齧齒動物的例子包括但不限於,小鼠、大鼠、松鼠、草原犬鼠、豪豬、海狸、豚鼠和倉鼠。在一個實施例中,齧齒動物是大鼠。在另一個實施例中,齧齒動物是小鼠。除非本文另有定義,否則本文使用的所有技術和科學術語的含義與本發明所屬領域的普通技術人員通常所理解的含義相同。如本文所用,單數術語「一個」、「一種」和「該」包括複數指代,除非上下文另有明確說明。預期在本說明書中通篇給出的每個上限值包括每個下限值,如同這種下限值在本文明確地寫出一樣。在本說明書中通篇給出的每個下限值將包括每個上限值,如同這種上限值在本文明確地寫出一樣。在本說明書中通篇給出的每個數值範圍將包括屬於該較寬的數值範圍內的每個較窄的數值範圍,如同這種較窄的數值範圍在本文明確地寫出一樣。以下實例僅出於說明的目的提供,而不旨在以任何方式限制本發明。實例實例1用人DPP4基因置換內源小鼠Dpp4基因用81.8kb人DPP4基因(含有人DPP4基因的外顯子2至外顯子26以及3』非翻譯區的一部分)置換78.8kb小鼠DPP4基因座,該小鼠基因座跨越外顯子2至外顯子26中的終止密碼子。參見圖1A和1B。使用基因工程技術構建在單個靶向步驟中用人DPP4基因置換小鼠基因的靶向構建體(參見Valenzuelaetal.(2003)High-throughputengineeringofthemousegenomecoupledwithhigh-resolutionexpressionanalysis,NatureBiotech,21(6):652-659(Valenzuela等人,2003年,「結合高解析度表達分析對小鼠基因組進行高通量工程改造」,《自然生物技術》,第21卷,第6期,第652-659頁))。小鼠和人DPP4DNA分別獲自細菌人工染色體(BAC)克隆RP23-362N15和RP11-68L22。簡而言之,將通過缺口修復克隆和floxedneo選擇盒產生的SgrDI線性化靶向構建體電轉化到VGB6小鼠胚胎幹(ES)細胞(來源於C57BL/6N小鼠)中,其中該缺口修復克隆含有與82kb人DPP4序列側接的小鼠Dpp4上遊同源臂和下遊同源臂,該82kb人DPP4序列從外顯子2上遊的內含子1延伸至外顯子26,包括終止密碼子和3』非翻譯區的一部分(整個人DPP4基因的基因組坐標:GRCh38:chr2:162,848,755-162,931,052(-鏈))。用瞬時Cre表達載體進一步電轉化正確靶向的ES細胞(MAID7326),以去除藥物選擇盒。利用法將不含藥物盒的被靶向ES細胞(MAID7327)克隆引入8細胞期SW小鼠胚胎中(參見美國專利No.7,294,754、No.7,576,259、No.7,659,442以及Poueymirouetal.(2007)F0generationmicethatareessentiallyfullyderivedfromthedonorgene-targetedEScellsallowingimmediatephenotypicanalysesNatureBiotech.25(1):91-99(Poueymirou等人,2007年,「基本上完全衍生自基因靶向的供體ES細胞的F0代小鼠可用於直接的表型分析」,《自然生物技術》,第25卷,第1期,第91-99頁))。利用等位基因修飾測定法對小鼠等位基因的丟失和人等位基因的獲得進行基因型分析,從而鑑定攜帶人源化DPP4基因的(完全衍生自供體ES細胞的F0代小鼠)(參見Valenzuela等人,2003年)。利用天然等位基因損失(loss-of-native-allele,LONA)測定法來鑑定正確靶向的ES細胞克隆(Valenzuela等人2003年),其中通過兩個TaqManTM定量聚合酶鏈反應(qPCR)來確定未經修飾的天然Dpp4基因的拷貝數,該聚合酶鏈反應對作為缺失靶標的小鼠Dpp4基因是特異性的。qPCR測定法包括以下引物-探針組(書寫順序為5』至3』):上遊正向引物TCGCCACTGTGCCTAACATAG(SEQIDNO:1);上遊反向引物CCGGGACTAAACTGGAACATTC(SEQIDNO:2);上遊探針FAM-TCAGTCAACTTCTTCTGGGTTGTTTCC-BHQ(SEQIDNO:3);下遊正向引物CAGCTCTGGTGGAGAACTAGAC(SEQIDNO:4):下遊反向引物GGAGGTCCTCGGTCTTTAGAAG(SEQIDNO:5);下遊探針FAM-TCACACTTAGGCTTATAAACCATTCCCGT-BHQ(SEQIDNO:6);其中FAM是指5-羧基螢光素螢光探針,BHQ是指黑洞猝滅劑型的螢光猝滅劑(生物搜索技術公司(BiosearchTechnologies))。從已吸收靶向載體且併入ES細胞克隆基因組的ES細胞克隆中純化DNA,按照製造商建議將該純化的DNA在384孔PCR板(美國生命技術公司的MicroAmpTM384孔光學反應板(MicroAmpTMOptical384-WellReactionPlate))中與TaqManTM基因表達母混合液(TaqManTMGeneExpressionMasterMix,美國生命技術公司)混合,然後使所得溶液在AppliedBiosystemsPrism7900HT中循環,AppliedBiosystemsPrism7900HT在PCR過程中收集螢光數據,並確定閾值循環(Ct)以及累積螢光達到預設閾值的PCR循環分數。每個DNA樣品都運行以下反應:上遊DPP4-特異性qPCR和下遊DPP4-特異性qPCR,以及非靶向參照基因的兩個qPCR。計算每個DPP4-特異性qPCR和每個參照基因qPCR之間的Ct值差值(ΔCt),然後計算所有測定樣品的每個ΔCt與中值ΔCt之間的差值,從而得到每個樣品的ΔΔCt值。每個樣品中的DPP4基因拷貝數通過以下公式計算:拷貝數=2×2-ΔΔCt。丟失一個天然拷貝的正確靶向克隆的Dpp4基因拷貝數等於1。通過TaqManTMqPCR測定法確認了人DPP4基因序列在人源化等位基因中置換了缺失的小鼠Dpp4基因序列,其中TaqManTMqPCR測定法包括以下引物-探針組(書寫序為5』至3』):人上遊正向引物GCGGTCTCCCTCTTCTAACG(SEQIDNO:7);人上遊反向引物GCAAGCCGAGCAGATCAAG(SEQIDNO:8);人上遊探針FAM-ACTCCCACCTGCAAATCCTGCTGC-BHQ(SEQIDNO:9);人下遊正向引物AACCGCACTGGCATATGGA(SEQIDNO:10);人下遊反向引物TACAAGGTAGTCTGGGATTACTAACAAAA(SEQIDNO:11);人下遊探針FAM-ACATTTATCTAGAAAGGCTC-BHQ(SEQIDNO:12)。將相同的LONA測定法用於測定從源於被靶向ES細胞的小鼠的尾部活檢組織中純化DNA,以確定小鼠的DPP4基因型並確認人源化DPP4等位基因已通過種系傳遞。將對於所述置換是雜合的兩隻小鼠進行繁育而產生對於用人DPP4基因置換內源小鼠Dpp4基因是純合的小鼠。將對於所述置換是純合的小鼠用於表型分析。小鼠Dpp4基因座與含有人DPP4基因的序列的上遊結合點被設計在5』-AGGAGAGAAGCCAACAAGATCATAAGATCATGCTCAGGGCCAAAATTCAAGGGCTTCTGC(CGTCGACG)(SEQIDNO:13)內,其中人DPP4序列為斜體,SgrDI限制性酶切位點帶括號。含有人DPP4基因的序列與floxedneo選擇盒的下遊結合點被設計在5』-ctcgag(ataacttcgtataatgtatgctatacgaagttat)atgcatggcctccgcgccgggttttggcgcctcccgcggg(SEQIDNO:14)內,其中人DPP4序列為斜體,neo盒序列為小寫,loxP位點帶括號。floxedneo選擇盒的序列與小鼠Dpp4基因座的下遊結合點被設計在5』-atgtctgga(ataacttcgtataatgtatgctatacgaagttat)gctagtaactataacggtcctaaggtagcgagctagcCAGCATAGCTCTCCATAGCTTATTTAAGACCACATTTGTTCTCATTATCTCAAAAGTGCACTGTTAAGATGAAGATCTTA(SEQIDNO:15)內,其中neo盒序列為小寫,loxP位點帶括號。移除neo選擇盒之後,含有人DPP4基因的序列、移除neo選擇盒之後剩下的loxP位點以及小鼠Dpp4基因座的結合點被設計在5』-ctcgag(ataacttcgtataatgtatgctatacgaagttat)gctagtaactataacggtcctaaggtagcgagctagcCAGCATAGCTCTCCATAGCTTATTTAAGACCACATTTGTTCTCATTATCTCAAAAGTGCACTGTTAAGATGAAGATCTTAATAATGTTGCATTGAGACATTTCAGGCTGCTTTCTCCAGTTTTACACCTGCAATCCTAACTAAGGATGCCTGTCCCCAGAAC(SEQIDNO:16)內,其中人DPP4序列為斜體,neo盒序列為小寫,loxP位點帶括號。圖2示出了MAID7326/7327中由人源化DPP4核酸序列編碼的DPP4的胺基酸序列(SEQIDNO:17)與人DPP4相同,因為小鼠Dpp4密碼子1僅僅編碼DPP4的前兩個胺基酸Met和Lys,這兩個胺基酸與由人DPP4密碼子1編碼的胺基酸相同。實例2用MERS-CoV感染人源化DPP4小鼠中東呼吸症候群冠狀病毒(MERS-CoV)是引發嚴重急性呼吸疾病的新型病毒。MERS-CoV的受體是二肽基肽酶IV(DPP4)(參見Rajetal.(2013)DipeptidylPeptidase4isaFunctionalReceptorfortheEmergingHumanCoronavirus-EMC,Natuere495(7440):251-254(Raj等人,2013年,「二肽基肽酶4是新興人類冠狀病毒EMC的受體」,《自然》,第495卷,第7440期,第251-254頁))。體內測試抗病毒分子需要易受MERS-CoV感染的動物模型,例如小動物模型,諸如齧齒動物(如小鼠或大鼠)。然而,最近的研究表明,小鼠Dpp4不支持MERS-CoV感染(參見例如Cockrelletal.(2014)MouseDipeptidylPeptidaseisNotaFunctionalReceptorforMiddleEastRespiratorySyndromeCoronavirus(MERS-CoV)Infection,J.Virol.88(9):5195-5199(Cockrell等人,2014年,「小鼠二肽基肽酶不是中東呼吸症候群冠狀病毒(MERS-CoV)感染的功能性受體」,《病毒學雜誌》,第88卷,第9期,第5195-5199頁);Colemanetal.(2014)Wild-TypeandInnateImmune-DeficientMiceareNotSusceptibletotheMiddleEastRespiratorySyndromeCoronavirus,J.Gen.Virol.95(2):408-412)(Coleman等人,「野生型和先天免疫缺陷小鼠不易受中東呼吸症候群冠狀病毒感染」,《普通病毒學雜誌》,第95卷,第2期,第408-412頁)),至少部分原因是MERS-CoV刺突蛋白與人DPP4而非小鼠DPP4相互作用(參見例如Coleman等人,2013年和Raj等人,2013年)。將小鼠DPP4序列和人DPP4序列進行序列比較,發現先前已被鑑定為MERS-CoV刺突(S)蛋白與其受體之間的接觸位點的胺基酸在兩個物種之間存在差異。此外,在小鼠細胞中表達人DPP4允許MERS-CoV病毒進入和增殖,從而意味著病毒進入是感染小鼠細胞的限制步驟,並且小鼠DPP4與MERS-CoV糖蛋白之間相互作用的缺乏限定了體外物種向性。參見例如Luetal.(2013)MolecularbasisofbindingbetweennovelhumancoronavirusMERS-CoVanditsreceptorCD26,Nature.500(7461):227-31(Lu等人,2013年,「新型人類冠狀病毒MERS-CoV及其受體CD26之間結合的分子基礎」,《自然》,第500卷,第7461期,第227-231頁);Cockrelletal.(2014)MouseDipeptidylPeptidaseisNotaFunctionalReceptorforMiddleEastRespiratorySyndromeCoronavirus(MERS-CoV)Infection,J.Virol.88(9):5195-5199(Cockrell等人,2014年,「小鼠二肽基肽酶不是中東呼吸症候群冠狀病毒(MERS-CoV)感染的功能性受體」,第88卷,第9期,第5195-5199頁)。因此,正常小鼠品系不能用於測量靶向MERS-CoV的治療劑的功效。Zhaoetal.(2014)RapidGenerationofaMouseModelforMiddleEastRespiratorySyndrome,Proc.Natl.Acad.Sci.USA111(13):4970-4975(Zhao等人,2014年,「用於中東呼吸症候群的模型的快速產生」,第111卷,第13期,第4970-4975頁)已通過腺病毒轉導在小鼠中表達了人DPP4,從而可感染MERS-CoV。然而,這種腺病毒模型存在若干局限性,包括:(a)該病毒被快速從感染的小鼠中清除;(b)隨時間推移人DPP4表達丟失;(c)病毒轉導的DPP4的組織分布不能反映在小鼠或人中所觀察到的表達;(d)腺病毒感染可誘導幹擾素響應。為了產生用於MERS-CoV感染的小鼠模型,按照上述實例1的方法產生人源化DPP4小鼠。如圖1B所示,用人DPP4的對應序列置換小鼠Dpp4的外顯子2至外顯子26。由於剩下的小鼠Dpp4編碼外顯子1僅僅編碼與對應人DPP4外顯子1中的胺基酸相同的Dpp4的前兩個胺基酸Met和Lys,因此在人源化DPP4小鼠中表達的DPP4蛋白完全是人DPP4蛋白(參見圖2,SEQIDNO:17)。因此,人源化DPP4小鼠在內源小鼠調控序列(即,5』側翼區(啟動子和增強子)和3』非翻譯區序列)的控制下表達完整的人DPP4。可以預計,與小鼠Dpp4在缺乏人DPP4核酸序列的野生型小鼠中的表達一樣,人源化DPP4在相同細胞和組織中以相同或相似水平表達。通過鼻內方式感染兩組F0代人源化DPP4小鼠:一組用MERS-CoV(Jordan毒株)處理,一組用PBS模擬處理。感染後4天,使用複製型MERS-CoV基因組的特異引物,通過實時PCR對肺中的MERS-CoVRNA進行定量。將數據歸一化至從模擬感染的小鼠的肺獲得的PCR產物的量(任意地設為1)。圖3顯示,可從MERS-CoV感染的人源化DPP4小鼠的肺中擴增MERS-CoVRNA。還對來自模擬感染和MERS-CoV感染的小鼠的肺組織進行H&E染色。圖4顯示,人源化DPP4小鼠的MERS-CoV感染不影響氣道,但是導致肺泡壁增厚並且肺泡細胞間的間隙縮小,這表明肺中產生了與MERS-CoV感染相關的炎症。此外,通過鼻內方式用MERS-CoV(例如,2×105pfu的MERS-CoV(Jordan))接種6至8周齡的小鼠。一直到接種後4天未觀察到疾病死亡或疾病臨床徵象。接種後第2天和第4天,對小鼠實施安樂死,並對小鼠的肺進行解剖。為了獲得病毒RNA水平,將肺在中均質化,提取RNA,並使用MERS-CoV特異引物,通過實時PCRMERS-CoV分析(圖10A和10B)。一組引物對包膜基因上遊病毒基因組區(UpE)是特異的,另一組引物對核殼mRNA的前導序列是特異的(前導引物)。用小鼠18SrRNA作為內源對照。為了獲得病毒滴度,將肺在磷酸鹽緩衝液(PBS)中均質化,通過離心使其澄清,然後在VeroE6細胞上滴定(圖10C)。例如,通過噬菌斑測定法在VeroE6細胞上分析上清液,以定量肺中存在的病毒水平。例如,按照Pageetal.(2012)Inductionofalternativelyactivatedmacrophagesenhancespathogenesisduringsevereacuterespiratorysyndromecoronavirusinfection,JVirol86:13334–13349(Page等人,2012年,「嚴重急性呼吸症候群冠狀病毒感染過程中誘導替代性活化巨噬細胞可增強發病」,《病毒學雜誌》,第86卷,第13334-13349頁)中所述進行噬菌斑測定法,其中將板靜置3天以待噬菌斑出現。在感染後第2天和第4天,肺中明顯出現穩健的MERS-CoV複製。使用MERS-CoV前導序列特異性引物組(被設計成僅擴增複製MERS-CoV)進行RNA定量,結果表明在感染後第2天收集的肺中具有高水平的MERS-CoV複製RNA,並且該水平維持到感染後第4天(圖10A至圖10B)。在VeroE6細胞上進行的肺勻漿物噬菌斑測定法將MERS-CoV(Jordan)水平定量為感染後第2天為約7.27×104pfu/mL肺,感染後第4天為約3.75×105pfu/mL肺(圖10C),這說明感染的人源化DPP4小鼠的肺中存在活躍的MERS-CoV複製。此外,針對病理變化,對通過鼻內方式接種MERS-CoV(Jordan毒株)或PBS(模擬感染)的人源化DPP4小鼠的肺進行了分析(圖10D)。在感染後第2天,發現整個肺中細支氣管細胞結構產生變化,細支氣管周圍炎症明顯。此時,觀察到極少的血管周圍炎症或對肺泡結構的影響。在感染後第4天,觀察到間質浸潤現象,伴隨血管周圍呈袖套徵並且大量肺泡增厚。此外,細支氣管也發生變化。參見圖10D。這種病理現象與MERS-CoV感染的人中所見的間質性肺炎和明顯肺部疾病的放射影像一致。以上數據表明,人源化DPP4小鼠(諸如本文所述的那些小鼠)易受MERS-CoV感染。這些數據還證明,本文所述的人源化DPP4小鼠是MERS-CoV感染的體內模型,其可重演在人的MERS-CoV感染中可觀察到的病理現象(例如,病理後遺症)。因此,人源化DPP4小鼠是可用於評估體內MERS-CoV治療的MERS-CoV可靠模型。例如,人源化DPP4小鼠是用於測量靶向MERS-CoV的治療性分子的藥代動力學、藥效動力學和治療功效的合適宿主動物。圖5示出了小鼠Dpp4(SEQIDNO:25)與人DPP4(由7326/7327轉基因小鼠編碼)(SEQIDNO:26)的蛋白序列比對結果。接下來,在人源化DPP4小鼠中進行了體重隨用MERS-CoV感染後的時間變化的劑量響應研究。如上所述用MERS-CoV(Jordan毒株)或PBS(模擬感染)感染小鼠,並在7天周期內分析體重減輕情況,體重減輕是有效感染的徵象。如圖14所示,人源化DPP4小鼠表現出有效感染(即顯現疾病病理現象),感染後第4天開始出現體重減輕。每組使用4至5隻小鼠。圖15顯示,人源化DPP4等位基因雜合的小鼠同樣易受MERS-CoV感染,因為與純合體比較時這些小鼠表現出相似程度的體重減輕。這一結果非常重要,其表明可使用雜合小鼠進行研究。另外,使用雜合小鼠可避免與功能性小鼠Dpp4敲除有關的任何潛在問題,這些問題可能潛在地存在於純合人源化DPP4小鼠中。還根據上述方法針對炎症對這些小鼠的肺進行組織學檢查。如圖16所示,暴露於高劑量病毒(每隻小鼠1×106pfu)的hDPP4小鼠表現出比PBS對照更強的病理現象。實例3通過隨機插入BAC產生含有人DPP4基因的轉基因小鼠產生含有人DPP4基因的轉基因小鼠,該基因序列和基因組信息在圖6中示出。使用含有人DPP4基因的兩個不同重疊BAC:BACRP11-68L22和BACRP11-345J9(圖7)。這兩個BAC都含有人DPP4基因的編碼區,以及DPP4基因的ATG起始密碼子上遊超過40kb的啟動子區和DPP4基因的終止密碼子下遊的幾千鹼基(圖7)。為了產生BAC轉基因小鼠,將每個BACDNA電轉化到VGB6小鼠胚胎幹(ES)細胞(來源於C57BL/6N小鼠)中。通過法用SW小鼠胚胎將含有人DPP4基因的編碼區以及該基因的啟動子區的ES細胞引入8細胞期SW小鼠胚胎中(參見例如美國專利No.7,294,754、No.7,576,259、No.7,659,442以及Poueymirouetal.(2007)F0generationmicethatareessentiallyfullyderivedfromthedonorgene-targetedEScellsallowingimmediatephenotypicanalysesNatureBiotech.25(1):91-99(Poueymirou等人,2007年,「基本上完全衍生自基因靶向的供體ES細胞的F0代小鼠可用於直接的表型分析」,《自然生物技術》,第25卷,第1期,第91-99頁))。將人等位基因獲得測定法用於篩選含有人DPP4基因以及該基因啟動子區的拷貝的ES細胞克隆。還將人等位基因獲得測定法用於鑑定攜帶人源化DPP4基因以及該基因啟動子區的(完全衍生自供體ES細胞的F0代小鼠)。簡而言之,利用標準方法從ES細胞克隆中提取基因組DNA,並使用兩組引物-探針在TaqManTM定量PCR(qPCR)測定法中測試所提取的基因組DNA,以檢測人DPP4編碼序列上遊的人DNA序列(7333hTU)和下遊的人DNA序列(7333hTD)(圖8)。每組引物-探針在人DPP4基因和側翼區(例如啟動子區域)內的退火位置在圖7中示出。TaqManTMqPCR測定法中高於背景的螢光讀數指示存在人DPP4基因和人DPP4基因的至少40kb的5』側翼區,它們已整合到轉基因小鼠基因組中。7333hTU引物-探針組(書寫順序為5』至3』)為:人上遊正向引物TGGCTTATTCTCTATTCCTCACCTA(SEQIDNO:18);人上遊探針FAM-TGCTTTCCCTCCTCCCTTCTGA-BHQ(SEQIDNO:19);人上遊反向引物GGCCTTAGCCCAGAAACTG(SEQIDNO:20)。7333hTD引物-探針組(書寫順序為5』至3』)為:人下遊正向引物TGCAGACTTGTCTTGACATTCATA(SEQIDNO:21);人下遊探針CAL-AGCCTCTGCAGACACAGGAATGGC-BHQ(SEQIDNO:22);人下遊反向引物TCTGGGCACTGGTGTACTC(SEQIDNO:23);其中FAM和CAL分別是指5-羧基螢光素螢光探針和CAL橙色螢光探針,BHQ是指黑洞猝滅劑型的螢光猝滅劑(生物搜索技術公司)。例如,按照製造商建議將來源於ES細胞克隆的基因組DNA在384孔PCR板(美國生命技術公司的MicroAmpTM384孔光學反應板)中與TaqManTM基因表達母混合液(TaqManTMGeneExpressionMasterMix,美國生命技術公司的)合併,然後使所得溶液在AppliedBiosystemsPrism7900HT中循環,AppliedBiosystemsPrism7900HT在PCR過程中收集螢光數據,並確定閾值循環(Ct)以及累積螢光達到預設閾值的PCR循環分數。每個DNA樣品都運行以下反應:上遊DPP4-特異性qPCR和下遊DPP4-特異性qPCR,以及非DPP4參照基因的兩個qPCR。計算每個DPP4-特異性qPCR和每個參照基因qPCR之間的Ct值差值(ΔCt),然後計算所有測定樣品的每個ΔCt與中值ΔCt之間的差值,從而得到每個樣品的ΔΔCt值。每個樣品中的DPP4基因拷貝數通過以下公式計算:拷貝數=2×2-ΔΔCt。含有至少一拷貝的整合到染色體中的人DPP4和啟動子區的克隆具有等於或大於一個的DPP4基因拷貝數。將相同的人等位基因獲得測定法用於測定從來源於ES細胞的小鼠尾部活檢組織中純化的DNA,以確定人源化DPP4等位基因以及人5』側翼區已通過種系傳遞。使用本文所述的BAC插入和篩選方法,含有編碼人DPP4的DNA的兩隻轉基因小鼠得以確認。將BACRP11-68L22用於產生ES細胞克隆和被稱為MAID7333的轉基因小鼠,將BACRP11-345J9用於產生ES細胞克隆和被稱為MAID7334的轉基因小鼠。MAID7333和MAID7334小鼠中由人源化DPP4核酸序列編碼的蛋白質具有圖9所示的胺基酸序列(SEQIDNO:24),該胺基酸序列與人DPP4(由轉錄物NM_001935.3編碼)相同。實例4處理MERS-CoV病毒感染的人源化DPP4小鼠測試含有人源化DPP4基因和側翼啟動子區的轉基因小鼠的被MERS-CoV感染的能力以及用作評估治療性分子用於治療或預防MERS-CoV的模型的能力。通過腹膜內注射(ip)用200μg針對MERS-CoV刺突蛋白的抗體或同種型對照處理轉基因MAID7333小鼠(例如,通過實例3中所述的方法產生)。注射抗體後一天,通過鼻內方式用MERS-CoV感染小鼠。感染後第四天,收集小鼠的肺,利用實時PCR(RT-PCR)測量病毒RNA水平。具體地講,測量MERS-CoV的基因組RNA(UpE)或複製RNA(前導序列)(特異於複製型MERS-CoV基因組)的水平。RT-PCR數據在下表中示出。抗體UpE1前導序列1抗MERS-CoV刺突蛋白1(Ab1)0.3568395620.273565089抗MERS-CoV刺突蛋白2(Ab2)0.2544932020.206006238抗MERS-CoV刺突蛋白3(Ab3)1.9895483161.112094283(IgG1)同種型對照104.0889287101.2578723(IgG4)同種型對照1001001平均值(同種型對照的百分比)用抗體處理轉基因小鼠使病毒RNA水平(UpE和前導序列兩者)降低了約50倍至約500倍。本文所述的數據表明,通過靶向整合法(實例1)和隨機BAC插入法(實例3)產生的含有人DPP4的轉基因小鼠易受MERS-CoV感染。此外,抗MERS-CoV抗體阻斷了轉基因小鼠的體內感染。因此,含有人DPP4的轉基因小鼠(例如,通過本文所述的方法產生的小鼠)可用於評價靶向MERS-CoV病毒的治療劑(例如抗體)的功效。實例5抗MERS-CoV抗體對人源化DPP4小鼠中的MERS-CoV感染的預防效果使用本文所述的人源化DPP4小鼠評價兩種單克隆抗體的體內預防能力。先通過腹膜內注射為小鼠注射一系列劑量的抗MERS-CoV抗體:200μg、20μg或2μg抗MERS-CoV刺突蛋白抗體2(Ab2)、抗MERS-CoV刺突蛋白抗體4(Ab4)或200μg人IgG1(hIgG1)同種型對照抗體,24小時後,通過鼻內方式用1×105pfuMERS-CoV(Jordan毒株)感染小鼠。Ab2和Ab4是完全人抗MERS-CoV刺突蛋白抗體。如上所述,從小鼠肺中提取RNA,並利用定量PCR進行分析。例如,利用ΔCt法對qPCR數據進行分析,其中將未感染對照設為1。相對於在用同種型匹配對照抗體處理的受感染小鼠中檢測到的RNA水平來表示檢測到的MERS-CoVRNA百分比(圖11A至圖11B)。此外,如上所述確定小鼠肺的病毒滴度。與同種型匹配對照抗體相比,兩種抗體都以每隻小鼠200μg的劑量使肺中的MERS-CoV特異性RNA水平顯著下降超過2log(圖11A至圖11B)。與相同劑量的Ab4相比,20μg劑量的Ab2對降低MERS-CoVRNA水平更加有效。與同種型對照處理的小鼠相比,2μg劑量的任一種抗體對降低病毒RNA水平沒有效果。當分析肺的MERS-CoV滴度時(圖11C),200μg和20μg劑量的Ab2使病毒水平降低到接近測定法中的檢測水平(2×103pfu/ml)。200μg劑量的Ab4與Ab2的效果相當,但20μg和2μg劑量的Ab4表現出病毒抑制的劑量依賴性抑制作用。這些數據表明,抗MERS-CoV抗體(例如,Ab2和Ab4)可有效阻斷體內MERS-CoV感染。在感染後第4天,還對來源於在感染前24小時用Ab2、Ab4或hIgG1同種型對照抗體處理的小鼠的肺進行組織學分析(圖12A)。例如,對間質炎症、細支氣管周圍炎症和血管周圍炎症程度進行評分(0至5)。還分析了其他組織學特徵,諸如細支氣管上皮和肺泡損傷、胸膜變化和支氣管血管周圍炎症程度。對於每個實驗組將每隻小鼠的總體炎症進行平均,分值表示為每組和每個時間點的所有小鼠的平均分值(圖12B)。來源於用hIgG1同種型對照預處理的小鼠的肺部表現出顯著的肺部病理現象,間質炎症加重、血管周圍呈袖套徵並且肺泡隔增厚。用200μgAb2或Ab4處理的小鼠的炎症減輕,間質中炎性細胞病灶極少、細支氣管袖套徵較輕並且肺泡壁增厚較少。在用20μgAb2和Ab4預處理的小鼠中,相較於較高劑量抗體組,血管周圍袖套徵和間質炎症水平中等。用2μg抗體預處理的組與hIgG1同種型對照具有相似的病理現象,表現出顯著的間質炎症和明顯的血管周圍炎症。盲法組織學評分表明,經處理的小鼠的炎症分值降低(圖12B)。這些發現表明,在MERS-CoV感染、確證小鼠中的病毒RNA水平和病毒滴度之後,抗MERS-CoV抗體(諸如,Ab2和Ab4)可導致肺部病理現象的劑量依賴性減輕。因此,抗MERS-CoV抗體(諸如,Ab2和Ab4)在MERS-CoV感染的體內模型中是有效的,當在感染前(例如感染前1天)注射這些抗體時,這些抗體可阻斷體內MERS-CoV感染和疾病。實例6用抗體處理已感染MERS-CoV的人源化DPP4小鼠為了確定抗MERS-CoV抗體(例如,Ab2和Ab4)的治療效果(例如,感染後抑制MERS-CoV複製和肺部病理現象的能力),用MERS-CoV感染人源化DPP4小鼠。感染後24小時,通過腹膜內注射為小鼠注射500μghIgG1同種型對照或者500μg或200μgAb2。感染後第4天,對小鼠實施安樂死,並分析小鼠肺部的病毒RNA、病毒滴度和肺部病理現象。與用對照抗體處理的小鼠相比,500μg和200μg劑量的Ab2都使小鼠肺部中的病毒RNA水平降低約10倍(圖13A至圖13B)。相同小鼠的肺部滴度證實,肺中的病毒水平顯著降低,其中感染後第4天病毒水平下降大於2log(圖13C)。這些數據表明,感染後(例如,感染後24小時),抗MERS-CoV抗體(例如,Ab2)顯著抑制了病毒複製。還對感染後24小時用hIgG1對照抗體、500μgAb2或200μgAb2處理的小鼠進行了組織學分析(圖14A至圖14B)。用對照抗體處理的小鼠表現出與實例2和實例5中的對照相似的病理現象,間質炎症顯著、血管周圍呈袖套徵以及肺泡隔增厚。用200μg或500μgAb2處理的小鼠的整個肺中間質炎症減輕,僅具有血管周圍炎症病灶。盲法組織學評分表明,經處理的小鼠的炎症分值降低(圖14B)。以上數據表明,即使在感染後(例如,感染後24小時)才給予抗體,抗MERS-CoV抗體(例如,Ab2)的治療劑量也能減輕MERS-CoV誘發的肺部病理現象。當前第1頁1 2 3 
