糖基β‑欖香烯衍生物及其製備方法和應用與流程
2023-05-04 07:35:01 5
本發明涉及醫藥技術領域,尤其涉及糖基β-欖香烯衍生物及其製備方法和應用。
背景技術:
β-欖香烯是我國研究人員首次從姜科植物溫鬱金根莖中提取出來的國家二類抗癌藥物,其通過抑制癌細胞增殖、誘導癌細胞凋亡、抑制癌細胞血管生成、遏制癌細胞轉移、影響端粒酶活性以及逆轉癌細胞耐藥性等發揮抗腫瘤作用,其抗癌作用療效確切、毒副作用小、可以通過多條途徑改善和提高機體免疫功能、且對一些容易產生耐藥性的惡性腫瘤也有較好的療效、具有廣譜的抗癌活性和良好的抗腫瘤應用前景。但是,由於β-欖香烯難溶於水、生物利用度低、不能實時監控治療腫瘤等缺點,使其在濃度和時間上呈現出較強的依賴性,嚴重限制了其臨床應用。因此,對其化合物進行改造以提高β-欖香烯水溶性和生物兼容性具有重要的科學意義。
β-欖香烯的結構如下:
技術實現要素:
本發明要解決的技術問題是提供糖基β-欖香烯衍生物及其製備方法和應用,具體是三類可實時監控治療腫瘤的糖基β-欖香烯衍生物以及其合成方法和在抗腫瘤方面的應用。
為解決上述技術問題,本發明採用以下技術方案:
糖基β-欖香烯衍生物,具有以下通式:
通式I、II、III中,為多羥基糖基。
通式I、II、III中,
通式I的化合物為:
通式II的化合物為:
通式III的化合物為:
上述糖基β-欖香烯衍生物的製備方法,首先通過環化反應將羅丹明B關環得到螢光猝滅的羅丹明衍生物,然後在氫化鈉催化下分別與不同末端炔基化合物進行親核取代反應得到含有不同末端炔基的羅丹明衍生物,該類化合物再分別與全乙醯糖基疊氮、疊氮化β-欖香烯的經過銅(I)催化點擊化學反應以及脫乙醯化反應得到目標化合物。
全乙醯糖基疊氮為乙醯化保護後的多羥基糖基疊氮。
上述糖基β-欖香烯衍生物在製備實時監控治療腫瘤的抗癌藥物方面的應用。
多羥基的糖類物質是人類重要的營養物質,具有較強的親水性,而且綠色環保。因此,在β-欖香烯引入親水性的糖類物質,是提高β-欖香烯水溶性很好的設計思路。而羅丹明類化合物具有高量子產率、高消光係數、極好的光穩定性、激發波長較長、檢測靈敏度高、價格便宜等諸多優點,而且在不同pH條件下表現出螢光「開-關」效應(鹼性條件下閉環後猝滅螢光,酸性條件下開環後發出螢光);另外,已有研究表明,腫瘤細胞呈偏酸性(胞外pH 6.2-6.9,胞內pH 4.5-5.5),閉環的羅丹明化合物可在腫瘤細胞內開環釋放出強烈的螢光。因此,在β-欖香烯引入羅丹明將有望實現實時監控治療腫瘤的目的。
為此,針對β-欖香烯難溶於水、生物利用度低、不能實時監控治療腫瘤等缺點,發明人根據腫瘤細胞偏酸性的性質將親水性的糖類物質和具有強螢光性質的羅丹明引入β-欖香烯結構中,設計合成了具有通式I、II、III的糖基β-欖香烯衍生物。研究表明,所得的糖基β-欖香烯衍生物水溶性較好、抗癌活性好,可作為實現實時監控治療腫瘤的抗癌藥物應用於惡性腫瘤的治療,對β-欖香烯在醫藥領域的研究與應用具有重要的科學意義。同時,發明人建立了相應化合物的製備方法,該法運用點擊化學反應技術,合成簡單、科學。
與現有技術相比,本發明的突出優點在於:
(1)本發明在β-欖香烯同時引入糖基1,2,3-三唑和羅丹明B,合成了糖基1,2,3-三唑羅丹明β-欖香烯衍生物,合成出一類水溶性好、可實現實時監控治療腫瘤的β-欖香烯衍生物;
(2)本發明引入的基團為糖基1,2,3-三唑,糖類物質是人類重要的營養物質,具有較強的親水性,而且綠色環保;
(3)本發明引入的羅丹明螢光染料價格便宜、量子產率高、光穩定性好、激發波長較長,可減少內源性螢光的幹擾;
(4)本發明糖基1,2,3-三唑羅丹明β-欖香烯衍生物能應用於醫藥技術領域惡性腫瘤的治療。
附圖說明
圖1是本發明糖基β-欖香烯衍生物pH響應的螢光測試曲線圖,圖中:從上至下各曲線分別表示不同pH值條件下化合物的螢光強度。
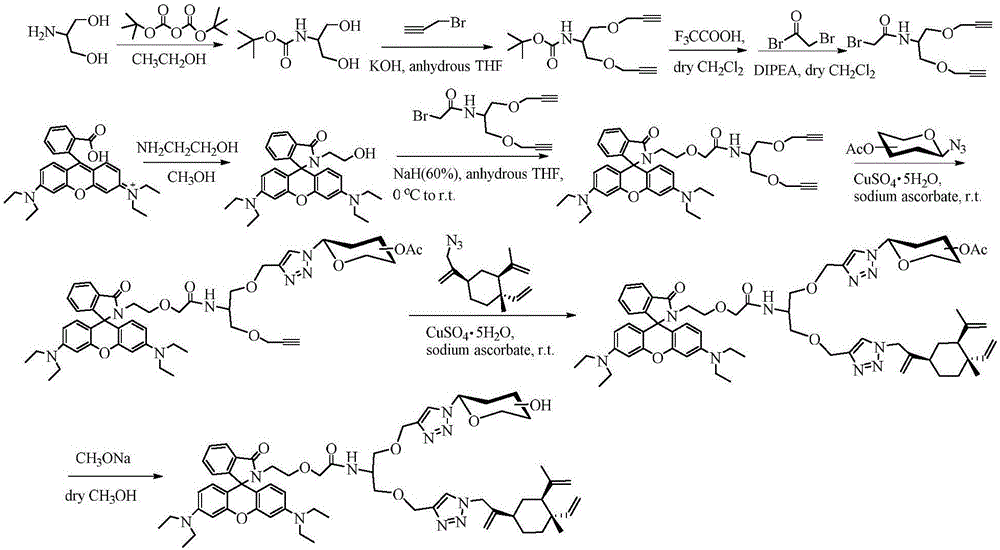
圖2是本發明糖基β-欖香烯衍生物的合成線路圖一。
圖3是本發明糖基β-欖香烯衍生物的合成線路圖二。
具體實施方式
本發明的糖基β-欖香烯衍生物可按圖1和圖2所示反應路線合成,具體製備方法為:首先通過環化反應將羅丹明B關環得到螢光猝滅的羅丹明衍生物,然後在氫化鈉催化下分別與不同末端炔基化合物進行親核取代反應得到含有不同末端炔基的羅丹明衍生物,該類化合物再分別與全乙醯糖基疊氮、疊氮化β-欖香烯的經過銅(I)催化點擊化學反應以及脫乙醯化反應得到目標化合物。
為了更好地理解本發明,下面結合實施例進一步闡明本發明β-欖香烯衍生物及其製備方法的內容。
實施例1
將羅丹明B(10g)溶於甲醇(20mL)後加入乙醇胺(25mL),Ar保護,放置75℃油浴下回流至紅色消失,冷切至室溫,加入100mL去離子水,CH2Cl2萃取,飽和食鹽水洗滌,無水Na2SO4乾燥,過濾,濃縮,矽膠柱純化(PE/EA=4∶1),得到灰白色固體1(3.84g,35%)。1H NMR(600MHz,CDCl3)δ7.92(dd,J=5.6,3.0Hz,1H),7.46(dd,J=5.6,3.1Hz,2H),7.09(dd,J=5.2,3.2Hz,1H),6.51(d,J=8.9Hz,2H),6.40(d,J=2.4Hz,2H),6.31(dd,J=8.9,2.4Hz,2H),3.51-3.47(m,2H),3.36(q,J=7.0Hz,8H),3.32-3.29(m,2H),1.19(t,J=7.1Hz,12H).13C NMR(151MHz,CDCl3)δ170.10,153.92,153.28,148.90,132.69,130.45,128.51,128.14,123.81,122.90,108.24,104.80,97.80,65.87,62.68,62.66,44.65,44.37,12.61.
將絲氨醇(5g)溶於150mL的無水乙醇,加入100mL BOC酸酐(12g)無水乙醇溶液,室溫反應6h,旋除溶劑,再用正庚烷重結晶得白色固體2(9.6g,91%)。1H NMR(600MHz,DMSO)δ4.51(t,J=5.3Hz,2H),3.35(m,5H),1.38(s,9H).
將粉狀的KOH(3.05g)和無水THF(15mL)懸浮液冷卻至0℃,Ar保護。將化合物2(2.06g)溶於無水THF(10mL)後,逐滴加入反應液中,加完後0℃反應15min,逐滴加入4.7mL的溴丙炔,0℃反應5min後升溫至35℃反應過夜,加入去離子水(100mL),CH2Cl2萃取,飽和食鹽水洗滌,無水Na2SO4乾燥,過濾,濃縮,過柱分離,得到黃色液體3(2.467g,88%)。1H NMR(600MHz,CDCl3)δ4.18(d,J=2.3Hz,4H),3.94(s,1H),3.65(dd,J=9.3,4.4Hz,2H),3.59(dd,J=8.9,6.1Hz,2H),2.45(t,J=2.4Hz,2H),1.46(s,9H).ESI-MS(m/z)268.2[M+H+].
化合物3(2.4g)溶於30mL乾燥的CH2Cl2,0℃下逐滴加入三氟乙酸(15mL),Ar保護下室溫反應3h,旋除溶劑,加入甲苯(6×10mL)帶除多餘的三氟乙酸後,加入15mL乾燥的CH2Cl2和4.5mL的N,N-二異丙基乙胺,Ar保護,冷卻至0℃後逐滴加入30mL混合液(1.2mL溴乙醯溴+30mL乾燥的CH2Cl2),加完後自然升溫至室溫反應過夜,加入30mL CH2Cl2稀釋,去離子水洗滌,無水Na2SO4乾燥,濃縮,過柱分離(PE/EA=7∶1),得到淡黃色液體4(1.78g,68%)。1H NMR(600MHz,CDCl3)δ6.81(d,J=8.5Hz,1H),4.26(dtt,J=8.7,5.6,4.5Hz,1H),4.19(dd,J=2.4,0.9Hz,4H),3.89(s,2H),3.69(dd,J=9.4,4.5Hz,2H),3.62(dd,J=9.5,5.6Hz,2H),2.47(t,J=2.4Hz,2H).
將NaH(60%,0.407g)和無水THF(10mL)懸浮液冷卻至0℃,Ar保護。將化合物1(1.31g)溶於無水THF(15mL)後,攪拌下逐滴加入反應液中,加完後0℃反應30min,再將預先配置的溶液(1.04g化合物4+5mL無水THF)逐滴加入反應體系中,加完後放置室溫反應過夜。加入去離子水猝滅反應,CH2Cl2萃取,飽和食鹽水洗滌,無水Na2SO4乾燥,過濾,濃縮,柱層析純化(PE/EA=4∶1),得到灰白色固體5(1.3g,68%)。
1H NMR(600MHz,CDCl3)δ7.95-7.91(m,1H),7.48-7.44(m,2H),7.13-7.07(m,2H),6.46(d,J=8.9Hz,2H),6.39(d,J=2.5Hz,2H),6.29(dd,J=8.9,2.5Hz,2H),4.30(dt,J=8.8,5.4Hz,1H),4.10(d,J=2.4Hz,4H),3.68-3.62(m,6H),3.42(t,J=6.2Hz,2H),3.35(q,J=7.1Hz,8H),3.07(t,J=6.2Hz,2H),2.40(t,J=2.3Hz,2H),1.18(t,J=7.1Hz,12H).ESI-MS(m/z)693.4[M+H+].
將化合物5(0.28g)溶於THF(2.5mL),Ar保護,室溫下將預先用去離子水(2.5mL)溶解的抗壞血酸鈉(13.5mg)和CuSO4·5H2O(1.6mg)溶液加入反應液中,少量多次分批加入全乙醯半乳糖疊氮(0.15g),TCL監控反應至產物點最濃時結束反應(總共約24h),加入去離子水,CH2Cl2萃取,飽和食鹽水洗滌,無水Na2SO4乾燥,過濾,濃縮,過柱分離,得到淡紅色固體6(0.19g,44%)。1H NMR(600MHz,CDCl3)δ7.93(ddd,J=10.2,8.5,3.7Hz,2H),7.46(dd,J=5.6,3.1Hz,2H),7.15-7.09(m,2H),6.47-6.44(m,2H),6.39(t,J=2.4Hz,2H),6.30-6.27(m,2H),5.87(dd,J=9.3,3.4Hz,1H),5.62(td,J=9.8,4.4Hz,1H),5.56(d,J=3.2Hz,1H),5.29-5.25(m,1H),4.67(d,J=3.9Hz,2H),4.34-4.28(m,1H),4.26-4.20(m,2H),4.17-4.12(m,1H),4.07-4.04(m,2H),3.69-3.58(m,6H),3.49(dddd,J=13.0,9.5,6.4,3.2Hz,1H),3.39-3.33(m,9H),3.12(dt,J=9.5,6.0Hz,1H),3.05-2.99(m,1H),2.43-2.41(m,1H),2.24(s,3H),2.06(s,3H),2.03(d,J=0.9Hz,3H),1.90(d,J=4.2Hz,3H),1.18(t,J=7.0Hz,12H).
將2.58mL的β-欖香烯和2mL的混合液放置冰浴冷卻至5℃以下,磁力攪拌下逐滴加入13.5mL的次氯酸鈉溶液(滴加時長4h以上),加完後放置室溫反應2h,加入CH2Cl2萃取,去離子水洗滌,無水Na2SO4乾燥,過濾,濃縮,矽膠柱小心分離(石油醚),得到1.1g的7-1和7-2混合液(7-1為主)。
將得到的7-1和7-2的混合液(0.85g)溶於5mL DMSO,室溫下分批加入NaN3(0.36g),室溫反應3h,將反應液傾入40mL的去離子水中,CH2Cl2萃取(4×15mL),飽和食鹽水洗滌,無水Na2SO4乾燥,過濾,濃縮,過柱分離(石油醚),得到較純的油狀液體8(仍然有微量14位取代的β-欖香烯,0.44g,50%)。
將化合物6(0.19g)和化合物8(56mg)溶於THF(3mL),Ar保護,室溫下將預先用去離子水(3mL)溶解的抗壞血酸鈉(13.5mg)和CuSO4·5H2O(1.6mg)溶液加入反應液中,室溫反應過夜,加入去離子水,CH2Cl2萃取,飽和食鹽水洗滌,無水Na2SO4乾燥,過濾,濃縮,過柱分離,得到淡紅色固體9(0.18g,77%)。
將化合物9(0.18g)溶於5mL的乾燥甲醇溶液中,加入甲醇鈉溶液調節pH至9-10,室溫反應過夜,加入氫離子交換樹脂調節pH至中性,過濾,濃縮,過柱分離,得到白色固體10(0.12g,76%)。1H NMR(600MHz,CD3OD)δ8.21(d,J=15.3Hz,1H),7.91(dd,J=7.5,3.9Hz,1H),7.80(d,J=1.2Hz,1H),7.59-7.51(m,2H),7.08-7.04(m,1H),6.44(s,2H),6.40-6.32(m,3H),6.31-6.27(m,1H),5.80(dd,J=17.5,10.8Hz,1H),5.59(dd,J=9.1,3.0Hz,1H),5.07(d,J=2.3Hz,1H),5.00(dd,J=12.8,9.3Hz,2H),4.90(d,J=3.0Hz,2H),4.86(s,1H),4.80(s,2H),4.57(dd,J=5.2,3.2Hz,3H),4.52(s,1H),4.24(dd,J=5.6,2.2Hz,1H),4.20(t,J=9.3Hz,1H),4.02(d,J=2.8Hz,1H),3.86(t,J=5.8Hz,1H),3.76(ddd,J=21.9,13.0,6.3Hz,3H),3.67-3.54(m,6H),3.49-3.34(m,10H),3.10-2.97(m,2H),1.96(dt,J=12.7,3.5Hz,1H),1.92(d,J=3.4Hz,1H),1.68(s,3H),1.61-1.48(m,3H),1.42(ddd,J=13.7,11.6,6.8Hz,3H),1.20-1.12(m,11H),1.05(t,J=7.0Hz,1H),1.00(s,3H).13C NMR(151MHz,CD3OD)δ170.75,169.10,153.74,153.38,153.35,149.89,149.09,148.66,148.65,147.20,144.66,144.59,132.89,130.59,130.56,128.29,123.99,123.97,123.67,122.56,122.52,112.08,112.03,111.57,109.23,108.23,108.13,104.66,104.54,97.65,88.86,78.52,73.95,70.07,69.47,68.98,68.74,68.39,65.54,63.68,61.03,53.67,52.41,48.50,44.01,42.07,39.57,39.37,39.13,32.81,26.78,23.98,15.72,11.58,11.57.ESI-MS(m/z)1143.6[M+H+].HRMS(MALDI)calcd for C62H83N10O11:[M+H+]1143.6237,found 1143.6245.
實施例2
用類似於化合物6的合成方法得到化合物12。1H NMR(600MHz,CDCl3)δ7.92-7.89(m,1H),7.87(s,1H),7.48-7.43(m,2H),7.16-7.08(m,2H),6.45(ddd,J=8.6,5.9,2.6Hz,2H),6.39(t,J=2.6Hz,2H),6.29(ddd,J=8.2,5.5,2.6Hz,2H),5.86(dd,J=9.3,2.7Hz,1H),5.49(q,J=9.4Hz,1H),5.44-5.40(m,1H),5.38(d,J=2.8Hz,1H),5.15(dd,J=10.4,7.9Hz,1H),4.99(dd,J=10.4,3.5Hz,1H),4.65(d,J=2.9Hz,2H),4.55(dd,J=7.9,2.1Hz,1H),4.49(d,J=12.2Hz,1H),4.32-4.27(m,1H),4.18-4.12(m,3H),4.06-4.03(m,2H),4.03-3.98(m,1H),3.93(dt,J=10.5,6.1Hz,2H),3.69(dd,J=14.8,3.5Hz,1H),3.65-3.61(m,3H),3.61-3.57(m,2H),3.48(dd,J=14.0,6.9Hz,1H),3.39-3.32(m,10H),3.11(dt,J=9.4,6.0Hz,1H),3.03-2.98(m,1H),2.41(dd,J=2.3,1.7Hz,1H),2.18(s,3H),2.11(s,3H),2.09(d,J=0.6Hz,3H),2.08(s,3H),2.07(s,3H),1.99(s,3H),1.87(d,J=4.5Hz,3H),1.18(td,J=7.0,1.3Hz,12H).
用類似於化合物9的合成方法得到化合物13,直接進行下一步反應。
用類似於化合物10的合成方法得到化合物14。1H NMR(600MHz,CD3OD)δ8.20(d,J=19.2Hz,1H),7.91-7.85(m,1H),7.76(d,J=1.6Hz,1H),7.57-7.50(m,2H),7.06(dd,J=5.3,1.5Hz,1H),6.54-6.21(m,6H),5.79(dd,J=17.5,10.8Hz,1H),5.64(dd,J=9.2,2.2Hz,1H),5.06(d,J=3.9Hz,1H),5.01-4.92(m,2H),4.88(t,J=1.1Hz,1H),4.85(s,2H),4.81-4.76(m,2H),4.59-4.53(m,3H),4.50(d,J=2.9Hz,2H),4.42(dd,J=7.7,3.6Hz,1H),4.21(dt,J=10.9,5.4Hz,1H),4.00(t,J=9.0Hz,1H),3.89(d,J=2.4Hz,2H),3.84(d,J=3.0Hz,1H),3.82-3.70(m,5H),3.63-3.54(m,7H),3.53-3.48(m,2H),3.46-3.32(m,9H),3.08-2.92(m,2H),1.98-1.87(m,2H),1.67(t,J=6.2Hz,3H),1.60-1.46(m,3H),1.46-1.37(m,3H),1.15(td,J=7.0,2.8Hz,11H),1.05-1.01(m,1H),0.98(d,J=1.0Hz,3H).ESI-MS(m/z)1305.7[M+H+].HRMS calcd for C68H93N10O16:[M+H+]1305.67655,found 1305.67712.
實施例3
將5g三羥甲基氨基甲烷溶於30mL甲醇和30mL叔丁醇組成的混合溶液,攪拌下加入BOC酸酐(11.75g)叔丁醇(50mL)溶液,室溫反應過夜,旋除溶劑,加入乙酸乙酯冷藏過夜,過濾得到白色固體15(8.5g,93%)。1H NMR(600MHz,DMSO-d6)δ4.49(s,3H),3.52(s,6H),1.37(s,9H).
將粉狀的KOH(2.3g)和乾燥的DMF(10mL)懸浮液冷卻至0℃,Ar保護。將化合物15(1.5g)溶於無水THF(10mL)後,逐滴加入反應液中,加完後0℃反應10min,逐滴加入3.3mL的溴丙炔,0℃反應5min後升溫至35℃反應過夜,加入去離子水(100mL),CH2Cl2萃取,飽和食鹽水洗滌,無水Na2SO4乾燥,過濾,濃縮,過柱分離(PE∶EA=15∶1-8∶1),得到黃色液體16(1.4g,61%)。1H NMR(600MHz,CDCl3)δ5.32(s,1H),4.17(d,J=2.3Hz,6H),3.81(s,6H),2.45(t,J=2.3Hz,3H),1.44(s,9H).
化合物16(1.27g)溶於15mL乾燥的CH2Cl2,0℃下逐滴加入三氟乙酸(6mL),Ar保護下室溫反應3h,旋除溶劑,加入甲苯(6×10mL)帶除多餘的三氟乙酸後,加入10mL乾燥的CH2Cl2和1.7mL的N,N-二異丙基乙胺,Ar保護,冷卻至0℃後逐滴加入20mL混合液(0.41mL溴乙醯溴+20mL乾燥的CH2Cl2),加完後自然升溫至室溫反應過夜,加入30mL CH2Cl2稀釋,去離子水洗滌,無水Na2SO4乾燥,濃縮,過柱分離(PE/EA=7∶1),得到淡黃色液體17(0.92g,68%)。1H NMR(600MHz,CDCl3)δ6.70(s,1H),4.18(d,J=2.4Hz,6H),3.87(s,6H),3.82(s,2H),2.47(t,J=2.3Hz,3H).13C NMR(151MHz,CDCl3)δ165.39,79.40,74.81,68.14,59.76,58.70,29.47.
將NaH(60%,0.2175g)和無水THF(5mL)懸浮液冷卻至0℃,Ar保護。將化合物1(0.643g)溶於無水THF(5mL)後,逐滴加入反應液中,加完後0℃反應30min,再將預先配置的溶液(0.592g化合物17+5mL無水THF)逐滴加入反應體系中,加完後放置室溫反應過夜。加入去離子水猝滅反應,CH2Cl2萃取,飽和食鹽水洗滌,無水Na2SO4乾燥,過濾,濃縮,過柱分離(PE/EA=1∶4),得到淡紅色固體18(0.733g,72.8%)。1H NMR(600MHz,CDCl3)δ7.94-7.91(m,1H),7.47-7.42(m,2H),7.11-7.06(m,1H),6.82(s,1H),6.46(d,J=8.9Hz,2H),6.39(d,J=2.3Hz,2H),6.29(dd,J=8.9,2.5Hz,2H),4.11(d,J=2.4Hz,6H),3.85(s,6H),3.55(s,2H),3.42(t,J=6.6Hz,2H),3.35(q,J=7.1Hz,8H),3.06(t,J=6.6Hz,2H),2.40(t,J=2.3Hz,3H),1.18(t,J=7.1Hz,12H).13C NMR(151MHz,CDCl3)6169.47,168.35,153.67,153.20,148.83,132.41,130.94,128.88,128.01,123.76,122.89,108.13,105.44,97.69,79.74,74.54,70.39,68.27,68.12,64.62,59.17,58.58,44.38,39.06,12.61.ESI-MS(m/z)761.4[M+H+].
將化合物18(1.04g)溶於THF(10mL),Ar保護,室溫下將預先用去離子水(10mL)溶解的抗壞血酸鈉(1.1g)和CuSO4·5H2O(12.6mg)溶液加入反應液中,少量多次分批加入全乙醯半乳糖疊氮(1.5g),TCL監控反應至產物點較濃時結束反應(總共約30h),加入去離子水,CH2Cl2萃取,飽和食鹽水洗滌,無水Na2SO4乾燥,過濾,濃縮,過柱分離得到淡紅色固體19(0.23g,15%)以及淡紅色固體20(0.395g,19%)。
將化合物19(0.23g)和化合物8(0.125g)溶於THF(4mL),Ar保護,室溫下將預先用去離子水(4mL)溶解的抗壞血酸鈉(32mg)和CuSO4·5H2O(20mg)溶液加入反應液中,室溫反應過夜,加入去離子水,CH2Cl2萃取,飽和食鹽水洗滌,無水Na2SO4乾燥,過濾,濃縮,過柱分離,得到淡紅色固體21(0.22g,67%)。
將化合物21(0.2g)溶於5mL的乾燥甲醇溶液中,加入甲醇鈉溶液調節pH至9-10,室溫反應過夜,加入氫離子交換樹脂調節pH至中性,過濾,濃縮,過柱分離,得到白色固體22(0.13g,72.5%)。1H NMR(600MHz,CD3OD)δ8.16(s,1H),7.93-7.76(m,3H),7.58-7.43(m,2H),7.11-7.00(m,1H),6.60-6.19(m,6H),5.79(dd,J=17.5,10.9Hz,2H),5.57(d,J=9.1Hz,1H),5.05(s,2H),5.01(d,J=6.2Hz,4H),4.88(s,2H),4.84(s,2H),4.79(s,4H),4.55(dd,J=25.4,12.2Hz,8H),4.18(t,J=9.3Hz,1H),4.00(d,J=2.8Hz,1H),3.84(t,J=5.9Hz,1H),3.80-3.69(m,9H),3.42(s,2H),3.35(dd,J=13.4,6.5Hz,8H),2.99(d,J=5.2Hz,2H),2.02-1.88(m,4H),1.67(s,6H),1.55(dt,J=17.6,12.6Hz,6H),1.48-1.37(m,6H),1.14(t,J=7.0Hz,10H),1.03(t,J=7.0Hz,2H),0.98(s,6H).13C NMR(151MHz,CD3OD)δ170.27,168.89,153.84,153.30,149.92,149.02,148.75,147.21,144.73,144.68,132.74,130.57,128.38,128.18,124.00,123.64,122.48,111.91,111.60,109.24,108.16,104.80,97.62,88.92,78.60,73.94,70.12,69.70,68.96,67.93,67.88,67.67,65.23,64.02,63.87,61.03,59.68,53.66,52.40,44.02,42.06,39.58,39.39,32.79,26.81,24.03,15.73,11.62.ESI-MS(m/z)1456.8[M+].HRMS(MALDI)calcd for C81H110N13O12:[M+H+]1456.8391,found 1456.8391.
實施例4
將化合物20(0.35g)和化合物8(0.086g)溶於THF(4mL),Ar保護,室溫下將預先用去離子水(4mL)溶解的抗壞血酸鈉(20mg)和CuSO4·5H2O(12mg),溶液加入反應液中,室溫反應過夜,加入去離子水,CH2Cl2萃取,飽和食鹽水洗滌,無水Na2SO4乾燥,過濾,濃縮,過柱分離,得到淡紅色固體23(0.29g,71%)。
將化合物23(0.25g)溶於6mL的乾燥甲醇溶液中,加入甲醇鈉溶液調節pH至9-10,室溫反應過夜,加入氫離子交換樹脂調節pH至中性,過濾,濃縮,過柱分離,得到白色固體24(0.15g,74%)。1H NMR(600MHz,CD3OD)δ8.19(d,J=4.4Hz,2H),7.92-7.87(m,1H),7.84(s,1H),7.56-7.50(m,2H),7.06(tt,J=5.5,2.8Hz,1H),6.44(d,J=2.4Hz,2H),6.41(dd,J=8.9,3.8Hz,2H),6.37-6.31(m,2H),5.80(dd,J=17.5,10.8Hz,1H),5.62(d,J=9.2Hz,2H),5.06(s,1H),5.02(d,J=8.3Hz,2H),4.90(d,J=1.1Hz,1H),4.80(d,J=1.3Hz,2H),4.56(dd,J=33.8,16.4Hz,8H),4.23(t,J=9.3Hz,2H),4.03(d,J=3.1Hz,2H),3.88(t,J=5.9Hz,2H),3.77(ddd,J=17.8,12.2,5.0Hz,12H),3.47(s,2H),3.42-3.34(m,10H),3.02(dd,J=8.2,5.7Hz,2H),2.02-1.88(m,2H),1.68(s,3H),1.62-1.52(m,3H),1.48-1.38(m,3H),1.16(t,J=7.1Hz,11H),1.04(dd,J=8.2,5.9Hz,1H),1.00(s,3H).13C NMR(151MHz,CD3OD)δ170.41,169.02,153.83,153.31,149.94,149.04,148.72,147.23,144.70,144.57,132.81,130.51,128.38,128.22,124.05,123.64,122.67,122.51,111.93,111.58,109.22,108.21,104.73,97.62,88.82,78.54,73.92,70.08,69.64,69.00,68.02,67.84,67.60,65.35,63.97,63.78,61.04,59.73,53.68,52.39,44.02,42.03,39.57,39.39,39.00,32.79,26.80,24.01,15.71,13.38,11.60.ESI-MS(m/z)1416.7[M+H+].HRMS(MALDI)calcd for C72H98N13O17:[M+H+]1416.7198,found 1416.7196.
實施例5
用類似於化合物19和20的合成方法得到化合物25和26。化合物26的1H NMR和13C NMR為:1H NMR(600MHz,CDCl3)δ7.90-7.86(m,2H),7.84(s,1H),7.45(dd,J=5.3,3.3Hz,2H),7.09(dd,J=5.7,2.6Hz,1H),6.83(s,1H),6.45(d,J=8.7Hz,2H),6.38(s,2H),6.28(d,J=8.4Hz,2H),5.91(dd,J=9.3,1.8Hz,2H),5.52(t,J=9.4Hz,2H),5.43(t,J=9.1Hz,2H),5.37(d,J=3.2Hz,2H),5.14(dd,J=10.0,8.3Hz,2H),4.99(dd,J=10.4,3.3Hz,2H),4.65-4.61(m,4H),4.56(d,J=7.9Hz,2H),4.50(d,J=12.9Hz,2H),4.19-4.14(m,3H),4.14-4.09(m,3H),4.06-4.02(m,2H),4.01-3.97(m,4H),3.92(dd,J=12.6,5.8Hz,2H),3.84-3.80(m,2H),3.80-3.75(m,4H),3.51(q,J=14.7Hz,2H),3.46-3.37(m,2H),3.34(q,J=6.9Hz,8H),3.07-2.98(m,2H),2.39(t,J=2.3Hz,1H),2.17(s,6H),2.09(s,6H),2.08-2.06(m,18H),1.98(s,6H),1.83(s,3H),1.81(s,3H),1.16(t,J=7.0Hz,12H).13C NMR(151MHz,CDCl3)δ170.40,170.33,170.17,170.09,169.68,169.66,169.60,169.18,169.05,169.02,168.46,153.62,153.19,148.87,145.66,132.57,130.81,128.80,128.14,123.83,122.79,121.89,121.76,108.15,101.12,97.69,85.28,85.26,79.75,75.76,75.69,74.82,72.84,70.97,70.79,70.51,70.35,69.09,68.73,68.69,68.22,68.11,66.66,64.81,64.78,64.76,61.89,60.84,59.43,58.38,56.81,44.37,39.09,21.79,20.80,20.74,20.65,20.64,20.62,20.51,20.20,20.16,12.57.ESI-MS(m/z)2084.8[M+H+].
用類似於化合物21的合成方法得到化合物27。1H NMR(600MHz,CDCl3)δ7.89-7.81(m,2H),7.61(d,J=11.2Hz,2H),7.44(ddd,J=5.7,4.9,3.6Hz,2H),7.10(dd,J=5.6,2.5Hz,1H),6.81(s,1H),6.44(d,J=8.9Hz,2H),6.39(d,J=2.5Hz,2H),6.30-6.24(m,2H),5.90(d,J=9.4Hz,1H),5.82-5.76(m,2H),5.56(t,J=9.5Hz,1H),5.43(t,J=9.3Hz,1H),5.38(d,J=3.3Hz,1H),5.16(dd,J=10.3,7.9Hz,1H),5.08(s,2H),5.01-4.96(m,5H),4.91(d,J=2.4Hz,2H),4.89(d,J=2.4Hz,2H),4.83(d,J=3.9Hz,4H),4.61-4.56(m,8H),4.18(dd,J=12.2,5.4Hz,1H),4.14(q,J=7.1Hz,5H),4.08(t,J=9.5Hz,1H),4.00-3.96(m,1H),3.93(d,J=6.7Hz,1H),3.80(dd,J=9.0,2.8Hz,3H),3.76(dd,J=9.7,6.3Hz,2H),3.51(s,2H),3.40(t,J=6.5Hz,2H),3.34(q,J=7.0Hz,8H),3.03(t,J=6.5Hz,2H),2.18(s,3H),2.10(s,3H),2.08(s,6H),2.07(s,3H),2.06(s,3H),1.98(d,J=5.9Hz,4H),1.96(d,J=3.9Hz,1H),1.91(s,2H),1.82(s,3H),1.69(s,6H),1.65(d,J=8.9Hz,2H),1.58(dd,J=24.0,12.8Hz,4H),1.48-1.40(m,6H),1.17(t,J=7.1Hz,12H),1.00(s,6H).ESI-MS(m/z)1914.0[M+H+].
用類似於化合物22的合成方法得到化合物28。1H NMR(600MHz,CD3OD)δ8.17(s,1H),7.87(dd,J=20.0,4.5Hz,3H),7.54(tt,J=13.0,6.7Hz,2H),7.08(dd,J=6.4,1.1Hz,1H),6.41(ddd,J=14.9,11.3,2.0Hz,4H),6.36-6.31(m,2H),5.81(dd,J=17.5,10.8Hz,2H),5.67(d,J=9.2Hz,1H),5.07(s,2H),5.03(s,4H),4.90(d,J=1.0Hz,2H),4.87(s,2H),4.81(s,4H),4.63-4.55(m,6H),4.53(s,3H),4.45(d,J=7.7Hz,1H),4.02(t,J=9.1Hz,1H),3.92(d,J=2.5Hz,2H),3.86(d,J=3.1Hz,1H),3.84-3.80(m,2H),3.78(s,2H),3.75(t,J=10.5Hz,6H),3.65-3.59(m,2H),3.53(dd,J=9.7,3.2Hz,1H),3.45(s,2H),3.38(dd,J=13.8,6.8Hz,10H),3.01(t,J=5.9Hz,2H),2.02-1.91(m,4H),1.69(s,6H),1.64-1.57(m,4H),1.54(t,J=10.0Hz,2H),1.44(ddd,J=14.3,13.5,7.7Hz,6H),1.16(t,J=7.0Hz,11H),1.01(s,6H),0.92(t,J=7.0Hz,1H).13C NMR(151MHz,CD3OD)6170.33,168.94,153.85,153.31,149.92,149.04,148.74,147.21,132.76,130.54,128.35,128.19,123.99,123.63,122.95,122.46,111.91,111.57,109.21,108.16,104.74,103.73,97.61,88.00,78.33,78.19,75.74,75.44,73.45,72.30,71.16,68.91,67.88,65.28,64.00,61.12,60.15,59.69,53.66,52.40,44.01,42.07,39.57,39.38,32.79,26.80,24.00,15.70,11.58.ESI-MS(m/z)1618.9[M+H+].HRMS(MALDI)calcd for C87H120N13O17:[M+H+]1618.8920,found 1618.8917.
實施例6
用類似於化合物23的合成方法得到化合物29,直接進行下一步的反應。1H NMR(600MHz,CDCl3)δ7.92-7.82(m,3H),7.60(s,1H),7.44(dd,J=8.7,5.3Hz,2H),7.10(d,J=6.0Hz,1H),6.82(d,J=9.3Hz,1H),6.47(dd,J=24.2,14.1Hz,2H),6.40-6.24(m,3H),5.92(dd,J=9.2,4.6Hz,2H),5.79(dd,J=17.7,10.6Hz,1H),5.58-5.51(m,2H),5.44(t,J=9.1Hz,2H),5.38(d,J=2.2Hz,2H),5.18-5.12(m,2H),5.08(s,1H),5.03-4.95(m,4H),4.90(dd,J=14.1,1.9Hz,2H),4.82(s,2H),4.65-4.54(m,10H),4.52(d,J=12.3Hz,2H),4.16(ddd,J=22.6,15.0,8.1Hz,7H),4.07(t,J=9.4Hz,2H),4.01(d,J=4.3Hz,2H),3.93(t,J=6.5Hz,2H),3.78(ddd,J=23.1,15.5,9.1Hz,6H),3.50(dd,J=13.9,4.3Hz,2H),3.38(ddd,J=19.9,13.6,6.8Hz,8H),3.20-3.12(m,1H),3.07-2.95(m,2H),2.18(s,6H),2.08(d,J=8.0Hz,24H),1.99(s,6H),1.82(s,3H),1.79(s,3H),1.69(s,3H),1.61-1.57(m,4H),1.44(s,3H),1.17(t,J=6.9Hz,11H),1.04(t,J=7.0Hz,1H),1.00(s,3H).ESI-MS(m/z)2351.9[M+Na+].
用類似於化合物24的合成方法得到化合物30。1H NMR(600MHz,CD3OD)δ8.16(s,2H),7.89(dd,J=10.5,5.8Hz,1H),7.81(s,1H),7.55-7.48(m,2H),7.06-7.01(m,1H),6.56-6.23(m,6H),5.78(dd,J=17.5,10.8Hz,1H),5.69(d,J=9.2Hz,2H),5.04(s,1H),4.99(d,J=7.9Hz,2H),4.88(s,2H),4.84(d,J=1.1Hz,1H),4.78(d,J=5.2Hz,2H),4.60(s,1H),4.55(s,1H),4.51(d,J=20.7Hz,6H),4.46(d,J=7.6Hz,2H),4.05(t,J=8.9Hz,2H),3.91(s,4H),3.87(d,J=3.0Hz,2H),3.84-3.81(m,3H),3.80(s,1H),3.78(d,J=8.6Hz,3H),3.74(dd,J=15.4,7.6Hz,9H),3.67-3.64(m,2H),3.63-3.60(m,2H),3.55(dd,J=9.7,3.1Hz,2H),3.46(s,2H),3.35(dd,J=13.6,6.6Hz,8H),2.99(s,2H),1.98-1.92(m,2H),1.66(s,3H),1.60-1.49(m,3H),1.46-1.36(m,3H),1.14(t,J=7.1Hz,11H),1.03(t,J=7.1Hz,1H),0.98(s,3H).13C NMR(151MHz,CD3OD)δ170.47,169.04,153.84,153.31,149.93,149.06,148.71,147.22,144.69,144.48,132.86,130.46,128.37,128.26,124.04,123.64,123.17,123.12,122.56,111.95,111.62,109.26,108.20,104.65,103.75,97.63,87.87,78.49,78.13,75.69,75.44,73.41,72.26,71.18,69.67,68.96,68.12,67.69,65.39,63.97,63.79,61.19,60.22,59.76,53.68,52.38,46.07,44.03,42.04,39.58,39.39,32.79,26.80,24.04,15.74,11.63.ESI-MS(m/z)1740.8[M+H+].HRMS(MALDI)calcd for C84H118N13O27:[M+H+]1740.8255,found 1740.8255.
螢光測試
將目標化合物配成2.5×10-4mol/L的溶液,進行螢光測試。
Britton-Robinson緩衝溶液的配製:在磷酸、硼酸、醋酸各樣品濃度均為0.04mol/L的100mL混合液中,加入不同體積0.2mol/L的NaOH溶液,分別配成pH為:2.31、3.25、3.93、4.35、4.81、5.15、5.74、6.25、6.40、6.82、7.19、7.5的Britton-Robinson緩衝溶液。
pH響應的螢光測試:先螢光光譜儀的參數設置為:激發波長為565nm,掃描範圍是575-700nm,掃描速度為中速,採樣間隔為1.0,激發波長的狹縫為3nm,發射波長的狹縫為1.5nm,響應時間為自動。然後將配好的測試溶液再次搖勻後,取4mL放入螢光池中開始測試。
如圖1所示,本發明的目標化合物為羅丹明衍生物,具有類似的螢光性能。在pH為4.5-5.5的範圍內pH越小螢光強度越強,說明本發明合成的螢光探針是潛在的腫瘤細胞內響應pH的螢光開關探針,可用於監測細胞pH的變化。
生物活性測試
應用presto blue試劑測定本發明糖基1,2,3-三唑β-欖香烯衍生物對肝癌細胞生長的抑制作用進行初步評價。具體實驗步驟如下:
(1)細胞培養基的配製:DMEM培養基含10%滅活胎牛血清和1%青黴素/鏈黴素。
(2)細胞的培養:分別將HepG2細胞接種於細胞培養基中,於37℃,5%CO2培養箱中培養。
(3)化合物樣品的配製:將化合物用DMSO溶解,使其濃度為10mM。用細胞培養基稀釋到合適濃度進行細胞活性測試。
(4)測定化合物樣品對腫瘤細胞生長的抑制作用
將人肝癌細胞株HepG2用胰酶消化,用培養基稀釋到5×104/mL,加到96孔板中,每孔100μL,放置於37℃、5%CO2培養箱中培養24小時。棄去原培養基,每孔加入含化合物樣品的培養基每孔100μL,放置於37℃、5%CO2培養箱中培養48小時。在細胞培養板中每孔加入10μL presto blue,在37℃、5%CO2培養箱孵育2小時,用酶標儀在570nm和600nm處測定吸光度,計算化合物樣品的IC50,其中欖香烯作為陽性對照,IC即測定結果如表1所示:
表1化合物生物活性測試結果
由上表可見,本發明的化合物10、14、24和30具有優良的抗肝癌活性,其效果優於欖香烯,具有較好的應用前景。
綜上所述,本發明提供了三類可實時監控治療腫瘤的糖基1,2,3-三唑β-欖香烯衍生物,該類化合物在醫藥技術領域實現實時監控治療腫瘤的研究與應用具有重要的科學意義。
