一種利用大孔吸附樹脂分離純化5‑氨基戊酸的方法與流程
2023-08-10 13:55:21 3
本發明屬於生物化學領域,具體涉及一種以大孔吸附樹脂分離生物轉化液中5-氨基戊酸的方法。
背景技術:
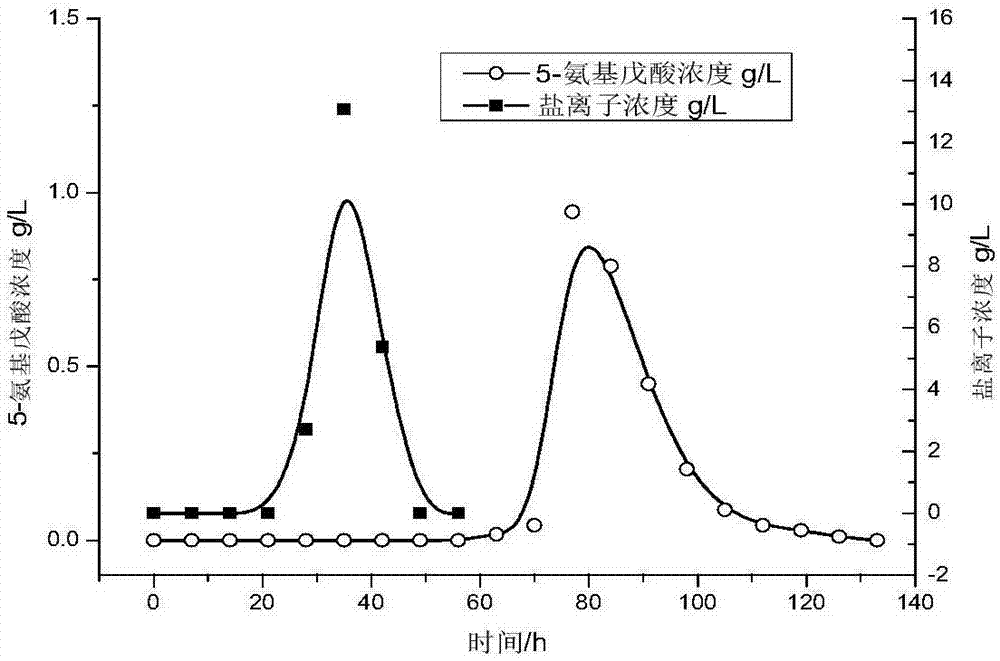
:尼龍是一種非常重要的工程材料,其單體聚醯胺多由石油化學法生產。因此,生物衍生化學品作為環境友好型材料有巨大的潛能去替代化石原料。5-氨基戊酸作為一種生物衍生化學品可用於合成尼龍5的戊內醯胺。除此之外,5-氨基戊酸作為一種c5平臺化合物還可用於合成戊二酸、戊二醇、5-戊酸等。目前已報導的5-氨基戊酸的生物合成途徑主要有三種:酶催化途徑,全細胞催化途徑和發酵途徑。aliakseiv.pukin,caimeng.boeriu等報導的通過酶催化途徑得到的5-氨基戊酸轉化液為ph7.8的nh4hco3溶液,轉化液中還含有少量的底物賴氨酸和產物5-氨基戊酸;xinwang,peipeicai等報導的利用全細胞催化的方法得到的5-氨基戊酸轉化液中含有大約14g/l的磷酸鹽緩衝溶液,大約2g/l的硫酸鹽,剩餘少量的賴氨酸和葡萄糖;sijaepark1,younghoonoh等報導的由發酵法得到的5-氨基戊酸發酵液中含有大約10g/l的磷酸鹽,大約16g/l的硫酸鹽,少量剩餘的葡萄糖和賴氨酸;sijaepark1,younghoonoh等報導利用分離γ-氨基丁酸的方法,通過離子交換樹脂分離5-氨基戊酸,其方法要經過絮凝過濾除菌體,大孔吸附樹脂脫色,最後通過離子交換樹脂分離5-氨基戊酸。其給出的方法較模糊,而且沒有給出回收率和純度等數據。但是,不管由何種途徑得到的5-氨基戊酸轉化液中都含有大量的鹽離子,離子交換樹脂會吸附鹽離子,這極大地降低離子交換樹脂對目標產物的吸附,並影響目標產物的純度。大孔吸附樹脂具有顆粒度均勻,再生容易等特點,因此其在分離方面的應用十分廣泛。但是,利用大孔吸附樹脂分離5-氨基戊酸的方法至今未見報導。技術實現要素:本發明的目的就在於提供一種以大孔吸附樹脂分離生物轉化液中5-氨基戊酸的方法,該方法可以從轉化液中回收90%純度達99.9%的5-氨基戊酸,並且適用於分離由任何途徑轉化得到的5-氨基戊酸轉化液,分離操作簡單便捷,分離效果顯著,樹脂再生容易。為了達到上述目的,本發明的技術方案為:一種利用大孔吸附樹脂分離純化5-氨基戊酸的方法,包括如下步驟:1)將5-氨基戊酸轉化液通過預處理好的大孔吸附樹脂柱進行吸附;2)達到吸附平衡後,用純水洗脫大孔吸附樹脂柱,直到沒有物質洗脫下來後,換用鹽酸進行洗脫;3)將步驟2)中純水洗脫液進行減壓濃縮後再經乙醇重結晶,得到5-氨基戊酸;將鹽酸洗脫液進行減壓濃縮得到5-氨基戊酸鹽酸鹽酸和l-賴氨酸鹽酸鹽的混合物。步驟1)中所述的5-氨基戊酸轉化液來源於酶催化過程、全細胞催化過程或者發酵過程。上述過程得到的5-氨基戊酸轉化液經離心,除去99%的菌體及蛋白,留上清溶液,上清液中可以含有緩衝鹽和其他少量的金屬鹽離子,底物l-賴氨酸,產物5-氨基戊酸以及少量的糖和蛋白。由於大孔吸附樹脂不吸附鹽離子的特性,因此不管由何種途徑得到的5-氨基戊酸轉化液都可以選擇大孔吸附樹脂分離回收轉化液中的各組分。步驟1)中所述的大孔吸附樹脂為非極性樹脂或弱極性樹脂。步驟1)中大孔吸附樹脂的預處理包括以下步驟:用乙醇浸泡24h後,以2bv/h的流速通過樹脂柱,至流出的液體不再渾濁為止,相同流速下,用純水洗至無醇;用1m的鹽酸浸泡4-5h,同樣流速下衝洗至流出液無色,然後用純水洗至中性;用1m的naoh浸泡4-5h,同樣流速下衝洗至流出液無色,然後用純水洗至中性。步驟1)中5-氨基戊酸轉化液上柱的濃度為10g/l-90g/l,上樣流速為0.34bv/h-1.35bv/h,吸附溫度為60℃-80℃。步驟2)中純水洗脫的流速為0.68bv/h-1.35bv/h,洗脫溫度與吸附溫度相同,鹽酸洗脫的濃度為0.5m-2m,流速為0.68bv/h-1.35bv/h,洗脫溫度同吸附溫度。所述弱極性樹脂包括ax-1,ax-13等樹脂,非極性樹脂包括hd-4,mr-8,mr-5等樹脂。優選ax-1樹脂。步驟3)中得到的5-氨基戊酸鹽酸鹽和l-賴氨酸鹽酸鹽的混合物,可以再次作為底物用於5-氨基戊酸的生產。本發明中純水和鹽酸能夠將吸附的5-氨基戊酸和l-賴氨酸完全解析,樹脂再生時只要用純水將樹脂柱洗至中性即可,再生方便。大孔吸附樹脂柱的再生包括以下步驟:先用1m的鹽酸通過樹脂柱至流出液不含任何其他組分,相同流速下,用純水洗至流出液為中性即可。目前市售的5-氨基戊酸的最高濃度為98%,本方法可以使5-氨基戊酸的純度達到99%以上,更優的純度可以達到99.9%,分離效果顯著,操作簡單。有益效果:本發明利用大孔吸附樹脂柱對5-氨基戊酸轉化液進行分離純化,可以回收70%-90%的5-氨基戊酸、10%-30%的5-氨基戊酸鹽酸鹽以及100%的回收賴氨酸鹽酸鹽,分離的5-氨基戊酸純度達99%以上,純水和鹽酸已經將吸附的5-氨基戊酸和l-賴氨酸完全解析,樹脂再生時只要用純水將樹脂柱洗至中性即可,再生方便。附圖說明圖1不同樹脂對5-氨基戊酸和l-賴氨酸的吸附情況;圖260℃下水洗色譜峰;圖360℃鹽酸洗色譜峰;圖480℃水洗色譜峰;圖580℃穿透曲線。具體實施方式實施例1樹脂的選擇1.樹脂預處理:將ax-1,ax-13,mr-5,hd-4,mr-8等樹脂裝柱,乙醇浸泡24h後,以2bv/h的流速通過樹脂柱,至流出的液體不再渾濁為止,相同流速下,換用純水洗至無醇;用1m的鹽酸浸泡4-5h,同樣流速下衝洗至流出液無色,換用純水洗至中性;用1m的naoh浸泡4-5h,同樣流速下衝洗至流出液無色,換用純水洗至中性,50℃下烘乾待用。2.5-氨基戊酸模擬液的配置:按照5-氨基戊酸轉化液中主要組分的濃度配置模擬液:以5-氨基戊酸與l-賴氨酸的質量比大約為25:1的比例稱取5-氨基戊酸標準品和l-賴氨酸標準品,溶於磷酸鹽緩衝液中,配置成25g/l的5-氨基戊酸和1g/l的l-賴氨酸溶液。3.靜態吸附進行樹脂的篩選:分別量取預處理過的吸附樹脂各1g和配置的5-氨基戊酸模擬液10ml,於100ml的錐形瓶中,室溫下150rpm振蕩12h。4.數據與分析:分別計算上述樹脂對5-氨基戊酸與l-賴氨酸的選擇吸附性,數據結果如圖1所示。ax-1樹脂對l-賴氨酸的分配係數最大,對5-氨基戊酸的分配係數較小,可見ax-1樹脂對l-賴氨酸強吸附,對5-氨基戊酸弱吸附,這樣就可以將5-氨基戊酸與l-賴氨酸分離開。因為ax-1樹脂對5-氨基戊酸弱吸附,因此可以考慮用水做洗脫劑。所以,實驗選擇ax-1樹脂為分離5-氨基戊酸的最優樹脂。實施例260℃下ax-1樹脂分離5-氨基戊酸1.樹脂預處理:將ax-1樹脂裝柱,乙醇浸泡24h後,以2bv/h的流速通過樹脂柱,至流出的液體不再渾濁為止,相同流速下,換用純水洗至無醇;用1m的鹽酸浸泡4-5h,同樣流速下衝洗至流出液無色,換用純水洗至中性;用1m的naoh浸泡4-5h,同樣流速下衝洗至流出液無色,換用純水洗至中性,純水浸泡並加熱到60℃,超聲處理30min,60℃裝柱,柱子高徑比40:1。2.5-氨基戊酸轉化液的製備與前處理按照xinwang,peipeicai等報導的全細胞催化的方法生產5-氨基戊酸。轉化液於8000rpm下,離心10min,除去轉化液中的菌體和蛋白。轉化液中的其他成分經測定後見表1。表1:組分含量(g·l-1)5-氨基戊酸25l-賴氨酸1蛋白0.012鹽離子21還原糖0.0173.上樣與洗脫:取上述得到的5-氨基戊酸轉化液10ml,流速0.68bv/h上柱,相同流速下,用60℃沸騰過的純水先進行洗脫,由自動接液器每隔10min接一管樣品,直到檢測到流出液中沒有任何物質時,相同流速下,換用60℃,0.5m的鹽酸進行洗脫,由自動接液器每隔10min接一管樣品,直到流出液中不含任何物質停止接樣。4.樹脂的再生:停止接樣後,相同流速下,換用1m的鹽酸溶液衝洗柱子2-3h,然後改用60℃沸騰過的純水衝洗至中性即可。5.實驗數據與結果分析:對每一管樣品測定其鹽離子濃度,5-氨基戊酸濃度,l-賴氨酸濃度,並以時間為橫坐標,物質濃度為縱坐標繪製物質的流出色譜峰,計算水對5-氨基戊酸的解析率為80.5%。鹽酸對5-氨基戊酸的解析率為18.9%,賴氨酸的解析率為99%。可見,通過水和鹽酸的洗脫可以將5-氨基戊酸與l-賴氨酸完全洗脫下來。水洗脫的色譜峰如圖2所示,經計算,鹽離子與5-氨基戊酸的分離度為1.43。鹽酸洗脫的色譜峰如圖3所示,可見鹽酸可以將5-氨基戊酸與l-賴氨酸同時洗脫下來。6.產品的濃縮:對純水洗脫部分進行減壓蒸餾,得微黃色固體,加入10ml水溶解後,再加入100ml乙醇結晶抽濾,50℃下烘乾,得純度99.9%的5-氨基戊酸0.19g,總收率78%。鹽酸洗脫部分經減壓濃縮後可以再次作為生產5-氨基戊酸的原料。實施例380℃下ax-1樹脂分離5-氨基戊酸1.樹脂預處理:將ax-1樹脂裝柱乙醇浸泡24h後,以2bv/h的流速通過樹脂柱,至流出的液體不再渾濁為止,相同流速下,換用純水洗至無醇;用1m的鹽酸浸泡4-5h,同樣流速下衝洗至流出液無色,換用純水洗至中性;用1m的naoh浸泡4-5h,同樣流速下衝洗至流出液無色,換用純水洗至中性,純水浸泡並加熱到80℃,超聲處理30min,80℃裝柱,柱子高徑比40:1。2.5-氨基戊酸轉化液的製備與前處理按照aliakseiv.pukin,caimeng.boeriu等報導的酶催化的方法生產5-氨基戊酸。將轉化液於8000rpm下,離心10min,除去轉化液中的菌體和蛋白。轉化液中的其他成分經測定後見表2。表2:組分含量(g·l-1)5-氨基戊酸29l-賴氨酸1蛋白0.012鹽離子28還原糖0.0173.上樣與洗脫:取上述得到的5-氨基戊酸轉化液10ml,其中5-氨基戊酸的濃度為29g/l,l-賴氨酸的濃度大約為1g/l。流速0.68bv/h上柱,相同流速下,用80℃沸騰過的純水先進行洗脫,由自動接液器每隔10min接一管樣品,直到檢測到流出液中沒有任何物質時,相同流速下,換用80℃,0.5m的鹽酸進行洗脫,由自動接液器每隔10min接一管樣品,直到流出液中不含任何物質停止接樣。4.樹脂的再生:停止接樣後,相同流速下,換用1m的鹽酸溶液衝洗柱子2-3h,然後改用80℃沸騰過的純水衝洗至中性即可。5.實驗數據與結果分析:對每一管樣品測定其鹽離子濃度,5-氨基戊酸濃度,l-賴氨酸濃度,並以時間為橫坐標,物質濃度為縱坐標繪製物質的流出色譜峰,計算水對5-氨基戊酸的解析率為92.1%。鹽酸對5-氨基戊酸的解析率為7.1%,賴氨酸的解析率為99.1%,可見,通過水和鹽酸的洗脫可以將5-氨基戊酸與l-賴氨酸完全洗脫下來。水洗脫的色譜峰如圖4所示,經計算,鹽離子與5-氨基戊酸的分離度為0.89。6.產品的濃縮:對純水洗脫部分進行減壓蒸餾,得微黃色固體,加入10ml水溶解後,再加入100ml乙醇結晶抽濾,50℃下烘乾,得純度99.9%的5-氨基戊酸0.24g,總收率83%。鹽酸洗脫部分經減壓濃縮後可以再次作為生產5-氨基戊酸的原料。ax-1樹脂可以很好的分離來自全細胞催化和酶催化的5-氨基戊酸轉化液。其中酶催化得到的5-氨基戊酸的解析率較高,這歸因於較高的吸附解吸溫度。為了提高5-氨基戊酸的解吸率,吸附解吸溫度優選為80℃。實施例4ax-1樹脂動態分離5-氨基戊酸。1.樹脂預處理:將ax-1樹脂裝柱乙醇浸泡24h後,以2bv/h的流速通過樹脂柱,至流出的液體不再渾濁為止,相同流速下,換用純水洗至無醇;用1m的鹽酸浸泡4-5h,同樣流速下衝洗至流出液無色,換用純水洗至中性;用1m的naoh浸泡4-5h,同樣流速下衝洗至流出液無色,換用純水洗至中性,純水浸泡並加熱到80℃,超聲處理30min,80℃裝柱,柱子高徑比40:1。2.上樣吸附:取實施例2全細胞催化途徑得到的5-氨基戊酸轉化液1000ml,其中5-氨基戊酸的濃度為25g/l,l-賴氨酸的濃度大約為1g/l。流速0.68bv/h通過柱子,由自動接液器每隔10min接一管樣品,直到檢測到流出液中得濃度與原液濃度相同時,停止吸附。3.洗脫:相同流速下,換用80℃純水,由自動接液器每隔10min接一管樣品,直到流出液中不含任何物質時,換用0.5m的鹽酸進行洗脫,同樣由自動接液器每隔10min接樣一次,直到流出液中不含有任何物質時停止接樣。4.樹脂的再生:停止接樣後,相同流速下,換用1m的鹽酸溶液衝洗柱子2-3h,然後改用80℃沸騰過的純水衝洗至中性即可。5.產品的檢測與結果分析:在吸附過程中,測量了流出液中吸附質濃度隨時間的變化曲線(穿透曲線),如圖4所示。由穿透曲線知5-氨基戊酸大約在70min時開始穿透,l-賴氨酸大約在190min開始穿透,這也說明,ax-1樹脂對l-賴氨酸的吸附能力大於對5-氨基戊酸的吸附能力,因此,5-氨基戊酸可以被水洗脫而l-賴氨酸需要由鹽酸洗脫。經計算ax-1樹脂對5-氨基戊酸的最大吸附量為107mg/g,對l-賴氨酸的最大吸附量為13mg/g。80℃純水對5-氨基戊酸的解析率為91.2%,0.5m的鹽酸對5-氨基戊酸的解析率為8.2%,對l-賴氨酸的解析率為99.8%,可見,純水和0.5m的鹽酸已經將吸附的5-氨基戊酸與l-賴氨酸全部洗脫。當前第1頁12
