金黃色葡萄球菌分選酶A高效突變體的製作方法
2023-09-20 23:57:25 7
本發明涉及生物工程領域的蛋白酶定向進化,特別涉及通過構建高通量的篩選平臺,進化得到了金黃色葡萄球菌分選酶A的突變體,其可以高效的催化LPXTG與α-Gly或α-Glyn之間的連接反應。
背景技術:
金黃色葡萄球菌分選酶A(Sa-SrtA)是革蘭氏陽性菌中普遍存在的一類半胱氨酸轉肽酶,典型的,其可以催化底物LPXTG(X代表任意胺基酸)與α-Glyn(寡聚甘氨酸)之間的連接反應,這一反應因此被命名為分選酶介導的連接反應(Sortase-Mediated Ligation,SML)。同時,分選酶A還可以催化LPXTG與α-Gly之間的反應,然而,相對於其催化α-Glyn的反應,反應活性更低。
利用分選酶介導的連接反應,可以實現各種蛋白質的定點標記與偶合,進而應用於生命科學的基礎研究以及製藥行業。然而,由於野生型分選酶A催化效率較低,基於高通量篩選的定向進化以及理性設計的方法提升分選酶A的活性成為一種必要。前人的研究中也發現了5個點突變P94R/D160N/D165A/K190E/K196T(Chen I.et al.ProcNatl AcadSci USA 2011,108,11399-11404),可以在一定程度上提升其活性。
野生型金黃色葡萄球菌分選酶A是一個包含206個胺基酸殘基的蛋白酶,是在前人的研究中發現,截掉氮端25個胺基酸殘基的截短體可以在大腸桿菌中高水平、可溶性的表達(Ton-That H.et al.ProcNatl AcadSci USA 1999,96,12424–12429),因此在研究中分選酶A基本上都以這種截短體的形式存在,本發明涉及的高效突變體描述的也是這種截短體的突變體。
技術實現要素:
本發明的技術目的是提供催化LPXTG與α-Gly反應活性更高的金黃色葡萄球菌分選酶A突變體,同時這些突變體也可以進一步提升LPXTG與α-Glyn之間反應的活性。本發明構建了基於兩個螢光蛋白的螢光共振能量轉移的篩選平臺,以野生型金黃色葡萄球菌分選酶A及其P94R/D160N/D165A/K190E/K196T突變體分別作為出發分選酶1和2,分別進行了定向進化和理性設計,最終構建得到活性更高的分選酶A突變體,使其可以更好的催化LPXTG與α-Gly或α-Glyn之間的連接反應。
本發明得到的分選酶A突變體既可以提升已知分選酶A催化LPXTG與非典型底物α-Gly之間反應的效率,同時又可以提升其催化LPXTG與典型底物α-Glyn之間反應的效率。
本發明所獲得的分選酶A突變體活性的提高,以測定的動力學常數Kcat,KmLPETG和KmGGG或KmGAG進行表徵,其中,Kcat代表反應的速率,KmLPETG、KmGGG和KmGAG分別代表酶對底物LPETG、GGG和GAG的識別效率。
具體的,本發明所提供的分選酶A突變體包含下述突變中的一種或多種:D124G、Y187L、E189R和F200L。
本發明提供的分選酶A突變體還可以包含下述突變中的一種或多種:P94R、D160N、D165A、K190E和K196T。
本發明優選的分選酶A突變體是下述突變體之一:
突變體1:P94R/D124G/D160N/D165A/K190E/K196T
突變體2:P94R/D160N/D165A/Y187L/E189R/K190E/K196T
突變體3:P94R/D124G/D160N/D165A/Y187L/E189R/K190E/K196T
突變體4:D124G/Y187L/E189R/F200L
突變體5:P94R/D124G/D160N/D165A/Y187L/E189R/K190E/K196T/F200L
下面的表1給出了野生型分選酶A已知突變體P94R/D160N/D165A/K190E/K196T(出發分選酶2)及突變體4和5催化LPXTG與α-Gly的連接反應的動力學常數Kcat,KmLPETG和KmGAG;表2給出了野生型分選酶A、出發分選酶2及上述五種突變體催化LPXTG與α-Glyn的連接反應的動力學常數Kcat,KmLPETG和KmGGG,以Kcat/KmLPETG指示催化效率,可以看出各個突變體的效率都有大幅度的提升。
表1
表2
本發明通過定向進化和理性設計相結合的方法構建得到催化活性提高的分選酶A突變體,由野生型金黃色葡萄球菌分選酶A的基因(GenBank登錄號:BA000018,ORFID:SA2316)及一種已知突變體(P94R/D160N/D165A/K190E/K196T)的基因出發,運用易錯PCR和位點飽和突變得到分選酶A突變文庫,再利用構建的基於螢光共振能量轉移的篩選平臺,經過多輪的篩選以及突變的整合得到一系列進化的分選酶A突變體,在突變的胺基酸序列中包含了D124G,Y187L,E189R,F200L和已知突變中的一個或多個突變。
本發明實施例在原核表達系統中表達的分選酶A及其突變體是其截去氮端25個胺基酸殘基的截短體形式,其中:包含有6個突變位點的分選酶A突變體1的胺基酸序列如序列表中SEQ ID NO.1所示;包含有7個突變位點的分選酶A突變體2的胺基酸序列如序列表中SEQ ID NO.2所示;包含有8個突變位點的分選酶A突變體3的胺基酸序列如序列表中SEQ ID NO.3所示;包含有4個突變位點的分選酶A突變體4的胺基酸序列如序列表中SEQ ID NO.4所示;包含有9個突變位點的分選酶A突變體5的胺基酸序列如序列表中SEQ ID NO.5所示。序列表中SEQ ID NO.1至SEQ ID NO.5均各自包含181個胺基酸殘基,對應於野生型金黃色葡萄球菌分選酶A的第26至206位胺基酸殘基序列,上述突變位點也是相對於全長野生型金黃色葡萄球菌分選酶A而言。
序列表中SEQ ID NO.1至SEQ ID NO.5所示胺基酸序列對應的基因序列依次可以分別如SEQ ID NO.6至SEQ ID NO.10所示,當然,根據密碼子的簡併性,也可以是利用同一胺基酸的不同密碼子而獲得的編碼相同蛋白質的其他核苷酸序列。
含有這些基因序列的載體、細胞和宿主菌也在本發明的保護範圍內。
本發明利用構建的篩選平臺,對通過易錯PCR及位點飽和突變的方法構建的金黃色葡萄球菌分選酶A的基因突變文庫進行了高通量篩選,得到了催化效率有很大提高的突變體,其催化LPXTG與典型底物α-Glyn以及非典型底物α-Gly的效率都有了很大提升。
附圖說明
圖1顯示了基於螢光共振能量轉移原理的分選酶A篩選平臺的構建原理。
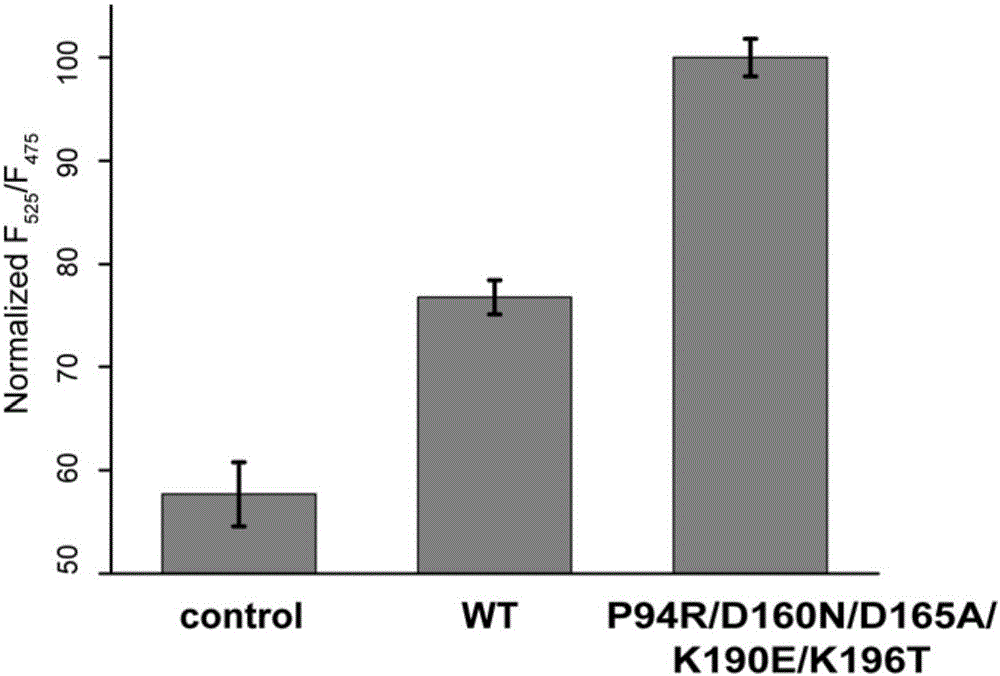
圖2顯示了篩選平臺指示分選酶A活性的效果。
圖3顯示了位點突變對於分選酶A活性的影響。
圖4顯示了野生型及突變體分選酶A催化LPXTG與α-Gly反應的動力學常數Kcat,KmLPETG與KmGAG。
圖5顯示了野生型及突變體分選酶A催化LPXTG與α-Glyn反應的動力學常數Kcat與KmLPETG。
圖6顯示了野生型及突變體分選酶A催化LPXTG與α-Glyn反應的動力學常數KmGGG。
具體實施方式
實施例中涉及的培養基配方如下:
LB液體培養基:蛋白腖1%,酵母提取物0.5%,NaCl 1%,pH7.4。
實施例1、利用易錯PCR構建金黃色葡萄球菌分選酶A隨機突變文庫
利用易錯PCR在體外向金黃色葡萄球菌分選酶A基因引入核苷酸突變,易錯PCR具體條件如下:
PCR模板是包含野生型金黃色葡萄球菌分選酶A基因的質粒,本質粒通過將野生型分選酶A的基因(Ton-That H.et al.ProcNatl AcadSci USA 1999,96,12424–12429)出發,利用亞克隆將第26位到206位的胺基酸序列對應的核苷酸序列克隆入pet28a載體的NdeI和XhoI酶切位點之間得到。
上遊引物:5』-GGAATTCCATATGAAACCACATATCGATAATTATC-3』(SEQ ID NO.11)
下遊引物:5』-GGTAGGCACTCGAGTTATTTGACTTCTGTAGCTAC-3』(SEQ ID NO.12)
PCR擴增條件:95℃5min;95℃1min,55℃1min,72℃1min,30個循環;72℃10min。
易錯PCR擴增產物經PCR產物純化試劑盒純化,限制性內切酶NdeI和XhoI分別對PCR產物和pet28a載體進行酶切,連接,轉化至大腸桿菌DH10B,塗布於含有100μg/mL卡那黴素的LB平板,37℃培養箱生長12小時後,收取全部克隆,稀釋至液體LB培養基中繼續生長,12小時後提取質粒,得到突變文庫。將得到的質粒轉化至大腸桿菌BL21(DE3),37℃培養箱生長12小時後,得到突變文庫的表達菌,待用。
實施例2、點突變PCR構建金黃色葡萄球菌分選酶A位點飽和突變文庫
利用點突變PCR的方法向分選酶A的P94R/D160N/D165A/K190E/K196T突變體的兩個位點Tyr187和Glu189引入飽和突變,PCR條件如下:
PCR模板是出發分選酶2的基因,通過將實施例1中含有野生型分選酶A基因的pet28a質粒突變所得到。
上遊引物:5』-CATTAATTACTTGTGATGATNNKAATNNKGAGACAGGCGTTTGGG-3』(SEQ ID NO.13)
下遊引物:5』-CCCAAACGCCTGTCTCMNNATTMNNATCATCACAAGTAATTAATG-3』(SEQ ID NO.14)
上述引物中,N代表A、C、G、T四種鹼基中的一種,K代表G或T,M代表A或C。
PCR擴增條件:95℃5min;95℃45s,55℃45s,72℃7min,23個循環;72℃10min。
點突變PCR產物經DpnI酶切,轉化於大腸桿菌DMT菌株中,塗布於含有100μg/mL卡那黴素的LB平板,37℃培養箱生長12小時後,收取全部克隆,稀釋至液體LB培養基中繼續生長,12小時後提取質粒,得到雙位點的飽和突變文庫。將得到的質粒轉化至大腸桿菌BL21(DE3),37℃培養箱生長12小時後,得到飽和突變文庫的表達菌,待用。
實施例3、基於螢光共振能量轉移的篩選系統構建及驗證
利用亞克隆的方法分別在pet28a載體上融合表達eGFP-LPETG和G-cpV的螢光蛋白,利用6×His標籤進行純化,純化得到的蛋白進行分選酶介導的連接反應,如圖1所示,EGFP和cpV蛋白是合適的螢光共振能量轉移(FRET)供體和受體,當分選酶A介導兩個蛋白之間的連接反應時,由於兩個蛋白距離的拉近,兩個蛋白之間的螢光共振能量轉移效率提升,分選酶活性越高,則螢光功能能量轉移效率越高。利用野生型分選酶A和出發分選酶2對篩選平臺進行驗證,證明了分選酶A活性與螢光共振能量轉移效率成正比,如圖2所示。
實施例4、高催化活性分選酶A突變體的篩選
挑取實施例1和2構建的基因文庫,在含有1ml LB(含100μg/ml卡那黴素)培養基的深孔96孔板中,37℃搖床中過夜培養,1:100轉接到新的深孔96孔板中,37℃搖床培養至OD600達0.6左右,加入1mM IPTG誘導,37℃繼續培養3小時。4700rmp離心10分鐘,棄上清,每孔加入200μL裂解液(30mM Tris,150mM NaCl,5mM CaCl2,1%Triton X-100,0.15mg/mL溶菌酶),37℃搖床裂解2小時,離心去除細胞碎片,得到細胞裂解液。200μL反應體系中加入50μL細胞裂解液,100μM eGFP-LPETG-His6,200μM G-cpV,37℃反應2小時。利用酶標儀,435nm激發,收取475nm和525nm螢光,通過525nm和475nm螢光強度比值代表不同的螢光共振能量轉移效率,從而得到不同催化效率的突變體。如圖3所示,本發明得到了四個可以提升分選酶A活性的突變,包含D124G,Y187L,E189R和F200L。將這四個突變中的一個或多個突變與出發分選酶2的五個突變進行整合,得到最終的突變體。
實施例5、金黃色葡萄球菌分選酶A活性測定
金黃色葡萄球菌分選酶A活性測定依據文獻的方法(Kruger R.G.;Dostal P;McCafferty D.G.Anal Biochem 2004,326:42–48),不同的是,測定LPXTG與α-Glyn反應的動力學常數,以GGG作為反應底物;測定LPXTG與α-Gly反應的動力學常數,以GAG作為反應底物。如圖4所示,以Abz-LPETGK(Dnp)-CONH2和GAG作為底物進行測定,突變體分選酶A催化LPETG與α-Gly反應的活性(Kcat/KmLPETG)相對於野生型得到了約7~79倍不同的提升,最好的突變體相對於出發分選酶2也有大於5倍的提升,同時其對於GAG的識別(KmGGG)也有1.3倍左右的提升。如圖5和6所示,以Abz-LPETGK(Dnp)-CONH2和GGG作為底物進行測定,可以看出相對於野生型分選酶A,突變體分選酶A催化LPETG與α-Glyn反應的活性(Kcat/KmLPETG)相對於野生型得到了20~245倍不同的提升,最好的突變體相對於出發分選酶2也有近11倍的提升,同時其對於GGG的識別(KmGGG)也有2倍左右的提升。
