一種克隆胚胎處理液及其使用方法以及該處理液的用途與流程
2023-10-10 06:31:09 3
本發明涉及體細胞克隆技術,特別涉及一種克隆胚胎處理液及其使用方法以及該處理液的用途。
背景技術:
體細胞克隆(somaticcellnucleartransfer,scnt),又稱體細胞克隆,是用於生產動物的一種輔助生殖技術。scnt指的是將供體體細胞移植到去核的卵母細胞的細胞質中,通過融合併激活從而獲得重構胚,使細胞恢復分裂,繼續發育得到與供體細胞基因型完全相同的後代。
通過體細胞克隆技術可以將單個分化的體細胞的細胞核在離體環境中培養得到整個生物機體,這對於農業技術、生物醫藥行業、瀕危物種保護來說具有巨大的潛力(yangetal.,2007)。在畜牧業上,可以通過建立優良家畜的細胞系作為核供體進行動物克隆,避免自然條件下選種所受到的動物生育周期和生育效率的限制,使育種年限大大縮短,動物育種的進程隨之加速,促進優良畜群繁育。在生物醫學上,用於克隆家畜和轉基因動物的體細胞克隆技術是非常有價值的(meurensetal.,2012)。克隆幹細胞經誘導分化後,構成相應的組織器官,用於組織或器官移植的供體,或者通過體細胞克隆技術生產轉基因動物作為生產人類藥物蛋白的生物反應器。通過體細胞克隆技術可用於製備基因修飾動物,體細胞克隆技術已成為目前生產基因修飾動物的主要技術手段,特別是轉基因大動物的生產,例如生產表達人α-乳清蛋白的轉基因山羊(fengetal.,2015)和表達綠色螢光蛋白的轉基因豬(hyunetal.,2003)和牛(aratetal.,2001;rosenetal.,1999)。藉助體細胞克隆技術拯救瀕臨滅絕的珍稀物種,可通過冷凍長期保存體細胞,並在需要的時候恢復,這極大提高了保護珍稀物種的簡便性,並且降低了成本,在保護物種多樣性方面發揮了重要作用,而且有望利用該技術增加珍稀物種的存活數量。
現在,對於體細胞去分化重編程為多能性狀態的研究主要集中於如何利用體細胞生產類胚胎幹細胞用於再生性治療。胚胎幹細胞(embryonicstemcell,esc)具有完整的全能性並且可以分化成所有細胞類型(buehretal.,2008;evansetal.,1981),甚至在特定培養條件下分化為胎盤細胞(murakamietal.,2011)。它們高活力的染色質結構(gaspar-maiaetal.,2011)和活躍的染色體轉錄活性(efronietal.,2008)使它們有別於分化的體細胞(meissner,2010)。但是,從更寬廣的層面上說,esc似乎可以看作一種體細胞,因為它們與其它體細胞或移植後的胚胎共有一些重要特徵。由於多能性的esc可以作為體外疾病建模和細胞/組織替代療法有價值的細胞來源(yangetal.,2007),而它可以從體細胞克隆技術中建立(wakayamaetal.,2001),因此,對於人類治療學來說體細胞克隆技術是一種很有前途的技術(hochedlingeretal.,2003)。dahl等(dahletal.,2010)已經證實了在es細胞衍生過程中,其導致組蛋白賴氨酸h3k4三甲基化(h3k4me3)和h3k27三甲基化(h3k27me3)發生明顯變化,強調了表觀遺傳重編程與胚胎幹細胞的衍生有關。正因為這一優勢,使用esc進行體細胞克隆,往往有著較高的克隆效率,但其效率依然不高。
技術實現要素:
本發明的一個目的是提供一種克隆胚胎處理液,另一個目的是提供一種該處理液的使用方法,還有一個目的是提供該處理液的用途。
根據本發明的一個方面,提供了一種克隆胚胎處理液,由bix-01294和pzm培養液構成,pzm培養液中bix-01294的濃度為5nm~500nm;其中,pzm培養液由以下組分組成:
在一些實施方式中,克隆胚胎處理液ph為7.2~7.4,滲透壓為288±2mosm。
在一些實施方式中,bix-01294的濃度為50nm~500nm。
根據本發明的另一個方面,提供了一種上述克隆胚胎處理液的使用方法,包括以下步驟:
(1)收集豬卵巢,放入含有1%雙抗的28-39℃生理鹽水的保溫瓶內,首先用39℃的生理鹽水清洗乾淨,然後用帶18號針頭的10ml注射器抽取直徑為4-6mm卵泡中的卵母細胞,抽取液在39℃水浴鍋中靜置15min,去上清液後加入dpbs重懸,靜置2-3min後去上清液並重複一次,最後在體式顯微鏡下挑選出細胞質均勻、卵丘緻密且包裹2層以上的卵丘細胞-卵母細胞複合體用dpbs和m199成熟培養液分別洗滌3次後,轉入在培養箱中已經平衡2h並覆蓋了胚胎級礦物油的的m199成熟培養液滴內或四孔板內,在39℃,5%co2飽和溼度的培養箱中成熟培養42h。
(2)將成熟培養的所述卵丘細胞-卵母細胞複合體轉移到含透明質酸酶的離心管中,移液器吹打約2min後轉移到30mm培養皿中,用口吸管將脫去卵丘的卵母細胞揀出,洗滌卵母細胞,在體式鏡下挑出帶有第一極體的成熟卵母細胞。
(3)將所述成熟卵母細胞,用外徑100-120μm的固定針,內徑為15-20μm的去核針採用盲吸法去核,具體步驟如下:在65mm無菌培養盤中滴4滴50μl大小的操作液滴,使用石蠟油覆蓋,再將30個左右的卵母細胞和適量的體細胞移入其中,用固定針輕輕固定住卵母細胞,用去核針撥動卵母細胞使極體在大概5點鐘的位置,然後用去核針沿3點位置刺進去,去除極體及附近的胞質,然後把針撤出,將極體和胞質吐出,隨後注入一個大小合適,表面光滑的體細胞,完成胚胎重構過程。重構胚放入胚胎培養液中恢復培養1h;
(4)將所述重構胚分批轉移到融合液中平衡2min後,然後每批5~8個放入已鋪滿融合液的融合槽內,用實心玻璃針撥動重構卵,使供核細胞和受體卵母細胞的細胞膜接觸面與電極平行,施加150v/mm,100μs,2dc的直流電脈衝誘導融合、激活重構胚胎,接著用胚胎培養液洗滌3遍後立即轉入礦物油覆蓋的胚胎培養液中,置於39℃、5%co2、飽和溼度的培養箱中培養。
(5)用培養液洗滌融合的重構胚5遍,轉入預平衡好的培養液中,置於39℃、飽和溼度、低氧條件的培養箱中培養,使用所述克隆胚胎處理液對胚胎進行繼續培養。
在一些實施方式中,上述步驟(5)中的低氧條件是指所述培養箱中的空氣組成為5%o2+5%co2+90%n2。
在一些實施方式中,在上述步驟(5)前還包括以下步驟:
復甦細胞後,待細胞匯合度達到95%以上時,改用不含血清的dmem培養基培養過夜。次日消化,用hn操作液將離心後的細胞重懸吹打均勻,準備克隆。
根據本發明的另一個方面,提供了上述克隆胚胎處理液在降低細胞suv39h1、setdb1、dnmt1或者dnmt3a的基因表達方面的應用。
根據本發明的又一個方面,提供了上述克隆胚胎處理液在下調胚胎早期發育階段的2cell、4cell的h3k9me2水平的應用。
採用以上技術方案的克隆胚胎處理液對克隆胚胎進行培養處理可以達到以下有益效果:
(1)能夠顯著降低細胞suv39h1、setdb1、dnmt1或者dnmt3a的基因表達;
(2)能夠明顯下調胚胎早期發育階段的2cell、4cell的h3k9me2水平。
附圖說明
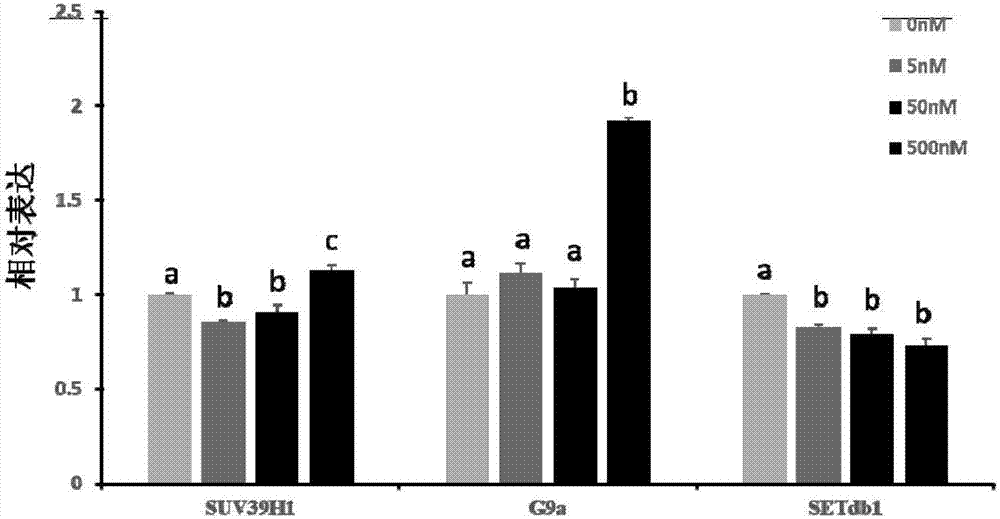
圖1為本發明中克隆胚胎處理液對細胞組蛋白甲基化酶相關基因表達的影響示意圖。
圖2為本發明中克隆胚胎處理液對細胞dna甲基化酶相關基因表達的影響示意圖。
圖3為本發明中克隆胚胎處理液處理組與對照組2cell、4cell免疫螢光結果圖。
圖4為本發明中克隆胚胎處理液對胚胎組蛋白甲基化酶相關基因表達水平示意圖。
圖5為本發明中克隆胚胎處理液對胚胎dna甲基化酶相關基因表達水平示意圖。
具體實施方式
下面結合附圖對本發明作進一步詳細的說明。
實驗材料
1、細胞株和豬克隆胚胎
豬成體成纖維細胞(513d)採自廣東溫氏種豬科技有限公司水臺原種豬場提供的種豬;豬克隆胚胎在廣東溫氏種豬科技有限公司克隆實驗室製備。
2、主要試劑、耗材
rna抽提試劑盒e.z.n.a.totalrnakiti購自omega公司;胚胎rna抽提試劑盒qiagenrneasyplusmicrokit(50)購自qiagen公司;反轉錄試劑盒primescripttmrtreagentkitwithgdnaeraser購自takara公司;實時定量pcr試劑盒sybrselectmastermix購自lifetechnologies公司;普通pcr用taq酶購自廣州東盛生物科技公司;dl500dnamarker購自大連寶生生物工程有限公司;溴化乙錠(ethidiumbromide,eb)購自廣州康龍生物科技有限公司;瓊脂糖購自invitrogen公司;dmem、胎牛血清(fetalbovineserum,fbs)、0.25%胰蛋白酶購自gibco公司;bix-01294購自sigma公司;各種細胞培養用的培養皿、培養板購自corning公司;15ml和50ml離心管購自excell公司;各種規格的dnase&rnase-free帶濾芯吸頭及pcr管購自axygen公司;胚胎注射級水購自sigma公司;組蛋白h3k9me2及h3k9me3免疫螢光所用抗體購自abcam生物公司;mtt購自thermo公司;dapi購自cellsignaling科技公司;q-pcr引物由金唯智生物科技有限公司合成。
3、主要溶液配置
3.1細胞凍存液:60%dmem+30%fbs+10%dmso.
3.2卵母細胞成熟培養液配方(m199):
tcm199+10%pff+10%fbs+10iu/mlhcg+10iu/mlecg+0.1mg/mll-半胱氨酸+10ng/mlegf,現配現用。
3.3顯微操作液(hm)配方:
0.7696gnacl,0.0168gnahco3,0.0356gkc1,0.0162gkh2po4,0.0293gmgso4·7h2o,0.1g葡萄糖,0.0146g穀氨醯胺,0.1501g牛磺酸,0.2383ghepes,0.4gbsa,0.0065g青黴素,0.0050g鏈黴素,sigmah2o溶解定容至100ml。將上述成分按順序加入混勻。調ph至7.2~7.4,滲透壓為270~290mosm,0.22μm濾器過濾分裝,4℃保存備用。
3.4hoechst33342配方:10ml純水溶解100mg,濃度為10mg/ml,-20℃凍存。
4、主要儀器設備
微量核酸濃度儀(nanodrop2000,thermo,美國)
定量pcr儀(ecotm,illumina,美國)
微量移液器(eppendorf,德國)
電熱恆溫水浴鍋(dk-s24,上海森信實驗儀器有限公司)
pcr儀(杭州博日科技有限公司,中國)
水平電泳槽及電泳儀(北京市六一儀器廠,中國)
凝膠成像系統(uvp,美國)
-80℃超低溫冰箱(thermo,美國)
超淨工作檯(蘇州安泰空氣技術有限公司,中國)
milli-q超純水純化系統(millipore公司,美國)
centrifuge5810r低溫離心機(eppemdorf,德國)
forma3111、3131二氧化碳培養箱(thermo,美國)
te300和te2000u倒置顯微鏡(nikon,日本)
顯微操作儀(narishige,日本)
體視顯微鏡配套熱臺(tokai,日本)
電熱恆溫鼓風乾燥箱:森信實驗儀器有限公司,上海
體視熱臺:東海公司(tokai),日本
拉針儀,pn-30,narishige,日本
微斷儀,mf900,narishige,日本
研磨儀,eg-400,narishige,日本
磁力攪拌器:海門市其林貝爾儀器製造有限公司,上海
電子分析天平:ac11.4,賽多利斯科學儀器(北京)有限公司,中國
5、分析軟體及網站
pcr引物設計及分析軟體:primerpremier5.0,genetool
dna序列資料庫:ncbi/genbank/nucleotide/ucsc/ensembl
圖片處理:photoshop7.0/acdsee9.0
凝膠成像系統軟體:biocaptmw
基因分析軟體:mega5.05
實驗方法
1、反轉錄及定量pcr
將細胞rna進行反轉錄得到cdna,具體實驗方法參照翻轉錄試劑盒takarareversetranscriptionkit說明書進行。冰上解凍細胞rna,同時在室溫(15-25℃)條件下解凍反轉錄試劑;去除基因組dna,按表1成分於冰上配製反應混合液,為了保證反應混合液準備的充分性,在配製時應按反應數+2的量進行mastermix的配製,在42℃條件下保溫2min。
表1去除基因組dna反應體系
再進行反轉錄反應。按照表2配製反應體系,所有操作均在冰上進行。
表2rna反轉錄反應體系
反應程序:7℃,15min;85℃,5s。在pcr儀上進行反應。反應結束後將反轉錄產物4℃短暫保存,-20℃長期保存或進行定量rt-pcr檢測。
表3實時定量pcr反應體系
實時定量pcr採用lifetechnologies公司的定量反應試劑盒(sybrselectmastermix)進行實驗,反應體系為10ul(見上述表3),每次3-4個技術重複。pcr反應程序為:95℃預變性、熱啟動5min;45~50輪pcr循環(95℃、10s,60℃、15s,72℃、20s);溶解曲線(95℃、15s,55℃、15s,95℃、15s)。定量引物見表4。
表4定量pcr引物設計
2、數據處理及統計分析
基因相對表達數據分析中,各基因ct值經過內參基因(β-actin)和對照樣品正態化處理後,用2-△△ct方法計算相對表達量。具體做法是將每組樣品目的基因ct均值減去內參基因ct均值得到△ct值,將其中一組樣品△ct值作為參照,將其它處理樣品△ct值減去參照組樣品△ct值得到各組樣品的△△ct值,最後將每個處理樣品相對參照組樣品的目的基因表達量用2-△△ct表示。採用spss17.0進行數據處理,利用卡方檢驗進行顯著性檢驗。概率值p<0.05時,平均值顯著差異。
一、克隆胚胎處理液對豬成體成纖維細胞克隆及其早期胚胎發育能力比較實驗
pzm培養液(胚胎培養液)的配製:
取200mlsigmah2o,按順序加入以下成分:3.156gnacl,1.053gnahco3,0.373gkc1,0.024gkh2po4,0.049gmgso4·7h2o,0.308g乳酸鈣,0.011g丙酮酸鈉,0.073gl-穀氨醯胺,0.273g亞牛磺酸,10mlbme,5mlmem,0.033g青黴素,0.025g鏈黴素,混勻後調節ph為7.2~7.4,滲透壓為288±2mosm,定容至500ml,4℃保存備用。
稱取計算量的bix-01294鹽酸鹽添加到pzm培養液溶解後,即可得到克隆胚胎處理液。
1、卵母細胞的收集及體外成熟培養
從屠宰收集豬卵巢,放入含有1%雙抗的28-39℃生理鹽水的保溫瓶內,4h內送回實驗室。首先用39℃的生理鹽水清洗乾淨,然後用帶18號針頭的10ml注射器抽取直徑為4-6mm卵泡中的卵母細胞,抽取液在39℃水浴鍋中靜置15min,去上清液後加入dpbs重懸,靜置2-3min後去上清液並重複一次。在體式顯微鏡下挑選出細胞質均勻、卵丘緻密且包裹2層以上的卵丘細胞-卵母細胞複合體(cumulusoocytecomplexes,cocs),用dpbs和m199成熟培養液分別洗滌3次後,轉入在培養箱中已經平衡2h並覆蓋了胚胎級礦物油的的m199成熟培養液滴內或四孔板內。39℃,5%co2飽和溼度的培養箱中成熟培養42h。
2、去除顆粒細胞
將成熟培養的cocs轉移到含透明質酸酶的離心管中,移液器吹打約2min後轉移到30mm培養皿中,用口吸管將脫去卵丘的卵母細胞揀出。洗滌卵母細胞,在體式鏡下挑出帶有第一極體的成熟卵母細胞備用。
3、供體細胞的預處理
為了提高重構胚的融合率,需對供體細胞做血清飢餓和接觸抑制處理。復甦細胞後,待細胞匯合度達到95%以上時,改用不含血清的dmem培養基培養過夜。次日消化,用hn操作液將離心後的細胞重懸吹打均勻,準備克隆。
4、豬成體成纖維細胞克隆
挑選已排出第一極體且形態良好的卵母細胞,用外徑100-120μm的固定針,內徑為15-20μm的去核針採用盲吸法去核。具體步驟如下:在65mm無菌培養盤中做4滴50μl大小的操作液滴中,石蠟油覆蓋,將30個左右的卵母細胞和適量的體細胞移入其中,用固定針輕輕固定住卵母細胞,用去核針撥動卵母細胞使極體在大概5點鐘的位置。然後用去核針沿3點位置刺進去,去除極體及附近的胞質,然後把針撤出,將極體和胞質吐出,隨後注入一個大小合適,表面光滑的體細胞,完成胚胎重構過程。重構胚放入胚胎培養液中恢復培養1h。
將恢復培養1h的重構胚分批轉移到融合液中平衡2min後,用融合/激活液洗滌3遍,然後每批5~8個放入已鋪滿融合液的融合槽內,用拉制的、極細的實心玻璃針撥動重構卵,使供核細胞和受體卵母細胞的細胞膜接觸面與電極平行,施加150v/mm,100μs,2dc的直流電脈衝誘導融合、激活重構胚胎,接著用胚胎培養液洗滌3遍後立即轉入礦物油覆蓋的胚胎培養液中,置於39℃、5%co2、飽和溼度的培養箱中培養,4h後在體視顯微鏡下判定融合情況並計算融合率。
5、採用克隆胚胎處理液培養24h後的胚胎23-24h
bix-01294鹽酸鹽添加到pzm培養液中分別配製成5nm、50nm、500nm的克隆胚胎處理液。用pzm培養液洗滌融合的重構胚5遍,轉入預平衡好的培養液中,置於39℃、飽和溼度、低氧(5%o2+5%co2+90%n2)條件的培養箱中培養。在胚胎融合激活時記為0天,將克隆胚胎處理液在第1天早上8點分別轉入預平衡好的新四孔板中,克隆胚胎處理液處理時間為23-24h,第2天早上8點結束該藥物處理時間,對胚胎進行換液後繼續培養。藥物處理的不同濃度分組情況如下表表5。第2天和第6天分別觀察並記錄卵裂數和囊胚數等克隆效率相關數據。
表5克隆胚胎處理液處理胚胎23-24h組別
6、克隆胚胎處理液處理胚胎16-17h
用培養液洗滌融合的重構胚5遍,轉入預平衡好的培養液中,置於39℃、飽和溼度、低氧(5%o2+5%co2+90%n2)條件的培養箱中培養。在胚胎融合激活時記為0天,胚胎融合4h後分別轉入預平衡好的新四孔板中,克隆胚胎處理液處理時間為16-17h,然後結束該藥物處理時間,對胚胎進行換液後繼續培養。藥物處理的不同濃度分組情況如下表6。第2天和第6天分別觀察並記錄卵裂數和囊胚數等克隆效率相關數據。
表6克隆胚胎處理液處理胚胎16-17h組別
兩種方案均培養至第6天早上,每組每次收集5-10個囊胚進行核染色統計囊胚內總細胞數,經hn操作液洗滌後,放入含10μg/mlhoechst33342的dpbs中避光染色10min,接著將囊胚微滴轉移到乾淨的載玻片上,輕蓋上蓋玻片,使囊胚受壓後膨大但不至於破碎,用指甲油封片。置於螢光顯微鏡下觀察,計算單個囊胚內的總細胞數目。另外,每組每次另外收集6-10個胚胎混合裝至50μl的rlt裂解液中,蓋好離心管蓋,用parafilm膜封口,迅速丟入液氮中速凍,-80℃保存,乾冰運輸,用於胚胎rna抽提。
採用spss17.0進行數據處理,利用卡方檢驗比較對照組和5nm、50nm、500nmbix-01294處理組進行克隆後重構胚胎的早期體外發育情況,包括融合率、卵裂率、囊胚率和囊胚平均細胞數的差異。概率值p<0.05時,平均值差異顯著。
二、克隆胚胎處理液處理後對胚胎特定基因表達水平檢測
1、胚胎的收集
準備好裝有50μl的rlt裂解液的離心管,發育到囊胚時從四孔板中取出6-10個胚胎放於離心管中,用parafilm膜封口,迅速丟入液氮中速凍,-80℃保存。
2、胚胎rna抽提
收集的胚胎用於rna抽提,胚胎rna的提取採用qiagen的rneasyplusmicrokit(50)試劑盒。具體操作如下:
(1)胚胎樣品預處理。39℃水浴解凍1~2min,簡易離心。向裂解液中添加5μl,4ng/μl的carrierrna,再加入1μlβ-巰基乙醇,混勻,渦旋30s,簡易離心。
(2)轉移預混液至allprepdnaspincolumn,8000×g或≥10,000rpm離心30s。
(3)向(2)中收集管內濾液裡加入等體積的70%乙醇溶液,吹打混勻。
(4)將(3)中收集管的乙醇混合液轉移至到rneasyminelutespincolumn,8000×g或≥10,000rpm離心15s,倒掉濾液。
(5)向柱子裡添加700μlbufferrw1,8000×g或≥10,000rpm離心15s,倒掉濾液。
(6)向柱子裡添加500μlbufferrpe,8000×g或≥10,000rpm離心15s,倒掉濾液。
(7)向柱子裡添加500μl80%乙醇,離心15s,小心取出柱子、棄去收集管。
(8)將柱子安裝到一根新的2ml收集管,間隔放置、打開蓋子,全速離心5min。
(9)洗脫rna:將柱子安裝到試劑盒自帶的1.5ml收集管,將14μlrnase-freewater直接加至離心柱膜的中心位置,輕蓋蓋子,全速離心1min,-80℃保存rna或立刻進行反轉錄。
胚胎rna反轉錄及定量pcr按照步驟2.3.2.6進行,檢測胚胎特定基因(dnmt1、dnmt3a、dnmt3b、nanog、sox2、cdx2、bmp4、esrrb、kdm1a、xist、oct4)的表達水平。比較各組克隆胚特定基因表達量的差異。定量引物見表7。
表7胚胎定量pcr引物設計
3、數據處理及統計分析
基因組相對表達數據分析中,各基因ct值經過內參基因(β-actin)和對照樣品正態化處理後,用2-δδct方法計算相對表達量。採用spss17.0進行數據處理,利用卡方檢驗。概率值p<0.05時,平均值差異顯著。
三、免疫螢光法檢測克隆胚胎中組蛋白h3k9me2表達水平
將第六天收集的囊胚放入預熱的0.5%鏈酶蛋白酶中作用1min去透明帶,去除透明帶後用dpbs-0.1%pva洗滌3次,15min;加入固定劑(用dpbs稀釋的4%pfa),室溫孵育15min後用dpbs-0.1%pva洗滌3次,15min;加入穿孔液(用dpbs稀釋的0.5%tritionx-100)室溫孵育30min後用dpbs-0.1%pva洗滌3次,15min;加入封閉液(用dpbs稀釋的1%bsa),4℃過夜。加入用1%bsa稀釋的一抗稀釋液,39℃孵育1h後用dpbs-0.1%pva洗滌12次,60min,再加入二抗稀釋液(注意避光處理)39℃孵育1h後用dpbs-0.1%pva洗滌12次,60min。最後加入1μg/mlpi,室溫孵育10min後用dpbs-0.1%pva幾次。準備好乾淨的載玻片,將染色處理過後的胚胎轉移上去,轉移過程中儘量使操作快速並且儘量少帶液體,以胚胎所在處為中心,在要放置蓋玻片的胚胎周圍的找到四角,滴凡士林/石蠟油,蓋上蓋玻片,輕壓蓋玻片,然後用指甲油封片,最後在nikone800螢光顯微鏡下觀察,拍照記錄。
實驗結果分析
1、克隆胚胎處理液處理對豬成體成纖維細胞特異基因表達的影響
待第5代豬成體成纖維細胞貼壁後利用不同濃度的克隆胚胎處理液(bix-01294濃度分別為0、5nm、50nm、500nm)分別處理24h後收集細胞,用omega的totalrnakiti試劑盒抽提rna並反轉成cdna;用q-pcr法檢測豬成體成纖維細胞細胞組蛋白甲基化酶相關基因(suv39h1、g9a、setdb1)的mrna表達情況。
結果如圖1顯示,圖1中字母不同說明差異顯著a,b,c(p<0.05)。如圖所示,使用bix-01294濃度為5、50nm的克隆胚胎處理液處理組細胞的suv39h1基因表達顯著低於無處理對照組(p<0.05),而500nm處理組則顯著高於其餘各組(p<0.05);5、50nm的bix-01294處理細胞後,g9a的表達量均有升高的趨勢,而500nm處理組g9a基因表達顯著高於無處理對照組(p<0.05);經0、5nm、50nm、500nmbix-01294處理後,setdb1的表達量均顯著低於無處理對照組(p<0.05)。
2、dna甲基化酶相關基因
dna甲基化水平主要由dna甲基化轉移酶互相協調發揮作用。因此,為了研究克隆胚胎處理液處理前後細胞dna甲基化是否發生重編程,對bix-01294處理前後的細胞中dnmt1、dnmt3a、dnmt3bmrna水平進行了q-pcr檢測並進行比較。在第5代豬成體成纖維細胞貼壁後利用不同濃度的克隆胚胎處理液(bix-01294濃度分別為0、5nm、50nm、500nm)分別處理24h後收集細胞,試劑盒抽提rna並反轉成cdna;用q-pcr法檢測豬成體成纖維細胞dna甲基化酶相關基因dnmt1、dnmt3a、dnmt3b的mrna表達情況。
結果如圖2所示,經5nm、50nm、500nmbix-01294的克隆胚胎處理液處理後,dnmt1的表達量顯著低於未處理的對照組(p<0.05),且5nm、50nm處理組的dnmt1表達量顯著降低(p<0.05);經5nm、50nm、500nmbix-01294處理後,dnmt3a的表達量顯著低於未處理的對照組(p<0.05),且50nm處理組的dnmt1表達量極顯著降低(p<0.01);5nmbix-01294處理細胞使dnmt3b基因表達水平顯著低於未處理組(p<0.05),而50nm、500nm處理組的dnmt3b基因表達較未處理組有降低的趨勢。
3、克隆胚胎處理液對組蛋白h3k9二甲基化的影響
為了研究豬體細胞克隆胚組蛋白甲基化修飾在體細胞克隆克隆胚胎早期發育過程中的影響,因此用不同濃度的克隆胚胎處理液處理克隆胚胎24h後恢復培養,在胚胎發育到2cell及4cell時收集胚胎檢測h3k9me2表達水平。
免疫螢光結果如圖3所示,克隆胚胎處理液對克隆胚胎2cell、4cell的h3k9me2水平具有明顯的下調作用。
4、克隆胚胎特異基因表達量的比較
4.1組蛋白甲基化酶基因
為了研究克隆胚胎處理液處理是否改變胚胎組蛋白甲基化酶相關基因的表達,5nm、50nm、500nmbix-01294的克隆胚胎處理液處理培養24h後的克隆胚胎23-24h,並在體外培養發育至囊胚階段收集胚胎5-6個於rtl裂解液中,用qiagen的qiagenrneasyplusmicrokit(50)試劑盒抽提rna並反轉成cdna;用q-pcr法檢測第6天收集的囊胚組蛋白甲基化酶相關基因(suv39h1、g9a、setdb1)的mrna表達情況。
結果如圖4顯示,不同濃度的克隆胚胎處理液處理組胚胎的suv39h1基因表達均有所下降,且50nm、500nm處理組胚胎的suv39h1基因表達顯著低於無處理對照組(p<0.05);5nm、50nmbix-01294處理組胚胎的g9a基因表達均有下降的趨勢,而500nm處理組g9a基因表達較未處理對照組有升高的趨勢;經5nmbix-01294處理後,setdb1的表達量顯著高於未處理對照組(p<0.05),而50、500nmbix-01294處理組胚胎的setdb1基因表達均有下降的趨勢。
4.2dna甲基化酶基因
mrna表達量結果如圖5所示,經5nm、50nm、500nmbix-01294的克隆胚胎處理液處理後,dnmt1的表達量極顯著高於未處理的對照組(p<0.01),且隨處理濃度的增加,dnmt1基因表達量增加;經5nm、50nm、500nmbix-01294處理後,dnmt3a的表達量極顯著高於未處理的對照組(p<0.01),且隨處理濃度的增加,dnmt3a基因表達量增加;5、50nmbix-01294處理細胞使dnmt3b基因表達水平較未處理對照組有下降的趨勢,而500nm處理組的dnmt3b基因表達較未處理對照組有提高的趨勢。
以上所述的僅是本發明的一些實施方式。對於本領域的普通技術人員來說,在不脫離本發明創造構思的前提下,還可以做出若干變形和改進,這些都屬於本發明的保護範圍。
