在種和/或亞種水平鑑定從臨床樣品分離的菌株的方法與流程
2023-10-23 11:37:52 5
本發明涉及鑑定從臨床樣品分離的菌株的方法。更具體而言,涉及通過使用基質輔助雷射解吸電離飛行時間質譜(MALDI-TOF-MS),在種和/或亞種水平精確並快速鑑定臨床分離物的方法。其還涉及用於該鑑定的資料庫。
MALDI-TOF-MS是用於檢查直接從完整細菌細胞表面檢測到的蛋白質的特徵譜的技術。
這是一種基於相對分子質量的軟電離方法,允許從整個的不同培養微生物中解吸附(desorption)肽和蛋白質。根據其分子質量和電荷來分離並檢測離子。通過其質量:電荷比率(m/z)來鑑定種。該方法在數分鐘內獲得可重複的譜圖(spectrum),其由500-20000m/z的一系列峰組成。每個峰對應於在雷射解吸附期間從細胞表面釋放的分子片段。
MALDI-TOF-MS已經被用於表徵細菌。然而,在譜圖中鑑定的多種組分中,只有一些出現在一大群的給定基因種的病菌(germ)中,其他則是分離特異性的或根據生長條件(溫育的培養基、溫度…)變化並且不能用於鑑定細菌以及更通常為病菌的種或亞種。
缺乏鑑定能夠區分不同基因種的那些峰的譜圖的全局性策略,阻礙了MALDI-TOF-MS在常規臨床微生物實驗室中用於診斷基因種的應用。實際上,這些峰必須對應於在給定基因種的分離物的大部分中出現的組分,以及大量存在於細胞壁中組分。考慮到基因種中可能的易變性,似乎是基因種的特徵不依賴於單個峰的出現而是依賴於一組峰的出現,這組峰或多或少地在基因種間是保守的。
本發明人已經發現可以通過如下方法克服這些問題:(i)通過在MALDI-TOF-MS分析前對待鑑定病菌進行表型分析,和(ii)通過在特定條件下,特別是涉及基質溶液和參照資料庫的選擇,進行MALDI-TOF-MS分析。
從而本發明的一個目的是提供基於MALDI-TOF-MS分析的新方法,用於在種和/或亞種水平鑑定從臨床樣品分離的菌株。
本發明的另一個目的是提供由針對於給定病菌的一組菌株而建立的資料庫。
因此本發明涉及使用MALDI-TOF-MS分析,在種和/或亞種水平鑑定從臨床樣品分離的菌株的方法,其包括在進行MALDI-TOF-MS分析前將所述菌株分類的步驟,其中所述分析包括在測試菌株的譜圖中保留如下峰的步驟,與具有最高強度並任意設置為1的峰相比,所述峰的相對強度大於0.02,特別地大於0.05,更特別地大於0.1。
本發明特別涉及如下方法,其中所述MALDI-TOF-MS分析包括將待鑑定菌株的譜圖特徵譜與稱為參照資料庫相比較,所述參照資料庫包含待鑑定菌株所屬病菌組的基因種的代表性菌株的特徵性MALDI-TOF-MS譜圖的,所述資料庫對於每個代表性菌株包含這樣的峰,與具有最高強度並任意設置為1的峰相比,所述峰的相對強度大於0.02,特別地大於0.05,更特別地大於0.1,直至其出現在至少2種亞培養物,優選5種或甚至10種或更多種亞培養物中。
根據本發明進行的峰的選擇使得能夠準確鑑定在臨床樣品中存在的病菌。
分類步驟基於生長條件,和/或菌落的特徵,和/或通過顯微鏡檢查的細菌形態,和/或革蘭氏染色,和/或簡單的表型測試。
在全部完整細胞上或者在裂解後得到的或對應於細胞組分(細胞壁、細胞質等)的級分的蛋白質提取物上進行MALDI-TOF-MS技術。該技術在待測菌株的分離的菌落上可以理想地進行,所述菌株得自在合適的生長培養基上培養並在合適的溫度下孵育的臨床樣品。
在進行MALDI-TOF-MS技術前,將基質培養基添加到分離菌落中。
例如,合適的基質培養基包括苯甲酸衍生物,例如羥基苯甲酸,特別是2,5-二羥基苯甲酸(DHB)。
每個譜圖是來自含有待分析菌株的孔的不同區域的至少400個,優選地大於1000個,甚至大於2000個雷射發射的總和,在m/z500-50000,更優選地500-2000,更優選地2000-20000的範圍內分析所述譜圖。
隨後使用軟體比較特徵譜,所述軟體通過分析給定基因種或基因亞種(genosubspecies)特異的一種或幾種參照菌株,選擇受試菌株和所述參照資料庫的所選峰之間的最佳匹配。每種菌株代表所研究的一個基因種或一組基因種,從而一組菌株對應於一組病菌的相關基因種或基因亞種。使用MALDI-TOF-MS技術記錄每種參照菌株的譜圖。如上所述,將具有最高強度並任意設置為1的峰,所有其他峰具有相對於該最高峰的相對強度的數值。保留具有相對強度大於0.02,或更特別地大於0.05或更特別地大於0.1的峰,直至它們出現在至少2種亞培養物,優選5種或甚至10種或更多種亞培養物中。這些峰就是所選的峰。
考慮到一些可能的變體,軟體選擇受試菌株和資料庫之間的最佳匹配,將m/z值得可能誤差考慮進去。誤差的範圍任意設置為+/-20或更優選地+/-10。
峰的存在或缺少被認為是特定分離物的指紋。
所述方法是用於快速鑑定病菌的有力工具,允許將其用於實驗室的常規診斷中。昂貴設備的需求被需要最少的操作時間的非常簡單的方案所彌補。尤其適合於得到大量的樣品的參照實驗室或醫院特。
根據本發明進行的MALDI-TOF-MS方法的高解析度使得例如獲得給定病菌的每個種或甚至亞種的特徵性譜圖指紋成為可能。
有利地,所述方法用於在種和/或亞種水平鑑定選自細菌、酵母、黴菌的病菌。
根據特定的實施方式,本發明涉及凝固酶陰性葡萄球菌(Staphyloccocci)(縮寫為CNS)的種和/或亞種的鑑定。
在種的水平鑑定CNS不是常規進行的,因為其經常被視為樣品汙染。另外,對臨床上重要的菌株進行的表型方法的結果是令人失望的。商業鑑定試劑盒對於鑑定CNS分離物只有有限的價值。
SodA序列測定儘管是鑑定CNS正確的種的更準確方法,但其費時、昂貴且在技術上有要求。另外,儘管基因型方法明顯優於表型鑑定,但基於序列的基因型方法的一個缺點是缺少資料庫中的保存序列的質量。
歸功於本發明,通過MALDI-TOF-MS相比於SodA方法在亞種水平,例如對於葡萄球菌的亞種的區分更加準確了,因為證明在頭狀葡萄球菌(S.capitis)、人葡萄球菌(S.hominis)、腐生葡萄球菌(S.saprophyticus)和施氏葡萄球菌(S.schleiferi)亞種中SodA基因沒有顯著區別。
根據另一個實施方式,本發明涉及鑑定非發酵革蘭氏陰性桿菌的種或亞種。
在所述方法中使用的資料庫也是本發明的部分。
它們構成了通過MALDI-TOF-MS分析菌株獲得的一組所選的峰,所述菌株在屬於相同基因種的菌株內至少是部分保守的。
優選地,所述參照峰對應於m/z大於0.02,更特別地大於0.05,更特別地大於0.1的主要的、保守的峰。
通過使用一組菌株,每個菌株代表研究中組的一個基因種,來有利地獲得對於每個組的這種資料庫,從而該組菌株對應於一組病菌的相關基因種。使用MALDI-TOF-MS技術記錄這樣的組的每個菌株的譜圖。每個菌株代表了該組病菌的基因種,並且被進一步指定為參照菌株。如上所述,將具有最高強度並任意設置為1的峰,所有其他的峰具有對應於該最高峰的相對強度的數值。保留主要的峰,這些峰優選地具有至少0.02,更優選大於0.05,更優選大於0.1的相對強度。隨後保留在對於給定參照菌株獲得的所有數據組中出現的、具有相對強度大於0.02,更優選大於0.05,更優選大於0.1的峰,直至它們出現在至少2種亞培養物,優選地5種或者甚至10種或更多種亞培養物中。
由此獲得的一組峰在給定生長條件下(培養基和持續時間)以及鑑於給定譜儀的特徵,是基因種特異的。
對於鑑定1)在種的水平的CNS和2)在囊腫性纖維化中分離的非發酵革蘭氏陰性桿菌,本發明的其他特徵和優點如下。它們用於示例說明本發明,而不是限制本發明的範圍。在本文中圖1-7中分別表示
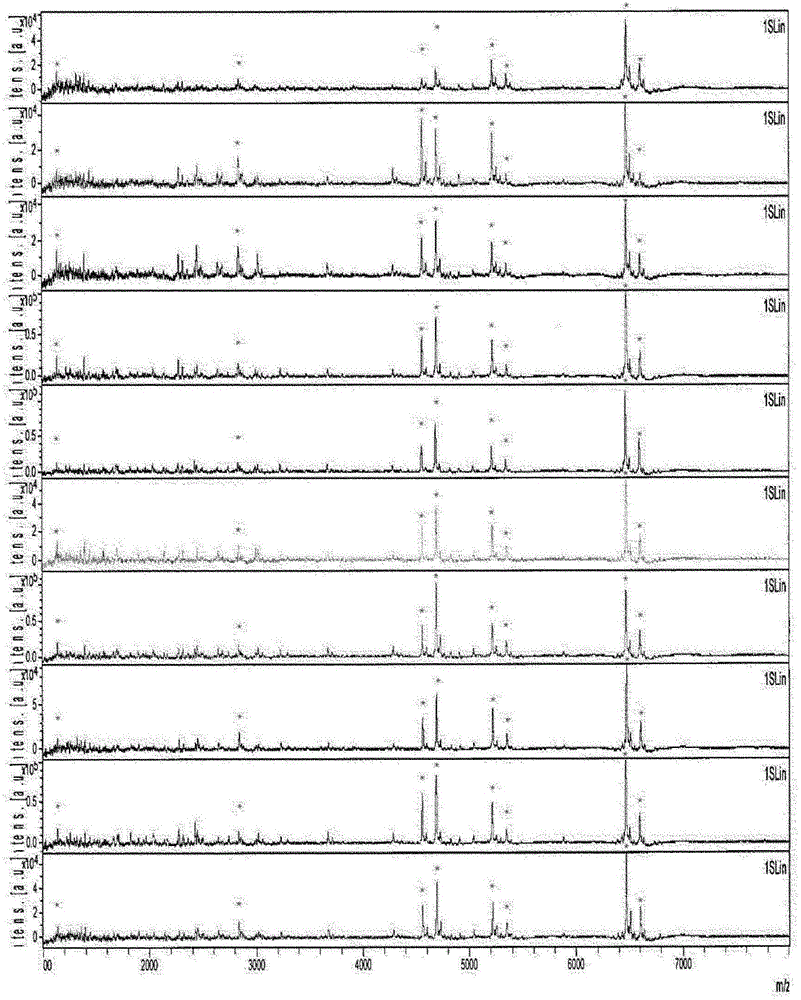
-圖1:金黃色葡萄球菌(S.aureus)CIP7625的相同菌株的10個分離物的MALDI-TOF-MS特徵譜;
-圖2:根據資料庫1(Muёller Hinton 24H)和2(Muёller Hinton 48H)的微球菌屬(Micrococcacae)物種的MALDI-TOF-MS系統樹圖,從而指定在該組病菌中待鑑定的基因種;
-圖3:對於葡萄球菌屬(Staphyloccocci)菌株,具有相對強度大於0.1的峰的m/z值;
-圖4和5:在屬於相同基因種的菌株中,所選菌株的一組峰的保守性;
-圖6:需氧和兼性厭氧細菌的分類;
-圖7:6種革蘭氏陰性桿菌的MALDI-TOF-MS特徵譜。
1.在種的水平鑑定CNS
材料和方法
細菌菌株
通過分析屬於微球菌屬細菌的51個菌株得到下文給出的結果,這些菌株從巴斯德研究所(Institut Pasteur,Paris,France)的保藏中心獲得。
用於建立MALDI-TOF-MS資料庫的所選菌株在表1中給出
表1
屬於微球菌科的菌株在表2中給出。
表2
*:使用不區分2個亞種的sodA基因的序列鑑定這些臨床菌株的基因種
也研究了116個臨床凝固酶陰性葡萄球菌(CNS)分離物:74個菌株分離自血液培養物,25個菌株分離自兒童縱隔炎(皮膚、縱隔液、電極),12個菌株分離自骨骼感染(Necker-Enfants malades,Paris;Raymond Poincaré,Garches,France),以及5個菌株分離自尿道感染。另外,分析了從混雜的感染中分離的金黃色葡萄球菌的68個臨床菌株。
表型和基因型鑑定
通過包括Slidex乳膠凝集試驗(bioMérieux,Marcy I』Etoile,France)和DNA酶試驗的常規表型試驗區分來自金黃色葡萄球菌的CNS臨床菌株。在這兩個試驗不相符合的情況下,進行試管凝固酶試驗。通過對如上所述的SodA基因的內部片段測序來獲得CNS的精確鑑定。簡言之,使用Quiagene試劑盒(Courtaboeuf,France)從CNS純培養物中進行基因組DNA的提取。擴增部分SodA基因,並且使用ABI Big Dye Terminator v1.1循環測序讀取反應試劑盒(Applied Biosystems,Foster City,CA,USA),如Poyart等人2001,J.Clin.Microbiol.39:4296-4301之前所述的對所得的擴增子測序。將核酸序列發送至GenBank資料庫用於物種分配。
使用該策略,鑑定了在表2中給出的116個臨床CNS分離物。
MALDI-TOF-MS技術
將菌株培養在Müeller Hinton瓊脂或Columbia瓊脂+5%馬血(bioMérieux)上,在37℃溫育24或48小時。對於每次鑑定,將分離的菌落收集在100μl的無菌水中;以3次重複將1μl的該混合物置於靶平板(Bruker Daltonics,Bremen,Germany)上並使之在室溫乾燥。隨後在每個孔中加入1μl無水乙醇,以及1μl基質溶液DHB(2.5二羥基苯甲酸50mg/ml、乙腈30%、三氟乙酸0.1%)。乾燥後,加入1μl基質溶液DHB。隨後用具有flex控制軟體(Bruker Daltonics)的譜儀MALDI-TOF-MS autoflex(Bruker Daltonics)處理樣品。以線性模式,20Hz的加速電壓提取陽離子。每個譜圖是來自相同孔的不同區域的5x200個雷射發射的離子的總和,並且在m/z1000-23000的範圍內分析每個譜圖。使用flex分析軟體進行該分析,並用蛋白質校準標準T(蛋白質I,Bruker Daltonics)進行校準。將3次重複中獲得的數據加和以最小化隨機效應。峰的出現和缺失被視為特定分離物的指紋。使用可在網站http://sourceforge.net/projects/bgp獲得的軟體BGP-資料庫對這些特徵譜進行分析和比較。
結果
表1中所列的菌株是作為基因種代表的任意選出的菌株。
如在材料和方法部分中所述,通過MALDI-TOF-MS分析這些所選菌株中每一個的10個分離物。
對於每個譜圖,對每個峰給出對應於強度的數值。
將具有最高強度的峰任意設置為1,所有其他峰具有對應於該最高峰的相對強度的數值(圖1)。
小峰(相對強度小於0.1)的出現不規律。隨後該分析集中在對於給定的菌株所得的所有10組數據中存在的、具有相對強度大於0.1的峰。
為了確定生長條件對細菌鑑定的影響,對培養在Müeller Hinton瓊脂或補充5%馬血的Columbia瓊脂上24或48小時的表1中所列的所有菌株進行上述步驟。
結果在表3中給出。
資料庫分別指定為1-4:它們通過使用在Müeller Hinton 24H(資料庫1),Müeller Hinton 48H(資料庫2),Columbia馬血培養基24H(資料庫3),Columbia馬血培養基24H(資料庫4)上的細菌培養物獲得。對於給定的菌株,每個保守峰的m/z數值的標準偏差從沒有大於7。具有大於0.1的相對強度並且在每種生長條件的所有10組數據中都存在的峰的m/z數值在圖3中報導。
表3
*:括號內的數目是具有資料庫1的那些的常見峰的數目
**:遲緩微球菌在馬血培養基上不生長
表3顯示了對於每個所選菌株和每個資料庫,已保留的峰的數目。然而,對於某個菌株,無論培養基或者培養時間如何有些峰都是保守的,而另一些峰隨改變培養條件而消失或出現。然而,對於給定的培養基和培養時間,一組峰是菌株特異性的,如樹狀圖所示(圖2)。
在屬於相同基因種的菌株中每個所選菌株的一組峰的保守性
為說明此點,使用在37℃在Müeller Hinton培養基上培養24小時的細菌進行MALDI-TOF MS。所用菌株是表2所列的分離物。
對於每個菌株,保留數值大於0.1的單峰。隨後就這些分離物的每一個,將所獲得的特徵譜與資料庫1的那些的特徵譜相比較。
為了進行該任務,開發了軟體(在http://sourceforge.net/projects/bgp可獲得的BGP-資料庫)以允許快速鑑定資料庫中與受試菌株的數值最接近的一組數值。考慮到已經測量的m/z數值的可能誤差,該軟體選擇受試菌株和資料庫的參照菌株之間的最佳匹配。該數值被任意地設置為多至7。
受試菌株經常與屬於資料庫的相同基因種的菌株具有最佳匹配。所有的數據記錄在圖4和圖5。
在Müeller Hinton培養基上培養24小時的受試菌株的保守峰的平均數目與每個資料庫的峰的數目相比較
通過在Müeller Hinton培養基上培養受試細菌24小時期間獲得的相同組數據針對資料庫2、3和4進行試驗。
結果在表4中給出。
表4
*在亞種水平不能區分、不能鑑定的菌株
**鑑定3個腐生葡萄球菌牛亞種
***鑑定6個人葡萄球菌人亞種
****鑑定1個腐生葡萄球菌腐生亞種
*****在人葡萄球菌人亞種和人葡萄球菌novobiosepticus亞種之間不能區分的3個菌株
表4顯示了對於每個基因種,在受試菌株和4個資料庫的每個之間保守的峰的平均數目。
既使當使用與受試菌株所用的不同培養條件建立用於基因種鑑定的資料庫時,峰的數目是保守,也可能在所有情況下在種的水平上進行鑑定。
通過使用資料庫2、3和4所觀察到的與使用資料庫1獲得的那些之間唯一的不同是:不同於使用資料庫1得到的結果,不可能在亞種水平的鑑定人葡萄球菌和腐生葡萄球菌。
總體來說,所述數據證明通過選擇適當的一組菌株並只保留具有大於0.1的m/z的保守峰,可以改造用於基因種鑑定的資料庫。另外,這些峰的保守性使得既使待鑑定菌株已經使用不同於用於改造資料庫的培養條件培養,也仍然可能進行基因種的鑑定。
2.鑑定非發酵革蘭氏陰性桿菌
第一步是針對屬於在人體中回收(recover)的一群非發酵革蘭氏陰性桿菌的所有種建立完整的資料庫革蘭氏。隨後驗證該資料庫,以使用MALDI-TOF MS來鑑定在1年期間的囊性纖維化(CF)患者中回收的所有臨床非發酵革蘭氏陰性桿菌。。
材料和方法
細菌菌株
用於改造MALDI-TOF MS資料庫的參照菌株屬於可以從患者中回收的非發酵革蘭氏陰性桿菌的52個種。這些菌株列於表4中。
表4
從06年1月1日到06年12月31日之間在Necker-Enfants Malades醫院(Paris,France)小兒科就診的CF兒童的痰液中回收非發酵革蘭氏陰性桿菌的臨床分離物。簡言之,將顯示綠色或黃綠色著色,氧化酶試驗陽性,生長在42℃,生長在溴棕三甲銨瓊脂並對結腸黴素易感的分離物被鑑定為銅綠假單胞菌。不顯示那些標準的分離物通過API 20NE系統鑑定。使用APILAB PLUS軟體包解釋說明API 20NE試驗的結果。當使用該軟體獲得的結果不被視為相應的對於銅綠假單胞菌、木糖氧化產鹼菌木糖氧化亞種和嗜麥芽糖寡養單胞菌的良好鑑定時,通過測序16S rDNA基因的內部片段來鑑定這些細菌。
在該研究中使用的所有細菌保存在-80℃補充有15%甘油的胰腖豆腖培養液。
MALDI-TOF-MS。將菌株培養在Mueller-Hinton瓊脂上並在37℃溫育24h。大多數分離物在24h後生長,而將24h後不生長的那些菌株進一步溫育48h或72h。將分離的菌落收集在100μl的無菌水中;以3次重複將1μl的該混合物放置在靶平板(Autoflex;Bruker Daltonics,Bremen,Germany)上並使之在室溫乾燥。隨後在每個孔中加入1μl無水乙醇,並使混合物乾燥。然後加入1μl基質溶液DHB(2.5二羥基苯甲酸50mg/ml、乙腈30%、三氟乙酸0.1%)。用具有flex控制軟體(Bruker Daltonics)的MALDI-TOF-MS譜儀(Bruker Daltonics)中處理樣品。以線性模式,20kV的加速電壓引出(extract)陽離子。每個譜圖是在相同孔的5不同區域的200個雷射發射的離子的總和。在m/z 2,000-20,000的範圍內分析譜圖。使用flex分析軟體進行該分析,並用蛋白質校準標準T(蛋白質I,Bruker Daltonics)進行校準。將3次重複中獲得的數據加和以最小化隨機效應。峰的出現和缺失被視為特定分離物的指紋。使用可在網站http://sourceforge.net/projects/bgp獲得的軟體BGP-資料庫對這些特徵譜進行分析和比較。
結果
非發酵革蘭氏陰性桿菌資料庫的改造
將表4中所列的參照菌株用於確定通過MALDI-TOF-MS獲得的m/z數值,其構成每個細菌種的特徵性譜圖並且隨後可用於細菌鑑定。圖7顯示了使用非發酵革蘭氏陰性桿菌的6個種獲得的譜圖。在Mueller Hinton上培養24H的這些所選菌株中每一個的10個分離物通過在材料和方法部分中描述的MALDI-TOF-MS來進行分析。對於每個譜圖,採用了對微球菌使用的相同策略。根據該策略,只保留在對於給定菌株所獲得的所有10組數據中一直存在的、具有大於0.1的強度的那些峰。對於每個菌株,每個保守峰的標準偏差的m/z數值(標準化的數據)從沒有超過8。
表5顯示了關於8個種,為資料庫保留的峰的數值。
對每個參照菌株保留的一組峰給出了特徵性譜圖。
鑑定臨床菌株
進行實驗以確定上述資料庫是否可以用於臨床非發酵革蘭氏陰性桿菌的鑑定,從而證明每個所選菌株的一組峰至少部分地在相同種的分離物中是保守的。從2006年1月到12月,回收非發酵革蘭氏陰性桿菌的811個菌株,並通過表型試驗和分子方法進行鑑定:699個銅綠假單胞菌(120個患者),54個木糖氧化產鹼菌(12個患者),32個嗜麥芽糖寡養單胞菌(12個患者),9個解甘露醇羅爾斯頓菌(1個患者),14個Bcc(2個患者),1個唐菖蒲伯克氏菌,1個欣氏博德特氏菌和1個I.limosus。在這些其中,在400個銅綠假單胞菌菌株的組和在所有剩餘的非銅綠假單胞菌菌株進行MALDI-TOF-MS分析。對於每一個分離物,譜圖的所有m/z數值都考慮在內。對於每個菌株,無論其強度如何保留所有的峰,並使用BGP-資料庫軟體將其與所述資料庫的峰進行比較。考慮到m/z數值的可能誤差,該軟體選擇受試菌株和所述資料庫之間的最佳匹配。將該數值設置為。將菌株鑑定為屬於所述資料庫的、給出最佳匹配的菌株的基因種。在如下表6中給出的結果顯示了通過BGP軟體提供的針對銅綠假單胞菌株獲得的匹配。
表6
特徵譜名稱:銅綠假單胞菌
匹配:13/13
特徵譜名稱:稻棲黃單胞菌(Flavimonas orzyhabitans)
匹配:7/12
表7顯示了對於所有臨床菌株所獲得的鑑定,與物種鑑定的第二選擇相比較
MALDI-TOF-MS正確鑑定了100%的銅綠假單胞菌,100%的木糖氧化產鹼菌和100%的嗜麥芽糖寡養單胞菌的菌株。MS在亞種水平鑑定木糖氧化產鹼菌臨床菌株。MS分析正確鑑定了11個BCC菌株為新洋蔥伯克氏菌。對於剩餘的3個BCC菌株,在新洋蔥伯克氏菌和嚴格意義上的洋蔥伯克氏菌之間沒有差別。應當指出除了1個(由MS鑑定為皮氏羅爾斯頓菌)外的9個解甘露醇羅爾斯頓菌被MS正確地鑑定。
結論
這些結果證明根據本發明改造的資料庫也適用於非發酵革蘭氏陰性桿菌的精確的種鑑定。從而有可能,通過使用MALDI-TOF-MS從非發酵革蘭氏陰性桿菌的一個菌落(培養條件、菌落特徵)中,在數分鐘內獲得準確的鑑定,而不需要另外的試驗。除了3個新洋蔥伯克氏菌和1個解甘露醇羅爾斯頓菌外,在種的水平準確地鑑定了受試的CF臨床菌株。有趣地注意到鑑定為唐菖蒲伯克氏菌的菌株也與椰毒唐菖蒲伯克氏菌的參照菌株相匹配,後者是被證明為唐菖蒲伯克氏菌的次異名(junior synonym)的細菌物種。
MALDI-TOF-MS能夠非常快速地鑑定細菌,而通過API 20NE的常規生化鑑定通常需要24h-48h以上,並經常有鑑定錯誤。因此MALDI-TOF-MS菌株鑑定是用於革蘭氏陰性桿菌物種鑑定的非常有趣的方法,並且有助於理解它們的臨床相關性和分布。
