疼痛治療中的CYP2J2拮抗劑的製作方法
2023-12-01 08:57:51 4
本發明涉及對神經病理性疼痛、尤其是化療誘導的外周神經病理性疼痛(CIPNP)的新療法。本發明提供了細胞色素P450表氧化酶(CYP)的拮抗劑,更具體地,CYP2J2的拮抗劑,作為治療劑用在諸如CIPNP的神經病理性疼痛的治療中。CYP2J2拮抗劑已在體內鑑定為緩解CIPNP,並由此與化療藥組合而額外提供,用於治療諸如癌症或其它增生性病症的疾病中。該CYP2J2拮抗劑減輕化療誘導的疼痛,於是在癌症治療期間允許使用更高和更佳的化療劑量。此外,本發明涉及使用CYP2J2激動劑、或CYP2J2的代謝物,用于敏化TRPV1。這種情況下,本發明提議使用CYP2J2激動劑或代謝物與瞬時受體電位香草酸亞型1(TRPV1)激動劑的組合來治療對TRPV1激動劑有應答的病症,例如神經病理性疼痛。
描述
神經病理性疼痛為持續的或慢性疼痛症候群,其可源自對神經系統、外周神經、背根神經節、背根、或者對中樞神經系統的損傷。神經病理性疼痛症候群包括異常性疼痛、諸如帶狀皰疹後神經痛和三叉神經痛的各種神經痛、幻覺痛、以及複雜性區域疼痛症候群,例如反射交感性營養不良和灼痛。灼痛通常的特徵是,伴有痛覺過敏和異常性疼痛的自發燒灼痛。不幸的是,沒有用於充分地、可預見地和特異性地治療已出現的神經病理性疼痛的現有方法,由於用於神經病理性疼痛的目前治療方法僅由試圖幫助患者應對心理或作業療法組成,而不是通過減輕或消除所承受的疼痛。對於神經病理性或者慢性疼痛的治療對於醫師和患者是一個挑戰,因為沒有藥物特異地靶向該狀況,以及因為目前使用的藥物僅帶來微小緩解並且基於它們在急性疼痛狀況中的功效或者它們緩解副作用如焦慮和抑鬱的功效。慢性疼痛的發病率在社會中是逐漸上升的,其對社會的負擔在健康護理和生產力損傷方面都是巨大的。當前,沒有經科學驗證的緩解慢性疼痛的療法。結果,衛生界致力於「疼痛管理」,其中同時使用多個模式療法,希望對生活質量提供一些改善。因此,亟需可緩解慢性疼痛的藥物。
化療誘導的外周神經病理性疼痛(CIPNP)為嚴重的細胞抑制劑(例如紫杉烷類、鉑衍生物、長春花生物鹼類等)劑量限制性副作用。症狀通常從麻刺感開始,並且可引起燒灼痛、刺痛和酸痛以及冷觸發痛和機械性觸痛。由於CIPNP,一些患者過早地停止了細胞抑制劑抗癌療法,產生了更高的腫瘤進展風險。遺憾的是,很多已批准用於治療不同的神經病理性疼痛的有前途的物質(例如加巴噴丁或阿米替林)在CIPNP的單一療法中看起來很少或者沒有鎮痛作用。對細胞和分子機制的了解對於治療或甚至預防CIPNP是必要的,可以改進細胞抑制劑療法的總成功率。
最近的研究鑑定出離子通道的瞬時受體電位家族的成員(TRPV1、TRPA1和TRPV4)在奧沙利鉑和紫杉醇誘導的神經病理期間作為機械性觸痛和冷觸發痛的促進者。激活或敏化TRPV1和TRPA1可導致CGRP和物質P的增強釋放,這二者都可引起神經源性炎症和T細胞的募集。
但是,仍不清楚哪種內源性介質參與了細胞抑制劑依賴的TRP通道激活或敏化,由於沒有細胞抑制劑可直接激活TRP通道。有趣的是,紫杉醇和奧沙利鉑都為CYP表氧化酶的誘導劑(紫杉醇:CYP2C8、CYP2C9,奧沙利鉑:CYP2E1、CYP1B1)。細胞色素P450(CYP)-表氧化酶可代謝ω-6脂肪酸,例如花生四烯酸(AA)和亞油酸(LA),產生脂環氧化物如EETs(環氧二十碳三烯酸)或ω-羥化物如20-HETE。
細胞色素P450單加氧酶花生四烯酸的代謝導致各種生物活性的類花生酸的形成。已知發生三種類型的氧化反應。第一,烯烴環氧化反應(表氧化酶催化)產生環氧二十碳三烯酸(EETs)。四種重要的EET區域異構體為[5,6]-EET、[8,9]-EET、[11,12]-EET、和[14,15]-EET。這些EET經環氧化物水解酶水解形成對應的二羥基二十碳三烯酸(DHET)。第二,ω末端氧化導致形成ω末端羥基二十碳三烯酸(HETE)。第三,烯丙位氧化導致形成中鏈HETE。
已經鑑定了幾種細胞色素P450表氧化酶,包括CYP1A、CYP2B、CYP2C、CYP2E和CYP2J亞族的成員。人們最近關注CYP2J亞族的蛋白。CYP2J的一個具體亞型CYP2J2在人心肌細胞中高度表達,在這裡花生四烯酸經代謝產生EET。CYP2J2蛋白也在氣管和腸道中的上皮細胞內被發現。與其它P450酶比較,CYP2J2蛋白沿腸道徑向在上皮細胞和非上皮細胞中均勻分布。在自主神經節的細胞中、上皮細胞中、以及腸平滑肌細胞中發現高水平的CYP2J2蛋白。在動物中已鑑定了幾種CYP2J同源物,包括大鼠CYP2J3、大鼠CYP2J4、小鼠CYP2J5和小鼠CYP2J6。
辣椒素為瞬時受體電位香草酸亞型1受體(TRPV1;之前也稱為香草酸受體1(VR1))的高度選擇性激動劑,該受體為配體門控的非選擇性陽離子通道,優先在較小直徑的感覺神經元上表達,特別是那些專門檢測疼痛或有害感覺的C纖維上。TRPV1應答有害刺激,包括辣椒素、熱、以及細胞外酸化,並且將整合同時暴露於這些刺激。對表達TRPV1的(辣椒素敏感的)傷害感受器的活化的最初效果為灼燒感覺、痛覺過敏、異常性疼痛、以及紅斑。但是,在持續暴露於低濃度辣椒素或單次暴露於高濃度辣椒素或其它TRPV1激動劑後,小直徑的感覺軸突變得對各種刺激(包括辣椒素或熱刺激)較不敏感。這種持續暴露也以減弱的疼痛應答為特徵。辣椒素的這些後期階段效應經常被稱為「脫敏」,為開發局部辣椒素製劑來治療各種疼痛症候群和其它情況的基本原理。
因此,辣椒素、辣椒素類物質和TRPV1激動劑可以用於緩解多種疾病。例如,它們可以用於治療神經病理性疼痛(包括與糖尿病性神經病變、帶狀皰疹後神經痛、HIV/AIDS、創傷性損傷、複雜性區域疼痛症候群、三叉神經痛、紅斑性肢痛和幻覺痛相關的疼痛)、混合傷害性和/或神經病理性混合病因產生的疼痛(例如,癌症)、骨關節炎、纖維肌痛、腰痛、炎性痛覺過敏、外陰前庭炎或外陰疼痛、竇息肉間質性膀胱炎、神經源性膀胱或膀胱過動症、前列腺增生、鼻炎、手術、創傷、直腸過敏、灼口綜合症、口腔黏膜炎、皰疹(或其它病毒感染)、前列腺肥大、皮炎、瘙癢、癢、耳鳴、牛皮癬、疣、癌症(特別是皮膚癌)、頭疼、以及皺紋。
因此,迄今為止,沒有可用於神經病理性疼痛的特異療法,特別是針對化療誘導的外周神經病理性疼痛(CIPNP),這限制了癌症治療期間化療劑的最大劑量,並且給經歷化療的患者的生活質量的帶來嚴重損害。因此本發明的目的為提供新的治療選擇來應對神經病理性疼痛,特別是CIPNP。
在第一方面,通過將細胞色素P450表氧化酶(CYP)拮抗劑用於在受試者中預防或治療疼痛來解決上述問題。在本發明的一些實施方案中,該CYP拮抗劑選自CYP1A、CYP2B、CYP2C、CYP2E、以及優選的CYP2J拮抗劑。最優選地,該CYP拮抗劑為CYP2J2的哺乳動物同源物的拮抗劑(CYP2J2拮抗劑),優選人CYP2J2的拮抗劑,例如替米沙坦、阿立哌唑或最優選特非那定。
本發明涵蓋任何CYP2J2拮抗劑(優選選擇性CYP2J2拮抗劑)的用途。術語「選擇性CYP2J2拮抗劑」涉及選擇性抑制CYP2J2而非其它相關酶如CYP3A分子的活性、功能或表達的CYP2J2拮抗劑。為了鑑定候選拮抗劑是否為CYP2J2拮抗劑,可採用發光的細胞色素P450發光測定法。CYP蛋白催化花生四烯酸代謝物的形成。發光的CYP測定使用用於螢光素酶的生光反應的底物前體。CYP將該底物前體轉化為螢光素或者螢光素酯,其在與稱為螢光素檢測試劑(LDR)的螢光素酶反應混合物的第二反應中生成光。在該第二反應中產生的光的量與CYP活性成比例。
為了測試候選CY2J2拮抗劑的選擇性,可採用特異於其它CYP酶(如CYP3A4)的發光CYP測定。將候選拮抗劑針對CYP2J2與該相同拮抗劑針對另一CYP蛋白(如CYP3A4)的抑制活性進行比較,由此提供關於候選拮抗劑的選擇性的信息。
在本發明上下文中,優選的選擇性CYP2J2拮抗劑選自本文新公開的CYP2J2拮抗劑:雌二醇、鹽酸酚苄明、氯雷他定、丙酸氯倍他索、多沙唑嗪甲磺酸鹽、非諾貝特、左炔諾孕酮、阿立哌唑、哈西奈德、替米沙坦、氯苯吩嗪、左旋甲狀腺素鈉、阿洛司瓊鹽酸鹽、醋酸氟輕鬆、碘塞羅寧鈉、美克洛嗪二鹽酸鹽和特非那定以及它們的衍生物。
在本文描述的發明的背景下,所述待治療的疼痛優選神經病理性疼痛(包括與糖尿病性神經病變相關的疼痛、帶狀皰疹後神經痛、HIV/AIDS誘導的神經病理性疼痛、創傷性損傷、複雜性區域疼痛症候群、三叉神經痛、紅斑性肢痛和幻覺痛)、混合傷害性和/或神經病理性混合病因產生的疼痛(例如,癌症)、骨關節炎、纖維肌痛、腰痛、炎性痛覺過敏、外陰前庭炎或外陰疼痛、竇息肉間質性膀胱炎、神經源性膀胱或膀胱過動症、前列腺增生、鼻炎、手術、創傷、直腸過敏、灼口綜合症、口腔黏膜炎、皰疹(或其它病毒感染)、前列腺肥大、皮炎、瘙癢、癢、耳鳴、牛皮癬、疣、癌症、頭疼、以及皺紋、由於中風或塊狀病變、脊髓損傷、或多發性硬化導致的中樞疼痛。但是,最優選的實施方案涉及化療誘導的外周神經病理性疼痛(CIPNP)。
本發明在此提供了疼痛療法,其包括抑制尤其是CYP2J2的活性,而CYP2J2產生代謝化合物9,10-EpOME—根據本發明,該化合物為離子通道介導的疼痛感覺的敏化劑。令人驚訝地,根據本發明,對CYP2J2的抑制證實在體內是有效的,緩解了在小鼠模型中通過紫杉醇誘導的神經病理性疼痛,表明了CYP2J2拮抗劑作為針對神經病理性疼痛尤其是CIPNP的止痛劑的用途。
本發明的一個另外實施方案涉及以上提到的疼痛的預防或治療,其包括給患有所述疼痛的受試者施用本發明的所述CYP拮抗劑,其中所述受試者接受了、正接受或將接受化療。因此,該受試者在優選的實施方案中為患有或診斷為具有癌症疾病的受試者。
在本發明上下文中,化療優選包括向有需要治療的受試者施用化療劑,該化療劑選自基於嘧啶酮的抗腫瘤藥,例如阿糖胞苷,5-氟尿嘧啶或鉑類藥物,例如順鉑,或紫杉烷類,例如紫杉醇、多西他賽或卡巴他賽,或者它們的衍生物。這些化療劑已知誘導神經病理性疼痛,尤其對於紫杉烷類是已知的,因此它們在本發明上下文中是優選的。最優選的是紫杉醇。
此外,根據本發明,所述疼痛的預防或治療包括同時或順序施用所述CYP拮抗劑和所述化療劑。對於這個實施方案,還參見以下對本發明的組合的描述。
本發明的問題在另一方面是通過用於預防或治療受試者中的疼痛的9,10-環氧-12Z-十八碳烯酸(9,10-EpOME)拮抗劑來解決的。發現9.10-EpOME是通過CYP活性而產生的。因此,代替拮抗CYP,本發明的結果可以通過直接拮抗9,10-EpOME以避免敏化介導疼痛的神經元而以另外方式實現。本發明的這些9,10-EpOME拮抗劑優選為小分子(但也可為蛋白或肽(例如,抗體或其片段)),其結合9,10-EpOME並抑制對TRPV1的敏化。
就此而言,以上描述的CYP拮抗劑的用途的具體實施方案也適用於本發明的9,10-EpOME拮抗劑,特別是涉及所述預防或治療以及化療的實施方案。
該問題又通過一組合來實現,該組合包括(i)CYP拮抗劑或9,10-EpOME拮抗劑以及(ii)用於在預防或治療疾病中同時或順序使用的化療劑,其中該疾病選自增生性病症,例如癌症,或疼痛,例如CIPNP。
在本文中,術語「增生性病症」在廣義上包括任何需要控制細胞周期的病症,例如心血管病症如再狹窄和心肌病,自身免疫病症如腎小球腎炎和類風溼性關節炎,皮膚病症如牛皮癬,抗炎、抗真菌、抗寄生物病症如瘧疾、肺氣腫和脫髮。在這些病症中,本發明的化合物可以根據需要在期望的細胞中誘導凋亡或保持停滯。優選地,該增生性病症為癌症或白血病,最優選乳腺癌、肺癌、前列腺癌、膀胱癌、頭頸癌、結腸癌、卵巢癌、子宮癌、肉瘤或淋巴瘤。
本實施方案還涉及治療患有疼痛的受試者組,其中受試者在接受化療劑治療。因此,本發明的CYP拮抗劑可以在癌症治療的同時期施用,或者在之前或之後進行,這可為優選的,以避免累積的不良反應。當本發明的CYP拮抗劑的生理效應和化療劑的疼痛誘導在有需要這種治療的受試者中組合時,實現了本發明的結果。在治療期間的最後一劑藥物給藥後,該藥物誘導的生理效應將不會立即消失,而最可能是之後消失。因此,在順序的治療周期中使用本發明的拮抗劑,例如本發明的拮抗劑不是同時而是在化療之前給藥,則仍在患者內導致兩種化合物的臨床效果的組合,因此落入本發明的組合治療的含義內。
術語「組合」在本上下文中指製劑中的兩種或更多種活性物質的活性物質組合,也指治療性處理中彼此以特定間隔施用的活性物質各個製劑意義上的組合。因此,術語「組合」應包括兩種或多種治療上有效的化合物的共給藥,如在本發明上下文中所描述的。
共施用:在本申請上下文中,兩種或更多種化合物的共施用定義為在一年內給患者施用兩種或更多種化合物,包括分開施用兩種或更多種藥物(每種含有化合物的一種),以及同時施用,無論兩種或更多個化合物是組合在一種製劑中,還是它們處於兩種或更多種分開的製劑中。
在一個實施方案中,本發明的組合包括(i)和(ii),通過在所述預防或治療期間給受試者順序或同時施用來組合,優選其中拮抗劑和化療劑在所述預防或治療期間同時施用。
化療劑優選選自基於嘧啶酮的抗腫瘤藥,例如阿糖胞苷、5-氟尿嘧啶,或鉑劑,例如順鉑,或紫杉烷類,例如紫杉醇或多西他賽,或它們的衍生物。最優選的化療劑為紫杉醇或多西他賽。
本文描述的發明的拮抗劑優選選自由抑制性RNA、抑制性抗體或其片段、和/或小分子組成的化合物組。下文提供了對優選的CYP拮抗劑的詳細描述。
在本發明上下文中,還優選給所述受試者施用至少一種另外的對疼痛有效的治療劑,例如嗎啡、阿片類或非阿片類鎮痛劑或其它鎮痛劑。
在本發明的另一方面,提供了在受試者中預防或治療疼痛的方法,該方法包括給所述受試者施用治療有效量的本發明的CYP拮抗劑或9,10-EpOME拮抗劑的步驟。該CYP拮抗劑優選選自CYP1A、CYP2B、CYP2C、CYP2E和CYP2J拮抗劑。該CYP2J拮抗劑優選為CYP2J2的哺乳動物同源物的拮抗劑(CYP2J2拮抗劑),優選人CYP2J2的拮抗劑,例如特非那定、替米沙坦、以及它們的生物類似物或衍生物。
其它優選的CYP拮抗劑選自雌二醇、鹽酸酚苄明、氯雷他定、丙酸氯倍他索、多沙唑嗪甲磺酸鹽、非諾貝特、左炔諾孕酮、阿立哌唑、哈西奈德、替米沙坦、氯苯吩嗪、左旋甲狀腺素鈉、阿洛司瓊鹽酸鹽、醋酸氟輕鬆、碘塞羅寧鈉、美克洛嗪二鹽酸鹽和特非那定。
在前述方法背景下可治療的疾病在上文中有描述。
在治療或預防期間,優選給所述患者施用至少一種另外的對疼痛有效的治療劑,例如其它的鎮痛劑,例如阿片類或非阿片類鎮痛劑。
接著,本發明的另外方面涉及增加受試者中瞬時受體電位香草酸亞型1(TRPV1)的敏感度的方法,包括給所述受試者施用治療有效量的9,10-EpOME或CYP2J2激動劑。
在本發明背景下,令人驚訝地發現9,10-EpOME敏化TRPV1通道蛋白,而其為疼痛感覺的主要介質。因此,在優選的實施方中,本發明提供了作為TRPV1激動劑的9,10-EpOME,這在醫藥中是尤其有用的。9,10-EpOME和TRPV1激動劑辣椒素的組合顯著增強辣椒素活性。一個實施方案例如涉及治療以病理性抑制的疼痛感覺或以疼痛不敏感為特徵的疾病。
在另一實施方案中,9,10-EpOME可以用在增強TRPV1激動劑如辣椒素的活性的方法中。辣椒素作為鎮痛劑用在局部軟膏、鼻噴劑、以及皮膚貼劑中以緩解疼痛。其可以以乳膏形式應用,用於暫時緩解肌肉和關節炎受累關節的小痛和疼痛、背痛、拉傷和扭傷,通常在具有其他發紅劑的化合物中。其還用於減輕外周神經病變的症狀,例如由帶狀皰疹引起的帶狀皰疹後神神經痛。
辣椒素的鎮痛和/或抗炎效果的發生機制通過模擬燒灼感覺而得到支持;通過鈣內流壓倒神經,導致傷害感受器脫敏和/或凋亡,並由此使得神經在增長的時間段內不能報告疼痛。長期暴露於辣椒素下,神經元的傷害感受器經歷凋亡,導致疼痛感覺減弱並阻斷神經源性炎症。如果去除了辣椒素,則傷害感受性神經元隨時間逐漸恢復。因此,本發明的9,10-EpOME的使用可以大大增強辣椒素和相關化合物的醫療效果,或者可以幫助減少辣椒素劑量。
因此,在本發明的優選實施方案中,提供了在受試者中治療疾病的方法,包括施用治療有效量的(i)9,10-EpOME或CYP2J2激動劑和(ii)TRPV1激動劑。至於順序或同時使用治療劑,可參照上文的說明,它們一樣地應用於本發明的這個方面。
疾病優選選自神經病理性疼痛(包括與糖尿病性神經病變、帶狀皰疹後神經痛、HIV/AIDS、創傷性損傷、複雜性區域疼痛症候群、三叉神經痛、紅斑性肢痛和幻覺痛相關的疼痛)、混合傷害性和/或神經病理性混合病因產生的疼痛(例如,癌症)、骨關節炎、纖維肌痛、腰痛、炎性痛覺過敏、外陰前庭炎或外陰疼痛、竇息肉間質性膀胱炎、神經源性膀胱或膀胱過動症、前列腺增生、鼻炎、手術、創傷、直腸過敏、灼口綜合症、口腔黏膜炎、皰疹(或其它病毒感染)、前列腺肥大、皮炎、瘙癢、癢、耳鳴、牛皮癬、疣、癌症、頭疼、以及皺紋。通常,包括任何可通過TRPV1激動劑治療的疾病。
本發明的示例性和優選的TRPV1激動劑選自辣椒素、胡椒鹼、6-姜酚、6-姜烯酚、α-山椒素、β-山椒素、γ-山椒素、δ-山椒素、羥基α-山椒素以及羥基β-山椒素。
於是,另一方面涉及9,10-EpOME或CYP2J2激動劑在上述方法中的應用。
再一方面涉及(i)9,10-EpOME或CYP2J2激動劑和(ii)TRPV1激動劑的組合在醫藥中的應用,優選在治療選自神經病理性疼痛(包括與糖尿病性神經病變、帶狀皰疹後神經痛、HIV/AIDS、創傷性損傷、複雜性區域疼痛症候群、三叉神經痛、紅斑性肢痛和幻覺痛相關的疼痛)、混合傷害性和/或神經病理性混合病因產生的疼痛(例如,癌症)、骨關節炎、纖維肌痛、腰痛、炎性痛覺過敏、外陰前庭炎或外陰疼痛、竇息肉間質性膀胱炎、神經源性膀胱或膀胱過動症、前列腺增生、鼻炎、手術、創傷、直腸過敏、灼口綜合症、口腔黏膜炎、皰疹(或其它病毒感染)、前列腺肥大、皮炎、瘙癢、癢、耳鳴、牛皮癬、疣、癌症(特別是皮膚癌)、頭疼、以及皺紋的疾病中的應用。
該TRPV1激動劑優選選自辣椒素、胡椒鹼、6-姜酚、6-姜烯酚、α-山椒素、β-山椒素、γ-山椒素、δ-山椒素、羥基α-山椒素以及羥基β-山椒素。
根據本文描述的發明,受試者優選哺乳動物,優選人,最優選接受化療治療的人,例如癌症患者。
CYP-拮抗劑
在本發明上下文中,「CYP拮抗劑」優選選自CYP1A、CYP2B、CYP2C、CYP2E、以及更優選的CYP2J拮抗劑。最優選地,該CYP拮抗劑為CYP2J2的哺乳動物同源物的拮抗劑(CYP2J2拮抗劑),優選人CYP2J2的拮抗劑。因此,在本文描述的發明的最優選的實施方案以及方面中,術語「CYP拮抗劑」為CYP2J2拮抗劑或人CYP2J2的哺乳動物同源物的拮抗劑。
在本文中,術語「CYP拮抗劑」指引起CYP表達或活性的量或速率降低的物質。這種物質可直接例如通過結合CYP和降低CYP表達或活性的量或速率來起作用。CYP拮抗劑還可降低CYP表達或活性的量或速率,例如通過結合CYP以使得減弱或防止CYP與CYP受體的相互作用;通過結合併修飾CYP,例如通過去除或添加一部分;以及通過結合CYP並降低其穩定性。CYP拮抗劑也可間接地起作用,例如通過結合調節分子或基因區域以調控調節蛋白或基因區域功能,並引起CYP表達或活性的量或速率的降低。因此,CYP拮抗劑可通過任何導致CYP表達或活性的量或速率的降低的機制起作用。
CYP拮抗劑可例如為天然或非天然存在的大分子,例如多肽、肽、肽模擬物、核酸、碳水化合物或脂質。CYP拮抗劑還可為抗體、或其抗原結合片段,例如單克隆抗體、人源化或人抗體、嵌合抗體、微抗體、雙功能抗體、單鏈抗體(scFv)、可變區片段(Fv或Fd)、Fab或F(ab)2。CYP拮抗劑還可為特異於CYP的多克隆抗體。CYP拮抗劑還可為天然存在的大分子的部分或完全合成的衍生物、類似物或模擬物,或小有機或無機分子。
作為抗體的CYP拮抗劑可例如為結合CYP並抑制與CYP受體結合的抗體,或者改變調節CYP表達或活性的分子的活性以使CYP表達或活性的量或速率降低的抗體。用在本發明方法中的抗體可為天然存在的抗體,包括單克隆或多克隆抗體或其片段,或者非天然存在的抗體,包括但不限於,單鏈抗體、嵌合抗體、雙功能抗體、互補決定區移植(CDR移植)抗體和人源化抗體或它們的抗原結合片段。
作為核酸的CYP拮抗劑可例如為反義核苷酸序列、RNA分子、或適體序列。反義核酸序列可結合細胞內的核苷酸序列並調控CYP的表達水平,或者調控另一控制CYP的表達或活性的基因的表達。類似地,諸如催化性核酶的RNA分子可結合併改變CYP基因或控制CYP的表達或活性的其它基因的表達。適體為具有能夠結合分子靶標的三維結構的核酸序列。
作為核酸的CYP-拮抗劑還可為用在RNA幹擾方法中的雙鏈RNA分子。RNA幹擾(RNAi)為通過轉錄後RNA降解進行的序列特異性基因沉默過程,其由在序列上與所沉默的基因同源的雙鏈RNA(dsRNA)起始。適用於RNAi的雙鏈RNA含有對應待靶向基因的約21個連續胺基酸的正義和反義鏈,它們形成19個RNA鹼基對,在每個3'末端留下兩個核苷酸的突出端(Elbashir等,Nature 411:494-498(2001);Bass,Nature 411:428-429(2001);Zamore,Nat.Struct.Biol.8:746-750(2001))。約25至30個核苷酸的dsRNA也已成功的用於RNAi(Karabinos等,Proc.Natl.Acad.Sci.USA 98:7863-7868(2001)。dsRNA可在體外合成,並通過本領域的已知方法導入細胞。
優選的CYP2J2拮抗劑選自雌二醇、鹽酸酚苄明、氯雷他定、丙酸氯倍他索、多沙唑嗪甲磺酸鹽、非諾貝特、左炔諾孕酮、阿立哌唑、哈西奈德、替米沙坦、氯苯吩嗪、左旋甲狀腺素鈉、阿洛司瓊鹽酸鹽、醋酸氟輕鬆、碘塞羅寧鈉、美克洛嗪二鹽酸鹽和特非那定。
治療或預防疼痛或其它神經病症的組合物和試劑盒。
本申請的另一方面涉及通過採用本發明的化合物或組合來治療或預防疼痛或增生性病症的組合物和試劑盒。在一個實施方案中,該組合物包括上文描述的化合物,其中所述化合物優選選自抗體、抗體片段、短幹擾RNA(siRNA)、適體、合成抗體(synbody)、結合劑、肽、適體-siRNA嵌合體、單鏈反義寡核苷酸、三鏈體形成寡核苷酸、核酶、外在引導序列、試劑編碼表達載體(agent-encoding expression vector)、小分子以及藥學上可接受的載體。
在本文中,用語「藥學上可接受的載體」旨在包括與藥物施用相符的任何和所有的溶劑、增溶劑、填充劑、穩定劑、粘結劑、吸附劑、鹼、緩衝劑、潤滑劑、控釋載體、稀釋劑、乳化劑、溼潤劑、潤滑劑、分散介質、塗層、抗菌或抗真菌劑、等張和吸收延緩劑,等等。將這些介質和試劑用於藥學上有活性的物質在本領域內是公知的。除了任何常規媒介物或試劑與該活性化合物不相容之外,考慮將其用在該組合物中。補充劑也可摻入到該組合物中。在某些實施方案中,該藥學上可接受的載體包括血清白蛋白。
本發明的藥物組合物配製為與其預期的施用途徑相容。施用途徑的實例包括胃腸外施用,例如鞘內、動脈內、靜脈內、皮內、皮下施用,口服,透皮(局部)和跨黏膜施用。
用於胃腸外、皮內或皮下應用的溶液或混懸液可包括以下組分:無菌稀釋劑如注射用水,鹽水溶液,不揮髮油,聚乙二醇,甘油,丙二醇或其它合成溶劑;抗菌劑例如苯甲醇或對羥基苯甲酸甲酯;抗氧化劑例如抗壞血酸或硫酸氫鈉;螯合劑例如乙二胺四乙酸;緩衝劑例如乙酸鹽,檸檬酸鹽或磷酸鹽以及用於調節張力的試劑如氯化鈉或葡萄糖。可用酸或鹼調節pH,例如鹽酸或氫氧化鈉。胃腸外配製物可封在安瓿瓶、一次性注射器或多重劑量小瓶中,它們由玻璃或塑料製成。
適合於可注射使用的藥物組合物包括無菌水溶液(當水溶時)或混懸液以及用於臨時製備無菌可注射溶液或混懸液的無菌粉末。對於靜脈內施用,適合的載體包括生理鹽水、抑菌水、商品名為Cremophor ELTM的物質(BASF,Parsippany,N.J.)或磷酸鹽緩衝鹽水(PBS)。所有情況下,可注射組合物應為無菌的,並且應為流體,其程度為易於注射。其在生產和保存條件下必須是穩定的,並且必須對微生物如細菌和真菌的汙染作用防腐。載體可為溶劑或分散介質,含有例如水、乙醇、多元醇(例如,甘油、丙二醇、以及液體聚乙二醇,等)、或它們的適當混合物。例如通過使用諸如卵磷脂的塗層、對於混懸液的情況通過維持所需的粒徑以及通過使用表面活性劑可維持適當的流動性。預防微生物作用可通過各種抗菌和抗真菌劑來實現,例如,對羥基苯甲酸酯、氯丁醇、酚、抗壞血酸、硫柳汞,等。很多情況下,優選在組合物中包括等張劑,例如,蔗糖、多元醇如甘露醇、山梨醇和氯化鈉。可注射組合物的長時間吸收可通過在組合物中包括進延緩吸收的試劑來實現,例如單硬脂酸鋁和明膠。
可通過將活性化合物(例如,神經調節蛋白)以所需量與以上列出的成分的一種或組合摻入適合的溶劑中,然後無菌過濾(需要的話),來製備無菌可注射溶液。通常,通過將活性化合物摻入含有基礎分散介質和所需的來自以上列出成分的其它成分的無菌載體中來製備分散體。對於用於製備無菌可注射溶液的無菌粉末的情況,優選的製備方法為真空乾燥和冷凍乾燥,其產生活性成分加上任何額外所需成分(來自其之前無菌過濾的溶液)的粉末。
口服組合物通常包括惰性稀釋劑或可食用載體。它們可包封在明膠膠囊中或壓縮為片劑。出於口服治療施用的目的,活性化合物可與賦形劑一起摻混,並以片劑、含片、或膠囊的形式使用。口服組合物還可採用流體載體來製備,以用作漱口水,其中流體載體中的化合物口服施用,在口中來回,並且吐出或咽下。藥學上相容的粘合劑和/或佐劑材料可作為組合的一部分包括進來。片劑、小丸、膠囊、含片等可含有以下成分或類似性質化合物的任何一種:粘合劑如微晶纖維素、黃蓍膠或明膠;賦形劑如澱粉或乳糖;崩解劑如褐藻酸、羥基乙酸澱粉鈉(Primogel)、或玉米澱粉;潤滑劑如硬脂酸鎂或斯泰特(Stertes);助流劑如膠體二氧化矽;甜味劑如蔗糖或糖精;或調味劑如薄荷、水楊酸甲酯、或橙香精。
對於通過吸入施用,化合物是以氣溶膠噴霧的形式從含有適合的推進劑(例如,諸如二氧化碳的氣體)的壓力容器或分配器或噴霧器遞送。
全身施用也可通過跨黏膜或透皮手段進行。對於跨黏膜或透皮施用,將適合於待滲透屏障的滲透劑用在製劑中。這些滲透劑通常在本領域是已知的,包括例如用於跨黏膜施用的洗滌劑、膽汁鹽、以及梭鏈孢酸衍生物。跨黏膜施用可通過使用鼻噴劑或者栓劑來完成。對於透皮施用,藥物組合物配製為軟膏、藥膏、凝膠、或乳膏,如本領域所公知的。
在某些實施方案中,藥物組合物配製為活性成分的持續或控制釋放。可使用生物可降解的、生物相容的聚合物,例如乙烯醋酸乙烯酯、聚酸酐、聚乙醇酸、膠原、聚原酸酯、以及聚乳酸。用於製備這些製劑的方法對本領域技術人員是顯而易見的。這些材料也可在商業上從例如從阿爾扎(Alza Corporation)和諾華製藥公司(Nova Pharmaceuticals,Inc.)獲得。脂質體混懸液(包括帶有針對病毒抗原的單克隆抗體的靶向感染細胞的脂質體)也可用作藥學上可接受的載體。這些可按照本領域技術人員已知的方法來製備。
特別有利的是,配製單位劑量形式的口服或胃腸外組合物,以方便施用和劑量一致性。單位劑量形式用在本文時包括物理上分開的單位,適合作為單一劑量用於待治療的受試者;每個單位含有預定量的活性化合物,經計算與所需的藥物載體聯合會產生期望的治療效果。本發明單位劑量形式的規格取決於並直接依賴於活性化合物的獨特特徵和待獲得的具體治療效果,以及本領域中配製這種用於個體治療的活性化合物的內在限制。
這些化合物的毒性和治療功效可通過標準藥學程序在細胞培養或試驗動物中確定,例如用於確定LD50(50%群體致死劑量)和ED50(50%群體治療上有效的劑量)。毒性和治療效果的劑量比例為治療指數,其可表示為比例LD50/ED50。顯示出大治療指數的化合物是優選的。儘管可以使用顯示出毒性副作用的化合物,但應考慮設計將這些化合物靶向受累組織位點的遞送系統,以便對非感染細胞的潛在損傷降至最小,並由此減小副作用。
從細胞培養測定和動物研究獲得的數據可用在制定用於人的劑量範圍中。這些化合物的劑量優選處於包括具有微小毒性或沒有毒性的ED50的循環濃度的範圍內。劑量可以在該範圍內隨採用的劑型和使用的施用途徑而變化。對於用在本發明方法中的任何化合物,治療有效劑量可從細胞培養測定初步估計。可在動物模型中制定獲得包括在細胞培養中確定的IC50(即,實現症狀的半數最大抑制的測試化合物的濃度)的循環血漿濃度範圍的劑量。這種信息可用於更精確地確定人類可用劑量。藥物組合物可連同施用說明書包括在容器、包裝盒、或分散器中。
現在將參照附圖和序列在以下實施例中進一步描述本發明,然而並不限於此。出於本發明的目的,本文提到的所有參考文獻都通過引用將它們的全文併入。在附圖中:
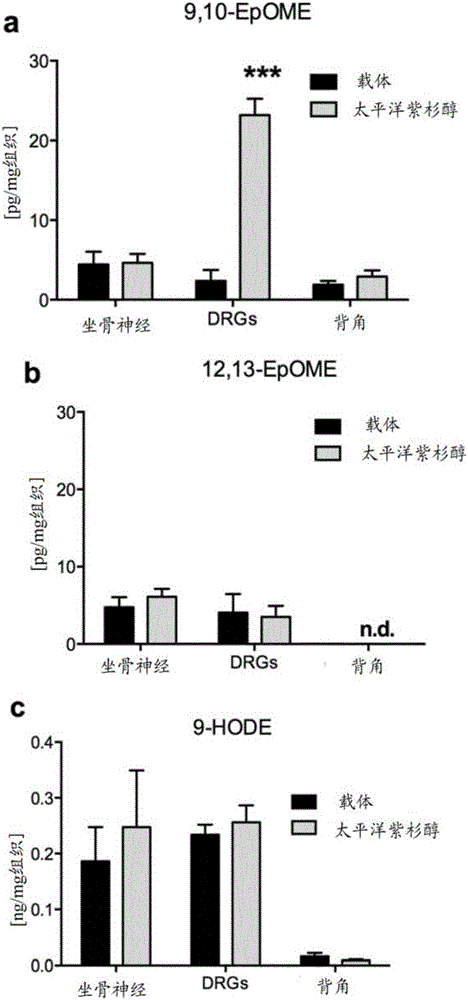
圖1:紫杉醇CIPNP或炎症期間氧化的亞油酸代謝物的濃度。所顯示的為C57B16/N小鼠i.p.注射載體(黑色)或紫杉醇(灰色,6mg·kg-1)24h後,坐骨神經、DRG和脊髓背角中9,10-EpOME(a)和12,13-EpOME(b)的濃度;n.d.:未檢測到。C57B16/N小鼠i.p.注射載體(黑色)或紫杉醇(灰色)24h後,坐骨神經、L4-L6-DRGs和對應的脊髓背角節段中9-HODE(c)和13-HODE(d)的濃度。(e)足底內注射酵母聚糖(12.5mg/ml,20μl)24h後,L4-L6-DRGs和背角的相應節段中的9,10-EpOME濃度關係。數據表示每組8至10隻動物的均值±SEM;***p<0.001,學生t檢驗。
圖2:9,10-EpOME對DRG神經元的直接作用。9,10-EpOME[10μM,30s]的應用在DRG神經元上引起鈣瞬變,其應答於高鉀(50mM KCl,30s)。顯示了代表性描記線。(b)DRG神經元中9,10-EpOME依賴的鈣相對於應答神經元數量增加的劑量反應關係。數據表示每個濃度5次測量的均值±SEM。(c)和(d)在9,10-EpOME刺激前和後2分鐘採用含有EGTA(2mM)的無鈣培養基洗入,可阻斷9,10-EpOME[10μM,30s]引起的鈣瞬變。數據表示24個(無鈣)或16個(對照)神經元的均值±SEM。(e)和(f)9,10-EpOME[10μM,30s]的鈣瞬變可被選擇性TRPV1拮抗劑(AMG 9810,1μM)而不是選擇性TRPA1拮抗劑(HC-030031,20μM)阻斷,這些阻斷劑在第二次9,10-EpOME刺激前2分鐘洗入。數據表示16個(對照)、31個(AMG 9810)或18個(HC-030031)神經元的均值±SEM;**p<0.01,學生t檢驗。
圖3:9,10-EpOME在DRG神經元中劑量依賴性敏化TRPV1,並在脊髓薄片的第二層神經元中增強辣椒素誘導的自發性EPSC頻率的增加。(a)用辣椒素雙刺激DRG神經元(200nM,每次15s),並在第二次辣椒素刺激前用載體或9,10-EpOME[1μM]溫浴2分鐘。(b)採用與(a)中描述相同的規程,第一次和第二次辣椒素應答之間比率的劑量依賴性差異。數據表示以下數量神經元的均值±SEM:27個(對照)、26個(250nM 9,10-EpOME)、21個(500nM 9,10-EpOME)、19個(750nM 9,10-EpOME)、41個(1μM 9,10-EpOME)、18個(2μM 9,10-EpOME)、或28個(採用50μM AITC 20s代替辣椒素);*p<0.05,**p<0.01,***p<0.001學生t檢驗。(c)自發性EPSC(sEPSC)在第二層神經元中的描記線。下方插圖,1、2、3和4為放大的,分別表示對基線、第一辣椒素(1mM)、9,10-EpOME(1mM)、以及第二辣椒素(1mM)加9,10-EpOME的記錄。(d)sEPSC的頻率。與基線sEPSC相比,辣椒素誘導了sEPSC頻率的深入增加(從6.9±0.4Hz和13.7±0.4Hz)。單獨的9,10-EpOME治療稍稍增加sEPSC頻率(8.2±0.8Hz),並由辣椒素顯著增強了該sEPSC頻率增加(18.7±1.1Hz)。*P<0.05,與無治療基線相比;#P<0.05,與第一次辣椒素治療(1mM)相比。n=5個神經元/組。(E)sEPSC的幅度。辣椒素和9,10-EpOME對sEPSC幅度沒有顯著影響。n=5個神經元/組。
圖4:9,10-EpOME在DRG神經元中對TRPV1的敏化由Gs偶聯受體和cAMP-PKA途徑所介導。(a)9,10-EpOME在大鼠DRGs中膜碎片中催化[y-35S]-GTP結合。在30μM GDP和載體(乙酸甲酯,0.7%(v/v))、腺苷[10μM]或9,10-EpOME[1μM]存在30分鐘下,採用大鼠DRGs的膜碎片進行實驗。從來自總共15隻動物的膜碎片的3次測量獲得數據。對於每次測量,將來自5隻動物的DRG合併;*p<0.05,**p<0.01,使用唐恩(Dunn’s)多重比較事後檢驗的克魯斯卡-沃利斯(Kruskal-Wallis)檢驗。(b)在9,10-EpOME、西卡前列素或毛喉素(每種1μM)刺激15分鐘後富含神經元的DRG培養物中的cAMP濃度。數據表示來自5隻小鼠的DRG培養物的均值±SEM。(c)和(d)9,10-EpOME[1μM]對TRPV1的敏化可通過以PKA抑制劑(H89-二鹽酸鹽,10μM,1h)預溫浴而減弱。數據表示15個(載體)、19個(EpOME)或33個神經元(EpOME和H89預溫浴)的均值±SEM。(e)和(f)9,10-EpOME[1μM]對TRPV1的敏化不受PKC抑制劑預溫浴(GF 109203X,10μM,1h)的影響。數據表示18個(載體)、23個(EpOME)或39個神經元(EpOME和GFX預溫浴)的均值±SEM;*p<0.05,**p<0.01學生t檢驗;n.s.非顯著的。
圖5:足底內或鞘內注射9,10-EpOME減弱了野生型小鼠中的疼痛閾值並敏化辣椒素誘導的機械閾值。(a)和(b)C57B1/6N小鼠接受足底內注射9,10-EpOME(10μM)或載體(DMSO鹽水溶液,0.3%(v/v))。在注射後5h監測熱(a)或機械(b)閾值。數據表示來自8隻小鼠的均值±SEM。(c)和(d)野生型BL/6N小鼠鞘內注射9,10-EpOME(10μM)或載體(DMSO鹽水溶液,0.3%(v/v))。在注射後監測熱(c)或機械(d)閾值2h(熱)或3h(機械),第一小時間隔15分鐘,第二小時間隔30分鐘。數據表示來自8隻小鼠的均值±SEM。圖中未包括。
圖6:分離的坐骨神經或富含神經元的DRG培養物在9,10-EpOME刺激後釋放iCGRP。(a)從野生型BL/6N小鼠的分離的坐骨神經釋放iCGRP,用以下溶液刺激,每種5分鐘:合成腸液(SIF)、SIF+EpOME(1μM)或載體(DMSO 0.03%(v/v))、SIF+EpOME(或載體)+辣椒素(500nM),SIF。數據表示來自6個單獨坐骨神經的均值±SEM。在PBS、9,10-EpOME、辣椒素或9,10-EpOME+辣椒素刺激15分鐘後富含神經元的DRG培養物的iCGRP釋放;a:9,10-EpOME 1μM,b:辣椒素400nM,c:9,10-EpOME 2.5μM。數據表示來自6隻小鼠的DRG培養物的均值±SEM;#,*p<0.05,**p<0.01,***p<0.001學生t檢驗。虛線表示測定靈敏度。
圖7:在紫杉醇誘導的神經病理性疼痛中CYP2J6上調。(a)野生型C57Bl/6N小鼠在注射紫杉醇(6mg·kg-1i.p.)後的機械閾值時程。bl:基線,數據表示每組10隻小鼠的均值±SEM。8天後,切下坐骨神經、DRG和脊髓背角。(b)紫杉醇注射(6mg·kg-1i.p.)後8天時鼠科CYP表氧化酶轉錄物的表達。數據表示來自每組4隻小鼠的DRG的均值±SEM;*p<0.05,**p<0.01,學生t檢驗。(c)在C57B16/N小鼠中i.p.注射載體(黑色)或紫杉醇(灰色,6mg·kg-1)後8天時坐骨神經、DRG、和脊髓背角中9,10-EpOME的濃度;**p<0.01,學生t檢驗。(d)通過LC-MS/MS分析揭示的,在紫杉醇治療後8至9天,鼠科DRG中類二十烷酸和亞油酸代謝物合成的方案。結構從網站(lipidmaps.org)獲得。
圖8:特非那定對CYP2J6的抑制在體內減小了脂濃度並緩解了紫杉醇誘導的CIPNP。(a)在紫杉醇(6mg·kg-1i.p.和1mg·kg-1特非那定(灰色)或載體(2%DMSO v/v,黑色))治療後8天時坐骨神經、DRG和脊髓背角中通過LC-MS/MS測定的9,10-EpOME的水平,顯示為對照的百分比。數據表示來自每組5隻小鼠的DRG的均值±SEM;*p<0.05,**p<0.01,學生t檢驗。(b)在特非那定施用(1mg·kg-1)後,所有測量的環氧化脂類和二氫代謝物(9,10-EpOME、12,13-EpOME、9,10-DiHOME、12,13-DiHOME和14,15-EET)在坐骨神經、DRGs、脊髓背角和血漿中的剩餘濃度。(c)經紫杉醇治療8天(6mg·kg-1i.p.)並接受了特非那定(1或2mgkg-1)或載體(DMSO 2.5or 5%(v/v))靜脈內注射的小鼠的機械閾值。在注射特非那定或載體後監測機械閾值長至5h。數據表示每組8至9隻小鼠的均值±SEM;#,*p<0.05,使用邦費羅尼(Bonferroni)事後檢驗的雙因素ANOVA(*1mg kg-1,#2mg kg-1特非那定)。(d)在紫杉醇注射後8天(6mg·kg--1i.p.)並接受了氯雷他定(1mg kg-1)或載體(DMSO 2.5or 2.5%(v/v))靜脈內注射的小鼠的機械閾值。數據表示每組6至9隻小鼠的均值±SEM。
圖9:計算的CYP2J2和CYP3A4的抑制值的相關性。位於左上象限的拮抗劑為CYP2J2選擇性的。根據製造商的規程進行發光CYP2J2測定(https://www.promega.de/resources/pubhub/enotes/cytochrome-p450-2j2-enzyme-assay-using-a-novel-bioluminescent-probe-substrate/)。為了測試候選CY2J2拮抗劑的選擇性,採用了特異於CYP3A4的另外的發光CYP測定,並將候選CYP2J2拮抗劑的抑制活性與該相同拮抗劑對CYP3A4的抑制活性進行比較。
SEQ ID NO:1至14:引物序列
實施例
材料與方法
動物
所有的動物實驗都按照國立衛生研究院的實驗動物護理和使用指南中的建議進行,並得到當地動物研究倫理委員會(Darmstadt)的批准,許可號碼F95/42。對於所有的行為實驗,發明人僅使用購自商業飼養公司(Charles River,Sulzfeld,Germany,Janvier,Le Geneset-Saint-Isle,FR)的6至12周齡的C57BL/6N小鼠。為了比較機械閾值,發明人採用了年齡和性別匹配的同窩小鼠作為對照。
前列腺素受體缺陷小鼠(DPI-/-、IP-/-、EP2-/-和EP4-/-)飼養在法蘭克福的臨床藥理學研究所(Institute of Clinical Pharmocology,Frankfurt),如之前所描述的。
化療誘導的神經病理性疼痛的紫杉醇模型
將紫杉醇溶解在1:1的聚氧乙烯蓖麻油(Cremophor EL)/乙醇中,並在鹽水中稀釋。腹膜內注射的劑量設置為6mg/kg,如之前所描述的。
行為測試
為了確定機械性觸痛或熱超敏,將小鼠保持在升高的格子上的試驗籠中至少2h,以讓它們適應。採用動態足底觸覺計或商品名為Hargreaves的裝置(Ugo Basile,Comerio,VA,Italy)進行基線測量,檢測機械刺激後後爪的收縮潛伏期。對於機械閾值的評估,將鋼杆推向後爪中部足底,壓力線性增加(10秒內0-5g,增加0.5g/s),直至出現快速的收縮反應。不對爪的緩慢移動計數。以秒±0.1確定爪收縮潛伏期(PWL),截止時間20s。非注射和注射爪輪流測量,間隔5至10min。為了確定熱閾值,將小鼠在第一天保持在升溫的玻璃板(32℃)上的試驗籠中至少2h,以讓它們適應。接著,用高強度投射燈構成的輻射熱設備刺激爪的中部足底區域,直至發生收縮。非注射和注射爪輪流測量,間隔5至10min。對於所有的行為測試,研究者都不知小鼠的治療或基因型。
治療:對於外周注射,將20ul的9,10-EpOME[5μM](Cayman,Ann Arbor,MI,USA)皮下(s.c.)注射進後爪的中部足底區域。對照動物接受相應體積的DMSO(Sigma,Deisenhofen,Germany;鹽水中1.6%(v/v))。對於鞘內注射,通過在清醒、有意識小鼠中直接腰椎穿刺來注射3.2%DMSO/鹽水(v/v)中的5ul 9,10-EpOME[10μM]。在尾靜脈中靜脈注射特非那定或氯雷他定(二者都來自Tocris,Bristol,UK)。
原發性背根神經節(DRG)培養
將鼠科DRG從脊髓節段切下並直接轉移到含有CaC12和MgC12(Invitrogen,Carsbad,CA,USA)的冰冷HBSS中。接著,在37℃將分離的DRG在含有L-穀氨醯胺[2mM]青黴素(100U/ml)、鏈黴素(100μg/ml)、B-27和慶大黴素(50μg/ml)(都來自Invitrogen,Carlsbad,CA,USA)的神經基的(neurobasal)培養基中與膠原酶/分散酶(500U/ml膠原酶;2.5U/ml分散酶)溫浴75min。在去除膠原酶/分散酶溶液後,用含有10%FCS的神經基的培養基清洗細胞兩次,並以0.05%胰蛋白酶(Invitrogen,Carlsbad,CA,USA)溫浴10min。重複清洗步驟,並用1ml吉爾森吸管將細胞機械解離。最終,將神經元置於聚L-賴氨酸(Sigma,Deisenhofen,Germany)包被的蓋玻片上,並以含有L-穀氨醯胺[2mM]青黴素(100U/ml)鏈黴素(100μg/ml)、B-27和慶大黴素(50μg/ml)的神經基的培養基溫浴過夜,直至通過鈣成像評估。
鈣成像實驗
採用兩種不同的方案來進行鈣成像實驗。首先,發明人採用帶有10x蔡司(Achroplan)水浸物鏡(Zeiss)的阿克斯科普2(Axio scope 2)正置顯微鏡(Zeiss,Jena,Germany)。該顯微鏡配備有伊梅戈(Imago)CCD相機和多色IV(Polychrome IV)單色器(都來自TILL Photonics,Grafelfmg,Germany)。在兩個波長(340nm和380nm)每2秒獲得圖像,並採用提爾維森(Tillvision)軟體23處理。隨後,採用了萊卡(Leica)鈣成像方案,其由配備了DFC360FX(CCD-)相機、芙拉2(Fura-2)濾鏡和N-普蘭(N-Plan)10x/0.25Ph1物鏡的萊卡(Leica)DMI 4000b倒置顯微鏡(都來自Leica Microsystems,Wetzlar,Germany)構成。每2秒照相,並採用LAS AF軟體處理。對於每個實驗,發明人選擇具有大量細胞的區域並同時監測40-110個細胞。採用製備後24-48小時的DRG神經元進行鈣成像實驗。讓細胞加載5μM芙蘭2(fura-2)-AM酯和0.02%普朗尼克(Pluronic)F-127(二者來自Biotium,Hayward,CA),並在37℃溫浴30至60min。然後,以外部溶液(以mM為單位,含有:NaCl[145]、CaCl2[1.25]、MgCl2[1]、KCl[5]、D-葡萄糖[10]、HEPES[10];調整至pH 7.3)洗滌細胞。在外部溶液中以1至2ml/min的流速進行基線測量。通過去除CaC12並添加EGTA[2mM]來產生無鈣溶液,通過將NaCl濃度增加至150mM來進行滲透壓控制。將HC-030031(Sigma,Deisenho-fen,Germany)、AMG 9810,H89-二鹽酸鹽、8-溴-cAMP、GF 109203X(都來自Tocris,Bristol,UK)和NGF(Merck Millipore,Darmstadt,GE)的儲備液在外部溶液中稀釋至它們的最終濃度。
定量實時PCR
在指出的時間點從小鼠切下腰部DRG,並採用商品名為mirVanaTM的miRNA分離試劑盒(Ambion,life technologies,Carlsbad,CA,USA)提取RNA。採用商品名為的系統(lifetechnologies,Carlsbad,CA,USA)進行逆轉錄和實時PCR,並按之前所描述的用AAC(T)方法評估24,25。以下的寡核苷酸用於cDNA的擴增:
表1:用於從鼠科組織進行定量實時PCR的引物序列,a=MGH引物庫,ID:160948617c2。
通過液相色譜-串聯質譜法(LC-MS/MS)確定EET
樣品提取和標準品:按之前所描述的方式進行樣品提取。簡言之,在甲醇中製備含有2500ng/ml所有分析物的儲備溶液。通過進一步稀釋獲得工作標準品,對於EET、EpOME和DiHOME以及HODE濃度範圍為0.1-250ng/ml。通過液液萃取進行樣品提取。因此,用600ul乙酸乙酯將組織或細胞培養培養基萃取兩次。在柔和的氮氣流下,於45℃的溫度去除合併的有機相。將殘留物以50ul的甲醇/水(50:50,v/v)重建,10,000xg離心2min,然後在注入LC-MS/MS系統前轉移到玻璃瓶(Macherey-Nagel,Duren,Germany)中。
測量環氧脂類和HODE的儀器:該LC-MS/MS系統由API 4000三重四極杆質譜儀(Applied Biosystems,Darmstadt,Germany)構成,配備有負ESI模式操作的圖伯-V-源(Turbo-V-source)、安捷倫1100(Agilent 1100)雙HPLC泵和脫氣器(Agilent,Waldbronn,Germany)以及帶有25ulLEAP注射器的HTC Pal自動加樣器(Chromtech,Idstein,Germany)。用於質譜的高純度氮通過NGM 22-LC-MS氮發生器(cmc Instruments,Eschbom,Germany)產生。對於色譜分離,使用了基迷你(Gemini)NX C18柱和前置柱(150mm x 2mm i.d.,5μM粒徑和孔徑,來自Phenomenex,Aschaffenburg,Germany)。採用線性梯度,流動相流速0.5ml/min,總運行時間17.5分鐘。流動相A為水/氨(100:0.05,v/v),B為乙腈/氨(100:0.05,v/v)。在12min內,讓梯度從85%A開始,直至10%。保持10%A 1min。在0.5min內,讓流動相移回85%A並保持3.5min以平衡色譜柱,用於下一樣品。樣品的注射體積為20ul。以分析軟體(Analyst Software)V 1.4.2(Applied Biosystems,Darmstadt,Germany)採用內標法(同位素稀釋質譜法)進行定量。將分析物峰面積和內標面積的比例(y軸)對濃度(x軸)作圖,通過最小二乘回歸計算標準曲線,以1/濃度2加權。
[35S]GTPγS結合測定
為了測量對預測的G蛋白偶聯受體的激活,採用1μM 9,10-EpOME(Cayman,Ann Arbor,MI,USA)和新制的[35S]GTPγS(1250Ci/mmol,Perkin Elmer,Waltham,MA,USA)對成年大鼠的DRG的膜製備物進行了GTPγS結合測定法。
iCGRP的測量
按之前的描述32,採用CGRP-酶免疫測定試劑盒(SpiBio,Bertin pharma,France)進行CGRP測量。對於來自DRG培養物的CGRP測量,將野生型BL/6N小鼠的DRG切下並按上文所述處理,並在48孔板中培養過夜。
數據分析和統計
所有的數據都表示均值±s.e.m。為了確定所有行為實驗中的統計學顯著差異,使用用於重複測量的方差分析(ANOVA),接著採用商品名為GraphPad Prism的軟體進行事後邦費羅尼校正。對於僅兩組比較的體外實驗,進行學生t檢驗。P<0.05被認為是統計上顯著的。
細胞色素P450螢光素酶測定
按照製造商的說明書進行CYP2J2和CYP3A4Glo測定(P450-GloTM,Promega)。
CYP2J2測定規程:
-採用商品名為MultiDrop的產品來製備CYP2J2-酶(2nM)/螢光素-2J2/4F12底物(2μM)混合物,5μl/孔,
-採用商品名為Echo的產品添加50nl/孔的化合物(10μM終濃度)/DMSO(0.5%終濃度)
-在37℃溫浴30min
-採用商品名為MultiDrop的產品添加NADPH再生溶液,5μl/孔
-在37℃溫浴30min
-採用商品名為MultiDrop的產品添加LDR-酯酶溶液,10μl/孔
-在37°溫浴30min,在讀取物(EnSpire)上讀出發光值
CYP3A4測定規程:
-採用商品名為MultiDrop的產品製備CYP3A4-酶(2nM)/螢光素-IPA底物(7μM)混合物,5μl/孔,
-採用商品名為Echo的產品添加50μl/孔的化合物(10μM終濃度/DMSO(0.5%終濃度)
-在37℃溫浴30min,
-採用商品名為MultiDrop的產品添加NADPH再生溶液,5ul/孔
-在37℃溫浴30min,
-採用商品名為MultiDrop的產品添加LDR-酯酶溶液,10μl/孔
-在37°溫浴30min,並在讀取物(EnSpire)上讀出發光值。
實施例1:化療誘導的神經病理性疼痛中的CYP衍生脂質
為了研究CYP衍生脂質是否可以在化療誘導的神經病理性疼痛中起作用,發明人將紫杉醇或載體注射進野生型BL/6N小鼠中,並在注射後24小時切下坐骨神經、DRG和脊髓背角。採用LC-MS/MS確定脂質濃度。發現是氧化的亞油酸代謝物9,10-EpOME的濃度(圖1A),而不是其姊妹脂質12,13-EpOME(圖1B)或他們的二氫代謝物9,10-和12,13-DiHOME(參見補充圖1)在DRG中強烈升高(圖1A)。還定量了9-和13-HODE的水平(圖1C,1D),它們在炎性疼痛期間產生,為TRPV1的內源性激活因子33。但是,發明人不能在紫杉醇處理後檢測到它們水平的任何差異。為了研究DRG中增加的9,10-EpOME濃度是否是紫杉醇處理特異性的,將酵母聚糖注射進野生型BL/6N小鼠的後爪,以誘導炎性疼痛。在注射後24h炎症高峰時,切下L4-L6-DRG和對應的背角節段。通過LC-MS/MS的脂質定量未揭示炎性疼痛期間9,10-EpOME水平的任何差異(圖1E)。
接著,發明人在鈣成像實驗中就9,10-EpOME對DRG神經元的影響進行了表徵。發明人觀察到,用10μM 9,10-EpOME短刺激30s在DRG神經元中引起鈣瞬變(圖2A)。發明人進行了劑量反應分析以研究9,10-EpOME引發鈣瞬變的效力,發現最多10.3%的DRG神經元應答25μM的9,10-EpOME,對於更高濃度,應答神經元百分比沒有顯著增加(圖2B)。為了分析9,10-EpOME引起的鈣瞬變是由細胞內鈣存儲的釋放還是由細胞外鈣的內流所導致的,發明人使用了含有2mM EGTA的無鈣外部溶液,並用10μM 9,10-EpOME刺激DRG神經元兩次,每次30s。在第二次刺激之前兩分鐘,洗入無鈣外部溶液,則神經元不再應答9,10-EpOME,由此表明9,10-EpOME導致外部鈣內流(圖2C,2D)。用於神經元的陽性對照為50mM KCl 30s的終刺激。
為了鑑定所涉及的離子通道,使用TRPV1(AMG 9810,1μM)和TRPA1(HC-030031,20μM)的選擇性拮抗劑,以便阻斷9,10-EpOME導致鈣內流。用9,10-EpOME(10μM,30s)刺激DRG神經元兩次,並在第二次9,10-EpOME刺激之前用TRP通道拮抗劑預溫浴細胞兩分鐘。發明人觀察到,是選擇性TRPV1拮抗劑AMG 9810,而不是TRPA1拮抗劑HC-030031可阻斷第二次9,10-EpOME引起的鈣瞬變,表明TRPV1為9,10-EpOME的靶向通道(圖2E,2F)。
實施例2:9,10-EpOME敏化TRPV1
然後,發明人分析了9,10-EpOME在較低的和更生理的濃度(1μM)下是否也能夠敏化TRPV1或TRPA1。由此,發明人用辣椒素刺激DRG神經元兩次(200nM,15s),並在第二次辣椒素刺激前用9,10-EpOME[1μM]或載體溫浴細胞兩分鐘,觀察到經9,10-EpOME溫浴的DRG神經元對辣椒素的顯著強烈的應答,表明9,10-EpOME敏化TRPV1(圖3A)。為了研究9,10-EpOME依賴性TRPV1敏化的效力,採用250nM至2μM的9,10-EpOME濃度進行了劑量反應分析。觀察到與載體相比的第二次辣椒素應答幅度的劑量依賴性增加。這種效應看起來特異於TRPV1,因為芥末油依賴的TRPA1應答不被9,10-EPOME[1μM]敏化(圖2B)。
為了用電生理手段確認9,10-EpOME對TRPV1敏化的作用,發明人採用兩次辣椒素刺激[1μM]並在第二次辣椒素刺激之前用9,10-EpOME[1μM]溫浴細胞,測量了來自脊髓切片的流明II(lumina II)神經元的sEPSC(圖3C)。單獨的9,10-EpOME處理稍稍增加sEPSC的頻率。但是,與辣椒素組合時,sEPSC頻率強烈增加(圖3D)。然而,無論是9,10-EpOME、TRPV1,還是兩種物質的組合,都沒有觀察到sEPSC的幅度差異(圖3E)。
因為已知脂質介導的TRPV1敏化大多數涉及到G蛋白偶聯受體的激活,發明人進行了GTPγS測定,以分析9,10-EpOME是否能夠在DRG中激活GPCR,並在用1μM 9,10-EpOME溫浴後觀察到顯著增加的GTPγS信號(圖4A)。為了鑑定9,10-EpOME介導的TRPV1敏化的機制,發明人接著測量了經載體、9,10-EpOME、IP受體激動劑西卡前列素或毛喉素[每種1μM]刺激15分鐘的富含神經元的DRG培養物中的cAMP。有趣的是,發明人觀察到,與其載體相比,9,10-EpOME引起了cAMP濃度的顯著增加(圖4B)。這些結果表明了9,10-EpOME對蓋爾菲斯(Galphas)偶聯受體的激活。
由於TRPV1可被PKA和PKC磷酸化,二者導致該通道增加的活性和敏化35,所以發明人在鈣成像實驗中用培養的來自野生型BL/6N小鼠的DRG神經元研究了PKA或PKC抑制劑是否可減弱9,10-EpOME引起的TRPV1敏化。發明人採用與上文提到的相同規程(兩次辣椒素刺激,之間用9,10-EpOME溫浴)可重複辣椒素依賴的TRPV1敏化。但是,發明人觀察到,用PKA-抑制劑(H89二鹽酸鹽,10μM,1h)預溫浴導致9,10-EpOME引起的TRPV1敏化的顯著減弱(圖4C,4D)。在相同條件下(10μM,預溫浴1h)使用PKC-抑制劑GF 109203X(GFX)對9,10-EpOME引起的TRPV1敏化無任何影響(圖4E,4F),由此表明9,10-EpOME引起PKA-而不是PKC-介導的TRPV1敏化。
發明人接著在鈣成像實驗中測試了蓋爾菲斯(Galphas)偶聯的前列腺素受體參與9,10-EpOME依賴的TRPV1敏化的可能性。前列腺素受體對它們的配體前列腺素類具有不同的特異性,也可能由其它的脂質激活。但是,發明人未能在前列腺素E受體EP2和EP4或者前列腺素D或I受體(DP和IP受體)缺陷小鼠中觀察到9,10-EpOME引起的TRPV1敏化的任何減弱。為了表徵9,10-EpOME的體內作用,發明人將該脂質注射進野生型BL/6N小鼠的後爪內,並測量熱(圖5A)和機械閾值(圖5B),直至注射後5h。兩種情況下,9,10-EpOME引起疼痛閾值的顯著降低,在注射後持續1h(熱)或2h(機械)(圖1A,1B)。然後,發明人將9,10-EpOME鞘內注射,並在短時間間隔內測量熱和機械閾值。在鞘內注射後30分鐘觀察到顯著但相當弱的熱閾值降低(圖5C)。但是,在9,10-EpOME鞘內注射後長至1.5h觀察到機械閾值降低(圖5D)。
由於TRPV1升高的活性導致促進神經源性炎症的降鈣素基因相關肽(CGRP)的釋放增加37,所以發明人分析9,10-EpOME是否能夠增加TRPV1依賴的CGRP釋放。發明人從野生型BL/6N小鼠切下坐骨神經,並將它們與單獨的9,10-EpOME[1μM]、或者連同辣椒素[500nM]一起溫浴,對於辣椒素和9,10-EpOME的共刺激觀察到CGRP釋放的強烈增加。CGRP釋放顯著高於僅採用辣椒素或9,10-EpOME(圖6A)。為了研究在細胞胞體中是否也可見這種作用,用9,10-EpOME、辣椒素或這兩物質刺激富含神經元的DRG培養物,採用兩種不同的EpOME濃度[1和2.5μM]。同樣,採用EpOME和辣椒素二者,與採用任一種物質相比,iCGRP的釋放顯著增加。但是,採用2.5μM 9,10-EPOME,沒有CGRP釋放的顯著增加(圖6B)。
實施例3:CYP2J2調節9,10-EpOME
接著,研究了9,10-EpOME合成在紫杉醇CIPNP期間是如何被調節的。因為9,10-EpOME被認為是由亞族2C和2J的CYP表氧化酶所合成的16,38,發明人考察了這些亞族的鼠科CYP表氧化酶的表達。在紫杉醇處理後第8天,發明人在紫杉醇處理小鼠的機械閾值中觀察到穩定的平臺(圖7A)。
然後發明人切下載體和紫杉醇處理小鼠的DRG,並研究了鼠科CYP2C29、CYP2C37、CYP2C38、CYP2C39、CYP2C44、CYP2J6和CYP3A11的表達。但是,在鼠科DRG中未能檢測到CYP亞型2C29和2C44。發明人觀察到,與載體處理相比,在紫杉醇處理小鼠的DRG中CYP2J6顯示出最強表達(圖7B)。紫杉醇處理後第8天時,CYP2J6的這種增加的表達與9,10-EpOME的增加的水平相關,如通過LC-MS/MS測量坐骨神經、腰DRG和脊髓所分析的。
實施例4:CYP2J2拮抗劑抑制9,10-EpOME合成並減輕CIPNP
將人CYP2J2(鼠科CYP2J6的同源蛋白)的強力抑制劑特非那定用作拮抗劑。因為對特非那定與人CYP2J2的作用位點已有描述,所以發明人將鼠科CYP2J6和人CYP2J2的胺基酸進行比對,並在兩種蛋白的相同位置發現了所有推測的與特非那定相互作用的位點(Leu83、Met116、Ile127、Phe30、Thr315、Ile376、Leu378、Val380、Leu402和Thr488),除了替換為穀氨醯胺的Arg117。基於CYP2J2和CYP2J6之間驚人的胺基酸序列相似性,特非那定也與CYP2J6相互作用,並抑制該蛋白。為了研究特非那定對脂質水平的影響,發明人向8天前接受了紫杉醇的小鼠靜脈注射1mg·kg-1特非那定。兩小時後,發明人切下坐骨神經、DRG和背側脊髓,並在這些組織中定量環氧化脂類。發明人可在所有研究的組織中觀察到9,10-EpOME濃度的顯著降低(圖8A)。發明人還觀察到,所有測量的環氧化脂類和它們的(9,10-EpOME、12,13-EpOME、9,10-DiHOME、12,13-DiHOME和14,15-EET)的剩餘濃度在DRG、脊髓背角和血漿中都有顯著降低,但在特非那定處理的動物的坐骨神經中並非如此(圖8B)。
發明人接著在小鼠中研究了特非那定處理是否可以減輕紫杉醇誘導的CIPNP。因此,發明人將特非那定(1或2mg·kg-1或載體(DMSO))靜脈注射進8天前接受了紫杉醇的小鼠中。
發明人在特非那定注射後的第1、2、4和5h測量了機械閾值,可觀察到經特非那定處理的小鼠的機械閾值的顯著升高,持續2h。但是,未觀察到兩劑量之間的顯著差異(圖8C)。由於特非那定為組胺-1-受體拮抗劑,發明人使用了另一種不抑制CYP2J2的H1受體拮抗劑氯雷他定來研究該抗傷害作用實際上是由CYP2J2、還是組胺-1-受體的抑制引起。但是,與載體相比,氯雷他定處理不減輕紫杉醇誘導的CIPNP(圖8D)。
實施例5:新的選擇性CYP2J2拮抗劑的篩選
對商品名為的物質(FDA Approved Drug Library v2)篩選CYP2J2的新的選擇性拮抗劑,用於本文描述的發明的情形。將基於酶催化的CYP-Glo螢光素酶的反應用於測定CYP2J2的活性,將CYP3A4作為非選擇性對照。在實驗中將特非那定用作陽性對照。兩種篩選的結果顯示在圖9中。顯示出對CYP2J2的抑制超過60%並且對CYP3A4的抑制約為0%的拮抗劑被認為是選擇性CYP2J2拮抗劑,可用於本文描述的方法和用途中,將它們列在以下的表2中:
表2:
討論
9,10-EpOME能夠通過cAMP-PKA依賴機制在亞微摩爾濃度敏化DRG神經元中的TRPV1,導致隨後的iCGRP從DRG釋放。其它的氧化亞油酸代謝物(OLAM),例如9和13-HODE(它們在皮膚過度加熱期間產生),已證實為直接的TRPV1激動劑並促進炎性痛覺過敏。發明人也可在鼠科組織中檢測到9-和13-HODE,最主要在外周組織中。
發明人採用CYP2J2抑制劑特非那定降低9,10-EpOME的合成,可降低環氧化脂類的水平至約50%。在紫杉醇CIPNP期間,特非那定處理導致小鼠中減弱的機械超敏。CYP2J2及其同源物的拮抗劑因此可用於治療或預防CIPNP,這是被證實的,因為經氯雷他定(選擇性H1受體拮抗劑,不影響CYP2J2)處理的動物未在紫杉醇CIPNP中顯示出改善,這表明所觀察到的特非那定作用是由於對CYP2J2而不是組胺-1-受體的抑制。
化療誘導的神經病理性疼痛和隨後的感覺障礙仍然為細胞抑制劑的最嚴重副作用。尤其是在紫杉醇處理中,可觀察到早期急性疼痛症候群,這看起來是由對傷害感受神經元的敏化所介導。但是,尚不知曉促進這種病理學生理狀態的內源性介導物。根據發明人的數據,9,10-EpOME依賴的TRPV1敏化和傷害感受神經元的增加的活性可能由此促進了紫杉醇急性疼痛症候群(P-APS)。
目前,對於CIPNP治療劑有強烈的未滿足的醫療需求。在大型隨機和安慰劑對照臨床試驗中,用諸如阿米福汀或穀胱甘肽的抗氧化劑或神經保護性物質治療患者未能緩解CIPNP,最近的Cochrane綜述得出結論,沒有這些物質用於功能性CIPNP療法的證據。此外,抗氧化劑可以幹擾細胞抑制劑的抗腫瘤效果。最近,有報導稱,用N-乙醯半胱氨酸(NAC)和維生素E處理通過減少DNA損傷而增加小鼠中肺腫瘤細胞增殖和腫瘤生長。就這點而言,CYP2J2抑制劑可能優於採用抗氧化劑,因為已有報導,它們通過激活半胱天冬酶-3、Bax和Bcl-2以及通過減少腫瘤細胞遷移和粘附,甚至在體外和體內減少腫瘤生長。
序列表
弗勞恩霍夫應用研究促進協會
疼痛治療中的CYP2J2拮抗劑
F30742WO
EP14181086.1
2014-08-14
EP14186624.4
2014-09-26
14
PatentIn version 3.5
1
19
DNA
Artificial
Primer sequence
1
gcctcaaagc ctactgtca 19
2
19
DNA
artificial
Primer sequence
2
aacgccaaaa cctttaatc 19
3
20
DNA
artificial
Primer sequence
3
atactctata tttgggcagg 20
4
18
DNA
artificial
Primer sequence
4
gttcctccac aaggcaac 18
5
19
DNA
artificial
Primer sequence
5
ttgccttctg taatccccc 19
6
22
DNA
artificial
Primer sequence
6
tctaacgcag gaatggataa ac 22
7
17
DNA
artificial
Primer sequence
7
ggagacagag ctgtggc 17
8
20
DNA
artificial
Primer sequence
8
taaaaacaat gccaaggccg 20
9
20
DNA
artificial
Primer sequence
9
ctttccaacg agcgattccc 20
10
22
DNA
artificial
Primer sequence
10
tgtttctcct cctcgatctt gc 22
11
19
DNA
artificial
Primer sequence
11
ggcctcccac ctagtggaa 19
12
22
DNA
Primer sequence
12
ataacctcgt ccagtaacct ca 22
13
21
DNA
artificial
Primer sequence
13
gacaaacaag cagggatgga c 21
14
21
DNA
artificial
Primer sequence
14
ccaagctgat tgctaggagc a 21
