一種基於螢光染色觀察的農藥降解菌活性檢測方法與流程
2024-04-05 05:36:05 2
本發明涉及的是一種可以快速、方便、直觀、準確檢測有機農藥降解菌活性的方法,具體涉及一種基於螢光染色觀察的農藥降解菌活性檢測方法,屬於微生物活性檢測技術領域。
背景技術:
農藥作為一種重要的農業生產資料,對防治作物病蟲害、提高農業產量發揮了重要作用,長時間、高頻次、過量地施用有機農藥在環境中產生大量殘留,嚴重威脅生態環境安全和人類健康,微生物修復因具有無毒高效、不產生二次汙染、操作簡便、經濟實用和應用範圍廣等優點,成為去除環境中有機農藥汙染的一種重要途徑。
國內外研究者已通過馴化、篩選、富集和分離從汙泥、汙水、土壤、沉積物等環境樣品中得到了多種有機農藥降解菌,並利用微生物固定化、降解菌劑製備等技術將一些農藥降解菌應用於汙染區域原位修復中,在進行微生物固定化、降解菌劑製備及原位修復時必須保證體系中活菌的數量、比例和降解活性,因此對農藥降解菌活性的檢測尤為重要,為保證農藥降解菌的原位修復效果的重要前提,農藥降解菌活性的傳統檢測方法多在一段時間內分析降解菌培養系統中目標汙染物的殘留量,計算降解效率以代表系統中降解菌的活性,傳統農藥降解菌活性監測方法取樣周期長、農藥殘留監測費時費力且花費較高。同時,傳統方法不具有時效性,待一個取樣分析周期完成時,系統中農藥降解菌的活性、豐度等生長狀態早已改變,並不能代表應用時的真實狀態;因此,亟需發展一種快速、實時、方便、直觀、準確檢測有機農藥降解菌活性的方法。
技術實現要素:
本發明提出的是一種基於螢光染色觀察的有機農藥降解菌活性檢測方法,其目的旨在彌補現有農藥降解菌活性檢測方法的不足,尤其克服現有方法耗時長、費用高、時效性差等方面的弊端。
本發明的技術解決方案:基於螢光染色觀察的有機農藥降解菌活性檢測方法,具體包括以下步驟:
(1)針對降解菌進行擴大培養;
(2)配置n組含不同活菌死菌比例的培養體系;
(3)計算活菌螢光和死菌螢光比值;
(4)通過降解實驗測定n組菌液的農藥降解活性;
(5)繪製螢光比值與降解活性的相關性曲線,建立降解菌活性計算公式;
(6)用未知活性菌液驗證公式準確性後用於後續測試。
本發明的優點:
1)本發明提出的基於螢光染色觀察的有機農藥降解菌活性檢測方法通過分析培養系統中活菌和死菌的不同顏色螢光強度,能夠直觀的反映培養體系中菌株的活性狀態;
2)檢測用時短、費用低,通過螢光強度即可以評價降解菌活性,不必費時、費力的去檢測系統中降解菌對農藥的降解量,且該方法一經建立,後續測試非常方便簡單,大大簡化了降解菌活性檢測的步驟;
3)能夠對降解菌活性進行實時快速檢測,具有時效性;
4)適用範圍廣,能用於在不同環境條件下檢測多種降解菌活性,也適用於原位修復中降解菌活性的監測。
附圖說明
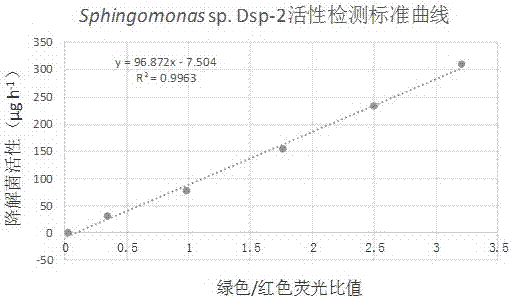
附圖1是實施例1中毒死蜱降解菌sphingomonassp.dsp-2綠色/紅色螢光比值與降解菌活性的相關性標準曲線。
具體實施方式
基於螢光染色觀察的有機農藥降解菌活性檢測方法,具體包括以下步驟:
(1)針對降解菌進行擴大培養;
(2)配置n組含不同活菌死菌比例的培養體系;
(3)計算活菌螢光和死菌螢光比值;
(4)通過降解實驗測定n組菌液的農藥降解活性;
(5)繪製螢光比值與降解活性的相關性曲線,建立降解菌活性計算公式;
(6)用未知活性菌液驗證公式準確性;
(7)測定樣品中的降解菌活性。
所述步驟(1)針對降解菌進行擴大培養:針對某種降解菌,準備相應培養基,培養基滅菌後,接種降解菌進行擴大培養,利用分光光度計設置波長od600檢測培養過程降解菌的生長情況。
所述步驟(2)配置n組含不同活菌死菌比例的培養體系:在降解菌生長達到穩定期後,取兩份等量的菌液,其中一份進行高溫滅活,將搖勻後的活菌液與滅活菌液以不同比例配比,形成n組培養體系,各培養體系中的活菌佔總菌的百分比在0%-100%間均勻分布,為確保方法準確性,每組至少三個重複,所述n≥6。
所述步驟(3)計算活菌螢光和死菌螢光比值:培養體系配置結束後,搖勻並立即取少量不同培養體系中的菌液,菌液經螢光染料染色後在螢光顯微鏡下鏡檢,所用螢光染料能夠區分活菌和死菌,在不同激發波長下,染色後的活菌和死菌的螢光顯色不同,拍照後利用圖像處理軟體分析視野中不同螢光光密度值,代表不同培養體系中活菌和死菌螢光強度比值。
所述步驟(4)通過降解實驗測定n組菌液的農藥降解活性:首次鏡檢後,向各培養體系中加入同樣濃度的有機農藥作為降解菌的底物,分時段取樣分析各培養體系中農藥殘留量,在活菌佔100%的培養組的有機農藥殘留量小於30%時終止降解實驗,分析各培養體系中的的農藥降解率。
所述步驟(5)繪製螢光比值與降解活性的相關性曲線,建立降解菌活性計算公式:以n組培養體系中活菌和死菌螢光強度比值為橫坐標,對應各組的農藥降解率為縱坐標,螢光強度和農藥降解率均為同組三個重複的平均值,選擇合適的曲線對二維平面中數據點進行擬合,繪製降解菌活性測試標準曲線,建立降解菌活性計算公式。
所述步驟(6)用未知活性菌液驗證公式準確性:對於繪製的降解菌活性測試標準曲線的準確性進行驗證,驗證方法為對未知活菌百分比的培養液取樣進行螢光染色觀察,同時測試培養液中降解菌的活性,通過比較降解菌活性測試標準曲線計算的降解菌活性與實際測得的活性,驗證降解菌活性測試標準曲線的準確性。
所述步驟(7)測定樣品中的降解菌活性:測定樣品中的降解菌活性時,震蕩搖勻菌液後取少量進行螢光染色觀察,分析樣品中活菌和死菌的螢光強度比值,然後根據螢光強度比值在標準曲線上直接查出該樣品中降解菌的活性。
以下通過具體實施例詳細說明發明的實施步驟,目的在於使本領域的技術人員進一步理解本發明,但不以任何形式限制本發明;應當指出的是,對本領域的普通技術人員來說,在不脫離本發明構思的前提下,還可以做出若干變形和改進,這些都屬於本發明的保護範圍。
實施例1
基於螢光染色觀察的有機磷農藥毒死蜱降解菌sphingomonassp.dsp-2的活性檢測。
利用本發明對純培養的sphingomonassp.dsp-2降解毒死蜱活性檢測由以下步驟組成:
(1)將sphingomonassp.dsp-2菌株接種至4llb培養基中(lb培養基含胰蛋白腖10g/l、酵母提取物5g/l、氯化鈉10g/l;ph7.0)在震蕩搖床進行擴大培養,搖床轉速200rmp,培養條件為溫度30oc,培養期間在超淨工作檯內取1ml均勻菌液,用分光光度計測定吸光度od600,檢測降解菌的生長情況;
(2)待降解菌生長至穩定期時,取2l培養液高溫滅活形成滅活培養液,剩餘2l為活菌培養液,按表1形成6組培養體系,每組設三個重複:
表1培養組1-6配置加入活菌及滅活培養液體積
(3)培養體系配置結束後,搖勻後準備降解菌懸浮液用於螢光染色,螢光染色試劑選擇l7012live/deadbaclightbacterialviability試劑盒(美國invitrogen公司),該試劑盒中syto9螢光染料結合與已死或將死的、細胞膜受損的細胞,在激發波長480nm/發射波長500nm時死細胞顯紅色;而試劑盒中propidiumidodide螢光染料結合與細胞膜完好的活細胞,在在激發波長490nm/發射波長635nm時這些活細胞顯綠色,降解菌懸浮液準備及染色步驟具體細節參照試劑盒說明書;染色結束後,在螢光顯微鏡下觀察、拍照,利用photoshop軟體獲得視野中綠色和紅色螢光光密度值,計算綠色螢光與紅色螢光光密度比值;
(4)螢光顯微鏡觀察結束後,對各培養組進行降解菌對毒死蜱降解活性檢測,向各培養組中加入100mg/l毒死蜱,每隔3h取2ml分析農藥殘留量,在第48h時測得1-6組毒死蜱殘留量、降解率、降解菌活性及螢光比值如表2所示(顯示數據為三個重複均值):
表2培養組1-6螢光比值及降解活性檢測結果
(5)以1-6組活菌和死菌螢光強度比值為橫坐標,對應各組的農藥降解率為縱坐標,螢光強度和降解菌活性均為同組三個重複的平均值,繪製降解菌活性測試標準曲線(請參照附圖1);由標準曲線可知,不同活菌和死菌配比的培養組中毒死蜱降解菌sphingomonassp.dsp-2綠色/紅色螢光比值與降解菌活性符合線性相關關係(r2=0.9963),降解菌活性的計算公式為降解菌活性(μg/h)=96.872×綠色/紅色螢光比值-7.504;
(6)取活菌百分比未知的菌液進行螢光染色觀察,分析綠色/紅色螢光比值為1.75,將比值代入步驟(5)中公式計算培養體系中降解菌活性為每小時降解毒死蜱162.0μg,利用降解實驗驗證方法的準確性,將毒死蜱加入至菌液中,終濃度為100mg/l,48h後菌液中殘留毒死蜱濃度為61.20mg/l,降解總量為7.76mg,降解菌活性為每小時降解毒死蜱161.7μg,與基於螢光比值計算的毒死蜱降解菌sphingomonassp.dsp-2降解活性(162.0μg/h)相差很小,表明螢光檢測方法和標準曲線具有準確性和可靠性。
實施例2
汙染水體修復過程中生物炭負載的毒死蜱降解菌sphingomonassp.dsp-2活性測定。
將毒死蜱降解菌sphingomonassp.dsp-2通過共培養方法與粉末狀生物炭負載後,將降解菌-生物炭複合體裝入透水袋中,在室內利用生態水槽模擬稻田退水系統複雜環境條件,為確保該複合體在實際原位修復中的高降解活性、強適應性,生態水槽中水體取自野外水稻退水系統,確定附著於生物炭上的降解菌sphingomonassp.dsp-2的生長狀態和降解活性,為原位修復策略的指定和降解系統穩定性的評價提供理論依據和數據支撐。
利用本發明提出的基於螢光染色觀察的方法檢測降解菌-生物炭複合體在生態水槽中放置不同時間後毒死蜱降解菌sphingomonassp.dsp-2的降解活性;
用取自野外稻田退水系統的水體作為培養基質,將未滅活和滅活後的負載降解菌的生物炭勻漿液以不同配比形成如實施例1中所述的1-6培養組,取少量培養液進行螢光染色觀察,計算綠色/紅色螢光比值,通過實施例1中所述的降解實驗計算負載於生物炭上的降解菌對毒死蜱的降解活性,綠色/紅色螢光比值和降解活性呈線性相關,計算公式為降解菌活性(μg/h)=112.3×綠色/紅色螢光比值+1.023,在生態水槽中放置裝有降解菌-生物炭複合體的透水袋,在實驗開始前(0h)首先進行螢光染色觀察,並計算得到降解菌-生物炭複合體降解毒死蜱活性為75.3μg/h,運行8h、12h、24h、48h、72h後從透水袋取降解菌-生物炭複合體進行螢光染色觀察,獲得綠色/紅色螢光比值,根據公式計算不同取樣時間的毒死蜱降解活性如表3所示(顯示數據為三個重複均值):
表3附著於生物炭的毒死蜱降解菌在不同運行時間時的螢光比值及降解活性檢測結果
利用本發明提出的基於螢光染色的農藥降解菌活性快速檢測方法,快速、直觀、準確的獲得該降解菌-生物炭複合體在應用不同時間時對毒死蜱的降解活性,進而確定該降解菌-生物炭複合體在應用24h後對毒死蜱的降解活性最高,在72h後降解活性低於初始值,暗示在農田退水系統原位農藥汙染修復中該降解菌-生物炭複合體最高降解活性在24h,而在應用72h後需要更換透水袋中的降解菌-生物炭複合體,以保障降解效果。
