烯醇酶1(ENO1)組合物及其用途的製作方法
2023-12-03 18:08:46 8
本申請要求2014年1月13日提交的美國臨時專利申請No.61/926,913,2014年6月9日提交的美國臨時專利申請No.62/009,783和2015年1月7日提交的美國臨時專利申請No.62/100,881的優先權,將其每篇的內容全部按引用併入本文中。
序列表的提交
通過EFS-Web以電子形式提交了與本申請相關的序列表並由此將其全部按引用併入說明書中。含有序列表的文本文件名為119992_10619_Sequence_Listing。該文本文件的大小為33KB,並且該文本文件於2015年1月13日生成。
背景技術:
隨著血糖水平在餐後升高,胰島素分泌並刺激外周組織(骨骼肌和脂肪)的細胞主動地從血液吸收葡萄糖作為能量源。作為胰島素分泌或機能失調的結果而喪失葡萄糖穩態通常導致代謝障礙,如糖尿病,其可能由肥胖共同引發或由肥胖進一步加劇。因為這些病症可能降低生活質量或甚至是致命的,因此需要恢復從血流中適當清除葡萄糖的策略。
儘管糖尿病可能由於引起胰腺大範圍損傷的任何病症(例如,胰腺炎、腫瘤、特定藥物(如皮質類固醇或噴他脒)的施用、鐵超負荷(即,血色素沉著)、獲得性或遺傳性內分泌病和外科手術切除)而繼發產生,但最常見形式的糖尿病通常由胰島素信號傳導系統的原發性失調產生。存在兩種主要類型的糖尿病,即1型糖尿病(也稱為胰島素依賴性糖尿病(IDDM))和2型糖尿病(也稱為胰島素無關性或非胰島素依賴性糖尿病(NIDDM)),儘管它們的發病機理不同,但都有共同的長期併發症。
1型糖尿病,其佔到所有原發性糖尿病病例的大約10%,是特徵在於胰腺的胰島素產生β細胞的大範圍破壞的器官特異性自身免疫疾病。隨之發生的胰島素產生的降低不可避免地導致葡萄糖代謝的失調。儘管胰島素的施用給患有這種病症的患者提供了相當大的益處,但胰島素的短血清半衰期是維持正常血糖的主要障礙。可替代的治療是胰島移植,但這種策略只獲得了有限的成功。
2型糖尿病,其影響較大比例的人群,特徵在於胰島素分泌的失調和/或外周組織對胰島素的應答降低,即,胰島素抵抗。儘管2型糖尿病的發病機理仍然不清楚,但流行病學研究表明這種形式的糖尿病由多重遺傳缺陷的集合或多態性產生,其各自引起其自身的易感風險並由環境因素改變,包括超重、飲食、不活動、藥物和過量飲酒。儘管各種治療性處理可以用於控制2型糖尿病,但它們與各種使人衰弱的副作用相關。因此,常常建議診斷為患有2型糖尿病或處於患2型糖尿病風險中的患者採用更健康的生活方式,包括減輕體重、改變飲食、鍛鍊和適當的飲酒。然後,這樣的生活方式改變不足以逆轉由糖尿病引起的血管和器官損傷。
技術實現要素:
在一個方面中,本發明提供了用於遞送至肌肉的包含烯醇酶1(Eno1)或其片段的組合物。在一個方面中,本發明提供了用於在血糖升高的受試者中使血糖正常化的方法,所述方法包括將包含Eno1或其片段的組合物施用於受試者,由此使受試者中的血糖正常化。在一個方面中,本發明提供了治療受試者的一種或多種病症的方法,所述病症包括受損的葡萄糖耐量、胰島素抵抗、前驅糖尿病和糖尿病,尤其是2型糖尿病,所述方法包括將包含Eno1或其片段的組合物施用於受試者,由此治療受試者的病症。在本發明的特定方法中,將Eno1遞送至肌肉。
本發明提供了用於遞送至肌細胞的包含Eno1或其片段的藥物組合物。
在特定實施方案中,Eno1包括Eno1多肽或其片段。在特定實施方案中,Eno1包括Eno1核酸或其片段。在特定實施方案中,Eno1包括人Eno1,例如,人Eno1多肽或人Eno1核酸,或其片段。
在特定實施方案中,組合物進一步包括微粒。在特定實施方案中,組合物進一步包括納米顆粒。在特定實施方案中,Eno1或其片段是生物活性的。在特定實施方案中,Eno1或其片段具有純化內源性人Eno1多肽的至少90%的活性。
在特定實施方案中,組合物進一步包括原位形成的組合物。在特定實施方案中,組合物進一步包括脂質體。在特定實施方案中,組合物包括樹狀聚合物。在特定實施方案中,組合物進一步包括表達載體,例如,編碼Eno1或其片段。在特定實施方案中,表達載體包括病毒載體。
在特定實施方案中,組合物包括含有Eno1或其片段(例如,Eno1多肽,例如,人Eno1多肽)和肌肉靶向部分的複合物。在特定實施方案中,肌肉靶向部分包括骨骼肌和/或平滑肌靶向肽(MTP)。在特定實施方案中,MTP包含選自ASSLNIA;WDANGKT;GETRAPL;CGHHPVYAC和HAIYPRH的胺基酸序列。在特定實施方案中,複合物包含連接物,例如,連接Eno1和SMTP。在特定實施方案中,連接物選自共價連接物、非共價連接和可逆連接物。在特定實施方案中,複合物包括藥物學上可接受的樹狀聚合物。在特定實施方案中,樹狀聚合物是PAMAN樹狀聚合物。在特定實施方案中,樹狀聚合物是G5樹狀聚合物。在特定實施方案中,樹狀聚合物是不帶電的樹狀聚合物。在特定實施方案中,樹狀聚合物是醯化樹狀聚合物。在特定實施方案中,樹狀聚合物是PEG化樹狀聚合物或乙醯化樹狀聚合物。在特定實施方案中,複合物包括脂質體。在特定實施方案中,複合物包括微粒或納米顆粒。在特定實施方案中,組合物包括原位形成的組合物。
在特定實施方案中,Eno1在遞送至肌細胞時從複合物釋放。
在特定實施方案中,Eno1或其片段和靶向部分以約1:1至約1:30的比率存在於複合物中。
在特定實施方案中,組合物配製成通過注射或輸注來施用。在特定實施方案中,組合物配製成用於口服施用。在特定實施方案中,組合物配製成用於腸胃外施用。在特定實施方案中,組合物配製成用於肌肉內施用、靜脈內施用或皮下施用。
本發明提供了降低血糖升高的受試者的血糖的方法,該方法包括將包含Eno1或其片段的藥物組合物施用於受試者。在特定實施方案中,藥物組合物包括本文中提供的任一藥物組合物。
本發明提供了提高葡萄糖耐量降低的受試者的葡萄糖耐量的方法,該方法包括將包含Eno1的藥物組合物施用於受試者。在特定實施方案中,藥物組合物包括本文中提供的任一藥物組合物。
本發明提供了提高胰島素敏感性降低和/或具有胰島素抵抗的受試者的胰島素反應的方法,該方法包括將包含Eno1或其片段的藥物組合物施用於受試者。在特定實施方案中,藥物組合物包括本文中提供的任一藥物組合物。
本發明提供了治療受試者糖尿病的方法,該方法包括將包含Eno1或其片段的藥物組合物施用於受試者。在特定實施方案中,糖尿病是2型糖尿病。在特定實施方案中,糖尿病是前驅糖尿病。在特定實施方案中,糖尿病是1型糖尿病。在特定實施方案中,糖尿病是妊娠糖尿病。在特定實施方案中,藥物組合物包括本文中提供的任一藥物組合物。
本發明提供了降低Hb1Ac水平升高的受試者的Hb1Ac水平的方法,該方法包括將包含Eno1或其片段的藥物組合物施用於受試者。在特定實施方案中,藥物組合物包括本文中提供的任一藥物組合物。
本發明提供了改善血糖水平控制異常的受試者的血糖水平控制的方法,該方法包括將包含Eno1或其片段的藥物組合物施用於受試者。在特定實施方案中,藥物組合物包括本文中提供的任一藥物組合物。
在特定實施方案中,通過注射或輸注來施用Eno1或其片段。在特定實施方案中,腸胃外施用Eno1或其片段。在特定實施方案中,口服施用Eno1或其片段。在特定實施方案中,通過選自肌肉內、靜脈內和皮下的途徑來施用Eno1或其片段。
本發明提供了用於診斷受試者的血糖水平升高的方法,包括:(a)檢測受試者的生物樣品中的Eno1水平,和(b)將生物樣品中的Eno1水平與預定的閾值進行比較,其中低於預定閾值的Eno1水平指示受試者中升高的血糖的存在。在特定實施方案中,該方法進一步包括檢測血糖升高的一種或多種診斷指標的水平。在特定實施方案中,血糖升高的一種或多種其他診斷指標選自HbA1c、空腹血糖、餐後血糖和葡萄糖耐量。在特定實施方案中,生物樣品是血液或血清。在特定實施方案中,通過免疫分析或ELISA測定Eno1的水平。在特定實施方案中,步驟(a)包括(i)將生物樣品接觸選擇性地結合Eno1以形成生物標誌物複合物的試劑,和(ii)檢測生物標誌物複合物。在特定實施方案中,試劑是選擇性地結合Eno1的至少一個表位的抗-Eno1抗體。
在特定實施方案中,步驟(a)包括測定生物樣品中Eno1 mRNA的量。在特定實施方案中,擴增反應用於測定生物樣品中Eno1 mRNA的量。在特定實施方案中,擴增反應是(a)聚合酶鏈式反應(PCR);(b)基於核酸序列的擴增試驗(NASBA);(c)轉錄介導的擴增(TMA);(d)連接酶鏈式反應(LCR);或(e)鏈置換擴增(SDA)。在特定實施方案中,將雜交試驗用於測定生物樣品中Eno1 mRNA的量。在特定實施方案中,將與Eno1 mRNA的一部分互補的寡核苷酸用於雜交試驗中來檢測Eno1 mRNA。
在本發明的特定實施方案中,升高血糖的診斷是選自2型糖尿病、前驅糖尿病、妊娠糖尿病和1型糖尿病的疾病或病症的診斷。
本發明提供了用於診斷受試者中升高血糖的存在的方法,包括:
(a)將生物樣品接觸選擇性地結合Eno1的試劑;
(b)允許試劑與Eno1之間形成複合物;
(c)檢測複合物的水平,和
(d)將複合物的水平與預定的閾值進行比較,其中高於預定閾值的複合物水平指示患者正遭受升高的血糖。在特定實施方案中,試劑是抗-Eno1抗體。在特定實施方案中,抗體包含可檢測標記。在特定實施方案中,檢測複合物水平的步驟進一步包括將複合物接觸可檢測的二抗並測量二抗的水平。在特定實施方案中,該方法進一步包括檢測一種或多種其他的升高血糖的指標的水平。在特定實施方案中,一種或多種其他的血糖指標選自HbA1c水平、空腹血糖、餐後血糖和葡萄糖耐量。在特定實施方案中,生物樣品是血液或血清。
在本發明的特定實施方案中,通過免疫分析或ELISA測定複合物的水平。在特定實施方案中,升高的血糖指示前驅糖尿病、2型糖尿病、1型糖尿病或妊娠糖尿病。在特定實施方案中,該方法進一步包括施用其中診斷表明受試者存在升高的血糖的治療方案,其中治療方案選自藥物治療和行為治療,或其組合。在特定實施方案中,藥物治療包括用選自(a)美格列奈,(b)磺醯脲,(c)二肽基肽酶-4(DPP-4)抑制劑,(d)雙胍,(e)噻唑烷二酮類,(f)α-葡糖苷酶抑制劑,(g)胰澱素(amylin)模擬物;(h)腸促胰島素模擬物;(i)胰島素;和(j)其任意組合的藥劑的治療。
在特定實施方案中,之前的任一方法進一步包括選擇懷疑具有升高的血糖或處於具有升高的血糖的風險中的受試者。
在特定實施方案中,之前的任一方法進一步包括從懷疑具有升高的血糖或處於具有升高的血糖的風險中的受試者獲得生物樣品。
在特定實施方案中,之前的任一方法進一步包括將生物樣品中一種或多種血糖升高相關的指標的水平與對照樣品中一種或多種血糖升高相關的指標的水平進行比較,所述對照樣品選自:在比該生物樣品早的時間點從同一受試者獲得的樣品,來自具有正常血糖的受試者的樣品,來自前驅糖尿病受試者的樣品,來自2型糖尿病受試者的樣品,來自妊娠糖尿病受試者的樣品和來自1型糖尿病受試者的樣品。
本發明提供了用於監控受試者的血糖升高的方法,該方法包括:
(1)測定在第一時間從血糖升高的受試者獲得的第一生物樣品中的Eno1水平;
(2)測定在第二時間從該受試者獲得的第二生物樣品中的Eno1水平,其中第二時間晚於第一時間;和
(3)將第二樣品中的Eno1水平與第一樣品中的Eno1水平進行比較,其中Enol水平的改變指示受試者中血糖升高狀態的改變。
在特定實施方案中,測定步驟(1)和(2)進一步包括測定選自HbA1c水平、空腹血糖、餐後血糖和葡萄糖耐量的一種或多種其他血糖指標的水平。
在特定實施方案中,在獲得第二樣品之前,受試者用針對血糖升高的藥物進行治療。在特定實施方案中,與第一生物樣品相比第二生物樣品中降低的Eno1水平指示受試者中血糖的升高。在特定實施方案中,與第一生物樣品相比第二生物樣品中提高或相等的Eno1水平指示受試者中血糖的正常化。在特定實施方案中,該方法進一步包括基於受試者的血糖水平選擇和/或施用用於該受試者的不同治療方案。在特定實施方案中,治療方案選自藥物治療和行為矯正治療。在特定實施方案中,藥物治療包括用選自(a)美格列奈,(b)磺醯脲,(c)二肽基肽酶-4(DPP-4)抑制劑,(d)雙胍,(e)噻唑烷二酮類,(f)α-葡糖苷酶抑制劑,(g)胰澱素模擬物;(h)腸促胰島素模擬物;(i)胰島素;和(j)其任意組合的藥劑的治療。
本發明提供了治療受試者的升高的血糖的方法,包括:(a)從懷疑具有血糖升高的受試者獲得生物樣品,(b)提交生物樣品以獲得關於Eno1水平的診斷信息,(c)如果Eno1水平高於閾值水平,施用治療有效量的抗糖尿病治療。
本發明提供了治療受試者的升高的血糖的方法,包括:(a)獲得生物樣品中關於Eno1水平的診斷信息,和(b)如果Eno1水平高於閾值水平,施用治療有效量的抗糖尿病治療。
本發明提供了治療受試者的升高的血糖的方法,包括:
(a)從懷疑血糖升高的受試者獲得生物樣品用於鑑定關於Eno1水平的診斷信息,
(b)測量生物樣品中的Eno1水平,
(c)如果Eno1水平低於閾值水平,給健康護理提供者推薦施用血糖降低治療。
在特定實施方案中,該方法進一步包括獲得關於血糖升高的一種或多種其他指標水平的診斷信息。
在特定實施方案中,該方法進一步包括測量血糖升高的一種或多種其他指標的水平。
在特定實施方案中,血糖升高的一種或多種其他指標選自HbA1c水平、空腹血糖水平、餐後血糖水平和葡萄糖耐量。
在特定實施方案中,如果Eno1的水平低並檢測了血糖升高的至少一種其他指標,步驟(c)進一步包括施用治療有效量的葡萄糖降低治療。在特定實施方案中,如果Eno1的水平低於閾值水平並且存在血糖升高的至少一種其他指標,步驟(c)進一步包括向健康護理提供者推薦施用葡萄糖降低治療。
在特定實施方案中,生物樣品是血液或血清。在特定實施方案中,通過免疫分析或ELISA來測定Eno1的水平。在特定實施方案中,通過(i)將生物樣品接觸選擇性地結合Eno1以形成生物標誌物複合物的試劑,和(ii)檢測生物標誌物複合物來測定Eno1的水平。在特定實施方案中,試劑是選擇性地結合Eno1的至少一個表位的抗-Eno1抗體。
在特定實施方案中,通過測量生物樣品中Enol mRNA的量來測定Enol的水平。在特定實施方案中,將擴增反應用於測量生物樣品中Enol mRNA的量。在特定實施方案中,擴增反應是(a)聚合酶鏈式反應(PCR);(b)基於核酸序列的擴增試驗(NASBA);(c)轉錄介導的擴增(TMA);(d)連接酶鏈式反應(LCR);或(e)鏈置換擴增(SDA)。在特定實施方案中,將雜交試驗用於測量生物樣品中Eno1 mRNA的量。在特定實施方案中,將與Eno1 mRNA的一部分互補的寡核苷酸用於雜交試驗中來檢測Eno1 mRNA。
本發明提供了用於檢測生物樣品中的Eno1的試劑盒,其包括至少一種用於測量生物樣品中的Eno1水平的試劑,和一套用於測量Eno1水平的說明。在特定實施方案中,試劑是抗-Eno1抗體。在特定實施方案中,試劑盒進一步包括檢測抗Eno1抗體的工具。在特定實施方案中,檢測抗Eno1抗體的工具是可檢測的二抗。在特定實施方案中,試劑是與Eno1 mRNA互補的寡核苷酸。在特定實施方案中,說明列出了用於檢測生物樣品中的Eno1水平的免疫分析或ELISA。在特定實施方案中,說明列出了用於分析生物樣品中的Eno1 mRNA水平的擴增反應。在特定實施方案中,將擴增反應用於測量生物樣品中Enol mRNA的含量。在特定實施方案中,擴增反應是(a)聚合酶鏈式反應(PCR);(b)基於核酸序列的擴增試驗(NASBA);(c)轉錄介導的擴增(TMA);(d)連接酶鏈式反應(LCR);或(e)鏈置換擴增(SDA)。在特定實施方案中,說明列出了用於測定生物樣品中Enol mRNA的量的雜交試驗。在特定實施方案中,試劑盒進一步包括至少一種與Enol mRNA的一部分互補的寡核苷酸。在特定實施方案中,試劑盒進一步包括至少一種用於測量生物樣品中的HbA1c和/或血糖水平的試劑。在特定實施方案中,試劑盒進一步包括用於測量從其獲得生物樣品的受試者中選自HbA1c水平、餐後血糖水平、空腹血糖水平和葡萄糖耐量的至少一種水平的說明。
本發明提供了用於檢測血糖升高的方法中的試劑組,該試劑組包括用於Eno1和HbA1c的檢測試劑。
本發明提供了用於治療血糖升高的方法中的試劑組,該試劑組包括用於Eno1和HbA1c的檢測試劑。
本發明提供了用於監控血糖升高的治療的方法中的試劑組,該試劑組包括用於Eno1和HbA1c的檢測試劑。
本發明提供了含有本文中提供的試劑組和一套用於獲得關於一種或多種血糖升高指標的水平的診斷信息的說明的試劑盒。
本發明提供了試劑組的用途,所述試劑組包括多種對於在用於診斷和/或治療血糖升高的方法中檢測血糖升高的標誌物特異性的檢測試劑,其中所述試劑組的至少一種檢測試劑對於檢測Eno1是特異性的,和其中其餘的一種或多種檢測試劑對於檢測選自HbA1c和葡萄糖的血糖升高標誌物指示劑是特異性的。
在上述方法的特定實施方案中,受試者骨骼肌細胞中的葡萄糖流量增加。
在另一個方面中,本發明提供了提高受試者的葡萄糖流量的方法,該方法包括將包含Eno1或其片段的藥物組合物施用於受試者。在特定實施方案中,施用於受試者的藥物組合物是上述任一種藥物組合物。在另一個方面中,本發明提供了提高受試者骨骼肌細胞中的糖酵解活性或能力的方法,該方法包括將包含Eno1或其片段的藥物組合物施用於受試者。在特定實施方案中,施用於受試者的藥物組合物是上述任一種藥物組合物。
在另一個方面中,本發明提供了提高受試者骨骼肌細胞中線粒體游離脂肪酸氧化的方法,該方法包括將包含Eno1或其片段的藥物組合物施用於受試者。在特定實施方案中,施用於受試者的藥物組合物是上述任一種藥物組合物。
在特定實施方案中,受試者具有血糖升高、葡萄糖耐量降低、胰島素敏感性降低和/或胰島素抵抗、糖尿病、Hb1Ac水平升高和異常血糖水平控制中的任何一種或多種。
在上述任一種方法的特定實施方案中,受試者是人。
在特定方面中,本發明涉及包含治療有效量的Eno1或其片段的藥物組合物。在特定實施方案中,藥物組合物是用於遞送至肌細胞。在特定方面中,本發明涉及包含Eno1或其片段和肌肉靶向肽的藥物組合物。在特定實施方案中,藥物組合物是用於遞送至肌細胞。在特定實施方案中,Eno1包括Eno1多肽或其片段。在特定實施方案中,Eno1包括Eno1核酸或其片段。在特定實施方案中,組合物進一步包括編碼Eno1或其片段的表達載體。在特定實施方案中,Eno1或其片段是生物活性的。在特定實施方案中,Eno1或其片段具有純化內源人Eno1多肽的至少90%的活性。在特定實施方案中,Eno1是人Eno1。在特定實施方案中,組合物進一步包括微粒。在特定實施方案中,組合物進一步包括納米顆粒。在特定實施方案中,組合物進一步包括原位形成組合物。在特定實施方案中,組合物進一步包括脂質體。在特定實施方案中,組合物進一步包括樹狀聚合物。在特定實施方案中,組合物包括含有Eno1多肽和肌肉靶向肽的複合物。在特定實施方案中,Eno1多肽是人Eno1多肽。在特定實施方案中,肌肉靶向肽包含選自ASSLNIA;WDANGKT;GETRAPL;CGHHPVYAC和HAIYPRH的胺基酸序列。在特定實施方案中,複合物進一步包含連接物。在特定實施方案中,連接物選自共價連接物、非共價連接和可逆連接物。在特定實施方案中,複合物進一步包括藥物學上可接受的樹狀聚合物。在特定實施方案中,藥物學上可接受的樹狀聚合物是PAMAN樹狀聚合物。在特定實施方案中,藥物學上可接受的樹狀聚合物是G5樹狀聚合物。在特定實施方案中,藥物學上可接受的樹狀聚合物是不帶電的樹狀聚合物。在特定實施方案中,藥物學上可接受的樹狀聚合物是醯化樹狀聚合物。在特定實施方案中,藥物學上可接受的樹狀聚合物是PEG化樹狀聚合物或乙醯化樹狀聚合物。
在前述的組合物的特定實施方案中,複合物進一步包括脂質體。在特定實施方案中,複合物進一步包括微粒。在特定實施方案中,複合物進一步包括原位形成的組合物。在特定實施方案中,Eno1在遞送至肌細胞時從複合物釋放。在特定實施方案中,樹狀聚合物和ENO1以約1:1至約10:1的比率存在於複合物中。在特定實施方案中,樹狀聚合物和ENO1以約3:1至約5:1的比率存在於複合物中。在特定實施方案中,肌肉靶向部分和樹狀聚合物以約0.1:1至約10:1的比率存在於複合物中。在特定實施方案中,肌肉靶向部分和樹狀聚合物以約1:1至約3:1的比率存在於複合物中。在特定實施方案中,Eno1和肌肉靶向部分以約1:1至約1:30的比率存在於複合物中。
在前述的組合物的特定實施方案中,組合物配製用於腸胃外施用。在特定實施方案中,組合物配製用於口服施用。在特定實施方案中,組合物配製用於肌肉內施用、靜脈內施用或皮下施用。
在特定方面中,本發明涉及降低血糖升高的受試者的血糖的方法,該方法包括將上述任一組合物施用於受試者,由此降低受試者的血糖。
在特定方面中,本發明涉及提高葡萄糖耐量降低的受試者的葡萄糖耐量的方法,該方法包括將上述任一組合物施用於受試者,由此提高受試者的葡萄糖耐量。
在特定方面中,本發明涉及提高具有胰島素敏感性降低和/或胰島素抵性的受試者的胰島素反應的方法,該方法包括將上述任一組合物施用於受試者,由此提高受試者的胰島素反應。
在特定方面中,本發明涉及治療受試者的糖尿病的方法,該方法包括將上述任一組合物施用於受試者,由此治療受試者的糖尿病。在特定實施方案中,糖尿病是2型糖尿病或1型糖尿病。在特定實施方案中,糖尿病是前驅糖尿病。
在特定方面中,本發明涉及降低Hb1Ac水平升高的受試者中的Hb1Ac水平的方法,該方法包括將上述任一組合物施用於受試者,由此降低受試者的Hb1Ac水平。
在特定方面中,本發明涉及改善具有異常血糖水平控制的受試者的血糖水平控制的方法,該方法包括將上述任一組合物施用於受試者,由此改善受試者的血糖水平控制。在上述方法的特定實施方案中,受試者的骨骼肌細胞中的葡萄糖流量增加。
在特定方面中,本發明涉及提高受試者的葡萄糖流量的方法,該方法包括將上述任一組合物施用於受試者,由此提高受試者的葡萄糖流量。
在特定方面中,本發明涉及提高受試者骨骼肌細胞中的糖酵解活性或能力的方法,該方法包括將上述任一組合物施用於受試者,由此提高受試者骨骼肌細胞中的糖酵解活性或能力。
在特定方法中,本發明涉及提高受試者骨骼肌細胞中的線粒體游離脂肪酸氧化的方法,該方法包括將上述任一組合物施用於受試者,由此提高受試者骨骼肌細胞中的線粒體游離脂肪酸氧化。
在上述方法的特定實施方案中,通過腸胃外施用Eno1。在上述方法的特定實施方案中,口服施用Eno1。在特定實施方案中,通過選自肌肉內、靜脈內和皮下的途徑施用Eno1。在上述方法的特定實施方案中,受試者具有血糖升高、葡萄糖耐量降低、胰島素敏感性降低和/或胰島素抵抗、糖尿病、Hb1Ac水平升高和異常血糖水平控制中的任何一種或多種。
在特定實施方案中,上述方法進一步包括選擇具有血糖升高、葡萄糖耐量降低、胰島素敏感性降低和/或胰島素抵抗、糖尿病、Hb1Ac水平升高和異常血糖水平控制中的任何一種或多種的受試者。
在前述方法的特定實施方案中,受試者是人。
下文中提供了其他實施方案。
附圖說明
圖1A是顯示了用或未用Eno1和胰島素處理的平滑肌成肌細胞中的葡萄糖攝取的圖。圖1B顯示了用0、500或1000ug/ml Eno1處理但未用胰島素處理的平滑肌成肌細胞中的葡萄糖攝取。
圖2A和2B顯示了用0、500或1000μg/ml Eno1處理的人骨骼肌肌管中的Eno1蛋白質水平。圖2C顯示了用0、500或1000μg/ml Eno1處理的人骨骼肌肌管中的Eno1活性。
圖3A顯示了原始和熱滅活的Eno1的Eno1活性。圖3B顯示了活性和熱滅活的Eno1的葡萄糖攝取的誘導。
圖4A和4B顯示了用或未用Eno1蛋白處理後,膳食誘導的肥胖症(DIO)小鼠模型中葡萄糖耐量測試的葡萄糖清除的(A)時間過程和(B)曲線下面積(AUC)。
圖5顯示了通過SDS-PAGE分析的含有各種濃度的Eno1的聚丙烯醯胺凝膠的考馬斯藍染色。L1:Precision Plus Protein Standard Dual Color,L2:Eno1(10.0μg),L3:Eno1(1.0μg),L4:Eno1(0.1μg)。
圖6顯示了通過SDS-PAGE分析的含有各種濃度的Eno1的聚丙烯醯胺凝膠的銀染。L1:Precision Plus Protein Standard Dual Color,L2:Eno1(10.0μg),L3:Eno1(1.0μg),L4:Eno1(0.1μg)。
圖7顯示了Eno1的Western印跡分析。L1:Precision Plus Protein Standard Dual Color,L2:Eno1(10.0μg),L3:Eno1(1.0μg),L4:Eno1(0.1μg)。
圖8顯示了用2:1比例的Eno1與樹狀聚合物SMTP製得的Eno1/G5-樹狀聚合物/SMTP的Zeta(ζ)電位測量。
圖9顯示了在各種溫度下儲存後,單獨的Eno1(單獨烯醇酶)和Eno1/G5-樹狀聚合物/SMTP(烯醇酶/G5-SMC)溶液的標準化活性。
圖10A和10B是(A)螢光標記的Eno1-G5-PAMAN樹狀聚合物複合物和(B)螢光標記的肌肉靶向的Eno-1-G5-PAMAM樹狀聚合物複合物在小鼠中的組織分布的代表性螢光圖像。
圖11是用溶媒、G5-PAMAM樹狀聚合物、G5-PAMAM樹狀聚合物+SMTP、G5-PAMAM樹狀聚合物+Enol、G5-PAMAM樹狀聚合物+Eno1+SMTP中的一種處理的瘦小鼠或DIO小鼠的體重的圖。
圖12是顯示了注射鹽水或G5-PAMAM樹狀聚合物+Eno1+SMTP(50ug/kg)後,在注射後1、4和24小時具有膳食誘導的肥胖症的小鼠中血糖水平的圖。
圖13A顯示了用G5-PAMAM樹狀聚合物+SMTP(DIO NP+SMTP)或G5-PAMAM樹狀聚合物+Enol+SMTP(DIO烯醇酶-1+NP+SMTP)處理1周後,瘦小鼠和膳食誘導肥胖症(DIO)的糖尿病小鼠模型中葡萄糖耐量測試的結果。圖13B顯示了圖13A中每個處理組的曲線下面積(AUC)。圖13C和13D顯示了用溶媒、G5-PAMAM樹狀聚合物(G5)、G5-PAMAM樹狀聚合物+SMTP、G5-PAMAM樹狀聚合物+Enol、G5-PAMAM樹狀聚合物+Eno1+SMTP中的一種處理兩周後,瘦小鼠或DIO小鼠的葡萄糖耐量測試中的葡萄糖清除的(C)時間過程和(D)曲線下面積(AUC)。
圖14A和14B顯示了用溶媒、G5-PAMAM樹狀聚合物、G5-PAMAM樹狀聚合物+SMTP、G5-PAMAM樹狀聚合物+Enol、G5-PAMAM樹狀聚合物+Eno1+SMTP中的一種處理四周後,瘦小鼠或DIO小鼠的葡萄糖耐量測試中葡萄糖清除的(A)時間過程和(B)曲線下面積(AUC)。
圖15顯示了8周治療後,瘦小鼠、膳食誘導的肥胖症(DIO)小鼠、用G5-樹狀聚合物處理的DIO小鼠(DIO+NP)和用Eno1/G5-樹狀聚合物/SMTP複合物處理療的DIO小鼠(DIO+Eno-1+NP+SMTP)中的血清乳酸鹽水平。
圖16A和16B顯示了用溶媒、G5-PAMAM樹狀聚合物(G5)+SMTP和G5-PAMAM樹狀聚合物+Eno1+SMTP(25ug/kg或50ug/kg)中的一種處理一周後,db/db小鼠(BKS.Cg-m+/+Leprdb/J)的腹膜內葡萄糖耐量測試中葡萄糖清除的(A)時間過程和(B)曲線下面積(AUC)。
圖17A和17B顯示了注射溶媒、所示劑量的G5-PAMAM樹狀聚合物+SMTP和G5-PAMAM樹狀聚合物+Eno1+SMTP後立即開始的時間過程中獲得的用溶媒、G5-PAMAM樹狀聚合物(G5)+SMTP和G5-PAMAM樹狀聚合物+Eno1+SMTP(25ug/kg或50ug/kg)中的一種處理兩周後db/db小鼠(BKS.Cg-m+/+Leprdb/J)的葡萄糖水平的時間過程。圖17A顯示了來自全部四個給藥方案的結果。圖17B顯示了來自G5-PAMAM樹狀聚合物+SMTP(G5+SMTP)和G5-PAMAM樹狀聚合物+Eno1+SMTP(Eno1+G5+SMTP)50ug/kg的結果,以顯示30分鐘時間點時葡萄糖水平的顯著差異。
圖18顯示了處理兩周後,每日一次皮下注射25μg/kg體重或50μg/kg體重的Eno1/G5-樹狀聚合物/SMTP複合物對db/db糖尿病小鼠模型的餐後血糖水平的作用。Eno1注射後24小時在沒有禁食的情況下測量餐後葡萄糖。「NP」是G5-樹狀聚合物。
圖19顯示了每日兩次(早晨和晚上)皮下注射100μg/kg體重或200μg/kg體重的Eno1/G5-樹狀聚合物/SMTP複合物對db/db糖尿病小鼠模型的餐後血糖水平的作用。
圖20顯示了用G5-PAMAM樹狀聚合物(G5)、G5-PAMAM樹狀聚合物+SMTP(G5-SMC)和醯化G5-PAMAM樹狀聚合物+SMTP(G5-SMC-Ac)處理後檢測的肌酸激酶和半胱天冬酶3活性。
圖21顯示了用或未用Eno1和胰島素處理的人骨骼肌肌管中的p-Akt蛋白水平。
圖22A顯示了用或未用純化的Eno1處理的人骨骼肌肌管中的Glut1、Glut4、HK2和成肌素mRNA水平。圖22B顯示了用或未用純化的Eno1處理的人骨骼肌肌管中的Glut1蛋白水平。Glut1蛋白水平是通過核糖體蛋白中值標準化的相對單位。
圖23顯示了用或未用純化的Eno1處理的葡萄糖飢餓(上圖)和葡萄糖刺激(下圖)的人骨骼肌肌管中的葡萄糖-6-磷酸(G6P)水平。
圖24顯示了用或未用純化的Eno1處理的葡萄糖飢餓(上圖)和葡萄糖刺激(下圖)的人骨骼肌肌管中的磷酸烯醇丙酮酸(PEP)水平。
圖25顯示了用或未用純化的Eno1處理的,順序地用棕櫚酸鹽、CCCP和乙莫克舍(etomoxir)處理的人骨骼肌肌管(HSMM)培養物中的氧消耗率(OCR)。
圖26顯示了用或未用純化的Eno1處理的,順序地用葡萄糖、寡黴素(oligomycin)和2-DG處理的人骨骼肌肌管(HSMM)培養物中的細胞外酸化率(ECAR)。
圖27A顯示了用500μg/ml或1000μg/ml Eno1處理的人骨骼肌肌管中相對於未處理的對照人骨骼肌肌管的線粒體含量。線粒體含量通過在Eno1處理48小時後將Mitotracker Green(一種綠色螢光線粒體染料)加入細胞中來測定。
圖27B顯示了用500μg/ml或1000μg/ml Eno1處理的人骨骼肌肌管中相對於未處理的對照人骨骼肌肌管(Eno1 0ug/ml)的線粒體活性氧物質(Mito-ROS)產生。通過用二氫若丹明123處理細胞來測定Mito-ROS,二氫若丹明123是一種不帶電的和非螢光的活性氧物質(ROS)指示劑,其可以被動跨膜擴散,在此處其氧化成陽離子若丹明123(其定位於線粒體中並且呈現綠色螢光)。二氫若丹明123處理後,將肌管胰蛋白酶化、洗滌並接受流式細胞分析以測定Mito-ROS水平。
圖28A顯示了用0、500或1000μg/ml Eno1處理的骨骼肌肌管中的5』AMP激活蛋白激酶(AMPK)和磷酸化AMPK(pAMPK)水平。將核纖層蛋白A/C用作加樣對照。
圖28B顯示了用0、500或1000μg/ml Eno1處理的基礎或血清飢餓的骨骼肌肌管中的pAMPK(p-AMPK)與AMPK的比例。
圖29顯示了描述Nampt在Eno1作用模式中的潛在作用的工作模型的示意圖。
圖30顯示了相對於未處理的對照人骨骼肌肌管(Eno1 0ug/ml),在4天分化後在分化培養基中用500ug/ml或1000μg/ml Eno1處理48小時的人骨骼肌肌管中的Nampt活性。
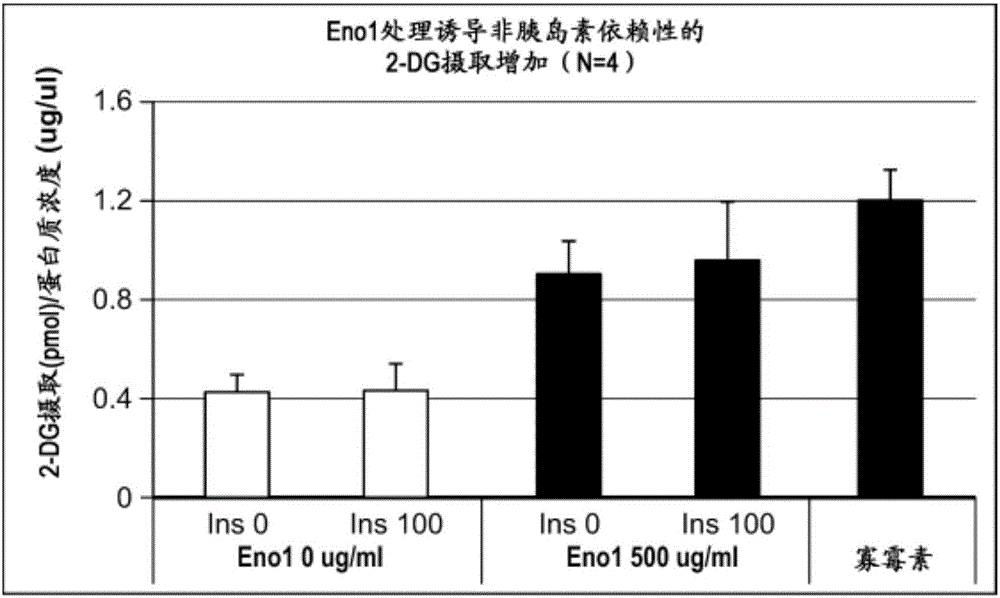
圖31顯示了用重組細胞外Nampt(eNampt)處理的血清飢餓人骨骼肌肌管中的2-DG攝取。
圖32顯示了在存在或不存在Nampt抑制劑FK866的情況下,在4天分化後在分化培養基中用0、500或1000μg/ml Eno1處理48小時的人骨骼肌肌管中的葡萄糖攝取。在開始Eno1處理後24小時加入FK866,並且用FK866處理肌管24小時。在3小時血清飢餓後測量2-DG攝取。FK866的Nampt抑制消除了Eno1誘導的葡萄糖攝取。
圖33顯示了糖酵解途徑的示意圖。
圖34A和34B顯示了人Eno1,變體1(NCBI登錄號NM_001428.3)的(A)胺基酸序列(SEQ ID NO:2)和(B)核酸編碼序列(SEQ ID NO:1)。
圖35A和35B顯示了人Eno1,變體2(NCBI登錄號NM_001201483.1)的(A)胺基酸序列(SEQ ID NO:4)和(B)核酸編碼序列(SEQ ID NO:3)。人Eno1,變體2蛋白也稱為MBP-1。
圖36A顯示了ENO2mRNA的核酸序列(SEQ ID NO:5)。圖36B顯示了Eno2的胺基酸序列(SEQ ID NO:6)。
圖37A和37B分別顯示了ENO3mRNA的變體1(SEQ ID NO:7)和變體2(SEQ ID NO:8)的核酸序列。圖37C顯示了Eno3蛋白的異形體1(SEQ ID NO:9),其由變體1和變體2兩者編碼。圖37D顯示了ENO3mRNA的變體3的核酸序列(SEQ ID NO:10)。圖37E顯示了Eno3的異形體2的胺基酸序列(SEQ ID NO:11),其由變體3編碼。與變體1相比,ENO3mRNA的變體3在5』UTR中不同並且在5』編碼區缺少兩個外顯子。Eno3蛋白的異形體2比異形體1短,但具有相同的N-和C-末端。
具體實施方式
使用發現平臺技術來描繪驅動糖尿病的病理生理的明顯不同的分子印記。通過這種發現平臺技術將Eno1鑑別為在人原發性體外糖尿病模型中被顯著調節的關鍵節點。本文中隨後討論的體外和體內研究證實了Eno1在胰島素依賴性和非胰島素依賴性葡萄糖攝取、葡萄糖耐受性、胰島素敏感性和/或糖尿病中的作用,所述糖尿病例如為1型糖尿病、2型糖尿病、前驅糖尿病和妊娠糖尿病。更具體地,用Eno1蛋白處理人肌管證明了提高肌管中非胰島素依賴性和胰島素依賴性葡萄糖攝取兩者,表明Eno1在1型和2型糖尿病兩者的治療中以及在存在和不存在胰島素和/或胰島素反應的兩種情況中的葡萄糖攝取中的作用。此外,Eno1蛋白的施用(單獨地或在骨骼肌靶向樹狀聚合物的環境中)改善了小鼠膳食誘導的肥胖症模型中的葡萄糖耐受性,並且預期在1型和2型糖尿病的遺傳模型中具有相似結果。這些結果證明了Eno1在使葡萄糖和胰島素反應正常化中是有效的,並且因此表明Eno1可用於改善葡萄糖耐受性和提高胰島素敏感性/降低胰島素抵抗,因此可用於治療糖尿病。
I.定義
烯醇酶1,(α),也稱為ENO1L、α-烯醇酶、烯醇酶-α、tau-晶體蛋白、非神經烯醇酶(NNE)、α烯醇酶樣1、磷酸丙酮酸水合酶(PPH)、纖溶酶原結合蛋白、MYC啟動子結合蛋白1(MPB1)和2-磷酸-D-甘油酸水解酶,是哺乳動物中發現的三種烯醇酶同工酶中的一種。本文在圖34和35中提供了人Eno1異形體的蛋白質和核酸序列。本申請提供了用於人疾病治療的人胺基酸和核酸序列。然而,將理解本發明的組合物和方法可以通過選擇待處理物種的Eno1容易地適應於非人動物的治療。非人物種的Eno1的胺基酸和核酸序列是本領域已知的並且可以在例如ncbi.nlm.nih.gov/genbank/中找到。在一些實施方案中,本發明的組合物和方法中使用的Eno1是哺乳動物Eno1。在優選實施方案中,Eno1是人Eno1。
如本文中使用的,「Eno1的施用」,除非另外指出,理解為Eno1蛋白或用於Eno1蛋白表達的核酸構建體的施用。在特定實施方案中,Eno1蛋白可以包括Eno1蛋白片段或用於編碼Eno1蛋白片段的核酸。在特定實施方案中,Eno1的施用是Eno1蛋白的施用。在特定實施方案中,Eno1的施用是Eno1多核苷酸的施用。本文中提供了人Eno1的蛋白質和核酸序列。在特定實施方案中,Eno1的施用包括人Eno1的第一變體或第二變體的施用。在特定實施方案中,Eno1的施用包括人Eno1的第一變體和第二變體的施用。在特定實施方案中,Eno1的施用包括人Eno1的第一變體的施用。在特定實施方案中,Eno1的施用包括人Eno1的第二變體的施用。在特定實施方案中,Eno1的施用包括僅人Eno1的第一變體的施用。在特定實施方案中,Eno1的施用包括僅人Eno1的第二變體的施用。
如本文中使用的,「生物活性的」是指具有內源性Eno1蛋白的至少一種活性的Eno1分子或其片段。例如,在一些實施方案中,生物活性Eno1分子或其片段催化2-磷酸-D-甘油酸(PGA)脫水成磷酸烯醇丙酮酸(PEP)。在一些實施方案中,生物活性Eno1分子或其片段催化PEP水合成PGA。在一些實施方案中,生物活性Eno1分子或其片段提高細胞的葡萄糖攝取,所述細胞例如為肌細胞,優選骨骼肌細胞。在一些實施方案中,生物活性Eno1分子或其片段降低血糖水平,例如,餐後血糖水平或葡萄糖耐量測試中的血糖水平。在一些實施方案中,生物活性Eno1分子或其片段結合Nampt,例如,細胞外Nampt(eNampt)。
如本文中使用的,「施用於肌肉」、「遞送至肌肉」或「遞送至肌細胞」包括骨骼肌細胞、平滑肌細胞等理解為將有效劑量的Eno1提供給肌肉,例如,肌細胞的製劑、方法或其組合,以提供所需的全身性效應,例如,血糖異常受試者中血糖的正常化,例如,通過提高葡萄糖耐量和/或胰島素敏感性,或治療糖尿病。在特定實施方案中,將Eno1配製用於直接施用於肌肉,並且優選停留在肌肉中。在特定實施方案中,用於直接施用於肌肉(即,肌肉內施用)的Eno1製劑,優選是持續釋放製劑允許相對低的施用頻率(例如,每周一次或更少,每隔一周或更少,每月一次或更少,每隔一月一次或更少,每三個月一次或更少,每四個月一次或更少,每五個月一次或更少,每六個月一次或更少)。在特定實施方案中,Eno1連接於靶向部分以提高Eno1至肌肉的遞送,使得不是必需將Eno1直接遞送至肌肉(例如,皮下或靜脈內遞送)。將理解施用於肌肉不需要將整個劑量的Eno1遞送至肌肉或肌細胞中。在特定實施方案中,至少5%,至少10%,至少15%,至少20%,至少25%,至少30%,至少35%的Eno1遞送至肌肉,優選骨骼肌和/或平滑肌。在特定實施方案中,遞送至肌細胞的非肌肉內施用肌肉靶向Eno1的量比遞送至肌肉的非靶向Eno1的量高約1.5倍或更高倍,2倍或更高倍,3倍或更高倍,4倍或更高倍,5倍或更高倍,或者6倍或更高倍。在特定實施方案中,將Eno1遞送至骨骼肌。在特定實施方案中,將Eno1遞送至平滑肌。在特定實施方案中,將Eno1遞送至骨骼肌和平滑肌。在特定實施方案中,與平滑肌相比,Eno1優先或以更高量遞送至骨骼肌。在特定實施方案中,遞送至肌肉的至少50%,60%,70%,75%,80%,85%,90%,95%或更多Eno1遞送至骨骼肌。在特定實施方案中,Eno1不遞送至平滑肌。測定通過靶向部分的有效載荷的相對靶向的試驗是本領域已知的,並且例如在Samoylova等,1999,Muscle Nerve,22:460-466中提供,其按引用併入本文中。
如本文中使用的,「肌肉靶向部分」包括至少肌肉靶向肽(MTP),例如,骨骼肌和/或平滑肌靶向肽(SMTP)。在特定實施方案中,靶向部分包括結合整聯蛋白αvβ5或αvβ3整聯蛋白的配體。在特定實施方案中,靶向部分包括CD-46配體。在特定實施方案中,靶向部分包括腺病毒peton蛋白,任選地結合腺病毒35纖維蛋白。在特定實施方案中,肌肉靶向Eno1的至少5%,至少10%,至少15%,至少20%,至少25%,至少30%,至少35%通過肌肉靶向部分遞送至肌肉,在一些實施方案中,優選骨骼肌和/或平滑肌。在特定實施方案中,遞送至肌細胞的非肌肉內施用肌肉靶向Eno1的量比遞送至肌肉的非靶向Eno1的量高約1.5倍或更高倍,2倍或更高倍,3倍或更高倍,4倍或更高倍,5倍或更高倍,或者6倍或更高倍。
如本文中使用的,「肌肉靶向肽」或「MTP」理解為提高其有效載荷(例如,Eno1)遞送至肌細胞(優選骨骼肌和/或平滑肌細胞)的肽序列。MTP是本領域已知的並且例如在美國專利No.6329501;美國專利公開No.20110130346和Samoylova等,1999,Muscle and Nerve 22:460-466中提供,將其每一篇全部按引用併入本文中。在特定實施方案中,MTP是骨骼肌靶向肽。「骨骼肌靶向肽」是提高其有效載荷(例如,Eno1)遞送至骨骼肌細胞的肽序列。在特定實施方案中,MTP是平滑肌靶向肽。「平滑肌靶向肽」是提高其有效載荷(例如,Eno1)遞送至平滑肌細胞的肽序列。在特定實施方案中,MTP提高其有效載荷(例如,Eno1)遞送至骨骼細胞和平滑肌細胞。在特定實施方案中,MTP,例如,骨骼肌靶向肽和/或平滑肌靶向肽,沒有提高其有效載荷遞送至心肌細胞。MTP,例如,骨骼肌靶向肽包括,但不限於,包含以下序列的肽:ASSLNIA;WDANGKT;GETRAPL;CGHHPVYAC和HAIYPRH。在優選實施方案中,MTP包含胺基酸序列ASSLNIA。
如本文中使用的,「有效載荷」理解為用於通過靶向部分遞送至靶細胞的部分。在特定實施方案中,有效載荷是肽,例如,Eno1肽。在特定實施方案中,有效載荷是核酸,例如,編碼Eno1肽的核酸。在特定實施方案中,有效載荷進一步包括與Enol有效載荷一起遞送至靶細胞的其他組分(例如,樹狀聚合物、脂質體、微粒)或藥劑(例如,治療劑)。
如本文中使用的,「連接物」理解為將靶向部分和有效載荷足夠接近地並置以使得有效載荷通過靶向部分遞送至所需的位點的部分。在特定實施方案中,連接物是共價連接物,例如,交聯劑,包括可逆交聯劑;肽鍵,例如,其中有效載荷是與靶向部分共翻譯的蛋白質。在特定實施方案中,連接物共價連接於有效載荷或靶向部分之一,並與另一個非共價連接。在特定實施方案中,連接物包括樹狀聚合物。在特定實施方案中,樹狀聚合物共價連接於靶向部分並且非共價連接於有效載荷,例如,Eno1。在特定實施方案中,連接物是脂質體或微粒,並且靶向部分暴露於脂質體的表面上,並且有效載荷(例如,Eno1)包封在脂質體或微粒中。在特定實施方案中,連接物和Eno1存在於微粒連接物的表面上。在特定實施方案中,靶向部分存在於病毒顆粒的表面上並且有效載荷包括編碼Eno1的核酸。
如本文中使用的,「連接的」、「可操作地連接的」、「接合的」等是指其中所描述的組分存在於允許它們以預定的方式起作用的複合物中的並置。組分可以共價連接(例如,肽鍵、二硫鍵、非天然化學鍵)、通過氫鍵連接(例如,蛋白質的鈕-扣(knob-into-holes)配對,參見,例如,美國專利5,582,996;Watson-Crick核苷酸配對),或者直接或通過連接物(例如,肽序列,通常為短肽序列;核酸序列;或化學連接物,包括使用用於連接於高階或較大結構(包括微粒、珠子或樹狀聚合物)的連接物)的離子結合(例如,螯合劑和金屬)。如本文中使用的,複合物的組分可以通過包裝在脂質體和/或樹狀聚合物之中和/或之上而彼此連接,其中複合物的一些組分可以共價連接,而一些非共價連接。連接物可以用於提供活性分子之間的分離,使得通過將第一分子連接於第二分子而分子的活性基本上沒有受到抑制(低於10%,低於20%,低於30%,低於40%,低於50%)。連接物可以用於例如將Eno1連接於靶向部分。如本文中使用的,在其中使用本發明試劑的情況(即,通常是生理條件)下,連接的(但非共價接合的)分子具有低於10-3、10-4、10-5、10-6、10-7、10-8、10-9、10-10、10-11或10-12,或那些值包括的任何範圍的彼此結合親和性(Kd)。
在特定實施方案中,有效負荷和靶向部分以約1:1摩爾比存在於複合物中。在特定實施方案中,靶向部分以相對於有效負荷的摩爾過量存在於複合物中。在特定實施方案中,有效負荷與靶向部分的比例為約0.1:1,約0.2:1,約0.3:1,約0.4:1,約0.5:1,約0.6:1,約0.7:1,約0.8:1,約0.9:1,約1:1,約2:1,約3:1,約4:1,約5:1,約6:1,約7:1,約8:1,約9:1,約10:1,約11:1,約12:1,約13:1,約14:1,約15:1,約16:1,約17:1,約18:1,約19:1或約20:1。
「樹狀聚合物」是由多個從中央核心徑向發射的分支單體組成的聚合分子。由於用於產生樹狀聚合物的結構和合成方法,來自樹狀聚合物合成的產物理論上是單分散性的。當除去樹狀聚合物的核心時,保留多個稱為樹突(dendron)的相同片段,樹突的數量取決於中央核心的多重性。從核心向外緣移向外緣時遇到的分支點的數量限定了其代數(generation),例如,G-1、G2、G-3等,較高代的樹狀聚合物與較低代數的樹狀聚合物相比更大、分支更多並且具有更多的末端基團。如本文中使用的,樹狀聚合物優選是藥物學上可接受的樹狀聚合物。
如本文中使用的,「血糖升高的受試者」或「提高的血糖」理解為具有認為是病理狀態的足夠持續時間和頻率的血糖升高的受試者,即沒有產生足夠的胰島素或對胰島素不夠敏感的受試者而使得受試者的葡萄糖水平在進食後的延長時間段內保持升高,例如,進食後持續超過兩小時,和/或具有升高的空腹血糖的受試者。在特定實施方案中,血糖升高的受試者理解為具有至少100mg/dl的空腹血糖和在75-g口服葡萄糖耐量測試中至少140mg/dl的2-小時血糖之一或兩者的受試者。在特定實施方案中,血糖升高的受試者理解為具有至少126mg/dl的空腹血糖;在75-g口服葡萄糖耐量測試中至少200mg/dl的2-小時血糖;或至少200mg/dl的隨機血糖中的一種或多種的受試者。在特定實施方案中,血糖升高的受試者理解為具有至少92mg/dl的空腹血糖;在75-g口服葡萄糖耐量測試中至少180mg/dl的1-小時血糖;和在75-g口服葡萄糖耐量測試中至少153mg/dl的2-小時血糖中的一種或多種的妊娠受試者。在如本文中使用的特定實施方案中,血糖升高的受試者不包括患有1型糖尿病或導致絕對胰島素缺陷的胰腺疾病的受試者。在如本文中使用的特定實施方案中,血糖升高的受試者包括患有1型糖尿病或導致絕對胰島素缺陷的胰腺疾病的受試者。
如本文中使用的,「HbA1c升高的受試者」或「A1c升高的受試者」理解為具有至少5.7%的HbA1c水平的受試者。在特定實施方案中,受試者具有至少6.5%的HbA1c水平。
如本文中使用的,「糖尿病」旨在指1型糖尿病或2型糖尿病,或1型和2型糖尿病兩者,任選地結合妊娠糖尿病。在特定實施方案中,糖尿病包括2型糖尿病。在特定實施方案中,糖尿病不包括1型糖尿病。在特定實施方案中,糖尿病包括妊娠糖尿病。在特定實施方案中,糖尿病不包括妊娠糖尿病。在特定實施方案中,糖尿病包括前驅糖尿病。在特定實施方案中,糖尿病包括前驅糖尿病、1型糖尿病和2型糖尿病。在特定實施方案中,糖尿病包括前驅糖尿病和2型糖尿病。
如本文中使用的,「胰島素抵抗」和「胰島素不敏感性」可以互換使用並指其中胰島素的量在降低血糖中的有效性比正常受試者低而導致血糖提高高於正常範圍(其不是由於胰島素的缺乏)的狀況,尤其是病理狀況。不希望受到機理的束縛,所述狀況通常與通過胰島素受體的信號傳導降低相關。通常,肌肉和脂肪細胞中的胰島素抵抗分別降低葡萄糖攝取以及作為糖原和甘油三酯的儲存。肝細胞中的胰島素抵抗導致降低的糖原合成並且不能抑制葡萄糖產生和釋放至血液中。
胰島素抵抗常常與「胰島素不足」一起存在於同一受試者中,其也導致非由於胰島素的缺乏引起的高於正常範圍的血糖提高,尤其是血糖的病理性提高。胰島素不足是與缺乏胰島素作用相關的狀況,其中胰島素存在並由身體產生。這與其中由於缺乏胰島細胞而不產生胰島素的1型糖尿病明顯不同。
對於本發明方法的目的,不需要區分受試者是否患有胰島素抵抗/不敏感性、胰島素不足或兩者。
術語「受損的葡萄糖耐量」(IGT)或「前驅糖尿病」用於描述在給予葡萄糖耐量測試時具有落入正常和高血糖之間的血糖水平的人員,即,具有異常的葡萄糖耐量,例如,病理上異常的葡萄糖耐量。這樣的人員處於產生糖尿病的較高風險中,儘管他們在臨床上沒有表徵為患有糖尿病。例如,受損的葡萄糖耐量是指其中患者高於110mg/dl並低於126mg/dl(7.00mmol/L)的空腹血糖濃度或空腹血清葡萄糖濃度,或高於140mg/dl(7.78mmol/L)並低於200mg/dl(11.11mmol/L)的2小時餐後血糖或血清葡萄糖濃度的狀況。前驅糖尿病,也稱為受損的葡萄糖耐量或受損的空腹血糖是產生2型糖尿病、心血管疾病和死亡的主要風險因素。許多焦點已經放在研發通過有效治療前驅糖尿病來防止2型糖尿病發生的治療幹預上(Pharmacotherapy,24:362-71,2004)。
如本文中使用的,「病理」狀況達到疾病或病症的臨床上可接受的閾值。如果病理狀況沒有解決,例如,血糖和/或HbA1c沒有正常化,病理狀況可以導致對受試者的顯著的不良作用,特別是長期的。病理狀況可以通過治療劑、外科手術和/或生活方式改變來逆轉。病理狀況可以是或不是慢性的。病理狀況可以是或不是可逆的。病理狀況可以是或不是終末的。
「高胰島素血症」定義為其中受試者具有胰島素抵抗而具有或不具有正常血糖的病症,其中空腹或餐後血清或血漿胰島素濃度升高高於不具有胰島素抵抗的正常瘦個體的血清或血漿胰島素濃度(即,空腹血糖測試中>100mg/dl,或在口服葡萄糖耐量測試中>140mg/dl)。
「高血糖症」(高血糖)的病症是其中血糖水平太高的狀況。通常,在血糖水平升高高於180mg/dl時產生高血糖症。高血糖症的症狀包括尿頻、煩渴以及在較長時間跨度內的體重減輕。
「低血糖症」(低血糖)的病症是其中血糖水平太低的狀況。通常,在血糖水平下降低於70mg/dl時產生低血糖症。低血糖症的症狀包括情緒化、四肢麻木(尤其是手和臂中)、混亂、顫抖和頭昏。由於這種狀況在存在超過可利用葡萄糖量的過量胰島素時產生,因此其有時候也稱為胰島素反應。
如本文中使用的,「HbA1c水平」或「A1c水平」理解為從HbA1c測試測定的血紅蛋白A1c(HbA1c)水平,其評價了之前兩個和三個月期間的平均血糖水平。沒有糖尿病的人員通常具有4%至6%範圍中的HbA1c值。前驅糖尿病特徵在於5.7%至6.5%的病理性HbA1c水平,其中高於6.5%的HbA1c水平指示糖尿病。HbA1c的每1%的提高反映出血糖水平提高大約30mg/dL,並且由於持久的血糖升高導致的提高的併發症風險。優選地,根據本發明待治療的患者的HbA1c值降低至低於9%,低於7%,低於6%,並且最優選至約5%。因此,待治療患者的過量HbA1c水平(即,超過5.7%的HbA1c水平)相對於治療前的該水平優選降低至少10%,20%,30%,40%,50%,60%,70%,80%,90%或更多(即,治療前水平-治療後水平/治療前水平)。
如本文中使用的,術語「受試者」是指人和非人動物,包括獸醫學受試者。術語「非人動物」包括全部脊椎動物,例如,哺乳動物和非哺乳動物,如非人靈長類、小鼠、兔、綿羊、狗、貓、馬、奶牛、雞、兩棲動物和爬行動物。在優選實施方案中,受試者是人並且可以稱為患者。
如本文中使用的,術語「治療(treat)」、「處理(treating)」或「療法(treatment)」優選是指獲得有益或所需臨床結果的活動,所述臨床結果包括但不限於,疾病或病症的一個或多個體徵或症狀的緩解或改善、減弱疾病的程度、疾病的穩定狀態(即,沒有惡化)、疾病狀態的改善或緩和。如本文中使用的,治療可以包括胰島素抵抗的減輕、提高胰島素敏感性、降低胰島素缺陷、提高或正常化HbAc1水平、改善或正常化HbAc1水平、改善或正常化血糖水平(例如,餐後血糖水平、空腹血糖水平、葡萄糖耐量)和改善糖尿病的至少一種體徵或症狀中的一種或多種。糖尿病(包括2型糖尿病)治療中的治療目標包括<6.5%的HbAc1水平;餐前血糖80-120mg/dl;和餐後2小時血糖Zn2+>Mn2+>Fe(II)2+>Cd2+>Co2+、Ni2+、Sm3+、Tb3+和大部分的其他二價金屬離子。在由烯醇酶催化的反應中,來自與PGA的羧酸基團鄰近的碳的α-質子被抽取,並且PGA轉化成烯醇化物陰離子中間體。這種中間體在各種化學反應中被進一步加工,包括外消旋、環異構化以及水或氨的β-消除。參見Atlas of Genetics and Cytogenetics in Oncology and Haematology database,atlasgeneticsoncology.org/Genes/GC_ENO1.Html。
酶活性的烯醇酶以二聚形式(同型-或異二聚體)存在,並且由兩個以反平行方式彼此面對的亞基組成。已經測定了來自酵母和人的烯醇酶的晶體結構並且提出了催化機理。Diaz-Ramos等,以上引用的。參與這種酶的催化活性的五個殘基在整個進化中是高度保守的。體外研究揭示了在位置Glu168、Glu211、Lys345、Lys396或His159處不同的突變烯醇酶顯示出顯著降低的活性水平。烯醇酶的組成和保守部分是參與烯醇酶活性位點的構象變化的兩個Mg2+離子,並且使得能夠結合底物或其類似物。Atlas of Genetics and Cytogenetics in Oncology database,以上引用的。在特定實施方案中,本發明的組合物包含金屬離子輔因子。金屬離子輔因子可以提供Eno1在組合物中提高的穩定性和/或提高的體內Eno1活性。在一個實施方案中,金屬離子輔因子是二價的。在一個實施方案中,二價金屬離子輔因子是Mg2+、Zn2+、Mn2+、Fe(II)2+、Cd2+、Co2+或Ni2+。在一個實施方案中,金屬離子輔因子是三價的,例如,Sm3+或Tb3+。
例如,可以使用丙酮酸激酶(PK)/乳酸脫氫酶(LDH)實驗測定Eno1活性。以下顯示了用於這種烯醇酶試驗的反應。
2-磷酸-D-甘油酸(DPG)
可以通過例如使用來自Photon Technology International,Inc.(pti-nj.com)的PTI Quantamaster 40分光光度計測量NADH螢光的降低來測定NADH至NAD+轉化的反應速率。用於通過比色丙酮酸激酶/乳酸脫氫酶試驗測量Eno1活性的試劑盒也是商業上可購得的,例如,從ABCAM(Cambridge,MA;目錄編號ab117994)。ABCAM Eno1活性試驗進一步描述於以下的實施例5中。
還如實施例2中所述的,通過測量Eno1對人骨骼肌肌管(HSMM)中的葡萄糖攝取的作用來測定Enol活性。
在特定實施方案中,Eno1或其片段具有純化內源性人Eno1多肽的至少10%,20%,30%,40%,50%,60%,70%,80%,90%,100%,110%,120%,130%,140%,150%,160%,170%,180%,190%,200%,300%,400%或500%的活性。在特定實施方案中,通過上述的丙酮酸激酶/乳酸脫氫酶試驗或HSMM葡萄糖攝取試驗測定Eno1、其片段和純化的內源性人Eno1多肽的活性。
在特定實施方案中,如本文中所述的與樹狀聚合物複合的Eno1多肽具有未與樹狀聚合物複合的純化內源性Eno1多肽的至少10%,20%,30%,40%,50%,60%,70%,80%,90%,100%,110%,120%,130%,140%,150%,160%,170%,180%,190%,200%,300%,400%或500%的活性。在特定實施方案中,通過上述的丙酮酸激酶/乳酸脫氫酶試驗或HSMM葡萄糖攝取試驗測定與樹狀聚合物複合的Eno1多肽的活性和未與樹狀聚合物複合的純化內源性Eno1多肽的活性。
在特定實施方案中,如本文中所述的與樹狀聚合物和靶向肽複合的Eno1具有未與樹狀聚合物和靶向肽複合的純化內源性人Eno1多肽的至少10%,20%,30%,40%,50%,60%,70%,80%,90%,100%,110%,120%,130%,140%,150%,160%,170%,180%,190%,200%,300%,400%或500%的活性。在特定實施方案中,通過上述的丙酮酸激酶/乳酸脫氫酶試驗或HSMM葡萄糖攝取試驗測定與樹狀聚合物和靶向肽複合的Eno1多肽的活性和未與樹狀聚合物和靶向肽複合的純化的內源性人Eno1多肽的活性。
在一個實施方案中,本發明組合物中的Eno1或其片段(其中該組合物包含金屬離子輔因子(例如,二價金屬離子輔因子,如Mg2+、Zn2+、Mn2+、Fe(II)2+、Cd2+、Co2+或Ni2+,或者三價金屬離子輔因子,如Sm3+或Tb3+))具有純化的內源性人Eno1多肽的至少10%,20%,30%,40%,50%,60%,70%,80%,90%,100%,110%,120%,130%,140%,150%,160%,170%,180%,190%,200%,300%,400%或500%的活性。在特定實施方案中,通過上述的丙酮酸激酶/乳酸脫氫酶試驗或HSMM葡萄糖攝取試驗測定如上所述在金屬離子輔因子的組合物中的Eno1或其片段的活性和純化的內源性人Eno1多肽的活性。
葡萄糖流量
肌肉葡萄糖攝取的調節涉及三步驟的過程,其由以下組成:(1)葡萄糖至肌肉的輸送,(2)葡萄糖通過葡萄糖轉運子GLUT4轉運至肌肉中和(3)肌肉內葡萄糖通過己糖激酶(HK)的磷酸化。肌肉葡萄糖攝取的生理調節需要葡萄糖從血液移動至間質並移動至胞內空間,並且隨後磷酸化成G6P。血糖濃度、肌肉血流和毛細管至肌肉的募集決定了葡萄糖從血液至間質的移動。質膜GLUT4含量控制葡萄糖轉運至細胞中。肌肉己糖激酶(HK)活性、細胞HK區室化和HK抑制劑(G6P)的濃度決定了葡萄糖磷酸化的能力。這三個步驟-葡萄糖的輸送、轉運和磷酸化-包括葡萄糖流,並且所有三個步驟對於葡萄糖流量控制都是重要的。然而,葡萄糖磷酸化下遊的步驟也可以影響葡萄糖攝取。例如,糖酵解或糖原合成的加速可以減少G6P,提高HK活性,提高葡萄糖磷酸化的能力,並潛在刺激肌肉葡萄糖攝取。Wasserman等,2010,J Experimental Biology,Vol.214,pp.254-262。
本發明至少部分地基於以下發現:Eno1影響葡萄糖流途徑的幾個組成部分,包括提高葡萄糖轉運子GLUT1和GLUT4以及己糖激酶HK2的表達,和提高糖酵解途徑中間體G6P和PEP的水平,因此表明Eno1處理起到提高葡萄糖流量的作用。
本發明還至少部分地基於以下發現:在來自正常受試者的肌細胞和來自患有2型糖尿病的受試者的肌細胞中Eno1被差異地調節。本發明進一步基於以下令人驚訝的發現:用Eno1處理肌細胞提高葡萄糖攝取至細胞中並且將Eno1施用於膳食誘導肥胖症的小鼠將葡萄糖耐量和胰島素反應正常化。
因此,本發明提供了通過將Eno1施用於受試者來治療通常與糖尿病(包括至少1型糖尿病、前驅糖尿病、2型糖尿病和妊娠糖尿病)相關的血糖升高的方法。此外,本發明提供了用於在哺乳動物中診斷和/或監控(例如,監控疾病進展或治療)和/或預後升高血糖狀態(例如,糖尿病)的方法。本發明還提供了基於關於血糖升高的受試者的血液或血清中的Eno1水平的診斷信息來治療或調節治療方案的方法。本發明進一步提供用於實施本發明方法的試劑組和試劑盒。
本發明還提供了用於提高受試者的葡萄糖流量的方法,包括將包含Eno1或其片段的藥物組合物施用於受試者。在特定實施方案中,施用於受試者的藥物組合物是本文中所述的任一種藥物組合物。本發明還提供了提高受試者的骨骼肌細胞中的葡萄糖流量的方法,該方法包括將包含Eno1或其片段的藥物組合物施用於受試者。在特定實施方案中,施用於受試者的藥物組合物是本文中所述的任一種藥物組合物。
本發明還提供了提高受試者骨骼肌細胞中的糖酵解活性的方法,該方法包括將包含Eno1或其片段的藥物組合物施用於受試者。在特定實施方案中,施用於受試者的藥物組合物是本文中所述的任一種藥物組合物。
本發明還提供了提高受試者骨骼肌細胞中的線粒體游離脂肪酸氧化的方法,該方法包括將包含Eno1或其片段的藥物組合物施用於受試者。在特定實施方案中,施用於受試者的藥物組合物是本文中所述的任一種藥物組合物。
如本文中使用的「提高葡萄糖流量」理解為提高(1)葡萄糖至肌肉的輸送,(2)葡萄糖至肌肉中的轉運和(3)肌肉內葡萄糖的磷酸化中的至少一種或多種。在特定實施方案中,提高葡萄糖流量包括提高肌細胞中的糖酵解活性或線粒體游離脂肪酸氧化。
IIA.烯醇酶2和烯醇酶3
烯醇酶2(Eno2)也稱為γ烯醇酶、神經元烯醇酶、神經元特異性烯醇酶(NSE)或HEL-S-279並且由ENO2基因編碼。Eno2是磷酸丙酮酸磷酸酶,糖酵解酶。Eno2是同型二聚體並且在中樞神經系統(CNS)的成熟神經元和神經元起源的細胞中找到。神經元在各種類型應激下將Eno2釋放至系統循環中。Yee等,2012,Invest.Ophthalmol.Vis.Sci.Vol.53,No.10,pp.6389-6392。ENO2mRNA的核酸序列和Eno2的胺基酸序列分別顯示於圖36A和36B中。
烯醇酶3(Eno3)也稱為β烯醇酶、肌肉烯醇酶、肌肉特異性烯醇酶(MSE)或GSD13並且由ENO3基因編碼。Eno3催化2-磷酸甘油酸和磷酸烯醇丙酮酸的互變。Eno3在成人骨骼肌細胞中發現,它在此處在肌肉發育和再生中起著作用。在成人肌肉中,超過90%的烯醇酶活性由Eno3引起。編碼Eno3的基因中的突變與糖原貯積病有關。Comi等,2001,Ann Neurol.Vol.50,No.2,pp.202-207。已經鑑定了ENO3mRNA的三個變體,變體1、2和3。變體1和2編碼Eno3蛋白的異形體1,而變體3編碼Eno3蛋白的異形體2。與變體1相比,ENO3mRNA的變體3在5』UTR不同並且在5』編碼區中缺少兩個外顯子。Eno3蛋白的異形體2比異形體1短,但具有相同的N-和C-末端。Eno3的變體1、2和3的核酸序列以及異形體1和2的胺基酸序列顯示於圖37A-37E中。
Eno2和/或Eno3也可以替代Eno1用於本文中所述的方法、藥物組合物、試劑組和試劑盒中。例如,Eno2和/或Eno3可以用於通過將包含Eno2和/或Eno3的藥物組合物施用於受試者而治療通常與糖尿病(包括至少1型糖尿病、前驅糖尿病、2型糖尿病和妊娠糖尿病)相關的血糖升高的方法中。此外,Eno2和/或Eno3可以用於在哺乳動物中診斷和/或監控(例如,監控疾病進展或治療)和/或預後升高的血糖狀態(例如,糖尿病)的方法中。Eno2和/或Eno3還可以用於基於關於血糖升高的受試者的血液或血清中的Eno2或Eno3水平的診斷信息來治療或調節治療方案的方法中,以及用於實施本發明的試劑組和試劑盒中。本發明還涉及包含Eno2和/或Eno3的藥物組合物,例如,用於遞送至肌細胞。
III.糖尿病診斷和分類
糖尿病(diabetes mellitus)(DM),常常簡稱為糖尿病(diabetes),是其中個人具有高血糖的一組代謝疾病,不管是因為身體沒有產生足夠的胰島素或是因為細胞不能對產生的胰島素作出反應。這種高血糖產生了多尿(頻繁排尿)、煩渴(增加的口渴)和多食(增加的飢餓)的經典症狀。
2型糖尿病由胰島素抵抗引起,這是其中細胞不能適當地使用胰島素的一種病症,有時合併絕對的胰島素缺乏。身體組織對胰島素反應性的缺陷據信至少部分地涉及胰島素受體。然而,具體的缺陷是未知的。
在2型糖尿病的早期階段,主要的異常是降低的胰島素敏感性。在這個階段,可以通過提高胰島素敏感性或降低肝臟的葡萄糖產生的多種措施和藥物來逆轉高血糖。前驅糖尿病表示個體的血糖水平高於正常但還不足夠高至進行2型糖尿病的診斷時發生的病症。
2型糖尿病是由於在胰島素抵抗的情況中β細胞的胰島素產生不足。胰島素抵抗(這是細胞不能適當地對正常水平的胰島素作出反應)主要發生在肌肉、肝臟和脂肪組織內。在肝臟中,胰島素通常抑制葡萄糖釋放。然而,在胰島素抵抗的情況中,肝臟不適當地將葡萄糖釋放至血液中。胰島素抵抗相對β細胞功能障礙的比例在個體之間是不同的,一些個體主要具有胰島素抵抗並且只具有胰島素分泌的很小缺陷,而其他個體具有輕微的胰島素抵抗且主要是缺乏胰島素分泌。
其他與2型糖尿病和胰島素抵抗相關的潛在重要機制包括:脂肪細胞內提高的脂質分解、對腸促胰島素的抗性和腸促胰島素的缺乏、血液中的高胰高血糖素水平、腎臟的鹽和水保留提高和中樞神經系統對代謝的不當調節。然而,不是所有具有胰島素抵抗的人員都發生糖尿病,因為還需要胰腺β細胞胰島素分泌的損害。
1型糖尿病由於身體不能產生胰島素而引起,並且目前需要用注射胰島素來治療。1型糖尿病的特徵在於胰腺中郎罕氏胰島的產胰島素β細胞的損失,導致胰島素缺乏。大部分受影響的人在開始發作時其他方面是健康的並且具有健康體重。對胰島素的敏感性和反應性通常是正常的,尤其是在早期階段。然而,特別是在後期階段,可能發生胰島素抵抗,包括由於免疫系統清除施用的胰島素引起的胰島素抵抗。
A.診斷標準
美國糖尿病協會在Diabetes Care,36:S67-74,2013中公開了糖尿病的診斷和分類標準,將其按引用併入文本中,其提供了更詳細的各種類型糖尿病的定義。以下進一步討論糖尿病的診斷標準。參考文獻如下分類1型糖尿病或2型糖尿病:
I.1型糖尿病(β-細胞破壞,通常導致絕對的胰島素缺陷)
A.免疫介導的
B.特發性的
II.2型糖尿病(範圍可以從具有相對胰島素缺陷的主要胰島素抵抗至具有胰島素抵抗的主要分泌缺陷)
III.其他特定類型
IV.妊娠糖尿病
本文中提供了用於進行診斷或評價方法的方法。本文中提供的糖尿病的診斷標準如下:
用於糖尿病診斷的標準
*在不存在明確的高血糖的情況下,標準1-3應當通過重複測試來證實。
本文中提供的糖尿病/前驅糖尿病的提高風險的診斷標準如下:
用於糖尿病(前驅糖尿病)的提高風險的標準*
*對於所有三個測試,風險是連續的,延伸低於範圍的下限並且在範圍的高端變得不成比例地高。
本文中提供的妊娠糖尿病的診斷標準如下:
妊娠糖尿病(GDM)的篩選和診斷
由於相對於進食的特定時間需求(例如,空腹血糖)或進行測試需要的時間量(例如,與口服葡萄糖耐量測試),用於血糖升高或糖尿病的診斷和/或監控的血糖測量可能是麻煩的。此外,診斷標準明確要求在不存在明確的高血糖的情況下,應當通過重複測試來確認標準1-3。使用HbA1c水平作為診斷指標可能是有利的,因為其提供隨著時間的血糖水平的指示,即,約之前1-2個月,並且不需要特殊的時間表來進行測試。相似地,可以測定Eno1水平而沒有特別的時間表需求或者食物消耗限制或需求。
因此,在一些方面中,本發明涉及用於診斷受試者中血糖升高的存在的方法,包括:(a)將生物樣品接觸選擇性結合Eno1的試劑;(b)允許試劑和Eno1之間形成複合物;(c)檢測複合物的水平,和(d)將複合物的水平與預定的閾值進行比較,其中樣品中複合物的水平低於預定閾值表明患者正遭受升高的血糖。在特定實施方案中,選擇性結合Eno1的試劑是抗Eno1抗體。在特定實施方案中,抗體包含可檢測的標記。
在上述方法的一些實施方案中,檢測複合物水平的步驟進一步包括將複合物接觸可檢測的二抗並且測量二抗的水平。該方法還可以進一步包括檢測血糖升高的一個或多個其他指標的水平。血糖的一個或多個其他指標可以選自HbA1c水平、空腹葡萄糖水平、餐後葡萄糖水平和葡萄糖耐量。
在上述方法的一些實施方案中,生物樣品是血液或血清。在一些實施方案中,通過免疫分析或ELIS檢測複合物的水平。在一些實施方案中,受試者中升高血糖的存在指示選自前驅糖尿病、2型糖尿病、1型糖尿病和妊娠糖尿病的疾病或病症。
B.糖尿病、胰島素抵抗和胰島素不足的繼發病理
由糖尿病(1型和2型兩者)、胰島素抵抗和胰島素不足引起的異常血糖調控與繼發病理相關,其中許多由差的循環引起。這樣的繼發病理包括黃斑變性、周圍神經病、潰瘍和降低的傷口癒合以及降低的腎功能。已經表明將葡萄糖水平和/或HbAc1水平維持在正常範圍內降低這些繼發病理的發生。應理解血糖、胰島素和HbAc1水平的正常化將通過限制原發性病理(例如,受損的葡萄糖耐量、提高的血糖)降低繼發病理的發生。在特定實施方案中,Eno1不用於治療與受損的葡萄糖耐量、提高的血糖、胰島素抵抗、胰島素不足、糖尿病或前驅糖尿病相關的繼發病理。在特定實施方案中,Eno1用於治療與受損的葡萄糖耐量、提高的血糖、胰島素抵抗、胰島素不足、糖尿病或前驅糖尿病相關的繼發病理。
IV.劑量和施用方式
施用的技術和劑量根據化合物的類型而改變(例如,蛋白質和/或核酸,單獨的或與微粒、脂質體或樹狀聚合物複合),並且是本領域技術人員公知的或容易確定的。
本發明的治療化合物可以與藥物學上可接受的稀釋劑、載體或賦形劑一起,以單位劑量形式來施用。施用可以是腸胃外、靜脈內、皮下、口服、外部(topical)或局部(local)。在特定實施方案中,施用不是口服的。在特定實施方案中,施用不是外部的。在特定的優選實施方案中,施用是全身性的。可以通過協同工作的多個人員來進行藥劑施用。施用藥劑包括,例如,開出施用於受試者的藥劑的處方和/或直接地或通過另一人提供服用特定的藥劑的說明,其或者通過自我遞送,例如,作為口服遞送、皮下遞送、通過中心線的靜脈內遞送等,或者通過受過訓練的專業人士來遞送,例如,靜脈內遞送、肌肉內遞送、皮下遞送等。
組合物可以是用於口服施用的丸劑、片劑、膠囊、液體或持續釋放片劑的形式;或用於靜脈內、皮下或腸胃外施用的液體;或用於全身性施用的聚合物或其他持續釋放溶媒。
本領域公知的用於製備製劑的方法可以在例如「Remington:The Science and Practice of Pharmacy」(第20版,編輯A.R.Gennaro,2000,Lippincott Williams&Wilkins,Philadelphia,Pa)中找到。用於腸胃外施用的製劑可以例如含有賦形劑、無菌水、鹽水、聚烷撐二醇(如聚乙二醇)、植物來源的油或氫化萘。生物相容的、生物可降解的丙交酯聚合物、丙交酯/乙交酯共聚物或聚氧乙烯-聚氧丙烯共聚物可以用於控制化合物的釋放。納米顆粒製劑(例如,生物可降解的納米顆粒、固體脂質納米顆粒、脂質體)可以用於控制化合物的生物分布。其他潛在有用的腸胃外遞送系統包括乙烯-乙酸乙烯酯共聚物顆粒、滲透泵、可植入輸注系統和脂質體。製劑中化合物的濃度根據多種因素而改變,包括待施用藥物的劑量和施用途徑。
化合物可以任選地作為藥物學上可接受的鹽來施用,如製藥業中通常使用的非毒性酸式加成鹽或金屬絡合物。酸式加成鹽的實例包括有機酸,如乙酸、乳酸、撲酸、馬來酸、檸檬酸、蘋果酸、抗壞血酸、琥珀酸、苯甲酸、棕櫚酸、辛二酸、水楊酸、酒石酸、甲磺酸、甲苯磺酸或三氟乙酸等;聚合酸,如單寧酸、羧甲基纖維素等;和無機酸,如鹽酸、氫溴酸、硫酸、磷酸等。金屬複合物包括鋅、鐵等。金屬絡合物包括鋅、鐵等。
用於口服使用的製劑包括含有在與無毒的藥物學上可接受的賦形劑的混合物中的活性成分的片劑。這些賦形劑可以是,例如,惰性稀釋劑或填充劑(例如,蔗糖和山梨糖醇)、潤滑劑、助流劑和抗粘劑(例如,硬脂酸鎂、硬脂酸鋅、硬脂酸、矽石、氫化植物油或滑石)。用於口服使用的製劑也可以作為咀嚼片,或作為硬明膠膠囊(其中將活性成分與惰性固體稀釋劑混合),或作為軟明膠膠囊(其中將活性成分與水或油介質混合)來提供。
施用化合物的劑量和時機根據各種臨床因素而改變,包括受試者的整體健康和疾病(例如,糖尿病、前驅糖尿病)的症狀的嚴重性。
A.用於長效注射藥物的製劑
經受高首過清除率的生物製劑和其他藥劑可能不適用於口服施用而需要通過腸胃外途徑來施用。然而,用於注射藥物的治療方案的依從性可能是低的,因為受試者常常牴觸通過注射來自身施用藥劑,例如,皮下注射,特別是當疾病沒有使受試者感到不舒服時。通過注射的其他施用途徑,例如,靜脈內、肌肉內,通常需要通過經訓練的專業人士來施用,使得頻繁的藥劑施用是不方便的並且常常是疼痛的。
已經製備了提供注射藥劑的持續遞送的製劑,包括,但不限於,油基注射液、注射藥物懸浮液、注射微球和原位注射系統。與相同化合物的常規製劑相比,長效注射製劑給予了許多優勢。這些優勢包括至少以下:每次注射後限定時間段內可預測的藥物釋放特性;更好的患者依從性;易於施用;通過避免首過代謝提高全身利用度;降低的給藥頻率(即,較少注射)而不損害治療的有效性;降低的副作用發生率;和醫療護理的總體成本降低。
1.油基注射液和注射藥物懸浮液。
常規長效注射由水性溶劑中的親脂性藥物組成(作為懸浮液)或由溶解於植物油中的親脂性藥物組成。商業上可購得的用於肌肉內施用的油基注射藥物包括,但不限於,癸酸氟哌啶醇、癸酸氟非那嗪、庚酸睪酮和戊酸雌二醇。這些長效製劑的施用頻率大約為每幾周。在懸浮液製劑中,藥物吸收的速率限制步驟是藥物顆粒在製劑或藥物製劑周圍的組織流體中的溶解。形成水溶性差的鹽可以用於控制藥物顆粒的溶解速率以延長吸收。然而,幾種其他因素,如注射部位、注射體積、藥物存庫(depot)在注射部位的擴散程度以及油溶媒本身的吸收和分布可能影響藥物的總體藥代動力學特性。調節這些因素以提供所需藥物釋放特性在本領域技術人員的能力範圍內。
2.基於聚合物的微球體和原位成型。
基於聚合物的長效注射劑的開發是用於大分子(如肽和蛋白質藥物)的最適合策略之一。商業上可購得的微球製劑包括,但不限於,醋酸亮丙瑞林、雙羥萘酸曲普瑞林、醋酸奧曲肽、醋酸蘭瑞肽、利培酮和納曲酮。商業上可購得的原位形成植入物包括醋酸亮丙瑞林,並且含有紫杉醇和丁哌卡因的原位形成植入物正在臨床試驗中。這些製劑用於肌肉內施用。用於大分子的基於聚合物的製劑的優勢包括:大分子的體外和體內穩定、全身利用度的提高、生物半衰期的延長、患者方便性和依從性的增強和給藥頻率的降低。
可注射微球和原位形成製劑的設計中的最關鍵因素是合適的生物可降解聚合物的選擇。藥物分子從生物可降解微球的釋放受到通過聚合物基質的擴散和聚合物降解的控制。聚合物的性質,如共聚物組成比例、聚合物結晶度、玻璃態轉化溫度和親水性在釋放過程中起著關鍵作用。儘管結構、固有聚合物特性、核心溶解度、聚合物親水性和聚合物分子量影響藥物釋放動力學,藥物從微球釋放的可能機制如下:初始從表面釋放、通過孔隙釋放、通過完整的聚合物屏障的擴散、通過水溶脹屏障的擴散、聚合物侵蝕和本體降解。所有這些機制一起在釋放過程中起作用。用於微球和原位形成製劑的聚合物包括,但不限於,過去數十年中廣泛研究的用於受控藥物遞送的多種生物可降解聚合物,包括聚丙交酯(PLA)、聚乙交酯(PGA)、聚(丙交酯-共-乙交酯)(PLGA)、聚(ε-己內酯)(PCL)、聚葡糖酸酯、聚酸酐、聚原酸酯、聚(二噁烷酮)和聚烷基氰基丙烯酸酯。原位形成製劑中使用的熱誘導膠凝系統顯示出熱可逆溶膠/凝膠轉變,並且通過低臨界溶解溫度表徵。它們在室溫下是液體並且在低臨界溶解溫度和更高溫度下產生凝膠。原位固化有機凝膠由水不溶性兩性液體組成,其在水中溶脹並形成各種類型的溶致液晶。
B.靶向藥物遞送
藥物至其作用位點的遞送可以通過降低提供所需全身性作用所需要的藥物量來提高治療指數。可以通過使用將限制全身性暴露的方法或製劑,例如,肌肉內注射、滑膜內(intrasinovial)注射、鞘內注射、眼內注射,將藥物施用於靶組織而將藥物遞送至作用位點。以上討論的多種持續遞送製劑是用於肌肉內施用的並且提供至肌肉組織的局部遞送。或者,靶向部分可以與用於施用於靶位點的治療性有效載荷締合或連接。靶向部分可以包括結合特定細胞類型的多種部分中的任何一種。
1.靶向部分
本發明的特定實施方案包括使用靶向部分,包括如上討論的相對小的肽(例如,25個胺基酸或更少,20個胺基酸或更少,15個胺基酸或更少,10個胺基酸或更少)、肌肉靶向肽(MTP)包括平滑肌和/或骨骼肌靶向肽、αvβ3整聯蛋白配體(例如,RGD肽和肽類似物)、αvβ5整聯蛋白配體或CD46配體。將理解這樣的肽可以包括一個或多個化學修飾以允許與Eno1形成複合物,從而改變肽的藥代動力學和/或藥效學特性。在特定實施方案中,靶向部分可以是小分子,例如RGD肽模擬物。在特定實施方案中,靶向部分可以包括蛋白質和任選地來自腺病毒35的纖維蛋白。在特定實施方案中,病毒蛋白質存在於病毒顆粒上。在特定實施方案中,病毒蛋白質不存在於病毒顆粒上。在特定實施方案中,靶向部分可以是抗體、抗體片段、抗體模擬物或T-細胞受體。
2.靶向複合物
可以通過肌肉內注射以外的其他途徑(例如,皮下注射、靜脈內注射)來施用靶向Eno1複合物,同時提供Eno1至肌肉的遞送。靶向複合物可以包括一個或多個直接或間接連接於Eno1的靶向部分。靶向複合物的形成沒有實質性地或不可逆地抑制Eno1的活性及其對正常化血糖水平和胰島素反應的作用。在特定實施方案中,使用靶向複合物可以降低提供有效劑量需要的Eno1的總量。以下討論靶向複合物的一些示例性的、非限制性的實施方案。
在特定實施方案中,有效載荷和靶向部分以約1:1摩爾比存在於複合物中。在特定實施方案中,靶向部分相對於有效載荷以摩爾過量(例如,2:1,3:1,4:1,5:1,6:1,7:1,8:1,9:1,10:1,11:1,12:1,13:1,14:1,15:1,16:1,17:1,18:1,19:1,20:1,21:1,22:1,23:1,24:1,25:1,26:1,27:1,28:1,29:1,30:1或更高;或任何兩個值包括的任何範圍)存在於複合物中。在特定實施方案中,有效載荷與靶向部分為約1:5-1:15;約1:7-1:13,約1:8-1:12。
將理解本發明的組合物和方法包括超過一種靶向部分-有效載荷複合物(即,靶向部分-有效載荷複合物群體)的施用。因此,將理解每個有效載荷的靶向部分數量可以表示複合物群體中每個有效載荷的平均靶向部分數。在特定實施方案中,至少70%的複合物具有選定的靶向部分與有效載荷的摩爾比。在特定實施方案中,至少75%的複合物具有選定的靶向部分與有效載荷的摩爾比。在特定實施方案中,至少80%的複合物具有選定的靶向部分與有效載荷的摩爾比。在特定實施方案中,至少85%的複合物具有選定的靶向部分與有效載荷的摩爾比。在特定實施方案中,至少90%的複合物具有選定的靶向部分與有效載荷的摩爾比。
a.連接物
多種化學連接物是本領域已知的並且可從商業來源(例如,Pierce Thermo Fisher Scientific Inc.,參見,例如,www.piercenet.com/cat/crosslinking-reagents)獲得。這樣的試劑可以用於將一個或多個靶向部分可逆或不可逆地化學連接於Enol。連接物還可以用於將靶向部分和Eno1附接於某結構,例如,微粒、樹狀聚合物,而不是將靶向部分直接連接於Eno1。在特定實施方案中,將Eno1與靶向複合物連接的連接物是可逆的,使得施用後Eno1從複合物釋放,優選基本上是在肌肉處釋放。
b.肽鍵
如本文中使用的,靶向複合物可以包括Eno1用肽靶向部分的轉化。產生包括用於靶向Eno1的胺基酸序列的表達構建體的方法完全在本領域技術人員的能力範圍內。
c.脂質體
脂質體遞送系統是本領域已知的,包括限制全身性暴露的製劑,由此降低全身性暴露和脫靶效應。例如,是其中阿黴素包裹在長循環PEG化脂質體中的用於治療特定類型癌症的組合物,所述脂質體進一步包含膽固醇。兩性黴素B的各種脂質體製劑(包括和)配製成用於在脂質體或含有各種磷脂、膽固醇和硫酸膽甾醇酯的脂質複合物中靜脈內施用。是在卵磷脂醯甘油和DMPC中配製為脂質體的維替泊芬(verteporfin),用於靜脈內施用。脂質體製劑也已知用於肌肉內注射。是滅活的A肝病毒,而是滅活的流感病毒A株和B株的血細胞凝集素(hemaglutinine)。兩種病毒製劑都在DOPC和DOPE的組合中配製。這樣的脂質體,或其他生理上可接受的脂質體,可以用於Eno1的包裝並且隨後用靶向部分表面修飾以將Eno1遞送至肌肉。還可以包括調節脂質體的細胞內運輸的其他部分。脂質體攝取至細胞中時,脂質體釋放Eno1,由此允許其具有其治療效果。
d.樹狀聚合物
樹狀聚合物可以用作用於將多個靶向部分與一個或多個Eno1分子連接的支架。在特定實施方案中,樹狀聚合物在與Eno1偶聯之前用靶向部分修飾。
e.微粒
微粒可以用作用於將多個靶向部分與一個或多個Eno1分子連接的支架,Eno1分子與微粒連接或包封在微粒中。在特定實施方案中,微粒在與Eno1偶聯之前用靶向部分修飾。
f.病毒載體
已經長期研究病毒嗜性,並用於指引病毒至目標細胞類型。Parker等,2013(Gene Therapy,20:1158-64)已經研發了具有血清型35的纖維和peton的腺病毒血清型5帽位點(capsite),以增強至骨骼肌和/或平滑肌的遞送。這樣的病毒載體和其他病毒載體可以用於將Eno1表達構建體遞送至肌細胞。
C.樹狀聚合物
樹狀聚合物在本發明的情況中可以用作用於靶向複合物的骨架,而用於將非肌肉內施用的Eno1遞送至肌肉。或者,樹狀聚合物可以用於調節肌肉內施用的Eno1的藥代動力學和藥效學特性。在本發明的組合物和方法中,樹狀聚合物理解為藥物學上可接受的樹狀聚合物。
基於樹狀聚合物的平臺已經獲得了對用於藥物應用中的關注。與其他聚合物載體相似,樹狀聚合物可以合成以避免結構毒性和免疫原性。樹狀聚合物模擬人蛋白質的大小、溶解性和形狀的能力使得該技術成為用於許多治療和診斷應用的理想選擇。1-10納米的大小使得樹狀聚合物能夠有效地穿過血管內皮擴散,內化至細胞中,並且通過腎臟快速清除。這有助於避免長期毒性並且降低對快速降解平臺的需求。多個反應性表面基團的可利用性使得樹狀聚合物能夠攜帶功能性分子的較高有效載荷,從而增強至作用位點的靶向遞送,由此提高功效。
已經生產或正在商業研發針對幾種生物醫學應用的樹狀聚合物。局部的、基於聚賴氨酸樹狀聚合物的殺菌劑,VivaGelTM,已經由Starpharma研發。是用於基因轉染的基於樹狀聚合物的材料。基於樹狀聚合物的診斷工具包括Gadomer-17,一種含有用釓螯合物功能化的聚賴氨酸樹狀聚合物的磁共振成像(MRI)造影劑,以及CS,一種用於心臟標誌物以快速診斷心臟病發作的生物傳感劑。
樹狀聚合物通過其芯-殼結構來限定,其中樹狀聚合物利用添加至芯的各個另外的殼(或代)使功能性表面基團的大小和數量大約翻倍。外殼通過本領域公知的方式通過交替的單體反應合成。可以通過改變單體單元來合成專門的樹狀聚合物骨架。樹狀聚合物的生物學特性很大程度上受到化學骨架和表面終止(surface termination)的影響。對於成為用於體內藥物遞送的合適載體的樹狀聚合物,它們必須是無毒的、非免疫原性的和能夠通過穿過合適的屏障而靶向和到達特定的位置,同時足夠穩定以保留在循環中。文獻中合成和公開的絕大部分樹狀聚合物在生理條件下是不溶的或不能夠在添加功能性分子後保持可溶並且不適用於生物學應用。然而,幾類樹狀聚合物已經顯示出對於生物醫學應用是有用的支架;實例包括聚酯、聚賴氨酸和聚丙烯亞胺(PPI或DAB)樹狀聚合物。
生物醫學應用中最廣泛使用的樹狀聚合物是聚(醯胺胺)(PAMAM)樹狀聚合物。從丙烯酸甲酯和乙烯-二胺的重複反應合成的聚醯胺骨架幫助大分子保持水溶性並最小化免疫原性。不同代的PAMAM樹狀聚合物還能夠模擬身體中容易發現的球狀蛋白的大小和特性。全代PAMAM樹狀聚合物的胺封端表面允許容易的表面修飾,使得平臺能夠在生理條件下攜帶和溶解疏水性治療分子,如氨甲喋呤。如果表面胺被中和或適當修飾(例如,醯基化),PAMAM樹狀聚合物呈現出很少的非特異性毒性。
主動靶向使用分子(如靶向部分)以通過結合於細胞特異性分子來介導其有效載荷(藥物或其他)遞送至細胞。靶向部分,如本文中提供的那些,常常通過靶細胞上高度表達的受體來結合。靶向配體和細胞表面受體之間的相互作用允許治療劑或有效載荷選擇性地到達肌細胞並且甚至通過受體介導的過程引導到細胞內。
與單一配體相比,與在樹狀聚合物表面上呈現多個結合配體相關的多價效應增強樹狀支架的攝取。由多個配體的同時結合引起的多價相互作用允許樹狀聚合物提高平臺的結合親合力,甚至在單個配體對靶向的受體具有低親和性時。PAMAM平臺已經成功地用作用於連接多價靶向分子(包括抗體、肽、T-抗原和葉酸)的支架。靶向配體將樹狀聚合物錨定至其中特定受體在細胞表面上表達的位置。靶向的樹狀聚合物-藥物偶聯物特異性地遞送更高劑量至靶向的細胞而同時避開正常細胞,因此避免潛在的全身性毒性。
用乙醯基中和PAMAM樹狀聚合物的表面胺最小化毒性和非特異性的樹狀聚合物攝取。樹狀聚合物的乙醯基加帽還允許提高從身體的清除,最小化長期治療的影響。氨基封端的PAMAM樹狀聚合物的PEG化降低免疫原性和提高溶解性。與陽離子母體材料相比,PEG封端的樹狀聚合物具有提高的血流半衰期。羥基和甲氧基封端的聚酯樹狀聚合物已經顯示出在高達40mg/kg的濃度下在體內是無毒的。已經在體內證實了陽離子和陰離子樹狀聚合物之間的毒性差異。使用斑馬魚胚模型,羧基封端的樹狀聚合物的毒性顯著低於G4胺封端的樹狀聚合物。在相同研究中,用RGD的表面修飾也降低了毒性。
將理解以上和本文中描述的所有樹狀聚合物可以用於本發明的Eno1組合物及其使用方法中。
在特定實施方案中,包含樹狀聚合物和Eno1的複合物中樹狀聚合物分子數與Eno1分子數的比率為約1:1至約10:1,例如,約1:1,約2:1,約3:1,約4:1,約5:1,約6:1,約7:1,約8:1,約9:1或約10:1。在一個實施方案中,包含樹狀聚合物和Eno1的複合物中樹狀聚合物分子數與Eno1分子數的比率為約3:1至7:1,例如,3:1,4:1,5:1,6:1或7:1。在一個實施方案中,包含樹狀聚合物和Eno1的複合物中樹狀聚合物分子數與Eno1分子數的比率為4:1至6:1,例如,3:1,4:1或5:1。在一個實施方案中,包含樹狀聚合物和Eno1的複合物中樹狀聚合物分子數與Eno1分子數的比率為3:1至5:1,例如,3:1,4:1或5:1。在再另一個實施方案中,包含樹狀聚合物和Eno1的複合物中樹狀聚合物分子數與Eno1分子數的比率為4:1至5:1。在另一個實施方案中,包含樹狀聚合物和Eno1的複合物中樹狀聚合物分子數與Eno1分子數的比率為3:1至4:1。在進一步優選的實施方案中,包含樹狀聚合物和Eno1的複合物中樹狀聚合物分子數與Eno1分子數的比率為約5:1。
可以通過使用本領域已知的任何常規方法,如,例如,丙酮酸激酶(PK)/乳酸脫氫酶(LDH)試驗或本文中描述的任何其他試驗,通過測定樹狀聚合物/Eno1複合物的Eno1活性(例如,與未複合的Eno1相比)來測試和選擇複合物中樹狀聚合物與Eno1的最佳比率。還可以通過在體外試驗中評價樹狀聚合物/Eno1複合物對葡萄糖攝取的作用,例如,按照本文中實施例2所述的通過測量人骨骼肌微管(HSMM)中的葡萄糖攝取或本領域已知的任何相似試驗,來測試和選擇樹狀聚合物與Eno1的最佳比率。還可以通過在體內測量樹狀聚合物/Enol複合物對血糖水平的作用,例如,按照本文中實施例7和8中所述的通過測量糖尿病小鼠模型中樹狀聚合物/Eno1複合物對血糖的作用,或本領域已知的任何相似模型或試驗,來測試和選擇樹狀聚合物與Eno1的最佳比率。複合物中樹狀聚合物與Eno1的最佳比率將優選保留體外和/或體內的Eno1活性,和/或提供Eno1至細胞的遞送。
將理解本發明的組合物和方法包括超過一種樹狀聚合物-Eno1-靶向肽複合物(即樹狀聚合物-Eno1-靶向肽複合物群體)的施用。因此,將理解每個Eno1分子的樹狀聚合物數可以表示複合物群體中每個Eno1的平均樹狀聚合物數。在特定實施方案中,至少70%的複合物具有選定的樹狀聚合物與Eno1的摩爾比。在特定實施方案中,至少75%的複合物具有選定的樹狀聚合物與Eno1的摩爾比。在特定實施方案中,至少80%的複合物具有選定的樹狀聚合物與Eno1的摩爾比。在特定實施方案中,至少85%的複合物具有選定的樹狀聚合物與Eno1的摩爾比。在特定實施方案中,至少90%的複合物具有選定的樹狀聚合物與Eno1的摩爾比。
在特定實施方案中,樹狀聚合物/Eno1/靶向肽複合物中樹狀聚合物分子數與靶向肽數的比率為1:0.1至1:10,1:1至1:10,1:1至1:5,或1:1至1:3。在特定實施方案中,樹狀聚合物分子數與靶向肽數的比率為約1:1,1:2,1:3,1:4,1:5,1:6,1:7,1:8,1:9或1:10。在優選實施方案中,樹狀聚合物/Eno1/靶向肽複合物中樹狀聚合物分子數與靶向肽數的比率為約1:1。在優選實施方案中,樹狀聚合物/Eno1/靶向肽複合物中樹狀聚合物分子數與靶向肽數的比率為約1:2。在優選實施方案中,樹狀聚合物/Eno1/靶向肽複合物中樹狀聚合物分子數與靶向肽數的比率為約1:3。
在特定實施方案中,樹狀聚合物/Eno1/靶向肽複合物中靶向肽數與樹狀聚合物分子數的比率為至少1:1,至少2:1,至少3:1,至少4:1,至少5:1,至少6:1,至少7:1,至少8:1,至少9:1或至少10:1。在一個實施方案中,樹狀聚合物/Eno1/靶向肽複合物中靶向肽數與樹狀聚合物分子數的比率為至少3:1。
將理解本發明的組合物和方法包括超過一個靶向肽-Eno1-樹狀聚合物複合物(即靶向肽-Eno1-樹狀聚合物複合物群體)的施用。因此,將理解每個樹狀聚合物的靶向肽數表示複合物群中每個樹狀聚合物的平均靶向肽數。在特定實施方案中,至少70%的複合物具有選定的靶向肽與樹狀聚合物的摩爾比。在特定實施方案中,至少75%的複合物具有選定的靶向肽與樹狀聚合物的摩爾比。在特定實施方案中,至少80%的複合物具有選定的靶向肽與樹狀聚合物的摩爾比。在特定實施方案中,至少85%的複合物具有選定的靶向肽與樹狀聚合物的摩爾比。在特定實施方案中,至少90%的複合物具有選定的靶向肽與樹狀聚合物的摩爾比。
可以通過測量樹狀聚合物/Eno1/靶向肽在體內對特定組織的靶向,例如,如本文中實施例6中所述的,通過測量可檢測地標記的樹狀聚合物/Eno1/靶向肽複合物在體內的靶向,來選擇樹狀聚合物與靶向肽的最佳比率。
V.血糖水平的指標的檢測和測量及控制
用於檢測和測量血糖升高的指標和血糖控制的方法可以根據待測量指標的性質而改變。可以直接(例如,通過測定血液中葡萄糖的量)或間接(例如,通過檢測糖化血紅蛋白(HbA1c)的量)測量升高的血糖,且由此測量血糖水平控制的喪失和糖尿病的嚴重性,糖化血紅蛋白是血紅蛋白和葡萄糖的反應產物。本發明進一步提供用於使用Eno1檢測血糖控制的方法。
本發明考慮任何合適的手段、技術和/或程序用於檢測和/或測量本發明的血糖水平指標。本領域技術人員將理解用於測量本發明指標的方法將至少取決於所檢測或測量的指標(例如,葡萄糖、酮類、mRNA或多肽,包括糖化多肽)和生物樣品(例如,全血、血清)的類型。特定的生物樣品在測量本發明的生物標誌物之前還可能需要特定的專門處理,例如,在待測量mRNA生物標誌物(例如,Eno1mRNA)的情況中mRNA的製備。
A.使用確定的指標直接或間接測量血糖和血糖控制
血糖監控是在單個時間點直接測試血液中的葡萄糖濃度(血糖)的方式。在糖尿病的護理中特別重要的,血糖測試通過刺穿皮膚(通常,在手指上)以抽血,然後將血液施加於化學活性的一次性「測試條」上來進行。不同的製造商使用不同的技術,但大部分系統測量電特徵,並且使用這種電特徵來測定血液中的葡萄糖水平。該測試通常稱作毛細血管血糖。用於周期性或連續使用的商業可購得的血糖監測器是本領域已知的。用於周期性檢測血糖水平的葡萄糖監測器包括,但不限於,TRUEResult血糖計(TRUE)、ACCU-CHEK血糖計(ACCU-CHEK)、OneTouch血糖計(ONETOUCH)和FreeStyle Lite Blood Glucose(FREESTYLE LITE)。將理解,直接測量的正常血糖水平將根據最後食用食物後的時間量而不同,正常的空腹血糖水平低於正常的餐後血糖水平。直接血糖監控也用於葡萄糖耐量測試中以監控對服用高劑量葡萄糖的反應和葡萄糖從血液清除的速率。
糖化血紅蛋白(血紅蛋白A1c、HbA1c、A1C、Hb1C、HbA1c)是主要測量來鑑定延長時間段上平均血糖濃度的血紅蛋白形式,即血糖的間接測量。HbA1c通過血紅蛋白暴露於血糖而在非酶促糖化途徑中形成。當存在正常血糖水平時,產生正常量的糖化血紅蛋白,其作為總血紅蛋白的百分比或特定的血液濃度測量。當血糖水平高時,產生升高的糖化血紅蛋白水平。糖化是不可逆的反應。因此,紅細胞內糖化血紅蛋白的量反映出細胞已經暴露於其中的葡萄糖的平均水平。測量糖化血紅蛋白通過監控長期血清葡萄糖調控而非通過葡萄糖監控提供的快照圖像來評價治療的有效性。HbA1c水平與之前四周至三個月內的平均血糖濃度成比例。例如,可以使用高性能液相色譜(HPLC)或免疫分析來測量HbA1c水平。以下詳細討論用於檢測和測量蛋白質分析物的方法。
B.核酸指示劑的檢測
在特定實施方案中,本發明涉及核酸生物標誌物(例如,Eno1 mRNA生物標誌物)的檢測,任選地結合血糖的其他指示劑,來監控受試者中的糖尿病和/或血糖控制,例如,血糖、酮類和/或HbA1c的直接測量。
在各種不同的實施方案中,本發明的診斷/預後方法通常涉及血樣中Eno1表達水平的測定。本發明方法實施中基因表達水平的測定可以通過任何合適的方法來進行。例如,可以通過檢測從目標基因表達的mRNA的表達和/或檢測由基因編碼的多肽的表達來進行基因表達水平的測定。
對於檢測編碼Eno1的核酸,可以使用任何合適的方法,包括但不限於,Southern印跡分析、northern印跡分析、聚合酶鏈式反應(PCR)(參見,例如,美國專利No.4,683,195;4,683,202和6,040,166;"PCR Protocols:A Guide to Methods and Applications(PCR實驗方案:方法和應用指導)",Innis等(編輯);1990,Academic Press:New York)、逆轉錄酶PCR(RT-PCR)、錨定PCR、競爭性PCR(參見,例如,美國專利No.5,747,251)、cDNA末端快速擴增(RACE)(參見,例如,"Gene Cloning and Analysis:Current Innovations(基因克隆和分析:目前的創新),1997,pp.99-115);連接酶鏈式反應(LCR)(參見,例如,EP 01 320 308);單邊PCR(Ohara等,Proc.Natl.Acad.Sci.,1989,86:5673-5677)、原位雜交、基於Taqman的分析(Holland等,Proc.Natl.Acad.Sci.,1991,88:7276-7280)、差異顯示(參見,例如,Liang等,Nucl.Acid.Res.,1993,21:3269-3275)和其他RNA指紋技術、基於核酸序列的擴增(NASBA)和其他基於轉錄的擴增系統(參見,例如,美國專利No.5,409,818和5,554,527)、Qbeta複製酶、鏈置換擴增(SDA)、修復鏈反應(RCR)、核酸酶保護分析、基於減法的方法(subtraction-based method)、等。
在其他實施方案中,可以通過擴增從mRNA產生的互補DNA(cDNA)或互補RNA(cRNA)並使用微陣列對其進行分析來測定Eno1的基因表達水平。多種不同的陣列構造及其生產方法是本領域技術人員已知的(參見,例如,美國專利No.5,445,934;5,532,128;5,556,752;5,242,974;5,384,261;5,405,783;5,412,087;5,424,186;5,429,807;5,436,327;5,472,672;5,527,681;5,529,756;5,545,531;5,554,501;5,561,071;5,571,639;5,593,839;5,599,695;5,624,711;5,658,734和5,700,637。微陣列技術允許同時測量大量基因的穩態mRNA水平。目前廣泛使用的微陣列包括cDNA陣列和寡核苷酸陣列。使用微陣列的分析通常是基於從標記探針接收的信號強度的測量,所述標記探針用於檢測來自樣品的與固定於微陣列上已知位置的核酸探針雜交的cDNA序列(參見,例如,美國專利No.6,004,755;6,218,114;6,218,122和6,271,002)。基於陣列的基因表達方法是本領域已知的並且在許多科學出版物以及專利中描述(參見,例如,M.Schena等,Science,1995,270:467-470;M.Schena等,Proc.Natl.Acad.Sci.USA 1996,93:10614-10619;J.J.Chen等,Genomics,1998,51:313-324;美國專利No.5,143,854;5,445,934;5,807,522;5,837,832;6,040,138;6,045,996;6,284,460和6,607,885)。
在一個特定的實施方案中,本發明包括通過擴增和檢測對應於Eno1的核酸,任選結合血糖升高的一種或多種其他指示劑,來鑑別遭受異常血糖的受試者的方法。
用作擴增模板的核酸可以根據標準方法(Sambrook等,1989)從生物樣品中所含的細胞分離。核酸可以是基因組DNA或者片段化或全細胞RNA。在使用RNA的情況中,將RNA轉化成互補cDNA可能是需要的。在一個實施方案中,RNA是全細胞RNA,並且直接用作擴增模板。
將與對應於本文中鑑定的任一Eno1核苷酸序列的核酸選擇性雜交的引物對在允許選擇性雜交的條件下接觸分離的核酸。一旦雜交,將核酸:引物複合物接觸一種或多種促進模板依賴性核酸合成的酶。進行多輪擴增,也稱為「循環」,直至產生足夠量的擴增產物。接著,檢測擴增產物。在特定應用中,可以通過視覺方式進行檢測。或者,檢測可以涉及通過化學發光、摻入的放射性標記或螢光標記的放射性閃爍掃描法或甚至通過使用電或熱脈衝信號的系統(AFFYMAX技術;Bellus,1994)的間接產物鑑定。檢測後,可以將給定患者中看到的結果與正常患者和血糖升高患者(例如,前驅糖尿病、2型糖尿病、妊娠糖尿病或1型糖尿病患者)的統計學顯著參照組進行比較。以這種方式,有可能將檢測的核酸量與各種臨床狀態相關聯。
如本文中限定的,術語引物表示包括能夠在模板依賴性方法中啟動新生核酸的合成的任何核酸。通常,引物是長度十至二十個,優選十五至二十個核苷酸的寡核苷酸,但也可以使用更長的序列。引物以雙鏈或單鏈形式來提供,儘管優選單鏈形式。
多種模板依賴性方法可用於擴增給定模板樣品中存在的核酸序列。最佳的已知擴增方法之一是聚合酶鏈式反應(稱為PCR),其詳細描述於美國專利No.4,683,195,4,683,202和4,800,159以及Innis等,1990中,將其每篇全部按引用併入本文中。
在PCR中,製備兩個引物序列,其與靶核酸序列的相對互補鏈上的區域互補。將過量的三磷酸脫氧核苷酸連同DNA聚合酶(例如,Taq聚合酶)一起加入反應混合物中。如果樣品中存在靶核酸序列,引物將結合靶核酸並且聚合酶將通過添加核苷酸引起引物沿著靶核酸序列延伸。通過升高和降低反應混合物的溫度,延伸的引物將與靶核酸解離以形成反應產物,過量引物將結合靶核酸和反應產物,並且重複該過程。
可以進行逆轉錄酶PCR擴增程序以定量擴增的mRNA的量。將RNA逆轉錄成cDNA的方法是公知的並且描述於Sambrook等,1989中。逆轉錄的替代方法利用熱穩定的DNA聚合酶。這些方法描述於1990年12月21日提交的WO 90/07641中。聚合酶鏈式反應方法是本領域公知的。
用於擴增的另一種方法是連接酶鏈式反應(「LCR」),公開於歐洲申請No.320 308中,將其全部按引用併入本文中。在LCR中,製備兩個互補探針對,並且在靶序列存在下,每個對結合靶標的相對互補鏈,使得它們鄰接。在連接酶的存在下,兩個探針對連接以形成單個單元。通過溫度循環,如PCR中那樣,結合的連接單元從靶標解離,並且隨後用作用於過量探針對連接的「靶序列」。美國專利No.4,883,750描述了一種與LCR類似的用於將探針對結合靶序列的方法。
Qbeta複製酶,描述於PCT申請No.PCT/US87/00880中,也可以用作本發明中的再另一種擴增方法。在這種方法中,在RNA聚合酶存在下,將具有與靶標的區域互補的區域的RNA的重複序列加入樣品中。聚合酶將複製該重複序列,其隨後可以被檢測到。
等溫擴增方法可以用於本發明的核酸擴增中,其中使用限制性核酸內切酶和連接酶來獲得在限制性位點的一條鏈中含有核苷酸5』-[α-硫代]-三磷酸的靶分子的擴增。Walker等(1992),將其全部按引用併入本文中。
鏈置換擴增(SDA)是進行核酸的等溫擴增的另一種方法,其涉及多輪鏈置換和合成,即,缺口平移。相似的方法,稱為修復鏈反應(PCR),涉及在靶向用於擴增的整個區域中使幾個探針退火,接著進行修復反應,其中只存在四種鹼基中的兩種。為了易於檢測,其他兩種鹼基可以作為生物素化的衍生物加入。相似的方法用於SDA中。也可以使用循環探針反應(CPR)檢測靶特異性的序列。在CPR中,具有非特異性DNA的3』和5』序列以及特異性RNA的中間序列的探針與樣品中存在的DNA雜交。雜交時,用RNase H處理反應,並且將探針的產物鑑別為截然不同的產物,其在消化後釋放。將原始模板與另一個循環探針退火併重複該反應。
根據本發明可以使用GB申請No.2 202 328和PCT申請No.PCT/US89/01025中描述的再另外的擴增方法,每篇都以其全部按引用併入。在前一申請中,將「修飾的」引物用於PCR樣的、模板和酶依賴性合成中。可以通過用捕獲部分(例如,生物素)和/或檢測部分(例如,酶)標記來修飾引物。在後一申請中,將過量的標記引物加入樣品中。在靶序列存在的情況下,探針結合併通過催化切割。切割後,靶序列完整釋放以被過量的探針結合。標記探針的切割給出靶序列存在的信號。
其他考慮的核酸擴增程序包括基於轉錄的擴增系統(TAS),包括基於核酸序列的擴增(NASBA)和3SR。Kwoh等(1989);Gingeras等,PCT申請WO 88/10315,將其全部按引用併入本文中。在NASBA中,核酸可以通過標準苯酚/氯仿萃取、臨床樣品的熱變性、用裂解緩衝液和用於DNA和RNA分離的minispin柱處理或者RNA的鹽酸胍提取來製備用於擴增。這些擴增技術涉及使具有靶特異性序列的引物退火。聚合後,用RNase H消化DNA/RNA雜合體,同時將雙鏈DNA分子再次熱變性。在任一種情況中,通過添加第二靶特異性引物,接著聚合將單鏈DNA製成完全雙鏈的。然後通過聚合酶如T7或SP6多重轉錄雙鏈DNA分子。在等溫循環反應中,將RNA逆轉錄成雙鏈DNA,並用聚合酶如T7或SP6再轉錄一次。將所得到的產物(不管是截短的或完整的)表明靶特異性的序列。
Davey等,歐洲申請No.329 822(將其全部按引用併入本文中)公開了涉及循環合成的單鏈RNA(「ssRNA」)、ssDNA和雙鏈DNA(dsDNA)的核酸擴增方法,其可以根據本發明來使用。ssRNA是用於第一引物寡核苷酸的第一模板,其通過逆轉錄酶(RNA依賴性DNA聚合酶)來延伸。RNA然後通過核糖核酸酶H(RNase H,對於DNA或RNA雙鏈體中的RNA特異性的RNA酶)的作用從所得到的DNA:RNA雙鏈體除去。所得到的ssDNA是用於第二引物的第二模板,其也包括5』側與模板同源性的RNA聚合酶啟動子的序列(通過T7RNA聚合酶舉例說明)。然後這個引物通過DNA聚合酶(通過大腸桿菌DNA聚合酶1的大「Klenow」片段來舉例說明)延伸,從而形成雙鏈DNA(「dsDNA」)分子,具有與引物之間的原始RNA序列相同的序列,並且在一端另外具有啟動子序列。這種啟動子序列可以被合適的RNA聚合酶利用來製備DNA的許多RNA拷貝。這些拷貝隨後可以重新進入循環,導致非常迅速的擴增。通過酶的適當選擇,可以等溫地進行這種擴增而不需要在每個循環添加酶。由於這種方法的循環性質,可以選擇DNA或RNA形式的起始序列。
Miller等,PCT申請WO 89/06700(將其全部按引用併入本文中)公開了基於啟動子/引物序列與單鏈靶DNA(「ssDNA」)雜交接著轉錄該序列的許多RNA拷貝的核酸序列擴增方案。這種方案不是循環的,即,新模板不是從所得到的RNA轉錄物產生。其他擴增方法包括「race」和「單側PCR.TM.」。Frohman(1990)和Ohara等(1989),將每篇都以其全部按引用併入本文中。
基於在具有所得到的「二-寡核苷酸」的序列的核酸存在下連接兩個(或更多個)寡核苷酸而由此擴增二-寡核苷酸的方法也可以用於本發明的擴增步驟中。Wu等(1989),將其全部按引用併入本文中。
根據特定的分析形式和特定的需求以及使用的靶向序列,本發明的寡核苷酸探針或引物可以是任何合適長度的。在優選實施方案中,寡核苷酸探針或引物長度為至少10個核苷酸(優選地,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,30,31,32…),優選長度至少15個核苷酸(15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,30,31,32…),並且它們可以適應地改變以尤其適合於選定的核酸擴增系統和/或使用的雜交系統。較長的探針和引物也在本發明的範圍內,如本領域公知的。具有超過30,超過40,超過50個核苷酸的引物和具有超過100,超過200,超過300,超過500,超過800和超過1000個核苷酸長度的探針也被本發明涵蓋。當然,較長的引物具有更昂貴的缺陷,並且因此,本領域中通常設計和使用具有15至30個核苷酸長度的引物。如本領域公知的,在本發明的方法中可以使用長度範圍為10至超過2000個核苷酸的探針。對於上述%同一性,非特意描述的探針和引物的大小(例如,16,17,31,24,39,350,450,550,900,1240個核苷酸…)也在本發明的範圍內。在一個實施方案中,本發明的寡核苷酸探針或引物與Eno1RNA(或其互補序列)或Eno1 mRNA特異性地雜交。更優選,選擇Eno1引物和探針來檢測與血糖升高或異常血糖調控相關的Eno1RNA,該血糖升高或異常血糖調控與例如前驅糖尿病、2型糖尿病、1型糖尿病或妊娠糖尿病相關。
在其他實施方案中,檢測手段可以利用雜交技術,例如,其中選擇特異性的引物或探針與目標靶生物標誌物(例如,Eno1)退火,並且此後進行選擇性雜交的檢測。如本領域通常所知的,可以通過考慮其雜交的熔點及其靶向的序列來設計寡核苷酸探針和引物(參見下文和Sambrook等,1989,Molecular Cloning--A Laboratory Manual(分子克隆--實驗室手冊),第2版,CSH Laboratories;Ausubel等,1994,見Current Protocols in Molecular Biology(分子生物學通用實驗方案),John Wiley&Sons Inc.,N.Y.)。
為了使得能夠在本發明的測試條件下發生雜交,寡核苷酸引物和探針應當包含與Eno1多核苷酸的一部分具有至少70%(至少71%,72%,73%,74%或更高),優選至少75%(75%,76%,77%,78%,79%,80%,81%,82%,83%,84%,85%,86%,87%,88%,89%或更高)和更優選至少90%(90%,91%,92%,93%,94%,95%,96%,97%,98%,99%,100%)同一性的寡核苷酸序列。本發明的探針和引物是在嚴格雜交條件下雜交的那些和在至少中等嚴格條件下與Eno1同源物雜交的那些。在特定實施方案中,本發明的探針和引物具有與Eno1基因序列(例如,cDNA或mRNA)的完全序列同一性。應當理解,通過使用本領域已知的計算機比對和序列分析的方法(參考Molecular Cloning:A Laboratory Manual(分子克隆:實驗室手冊),第三版,由Cold Spring Harbor Laboratory編輯,2000),可以基於本文中公開的Eno1序列容易地設計其他探針和引物並用於本發明中。
C.血糖控制的血糖多肽指示劑的檢測
本發明考慮用於檢測血糖的多肽指示劑(包括Eno1或HbA1c)的任何合適方法。在特定實施方案中,檢測方法是涉及特異性地結合Eno1和血紅蛋白中的一種或多種的抗體的免疫檢測方法,尤其是特異性地結合糖化血紅蛋白。各種有用的免疫檢測方法的步驟已經描述於科學文獻中,如,例如,Nakamura等(1987),將其按引用併入本文中。
通常,免疫檢測方法包括獲得懷疑含有血糖升高的蛋白質或肽指示劑的樣品,並且根據具體情況,在有效地允許免疫複合物形成的條件下將樣品接觸根據本發明的抗體。
免疫結合方法包括用於檢測或定量樣品中的反應性組分的量,該方法需要檢測或定量在結合過程中形成的任何免疫複合物。在此,將獲得懷疑含有血糖升高的蛋白質或肽指示劑的樣品,並將樣品接觸抗體,然後檢測或定量在特定條件下形成的免疫複合物的量。
就血糖指標的檢測而言,分析的生物樣品可以是懷疑含有血糖的蛋白質或肽指示劑(如Eno1或HbA1c)的任何樣品。在HbA1c的情況中,生物樣品可以是例如血液,或在Eno1的情況中,可以是血液或血清。
在有效地允許免疫複合物(初級免疫複合物)形成的條件下並持續足夠的時間將選定的生物樣品接觸抗體(例如,作為結合生物樣品中的Eno1、HbA1c或血紅蛋白的檢測劑)。通常,複合物形成是將組合物簡單地加入生物樣品中並將混合物孵育對於抗體與存在的任何抗原形成複合物(即,結合存在的任何抗原)足夠長的時間的問題。在這個時間後,通常洗滌樣品-抗體組合物,如組織切片、ELISA平板、點印跡或western印跡,以除去任何非特異性結合的抗體物質,從而只允許在初級免疫複合物內特異性結合的那些抗體被檢測到。
通常,免疫複合物形成的檢測是本領域公知的並可以通過應用多種途徑來實現。這些方法通常基於標記或標誌物的檢測,如本領域標準用途的任何放射性、螢光、生物或酶標籤或標記。關於此類標記使用的美國專利包括美國專利No.3,817,837;3,850,752;3,939,350;3,996,345;4,277,437;4,275,149和4,366,241,將每篇都按引用併入本文中。當然,如本領域已知的,可以通過使用第二結合配體如第二抗體或生物素/抗生物素蛋白配體結合設置發現另外的優勢。
檢測中使用的抗體(例如,抗Eno1抗體、抗血紅蛋白或抗糖化血紅蛋白抗體)可以自身連接於可檢測標記,其中隨後可以簡單地檢測這種標記,由此允許測定組合物中初級免疫複合物的量。
或者,可以通過對於結合的抗體具有結合親和性的第二結合配體來檢測成為結合在初級免疫複合物內的第一添加組分。在這些情況中,第二結合配體可以連接於可檢測標記。第二結合配體自身常常是抗體,其因此可以被稱為「第二」抗體。將初級免疫複合物在有效地允許次級免疫複合物形成的條件下接觸標記的第二結合配體或抗體持續足夠的時間。然後通常洗滌次級免疫複合物以除去任何非特異性結合的標記的第二抗體或配體,並且隨後檢測次級免疫複合物中保留的標記。
更多的方法包括通過兩步法檢測初級免疫複合物。如上所述,將對編碼的蛋白質、肽或相應的抗體具有結合親和性的第二結合配體(如抗體)用於形成次級免疫複合物。洗滌後,將次級免疫複合物再次在有效地允許免疫複合物(三級免疫複合物)形成的條件下接觸對於第二抗體具有結合親和性的第三結合配體或抗體持續足夠的時間。第三配體或抗體連接於可檢測標記,從而允許檢測由此形成的三級免疫複合物。該系統可以提供信號擴大,如果這是希望的。
本發明的免疫檢測方法在病症的診斷中具有明顯的實用性,所述病症如升高的血糖、血糖控制的喪失和糖尿病。在此,使用懷疑含有編碼的蛋白質或糖化肽的生物或臨床樣品。然而,這些實施方案對非臨床樣品也具有用途,如在抗原或抗體樣品的滴定中、在雜交瘤的選擇中等等。
本發明特別考慮了將ELISA用作一種免疫檢測分析類型的用途。考慮了本發明的生物標誌物蛋白或肽將發現在診斷和預後監控異常血糖和糖尿病的ELISA試驗中作為免疫原的用途。免疫分析,以其最簡單和直接的意義,是結合測試。特定的優選免疫分析是本領域已知的各種類型的酶聯免疫吸附試驗(ELISA)和放射免疫試驗(RIA)。使用組織切片的免疫組織化學檢測可能是有用的。然而,將容易地認識到檢測不限於這樣的技術,並且western印跡、點印跡等也可以使用。
在一個示例性的ELISA中,將與本發明的蛋白指示劑結合的抗體固定於呈現蛋白親和性的選定表面上,如聚苯乙烯微滴定平板的孔。然後,將懷疑含有血糖水平指示劑的測試組合物,如血液或血清樣品,加入孔中。在結合併洗滌除去非特異性結合的免疫複合物後,可以檢測結合的抗原。通常通過添加與可檢測標記連接的對於指示劑蛋白特異性的第二抗體來實現檢測。這種類型的ELISA是簡單的「夾心ELISA」。還可以通過添加第二抗體,接著添加對第二抗體具有結合親和性的第三抗體來實現檢測,所述第三抗體連接於可檢測標記。
在另一個示例性的ELISA中,將懷疑含有血糖指示劑蛋白的樣品固定於孔表面上,並隨後接觸用於結合指示劑的特異性抗體。在結合併洗滌以除去非特異性結合的免疫複合物後,檢測結合的抗原。在初始抗體連接於可檢測標記的情況中,可以直接檢測免疫複合物。再次,可以使用對第一抗體具有結合親和性的第二抗體來檢測免疫複合物,所述第二抗體連接於可檢測標記。
與使用的形式無關,ELISA具有特定的共同特徵,如塗覆、孵育或結合,洗滌以除去非特異性結合的物質,並檢測結合的免疫複合物。這些如下所述。
在用抗原或抗體塗覆平板中,通常將用抗原或抗體的溶液孵育平板的孔,孵育過夜或持續指定的時間段。然後洗滌平板的孔以除去未完全吸附的材料。然後用對於測試抗血清在抗原上是中性的非特異性蛋白「塗覆」任何剩餘的可用孔表面。這些包括牛血清白蛋白(BSA)、酪蛋白和奶粉溶液。塗覆允許封閉固定表面上的非特異性吸附位點並由此降低由抗血清非特異性結合在表面上引起的背景。
在ELISA中,習慣上使用次級或三級檢測方式而不是直接程序。因此,蛋白質或抗體與孔結合後,用非反應性物質塗覆來降低背景,並洗滌以除去未結合的物質,固定表面與對照生物樣品接觸,例如來自具有正常血糖的受試者和/或足夠血糖控制的受試者的血液或血清,以在有效地允許免疫複合物(抗原/抗體)形成的條件下測試。然後免疫複合物的檢測需要標記的第二結合配體或抗體,或第二結合配體或抗體與標記的第三抗體或第三結合配體結合。
短語「在有效地允許免疫複合物(抗原/抗體)形成的條件下」表示所述條件優選包括用溶液如BSA、牛γ球蛋白(BGG)和磷酸鹽緩衝鹽水(PBS)/Tween稀釋抗原和抗體。這些添加的試劑也傾向於有助於非特異性背景的降低。
「合適的」條件也表示孵育是在足以允許有效結合的溫度下並持續足夠的時間段。孵育步驟通常為約1至約4小時,優選在大約25至27℃的溫度下,或在約4℃下過夜等等。
在ELISA中的所有孵育步驟後,洗滌接觸的表面以除去非複合的物質。優選的洗滌程序包括用溶液洗滌,所述溶液如PBS/Tween或硼酸鹽緩衝液。測試樣品和初始結合的物質之間形成特異性免疫複合物並隨後洗滌後,可以測定甚至極少量的免疫複合物的出現。
為了提供檢測手段,第二或第三抗體具有連接的標記以允許檢測。優選地,標記是在用合適的發色底物孵育時導致生色的酶。因此,例如,初級或次級免疫複合物在有利於發生更多免疫複合物的形成的條件下用脲酶、葡萄糖氧化酶、鹼性磷酸酶或過氧化氫酶偶聯的抗體接觸和孵育一段時間(例如,在含有PBS的溶液如PBS-Tween中在室溫下孵育2h)。
用標記的抗體孵育並隨後洗滌除去未結合的物質後,將標記的量定量,例如,通過用發色底物(如脲和溴甲酚紫)孵育來定量。然後通過測量顏色產生的程度來定量,例如,使用可見光譜分光光度計來定量。
也可以使用蛋白質質譜方法和儀器來測量、定量、檢測和另外分析本發明的蛋白質生物標誌物/指示劑(例如,Eno1、HbA1c)。蛋白質質譜是指將質譜應用於研究蛋白質。儘管不意圖受到限制,兩種途徑通常使用質譜來表徵蛋白質。在第一種中,將完整的蛋白質電離,然後引入質譜儀中。將這種途徑稱為蛋白質分析的「自上而下」策略。用於完整蛋白質電離的兩種主要方法是電噴霧電離(ESI)和基質輔助雷射解吸/電離(MALDI)。在第二種途徑中,使用蛋白酶如胰蛋白酶將蛋白質酶促消化成較小的肽。隨後將這些肽引入質譜儀中,並通過肽質量指紋譜或串聯質譜法來鑑定。因此,這後一種途徑(也稱為「自下而上」蛋白質組學)使用肽水平的鑑定來推斷蛋白質的存在。
可以使用飛行時間(TOF)MS或傅立葉變換離子迴旋共振(FT-ICR)來進行本發明的生物標誌物的全蛋白質質量分析。因為它們的寬質量範圍,並且在FT-ICR的情況中,由於其高質量準確性,這兩種類型的儀器是有用的。用於肽質量分析的最廣泛使用的儀器是MALDI飛行時間儀器,因為它們允許以高步幅獲取肽質量指紋(PMF)(1PMF可以在大約10秒內分析)。本申請中還可以使用多階段四極飛行時間和四極離子阱。
還可以在共同存在於生物介質或樣品中的蛋白質和分子的複雜混合物中測量蛋白質指示劑,然而,本文中可能需要在考慮樣品的分級。將理解,蛋白質的複雜混合物的電離可能導致其中更豐富的蛋白質具有「淹沒」或遏制來自同一樣品中較不豐富的蛋白質的信號的趨勢。此外,由於混合物組分的巨大數量,來自複雜混合物的質譜可能難以解釋。在質譜分析前,可以使用分級來首先分離蛋白質的任何複雜混合物。有兩種方法廣泛用於將蛋白質或其來自酶消化的肽產物分級。第一種方法將完整蛋白質分級並且稱為二維凝膠電泳。第二種方法,高效液相色譜(LC或HPLC),用於將酶消化後的肽分級。在一些情況中,結合這兩種技術可能是理想的。本文中也考慮了本領域已知的用於將蛋白質混合物分級的任何其他合適的方法。
2D凝膠上確定的凝膠斑點通常可歸屬於一種蛋白質。如果蛋白質的身份是所需要的,通常應用凝膠內消化的方法,其中切除目標蛋白質斑點,並通過蛋白水解消化。可以使用肽質量指紋譜通過質譜測定從消化獲得的肽質量。如果這種信息不允許蛋白質的明確鑑定,則可以將其肽進行串聯質譜法用於從頭測序。
使用HPLC/MS表徵蛋白質混合物在本領域中也可以稱為「鳥槍法蛋白質組學」和MuDPIT(多維蛋白質鑑定技術)。通過一個或兩個液相色譜(LC)步驟將從蛋白質混合物的消化得到的肽混合物分級。來自色譜階段的洗脫液可以通過電噴霧電離直接引入質譜儀,或設置在一系列斑點上用於之後使用MALDI的質量分析。
可以利用各種技術使用MS來鑑定蛋白質指示劑(例如,Eno1或Hb1Ac),本文中考慮了全部這些技術。肽質量指紋譜使用蛋白水解肽的質量作為檢索資料庫的預測質量的輸入,其從一系列已知蛋白質的消化產生。如果參照列表中的蛋白質序列產生了相當大數量的匹配實驗值的預測質量,存在這種蛋白質存在於原始樣品中的一些證據。將進一步理解,用於自動化的、數據依賴性電噴霧電離(ESI)串聯質譜法(MS/MS)結合微毛細管液相色譜(LC)和資料庫檢索的方法和儀器的開發已經顯著提高了凝膠分離蛋白質的鑑定靈敏度和速度。微毛細管LC-MS/MS已經成功用於直接來自混合物的單個蛋白質的大規模鑑定而沒有凝膠電泳分離(Link等,1999;Opitek等,1997)。
幾種最近的方法允許通過質譜來定量蛋白質。例如,碳(13C)或氮(15N)的穩定的(例如,非放射性的)重同位素可以加入一個樣品中,同時另一個可以用相應的輕同位素(例如,12C和14N)標記。在分析前,將兩個樣品混合。由於其質量差異,可以區分源自不同樣品的肽。其峰強度的比例對應於肽(和蛋白質)的相對豐度比率。用於同位素標記的最常用方法是SILAC(細胞培養物中通過胺基酸的穩定同位素標記)、胰蛋白酶催化的18O標記、ICAT(同位素編碼的親和性標籤)、iTRAQ(用於相對和絕對定量的同重同位素標記)。可以進行「半定量」質譜而不需要樣品的標記。通常,這使用MALDI分析來進行(以線性模式)。來自單個分子(通常是蛋白質)的峰強度或峰面積在此與樣品中的蛋白質量相關聯。然而,單個信號取決於蛋白質的初級結構、樣品的複雜性和儀器的設置。其他類型的「無標記」定量質譜使用消化蛋白質的譜計數(或肽計數)作為用於測定相對蛋白質量的手段。
在一個實施方案中,可以根據以下示例性方法,使用質譜從複雜生物樣品鑑別和定量任何一種或多種蛋白質指示劑(例如,Enol,HbA1c),所述示例性方法不是意圖限制本發明或其他基於質譜的方法的使用。
在這個實施方案的第一個步驟中,(A)將包含蛋白質的複雜混合物(包括至少一種目標指示劑)的生物樣品,例如,懷疑血糖提高的生物樣品分級,並用穩定的同位素X標記。(B)接著,將已知量的內標加入生物樣品中,其中通過將與該至少一種目標靶生物標誌物相同的標準蛋白質分級並用穩定的同位素Y標記來製備內標。(C)然後將獲得的這種樣品引入LC-MS/MS設備中,並且使用針對內標選擇的多反應監測(MRM)過渡進行MRM分析以獲得MRM色譜圖。(D)然後觀察MRM色譜圖以鑑定源自生物樣品的顯示出與源自內標的肽(內標肽)相同的保留時間的靶肽生物標誌物,並通過將內標肽的峰面積與靶肽指示劑的峰面積進行比較來定量測試樣品中的靶蛋白指示劑。
任何合適的生物樣品可以用作LC-MS/MS/MRM分析的起始點,包括源自血液、尿液、唾液、毛髮、細胞、細胞組織、活檢材料及其處理產物的生物樣品;以及通過基因重組技術製備的含蛋白質樣品。本發明的優選實施方案包括使用血液或血清樣品。
以下進一步描述以上步驟(A)至(D)中的每一個。
步驟(A)(分級和標記)。在步驟(A)中,將靶蛋白指示劑分級成肽的集合,其隨後用穩定的同位素X來標記。為了將靶蛋白分級,例如,可以使用用蛋白水解酶(蛋白酶)(如胰蛋白酶)和化學切割方法(如使用溴化氰的方法)消化靶蛋白的方法。優選通過蛋白酶的消化。如果允許蛋白水解消化進行完全,則已知給定摩爾量的蛋白質對於每種胰蛋白酶肽切割產物產生相同的摩爾量。因此,測定給定蛋白質的胰蛋白酶肽的摩爾量允許測定樣品中原始蛋白質的摩爾量。可以通過測定蛋白酶消化中含有的靶蛋白衍生的肽(肽集合)的絕對量來完成靶蛋白的絕對定量。因此,為了允許蛋白水解消化進行完全,優選在用胰蛋白酶進行蛋白酶消化前進行還原和烷基化處理以還原並烷基化靶蛋白中所含的二硫鍵。
隨後,將獲得的消化產物(肽集合,包含生物樣品中靶生物標誌物的肽)進行用穩定的同位素X的標記。穩定的同位素X的實例包括氫原子的1H和2H、碳原子的12C和13C以及氮原子的14N和15N。可以從其合適地選擇任何同位素。可以通過將消化產物(肽集合)與含有穩定同位素的試劑反應來進行穩定同位素X的標記。商業上可購得的此類試劑的優選實例包括(由Applied Biosystems生產),其是胺特異性的穩定同位素試劑盒。由2種或3種作為同位素標記結果在其間具有恆定質量差異並且結合肽的N-端或賴氨酸殘基的伯胺的試劑(-輕和-重;或-D0、-D4和-D8)組成。
步驟(B)(內標的添加)。在步驟(B)中,將已知量的內標加入步驟(A)獲得的樣品中。本文中使用的內標是通過將由與待測量的靶蛋白(靶生物標誌物)相同的胺基酸序列組成的蛋白質(標準蛋白質)分級並用穩定的同位素Y標記獲得的消化產物(肽集合)而獲得的消化產物(肽集合)。分級處理可以與以上針對靶蛋白的相同方式來進行。用穩定的同位素Y標記也可以與以上針對靶蛋白的相同方式來進行。然而,本文中使用的穩定同位素Y必須具有與用於標記靶蛋白消化產物的穩定同位素X不同的質量。例如,在使用上述mTRAQ(註冊商標)(由Applied Biosystems生產)的情況中,在將mTRAQ-輕用於標記靶蛋白消化產物時,應當使用mTRAQ-重來標記標準蛋白消化產物。
步驟(C)(LC-MS/MS和MRM分析)。在步驟(C)中,首先將步驟(B)中獲得的樣品放置在LC-MS/MS設備中,然後使用針對內標選定的MRM過渡來進行多反應監測(MRM)分析。通過使用LC-MS/MS設備的LC(液相色譜),首先通過一維或多維高效液相色譜來分離步驟(B)中獲得的樣品(用穩定同位素標記的肽集合)。這樣的液相色譜的特定實例包括陽離子交換色譜,其中通過利用肽之間的電荷差異來進行分離;和反相色譜,其中通過利用肽之間的疏水性差異來進行分離。這兩種方法可以結合使用。
隨後,將每種分離的肽通過使用包括兩臺串聯連接的質譜儀的串聯質譜儀(MS/MS質譜儀)進行串聯質譜分析。使用這樣的質譜儀使得能夠檢測幾飛摩爾(fmol)水平的靶蛋白。此外,MS/MS分析使得能夠分析肽上的內部序列信息,因此能夠實現無假陽性的鑑別。其他類型的MS分析儀也可以使用,包括扇形磁場質譜儀(Sector MS)、四極質譜儀(QMS)、飛行時間質譜儀(TOFMS)和傅立葉變換離子迴旋共振質譜儀(FT-ICRMS),以及這些分析儀的組合。
隨後,將獲得的數據通過搜尋引擎來進行譜比對和列出針對每個蛋白質實驗檢測的肽。優選將檢測的肽針對每個蛋白質分組,並且優選至少三個具有大於前體離子的m/z值的片段和至少三個具有優選500或更大的m/z值的三個片段在譜上以信號強度遞減的順序選自各個MS/MS譜。以強度的遞減順序從這些選擇兩個或更多個片段,並且將強度的平均值限定為MRR過渡的預期靈敏度。當從一個蛋白質檢測到多個肽時,使用預期靈敏度作為指數選擇至少兩個具有最高靈敏度的肽作為標準肽。
步驟(D)(測試樣品中靶蛋白的定量)。步驟(D)包括在步驟(C)中檢測的MRM色譜圖中鑑別顯示出與源自內標的肽(內標肽)相同的保留時間的源自靶蛋白(目標靶生物標誌物)的肽,並通過將內標肽的峰面積與靶肽的峰面積進行比較來定量測試樣品中的靶蛋白。可以通過利用之前製備的標準蛋白的校準曲線來定量靶蛋白。
可以通過以下方法來製備校準曲線。首先,如上所述,用蛋白酶(如胰蛋白酶)消化由與靶生物標誌物蛋白相同的胺基酸序列組成的重組蛋白。隨後,用兩種不同類型的穩定同位素單獨地標記已知濃度的前體片段過渡選擇標準(PFTS)(即,一種用用於標記內標肽的穩定異構體標記(用IS標記),而另一種用用於標記靶肽的穩定異構體標記(用T標記))。通過將特定量的IS標記的PTFS與各種濃度的T標記的PTFS混合來產生多個樣品。將這些樣品置於上述LC-MS/MS設備中以進行MRM分析。將獲得的MRM色譜圖上的T-標記的PTFS與IS-標記的PTFS的面積比(T-標記的PTFS/IS-標記的PTFS)相對於T-標記的PTFS的量進行作圖以製備校準曲線。可以通過參照校準曲線來計算測試樣品中所含的靶蛋白的絕對量。
D.抗體和標記(例如,螢光部分和染料)
在一些實施方案中,本發明提供了包括用於本發明生物分子(例如,單獨或結合血糖和血糖控制的至少一種其他指示劑(例如,HbA1c、酮類)的Eno1)的高靈敏度檢測和定量或用於血糖的直接測量的標記的方法和組合物。本領域技術人員將認識到許多策略可以用於標記靶分子以使得其能夠在顆粒混合物中檢測或區分(例如,標記的抗Eno1抗體或標記的二抗,或與Eno1 mRNA特異性地雜交的標記的寡核苷酸探針)。標記可以通過任何已知方式來連接,包括利用標記和靶標的非特異性或特異性相互作用的方法。標記可以提供可檢測的信號或影響顆粒在電場中的移動性。此外,標記可以直接地或通過結合伴體來完成。
在一些實施方案中,標記包括結合目標指示劑的結合伴體,其中結合伴體連接於螢光部分。本發明的組合物和方法可以利用高螢光部分,例如,在通過所述部分激發波長下的雷射發射光刺激時能夠發射至少約200個光子的部分,其中雷射聚焦於含有所述部分的不小於約5微米直徑的點上,並且其中在所述點處由雷射指引的總能量不超過約3微焦耳。以下更詳細地描述適用於本發明的組合物和方法的部分。
在一些實施方案中,本發明提供了用於檢測生物分子的標記,包括連接於螢光部分的生物分子的結合伴體,其中當通過所述部分激發波長下的雷射發射光刺激時,所述螢光部分能夠發射至少約200個光子,其中雷射聚焦於含有所述部分的不小於約5微米直徑的點上,並且其中在所述點處由雷射指引的總能量不超過約3微焦耳。在一些實施方案中,所述部分包含多個螢光實體,例如,約2至4,2至5,2至6,2至7,2至8,2至9,2至10,或約3至5,3至6,3至7,3至8,3至9,或3至10個螢光實體。在一些實施方案中,所述部分包括約2至4個螢光實體。在一些實施方案中,生物分子是蛋白質或小分子。在一些實施方案中,生物分子是蛋白質。螢光實體可以是螢光染料分子。在一些實施方案中,螢光染料分子包含至少一個取代的吲哚環系統,其中吲哚環的3-碳上的取代基含有化學反應性基團或偶聯物質。在一些實施方案中,染料分子是選自Alexa Fluor 488、Alexa Fluor 532、Alexa Fluor 647、Alexa Fluor 680或Alexa Fluor 700的Alexa Fluor分子。在一些實施方案中,染料分子是選自Alexa Fluor 488、Alexa Fluor 532、Alexa Fluor 680或Alexa Fluor 700的Alexa Fluor分子。在一些實施方案中,染料分子是Alexa Fluor 647染料分子。在一些實施方案中,染料分子包括第一類型和第二類型的染料分子,例如,兩種不同的Alexa Fluor分子,例如,在第一類型和第二類型的染料分子具有不同發射譜的情況中。第一類型與第二類型染料分子的數量比可以為例如,4:1,3:1,2:1,1:1,1:2,1:3或1:4。結合伴體可以是例如抗體。
在一些實施方案中,本發明提供了用於檢測本發明的生物指示劑的標記,其中標記包含指示劑的結合伴體和螢光部分,其中當通過所述部分激發波長下的雷射發射光刺激時,所述螢光部分能夠發射至少約200個光子,其中雷射聚焦於含有所述部分的不小於約5微米直徑的點上,並且其中在所述點處由雷射指引的總能量不超過約3微焦耳。在一些實施方案中,螢光部分包含螢光分子。在一些實施方案中,螢光部分包含多個螢光分子,例如,約2至10,2至8,2至6,2至4,3至10,3至8或3至6個螢光分子。在一些實施方案中,標記包含約2至4個螢光分子。在一些實施方案中,螢光染料分子包含至少一個取代的吲哚環系統,其中吲哚環的3-碳上的取代基含有化學反應性基團或偶聯物質。在一些實施方案中,螢光分子選自Alexa Fluor 488、Alexa Fluor 532、Alexa Fluor 647、Alexa Fluor 680或Alexa Fluor 700。在一些實施方案中,螢光分子選自Alexa Fluor 488、Alexa Fluor 532、Alexa Fluor 680或Alexa Fluor 700。在一些實施方案中,螢光分子是Alexa Fluor 647分子。在一些實施方案中,結合伴體包括抗體。在一些實施方案中,抗體是單克隆抗體。在其他實施方案中,抗體是多克隆抗體。
在各種不同的實施方案中,用於檢測目標指示劑(例如,Eno1或HbA1c)的結合伴體是抗體或其抗原結合片段。如本文中使用的術語「抗體」是寬泛術語並且以其普通含義來使用,包括,不限於,是指天然產生的抗體以及非天然產生的抗體,包括,例如,單鏈抗體、嵌合、雙功能和人源化抗體,及其抗原結合片段。抗體的「抗原結合片段」是指抗體參與抗原結合的部分。抗原結合位點由重(「H」)和輕(「L」)鏈的N-末端可變(「V」)區的胺基酸殘基形成。將認識到抗體由其產生的表位或分子區域的選擇將決定其特異性,例如,對於分子的各種形式(如果存在)的特異性,或對於總體(例如,全部,或基本上全部的分子)的特異性。
用於生產抗體的方法是良好確定的。本領域技術人員將認識到許多程序可用於抗體的生產,例如,如Antibodies,A Laboratory Manual(抗體,實驗室手冊),Harlow和David Lane編輯,Cold Spring Harbor Laboratory(1988),Cold Spring Harbor,N.Y中描述的。本領域技術人員還理解,模擬抗體的結合片段或Fab片段也可以通過各種程序從遺傳信息製備(Antibody Engineering:A Practical Approach(抗體工程:實踐方法)(Borrebaeck,C.等),1995,Oxford University Press,Oxford;J.Immunol.149,3914-3920(1992))。分子(例如,蛋白質)和標誌物的單克隆和多克隆抗體也可以從商業上購得(R and D Systems,Minneapolis,Minn.;HyTest,HyTest Ltd.,Turku Finland;Abcam Inc.,Cambridge,Mass.,USA,Life Diagnostics,Inc.,West Chester,Pa.,USA;Fitzgerald Industries International,Inc.,Concord,Mass.01742-3049USA;BiosPacific,Emeryville,Calif.)。
在一些實施方案中,抗體是多克隆抗體。在其他實施方案中,抗體是單克隆抗體。
可以通過本領域普通技術人員已知的多種技術中的任何一種來製備抗體(參見,例如,Harlow和Lane,Antibodies:A Laboratory Manual(抗體:實驗室手冊),Cold Spring Harbor Laboratory,1988)。通常,可以通過細胞培養技術來生產抗體,包括如本文中所述的單克隆抗體的產生,或通過抗體基因轉染至合適的細菌或哺乳動物細胞宿主中,以允許產生重組抗體。
可以使用雜交瘤方法,如Kohler和Milstein(Eur.J.Immunol.6:511-519,1976)的技術,及其改進來製備單克隆抗體。這些方法涉及能夠產生具有所需特異性的抗體的永生細胞系的製備。還可以通過重組DNA方法,如美國專利No.4,816,567中所述的那些,來製得單克隆抗體。可以使用常規程序來分離和測序編碼所公開的方法中使用的抗體的DNA。重組抗體、抗體片段和/或其融合體可以在體外或在原核細胞(例如,細菌)或真核細胞(例如,酵母、昆蟲或哺乳動物細胞)中表達,並進一步按照需要使用公知方法來純化。
更特別地,可以通過使用公知技術,如美國專利No.4,196,265(按引用併入本文中)中舉例說明的那些,來容易地製備單克隆抗體(MAb)。通常,這種技術涉及用選定的免疫原組合物(例如,純化或部分純化的表達的蛋白質、多肽或肽)免疫合適的動物。免疫組合物以有效刺激抗體產生細胞的方式來施用。用於產生單克隆抗體(MAb)的方法通常沿著與用於製備多克隆抗體的那些相同的路線開始。齧齒動物,如小鼠和大鼠,是優選的動物,然而,使用兔子、綿羊或青蛙細胞也是可能的。使用大鼠可以提供特定的優勢(Goding,1986,pp.60-61),但優選是小鼠,BALB/c小鼠是最優選的,因為這是最常規使用的並且通常給予較高百分比的穩定融合體。
給動物注射如上所述的抗原。如果需要,抗原可以與載體分子如鑰孔血藍蛋白偶聯。抗原通常與佐劑混合,如弗氏完全或不完全佐劑。用相同抗原的增強注射將以大約兩周間隔進行。免疫後,選擇具有產生抗體潛能的體細胞,尤其是B淋巴細胞(B細胞),用於MAb產生方案中。這些細胞可以獲自活檢的脾、扁桃體或淋巴結,或來自外周血樣品。脾細胞和外周血細胞是優選的,前者是因為它們是處於分裂漿母細胞期中的抗體產生細胞的豐富來源,而後者是因為外周血容易獲得。通常,一組動物進行免疫並去除具有最高抗體滴度的動物的脾,且通過用注射器均質脾來獲得脾淋巴細胞。
然後將來自免疫動物的抗體產生B淋巴細胞與永生化骨髓瘤細胞的細胞融合,通常是與免疫動物相同物種的細胞。適用於雜交瘤產生融合過程的骨髓瘤細胞系優選是非抗體產生的,具有高融合效率和使得其不能夠在只支持所需融合細胞(雜交瘤)生長的特定選擇性培養基中生長的酶缺陷。
然後將選定的雜交瘤連續稀釋,並克隆至單個抗體產生細胞系中,該克隆隨後可以無限繁殖以提供MAb。可以以兩種基本方式來利用細胞系用於MAb生產。可以將雜交瘤的樣品注射(常常是注射入腹膜腔中)到用於提供原始融合的體細胞和骨髓瘤細胞的類型的組織相容性動物中。被注射的動物產生分泌由融合細胞雜合體產生的特異性單克隆抗體的腫瘤。然後可以汲取動物的體液,如血清或腹水,以提供高濃度的MAb。也可以在體外培養單獨的細胞系,其中MAb天然地分泌至培養基中,從其中可以容易地獲得高濃度的MAb。如果需要,通過任一種方式產生的MAb可以使用過濾、離心和各種色譜方法,如HPLC或親和性色譜來進一步純化。
還可以通過在體內繁殖雜交瘤細胞來獲得大量的本發明的單克隆抗體。將細胞克隆注射入與親本細胞組織相容的哺乳動物中,例如,同系小鼠,以引起抗體產生腫瘤的生長。任選地,在注射前,用烴,尤其是油,如姥鮫烷(四甲基十五烷),刺激動物。
根據本發明,可以通過包括用酶(如胃蛋白酶或木瓜蛋白酶)消化和/或通過化學還原切割二硫鍵的方法從按照上述產生的單克隆抗體獲得本發明的單克隆抗體的片段。或者,可以使用自動化肽合成儀來合成本發明包括的單克隆抗體片段。
抗體還可以源自基於胺基酸序列的重組抗體文庫,所述胺基酸序列在計算機(in silico)中設計並由合成產生的多核苷酸編碼。用於設計和獲得計算機產生的序列的方法是本領域已知的(Knappik等,J.Mol.Biol.296:254:57-86,2000;Krebs等,J.Immunol.Methods254:67-84,2001;美國專利No.6,300,064)。
可以使用本領域公知的技術來進行抗體的消化以產生其抗原結合片段。例如,蛋白水解酶木瓜蛋白酶優先切割IgG分子以產生幾個片段,其中兩個(「F(ab)」片段)各自包括共價異二聚物(其包括完整的抗原結合位點)。胃蛋白酶能夠切割IgG分子以提供幾個片段,包括「F(ab』)2」片段,其包括兩個抗原結合位點。「Fv」片段可以通過IgM、IgG或IgA免疫球蛋白分子的優先蛋白水解切割來產生,但更通常使用本領域已知的重組技術來衍生。Fv片段包括非共價VH::VL異二聚體(其包括抗原結合位點),其保留天然抗體分子的許多抗原識別和結合能力(Inbar等,Proc.Natl.Acad.Sci.USA 69:2659-2662(1972);Hochman等,Biochem.15:2706-2710(1976)和Ehrlich等,Biochem.19:4091-4096(1980))。
也可以使用已知技術,如美國專利No.5,885,793中描述的那些,從scFv文庫分離特異性地結合本文中公開的多肽指示劑的抗體片段。
廣泛的表達系統在本領域中可得而用於抗體片段的產生,包括Fab片段、scFv、VL和VH。例如,原核和真核兩者來源的表達系統可以用於抗體片段的大規模生產。特別有利的是允許大量抗體片段分泌至培養基中的表達系統。已經描述了用於抗體片段和抗體融合蛋白的大規模生產的真核表達系統,其基於哺乳動物細胞、昆蟲細胞、植物、轉基因動物和低等真核細胞。例如,可以在酵母發酵系統中實現抗體片段的經濟的、大規模的生產。這些生物體的大規模發酵是本領域公知的並且目前用於幾種重組蛋白的大量生產。
結合本發明方法中使用的多肽生物標誌物的抗體是本領域技術人員公知的並且在一些情況能夠使商業上可購得的或不需要過度實驗即可獲得。
在再其他實施方案中,特別是在其中將寡核苷酸用作結合伴體來檢測和與mRNA生物標誌物或其他基於核酸的生物標誌物雜交的情況中,結合伴體(例如,寡核苷酸)可以包括標記,例如,螢光部分或染料。此外,本發明的任何結合伴體,例如,抗體,也可以用螢光部分來標記。作為本文中使用的術語,「螢光部分」包括一種或多種其總螢光使得在本文中所述的單分子檢測儀中可以檢測所述部分的螢光實體。因此,螢光部分可以包括單個實體(例如,量子點或螢光分子)或多個實體(例如,多個螢光分子)。將認識到作為本文中使用的術語,在「部分」是指一組螢光實體時,例如,多個螢光染料分子,每個單獨實體可以獨立地連接於結合伴體或所述實體可以一起連接,只要實體作為一組提供待檢測的足夠螢光。
通常,所述部分的螢光涉及量子效率和缺乏漂白的組合,足夠使得所述部分在單分子檢測器中高於背景水平而可檢測,具有對於試驗的期望檢測限、準確性和精確性所需要的一致性。例如,在一些實施方案中,螢光部分的螢光使得其允許在本文中所述的儀器中以低於約10,5,4,3,2,1,0.1,0.001,0.00001或0.000001pg/ml的檢測限和低於約20,15,14,13,12,11,10,9,8,7,6,5,4,3,2,1%或更低的變異係數,例如,約10%或更低,檢測和/或定量分子,例如,標誌物。在一些實施方案中,螢光部分的螢光使得其允許在本文中所述的儀器中以低於約5,1,0.5,0.1,0.05,0.01,0.005,0.001pg/ml的檢測限和低於約10%的變異係數檢測和/或定量分子,例如,標誌物。作為本文中使用的那些術語,「檢測限」或LoD,包括可以將樣品鑑定為含有目標物質的分子的最低濃度,例如,第一個非零值。其可以通過零位(zeros)的變化性和標準曲線的斜率來定義。例如,可以通過運行標準曲線,確定標準曲線零值並給該值添加2個標準偏差來確定試驗的檢測限。可以產生等於該值的信號的目標物質的濃度即為「檢測下限」濃度。
此外,所述部分具有與其在所選擇的試驗中的使用一致的特性。在一些實施方案中,所述試驗是免疫分析,其中螢光部分連接於抗體;所述部分必須具有使得其不會與其他抗體或蛋白聚集或不經歷超過與所需的試驗準確性和精確性一致的聚集的特性。在一些實施方案中,優選的螢光部分是具有1)高吸收係數;2)高量子產率;3)高光穩定性(低光漂白);和4)與目標分子(蛋白)的標記的相容性的組合的螢光部分,例如,染料分子,使得其可以使用本發明的分析儀和系統進行分析(例如,沒有引起目標蛋白的沉澱、所述部分已經連接的蛋白的沉澱)。
可以使用任何合適的螢光部分。實例包括,但不限於,Alexa Fluor染料(Molecular Probes,Eugene,Oreg.)。Alexa Fluor公開於美國專利No.6,977,305;6,974,874;6,130,101和6,974,305中,將其全部按引用併入本文中。本發明的一些實施方案利用選自Alexa Fluor 647、Alexa Fluor 488、Alexa Fluor 532、Alexa Fluor 555、Alexa Fluor 610、Alexa Fluor 680、Alexa Fluor 700和Alexa Fluor 750的染料。本發明的一些實施方案利用選自Alexa Fluor 488、Alexa Fluor 532、Alexa Fluor 647、Alexa Fluor 700和Alexa Fluor 750的染料。本發明的一些實施方案利用選自Alexa Fluor 488、Alexa Fluor 532、Alexa Fluor 555、Alexa Fluor 610、Alexa Fluor 680、Alexa Fluor 700和Alexa Fluor 750的染料。本發明的一些實施方案利用Alexa Fluor 647分子,其具有約650至660nm之間的最大吸收和約660至670nm之間的最大發射。單獨或結合其他Alexa Fluor染料來使用Alexa Fluor 647染料。
在一些實施方案中,用於使用本發明的分析儀系統檢測樣品中的指示劑的螢光標記部分是量子點。量子點(QD),也稱為半導體納米晶體或人造原子,是含有100至1,000個之間的任何數目的電子並且範圍為2-10nm的半導體晶體。一些QD可以直徑為10-20nm。QD具有高量子產率,這使得它們對光學應用特別有用。QD是通過形成激子而發螢光(這與傳統螢光團的激發態相似),但具有長達200納秒的長各多的壽命。這種特性提供了具有低光漂白的QD。QD的能量水平可以通過改變QD的大小和形狀以及QD電位的深度來控制。小的激子QD的一種光學特徵是著色,其通過點的大小來決定。點越大,螢光越紅,或更朝向於光譜的紅光端。點約小,螢光越藍或更朝向於其藍光端。決定能量並因此決定螢光顏色的帶隙能量與QD的大小的平方成反比。越大的QD具有更高能量水平,其更緊密地間隔,因此允許QD吸收含有較低能量的光子,即更接近於光譜紅光端的那些。因為點的發射頻率取決於帶隙,有可能以極高精確性控制點的輸出波長。在一些實施方案中,使用單分子分析儀系統檢測的蛋白用QD標記。在一些實施方案中,使用單分子分析儀來檢測用一個QD標記的蛋白,並使用濾波器以允許在不同波長下檢測不同蛋白質。
E.分離的大分子血糖指示劑
1.分離的多肽指示劑
本發明的一個方面涉及分離的指示劑蛋白及其生物活性部分,以及適宜用作免疫原來產生針對指示劑蛋白或其片段的抗體的多肽片段。在一個實施方案中,可以使用標準蛋白質純化技術通過合適的純化方案從細胞或組織源分離天然指示劑蛋白。在另一個實施方案中,通過重組DNA技術產生包含完整指示劑蛋白或其區段的蛋白質或肽。作為重組表達的替代方案,可以使用標準肽合成技術通過化學方式合成這樣的蛋白質或肽。重組蛋白可以被修飾,例如,糖化,以提供用於HbA1c檢測的合適抗原。相似地,血紅蛋白的非糖化片段可以用於產生結合單獨的非糖化血紅蛋白或總血紅蛋白的抗體。
「分離的」或「純化的」蛋白質或其生物活性部分基本上不含來自蛋白質從其衍生的細胞或組織源的細胞物質或其他汙染蛋白質,或在化學合成時,基本上不含化學前體或其他化學物質。語言「基本上不含細胞物質」包括其中蛋白質與該蛋白質從其分離或重組產生的細胞組分分離的蛋白質製備物。因此,基本上不含細胞物質的蛋白質包括具有少於約30%,20%,10或5%(乾重)的異源蛋白質(在本文中也稱為「汙染蛋白質」)的蛋白質製備物。當重組產生蛋白質或其生物活性部分時,還優選基本上不含培養基,即,培養基佔蛋白質製備物的低於約20%,10%或5%體積。當通過化學合成產生蛋白質時,優選基本上不含化學前體或其他化學物質,即,其與參與蛋白質合成的化學前體或其他化學物質分離。因此,這樣的蛋白質製備物具有低於約30%,20%,10%,5%(乾重)的除目標多肽以外的化學前體或化合物。
指示劑蛋白的生物活性部分包括包含與指示劑蛋白的胺基酸序列足夠相同的或源自指示劑蛋白的胺基酸序列的胺基酸序列的多肽,其包括少於全長蛋白質的胺基酸,並且呈現出相應全長蛋白的至少一種活性。通常,生物活性部分包含具有相應全長蛋白的至少一種活性的結構域或基序。指示劑蛋白的生物活性部分可以是例如為長度10,25,50,100或更多個胺基酸的多肽。此外,其中標誌物蛋白的其他區域被刪除的其他生物活性部分可以通過重組技術來製備,並且針對天然形式的指示劑蛋白的一種或多種功能活性進行評價。
優選的指示劑蛋白由序列表中提供的核苷酸序列來編碼。其他有用的蛋白與這些序列之一基本上相同(例如,至少約40%,優選50%,60%,70%,80%,90%,91%,92%,93%,94%,95%,96%,97%,98%或99%)並且保留相應的天然產生指示劑蛋白的功能活性,但由於天然等位基因變異或誘變,胺基酸序列不同。
為了測定兩個胺基酸序列或兩個核酸的百分同一性,序列為了最佳比較目的進行比對(例如,為了與第二胺基酸或核酸序列最佳比對,可以在第一胺基酸或核酸序列中引入空位)。然後比較相應胺基酸位置或核苷酸位置處的胺基酸殘基或核苷酸。在第一序列中的位置被與第二序列中相應位置處相同的胺基酸殘基核苷酸佔據時,那麼分子在該位置處是相同的。優選地,使用全局比對來計算兩個序列之間的百分同一性。或者,使用局部比對來計算兩個序列之間的百分同一性。兩個序列之間的百分同一性是序列共有的相同位置數的函數(即,%同一性=相同位置#/總位置#(例如,重疊位置)×100)。在一個實施方案中,兩個序列是相同長度的。在另一個實施方案中,兩個序列是不同長度的。
可以使用數學算法來完成兩個序列之間百分同一性的測定。用於兩個序列比較的數學算法的優選的、非限制性實例是Karlin和Altschul(1990)Proc.Natl.Acad.Sci.USA 87:2264-2268的算法,如Karlin和Altschul(1993)Proc.Natl.Acad.Sci.USA 90:5873-5877中改進的。將這樣的算法結合至Altschul等,(1990)J.Mol.Biol.215:403-410的BLASTN和BLASTX程序中。使用BLASTN程序進行BLAST核苷酸檢索,評分=100,字長=12,以獲得與本發明的核酸分子同源的核苷酸序列。可以使用BALSTP進行BLAST蛋白質檢索,評分=50,字長=3,以獲得與本發明的蛋白質分子同源的胺基酸序列。為了獲得用於比較目的的空位比對,可以按照Altschul等,(1997)Nucleic Acids Res.25:3389-3402中所述的,利用稱為空位BLAST的BLAST算法的較新版本,其能夠進行用於程序BLASTN,BLASTP和BLASTX的空位局部比對。或者,可以使用PSI-Blast來進行迭代檢索,其檢測分子之間的距離關係。利用BLAST、空位BLAST和PSI-Blast程序時,可以使用相應程序(例如,BLASTX和BLASTN)的預設參數。參見http://www.ncbi.nlm.nih.gov。用於序列比較的數學算法的另一種優選的非限制性實例是Myers和Miller(1988)CABIOS 4:11-17的算法。將這樣的算法結合至ALIGN程序(版本2.0)中,其是GCG序列比對軟體包的部分。當利用ALIGN程序比較胺基酸序列時,可以使用PAM120加權殘差表,12的空位長度罰分和4的空位罰分。用於鑑定局部序列相似性的區域和比對的再另一個有用的算法是FASTA算法,如Pearson和Lipman(1988)Proc.Natl.Acad.Sci.USA 85:2444-2448中所述的。當使用FASTA算法比較核苷酸或胺基酸序列時,例如,PAM120加權殘差表可以與2的k-tuple值一起使用。
可以使用與上述那些相似的技術來測定兩個序列之間的百分同一性,具有或不具有允許的空位。在計算百分同一性時,只對精確匹配計數。
本發明的另一個方面涉及針對本發明蛋白質的抗體。在優選實施方案中,所述抗體特異性地結合標誌物蛋白或其片段。術語「抗體(antibody)」和「抗體類(antibodies)」在本文中可互換使用,是指免疫球蛋白分子及其包含免疫球蛋白分子的免疫活性部分的片段和衍生物,(即,這樣的部分含有特異性結合抗原(如標誌物蛋白,例如,標誌物蛋白的表位)的抗原結合位點)。特異性地結合本發明蛋白質的抗體是結合蛋白但基本上不結合天然地含有該蛋白質的樣品(例如,生物樣品)中的其他分子的抗體。免疫球蛋白分子的免疫活性部分的實例包括,但不限於,單鏈抗體(scAb)、F(ab)和F(ab』)2片段。
本發明的分離蛋白質或其片段可以用作免疫原來產生抗體。可以使用全長蛋白,或可選地,本發明提供用作免疫原的抗原性肽片段。本發明蛋白質的抗原性肽包含本發明蛋白質之一的胺基酸序列的至少8個(優選10、15、20或30或更多個)胺基酸殘基,並且包括該蛋白質的至少一個表位,使得針對該肽產生的抗體與蛋白質形成特異性的免疫複合物。在特定實施方案中,蛋白質是翻譯後修飾的。抗原性肽包括的優選表位是位於蛋白質表面上的區域,例如,親水性區域。疏水性序列分析、親水性序列分析或相似分析可以用於鑑定親水性區域。在優選實施方案中,將分離的標誌物蛋白或其片段用作免疫原。
本發明提供了多克隆和單克隆抗體。如本文中使用的,術語「單克隆抗體組合物」或「多克隆抗體組合物」是指只含有能夠與特定表位免疫反應的一個種類的抗原結合位點的抗體分子群。優選的多克隆和單克隆抗體組合物是針對本發明蛋白質的抗體已經選擇的那些組合物。特別優選的多克隆和單克隆抗體製備物是只含有針對標誌物蛋白或其片段的抗體的製備物。製備多克隆、單克隆以及重組抗體和抗體片段的方法是本領域公知的。
2.分離的核酸指示劑
本發明的一個方面涉及分離的核酸分子,包括編碼Eno1或其一部分的核酸。本發明的分離的核酸還包括足以用作雜交探針來鑑定Eno1核酸分子及其片段的核酸分子,例如,適宜用作PCR引物用於標誌物核酸分子的特定產物或突變的擴增的那些。如本文中使用的,術語「核酸分子」打算包括DNA分子(例如,cDNA或基因組DNA)和RNA分子(例如,mRNA)以及使用核苷酸類似物產生的DNA或RNA的類似物。核酸分子可以是單鏈或雙鏈的,但優選是雙鏈DNA。
「分離的」核酸分子是與存在於核酸分子的天然來源中的其他核酸分子分離的核酸分子。在一個實施方案中,「分離的」核酸分子(優選蛋白編碼序列)是不含在所述核酸來源的生物體基因組DNA中天然側鄰該核酸的序列(即,位於該核酸5』和3』端的序列)。例如,在各種不同的實施方案中,分離的核酸分子可以含有少於約5kb、4kb、3kb、2kb、1kb、0.5kb或0.1kb的在所述核酸來源的細胞基因組DNA中天然側鄰該核酸分子的核苷酸序列。在另一個實施方案中,「分離的」核酸分子(如cDNA分子)通過重組技術生產時,可以基本上不含其他細胞物質或培養基,或在化學合成時,基本上不含化學前體或其他化學物質。基本上不含細胞物質的核酸分子包括具有低於約30%、20%、10%或5%的異源核酸(在本文中也稱為「汙染核酸」)的製備物。
可以使用標準分子生物學技術和本文中所述的資料庫記錄中的序列信息來分離本發明的核酸分子。使用這樣的核酸序列的全部或一部分,可以使用標準雜交和克隆技術(例如,如Sambrook等編輯,Molecular Cloning:A Laboratory Manual(分子克隆:實驗室手冊),第2版,Cold Spring Harbor Laboratory Press,Cold Spring Harbor,NY,1989中所述的)來分離本發明的核酸分子。
可以根據標準PCR擴增技術,使用cDNA、mRNA或基因組DNA作為模板和合適的寡核苷酸引物來擴增本發明的核酸分子。可以將由此擴增的核酸克隆至合適的載體中並通過DNA序列分析來表徵。此外,可以通過標準合成技術,例如,使用自動化DNA合成儀,來製備對應於本發明的核酸分子的全部或一部分的核苷酸。
在另一個優選實施方案中,本發明的分離核酸分子包括具有與標誌物核酸的核苷酸序列或與編碼Eno1的核酸的核苷酸序列互補的核苷酸序列的Eno1分子。與給定的核苷酸序列互補的核酸分子是與與給定核苷酸序列充分互補使得其可以與給定的核苷酸序列雜交由此形成穩定的雙鏈體的核酸分子。
此外,本發明的核酸分子可以只包含核酸序列的一部分,其中全長核酸序列包括Eno1核酸或其編碼Eno1蛋白。這樣的核酸可以用作例如探針或引物。探針/引物通常作為一個或多個基本上純化的寡核苷酸使用。寡核苷酸通常包含在嚴格條件下與至少約15個,更優選至少約25,50,75,100,125,150,175,200,250,300,350或400個或更多個Eno1的連續核苷酸雜交的核苷酸序列區域。
基於Eno1序列的探針可以用於檢測對應於Eno1的轉錄物或基因組序列。在特定實施方案中,探針與跨越剪接點的核酸序列雜交。探針包括與其連接的標記基團例如放射性同位素、螢光化合物、酶或酶輔因子。這樣的探針可以用作用於鑑定表達或錯表達Eno1蛋白的細胞、組織或個體的診斷測試試劑盒或試劑組的部分,如通過測量來自受試者的樣品中編碼Eno1的核酸分子的水平,例如,檢測mRNA水平或確定編碼Eno1的基因或其翻譯控制序列是否已經突變或刪除。
本發明進一步包括由於遺傳密碼的簡併性而不同於編碼Eno1蛋白(例如,具有序列表中提供的序列的蛋白質)的核酸的核苷酸序列的核酸分子,並由此編碼相同的蛋白。
本領域技術人員將認識到導致胺基酸序列變化的DNA序列多態性可以存在於群體(例如,人群)內。由於天然的等位基因變異,這樣的遺傳多態性可以存在於群體內的個體之間。等位基因是在給定的基因座處擇一地出現的一組基因之一。此外,將認識到影響RNA表達水平的DNA多態性也可以存在,其可能影響該基因的整體表達水平(例如,通過影響調控或降解)。
如本文中使用的,短語「等位基因變體」是指在給定基因座處存在的核苷酸序列或由核苷酸序列編碼的多肽。
如本文中使用的,術語「基因」和「重組基因」是指包含編碼對應於本發明指示劑的多肽的開放閱讀框的核酸分子。這樣的天然等位基因變異通常可以導致給定基因的核苷酸序列中1-5%的變異度。可以通過將許多不同個體中的目標基因測序來鑑定可選的等位基因。這可以通過使用雜交探針以鑑別多個個體中相同基因座來容易地進行。作為天然等位基因變異的結果並且沒有改變功能活性的任何的所有這樣的核苷酸變異和所得到的胺基酸多態性或變異意圖在本發明的範圍內。
在另一個實施方案中,本發明的分離核酸分子長度為至少15,20,25,30,40,60,80,100,150,200,250,300,350,400,450,550,650,700,800或更多個核苷酸並且在嚴格條件下與Eno1核酸或編碼Eno1的核酸雜交。如本文中使用的,術語「在嚴格條件下雜交」是旨在描述至少60%(65%,70%,優選75%)彼此相同的核苷酸序列通常保持彼此雜交的雜交和洗滌條件。這樣的嚴格條件是本領域技術人員已知的並且可以在Current Protocols in Molecular Biology(分子生物學中的通用實驗方案),John Wiley&Sons,N.Y.(1989)的6.3.1-6.3.6章節中找到。嚴格雜交條件的優選的、非限制性實例是在約45℃下在6×氯化鈉/檸檬酸鈉(SSC)中雜交,接著在50-65℃下在0.2×SSC,0.1%SDS中洗滌一次或多次。
F.指標應用
本發明提供了用於診斷受試者中升高的血糖的方法,例如,前驅糖尿病、2型糖尿病、1型糖尿病、妊娠糖尿病。本發明進一步提供了用於預後或監測血糖升高的受試者的進展或監測血糖升高的受試者對治療性處理的反應的方法。
在一個方面中,本發明構成了結合分析、檢測和/或測量Eno1及至少一種血糖的其他指標(例如,血糖,例如,餐後血糖、空腹血糖、葡萄糖耐量、酮水平)的水平和HbA1c水平通過本發明的方法可獲得的診斷信息的應用。
例如,按照本文中所述的,當進行本發明的用於檢測和/或測量多肽指示劑的方法時,將生物樣品接觸選擇性地結合目標指示劑的檢測試劑,例如,單克隆抗體,從而形成蛋白質-蛋白質複合物,其隨後被直接(如果抗體包括標記)或間接(如果使用第二檢測試劑,例如,第二抗體,其隨之被標記)地進一步檢測。因此,本發明的方法將本發明的多肽指示劑轉化成包括可檢測初級抗體或者初級抗體和進一步第二抗體的蛋白質-蛋白質複合物。為了鑑定目標生物標誌物的存在,需要形成這樣的蛋白質-蛋白質複合物,並且作為進行本發明方法的結果,必定改變目標指示劑的物理特徵和特性。
當進行用於檢測Eno1核酸的本發明方法時,適用同樣的原理。特別地,將擴增方法用於檢測Eno1 mRNA時,擴增方法實際上導致形成新的擴增子群體-即,新合成的並且不存在於初始生物樣品中的分子,由此物理轉化生物樣品。相似地,當使用雜交探針來檢測Eno1時,實際上通過探針(任選包括標記)與靶生物標誌物mRNA(或其他核酸)雜交形成了物理上新的分子物質,其隨後檢測。作為進行本發明方法的結果,有效地新產生或形成了這樣的多核苷酸產物。
在一個實施方案中,本發明提供了用於診斷升高的血糖的方法,例如,前驅糖尿病、糖尿病(例如,2型糖尿病、1型糖尿病、妊娠糖尿病)。本發明的方法可以結合本領域技術人員用來預後血糖升高的發生或復發和/或對待治療血糖升高的受試者的治療幹預的反應的任何其他方法來進行。本文中提供的診斷和預後方法可以用來確定是否應當對受試者進行其他和/或更多的複雜或麻煩的測試或監測(例如,葡萄糖耐量測試、持續的葡萄糖監測)。將理解很少能使用單一測試來診斷如前驅糖尿病或糖尿病這樣複雜的疾病。因此,將理解本文中提供的診斷、預後和監測方法通常結合本領域已知的其他方法來進行。例如,本發明提供的用於檢測Eno1水平的方法可以結合Hb1Ac水平的檢測、空腹或餐後條件下的血糖水平的檢測或葡萄糖耐量測試來進行。
還提供了用於評價治療方案(例如,藥物治療、行為矯正、外科手術或用於治療受試者的升高血糖的任何其他治療途徑)的功效的方法。在這些方法中,評價了一對樣品(較早時間點或治療方案之前從受試者獲得的第一樣品和較後時間點(例如,受試者已經經歷至少一部分治療方案時的較後時間點)從受試者獲得的第二樣品)中的Eno1量。將理解本發明的方法包括以規律或不規律的間隔獲得和分析超過兩個樣品(例如,3,4,5,6,7,8,9或更多個樣品)用於評價標誌物水平。可以在連續或非連續受試者樣品之間進行成對比較。可以針對任何兩個或更多個連續或非連續受試者樣品分析標誌物水平的趨勢和標誌物水平的變化率。可以結合用於檢測血糖監控的其他方法來進行Eno1水平的測量。
本發明的方法還可以用於選擇能夠通過Eno1表達或活性的調節來調節血糖的化合物。在這種方法中,將細胞,優選具有改變的胰島素敏感性或改變的葡萄糖攝取的細胞,接觸測試化合物,並且測定測試化合物調節細胞中的Eno1表達和/或活性的能力,由此選擇能夠調節Eno1表達或活性(優選提高Eno1表達或活性,由此提高細胞中的葡萄糖攝取)的化合物。
使用本文中所述的方法,可以篩選多種分子以鑑別調節(優選提高)Eno1的表達和/或活性的分子。可以將由此鑑別的化合物提供給受試者以通過提高血糖攝取、提高胰島素敏感性和/或降低胰島素抵抗中的一種或多種使血糖標準化,由此治療升高的血糖,例如,前驅糖尿病或糖尿病,例如,2型糖尿病、1型糖尿病或妊娠糖尿病。
本發明涉及預測醫學的領域,其中將診斷分析、預後分析、藥物基因組學和監控臨床試驗用於預後(預測)目的,以由此預防性地治療個體。因此,本發明的一個方面涉及用於測定Eno1蛋白或核酸表達水平的診斷分析,以確定個體是否處於產生與血糖升高相關的疾病或失調的風險中,所述疾病或失調如,不限於,前驅糖尿病或糖尿病,包括2型糖尿病、1型糖尿病或妊娠糖尿病。這樣的分析可以用於預後或預測目的,以由此在失調發作之前預防性地治療個體。
本發明的再另一個方面涉及監控臨床試驗中試劑(例如,藥物或其他治療化合物)或行為和/或膳食改變對Eno1的表達或活性的影響。在以下部分中將進一步詳細地描述這些和其他應用。
1.診斷分析
用於檢測生物樣品中指示劑蛋白質或核酸的存在或不存在或變化的示例性方法包括從測試受試者獲得生物樣品(例如,血液或血清)並將生物樣品接觸能夠檢測多肽或核酸(例如,mRNA或cDNA)的化合物或試劑。因此本發明的檢測方法可以在體外以及在體內檢測例如生物樣品中的mRNA、cDNA或蛋白質,包括翻譯後修飾的蛋白質。
本文中提供的用於檢測生物樣品中的指示劑蛋白或核酸的存在、不存在、水平變化的方法包括從受試者獲得可能含有或不含待檢測標誌物蛋白或核酸的生物樣品,將樣品接觸能夠與待檢測的指示劑蛋白或核酸形成複合物的指示劑特異性的結合劑(例如,一種或多種標誌物特異性的結合劑),並且將樣品接觸用於檢測指示劑-指示劑特異性結合劑複合物(如果形成)的檢測試劑。將理解本文中提供的用於檢測生物樣品中的指示劑水平的方法包括進行所述分析的步驟。在檢測方法的特定實施方案中,樣品中的指示劑蛋白或核酸的水平為零或低於檢測閾值。
所述方法包括指示劑和指示劑特異性結合劑之間瞬時或穩定複合物的形成。所述方法需要複合物(如果形成)形成足夠的時間以允許檢測試劑與複合物結合併產生可檢測信號(例如,螢光信號、來自酶促反應的產物的信號,例如,過氧化物酶反應、磷酸酶反應、β-半乳糖苷酶反應或聚合酶反應)。
在特定實施方案中,使用相同方法檢測全部指示劑。在特定實施方案中,使用相同生物樣品(例如,相同體液)檢測全部指示劑。在特定實施方案中,使用不同方法檢測不同指示劑。在特定實施方案中,在不同生物樣品(例如,血液和血清)中檢測指示劑。
2.蛋白質檢測
在本發明的特定實施方案中,待檢測的指示劑是蛋白質。在特定實施方案中,待檢測的指示劑是翻譯後修飾的蛋白質。使用多種分析來檢測蛋白質,其中待檢測的指示劑蛋白和指示劑特異性結合劑之間的複合物不是天然存在的,例如,因為組分之一不是天然存在的化合物或者用於檢測的指示劑和指示劑特異性結合劑不是來自相同的生物體(例如,使用來自小鼠、大鼠或山羊的指示劑特異性結合抗體來檢測人指示劑蛋白)。在本發明的優選實施方案中,用於檢測的指示劑是人指示劑蛋白。在某些檢測分析中,用於檢測的人指示劑被指示劑特異性的非人抗體結合,因此,複合物在自然界中不會形成。指示劑蛋白的複合物可以直接檢測,例如,通過使用直接結合指示劑的經標記的指示劑特異性抗體,或者通過將進一步的組分結合指示劑-指示劑特異性抗體複合物來檢測。在特定實施方案中,進一步的組分是能夠在與第一指示劑特異性抗體同時結合指示劑的第二指示劑特異性抗體。在特定實施方案中,進一步的組分是結合指示劑特異性抗體的第二抗體,其中第二抗體優選連接可檢測標記(例如,螢光標記、酶標記、生物素)。在第二抗體連接於酶學可檢測標記(例如,過氧化物酶、磷酸酶、β-半乳糖苷酶)時,通過將酶學可檢測標記接觸合適的底物以產生比色、螢光或其他可檢測的(優選可定量檢測的)產物來檢測第二抗體。用於本發明的方法中的抗體可以是多克隆的,然而,在優選實施方案中,使用單克隆抗體。完整抗體或其片段或衍生物(例如,Fab或F(ab』)2)可以用於本發明的方法中。指示劑蛋白的這類檢測策略可以用於例如ELISA、RIA、western印跡和免疫螢光分析方法中。
在特定檢測分析中,在用於檢測的生物樣品中存在的指示劑是酶,例如,Eno1,並且檢測試劑是酶底物(例如,2-磷酸甘油酸(2-PG)或磷酸烯醇丙酮酸(PEP),或產生可檢測產物的任一化合物的類似物)。在優選實施方案中,與待檢測的指示劑酶形成複合物的底物不是人受試者中的酶的底物。
在特定實施方案中,將指示劑-指示劑特異性結合劑複合物連接於固體支持物用於指示劑的檢測。複合物可以在基質上形成或在捕獲於基質上之前形成。例如,在ELISA、RIA、免疫沉澱分析、western印跡、免疫螢光分析、凝膠酶學分析中,將用於檢測的指示劑直接或間接地連接於固體支持物。在ELISA、RIA或免疫螢光分析中,指示劑通常通過抗體或結合蛋白間接連接於固體支持物。在western印跡或免疫螢光分析中,指示劑通常直接連接於固體支持物。對於凝膠酶學分析,指示劑溶解於凝膠中,通常是丙烯醯胺凝膠,其中摻入了酶的底物。
3.核酸檢測
在本發明的特定實施方案中,指示劑是核酸,例如,Eno1核酸。使用多種分析來檢測核酸,其中待檢測的指示劑核酸和指示劑特異性探針之間的複合物不是天然存在的,例如,因為組分之一不是天然存在的化合物。在特定實施方案中,分析物包括核酸,而探針包括一個或多個合成的單鏈核酸分子,例如,DNA分子、DNA-RNA雜合體、PNA或含有一個或多個人造鹼基、糖或主鏈部分的修飾核酸分子。在特定實施方案中,合成的核酸是單鏈的,是包括螢光標記的DNA分子。在特定實施方案中,合成的核酸是約12至約50個核苷酸長的單鏈寡核苷酸分子。在特定實施方案中,待檢測核酸是mRNA,並且形成的複合物是與單鏈DNA分子雜交的mRNA,所述單鏈DNA分子與mRNA互補。在特定實施方案中,通過使用作為引物與RNA雜交的單鏈DNA首先從RNA模板產生DNA分子(即,cDNA分子)來檢測RNA,所述引物例如通用多聚-T引物以轉錄多聚A RNA。然後可以使用標誌物特異性的探針,將cDNA用作用於擴增反應的模板,例如,PCR、引物延伸試驗。在特定實施方案中,標記的單鏈DNA可以與樣品中存在的RNA雜交用於通過原位螢光雜交(FISH)的RNA檢測或用於通過northern印跡的RNA檢測。
例如,用於mRNA檢測的體外技術包括northern雜交、原位雜交和rtPCR。用於檢測基因組DNA的體外技術包括Southern雜交。用於mRNA檢測的技術包括PCR、northern雜交和原位雜交。方法包括定性和定量方法。
這樣的診斷、預後和監測分析的一般原理涉及製備可能含有用於檢測的核酸和探針的樣品或反應混合物,其在合適的條件下和足以允許指示劑核酸和探針相互作用並結合的時間,由此形成可以在反應混合物中取出和/或檢測的複合物。這些分析可以以本領域已知的多種方式來進行,例如,PCR、FISH、northern印跡。
4.表達水平的檢測
可以基於絕對表達水平或者標準化的或相對表達水平來檢測Eno1水平。在監控受試者治療或確定受試者中血糖水平或血糖調節是否存在變化時,絕對Eno1水平的檢測可能是優選的。例如,可以監測正接受異常血糖治療的受試者的Enol的表達水平,例如,以規律的間隔來監測,如每月間隔。可以隨著時間監測Eno1水平的調節以觀察Eno1水平的變化趨勢。受試者中Eno1的表達水平可能高於正常樣品中的Eno1表達水平,但也可能高於之前的表達水平,因此表明治療方案對於受試者的益處。相似地,Eno1水平的變化率在用行為或膳食矯正而不是治療性幹預治療的受試者中可能是重要的。個體受試者中Eno1水平的變化或無變化與群體中存在的Eno1水平相比,可能與針對受試者的治療決策更相關。另外顯示出具有正常血糖的受試者中Eno1水平的快速變化可能指示異常血糖或具有產生與異常血糖相關的病症的傾向,即使標誌物在該群體的正常範圍內。可以結合一種或多種血糖升高的其他指示劑,例如,HbA1c,提高的血糖(包括提高的餐後或空腹血糖中的一種或多種)或葡萄糖耐量測試中降低的葡萄糖清除率,來測定或監測Eno1水平。
作為基於Eno1的絕對表達水平做出決定的替代方案,表達水平可以基於Eno1的標準化表達水平來決定。通過將指示劑的絕對表達水平與不是指示劑的基因(例如,組成型表達的管家基因)的表達進行比較來標準化。用於標準化的合適基因包括管家基因如肌動蛋白基因,以及用於血液或血清中的標準化的合適蛋白質包括白蛋白。這種標準化允許一個樣品(例如,來自血糖正常受試者的樣品)中的表達水平與另一個樣品(例如,來自懷疑具有或具有異常血糖的樣品)的比較,或來自不同來源的樣品之間的比較。
或者,表達水平可以作為與合適的對照(例如,群體對照、較早時間點對照等)比較的相對表達水平來提供。優選地,基線測定中使用的樣品將來自正常血糖的受試者的樣品。細胞來源的選擇取決於相對表達水平的使用。此外,隨著更多數據累積,可以修正平均表達值,從而基於累積的數據提供改進的相對表達值。
5.監測臨床試驗
監測藥劑(例如,藥物化合物)對血糖指示劑水平的影響不僅可以應用於基礎藥物篩選或監測單一受試者的治療中,而且也可以應用於臨床試驗中。例如,可以在接受針對血糖升高的治療的受試者的臨床試驗中監測藥劑影響Eno1表達的有效性。在優選實施方案中,本發明提供了監測使用藥劑(例如,激動劑、拮抗劑、肽模擬物、蛋白質、肽、核酸、小分子或其他藥物候選物)治療受試者的有效性的方法,包括步驟(i)在施用藥劑前,從受試者獲得施用前樣品;(ii)檢測施用前樣品中的指示劑Eno1的表達水平和任選一種或多種其他的血糖指示劑(例如,血糖、酮或HbA1c);(iii)從受試者獲得一個或多個施用後樣品;(iv)檢測施用後樣品中的指示劑的表達水平;(v)將施用前樣品中的指示劑水平與一個或多個施用後樣品中的指示劑水平進行比較;和(vi)因此改變對受試者的藥劑施用。例如,在治療過程中降低的Eno1表達和缺少其他指示劑的正常化可以表明無效的劑量並希望提高劑量。相反,提高的Eno1表達和其他指示劑的正常化可以表明有效的治療並且不需要改變劑量。
VI.受損的血糖水平、受損的血糖水平控制和糖尿病的治療
如本文中證明的,Eno1蛋白的施用提高了葡萄糖攝取和反應,從而使血糖水平和血糖水平的控制正常化。本發明提供了通過將Eno1施用於受試者來改善病症的至少一個體徵或症狀治療患有受損的葡萄糖耐量、提高的血糖、胰島素抵抗、胰島素不足和糖尿病(例如,2型糖尿病、1型糖尿病、前驅糖尿病和妊娠糖尿病)的受試者的方法。在特定實施方案中,Eno1,優選Eno1的轉錄物變體1,可以施用於受試者,其中將用於治療受損的葡萄糖耐量、提高的血糖、胰島素抵抗、胰島素不足或糖尿病的至少一種其他藥劑施用於受試者。如本文中使用的,藥劑可以以任何順序按序施用或同時施用。多種藥劑施用於受試者不需要藥劑的共同配製或相同的給藥方案。
使用Eno1治療受損的葡萄糖耐量、提高的血糖、胰島素抵抗、胰島素不足或糖尿病(尤其是2型糖尿病)的方法可以結合用於糖尿病治療的已知方法和藥劑。許多藥劑和方案目前可用於糖尿病的治療。選擇用於治療的特定藥劑取決於受試者、特定的症狀和病況的嚴重性。例如,在特定實施方案中,Eno1可以結合膳食和/或行為矯正(例如,熱量限制)來施用(單獨地或結合減肥手術和/或增加的身體活動)。在特定實施方案中,Eno1可以與用於治療2型糖尿病的藥劑一起施用,例如,二甲雙胍(Glucophage、Glumetza、其他)、格列酮類,例如,匹格列酮(Actos)、格列吡嗪(Glucotrol)、格列本脲(Diabeta、Glynase)、格列美脲(Amaryl)、阿卡波糖(Precose)、二甲雙胍(Glucophage)、西格列汀(Januvia)、沙格列汀(Onglyza)、瑞格列奈(Prandin)、那格列奈(Starlix)、艾塞那肽(Byetta)、利拉魯肽(Victoza)或胰島素。胰島素通常只用於晚期2型糖尿病的治療中,並且包括速效胰島素(門冬胰島素(NovoLog)、賴谷胰島素(Apidra)和賴脯胰島素(Humalog));短效胰島素(常規胰島素(Humulin R,Novolin R));中效胰島素(胰島素NPH人(Humanlin N,Novolin N))和長效胰島素(甘精胰島素(Lantus)和地特胰島素(Levemir))。用於糖尿病的治療還可以包括行為矯正,包括鍛鍊和減重,其可以通過使用藥物或外科手術來促進。可以結合用於升高的血糖和糖尿病的治療。例如,藥物治療可以結合行為矯正治療。用於1型糖尿病治療中的胰島素包括,但不限於,通常僅用於後期2型糖尿病治療中的胰島素,並且包括速效胰島素(門冬胰島素(NovoLog)、賴谷胰島素(Apidra)和賴脯胰島素(Humalog));短效胰島素(常規胰島素(Humulin R,Novolin R));中效胰島素(胰島素NPH人(Humanlin N,Novolin N))和長效胰島素(甘精胰島素(Lantus)和地特胰島素(Levemir))。
因此,在一些方面中,本發明涉及治療受試者的升高的血糖的方法,包括:(a)從懷疑具有升高血糖的受試者獲得生物樣品,(b)提交生物樣品以獲得關於Eno1水平的診斷信息,和(c)當樣品中的Eno1水平高於閾值水平時,將治療有效量的抗糖尿病治療施用於受試者。
在一些方面中,本發明涉及治療受試者的升高的血糖的方法,包括:(a)獲得關於來自受試者的生物樣品中的Eno1水平的診斷信息,和(b)在樣品中的Eno1水平高於閾值水平時,將治療有效量的抗糖尿病治療施用於受試者。
在一些方面中,本發明涉及治療受試者的升高的血糖的方法,包括:(a)從懷疑具有升高血糖的受試者獲得生物樣品用於鑑定關於Eno1水平的診斷信息,(b)檢測生物樣品中的Eno1的水平,(c)在樣品中的Eno1水平低於閾值水平時,向健康護理提供者推薦血糖降低治療以施用於受試者。
上述的方法可以進一步包括獲得關於升高血糖的一種或多種其他指示劑水平的診斷信息。在一些實施方案中,所述方法進一步包括測量升高血糖的一種或多種其他指示劑的水平。升高血糖的一種或多種其他指示劑可以選自HbA1c水平、空腹血糖水平、餐後血糖水平和葡萄糖耐量。
在上述方法的一些實施方案中,如果樣品中的Eno1水平低於閾值水平並且檢測到升高血糖的至少一種其他指標,步驟(c)進一步包括將治療有效量的葡萄糖降低治療施用於受試者。在一些實施方案中,如果樣品中的Eno1水平低於閾值水平並且檢測到升高血糖的至少一種其他指標,步驟(c)進一步包括對健康護理提供者推薦葡萄糖降低治療以施用於受試者。
在上述方法的一些實施方案中,生物樣品是血液或血清。在一些實施方案中,通過免疫分析或ELISA來測定Eno1的水平。在一些實施方案中,Eno1的水平通過(i)將生物樣品接觸選擇性地結合Eno1的試劑以形成生物標誌物複合物,和(ii)檢測生物標誌物複合物來測定。在一些實施方案中,選擇性地結合Eno1以形成生物標誌物複合物的試劑是選擇性地結合Eno1的至少一個表位的抗Eno1抗體。
在上述方法的一些實施方案中,通過測量生物樣品中的Eno1mRNA的量來檢測Eno1的水平。例如,可以通過擴增反應來檢測Eno1 mRNA的量。在一些實施方案中,擴增反應是(a)聚合酶鏈式反應(PCR);(b)基於核酸序列的擴增試驗(NASBA);(c)轉錄介導的擴增(TMA);(d)連接酶鏈式反應(LCR);或(e)鏈置換擴增(SDA)。
在一些實施方案中,將雜交分析用於檢測生物樣品中的Eno1mRNA的量。在一些實施方案中,將與Eno1 mRNA的一部分互補的寡核苷酸用於雜交試驗中來檢測Eno1 mRNA。
VI.糖尿病和胰島素抵抗的動物模型
本領域中充分表徵了代謝症狀(如1型糖尿病和2型糖尿病、胰島素抵抗、高脂血症)的多種遺傳和誘導的動物模型。這樣的動物可以用於證明Eno1在胰島素抵抗和糖尿病治療中的作用。1型糖尿病的模型包括,但不限於,NOD小鼠以及大鼠和小鼠中鏈脲黴素誘導的糖尿病(1型糖尿病模型)。2型糖尿病的遺傳和誘導模型包括,但不限於,瘦素缺陷ob/ob小鼠,瘦素受體缺陷db/db小鼠和高脂飲食小鼠或大鼠模型。在每種模型中,產生特定疾病特徵的時間線是公知的。可以在糖尿病或胰島素抵抗症狀出現之前或之後施用Eno1,以證明Eno1在這些動物模型中預防或治療糖尿病和/或胰島素抵抗中的功效。
根據選擇的特定動物模型和幹預時間,例如,在糖尿病和/或胰島素抵抗出現之前或之後,動物模型可以用於證明本文中提供的方法用於預防、治療、診斷和監控糖尿病和/或胰島素抵抗的功效。
VII.藥物篩選
Eno1的施用導致具有誘導的糖尿病的動物中血糖的正常化,使得Eno1成為用於通過篩選來檢測增強Eno1表達的化合物或實體而鑑定新治療劑的有吸引力的靶標。因此,本發明提供了用於鑑定對於調節血糖和糖尿病潛在有用的化合物的方法。特別地,本發明提供了用於鑑定對於調節Eno1潛在有用的化合物的方法,其中所述化合物調節血糖和糖尿病。
這樣的分析通常包括Eno1和一種或多種分析組分(例如,測試化合物)之間的反應。其他組分可以是測試化合物自身,或測試化合物和Eno1的天然結合伴體的組合。通過如本文中所述那些分析鑑定的化合物例如對於調節(例如,抑制、緩解、治療或預防)疾病是有用的。針對調節Eno1的表達水平鑑定的化合物優選進一步針對在異常血糖和/或糖尿病治療中有用的活性(例如,使餐後和/或空腹血糖正常化、在葡萄糖耐量測試中使葡萄糖清除和/或胰島素水平正常化、使HbA1c水平正常化)進行測試。
本發明的篩選分析中使用的測試化合物可以獲自任何可用的來源,包括天然和/或合成化合物的系統文庫。還可以通過本領域已知的組合文庫方法中的多種途徑中的任何一種來獲得測試化合物,所述文庫包括:生物學文庫;類肽文庫(具有肽的功能性但具有抵抗酶降解的新的、非肽主鏈的分子的文庫,但所述分子仍然保留生物學活性;參見,例如,Zuchermann等,1994,J.Med.Chem.37:2678-85);空間尋址的平行固相或液相文庫;需要去卷積的合成文庫方法;『一珠一化合物』文庫方法;和使用親和性色譜選擇的合成文庫方法。生物學文庫和類肽文庫途徑限於肽文庫,而其他四種途徑適用於肽、非肽寡聚物或化合物的小分子文庫(Lam,1997,Anticancer Drug Des.12:145)。
用於分子文庫合成的方法的實例可以在現有技術中找到,例如,在:DeWitt等,(1993)Proc.Natl.Acad.Sci.U.S.A.90:6909;Erb等,(1994)Proc.Natl.Acad.Sci.USA 91:11422;Zuckermann等,(1994).J.Med.Chem.37:2678;Cho等,(1993)Science 261:1303;Carrell等,(1994)Angew.Chem.Int.Ed.Engl.33:2059;Carell等,(1994)Angew.Chem.Int.Ed.Engl.33:2061;和Gallop等,(1994)J.Med.Chem.37:1233。
化合物文庫可以存在於溶液中(例如,Houghten,1992,Biotechniques 13:412-421),或者珠子(Lam,1991,Nature 354:82-84)、晶片(Fodor,1993,Nature 364:555-556)、細菌和/或孢子(Ladner,USP 5,223,409)、質粒(Cull等,1992,Proc Natl Acad Sci USA 89:1865-1869)或噬菌體上(Scott和Smith,1990,Science249:386-390;Devlin,1990,Science 249:404-406;Cwirla等,1990,Proc.Natl.Acad.Sci.87:6378-6382;Felici,1991,J.Mol.Biol.222:301-310;Ladner,上文)。
本發明的篩選方法包括將細胞,例如,患病的細胞,尤其是具有異常胰島素反應和/或葡萄糖攝取的細胞,接觸測試化合物並測定測試化合物調節細胞中Eno1的表達和/或活性的能力。可以使用本領域已知的任何方法,如本文中所述的那些,來測定Eno1的表達和/或活性,任選結合血糖水平的檢測方法。
在另一個實施方案中,本發明提供了用於篩選作為Eno1或其生物活性部分的底物的候選物或測試化合物的測試。在再另一個實施方案中,本發明提供了用於篩選結合Eno1或其生物活性部分的候選物或測試化合物的分析。例如,以通過本領域已知的任一種方法來完成測試化合物直接結合Eno1的能力的測定。
本發明進一步涉及通過上述篩選分析鑑定的新藥劑。因此,進一步將按照本文中所述鑑定的藥劑用於合適的動物模型中在本發明的範圍內。例如,能夠調節Eno1的表達和/或活性的藥劑可以用於動物模型中來測定使用這樣的藥劑治療的功效、毒性或副作用。或者,如本文中所述鑑定的藥劑可以用於動物模型中來測定這種藥劑的作用機理。此外,本發明涉及通過上述篩選分析鑑定的新藥劑用於如上所述的治療中的用途。
在特定實施方案中,使用多孔分析平板的多個孔中所含的細胞來進行篩選方法。這樣的分析平板是商業上可購得的,例如,從Stratagene Corp.(La Jolla,Calif.)和Corning Inc.(Acton,Mass.)購得,並且包括例如,48-孔、96-孔、384-孔和1536-孔平板。
通過使用相同濃度的相同候選化合物進行超過一次的分析來測試結果的可重複性(例如,通過在分析平板的超過一個孔中孵育細胞)。另外,由於根據化合物的性質及其作用機理的性質,候選化合物在不同濃度下可能是有效的,因此可以測試候選化合物的不同濃度。通常,將1fM至約10mM的候選化合物濃度用於篩選。優選的篩選濃度通常為約10pM至約100μM。
本發明的篩選方法將提供「命中物(hits)」或「先導物(leads)」,即,具有所需的但不是最佳的生物活性的化合物。對這些化合物進行滿足臨床有用性需要的所有理化、藥代動力學和毒理學因素的先導優化可以提高改進的藥物候選物。本發明還包括這些改進的藥物候選物及其作為用於調節血糖和胰島素反應的治療劑的用途。
VIII.試劑盒/試劑組
本發明還提供了用於診斷、預後或監控疾病或失調、失調的復發或待治療失調(例如,異常血糖和/或糖尿病)的受試者的存活的組合物。這些試劑盒包括以下的一個或多個:特異性地結合Eno1的可檢測抗體,特異性地結合Eno1的可檢測抗體,用於獲得和/或製備用於染色的受試者組織樣品的試劑和使用說明書。
本發明還包括用於檢測生物樣品中的Eno1蛋白或核酸的存在的試劑盒。這樣的試劑盒可以用於確定受試者是否患有異常血糖和/或糖尿病或處於產生異常血糖和/或糖尿病的提高風險中。例如,試劑盒可以包括能夠檢測生物樣品中的Eno1蛋白或核酸的標記化合物或試劑和用於測定樣品中的蛋白或mRNA量的工具(例如,結合蛋白或其片段的抗體,或結合編碼蛋白的DNA或mRNA的寡核苷酸探針)。試劑盒還可以包括試劑盒用於實施本文中提供的任一種方法或基於本文中提供的教導解釋使用試劑盒獲得的結果的使用說明書。試劑盒還可以包括包括用於檢測樣品中與異常血糖不相關的對照蛋白的試劑,例如,組織樣品的肌動蛋白、用於對樣品中存在的Eno1量標準化的血液或血液衍生樣品中的白蛋白。試劑盒還可以包括用於檢測的純化標誌物,用作對照或用於使用試劑盒進行的分析的定量。
試劑盒包括用於方法中以診斷受試者中的異常血糖(或鑑定易於產生異常血糖和/或糖尿病的受試者)的試劑組,所述試劑組包括至少兩種檢測試劑,其包括用於檢測Eno1水平的試劑和用於檢測血糖的另一種指標(例如,HbA1c)的試劑。
對於基於抗體的試劑盒,試劑盒可以包括,例如:(1)結合Eno1的第一抗體(例如,連接於固體支持物);和任選地(2)結合Eno1或第一抗體並與可檢測標記偶聯的不同的第二抗體。在特定實施方案中,試劑盒包括(1)結合第二標誌物蛋白的第二抗體(例如,連接於固體支持物);和任選地(2)結合HbA1c或血紅蛋白(總的或未修飾的血紅蛋白)或結合第二抗體並與可檢測標記偶聯的不同的第二抗體。第一和第二標誌物蛋白是不同的。
對於基於寡核苷酸的試劑盒,試劑盒可以包括,例如:(1)與編碼Eno1的核酸序列雜交的寡核苷酸,例如,可檢測地標記的寡核苷酸,或(2)一對可用於擴增Eno1核酸分子的引物。在特定實施方案中,試劑盒包括對於每種核酸標誌物特異性的第三引物以允許使用定量PCR方法的檢測。在特定實施方案中,試劑盒進一步包括直接或間接(例如,使用HbA1c水平)地測量受試者中的血糖的說明書。
對於色譜方法,試劑盒可以包括標誌物,包括標記的標誌物,以允許通過色譜法檢測和鑑定一種或多種血糖指標,例如,Eno1和HbA1c。在特定實施方案中,用於色譜方法的試劑盒包括用於一種或多種血糖指示劑衍生化的化合物。在特定實施方案中,用於色譜方法的試劑盒包括用於解析所述方法的指示劑的柱。
對於Eno1的檢測特異性的試劑允許檢測和定量複雜混合物(例如,血清、血液)中的標誌物。在特定實施方案中,試劑是物種特異性的。在特定實施方案中,Eno1試劑不是物種特異性的。在特定實施方案中,Eno1試劑是異形體特異性的。在特定實施方案中,Eno1試劑不是異形體特異性的。在特定實施方案中,試劑檢測總Eno1。
在特定實施方案中,用於升高的血糖和/或糖尿病的診斷、監控或表徵的試劑盒包括至少一種對於Eno1表達水平的檢測特異性的試劑。在特定實施方案中,試劑盒進一步包括檢測(直接或間接或兩者)樣品中的血糖水平的說明書。在特定實施方案中,試劑盒包括至少一種用於檢測HbA1c水平的試劑。
在特定實施方案中,試劑盒還可以包括例如緩衝劑、防腐劑、蛋白穩定劑、反應緩衝劑。試劑盒可以進一步包括檢測可檢測標記(例如,酶或底物)所必需的組分。試劑盒還可以含有可以測定並與測試樣品比較的對照樣品或一系列對照樣品。對照可以是對照血清樣品或(適宜的話)純化蛋白或核酸的對照樣品,具有已知水平的指示劑。試劑盒的每種組分可以包裝在單個容器內並且所有的各種不同容器可以在單一包裝內,連同用於解釋使用試劑盒進行的分析的結果的說明書一起。
本發明的試劑盒可以任選地包括可用於進行本發明的方法的其他組分。
例如,在一些方面中,本發明涉及用於檢測生物樣品中的Eno1的試劑盒,其包括至少一種用於測量生物樣品中的Eno1水平的試劑,和用於測量Eno1水平的一套說明。在一些實施方案中,試劑是抗Eno1抗體。在一些實施方案中,試劑盒進一步包括檢測抗Eno1抗體的工具。在一些實施方案中,檢測抗Eno1抗體的工具是可檢測的第二抗體。在一些實施方案中,用於測量Eno1水平的試劑是與Eno1 mRNA互補的寡核苷酸。
在上述試劑盒的一些實施方案中,說明書給出了用於檢測生物樣品中的Eno1水平的免疫分析或ELISA。在一些實施方案中,說明書給出了用於測定生物樣品中的Eno1 mRNA水平的擴增反應。在一些實施方案中,擴增反應用於檢測生物樣品中的Eno1 mRNA的量。在一些實施方案中,擴增反應是(a)聚合酶鏈式反應(PCR);(b)基於核酸序列的擴增分析(NASBA);(c)轉錄介導的擴增(TMA);(d)連接酶鏈式反應(LCR);或(e)鏈置換擴增(SDA)。
在上述試劑盒的一些實施方案中,說明書給出了用於檢測生物樣品中的Eno1 mRNA的量的雜交分析。在一些實施方案中,試劑盒進一步包括至少一個與Eno1 mRNA的一部分互補的寡核苷酸。
本發明進一步提供了用於檢測受試者樣品中的一種或多種血糖指示劑的試劑組和至少一種對照試劑。在特定實施方案中,對照試劑用於檢測生物樣品中的指示劑,其中試劑組提供含有用作陽性對照以及任選用於定量生物樣品中存在的指示劑量的指示劑的對照樣品。在特定實施方案中,試劑組包括用於已知存在或不存在於生物樣品中的與異常血糖不相關的蛋白質或核酸的檢測試劑以分別提供陽性或陰性對照。試劑組可以提供用於檢測樣品中與異常血糖不相關的對照蛋白的試劑,例如,血液或血液衍生樣品中的白蛋白,用於樣品中存在的指示劑量的標準化。試劑組可以提供純化的指示劑,例如,Eno1,用作對照用於檢測或用於使用所述試劑組進行的分析的定量。
在優選實施方案中,試劑組包括用於Eno1檢測的試劑,優選結合對照試劑。在該試劑組中,通過對於該Eno1特異性的試劑來檢測Eno1。在特定實施方案中,試劑組進一步包括用於HbA1c檢測的試劑。在特定實施方案中,試劑組包括重複孔、點或部分以允許各種稀釋度(例如,連續稀釋)的生物樣品和對照樣品的分析。在優選實施方案中,試劑組允許血糖的一種或多種指示劑的定量檢測。
在特定實施方案中,試劑組是用於檢測一種或多種標誌物的蛋白質晶片。在特定實施方案中,試劑組是用於檢測一種或多種標誌物的ELISA平板。在特定實施方案中,套組是用於檢測一種或多種標誌物的定量PCR的平板。
在特定實施方案中,在單一裝置上提供檢測試劑組,包括用於本發明的一種或多種標誌物的檢測試劑和至少一個對照樣品。在特定實施方案中,可以在單一裝置上提供檢測試劑組,包括用於本發明的兩種或更多種標誌物的檢測試劑和至少一個對照樣品。在特定實施方案中,用於檢測本發明的不同標誌物的多個試劑組提供有至少一種統一的對照樣品以有助於試劑組之間的結果比較。
在特定實施方案中,試劑組和試劑盒進一步包括用於測量受試者中的血糖的說明或建議。在特定實施方案中,試劑盒或試劑組提供有一種或多種用於血糖測量的試劑或裝置。
本發明還提供了用於治療至少一種糖尿病的試劑盒,例如,1型糖尿病、2型糖尿病、妊娠糖尿病、前驅糖尿病、胰島素抵抗、葡萄糖不耐性、異常血糖和血糖控制的喪失。試劑盒包括Eno1以及使用說明和(按照需要)用於施用的裝置中的一個或多個。
通過以下實施例來進一步說明本發明,所述實施例不應當解釋為限制。在整個申請中引用的所有參考文獻以及公開專利和專利申請的內容在此按引用併入。
實施例
實施例1-使用平臺技術來鑑定作為糖尿病病因學中的重要活性節點的烯醇酶1(Eno1)
在這個實施例中,使用國際專利申請No.PCT/US2012/027615中詳細描述的平臺技術來整合獲自定製的糖尿病模型的數據和鑑定驅動糖尿病(特別是2型糖尿病)的發病機理的新蛋白質/途徑。從這個分析獲得的關係圖已經鑑定了Eno1作為糖尿病病因學中的重要活性節點。因此,Eno1是重要的糖尿病治療靶標,以及與糖尿病相關的診斷/預後標誌物。
實施例2-肌管中葡萄糖攝取的Eno1調節
使用商業上可購得的表達載體,Eno1在大腸桿菌中作為6X HIS蛋白標籤重組表達。使用本領域已知的親和性色譜方法純化標記的Eno1。優選地,切割6X HIS標籤以產生用於本文中提供的方法中的蛋白質。
人骨骼肌成肌細胞(HSMM)獲自PromoCell並且在零售商推薦的生長培養基中培養。在實驗前,在96孔平板中用2%馬血清將HSMM成肌細胞(20,000細胞/孔)分化7天。用人Eno1(500ug/ml)處理細胞。用200μl含有0.1%BSA的MBSS改良平衡鹽溶液(MBSS)緩衝液洗滌細胞兩次,然後用100ul MBSS 0.1%BSA進行血清飢餓4小時。開始胰島素刺激時,將MBSS 0.1%BSA緩衝液中的100ul 2×試劑加入100ul飢餓培養基中以製得用於實驗的1×濃度。2×試劑為:胰島素(0,20nM和200nM);螢光葡萄糖類似物2-NBDG(500uM)。用胰島素和螢光脫氧-葡萄糖類似物2-NBDG處理細胞30min,然後用MBSS緩衝液洗滌兩次,然後將50ul MBSS緩衝液加入孔中。用螢光計檢測葡萄糖攝取,連同使用其中無細胞的孔的背景檢測。螢光計讀出後,將固定劑(福馬林,50ul)加入孔中的50ul MBSS中,然後將100ul 1Um DAPI加入100ul福馬林和MBSS混合物中。
如圖1A和1B中所示,用Eno1處理肌管顯著提高了不存在和存在胰島素的情況下的葡萄糖攝取(p=0.025非胰島素依賴性葡萄糖攝取,未處理的vs.Enol處理的)。這些結果證明了Eno1在胰島素依賴性和非胰島素依賴性葡萄糖攝取中的作用。由Eno1誘導的胰島素依賴性葡萄糖攝取證明了Eno1在受試者中對於胰島素敏感的至少骨骼肌中與胰島素信號傳導途徑複雜地關聯。結果還證明了Eno1在非胰島素依賴性葡萄糖攝取中的作用。這種觀察對於1型和2型糖尿病受試者的治療是重要的,所述受試者患有胰島素抵抗且還具有高胰島素血症,使得胰島素作用受損並且因此是非胰島素依賴性的。這些結果證明Eno1在刺激葡萄糖攝取中是有用的,即使在不再具有正常胰島素信號傳導的個體中。
用上述純化Eno1蛋白處理人骨骼肌肌管的細胞培養物48小時以測量Eno1攝取。然後通過Western印跡測定細胞中的Eno1水平。如圖2A和2B中所示,用500μg/ml Eno1或1000μg/ml Eno1處理的細胞中的Eno1水平相對於未處理細胞具有顯著較高的Eno1水平。用1000μg/ml Eno1處理的細胞中的Eno1水平也高於用500μg/ml Eno1處理的細胞中的水平。這些結果表明Eno1以劑量依賴性的方式遞送至人骨骼肌肌管中。
為了測定Eno1酶活性在葡萄糖攝取中的作用,通過在88℃下處理90秒來熱滅活純化的Eno1,並且比較原始的和熱滅活的Eno1的活性水平。使用來自Abcam(Cambridge,MA;Cat.No.ab117994)的Eno1人活性分析試劑盒通過比色分析測定Eno1活性。如圖3A中所示,熱滅活極大地降低了Eno1酶活性,但保留了一些殘留活性。
按照上述方法,在人骨骼肌肌管中比較了原始和熱滅活的Eno1對葡萄糖攝取的作用。如圖3B中所示,相對於未用Eno1處理的肌管,用原始(活性)Eno1處理的肌管呈現出顯著較高的葡萄糖攝取。與用活性Eno1處理的肌管相比,用熱滅活的Eno1處理的肌管呈現出顯著較低的葡萄糖攝取。這些結果表明Eno1對葡萄糖攝取的作用依賴於Eno1酶活性。熱滅活的Eno1相對於不含Eno1的對照觀察到的葡萄糖攝取的提高很可能是由於熱滅活酶的殘留Eno1活性。
實施例3-膳食誘導肥胖(DIO)小鼠的小鼠模型
將兩個基本上等同的膳食誘導肥胖症模型用於本文中提供的方法中。
在第一種方法中,雄性C57BL/6J小鼠獲自Jackson實驗室(Bar Harbor,ME)並且最初4-5隻/籠圈養在22℃下,使用12:12hr白天-黑夜循環。在6周齡開始,給小鼠飼餵高脂肪膳食(Research Diets Cat#:D12492;60kcal%脂肪、20kcal%蛋白和20kcal%碳水化合物)。還獲得了瘦的對照小鼠並飼餵標準膳食。實驗前DIO小鼠的體重顯著重於瘦對照小組。在一個研究中,DIO小鼠稱重38.4±0.6g,而瘦小鼠稱重29.9±0.5g(p<0.05)。
在第二種方法中,膳食誘導肥胖雄性C57BL/6J小鼠(12周大)和對照瘦小鼠(12周大)獲自Jackson實驗室(Bar Harbor,ME),並且最初4-5隻/籠圈養在22℃下,使用12:12hr白天-黑夜循環。在處理前將小鼠在動物實驗設施中適應一周並對DIO組維持高脂肪膳食(Research Diets Cat#:D12492;60kcal%脂肪、20kcal%蛋白和20kcal%碳水化合物)或對瘦組維持低脂肪膳食(10%kcal%脂肪)。
實施例4-在膳食誘導肥胖症(DIO)小鼠中用Eno1治療葡萄糖不耐性
在高脂肪膳食維持7周後小鼠(n=10隻/組)肥胖時,開始實驗方案。按照製造商的指導,將微型滲透泵(型號1004,Alzet,Cupertino,CA)填充0.1ml Eno1肽或溶媒(磷酸鹽緩衝鹽水(PBS),pH 7.0)。將泵在無菌鹽水中在4℃下準備過夜。用異氟烷將小鼠麻醉(100%氧中1-3%)並在外科手術前用70%異丙醇和聚維酮碘溶液擦洗。在中肩胛區域中形成小的皮下切口,將泵插入並且縫合傷口。在返回其圈養籠子之前,使得動物恢復。皮下微型滲透泵的植入以0.11μl/hr的恆定速率持續灌注肽,持續四周。每4周進行泵更換手術。通過泵灌注速率計算的純化Eno1處理劑量為10μg/kg體重。
在6h禁食後,使用常規方法進行葡萄糖耐量測試(GTT)。簡而言之,測定了初始空腹血糖水平,接著以1.5g/kg體重的劑量腹膜內(ip)注射20%右旋糖溶液。在葡萄糖注射後15,30,60,90和120分鐘,使用 Advantage血糖儀(Diagnostics,Indianapolis,IN)從尾靜脈測量血糖水平。使用Graphpad軟體計算GTT過程中的曲線下面積(AUC),並且針對不同處理組之間的顯著性進行了student t-檢驗。結果顯示於圖4A和4B中。
如可以容易地觀察到的,用Eno1處理的小鼠與未處理小鼠相比,血糖曲線下面積顯著降低(p=0.017)。這些數據證明了用Eno1蛋白處理肥胖小鼠提高了葡萄糖耐量,如通過葡萄糖耐量測試證明的,並且表明了Eno1在胰島素抵抗、葡萄糖不耐性和2型糖尿病的治療中是有效的。
實施例5-PAMAM樹狀聚合物、肌肉靶向Eno1的產生
已經證明了全身施用時Eno1提高肌管中的葡萄糖攝取和提高葡萄糖耐量的功效,因此產生了肌肉靶向的Eno1來分析其提高葡萄糖耐量的功效。使用下文所述的方法產生了含有肌肉靶向肽(MTP)ASSLNIA和/或Eno1的可檢測地標記的G5-PAMAM樹狀聚合物。評價了各種不同比率的MTP與樹狀聚合物,包括含有MTP的樹狀聚合物,其含有約10個MTP肽/樹狀聚合物,約3個MTP肽/聚合物或約1個MTP肽/樹狀聚合物。
製備Eno1樹狀聚合物複合物的過程包括試劑的最佳比例和濃度的鑑定。在緩衝液中製備了Eno1的原液,並將蛋白溶液以不同比率與G5樹狀聚合物-肌肉靶向肽(MTP)偶聯物混合。還評價了各種不同比率的樹狀聚合物與Eno1,包括含有Eno1的樹狀聚合物,其含有約一個樹狀聚合物/Eno1蛋白分子或約五個樹狀聚合物/Eno1蛋白分子。
在不同溫度下評價了Eno1-樹狀聚合物-SMTP複合物的穩定性,並且使用商業上可購得的Eno1分析通過測量Eno1活性測定了在3-4個月的時間段內的穩定性。還是用生物物理技術,包括動態光散射(DLS)和UV-Vis光譜學,來評價選定的偶聯物以證實樹狀聚合物-肽偶聯物和Eno1之間的複合。
Eno1純度的測定:通過考馬斯和銀染以及Western印跡檢查了Eno1蛋白的5.32mg/L溶液的純度。製備了範圍從10μg/孔至100ng/孔的Eno1蛋白的幾個稀釋液並加載於12-孔,4-12% TGX凝膠[BIO-RAD Cat#456-1095Lot#4000 79200]上。泳道分配如下:泳道1:梯(Precision Plus Protein Standard Dual Color[BIO-RAD Cat#161-0374];泳道2:Eno1(10.0μg);泳道3:Eno1(1.0μg);泳道4:Eno1(0.1μg);泳道5:梯(Precision Plus Protein Standard Dual Color[BIO-RAD Cat#161-0374];泳道6:Eno1(10.0μg);泳道7:Eno1(1.0μg);泳道8:Eno1(0.1μg);泳道9:梯(Precision Plus Protein Standard Dual Color[BIO-RAD Cat#161-0374];泳道10:Eno1(10.0μg);泳道11:Eno1(1.0μg);泳道12:Eno1(0.1μg)。SDS-PAGE在200V下運行20-25min。
考馬斯染色:跑膠後,將凝膠分割成3個相等部分。一個部分用考馬斯染色。簡而言之,將凝膠浸沒在100mL考馬斯染色液(40%甲醇和7%乙酸中的0.025%考馬斯染料)中並在微波爐中加熱一分鐘。然後,凝膠伴隨溫和攪拌使染色45分鐘。完成染色後,使用脫色液(40%甲醇和7%乙酸)將凝膠脫色直至背景染色可接受。
如圖5中所示,蛋白呈現為約47kDa的單個條帶,這與Eno1的大小一致。
銀染:由於考馬斯染色對於蛋白條帶的可視化不是一種靈敏的方法,另一部分的凝膠使用BIO-RAD的銀染試劑盒[BIO-RAD Cat#161-0443]用銀染來染色。遵循改良的銀染實驗方案進行。
如圖6中所示,在每個泳道中看到了額外的條帶,其對應於梯的條帶。這是由於梯狀條帶漏入了鄰近泳道中。用箭頭標記的三個條帶不是來自梯。最明顯的條帶為約47kDa,這與Eno1的大小一致。在純化蛋白中存在兩個額外條帶,但這些條帶微弱,表明Eno1的整體純度是相對高的。
Western印跡分析:通過Western印跡進一步確認Eno1的身份。為了這個目的,將最後部分的凝膠轉移至100mL Tris-甘氨酸緩衝液中並使用transblot SD半乾式轉移裝置(BIO-RAD)在20V下轉移至0.2μm PVDF膜(BIO-RAD)上2.0h。通過觀察膜上預染色梯狀條帶的存在來檢查轉移的效率。將膜乾燥1.0h。然後膜用甲醇潤溼1.0min,並用15.0mL封閉緩衝液(LICOR)在室溫下封閉2.0h。
封閉完成後,用15.0mL的含有30μL抗-ENOA-1 m-Ab(小鼠)(購自ABNOVA)的封閉緩衝液將膜在4℃下孵育過夜。然後用3×30mL的1×PBS-T洗滌膜,每次振蕩5分鐘。然後用15.0mL的含有5μL用800CW(購自LICOR)標記的山羊抗小鼠二抗的封閉緩衝液將膜在室溫下孵育2.0h。孵育後,用3×30mL的1×PBS-T,接著2×30mL的1×PBS洗滌膜,每次振蕩5分鐘。最後,使用LICOR ODYSSEY紅外成像儀將膜成像。如圖7中所示,Western印跡分析證實了47kDa的主要訂帶是Eno1。
烯醇酶-I/G5-PAMAM-SMTP的Zeta(ζ)-電位表徵:以改變的比率複合Eno1和帶有2-3個骨骼肌靶向肽(SMTP)的5代PAMAM樹狀聚合物以形成Eno1/G5-SMTP蛋白/樹狀聚合物複合物。將樹狀聚合物的濃度保持恆定在1.0μM,而Eno1濃度在0.1μM-10.0μM之間變化。以下表2描述了怎樣製備烯醇酶-I/G5-樹狀聚合物/SMTP混合物。
表2.用於形成樹狀聚合物複合物的Eno1和G5-樹狀聚合物/SMTP的各種組合
通過將G5-樹狀聚合物/SMTP加入相應量的PBS中製備了各個樣品。然後將烯醇酶以逐滴方式加入G5-樹狀聚合物/SMTP溶液中,同時低速渦旋。然後在分析前,將樣品在室溫下孵育20分鐘。
使用來自Malvern Instruments的Zetasizer Nano Z90s儀器進行大小測量。使用預設參數用於測量,並且收集每個樣品的三個單獨測量。圖8顯示了針對具有2:1的Eno1與樹狀聚合物/SMTP摩爾比的Eno1/G5-樹狀聚合物/SMTP複合物的三個樣品的Zeta(ζ)-電位數據。使用動態光散射測量Zeta(ζ)-電位。如圖8中所示,三個樣品的峰匹配,表明烯醇酶-SMTP樹狀聚合物複合物的均一電荷分布。
烯醇酶-I/G5-SMTP複合物的穩定性:通過使用ENO1人活性分析試劑盒(ABCAM,Cambridge,MA;目錄No.ab117994)測量了烯醇酶-I/G5-樹狀聚合物/SMTP偶聯物的穩定性。簡而言之,將樣品加入含有Eno1特異性的單克隆小鼠抗體的微平板中。將微平板在室溫下孵育2小時,並將Eno1免疫捕獲在微平板的孔內。洗滌微平板的孔以除去所有其他酶。通過按照在包括丙酮酸激酶(PK)、乳酸脫氫酶(LDH)以及所需底物2-磷酸-D-甘油酸(2PG)和NADH的分析緩衝液中的NADH消耗來測定Eno1活性。Eno1將2PG轉化成磷酸烯醇丙酮酸,其通過PK轉化成丙酮酸。丙酮酸通過LDH轉化成乳酸,並且這種反應需要NADH。作為340nm處吸光度的下降來監測NADH的消耗。
使用上述分析測量了不同時間點在不同溫度下儲存的烯醇酶-I/G5-樹狀聚合物/SMTP偶聯物的活性。選擇500ng的Eno1濃度用於測試,因為這個濃度落入分析試劑盒的動態範圍的中間。製備了兩個不同組的溶液。一組(對照)僅含有Eno1(即,未偶聯的Eno1),而另一組含有Eno1/G5-樹狀聚合物/SMTP混合物。然後將這些混合物保持在-80℃、-20℃、4℃、22℃和37℃。結果顯示出在第一周中,全部樣品是有活性的,並且Eno1/G5-樹狀聚合物/SMTP偶聯物看來具有略高於單獨的Eno1的活性。然而,溶液的活性,無論是否它們含有樹狀聚合物,在接下來的兩周中穩定地降低。到第3周,儲存在4℃、22℃和37℃下的溶液未顯示出活性,而儲存在-80℃和-20℃的溶液顯示出顯著的穩定性。在研究結束時(第10周),保持在-80℃的Eno1/G5-樹狀聚合物/SMTP溶液保留約90%的活性,而單獨的Eno1僅有35%活性。另一方面,保持在-20℃的Eno1/G5-樹狀聚合物/SMTP溶液為約24%活性的,而儲存在-20℃的單獨Eno1無活性(圖9)。
實施例6-使用G5 PAMAM樹狀聚合物的體內Eno1靶向研究
使用之前實施例中提供的方法製備了含有Eno1的可檢測地標記的PAMAM樹狀聚合物並在皮下注射後分析在小鼠中的組織分布。具體地,在注射前72小時,給小鼠飼餵無苜蓿食物以限制背景螢光。給小鼠皮下注射3μg ENO1/小鼠,總共150μl(75μl左側,75μl右側)。複合物中樹狀聚合物與Eno1的摩爾比為5:1。注射後1、4和24小時,將動物處死、去皮並取出器官準備用於LI-COR成像。結果顯示於圖10A中。
如所示的,在1小時時,觀察到了Eno1-PAMAM樹狀聚合物的總體全身分布。4小時後,觀察到了Eno1-PAMAM樹狀聚合物在肝臟、腎臟和皮下脂肪以及在上部軀體中的明顯累積。24小時後,Eno1-樹狀聚合物基本上清除,並且基本上在肝臟和腎臟中觀察到。
使用骨骼肌靶向的含有SMTP「ASSLNIA」的Eno1-PAMAM樹狀聚合物複合物進行了追蹤研究。使用之前實施例中提供的方法製備了含有Eno1和SMTP的可檢測地標記的PAMAM樹狀聚合物複合物((烯醇酶-Vivo Tag680xl)-(G5-SMTP))。複合物中樹狀聚合物與SMTP的摩爾比為1:1。基本上按照以上所述的進行了實驗。以50μg/kg體重的劑量施用了骨骼肌靶向的Eno1-PAMAM樹狀聚合物複合物。在注射1hr後獲取了圖10B中的這些圖像。心臟以外的器官保留在體內。如可以容易地觀察到的,肌肉靶向Eno1樹狀聚合物複合物靶向骨骼肌而不是心臟。這些結果證明了骨骼肌靶向Eno1-PAMAM樹狀聚合物複合物可以用於將Eno1遞送至骨骼肌細胞。
實施例7-用肌肉靶向Eno1在膳食誘導肥胖症(DIO)小鼠中治療葡萄糖不耐性
膳食誘導肥胖雄性C57BL/6J小鼠(12周大)和對照瘦小鼠(12周大)獲自Jackson實驗室(Bar Harbor,ME)並且最初4-5隻/籠圈養在22℃下,使用12:12hr白天-黑夜循環。在處理前將小鼠在動物實驗設施中適應一周並對DIO組維持高脂肪膳食(Research Diets Cat#:D12492;60kcal%脂肪、20kcal%蛋白和20kcal%碳水化合物)或對瘦組維持低脂肪膳食(10%kcal%脂肪)。
在13周大開始,所有小鼠接受每日皮下注射鹽水或具有G5樹狀聚合物、骨骼肌靶向肽(SMTP)和純化Eno1(50μg/kg體重)的組合的不同複合物,持續4周。在實驗的處理部分的4周過程中,每周進行了腹膜內葡萄糖耐量測試(IPGTT)。在處理期過程中,每周測量體重、餐後血糖和空腹血糖。處理組如下所示:
1.LFD-瘦對照-無注射
2.HFD-鹽水對照(體積等同於G5+SMTP+Eno1)
3.HFD-只有G5(等同於50μg/kg的G5+SMTP+Eno1)
4.HFD--G5+SMTP(等同於50μg/kg的G5+SMTP+Eno1)
5.HFD--G5+Eno1(50μg/kg體重)
6.HFD--G5+SMTP+Enol(50μg/kg體重)
複合物中樹狀聚合物與Eno1的摩爾比為5:1,複合物中樹狀聚合物與SMTP的摩爾比為1:1,並且樹狀聚合物是乙醯化的。來自該研究的結果提供於圖11、12、13、14和15中。
在這個小群組中,發現沒有治療方案在研究過程中的任何時間對DIO小鼠的體重具有顯著影響(參見圖11)。
用單劑量的樹狀聚合物結合的肌肉靶向Eno1處理小鼠證明了在最早測試時間點對血糖水平具有作用。如圖12中所示的,在施用50μg/kg的G5+SMTP+Eno1後一小時,與鹽水對照相比觀察到血糖的降低,在4小時時觀察到最大降低。在單次注射後24小時時不再觀察到作用。
在開始施用樹狀聚合物結合的肌肉靶向Eno1後一周時,用Eno1樹狀聚合物SMTP複合物(DIO烯醇酶-1+NP+SMTP)處理的DIO小鼠中的葡萄糖耐量顯著低於用單獨的樹狀聚合物SMTP複合物(DIO NP+SMTP)處理的DIO小鼠中的葡萄糖耐量(參見圖13A和13B)。
在開始施用樹狀聚合物結合的肌肉靶向Eno1後兩周時,DIO小鼠中的葡萄糖耐量仍然顯著提高(參見圖6C和6D)。葡萄糖耐量的提高依賴於樹狀聚合物複合物中Eno1的存在(DIO G5+SMTP vs.DIO Eno1G5+SMTP,p=5.7×10-5,p=0.002)。在單次注射後23小時不再觀察到作用(數據未顯示)。
在第1和第2周時觀察到的G5+SMTP+Eno1處理的有益作用持續至第4周(參見圖14A和14B)。具體地,DIO Eno1G5+SMTP處理小鼠中的葡萄糖耐量與瘦小鼠中的相似。葡萄糖耐量的提高是顯著的並且依賴於樹狀聚合物複合物中Eno1的存在(DIO G5+SMTP vs.DIO Eno1G5+SMTP,p=0.0017)。在單次注射後23小時不再觀察到作用(數據未顯示)。
這些結果表明樹狀聚合物結合的肌肉靶向Eno1在提高膳食誘導肥胖症模型中的葡萄糖耐量中是有效的,並且G5+SMTP+Eno1在使膳食誘導肥胖症小鼠模型中的血糖正常化是有效的。這些結果證明了Eno1在升高的血糖、葡萄糖不耐性和糖尿病,特別是2型糖尿病的治療中是有用的。
按照以上所述的將小鼠再處理4周(總共8周處理),並且測定了瘦小鼠、膳食誘導肥胖症(DIO)小鼠、用G5-樹狀聚合物處理的DIO小鼠和用Eno1/G5-樹狀聚合物/SMTP複合物處理的小鼠在處理8周後的血清乳酸鹽水平。使用來自Biovision(Milpitas,CA)的乳酸鹽比色分析試劑盒測量了血清中的乳酸鹽水平。如圖15中所示,Eno1/G5-樹狀聚合物/SMTP複合物顯著降低了乳酸鹽血清水平。這個結果表明用Eno1/G5-樹狀聚合物/SMTP複合物處理的DIO小鼠中觀察到的降低的葡萄糖水平是由於提高的葡萄糖氧化,而不是糖酵解至乳酸鹽的分流。這將最小化乳酸鹽酸中毒的不利影響。
實施例8-用肌肉靶向Eno1在肥胖的遺傳模型db/db小鼠中治療葡萄糖不耐性
雄性肥胖和糖尿病db/db小鼠(雄性BKS.Cg-m+/+Leprdb/J)小鼠獲自商業零售商。所有小鼠2-3隻/籠圈養在22℃下,使用12:12hr白天-黑夜循環,並且在動物實驗設施中飼餵標準飼料適應3周。在8周大時,通過皮下施用(n=6/組),每日一次施用鹽水或具有G5樹狀聚合物、骨骼肌靶向肽(SMTP)和純化Eno1組合的不同複合物的以下皮下注射。處理組如下:
1.使用鹽水注射的db/db
2.使用G5+SMTP(體積等同於25ug/kg劑量的Eno1+G5+SMTP)的db/db
3.使用Eno1(25ug/kg體重)+G5+SMTP的db/db
4.使用Eno1(50ug/kg體重)+G5+SMTP的db/db
複合物中樹狀聚合物與Eno1的摩爾比為5:1,而複合物中樹狀聚合物與SMTP的摩爾比為1:1,並且樹狀聚合物是乙醯化的。
在第7天,小鼠施用合適的藥劑並在按照以上實施例所述的施用IPGTT之前返回籠子6小時而沒有食物。結果顯示於圖16A和16B中。如可以容易地觀察到的,用Eno1+G5+SMTP處理小鼠導致葡萄糖負荷後葡萄糖耐量提高,與用G5+SMTP處理的小鼠相比用Eno1(50ug/kg體重)+G5+SMTP處理的小鼠中觀察到葡萄糖清除的顯著提高(p=0.015)。
使用上述所列每個處理組中六隻小鼠中的三隻繼續研究。小鼠施用所示藥劑再一周(總共2周)。測試了Eno1對降低餐後血糖的作用。具體地,在不控制食物攝入的情況下,在施用活性劑後立即評價小鼠中的血糖水平兩小時。如所示的,Eno1(50ug/kg體重)+G5+SMTP的施用證明了降低餐後血糖並且導致與G5+SMTP的施用相比在施用後30分鐘血糖的統計學顯著的降低。然而,Eno1+G5+SMTP處理後30分鐘觀察到的降低的血糖在Eno1注射後24小時時沒有維持(圖18)。
因此,還在db/db小鼠中評價了每日兩次給藥Eno1+G5+SMTP對血糖水平的作用。每日兩次通過皮下注射來給予處理,一次在早晨和一次在晚上,持續四周。處理組如下:
1.PBS
2.100μg/kg體重Eno1+G5+SMTP
3.200μg/kg體重Eno1+G5+SMTP
Eno1+G5+SMTP複合物中樹狀聚合物與Eno1的摩爾比為5:1,而Eno1+G5+SMTP複合物中樹狀聚合物與SMTP的摩爾比為1:1,並且樹狀聚合物是乙醯化的。
處理組2的總日劑量為200μg/kg體重Eno1+G5+SMTP,和處理組3的總日劑量為400μg/kg體重Eno1+G5+SMTP。在不控制食物攝入的情況下,在晚上注射後16小時(即在早晨注射前)評價了小鼠中的餐後血糖水平。如圖19中所示,每日兩次注射200μg/kg體重Eno1+G5+SMTP相對於對照PBS處理降低了餐後血糖水平。
因此,用Eno1G5+SMTP處理小鼠顯示出使db/db小鼠中的葡萄糖反應標準化。實施例7和8中所述的數據一起證明了Eno1在提高2型糖尿病的誘導模型和遺傳模型中的葡萄糖耐量都是有效的。
實施例9-含樹狀聚合物的乙醯化vs.非乙醯化SMTP的比較毒性
使用肌氨酸激酶和半胱天冬酶3分析比較了含有乙醯化和非乙醯化樹狀聚合物的SMTP的毒性。給小鼠注射十字孢鹼(staurosporine)(陽性對照)、十字孢鹼+抑制劑(陰性對照);G5 PAMAM樹狀聚合物、SMTP-G5 PAMAM樹狀聚合物和乙醯化SMTP-G5 PAMAM樹狀聚合物中的一種。複合物中樹狀聚合物與Eno1的摩爾比為5:1,而複合物中樹狀聚合物與SMTP的摩爾比為1:1。注射後,收集樣品並使用商業上可購得的試劑盒測定作為總細胞裂解物的百分比的肌氨酸激酶水平和半胱天冬酶3活性。結果顯示於圖20中。如圖20中所示,1uM和3uM濃度的G5 PAMAM樹狀聚合物的施用以及3uM濃度的SMTP-G5 PAMAM樹狀聚合物的施用導致肌氨酸激酶活性的顯著提高。使用乙醯化SMTP-G5 PAMAM樹狀聚合物觀察到沒有這種作用。相似地,3uM G5 PAMAM樹狀聚合物和SMTP-G5 PAMAM樹狀聚合物施用後,觀察到半胱天冬酶3活性的顯著提高。然而,施用乙醯化SMTP-G5 PAMAM樹狀聚合物時,沒有觀察到半胱天冬酶3活性的提高。這些結果證明了SMTP-G5 PAMAM樹狀聚合物的乙醯化降低了毒性。
實施例10-在2型和1型糖尿病的遺傳和誘導模型中用肌肉靶向Eno1治療葡萄糖不耐性
獲得或產生雄性肥胖小鼠、糖尿病db/db小鼠(雄性BKS.Cg-m+/+Leprdb/J)小鼠、NOD1小鼠或鏈脲黴素處理的小鼠。所有小鼠2-3隻/籠圈養在22℃下,使用12:12hr白天-黑夜循環,並且在動物實驗設施中飼餵合適飼料(即,用於肥胖小鼠的高脂肪膳食,用於其他小鼠的正常飼料)適應至少1周。在合適年齡時,通常約8周大時,每日施用鹽水或具有G5樹狀聚合物、骨骼肌靶向肽(SMTP)和純化Eno1(25或50μg/kg體重)的組合的不同複合物的皮下注射,持續1-2周。可以將如上所述的可植入泵(例如,ALZET泵)用於每日或持續的施用。或者,可以在不同配方中通過肌肉內施用藥劑。通常以低於皮下注射的頻率來進行肌肉內注射(例如,通常約每周一次)。
在2周時間過程中,進行了腹膜內葡萄糖耐量測試(IPGTT),並監控空腹和餐後血糖(隨機地或在藥劑施用後的時間過程中)。在處理期間,每周測量體重。處理組包括至少一個對照(例如,1或2)和至少一個來自以下所示列表中的Eno1處理:
1.鹽水注射
2.G5+SMTP(體積等同於25ug/kg體重/天的Eno1+G5+SMTP)
3.Eno1(25ug/kg體重/天)+G5+SMTP
4.Eno1(50ug/kg體重/天)+G5+SMTP
5.Eno1(25ug/kg體重/天)
6.Eno1(50ug/kg體重/天)
提供的劑量是示例性的並且不認為是限制性的。
用Eno1 G5+SMTP處理小鼠證明使糖尿病小鼠中的葡萄糖反應正常化。
實施例11-小鼠中血糖水平和葡萄糖反應的評價
以上描述了腹膜內葡萄糖耐量測試(IPGTT)並常規地用於評價葡萄糖耐量和胰島素反應。以下提供了可以用來證實Eno1在正常化血糖和胰島素反應中的功效的其他示例性方法。以下還提供了評價身體組成和代謝的方法。
腹膜內胰島素耐量測試(IPITT)
在禁食1小時後進行胰島素耐量測試(ITT)來評價丙酮酸代謝。測定了初始的血糖水平,接著注射(ip)人胰島素(1-2U/kg;Humulin R;Eli Lilly,Indianapolis,IN)。在胰島素注射後15、30、60、90和120min時,如上所述從尾靜脈測量血糖水平。由於接受高脂肪膳食的小鼠中肝胰島素抗性的發作,胰島素注射量通過胰島素反應根據經驗確定。
腹膜內丙酮酸耐受測試(IPPTT)
在禁食6h後給予丙酮酸耐受試驗。測定了初始血糖水平,接著注射(ip)溶解於鹽水中的丙酮酸(2g/kg;Sigma,St.Louis,MO)。在丙酮酸注射後15、30、60、90和120min,如上所述從尾靜脈測量血糖水平。計算測試過程中的曲線下面積(AUC)。
餐後血糖水平
從自由進食的小鼠獲得血液樣品(隨機地或在在目標藥劑施用後限定的時間或時間間隔)。測量血糖水平。
空腹血糖水平
在禁食預定時間段(通常約6-8小時)後,在目標藥劑施用後的限定時間或時間間隔從小鼠獲得血液樣品。測量血糖水平。
指示劑水平的評價來評價血糖水平
用本發明的一種或多種藥劑和合適的對照處理1型或2型糖尿病的小鼠模型。監測HbA1c和/或Eno1蛋白和/或RNA的水平來測定持續時間段內的血糖水平。
雙能X-射線吸收測定法(DEXA)
按照製造商推薦的程序,使用LUNAR小鼠光密度計通過雙能x-射線吸收測定法(DEXA)掃描來測定不同處理組的身體質量組成。記錄並分析了瘦體質量、脂肪體質量、總身體組織重量、骨密度和骨礦物質含量。
綜合實驗室動物監控系統(CLAMS)
使用CLAMS(Columbus Instruments,Columbus,OH,USA)代謝監測籠來同時監測水平和垂直活動、進食和飲水、氧消耗和CO2產生。ASO注射的和對照小鼠單獨地置於CLAMS籠中並在籠中適應1-2天後監測4-天時間。在禁食和進食條件下記錄各種參數。作為累積數據直接測量食物和水消耗。每小時文件顯示了針對每個參數的所有測量:消耗的氧的體積,ml/kg/h(VO2),產生的二氧化碳的體積,ml/kg/h(VCO2),呼吸交換率,熱量(kcal/h),累積的食物(g),累積的飲水(g),XY總活動(全部水平束中斷計數),XY走動活動(最少三個不同的、連續水平束中斷計數)和Z活動(全部垂直束中斷計數)。在30-s取樣時間段中記錄數據。通過用瘦體質量標準化來分析CLAMS數據。
實施例12-Eno1對人骨骼肌肌管中胰島素刺激的p-Akt的作用
在具有或不具有胰島素處理的情況下在人骨骼肌肌管的細胞培養物中測定了純化的Eno1對胰島素刺激的p-Akt(S473)蛋白水平的作用。通過ELISA測量p-Akt蛋白水平。如圖21中所示,在Enol處理不存在的情況下,胰島素處理提高了p-Akt蛋白水平,且胰島素對p-Akt蛋白水平的作用在具有或不具有Eno1處理的情況下是相似的。這些結果顯示Eno1不影響p-Akt蛋白水平的胰島素刺激,表明Eno1對肌細胞中的葡萄糖攝取的作用與胰島素無關並且將在呈現胰島素抵抗的細胞中出現。
實施例13-Eno1與人骨骼肌肌管中提高的葡萄糖流量相關
葡萄糖轉運蛋白1(Glut1)和葡萄糖轉運蛋白4(Glut4)涉及葡萄糖跨越質膜的轉運,並且是骨骼肌內的主要促進性葡萄糖轉運蛋白(Jones等,1998,Journal of Applied Physiology,Vol.84,pp.1661-1666)。Glut4負責胰島素調節的至細胞中的葡萄糖轉運。肌細胞生成素是可以參與調節Glut1和Glut4表達的肌肉特異性轉錄因子(參見Jones等,上文)。己糖激酶2(HK2)將葡萄糖磷酸化以形成葡萄糖-6-磷酸(G6P)並且是骨骼肌中的主要己糖激酶。
在具有或不具有Eno1處理的情況下,在人骨骼肌肌管細胞培養物中測量了Glut1、Glut4、HK2和肌細胞生成素的表達。用按照實施例2中所述製備的純化Eno1處理肌管。通過定量PCR測定了Glut1、Glut4、HK2和肌細胞形成素mRNA水平。通過MS蛋白質組學分析測定了Glut1蛋白水平。如圖22A和22B中所示,Eno1處理提高了Glut1、Glut4和HK2mRNA水平,以及Glut1蛋白水平。因為這些蛋白質參與葡萄糖轉運和代謝,這些結果表明Eno1處理與骨骼肌中提高的葡萄糖流量相關。
為了進一步研究Eno1在葡萄糖流量中的作用,在具有或不具有純化Eno1處理的情況下測量葡萄糖飢餓和葡萄糖刺激的人骨骼肌肌管中G6P和磷酸烯醇丙酮酸(PEP)水平。通過在無葡萄糖DMEM中孵育肌管15min來進行葡萄糖飢餓。通過用5mM葡萄糖處理肌管15min進行葡萄糖刺激。使用來自Biovision的分析試劑盒(Milpitas,CA;Cat.No.K657-100和K365-100)測量了G6P和PEP水平。如圖23和24中所示,Eno1處理提高了葡萄飢餓和葡萄糖刺激的人骨骼肌肌管中的G6P和PEP水平,進一步表明Eno1處理與骨骼肌中提高的葡萄糖流量相關。
實施例14-Eno1作用方式
為了進一步研究在葡萄糖攝取中的Eno1作用方式,測量了人骨骼肌肌管細胞中的氧消耗率(OCR)和細胞外酸化率(ECAR)。OCR是線粒體呼吸的指示,而ECAR是糖酵解的指示。
對於OCR實驗,將各種化合物按序添加到細胞以誘導OCR的變化。例如,加入棕櫚酸鹽和羰基氰化物m-氯苯基腙(CCCP,氧化磷酸化的解偶聯劑)以提高OCR,並加入乙莫克舍(脂肪酸氧化抑制劑)以降低OCR。將KHB緩衝劑(pH 7.4)加入每個孔中,並每3min進行測量,具有2min的測量間混合。按序注射BSA偶聯的棕櫚酸鹽(終濃度200mmol/L)、CCCP(終濃度2μM)和乙莫克舍(終濃度50mmol/L)。如圖25中所示,Eno1處理提高了OCR。這些結果表明Eno1處理與人骨骼肌肌管中提高的線粒體游離脂肪酸氧化相關。
對於使用葡萄糖作為底物的ECAR實驗,使用無碳酸鈉和葡萄糖/丙酮酸的DMEM培養基。按序注射葡萄糖、寡黴素和2-DG以獲得25mmol/L的終濃度。如圖26中所示,Eno1處理提高了ECAR,表明Eno1處理與提高的糖酵解活性和能力相關。
為了測定用Eno1處理的人骨骼肌肌管的線粒體含量,用500ug/ml或1000μg/ml Eno1處理肌管48小時,並隨後加入Mitotracker green(Invitrogen),一種綠色螢光線粒體染料。15min染色後,將肌管胰蛋白酶化、洗滌並接受流式細胞術分析以測定線粒體含量。如圖27A中所示,Eno1處理沒有影響線粒體含量。
還檢測了上述Eno1處理的人骨骼肌肌管中的線粒體ROS。通過用二氫若丹明123(Life Technologies)處理細胞來測定線粒體ROS,二氫若丹明123是一種不帶電的和非螢光的反應性氧物質(ROS)指示劑,其可以被動跨膜擴散,在其中氧化成陽離子若丹明123(其定位於線粒體中並呈現出綠色螢光)。然後將肌管胰蛋白酶化、洗滌並接受流式細胞術分析。用Eno1處理人骨骼肌肌管沒有影響線粒體的反應性氧物質產生(圖27B)。
這些結果表明Eno1的作用方式不是由於線粒體含量或ROS產生的變化。
為了進一步研究Eno1的作用方式,在用0、500或1000μg/ml Eno1處理的基礎的和血清飢餓的人骨骼肌肌管中測量了非磷酸化的5』AMP激活的蛋白激酶(AMPK)和磷酸化AMPK(pAMPK)水平。用含有2%馬血清的正常分化培養基處理基礎人骨骼肌肌管,而血清飢餓的肌管在肌管裂解前用含有0.5%BSA的無血清DMEM飢餓3小時。使用對於激酶的磷酸化或非磷酸化形式特異性的抗體通過Western印跡測定了AMPK和pAMPK水平。將對於核纖層蛋白(Lamin)A/C特異性的抗體用於證實樣品之間均勻的加載。如圖28A和28B中所示,Eno1處理沒有影響基礎或血清飢餓肌管中的pAMPK水平。AMPK激活或磷酸化是調節骨骼肌中的葡萄糖攝取的主要非胰島素依賴性途徑之一,例如,在肌肉收縮過程中。因此,Eno1對pAMPK水平的作用的缺乏表明超越了常規信號轉導的Eno1的新作用方式。
實施例15-人骨骼肌肌管中的Eno1結合伴體
為了進一步研究Eno1的作用方式,在未處理的人骨骼肌肌管(含有內源性Enol)和用50μg/ml或100μg/ml 6X組氨酸標記的外源性Enol處理的人骨骼肌肌管中比較了Eno1的結合伴體。使用Eno1特異性的抗體在未處理肌管中免疫沉澱內源性Eno1。使用6X組氨酸標籤抗體將外源性Eno1免疫沉澱。通過定量蛋白質組學鑑定內源性Eno1和外源性Eno1的結合伴體,並且通過Western印跡和/或反向免疫沉澱來證實結合伴體的性質。
煙醯胺磷酸核糖基轉移酶(Nampt)被鑑定為內源性和外源性Eno1兩者的結合伴體。Nampt催化從煙醯胺合成煙醯胺單核苷酸(NMN)並且參與肌肉收縮和分泌。Eno1可以與作為糖酵解複合物的部分的Nampt相互作用,如圖29中所示。
實施例16-Eno1和Nampt的相互作用
在4天分化後,在分化培養基中用500ug/ml或1000μg/ml Enol處理48小時的人骨骼肌肌管中測定了Nampt活性。將肌管裂解物使用IgG或來自Cyclex(Nagano,日本)的抗Nampt抗體(Clone AF-1E12)進行免疫沉澱。將免疫沉澱的肌管裂解物使用Cyclex Nampt活性分析試劑盒(#CY-1251)進行Nampt活性分析。如圖30中所示,Eno1處理提高了Nampt活性。Eno1處理還提高了人骨骼肌肌管中Nampt(eNampt)的分泌(數據未顯示)。
在已經血清飢餓3小時並隨後用來自Abcam(Cambridge,MA)的重組細胞外Nampt(eNampt)處理的人骨骼肌肌管中測量2-DG攝取。使用來自Abcam的螢光葡萄糖攝取分析試劑盒(Cat.No.ab136956)測量了2-DG攝取。如圖31中所示,eNampt的添加提高了2-DG攝取。
為了測定Nampt在Eno1誘導的葡萄糖攝取中的作用,如上所述用Eno1處理人骨骼肌肌管48小時,並在Eno1處理開始後24小時加入Nampt抑制劑FK866,總的FK866處理時間為24小時。使用上述Abcam葡萄糖攝取分析試劑盒,在3小時血清飢餓後測量了2-DG攝取。如圖32中所示,通過FK866的Nampt抑制消除了Eno1誘導的葡萄糖攝取。這個結果表明Nampt在Eno1誘導的葡萄糖攝取中起著作用。
等同
本領域技術人員將認識到或僅使用常規實驗能夠獲知本文中所述的特定實施方案和方法的許多等同物。這樣的等同物打算包括在以下權利要求的範圍中。
按引用併入
將本申請中提及的每篇參考文獻、專利、專利申請和GenBank編號由此按引用併入,如同每篇參考文獻註明單獨併入。
序列描述
