一種溶液中過氧化氫含量的快速測定方法與流程
2023-12-10 07:13:57 4
本發明涉及一種過氧化氫的快速測定方法,具體涉及一種以亞鐵離子為活化劑、以n,n-二乙基對苯二胺為指示劑快速檢測溶液中過氧化氫含量的方法。
背景技術:
由於具有較強的氧化能力以及綠色環保的特點,過氧化氫在環保、日化、食品、醫療以及印染行業中,被廣泛的用作氧化劑、消毒劑、滅菌劑以及漂白劑。此外,過氧化氫還可以被過渡金屬離子、金屬氧化物、微波輻射以及紫外線輻射等活化產生具有更強氧化能力的羥基自由基(e0=1.8-2.7v),被廣泛用於環保領域,尤其水處理領域中去除難降解有機汙染物以及滅活致病微生物。在使用過氧化氫過程中,往往會伴隨著氧化劑的分解以及殘餘。據報導,人體中殘餘的過氧化氫會消耗抗氧化物質使得人體加速衰老;長期接觸或誤食低濃度的殘餘過氧化氫會導致人體遺傳物質損傷以及基因突變,甚至誘發癌症。因此,在過氧化氫的使用過程中,需要監測過氧化氫殘餘量的變化。
目前,過氧化氫含量的測定方法主要有滴定法、化學發光法、色譜法、分光光度法、試紙比色法、電流分析法等。滴定法中主要有碘量法和高錳酸鉀法,該方法靈敏度高、測定結果準確,但也存在操作複雜、幹擾因素多等不足。色譜法具有專一性強、準確度高、抗幹擾能力強等優點,如專利zl201310745895.7,然而色譜法需要使用昂貴的色譜儀,導致測定成本高昂。化學發光法具有靈敏度高、檢出限低、測定結果準確等優點,但同樣存在測定時間長、測定成本高等不足之處。紫外-可見分光光度法測定結果可靠、測定速度快、操作相對簡便,如專利zl201310745891.9和zl201410034574.0,但也存在反應時間較長、反應試劑有毒易造成環境汙染等不足之處,試紙比色法具有操作簡便、測定速度快等優點,如專利zl201310337923.1,但也存在試紙製備成本較高、測定結果準確性較差、靈敏度較低等不足之處。電流分析法測定結果準確可靠、靈敏度高,如專利zl200780034519.x,但同樣存在著測定成果高昂、測定所需時間長、抗幹擾能力差等不足之處。
技術實現要素:
本發明為了解決現有過氧化氫測定方法存在的操作複雜繁瑣、測定結果誤差大、測定時間長、反應試劑有毒以及測定成本高昂等問題,提出了一種溶液中過氧化氫含量的快速測定方法。
本發明的一種溶液中過氧化氫含量的快速測定方法,它包括以下步驟:
步驟一:製作標準曲線:將亞鐵離子溶液和n,n-二乙基對苯二胺溶液加入純淨水中得混合溶液a,測定混合溶液a在特定吸收波長處的吸光度值,並校零;分別向混合溶液a中加入不同濃度的過氧化氫標準樣形成混合溶液b,使過氧化氫在混合溶液b中形成濃度梯度;混合溶液b進行氧化顯色反應一段時間後,測定顯色後混合溶液b在所述特定吸收波長處的吸光度值,記為a;以a作為橫坐標,以過氧化氫在混合溶液b中的最終濃度作為縱坐標,建立標準曲線及其線性回歸方程;其中,所述亞鐵離子溶液濃度為5~100mmoll-1,所述n,n-二乙基對苯二胺溶液濃度為10~200mmoll-1;所述亞鐵離子溶液、n,n-二乙基對苯二胺溶液與純淨水的體積比為(0.01~0.2):(0.01~0.2):1;
步驟二:測定樣品中過氧化氫含量:向混合溶液a中加入待測的過氧化氫樣品形成混合溶液b,反應一段時間後,測定顯色後混合溶液b在特定吸收波長處的吸光度值,記為b;將b值代入到步驟一中所得標準曲線的線性回歸方程中,再通過待測過氧化氫樣品與混合溶液b的體積關係計算得出待測樣品中過氧化氫的含量;其中,所述待測過氧化氫樣品與純淨水的體積比為(0.01~0.2):1。
可選的,所述亞鐵離子溶液為高氯酸亞鐵、氯化亞鐵、硝酸亞鐵、硫酸亞鐵和硫酸鐵溶液中一種或多種按任意比例混合。
可選的,所述n,n-二乙基對苯二胺溶液為n,n-二乙基對苯二胺、n,n-二乙基對苯二胺鹽酸鹽和n,n-二乙基對苯二胺硫酸鹽溶液中一種或多種按任意比例混合。
可選的,所述混合溶液a的ph值為2~4。
可選的,所述混合溶液b的氧化顯色反應時間為0.5~5分鐘,反應溫度為0~35℃。
可選的,所述特定吸收波長為510nm或551nm。
本發明包括以下有益效果:
本發明與現有測定方法相比,利用亞鐵離子活化過氧化氫生成羥基自由基快速氧化n,n-二乙基對苯二胺生成紅色自由基來測定過氧化氫含量,即在含有亞鐵離子、過氧化氫以及n,n-二乙基對苯二胺的反應液中,亞鐵離子與過氧化氫首先快速反應生成羥基自由基,然後n,n-二乙基對苯二胺與生成的羥基自由基快速反應生成紅色物質n,n-二乙基對苯二胺自由基,再依據n,n-二乙基對苯二胺自由基的吸光度值來測定過氧化氫含量。亞鐵離子活化過氧化氫生成的羥基自由基氧化還原電位非常高,高達1.8-2.7v,氧化能力非常強,可快速與n,n-二乙基對苯二胺發生定量顯色反應,從而達到快速測定過氧化氫含量的目的。
本發明方法簡單易行,不需要再額外進行紫外輻照、微波輻照、電子束輻照、超聲空化、曝氣、外加電磁場及加熱;與傳統碘量法相比,本發明測定時間由30~45分鐘縮短至僅需0.5分鐘;與高錳酸鉀滴定法相比,本發明具有操作簡便、結果可靠、受其他離子以及有機物影響小的特點;與化學發光法相比,本發明使用的藥劑廉價易獲取、測定時間短;與色譜法相比,本發明使用儀器相對廉價;與基於偶氮染料褪色的紫外-可見分光光度法相比,本發明具有綠色環保的優點,測定過程中投加的fe2+、n,n-二乙基對苯二胺及產物均為對環境友好的化學物質;與利用過氧化氫酶—n,n-二乙基對苯二胺試紙比色法相比,本發明具有實驗藥品廉價、易保存、易配置、易獲取、靈敏度高等特點;與電流分析法相比,本發明具有操作簡便、測試時間短、測試成本低等特點。
此外,本發明不需要昂貴儀器設備及試劑,僅需一臺普通的紫外可見分光光度計即可滿足測定要求,降低了測定成本。本發明方法可廣泛用於環保、日化及醫療行業中,對各種經氧化、漂白或消毒的樣品中過氧化氫含量進行快速、簡單、準確的檢測。
以下結合附圖和實施例對本發明做進一步說明,但本發明不局限於實施例。
附圖說明
圖1為實施例1的標準曲線圖;
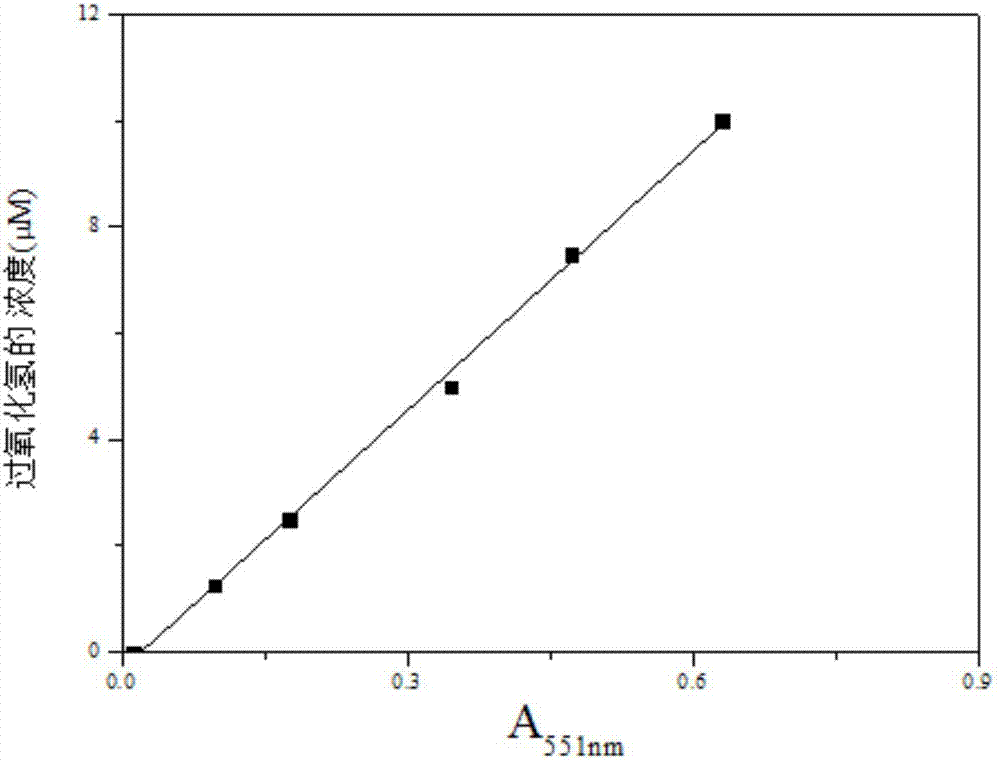
圖2為實施例2的標準曲線圖。
具體實施方式
實施例1:
本實施例的一種溶液中過氧化氫含量的快速測定方法,它是按以下步驟進行:
步驟一:製作標準曲線:
1、將3ml硫酸亞鐵溶液和1mln,n-二乙基對苯二胺硫酸鹽溶液加入5.95ml的蒸餾水中,得混合溶液a,測定混合溶液a在510nm處的吸光度值,並校零;
2、分別向混合溶液a中加入0.05ml不同濃度的過氧化氫溶液標準樣形成混合溶液b,使不同混合溶液b中的過氧化氫形成濃度梯度,反應總體積為10ml;
3、對混合溶液b進行氧化顯色反應0.5分鐘後,測定顯色後混合溶液b在510nm處的吸光度值,記為a;
4、以a作為橫坐標,以過氧化氫在混合溶液b中的最終濃度作為縱坐標,建立標準曲線及其線性回歸方程;
說明:
其中,硫酸亞鐵溶液濃度為20mmoll-1,n,n-二乙基對苯二胺硫酸鹽溶液濃度為75mmoll-1;硫酸亞鐵溶液、n,n-二乙基對苯二胺硫酸鹽溶液與蒸餾水的體積比為0.504:0.168:1;所述的加入過氧化氫形成濃度梯度是指使得過氧化氫在混合溶液b中的最終濃度達到0、1.25、2.5、5、7.5及10μmoll-1。
步驟二:測定樣品中過氧化氫含量:
1、將3.0ml的硫酸亞鐵溶液和1ml的n,n-二乙基對苯二胺硫酸鹽溶液加入到5.95ml的蒸餾水中,得混合溶液a,測定混合溶液a在510nm處的吸光度值,並校零;
2、向混合溶液a中加入0.05ml已知過氧化氫濃度為700μmoll-1的水樣形成混合溶液b,過氧化氫與n,n-二乙基對苯二胺硫酸鹽氧化顯色反應0.5分鐘後,測定顯色後混合溶液b在510nm處的吸光度值,記為b;
3、將b值代入到步驟一中所得標準曲線的線性回歸方程中,計算得出水樣中過氧化氫的含量。
本實施例所得的標準曲線如圖1所示,所得線性回歸公式如下:
[過氧化氫]反應=17.35a510—0.208
因此,水樣中過氧化氫計算公式如下:
[過氧化氫]樣品=v總÷v樣品×[過氧化氫]反應
=10÷0.05×(17.35a510—0.208)
本實施例測得的a510為0.218,代入上述公式中計算得出水樣中過氧化氫含量為714.86μmoll-1,測定偏差為2.12%,說明本測定方法準確可靠。
本實施例利用硫酸亞鐵活化過氧化氫生成羥基自由基快速氧化n,n-二乙基對苯二胺硫酸鹽生成紅色自由基,方法簡單易行,不需要再額外進行紫外輻照、微波輻照、電子束輻照、超聲空化、曝氣、外加電磁場及加熱,測定時間短,測定結果誤差小,投加的硫酸亞鐵、n,n-二乙基對苯二胺硫酸鹽及它們的反應產物均為對環境友好的化學物質,不需要昂貴儀器設備及試劑,僅需一臺普通的紫外可見分光光度計即可滿足測定要求,降低了成本。測定方法可廣泛用於環保、印染及醫療行業中,對各種經氧化、漂白或消毒的樣品中過氧化氫含量進行快速、環保、有效的檢測。
實施例2
本實施例的一種溶液中過氧化氫含量的快速測定方法,它是按以下步驟進行:
步驟一:製作標準曲線:
1、將3ml硫酸亞鐵溶液和1mln,n-二乙基對苯二胺硫酸鹽溶液加入6.95ml的蒸餾水中,得混合溶液a,測定混合溶液a在551nm處的吸光度值,並校零;
2、分別向混合溶液a中加入0.05ml不同濃度的過氧化氫溶液標準樣形成混合溶液b,使不同混合溶液b中的過氧化氫形成濃度梯度,反應總體積為10ml;
3、對混合溶液b進行氧化顯色反應0.5分鐘後,測定顯色後混合溶液b在551nm處的吸光度值,記為a;
4、以a作為橫坐標,以過氧化氫在混合溶液b中的最終濃度作為縱坐標,建立標準曲線及其線性回歸方程;
說明
其中,氯化亞鐵溶液濃度為20mmoll-1,n,n-二乙基對苯二胺鹽酸鹽溶液濃度為250mmoll-1;氯化亞鐵溶液、n,n-二乙基對苯二胺鹽酸鹽溶液與去離子水的體積比為0.504:0.168:1;所述的加入過氧化氫形成濃度梯度是指使得過氧化氫在混合溶液b中的最終濃度達到0、1.25、2.5、5、7.5及10μmoll-1。
步驟二:測定樣品中過氧化氫含量:
1、將3ml硫酸亞鐵溶液和1mln,n-二乙基對苯二胺硫酸鹽溶液加入5.95ml的蒸餾水中,得混合溶液a,測定混合溶液a在551nm處的吸光度值,並校零;
2、向混合溶液a中加入0.05ml已知過氧化氫濃度為950μmoll-1的水樣形成混合溶液b,過氧化氫與n,n-二乙基對苯二胺鹽酸鹽氧化顯色反應0.5分鐘後,測定顯色後混合溶液b在551nm處的吸光度值,記為b;
3、將b值代入到步驟一中所得標準曲線的線性回歸方程中,計算得出水樣中過氧化氫的含量。
本實施例所得的標準曲線如圖2所示,所得線性回歸公式如下:
[過氧化氫]反應=16.28a551—0.322
因此,水樣中過氧化氫計算公式如下:
[過氧化氫]樣品=v總÷v樣品×[過氧化氫]反應
=10÷0.05×(16.28a551—0.322)
本實施例測得的a551為0.314,代入上述公式中計算得出水樣中過氧化氫含量為957.98μmoll-1,測定偏差僅為0.84%,說明本測定方法準確可靠。
本實施例利用氯化亞鐵活化過氧化氫生成羥基自由基快速氧化n,n-二乙基對苯二胺鹽酸鹽生成紅色自由基,方法簡單易行,不需要再額外進行紫外輻照、微波輻照、電子束輻照、超聲空化、曝氣、外加電磁場及加熱,測定時間短,測定結果誤差小,投加的氯化亞鐵、n,n-二乙基對苯二胺鹽酸鹽及它們的反應產物均為對環境友好的化學物質,不需要昂貴儀器設備及試劑,僅需一臺普通的紫外可見分光光度計即可滿足測定要求,降低了成本。本發明方法可廣泛用於環保、日化及醫療行業中,對各種經氧化、漂白或消毒的樣品中過氧化氫含量進行快速而準確的檢測。
本領域普通技術人員可知,本發明的具體參數和組分在下述範圍內變化時,仍能夠得到與上述實施例相同或相近的技術效果:
一種溶液中過氧化氫含量的快速測定方法,它包括以下步驟:
步驟一:製作標準曲線:將亞鐵離子溶液和n,n-二乙基對苯二胺溶液加入純淨水中得混合溶液a,測定混合溶液a在特定吸收波長處的吸光度值,並校零;分別向混合溶液a中加入不同濃度的過氧化氫標準樣形成混合溶液b,使過氧化氫在混合溶液b中形成濃度梯度;混合溶液b進行氧化顯色反應一段時間後,測定顯色後混合溶液b在所述特定吸收波長處的吸光度值,記為a;以a作為橫坐標,以在混合溶液b中的過氧化氫最終濃度作為縱坐標,建立標準曲線及其線性回歸方程;其中,所述亞鐵離子溶液濃度為5~100mmoll-1,所述n,n-二乙基對苯二胺溶液濃度為10~200mmoll-1;所述亞鐵離子溶液、n,n-二乙基對苯二胺溶液與純淨水的體積比為(0.01~0.2):(0.01~0.2):1;
步驟二:測定樣品中過氧化氫含量:向混合溶液a中加入待測的過氧化氫樣品形成混合溶液b,反應一段時間後,測定顯色後混合溶液b在特定吸收波長處的吸光度值,記為b;將b值代入到步驟一中所得標準曲線的線性回歸方程中,再通過待測過氧化氫樣品與混合溶液b的體積關係計算得出待測樣品中過氧化氫的含量;其中,所述待測過氧化氫樣品與純淨水的體積比為(0.01~0.2):1。
其中,所述混合溶液b的氧化顯色反應時間為0.5~5分鐘,反應溫度為0~35℃。所述特定吸收波長為510nm或551nm。所述純淨水均為蒸餾水、去離子水、超純水中的一種或其中幾種按任意體積比的組合。所用比色皿材質為玻璃或石英,比色皿長度為1cm、2cm、3cm、5cm或10cm。
上述實施例僅用來進一步說明本發明的一種溶液中過氧化氫含量的快速測定方法,但本發明並不局限於實施例,凡是依據本發明的技術實質對以上實施例所作的任何簡單修改、等同變化與修飾,均落入本發明技術方案的保護範圍內。
