一種基於微納米技術的彈性薄膜可變電容式的血小板微力傳感器的製作方法
2024-03-30 17:12:05 4
本發明屬於醫療器械技術領域,涉及一種用於快速定性檢測血小板綜合功能的新型微納米即時監測傳感器。
背景技術:
血小板作為人體中最小的細胞,除了在正常的生理性止血上發揮著至關重要的作用,在病理性血栓形成和動脈粥樣硬化過程中也同樣扮演著關鍵的角色。如圖6所示,血小板在皮膚破損後激活的示意,其中:(a)當血管壁上的內皮細胞層未出現破損時,血小板處於未激活狀態;(b)當內皮細胞層出現破損時,血小板被快速激活,粘附到受損部位的細胞外基質上;(c)被激活的血小板會通過改變自身形狀來增大表面積,覆蓋受損的血管壁;(d)被激活的血小板會分泌促凝因子,激活更多的血小板;(e)被激活的眾多血小板鬆散的聚集形成止血栓,達到快速暫時止血的效果;(f)血小板產生收縮力,使鬆散的止血栓變得緊緻,從而起到徹底長期止血的效果。如果產生的收縮力不夠大,血小板在止血過程中所起到的作用是極其有限的,並且鬆弛的止血栓容易從受損的血管壁上脫落,不僅會導致患處重新出血,還會誘發其他部位出現栓塞;相反的,如果血小板收縮力超過正常範圍,處於過度活躍狀態下的血小板會生成過多的止血栓,引發血栓。
越來越多的實驗表明血小板收縮力在定量綜合評估血小板功方面有著巨大的潛力。但是目前世界上對血小板進行功能性檢測與研究依然主要依賴於測量血小板在止血響應過程中的一些中前期指標和止血栓的粘彈性特徵(諸如lta、verifynowp2y12assay、plateletworks、impact-r、pfa100血小板功能分析儀等),缺乏針對血小板在後期時功能發揮的評估,這限制了其在科學研究和臨床診斷中的應用,難以對血小板的綜合功能提供確鑿有力的結論。而且現階段對血小板收縮力的測量依賴於封閉式大尺度的檢測系統,其測量精度低,且無法實時觀測動態亞細胞尺度下血小板的機械交互作用現象。
技術實現要素:
為了實現從微觀角度上對中後期血小板功能表達進行精確測量,本發明提供一種基於微納米技術的彈性薄膜可變電容式的血小板微力傳感器。
一種基於微納米技術的彈性薄膜可變電容式的血小板微力傳感器為平行板可變電容器,包括相互平行的陽極板1和陰極板2,陽極板1位於上方、陰極板2位於下方,且陽極板1的陽極工作面對應著陰極板2的陽極工作面;
所述陽極板1包括板狀的陽極本體11,所述陽極本體11上設有陽極孔,陽極孔的孔底和孔壁上設有陽極材料構成陽極材料區域15,所述陽極材料區域15由桶狀的陽極金膜31和陽極引出測量觸點32組成,所述陽極引出測量觸點32位於陽極本體11的一側面;陽極本體11的另一側面為陽極工作面,陽極工作面上設有有機矽中間體材料層;
陽極孔內陽極金膜的底面上設有人纖維連接蛋白層;
所述陰極板2包括板狀的陰極本體21,與陽極孔的孔底對應的陰極本體21的一側面為陰極工作面,陰極工作面上設有陰極材料區域22,所述陰極材料區域22由陰極金膜41和陰極引出測量觸點42組成;
所述陽極本體11和陰極本體21的材料均為矽片;
所述陽極工作面和陰極工作面之間的間距為10微米-1000微米;
測試時,直接將待檢測的血小板懸浮液滴在陽極板1的陽極孔內桶狀的陽極金膜31上,同時將陽極引出測量觸點32和陰極引出測量觸點42分別接阻抗分析儀的電容檔,根據阻抗分析儀測得的電容值變化率,換算出血小板的凝結能力。
進一步限定的技術方案如下:
所述陽極本體11的厚度和陰極本體21的厚度為400-1000微米。
所述陽極孔的孔徑為50微米~500微米。
所述桶狀的陽極金膜31的底面為向上凸起的圓弧面。
所述陽極金膜31的厚度和陰極金膜41的厚度均為100nm。
所述有機矽中間體材料層14的厚度為10nm,有機矽中間體材料為二甲基矽氧烷(pdms)。
所述人纖維連接蛋白層的厚度為50nm。
陰極金膜41的面積至少大於桶狀的陽極金膜31底部面積的10%。
製備基於微納米技術的彈性薄膜可變電容式的血小板微力傳感器包括陽極板的製作和陰極板的製作兩大工序,具體操作步驟如下:
一、陽極板製作
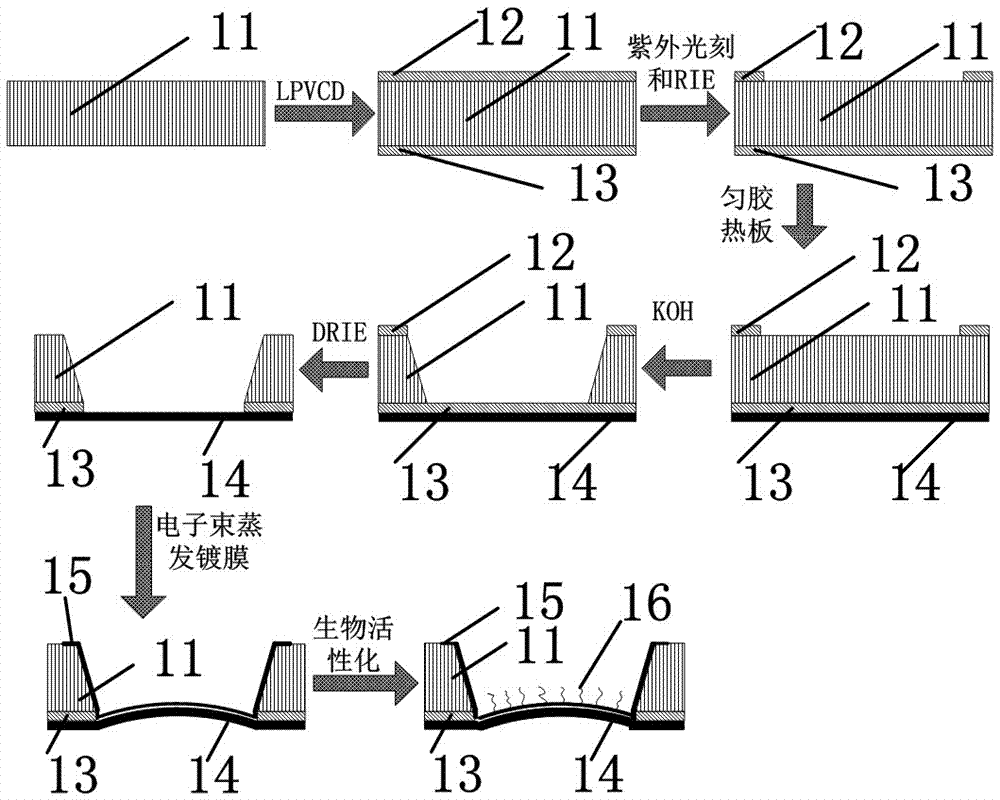
步驟(1):使用低壓化學氣相沉積(lpvcd)方法,在一片雙面拋光的陽極本體11兩側面上分別鍍50nm厚的氮化矽(sin)薄膜,形成上氮化矽薄膜12和下氮化矽薄膜13;
步驟(2):使用標準紫外光刻技術(uvphotolithography)和反應式離子刻蝕技術(reactiveionetching,rie),在上氮化矽薄膜12上蝕刻出若干個直徑為2mm的陽極孔,使陽極本體11暴露出來;
步驟(3):在陽極本體11的下氮化矽薄膜13上用勻膠熱板技術鍍上10um厚的二甲基矽氧烷材料層(pdms)14;
步驟(4):用氫氧化鈉(koh)溼法刻蝕技術蝕刻掉陽極孔內的陽極本體11材料;
步驟(5):為了降低薄膜破損的概率,提高良品率,採用深反應式離子刻蝕技術(deepreactiveionetching,drie)去除上氮化矽薄膜12的剩餘部分和陽極孔內所剩的最後一部分氮化矽13,但是,不貫通二甲基矽氧烷材料層(pdms)14;
步驟(6):通過電子束蒸發鍍膜技術,在陽極孔內鍍上100nm厚度的金膜形成陽極材料區域15,陽極材料區域15由陽極孔內桶狀的陽極金膜31和陽極引出測量觸點32組成,其中陽極引出測量觸點32位於陽極本體11的陽極工作面;
步驟(7):對桶狀的陽極金膜31內的底部表面進行生物活性化處理,塗設人纖維連接蛋白層(humanfibrinogen)16;完成陽極板1製作;
二、陰極板製作
步驟(8):在陰極本體21的陰極工作面上用電子蒸發鍍膜技術,鍍上一層100nm厚度的陰極材料區域22,陰極材料區域22包括陰極金膜41和陰極引出測量觸點42組成;
步驟(9):用勻膠熱板技術在陰極材料區域22上均勻塗覆一層對紫外線敏感的光刻膠層;
步驟(10):用標準紫外光刻技術,在光刻膠層上預定圖形,所述預定圖形與陽極板1上的陽極孔的孔形一致,並在空間上互相對應與對齊;
步驟(11):用王水將未被光刻膠保護的預定圖形以外的金洗除,保留下陰極金膜41和陰極引出測量觸點42;
步驟(12):用光刻膠去除液將覆蓋在下陰極金膜41和陰極引出測量觸點42上的光刻膠去除,完成陰極板2製作;
三、血小板微力傳感器的組裝
將陽極板1的二甲基矽氧烷材料層(pdms)14對應配合位於陰極板2的陰極材料區域22上方,即得到血小板微力傳感器。
本發明的有益技術效果體現在以下方面:
1、本發明將微納米生物微力傳感器和血小板收縮力的研究相結合,旨在快速定量評估血小板的綜合功能。
2、現如今對血小板功能的檢測和血小板生理以及病理性研究都嚴重受制於實驗檢測設備的精度,本發明提出的通過微納米加工工藝製造出的電容式柔性薄膜生物微力傳感器,能實現從微觀上對血小板收縮力進行定量快速的測量,為早期發現血小板功能異常,指導血小板抗凝藥物開發和闡明相關疾病的形成機理,提供必要的技術設備和奠定一定的理論和實驗基礎。
3、本發明的順利開展將為把血小板收縮力作為對血小板功能進行綜合評測的新的臨床標準提供必要的理論依據和實驗結果。
附圖說明
圖1為本發明傳感器結構示意圖。
圖2為傳感器陽極的製作過程示意圖。
圖3為傳感器陽極工作面的俯視圖。
圖4為傳感器陰極工作面的俯視圖。
圖5為本發明測量血小板凝結時收縮力的原理圖。
圖6為血小板在皮膚破損後激活的示意圖。
圖1-5中序號:陽極板1、陰極板2、陽極本體11、上氮化矽薄膜12、下氮化矽薄膜13、二甲基矽氧烷材料層14、陽極材料區域15、人纖維連接蛋白層16、17、18、陽極金膜31、陽極引出測量觸點32、陰極本體21、陰極材料區域22、陰極金膜41、陰極引出測量觸點42。
具體實施方式
下面結合實施例,對本發明作進一步地描述。
參見圖1,一種基於微納米技術的彈性薄膜可變電容式的血小板微力傳感器為平行板可變電容器,包括相互平行的陽極板1和陰極板2,陽極板1位於上方、陰極板2位於下方,且陽極板1的陽極工作面對應著陰極板2的陽極工作面,陽極工作面和陰極工作面之間的間距為500微米。
參見圖1和圖3,陽極板1包括板狀的陽極本體11,陽極本體11上設有陽極孔,陽極孔的孔徑為250微米。陽極孔的孔底和孔壁上設有陽極材料構成的陽極材料區域15;陽極材料區域15由桶狀的陽極金膜31和陽極引出測量觸點32組成,陽極金膜31的底面為向上凸起的圓弧面,陽極金膜31的厚度為100nm。陽極引出測量觸點32位於陽極本體11的一側面;陽極本體11的另一側面為陽極工作面,陽極工作面上設有有機矽中間體材料層14,有機矽中間體材料層14的厚度為10nm,有機矽中間體材料為二甲基矽氧烷(pdms)。
陽極孔內陽極金膜的底面上設有人纖維連接蛋白層16,人纖維連接蛋白層16的厚度為50nm。
參見圖1和圖4,陰極板2包括板狀的陰極本體21,與陽極孔的孔底對應的陰極本體21的一側面為陰極工作面,陰極工作面上設有陰極材料區域22,陰極材料區域22由陰極金膜41和陰極引出測量觸點42組成,陰極金膜41的厚度為100nm,陰極金膜41的面積至少大於桶狀的陽極金膜31底部面積的10%。
陽極本體11和陰極本體21的材料均為矽片,厚度為800微米。
製備基於微納米技術的彈性薄膜可變電容式的血小板微力傳感器包括陽極板的製作和陰極板的製作兩大工序,具體操作步驟如下:
一、陽極板製作
參見圖2,製作陽極板的操作如下:
步驟(1):使用低壓化學氣相沉積(lpvcd)方法,在一片雙面拋光的陽極本體11兩側面上分別鍍50nm厚的氮化矽(sin)薄膜,形成上氮化矽薄膜12和下氮化矽薄膜13。
步驟(2):使用標準紫外光刻技術(uvphotolithography)和反應式離子刻蝕技術(reactiveionetching,rie),在上氮化矽薄膜12上蝕刻出若干個直徑為250微米的陽極孔,使陽極本體11暴露出來。
步驟(3):在陽極本體11的下氮化矽薄膜13上用勻膠熱板技術鍍上10um厚的二甲基矽氧烷材料層(pdms)14。
步驟(4):用氫氧化鈉(koh)溼法刻蝕技術蝕刻掉陽極孔內的陽極本體11材料。
步驟(5):為了降低薄膜破損的概率,提高良品率,採用深反應式離子刻蝕技術(deepreactiveionetching,drie)去除上氮化矽薄膜12的剩餘部分和陽極孔內所剩的最後一部分氮化矽13,但是,不貫通二甲基矽氧烷材料層(pdms)14。
步驟(6):通過電子束蒸發鍍膜技術,在陽極孔內鍍上100nm厚度的金膜形成陽極材料區域15,陽極材料區域15由陽極孔內桶狀的陽極金膜31和陽極引出測量觸點32組成,其中陽極引出測量觸點32位於陽極本體11的陽極工作面。
步驟(7):對桶狀的陽極金膜31內的底部表面進行生物活性化處理,塗設厚度50nm的人纖維連接蛋白層(humanfibrinogen)16;完成陽極板1製作。
二、陰極板製作
步驟(8):在陰極本體21的陰極工作面上用電子蒸發鍍膜技術,鍍上一層100nm厚度的陰極材料區域22,陰極材料區域22包括陰極金膜41和陰極引出測量觸點42組成。
步驟(9):用勻膠熱板技術在陰極材料區域22上均勻塗覆一層對紫外線敏感的光刻膠層。
步驟(10):用標準紫外光刻技術,在光刻膠層上預定圖形,所述預定圖形與陽極板1上的陽極孔的孔形一致,並在空間上互相對應與對齊。
步驟(11):用王水將未被光刻膠保護的預定圖形以外的金洗除,保留下陰極金膜41和陰極引出測量觸點42。
步驟(12):用光刻膠去除液將覆蓋在下陰極金膜41和陰極引出測量觸點42上的光刻膠去除,完成陰極板2製作。
三、血小板微力傳感器的組裝
將陽極板1的二甲基矽氧烷材料層(pdms)14對應配合位於陰極板2的陰極材料區域22上方,得到血小板微力傳感器,並放置在亞克力材料的支架上。
本發明的典型應用如下
用於檢測時,由一對血小板微力傳感器同時使用,一個對生物微力進行測量,另外一個則被用作參考,這樣可以最大限度的降低實驗環境噪音對生物微力測量精度的影響。整個實驗過程參見圖5,本發明血小板微力傳感器測量血小板凝結時收縮力的原理,其中:圖5(a)為一個電容的示意圖;由於是微納米加工,實際操作中一個矽片上是加工多個微納米傳感器電容的,圖5(b)為1個矽片上2個相鄰的傳感器電容的示意圖;圖5(c)為血小板懸浮液滴入一個傳感器電容的示意圖。
具體測試時,先將血小板懸浮液滴在陽極孔的人纖維連接蛋白層16上,測量此時傳感器電容陽極和陰極間的電容值。然後將凝血劑滴入血小板懸浮液滴上,等血小板懸浮液滴完全凝固後,由於血小板的收縮力,陽極孔底部的二甲基矽氧烷材料層14會向上進一步凸起,此時再次通過陽極板1的陽極引出測量觸點32和陰極板2的陰極引出測量觸點42測量傳感器電容陽極和陰極間的電容值。根據兩次測量的電容差值變化的大小,可以測量出血小板凝血收縮能力的大小。
