培養基及其用途與誘導多能幹細胞向間充質幹細胞轉化的方法與流程
2024-03-27 22:25:05 3
本發明涉及幹細胞及基因工程技術領域,尤其涉及培養基及其用途與間充質幹細胞的製備方法。
背景技術:
隨著組織工程及臨床移植醫學的興起,種子細胞的研究越來越受關注。間充質幹細胞(msc,mesenchymalstemcells)是一類存在於多種組織(如骨髓、臍帶血和臍帶組織、胎盤組織、脂肪組織等)的多能幹細胞。其具有高度增殖、自我更新的能力,且具有多向分化的潛能。可在不同誘導條件下分化為軟骨、骨、骨骼肌、肌腱、脂肪、真皮、神經及腎實質的細胞等。因此,間充質幹細胞常被作為種子細胞。
間充質幹細胞的臨床研究已經在許多國家開展,美國批准了60餘項臨床試驗,隨著間充質幹細胞及其相關技術的日益成熟,我國也批准了多項臨床試驗,走入了間充質幹細胞核心技術研發的舞臺。目前,臨床試驗證實,mscs抑制可用於組織修復及治療間充質組織遺傳缺陷性疾病,例如:血液系統疾病,心血管疾病,肝硬化,神經系統疾病,膝關節半月板部分切除損傷修復,自身免疫性疾病等。間充質幹細胞的特性決定其具有良好的臨床應用前景。
目前,間充質幹細胞的主要來源是骨髓和臍帶組織,骨髓間充質幹細胞隨著年齡的老化,幹細胞數目顯著降低、增殖分化能力大幅度衰退,製備過程不容易質控,移植給異體可能引起免疫反應且對人體傷害較大。臍帶間充質幹細胞雖免疫性較低但是臍帶血的保存比較昂貴。而其他組織來源的幹細胞的數量則非常的稀少,分離和培養也十分的困難。因此,進一步研究間充質幹細胞的製備方法仍是目前該領域研究的熱點。
技術實現要素:
有鑑於此,本發明要解決的技術問題在於提供培養基及其用途與間充質幹細胞的製備方法。本發明提供的培養基能夠將尿液細胞重新編程為ips細胞,再將ips細胞誘導為擬胚體然後定向分化為間充質幹細胞。
本發明提供的間充質幹細胞誘導培養基包括基礎培養基和:
一些實施例中,間充質幹細胞誘導培養基由基礎培養基和以下組分組成:
fbs是胎牛血清;bfgf為鹼性成纖維細胞生長因子;scf為幹細胞因子。本發明中,在基礎培養基中添加fbs、l-穀氨醯胺、胰島素、bfgf和scf,該培養基能夠誘導ips細胞向間充質幹細胞轉化。所述基礎培養基為dmem培養基。
本發明還提供了一種誘導ips細胞轉化為間充質幹細胞的方法,將ips細胞以mtesr培養基培養至融合度為60%~80%時,更換培養基為間充質幹細胞誘導培養基,誘導5~7天獲得間充質幹細胞。
一些實施例中,誘導條件為37℃,飽和溼度,5%co2。所述誘導在以明膠包被的培養板中進行。所述培養過程中每天更換新鮮培養基。
實驗表明,以該方法誘導ips細胞,5~7d細胞發生形變。
一種由尿液細胞製備間充質幹細胞的方法,包括以下步驟:
將轉錄調控因子oct4、sox2、nanog、klf4和lin28導入尿液細胞,培養獲得ips細胞;
將ips細胞以mtesr培養基培養至融合度為60%~80%時,更換培養基為間充質幹細胞誘導培養基,誘導5~7天獲得間充質幹細胞。
一些實施例中,誘導條件為37℃,飽和溼度,5%co2。所述誘導在以明膠包被的培養板中進行。所述培養過程中每天更換新鮮培養基。
本發明中,獲得間充質幹細胞後還包括增殖、傳代的步驟,所述增殖、傳代採用間充質幹細胞培養基;
所述間充質幹細胞培養基包括基礎培養基和:
一些實施例中,間充質幹細胞由基礎培養基和以下組分組成:
hgf是肝細胞生長因子、pdgf為血小板衍生因子,tgf-β為轉化生長因子-β。本發明將fbs、egf、hgf、bfgf、pdgf和tgf-β添加入基礎培養基,所得培養基能夠用於間充質幹細胞的培養。所述基礎培養基為dmem培養基。
本發明中,尿液細胞的製備方法為:離心尿液,沉澱經滅菌後,以含有primocin的regm培養基培養,獲得尿液細胞。
本發明中,尿液細胞的具體製備方法為:
步驟1:在含有青黴素/鏈黴素雙抗的容器中收集尿液,400g離心10min,沉澱以含有青黴素/鏈黴素的pbs(每95mlpbs加入5ml青黴素/鏈黴素)清洗一次後,轉移至經0.1%明膠包被的培養板;
步驟2:含有primocin的regm培養基(每2mlregm培養基添加3μlprimocin)培養,培養條件為37℃,飽和溼度,5%co2;待細胞貼壁後,吸去培養基,用pbs洗一遍,再進行換液處理;當尿液細胞融合度達到80%,進行傳代培養。
所述轉錄調控因子oct4、sox2、nanog、klf4和lin28導入尿液細胞後,細胞以regm與mef的混合培養基(體積比1:1)在用明膠包被後的培養板上進行培養;導入轉錄調控因子後第2天,將培養基更換為ips培養基mtesr,每天更換新鮮培養基,使克隆繼續增殖;導入轉錄調控因子後第7天,鏡下觀察形態與人胚胎幹細胞相近的挑取單克隆,並接種於用明膠包被的培養板,培養基mtesr培養獲得誘導多能幹細胞(ips細胞)。
ips細胞用0.03%-0.3%膠原酶iv將細胞消化成單個細胞後,再誘導形成間充質幹細胞。
rt-pcr檢測間充質幹細胞中基因表達情況,naong和oct-4在間充質幹細胞中的表達量幾乎不表達,說明誘導的間充質幹細胞喪失了多能幹性基因的表達,間充質幹細胞屬於中胚層msx-1是中胚層基因在間充質幹細胞中的表達量顯著增高,符合間充質幹細胞的特徵。免疫螢光檢測製得的間充質幹細胞,結果顯示波型蛋白表達為陽性而巢蛋白表達為陰性,這與間充質幹細胞表達中胚層標vimentin,而不表達外胚層標誌nestin的結果相符合。
本發明提供了培養基以及使用該培養基誘導尿液細胞成為間充質幹細胞的方法,尿液細胞來源廣泛,不受倫理限制,採用本發明提供的方法,尿液細胞形成ips細胞後經誘導形成間充質幹細胞。全部誘導能夠在12~15天內完成,所獲得的細胞經檢測符合間充質幹細胞的特性,數量較大,活率較高。
附圖說明
圖1示實施例1製備間充質幹細胞的表面標記抗原檢測情況;
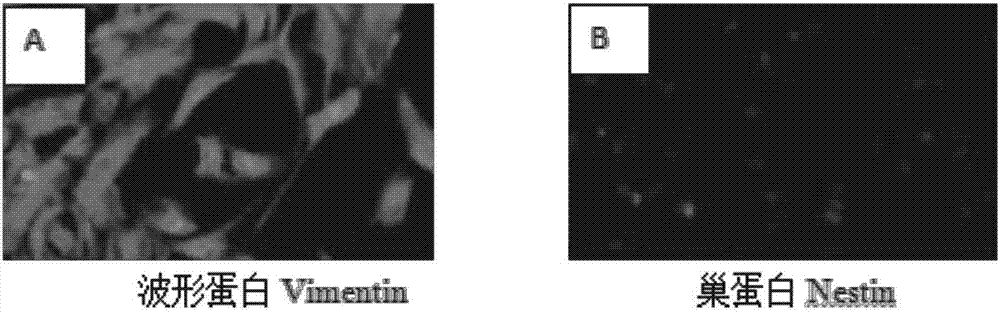
圖2示實施例1製備間充質幹細胞的免疫螢光檢測情況。
具體實施方式
本發明提供了培養基及其用途與間充質幹細胞的製備方法,本領域技術人員可以借鑑本文內容,適當改進工藝參數實現。特別需要指出的是,所有類似的替換和改動對本領域技術人員來說是顯而易見的,它們都被視為包括在本發明。本發明的方法及應用已經通過較佳實施例進行了描述,相關人員明顯能在不脫離本發明內容、精神和範圍內對本文的方法和應用進行改動或適當變更與組合,來實現和應用本發明技術。
本發明採用的試材皆為普通市售品,皆可於市場購得。
下面結合實施例,進一步闡述本發明:
實施例1
1、培養基的製備
ips誘導培養基(配置培養基a):regm與mef培養基按體積比的比例混合。
間充質幹細胞誘導培養基(配置培養基b):450mldmem基礎培養基、50mlfbs、80pm胰島素、5mml-穀氨醯胺、85ug/lbfgf、15ug/lscf、3×10-8mol/l地塞米松。
間充質幹細胞培養基(配置培養基c):450mldmem基礎培養基、50mlfbs、10ng/mlhegf、10ng/mlbfgf、3ng/mlhgf、5ng/mlpdgf、5ng/mltgf-β。
2、尿液細胞的獲取
1)收集杯每個加2ml青黴素/鏈黴素雙抗。
2)收集尿液,如不立刻進行後續操作,則將尿液存儲於4℃冰箱並於當天完成後續操作。
3)每份尿液準備六孔板1孔,將此孔用0.1%明膠包被20min以上,使用前吸去孔內液體。
4)把尿液倒到合適數量的50ml離心管裡,離心400g,10min。
5)吸去上清,每管留下約1-5ml,混合到一個離心管內。
6)加入含有青黴素/鏈黴素的pbs(pbs95ml加入5ml青黴素/鏈黴素混勻)約10-30ml。輕輕混勻。
7)離心400g,10min。
8)吸去上清至剩餘0.5-1ml液體。
9)把剩餘的液體加入包被好的孔中,加入2mlregm培養基加入3μlprimocin。
10)將培養皿放置於37℃培養箱內培養,待尿液細胞貼壁後(7天),吸去培養基,用pbs洗一遍,再進行換液處理。
11)當尿液細胞融合度達到80%,則可進行傳代培養。
3、尿液細胞重編程為ips細胞
1)將表達轉錄調控因子oct4、sox2、nanog、klf4和lin28或其它轉錄因子的各種組合共同導入尿細胞,將細胞分至預先用matrigel包被的6孔板中,用培養液a培養;
2)轉染後第2天,將培養基更換為ips培養基mtesr,每天更換新鮮培養基;使克隆繼續增殖
3)轉染後第7天,鏡下觀察形態與人胚胎幹細胞相近的挑取單克隆,並接種於用matrigel包被的12孔板中,培養基mtesr培養獲得誘導多能幹細胞。
4、ips誘導間充質幹細胞
1)將製備好的ips細胞,0.25%的胰酶進行消化,收集細胞按1:3的比例接種至matrigel包被好六孔板中,mtesr培養基進行培養。
2)待六孔板中的ips細胞融合度達到70%時,pbs清洗將ips培養基清除乾淨,加入培養液b進行誘導培養,每天更換培養液。
3)培養5-7d細胞發生形變,更換培養液c進行培養。
實施例2
1、培養基的製備
ips誘導培養基(配置培養基a):regm與mef培養基按體積比的比例混合。
間充質幹細胞誘導培養基(配置培養基b):450mldmem基礎培養基、50mlfbs、1pm胰島素、1mml-穀氨醯胺、50ug/lbfgf、5ug/lscf、2×10-8mol/l地塞米松。
間充質幹細胞培養基(配置培養基c):450mldmem基礎培養基、50mlfbs、1ng/mlhegf、1ng/mlbfgf、1ng/mlhgf、、2ng/mlpdgf、1ng/mltgf-β。
2、尿液細胞的獲取
1)收集杯每個加2ml青黴素/鏈黴素雙抗。
2)收集尿液,如不立刻進行後續操作,則將尿液存儲於4℃冰箱並於當天完成後續操作。
3)每份尿液準備六孔板1孔,將此孔用0.1%明膠包被20min以上,使用前吸去孔內液體。
4)把尿液倒到合適數量的50ml離心管裡,離心400g,10min。
5)吸去上清,每管留下約1-5ml,混合到一個離心管內。
6)加入含有青黴素/鏈黴素的pbs(pbs95ml加入5ml青黴素/鏈黴素混勻)約10-30ml。輕輕混勻。
7)離心400g,10min。
8)吸去上清至剩餘0.5-1ml液體。
9)把剩餘的液體加入包被好的孔中,加入2mlregm培養基加入3μlprimocin。
10)將培養皿放置於37℃培養箱內培養,待尿液細胞貼壁後(7天),吸去培養基,用pbs洗一遍,再進行換液處理。
11)當尿液細胞融合度達到80%,則可進行傳代培養。
3、尿液細胞重編程為ips細胞
1)將表達轉錄調控因子oct4、sox2、nanog、klf4和lin28或其它轉錄因子的各種組合共同導入尿細胞,將細胞分至預先用matrigel包被的6孔板中,用培養液a培養;
2)轉染後第2天,將培養基更換為ips培養基mtesr,每天更換新鮮培養基;使克隆繼續增殖
3)轉染後第7天,鏡下觀察形態與人胚胎幹細胞相近的挑取單克隆,並接種於用matrigel包被的12孔板中,培養基mtesr培養獲得誘導多能幹細胞。
4、ips誘導間充質幹細胞
1)將製備好的ips細胞,0.25%的胰酶進行消化,收集細胞按1:3的比例接種至matrigel包被好六孔板中,mtesr培養基進行培養。
2)待六孔板中的ips細胞融合度達到70%時,pbs清洗將ips培養基清除乾淨,加入培養液b進行誘導培養,每天更換培養液。
3)培養5-7d細胞發生形變,更換培養液c進行培養。
實施例3
1、培養基的製備
ips誘導培養基(配置培養基a):regm與mef培養基按體積比的比例混合。
間充質幹細胞誘導培養基(配置培養基b):450mldmem基礎培養基、50mlfbs、160pm胰島素、10mml-穀氨醯胺、200ug/lbfgf、50ug/lscf、5×10-8mol/l地塞米松。
間充質幹細胞培養基(配置培養基c):450mldmem基礎培養基、50mlfbs、100ng/mlhegf、100ng/mlbfgf、50ng/mlhgf、、20ng/mlpdgf、25ng/mltgf-β。
2、尿液細胞的獲取
1)收集杯每個加2ml青黴素/鏈黴素雙抗。
2)收集尿液,如不立刻進行後續操作,則將尿液存儲於4℃冰箱並於當天完成後續操作。
3)每份尿液準備六孔板1孔,將此孔用0.1%明膠包被20min以上,使用前吸去孔內液體。
4)把尿液倒到合適數量的50ml離心管裡,離心400g,10min。
5)吸去上清,每管留下約1-5ml,混合到一個離心管內。
6)加入含有青黴素/鏈黴素的pbs(pbs95ml加入5ml青黴素/鏈黴素混勻)約10-30ml。輕輕混勻。
7)離心400g,10min。
8)吸去上清至剩餘0.5-1ml液體。
9)把剩餘的液體加入包被好的孔中,加入2mlregm培養基加入3μlprimocin。
10)將培養皿放置於37℃培養箱內培養,待尿液細胞貼壁後(7天),吸去培養基,用pbs洗一遍,再進行換液處理。
11)當尿液細胞融合度達到80%,則可進行傳代培養。
3、尿液細胞重編程為ips細胞
1)將表達轉錄調控因子oct4、sox2、nanog、klf4和lin28或其它轉錄因子的各種組合共同導入尿細胞,將細胞分至預先用matrigel包被的6孔板中,用培養液a培養;
2)轉染後第2天,將培養基更換為ips培養基mtesr,每天更換新鮮培養基;使克隆繼續增殖
3)轉染後第7天,鏡下觀察形態與人胚胎幹細胞相近的挑取單克隆,並接種於用matrigel包被的12孔板中,培養基mtesr培養獲得誘導多能幹細胞。
4、ips誘導間充質幹細胞
1)將製備好的ips細胞,0.25%的胰酶進行消化,收集細胞按1:3的比例接種至matrigel包被好六孔板中,mtesr培養基進行培養。
2)待六孔板中的ips細胞融合度達到70%時,pbs清洗將ips培養基清除乾淨,加入培養液b進行誘導培養,每天更換培養液。
3)培養5-7d細胞發生形變,更換培養液c進行培養。
實施例4
對實施例1~3製得的間充質幹細胞進行檢測:
1、流式細胞術表面抗原檢測
實驗步驟
①將各實施例備好的間充質幹細胞待其融合度達到80%時,0.25%胰酶消化間充質幹細胞並收集細胞,使其細胞數為2×105個/每例樣本;
②細胞胞重懸於1mldpbs中洗滌2次,200g,離心5min;
每管樣本加入1ml70%預冷的酒精重懸固定2h;
③離心棄去固定液,加入200μl鼠源cd29、cd44、cd73、cd90、cd105、cd34、cd45一抗抗體(稀釋度為1:100)常溫下孵育30min;
④1mlpbs洗滌後,分別與fitc標記二抗(稀釋度為1:200)常溫避光孵育1h;
⑤pbs洗兩次後,棄去,根據細胞量加入適量的pbs重懸細胞,利用流式細胞儀檢測。
通過流式細胞儀分析顯示,在實施例1~3製得的間充質幹細胞中cd29、cd44、cd73、cd90、cd105表達為陽性,而cd34、cd45表達為陰性,符合間充質幹細胞表面標記物的表達結果。圖2示對實施例1製得間充質幹細胞表面標記抗原的檢測結果。實施例2~3製得幹細胞的檢測結果與此相似。
2、免疫螢光檢測間充質幹細胞
①0.25%胰酶消化成纖維細胞,以1×105的接種量接種於放有細胞爬片的6孔板中,待其貼壁,4%的多聚甲醛固定2h,pbs洗三遍;
②加200μl的一抗稀釋液(pbs+10%血清+0.3%tritonx-100)常溫封閉1-2h;
③棄去一抗稀釋液,分別加入200μl鼠源vimentin和nestin一抗抗體(稀釋濃度為1:100),4℃孵育過夜,pbs衝洗三次3次,每次5min;
④分別加200μl羊抗鼠二抗(1:400),常溫避光反應1h,dapi復染,10%的甘油封片,螢光顯微鏡下觀察。結果見圖2。
結果表明,實施例1~3製得的間充質幹細胞中,波型蛋白表達為陽性而巢蛋白表達為陰性,這與間充質幹細胞表達中胚層標vimentin,而不表達外胚層標誌nestin的結果相符合。其中,對實施例1製得間充質幹細胞的檢測結果如圖1。實施例2~3製得幹細胞的檢測結果與此相似。
3、細胞活力檢測
採用mtt法對各實施例製得細胞的活率進行檢測,結果表明,實施例1~3製得間充質幹細胞的活力依次為95%、65%、55%,其中實施例1製得的幹細胞的活力顯著高於實施例2~3(p<0.05)
以上僅是本發明的優選實施方式,應當指出,對於本技術領域的普通技術人員來說,在不脫離本發明原理的前提下,還可以做出若干改進和潤飾,這些改進和潤飾也應視為本發明的保護範圍。
