一種針對細胞的雷射導向微流控晶片的製作方法
2023-06-08 21:11:52 2
本實用新型涉及生物醫學技術,具體是利用雷射的光阱力側向推動細胞來改變細胞的運動軌跡的微流控晶片。
背景技術:
早在20世紀初期,生物學、醫學領域的科研人員已經開始進行細胞培養等工作。為了能更直觀地觀察細胞在生物體內的活動情況,人們開始在更開放的環境下模擬體內細胞所需的生活環境。微流控晶片的出現與發展促進了體外仿真的研究進程,由於微流控晶片具有高精度、高通量以及可塑造性強的特點,可以根據情況用不同工藝和材料製造出應用於不同領域的微流控晶片。
近年來,由於人們對循環腫瘤細胞的關注,對循環腫瘤細胞的分選的需求也在日益增加,在科研與臨床應用中需要高通量和高分選率。雖然現有的幾種方法分離效率高,但從製作工藝上來看比較複雜,或是需要對樣品進行預處理,從而或多或少汙染了樣品。
近年來國內通過光壓、光學鑷子等手段來微觀操作細胞成為研究熱點。李銀妹等人和張文靜等人實現了用光學鑷子捕獲、操縱和分離細胞,並研究了不同液體中黏滯係數對其的影響;趙恩銘和劉志海已經實現了對聚苯乙烯顆粒和酵母細胞的捕獲和彈射等作用,並探究了光阱力對不同尺寸微粒的力學作用。但利用精密微移平臺通過光鑷在垂直於晶片方向移動細胞效率不高,不適用於高通量的細胞篩選;用大功率雷射捕獲與彈射需要大功率雷射器,還可能影響細胞活性。還未實現在微流控晶片中利用微小的側向光阱力來改變細胞軌跡。
技術實現要素:
針對現有技術不足,本實用新型擬解決的技術問題是,提供一種可以使目標細胞運動軌跡發生偏轉的微流控晶片,引入嵌入光纖可以降低對雷射功率的要求,而且實際操作中簡化操作步驟(不用現場建立光路),相對於之前發表在《微納電子技術》上論文中所述晶片結構,此次使用兼容性更好的多模光纖,並且根據仿真與實際情況對通道進行了結構優化,加入了光纖嵌入位置,便於操作。該晶片具有通量高,無標記,適於實際應用等特點。
本實用新型的技術方案是,
一種針對細胞的雷射導向微流控晶片,該晶片包括十字通道、上部廢液通道、1號細胞收集通道、2號細胞收集通道、下部廢液通道、上廢液池、1號細胞收集器、2號細胞收集器、下廢液池和光纖;
所述的十字通道的上通道和下通道連接,作為緩衝液通道;十字通道的前通道為細胞液通道,十字通道的後通道作為主通道,主通道的末端分離形成四個射線狀連接的分支通道,其中,四個分支通道由上到下依次為上部廢液通道、1號細胞收集通道、2號細胞收集通道、下部廢液通道,每個通道之間夾角為30°,其中,2號細胞收集通道處於主通道的水平延長段;光纖垂直嵌入主通道末端之前的80um處下部;
上部廢液通道的末端為上廢液池、1號細胞收集通道的末端為1號細胞收集器、2號細胞收集通道的末端為2號細胞收集器、下部廢液通道的末端為下廢液池;
所述的十字通道、上部廢液通道、1號細胞收集通道、2號細胞收集通道、下部廢液通道材質均為聚二甲基矽氧烷。
所述的十字通道、上部廢液通道、1號細胞收集通道、2號細胞收集通道、下部廢液通道的內部通道寬度相等,通道厚度相等。
所述的十字通道、上部廢液通道、1號細胞收集通道、2號細胞收集通道、下部廢液通道的內部通道寬度均為100μm,通道厚度均為100μm。
與現有技術相比,本實用新型的微流控晶片結構設計巧妙,功能明確,便於加工,工作效率或篩選效率可達幾個-幾十個/秒,大幅提高,而且不需要採用任何試劑標註目標細胞,真正實現了無標記、高通量的細胞篩選現代醫學要求。
附圖說明
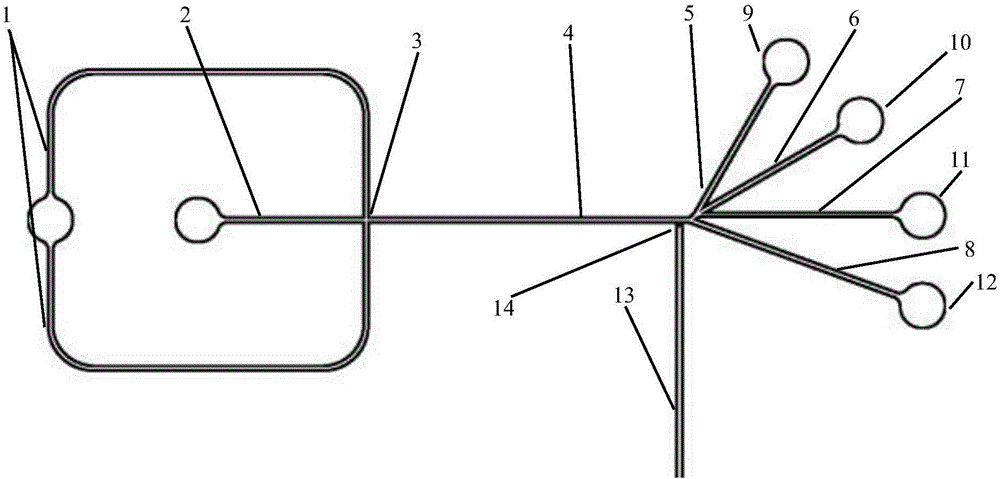
圖1為本實用新型晶片結構示意圖。
具體實施方式
下面結合實施例及其附圖進一步描述本實用新型。
本實驗所需微流控晶片結構設計為圖1所示,其中包括了最常用的十字型通道作為鞘流結構,並且創新了獨特的多分支通道結構,便於細胞的篩選和分類。該晶片包括:緩衝液通道(1)、細胞液通道(2)、十字通道(3)、主通道(4)、上部廢液通道(5)、1號細胞收集通道(6)、2號細胞收集通道(7)、下部廢液通道(8)、上廢液池(9)、1號細胞收集器(10)、2號細胞收集器(11)、下廢液池(12)和光纖(14);其十字通道(3)(包括主通道(4))上部廢液通道(5)、1號細胞收集通道(6)、2號細胞收集通道(7)、下部廢液通道(8)的設計寬度相等,製作時通道厚度也相等;
所述的十字通道(3)的上通道和下通道連接,作為緩衝液通道;十字通道(3)的前通道(2)為細胞液通道,十字通道的後通道(4)作為主通道,主通道的末端分離形成四個射線狀連接的分支通道,共屬同一節點,其中,四個分支通道由上到下依次為上部廢液通道(5)、1號細胞收集通道(6)、2號細胞收集通道(7)、下部廢液通道(8),每個通道之間夾角為30°,其中,2號細胞收集通道(7)處於主通道(4)的水平延長段;光纖垂直嵌入主通道末端之前的80um處;
上部廢液通道(5)的末端為上廢液池(9)、1號細胞收集通道(6)的末端為1號細胞收集器(10)、2號細胞收集通道(7)的末端為2號細胞收集器(11)、下部廢液通道(8)的末端為下廢液池(12)。
實施例1
本實用新型中,所述的十字通道(3)的上通道和下通道連接(呈方形),作為緩衝液通道;十字通道(3)的前通道(2)為細胞液通道,十字通道的後通道(4)作為主通道(主通道長24mm),主通道的末端分離形成四個射線狀連接的分支通道,即1號細胞收集通道(6)、2號細胞收集通道(7)、上部廢液通道(5)和下部廢液通道(8)左端共同接入主通道(4)的尾端,其中2號細胞收集通道(7)處於主通道(4)的水平延長段,並且1號細胞收集通道(6)、2號細胞收集通道(7)、上部廢液通道(5)和下部廢液通道(8)的直徑與主通道(4)直徑相等,均為100μm,通道厚度也均為100μm,每個通道之間夾角為30°,以上四個通路的尾端分別對應1號細胞收集器(10)、2號細胞收集器(11)、上廢液池(9)和下廢液池(12)。為了能在微流控晶片中嵌入光纖,本實驗採用聚二甲基矽氧烷(PDMS)作為晶片的主要製作材料,即十字通道(3)、上部廢液通道(5)、1號細胞收集通道(6)、2號細胞收集通道(7)、下部廢液通道(8)材質均為聚二甲基矽氧烷。在模板上對應位置(13)預留光纖(14)大小(光纖直徑125um)的通道(光纖垂直嵌入主通道末端之前的80um處),使其端面垂直對準分岔路前端通道處。然後插入光纖後用PDMS注入光纖與通道之間的縫隙中,並用矽膠加固光纖與微流控晶片接口處使光纖與晶片形成整體。本實用新型晶片的工作原理及過程是:十字通道(3)更容易使從緩衝液通道(1)和細胞液通道(2)注入的緩衝液和被緩衝液包裹著的細胞液匯聚形成鞘流,並且通過控制進樣器的流速來控制緩衝液通道(1)的流速和壓力,保證細胞可以在主通道(4)裡形成單細胞流,並且沿著流線的方向進入光纖嵌入位置(13)受到通過光纖的雷射的照射,由於不同細胞不同的細胞膜和細胞質,所以對於不同波長、功率的雷射照射下所受到的力也不同,從而實現對不同種類、大小的細胞進行篩選,通過調節功率使得軸向光阱力可以產生0-40μm的橫向偏移量,足以將細胞分離到不同的通道中。經過細胞篩選的細胞進入最終的細胞1號收集通道(6)和2號細胞收集通道(7),完成具有高通量、無標記的細胞篩選過程。
本實用新型未述及之處適用於現有技術。
