一種鐵基硫化物電極材料、製備方法以及在固態電池中的應用與流程
2023-12-03 08:20:21 3
本發明屬於鋰二次電池技術領域,涉及一種鐵基硫化物電極材料、製備方法與其在固態電池中的應用。
背景技術:
鋰離子電池由於具有能量密度高、放電電壓高、循環壽命長和無記憶效應等優點,已經在消費電子和通訊等領域得到廣泛的應用,未來在混合電動汽車和規模化儲能領域具有廣闊的發展前景。但是,傳統鋰離子電池通常採用有機電解液作為鋰離子導電介質,存在易燃、易腐蝕和熱穩定性差等安全性問題,使得鋰離子電池的應用受到限制。同時,金屬鋰在液態電池中會與液體電解質發生一系列的副反應,例如金屬鋰表面直接接觸電解液會發生化學發應,而在金屬鋰表面生成一層不均勻的固體電解質膜。而在充放電過程中由於電流密度分布不均勻,會導致金屬鋰表面的固體電解質膜出現裂紋甚至脫落的情況,金屬鋰負極不斷溶解。此外,鋰枝晶的生長會造成隔膜刺穿,最終導致電池短路而失效。
固態電池採用無機固體電解質或者聚合物電解質取代傳統鋰離子電池中的有機電解液,具有更高的安全性能和熱穩定性能,被認為是徹底解決鋰離子電池安全性問題的終極方案。目前研究最多的無機固體電解質包括硫化物固體電解質和氧化物固體電解質兩大類。無機固體電解質材料具有較高的室溫離子電導率和機械強度,電化學窗口寬,熱穩定性好。而聚合物固體電解質主要是以聚環氧乙烷為基體的材料體系。這類材料的高溫離子電導率較高,易成膜,機械加工性能好。採用固體電解質製成的全固態鋰電池安全性能明顯優於液態電池,有效解決了有機電解液在使用過程中出現的洩露、燃燒和爆炸的危險。另一方面,固態電解質高的機械強度能有效抑制鋰枝晶的生長,且沒有界面副反應,循環穩定性和安全性能得到顯著提高。同時也使得金屬鋰作為負極材料應用於電池中成為可能,進一步提高電池的能量密度。
目前廣泛使用的正極材料多為含鋰過渡金屬氧化物和磷酸鹽電極(LiCoO2,LiMn2O4,LiNiO2,LiFePO4),這類材料具有高的工作電壓和循環穩定性,但是理論比容量通常較低,提高電池的能量密度的能力有限。硫基和過渡金屬硫化物電極儘管工作電壓較低,但是其理論比容量很高,有助於提高電池的能量密度。固態電池中,如何降低界面電阻是提高電池循環穩定性,充分發揮正極容量的關鍵所在。採用過渡金屬硫化物作為正極材料在充放電過程中通常伴有顯著地體積變化,這可能會導致電極粉化或者電極與電解質接觸界面出現接觸不良的情況。微觀形貌為片狀的過渡金屬硫化物電極材料能夠緩解循環過程中的內應力,抑制體積變化效應而導致的電極結構的破壞。同時,二維片狀結構具有較大的比表面積,能夠增加電極與固體電解質的接觸面積,降低界面接觸電阻,增加電化學反應的活性位點。薄的納米片也有助於縮短鋰離子和電子的傳輸距離,提高電化學反應動力學。
鐵基硫化物電極因為原料便宜且儲量豐富,同時環境友好、比容量高具有良好的研究前景。目前,通常採用工藝複雜且耗時的溶劑熱和水熱法合成具有一定微觀形貌的過渡金屬硫化物電極材料。因此,開發簡單省時的合成方法獲得具有特定形貌的鐵基硫化物電極材料至關重要。
技術實現要素:
本發明提供了一種鐵基硫化物電極材料,此鐵基硫化物電極材料能提高固態電池的電化學性能,一方面是由於鐵基硫化物具有較高的理論比容量和適中的工作電壓,應用於固態鋰電池中能夠提高固態電池的能量密度;另一方面本申請中鐵基硫化物電極材料微觀形貌為二維片狀結構,能夠增加電極與固體電解質的接觸面積,降低界面接觸電阻,同時納米片結構能夠有效縮短鋰離子傳輸距離,提高電化學反應動力學,從而提高固態電池的電化學性能。因此,本申請製備的鐵基硫化物電極材料具有較好的循環性能。
本發明又提供一種鐵基硫化物電極材料的製備方法,本申請提供的鐵基硫化物電極材料製備方法可提高固態電池的性能,具體的,通過合成二維片狀的活性物質,增加其與電解質以及導電添加劑的接觸面積,降低界面接觸電阻的同時緩解循環過程中的體積效應,最終提高固態電池的能量密度和循環穩定性。
本申請提供了一種鐵基硫化物電極材料的製備方法,包括以下步驟:
A)將亞鐵鹽溶液加入到聚乙烯醇水溶液中,攪拌獲得混合溶液;在惰性氣氛保護下,將上述混合溶液硫化鈉水溶液攪拌混合,反應後得到黑色沉澱。
B)將黑色沉澱離心洗滌後乾燥,獲得最後的鐵基硫化物電極材料。
優選的,所述製備原料的水溶液,亞鐵鹽的濃度為1wt%~80wt%;聚乙烯醇水溶液的濃度為0.01wt%~30%;硫酸鈉水溶液的濃度為1wt%~80wt%。
優選的,所述混合攪拌溫度為0~100℃,所述攪拌時間為0.001~10h。
優選的,所述乾燥選擇冷凍乾燥或者80℃真空乾燥,所述乾燥時間為12~36h。
優選的,所述選擇的亞鐵鹽為FeSO4·7H2O和FeCl2·4H2O的一種或多種。
本申請還提供了一種固態電池,包括上述方案所述的製備方法所製備的鐵基硫化物電極材料。
本申請提供了一種鐵基硫化物電極材料的製備方法,其包括以下步驟:將亞鐵鹽溶液加入到聚乙烯醇水溶液中,攪拌獲得混合溶液。在惰性氣氛保護下,將上述混合溶液與硫化鈉水溶液攪拌混合,反應後得到黑色沉澱。將黑色沉澱離心洗滌後乾燥,獲得最後的鐵基硫化物電極材料。本申請採用聚乙烯醇輔助共沉澱法獲得鐵基硫化物電極材料,在將亞鐵鹽溶液與聚乙烯醇水溶液混合的過程中,亞鐵離子與聚乙烯醇發生絡合反應,在與硫化鈉水溶液共沉澱的過程中,聚乙烯醇長鏈不僅能夠使共沉澱反應緩慢進行,還能有效控制沉澱的形貌。最終獲得具有由納米片組成的納米花結構的鐵基硫化物電極材料。二維片狀結構的電極材料有助於提高電極與固體電解質的接觸,縮短鋰離子和電子的傳輸距離。
本申請中鐵基硫化物電極材料能夠提高固態電池的電化學性能,一方面是由於鐵基硫化物具有較高的理論比容量和適中的工作電壓,應用於固態電池中能夠提高固態電池的能量密度;另一方面本申請中鐵基硫化物電極材料微觀形貌為二維片狀結構,能夠增加電極與固體電解質的接觸面積,同時緩解循環過程中的體積效應,提高固態電池的循環穩定性;因此,本申請製備的鐵基硫化物電極材料具有較好的循環性能。
附圖說明
圖1為本發明實施例1製備的鐵基硫化物電極材料的掃描電子顯微鏡照片。
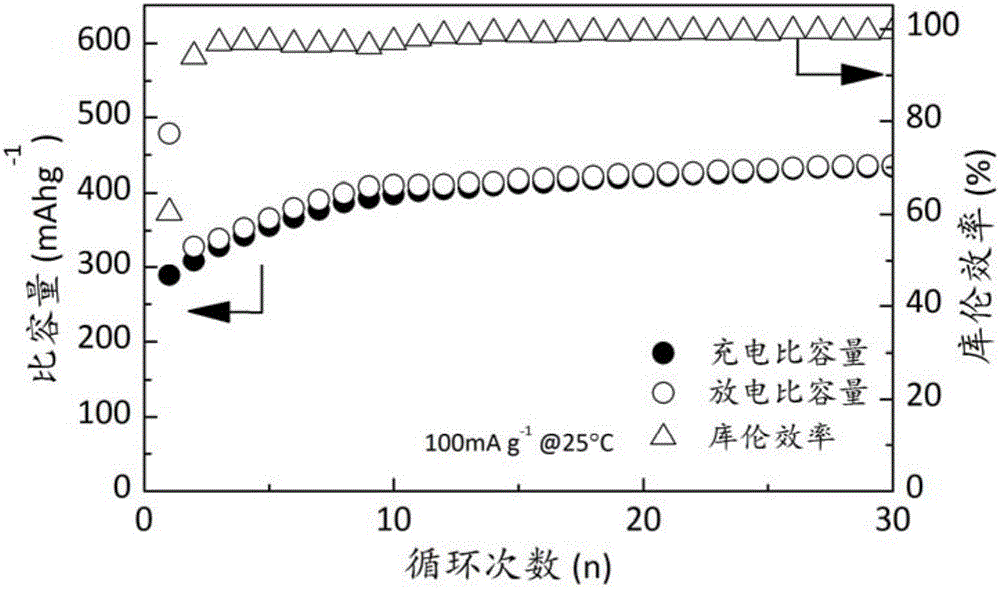
圖2為本發明實施例1製備的鐵基硫化物電極材料應用於固態電池的循環性能測試圖。
具體實施方式
為了進一步理解本發明,下面結合實施例對本發明優選實施方案進行描述,但是應當理解,這些描述只是為進一步說明本發明的特徵和優點,而不是對本發明權利要求的限制。
本發明實施例公開了一種複合聚合物電解質的製備方法,包括以下步驟:
A)將亞鐵鹽溶液加入到聚乙烯醇水溶液中,攪拌獲得混合溶液;在惰性氣氛保護下,將上述混合溶液硫化鈉水溶液攪拌混合,反應後得到黑色沉澱;
B)將黑色沉澱離心洗滌後乾燥,獲得最後的鐵基硫化物電極材料;
本申請採用聚乙烯醇輔助共沉澱的方法製備了鐵基硫化物電極材料,即本發明採用共沉澱製備的方法獲得具有由納米片組成的納米花結構且循環穩定性好的鐵基硫化物電極材料。本申請提供的鐵基硫化物電極材料的製備方法,使鐵基硫化物納米片自組裝成納米花微觀結構,有助於緩解體積效應,同時增加電極與固體電解質的接觸面積,提高固態電池整體性能。
在本發明中,首先進行了亞鐵鹽溶液與聚乙烯醇水溶液的混合,攪拌發生絡合反應。然後將上述混合溶液與硫化鈉水溶液混合,攪拌反應一段時間後,離心洗滌,乾燥得到最後的產物。
在上述製備混合溶液的過程中,所述亞鐵鹽為本領域技術人員熟知的,對此本申請沒有特別的限制,示例的,本申請所述亞鐵鹽優選為FeSO4·7H2O、FeCl2·4H2O中的一種或多種,在實施例中,所述聚合物基體更優選為FeSO4·7H2O。本申請所述聚乙烯醇的優選為牌號為聚乙烯醇2499、聚乙烯醇1799、聚乙烯醇1788和聚乙烯醇1750四種。本申請所述聚乙烯醇是作為絡合劑,其與亞鐵離子進行配位絡合形成Fe2+-聚乙烯醇,然後與S2-混合發生共沉澱反應生成具有一定納米形貌的鐵基硫化物電極材料。
所述混合攪拌溫度優選為0~100℃,所述攪拌時間為0.001~10h。最優為1.0h。所述乾燥選擇冷凍乾燥或者80℃真空乾燥,所述乾燥時間優選為12~36h。在實施例中更優選為18~32h,最優選為24h。所述攪拌溫度過高,Fe2+極易被氧化為Fe3+,產生雜質;
本申請製備的鐵基硫化物電極材料中,Fe2+與聚乙烯醇鏈發生絡合反應,能夠有效控制反應速率和產物形貌,二維納米片結構的鐵基硫化物電極材料能緩解體積效應,增加電極與固體電解質的接觸面積,縮短鋰離子傳輸距離。
本申請還提供了一種固態電池,其包括上述方案所述的製備方法所製備的鐵基硫化物電極材料。
本申請製備的鐵基硫化物電極材料作為固態電池的正極,由於鐵基硫化物電極具有較好的電子導電性和特殊的納米結構,而使鋰二次電池具有較好的倍率性能與循環穩定性。
為了進一步理解本發明,下面結合實施例對本發明提供的鐵基硫化物電極材料的製備方法進行詳細說明,本發明的保護範圍不受以下實施例的限制。
實施例1
FeSO4·7H2O水溶液加入到濃度為1.0wt%、牌號為聚乙烯醇1750的水溶液中,室溫攪拌0.5h後,獲得混合溶液;隨後在氬氣氣氛保護下,將混合溶液加入到濃度為20wt%的Na2S·9H2O水溶液中,室溫反應0.5h,離心洗滌黑色沉澱,冷凍乾燥24h後獲得鐵基硫化物電極材料。微觀形貌為二維納米片狀的鐵基硫化物電極材料如圖1所示。
以Li10GeP2S12-75Li2S·25P2S5·1%P2O5雙層固態電解質作為導電介質,金屬鋰作為對電極組裝成固態電池,在室溫條件下進行電化學性能測試。圖2中曲線為實施例1製備的鐵基硫化物電極材料的循環性能,由圖2可知,在室溫下,此電極應用於固態電池中具有較好的循環性能,在1000mA/g電流密度下循環30次後,可逆容量仍保持436mAh/g左右。
實施例2
FeSO4·7H2O水溶液加入到濃度為0.5wt%、牌號為聚乙烯醇1799的水溶液中,室溫攪拌0.5h後,獲得混合溶液;隨後在氬氣氣氛保護下,將混合溶液加入到濃度為5wt%的Na2S·9H2O水溶液中,室溫反應0.5h,離心洗滌黑色沉澱,80℃下真空乾燥24h後獲得鐵基硫化物電極材料。微觀形貌為二維納米片狀的鐵基硫化物電極材料。
以Li10GeP2S12-70Li2S·30P2S5雙層固態電解質作為導電介質,金屬鋰作為對電極組裝成固態電池,在室溫條件下進行電化學性能測試。應用實施例2製備的鐵基硫化物電極材料組裝固態電池,在800mA/g電流密度下循環30次後,可逆容量仍保持在423mAh/g左右。
實施例3
FeCl2·4H2O水溶液加入到濃度為3.0wt%、牌號為聚乙烯醇1788的水溶液中,室溫攪拌0.5h後,獲得混合溶液;隨後在氬氣氣氛保護下,將混合溶液加入到濃度為20wt%的Na2S·9H2O水溶液中,室溫反應0.5h,離心洗滌黑色沉澱,冷凍乾燥後獲得鐵基硫化物電極材料。微觀形貌為納米片自組裝成的納米花結構。
以Li10GeP2S12-80Li2S·20P2S5雙層固態電解質作為導電介質,金屬鋰作為對電極組裝成固態電池,在室溫條件下進行電化學性能測試。應用實施例3製備的鐵基硫化物電極材料組裝固態電池,在500mA/g電流密度下循環30次後,可逆容量仍保持在352mAh/g左右。
對比例1
在氬氣氣氛保護下,FeSO4·7H2O水溶液加入到濃度為20wt%的Na2S·9H2O水溶液中,室溫反應0.5h,離心洗滌黑色沉澱,冷凍乾燥24h後獲得鐵基硫化物電極材料,微觀形貌為納米顆粒團聚而成的二次顆粒。
以Li10GeP2S12-75Li2S·25P2S5·1%P2O5雙層固態電解質作為導電介質,金屬鋰作為對電極組裝成固態電池,在室溫條件下進行電化學性能測試。1000mA/g電流密度下充放電循,可逆容量只有264mAh/g左右。這主要是因為納米顆粒團聚導致活性物質與固體電解質接觸面積減小,界面電阻升高。且循環過程中較大的體積膨脹導致電極被破壞,循環穩定性降低。
對比例2
在氬氣氣氛保護下,FeSO4·7H2O水溶液加入到濃度為20wt%的Na2S·9H2O水溶液中,室溫反應0.5h,離心洗滌黑色沉澱,80℃下真空乾燥24h後獲得鐵基硫化物電極材料。微觀形貌為微米級顆粒狀。
以Li10GeP2S12-70Li2S·30P2S5雙層固態電解質作為導電介質,金屬鋰作為對電極組裝成固態電池,在室溫條件下進行電化學性能測試。在室溫下,此電極應用於固態電池中,800mA/g電流密度下充放電循環30次後,可逆容量只有282mAh/g。
對比例3
FeCl3·6H2O(0.5mmol),Na2S·9H2O(2mmol)和S(2mmol)溶解在30mL去離子水中形成均勻的水溶液。然後10mL乙二胺緩慢加入到不斷攪拌的上述混合溶液中,隨後轉移到水熱反應釜中,加熱到160℃保溫12h。當溫度自然冷卻至室溫後,經過去離子水和無水乙醇超聲清洗後60℃乾燥5h獲得前驅體。將前驅體置於真空爐中加熱到250℃保溫2h獲得FeS。
以有機電解液作為導電介質,金屬鋰作為對電極組裝成半電池,在室溫條件下進行電化學性能測試。1000mA/g電流密度下充放電循環30次後,可逆容量只有257mAh/g。其循環性能明顯低於固態電池。且採用有機電解液才在漏液、燃燒和爆炸的安全隱患。
對比例4
2g FeSO4·7H2O和0.216g蔗糖溶於7.5mL的去離子水中形成混合溶液,3.45g的Na2S·9H2O溶於7.5mL去離子水中,然後將上述兩種溶液在15mL的無水乙醇中分散均勻得到懸濁液。最後將上述混合溶液轉移到水熱反應釜中加熱到180℃保溫18h。當溫度自然冷卻至室溫後,經去離子水和無水乙醇洗滌後乾燥獲得最終產物FeS。
以有機電解液作為導電介質,金屬鋰作為對電極組裝成半電池,在室溫條件下進行電化學性能測試,發現其可逆容量衰減嚴重。在室溫下,此電極應用於固態電池中,500mA/g電流密度下充放電循環30次後可逆容量只有243mAh/g。
對所公開的實施例的上述說明,使本領域專業技術人員能夠實現或使用本發明。對這些實施例的多種修改對本領域的專業技術人員來說將是顯而易見的,本文中所定義的一般原理可以在不脫離本發明的精神或範圍的情況下,在其它實施例中實現。因此,本發明將不會被限制於本文所示的這些實施例,而是要符合與本文所公開的原理和新穎特點相一致的最寬的範圍。
