一系列基於萊啉基化合物的水溶性聚合物的製備及其作為光熱試劑在生物醫學的應用的製作方法
2023-11-06 13:00:02 5
本發明屬於光熱試劑技術領域,特別涉及一系列基於萊啉基化合物的水溶性聚合物的製備及其作為光熱試劑在生物醫學的應用。本發明是通過在萊啉基化合物的醯亞胺位和「海灣位」的化學修飾得到可用作光熱試劑的基於萊啉基化合物的水溶性聚合物。
背景技術:
腫瘤已經成為危害人類健康最主要的疾病之一。現階段癌症的治療手段主要集中在外科手術、化療以及放療:外科手術是快捷的治療手段,但是由於腫瘤細胞活性沒有抑制以及病灶處的物理摘除不徹底,往往伴隨著高復發,無法治癒的隱患;化療和放療在一定程度上可以有效地抑制癌細胞的活性及復發,通常也伴隨著人體正常組織的損傷以及人體免疫機能的下降。利用近紅外光的生物組織穿透限制小的特點,近紅外雷射誘導熱療的腫瘤治療方法正在興起。單純的雷射誘導熱療的方式,並不能達到有效的治療,反而引起腫瘤的爆發式的復發。光熱試劑在均勻的分散到組織深處後,接受定向雷射的輻射,不僅可以使光能高效地轉化為熱能,而且能將熱能帶入深層腫瘤組織,達到治療的目的。但是無論是已經商業化的試劑,還是已經研究報導過的光熱試劑,比如:icg衍生物,卟啉及其衍生物等,都不能穩定的維持高效的光熱轉化過程。因此,發明一種穩定的高轉化效率的光熱試劑,從而達到光診療一體的作用,對於生物學、醫學研究具有重要的學術及臨床轉化意義。
由於本身穩定的化學結構,萊啉類化合物具有穩定高效地螢光發射,並且作為優異的能量轉化材料在光電、雷射列印以及生物檢測染色等領域表現了很高的光、熱以及化學穩定性。但是由於萊啉類未修飾時,具有強烈的疏水性,所以如果將此高性能的材料引入到生物領域用於光熱治療,第一個亟待解決的問題就是水溶性及生物相容性。
隨著光熱治療在臨床的逐漸興起,克服不穩定性,低效的新型光熱試劑的設計研發是急需解決的問題。延長共軛度的萊啉類化合物繼承了萊啉染料家族的高穩定性,並且可以隨著共軛度增加,光熱轉化效率隨之增加的性質。開發一系列基於萊啉基化合物,具有高穩定性和高光熱轉化效率的的光熱試劑,用於癌症及其他疾病的光聲成像和光熱治療,具有良好的臨床前景。
技術實現要素:
本發明提供了一系列基於萊啉基化合物的水溶性聚合物的製備方法,製備了一系列拓展共軛度後的萊啉染料核修飾水溶性聚合物及其衍生物,並且驗證了所得到的萊啉基水溶性聚合物及其衍生物的水溶液能穩定地保持高光熱轉化效率的特點,在細胞水平以及小鼠水平驗證了這一系列聚合物作為光熱試劑展開光聲成像和光熱治療方法。
本發明所述的一系列基於萊啉基化合物的水溶性聚合物,其由萊啉基化合物和一系列水溶性聚合物及其衍生物反應得到;所述的萊啉基化合物的結構式如(i),
其中,m為重複單元數,取值範圍1-4。
所述的r』為支化或未支化且具有保護性或者活化性的化學基團,選自苯衍生物基、醯胺、酯鍵、羥基、硫醇、羧基、滷素、胺類、不飽和烯烴、不飽和炔烴或醚中的任意至少一種。
所述的r2=-h或
x是n、o或者s原子中的任意一種;
r3為支化的反應基團;
r4是未支化的反應基團。
所述的r3含有的官能基團是具有保護性或者活化性的化學基團,所述的官能基團選自苯衍生物基、醯胺、酯鍵、羥基、硫醇、羧基、滷素、胺類、不飽和烯烴、不飽和炔烴、醚或多肽中的任意至少一種。
所述的r4含有的官能基團是具有保護性或者活化性的化學基團,所述的官能基團選自醯胺、酯鍵、羥基、硫醇、羧基、滷素、胺類、不飽和烯烴、不飽和炔烴、醚或多肽中的任意至少一種。
優選的,萊啉基化合物和(甲基)丙烯酸酯類及其衍生物、己內酯或丙交酯通過活性可控聚合反應atrp或開環聚合反應raft得到基於萊啉基化合物的水溶性聚合物。
優選的,萊啉基化合物和聚乙二醇或胺基酸類化合物通過酯化反應或醯胺化反應得到含有水溶性側基的基於萊啉基化合物的水溶性聚合物。
將上述得到的基於萊啉基化合物的水溶性聚合物用作光熱試劑。該光熱試劑可應用於腫瘤,心血管類等疾病。
本發明將萊啉基化合物用作製備萊啉基水溶性聚合物的聚合反應的引發劑,或者用作製備大分子的反應劑,其修飾水溶性聚合物及其衍生物後(例如丙烯酸或者聚乙二醇衍生物),萊啉基化合物表現出完美的水溶性,克服了苯環骨架強烈的疏水性,得到了一系列具有水溶性聚合物或大分子。延長共軛度後的萊啉基化合物可以高效地吸收近紅外光能並且快速轉化為熱能的性質,並進一步實現了目標產物在細胞(體外)、小鼠(體內)活體水平的光聲成像和光熱治療應用。這一系列光熱試劑分子具有高生物相容性並且表現了對臟器及血液的低毒性。分子外圍水溶性聚合物能將光熱分子攜帶進入腫瘤組織深處,在定向雷射的輻射下,能高效地使腫瘤局部升溫,不影響正常組織的新陳代謝活動,達到安全高效的熱療目的,並且對其他正常組織沒有明顯的熱傷害。
本發明具有如下的有益效果:
1.本發明設計合成的一系列萊啉基水溶性聚合物及其衍生物具有優異的水溶性,克服了共軛延展度增大帶來的水溶性難度。
2.本發明設計合成的一系列萊啉基水溶性聚合物及其衍生物的水溶液具有穩定的光熱轉化效果,能有效的將吸收的光能轉化為熱能。
3.本發明設計合成的一系列萊啉基水溶性聚合物及其衍生物的細胞培養基溶液可以在雷射輻射條件下快速地產生熱效應殺死癌細胞。
4.本發明設計合成的一系列萊啉基水溶性聚合物及其衍生物在小鼠水平可以達到高對比度的光聲成像效果。
5.本發明設計合成的一系列萊啉基水溶性聚合物及其衍生物可以快速(12小時內)無痛治癒負瘤小鼠,愈後恢復快且無復發。
附圖說明
圖1為本發明中基於共軛度延展後的基於萊啉基化合物的水溶性聚合物具有光熱效果的主骨架結構。
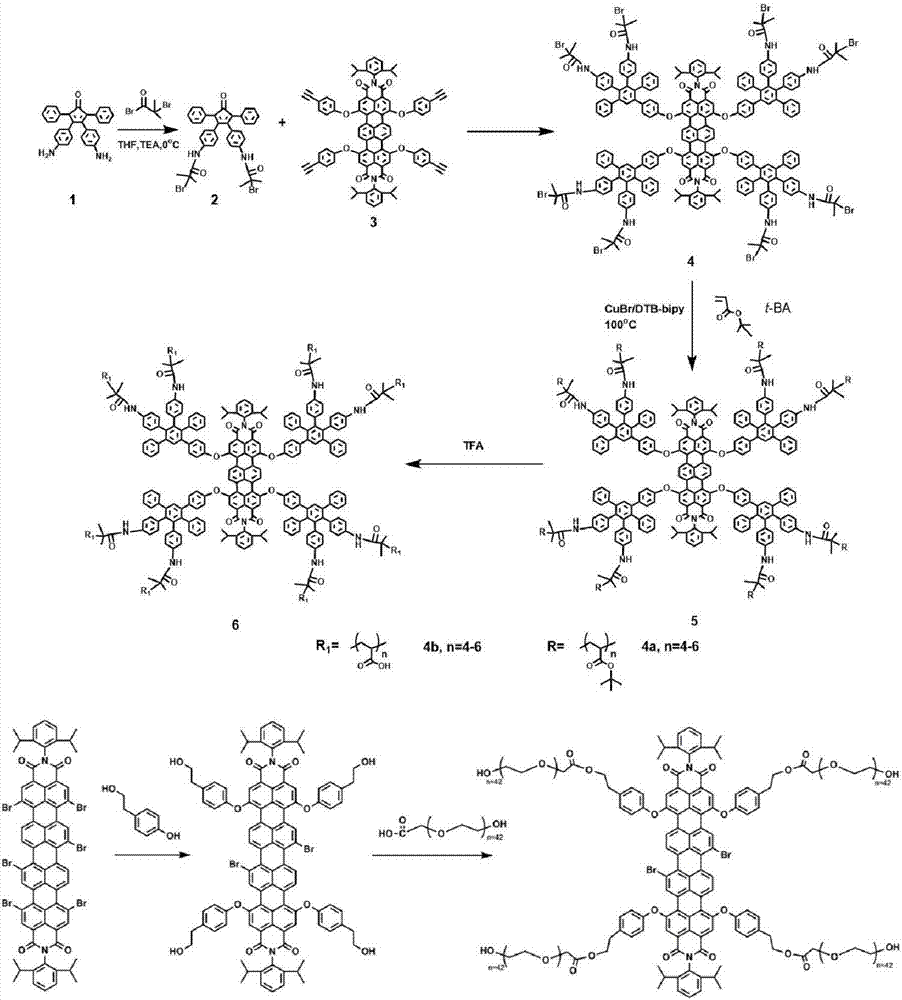
圖2製備一系列共軛度延展的基於萊啉基化合物的水溶性聚合物(實施例1中目標產物tdi-paa和實施例2中目標產物qdi-peg)的合成路徑。
圖3為實施例1中中間產物引發劑的核磁譜圖。
圖4為本系列新型光熱試劑水溶液在可見光-近紅外光譜區域的吸收表徵。
圖5為實施例1中目標產物tdi-paa不同濃度的水溶液在660nm雷射照射下的升溫曲線。
圖6為實施例1中目標產物tdi-paa不同濃度的細胞培養基溶液,在660nm雷射照射下對癌細胞(4t1和mcf-7)的殺傷效果圖。
圖7為實施例1中目標產物tdi-paa不同濃度的水溶液的光聲信號,符合線性規律。
圖8為實施例1中目標產物tdi-paa在小鼠腫瘤處的光聲成像效果圖,隨著注射後時間的推移,藥物在腫瘤處富集呈現上升再下降趨勢,並通過光聲信號得以檢測。
圖9為實施例1中目標產物tdi-paa進行光熱治療後小鼠腫瘤的變化趨勢,可以看出治療組的腫瘤呈現快速消退,且無復發的變化規律。(對照組條件是pbs,只有藥物tnms,只有雷射照射)。
圖10為實施例2中中間產物qdi-4oh的質譜譜圖。
圖11為實施例2中最終產物qdi-peg的核磁譜圖。
圖12為實施例2中最終產物qdi-peg的質譜譜圖。
圖13為實施例2中目標產物qdi-peg不同濃度的水溶液在660nm雷射照射下的升溫曲線。
圖14為實施例2中目標產物qdi-peg不同濃度的細胞培養基溶液,在660nm雷射照射下對癌細胞(4t1、mcf-7和hela細胞)的殺傷效果圖。
圖15為實施例2中目標產物qdi-peg不同濃度的水溶液的光聲信號,符合線性規律。
圖16為實施例2中目標產物qdi-peg在小鼠腫瘤處的光聲成像效果圖,隨著注射後時間的推移,藥物在腫瘤處富集呈現上升再下降趨勢,並通過光聲信號得以檢測。
圖17為實施例2中目標產物qdi-peg進行光熱治療後小鼠腫瘤的變化趨勢,可以看出治療組的腫瘤呈現快速消退,且無復發的變化規律。(對照組條件是pbs,只有藥物qdi-peg,只有雷射照射)。
圖18是本發明提供的萊啉基化合物的結構式及用途示例。
具體實施方式
下面將通過實施例並且結合附圖對本發明進行進一步詳細的描述,但實施例並不用於限制本發明的保護範圍。
實施例1
1.將2-溴異丁醯溴(1.5g,7.92mmol)和氨基苯撐(1.0g,2.41mmol)加入0℃反應瓶中,50ml四氫呋喃作為溶劑,7ml三乙胺為縛酸劑,逐漸恢復室溫,攪拌反應4-10h;反應結束後,除去溶劑,柱狀層析法(二氯甲烷)分離產物得到中間產物標記為cp-nhcoc(ch3)2br:
1h-nmr譜:(250mhz,cd2cl2,303k):δ(ppm)=8.38(s,2h,nh),7.43-7.40(d,2h,aromatich),7.26-7.24(m,10h,aromatich),6.96-6.92(d,2h,aromatich),2.01(s,6h;ch3);
13c-nmr譜(75mhz,cd2cl2,303k):δ(ppm)=200.4,170.6,154.5,138.8,131.8,131.1,130.9,128.8,128.2,126.3,119.7,63.3,32.9.
fd-massspectra(8kv):m/z[%]:713(100%)calcd.forc37h32br2n2o3(712.49).
2.將步驟1)的產物nhcoc(ch3)2br(271mg,0.38mmol)和tdi-4al(50mg,0.038mmol)同時加入微波反應管,溶劑鄰二甲苯5ml,反應溫度設置為150-200℃,反應結束後用柱狀層析法(二氯甲烷)分離產物得到tdi引發劑標記為tdi-initiator:
ms(maldi-tof):m/z(%)=4038([m+h]+);(calcdfor:4037.41).
1h-nmr(300mhz,cd2cl2,300k):δppm;9.42(s,4h),8.22-8.18(s,nh,12h),7.55-6.85(m,142h),2.68(m,4h,ch),1.97(s,24h,ch3),1.96(s,24h,ch3),1.13(d,j=6.6hz,24h,ch3);
13c-nmr(75mhz,cd2cl2):δppm;170.1,163.5,154.8,154.6,146.5,142.0,141.5,140.3,140.2,139.9,139.3,138.5,137.2,136.8,135.8,131.5,129.8,129.2,126.5,123.4,122.5,119.3,63.1,31.9,29.5,24.2.
3.用步驟2)的產物作為atrp引發劑,引發丙烯酸叔丁酯單體,(cubr和dtb-bipy作為催化劑),氮氣保護環境,反應溫度85℃,通過核磁監控聚合度,得到最終中間產物tdi-p(t-ba),在三氟乙酸條件下得到最終產物樹枝狀大分子tdi-paa:
實施例2
1.將qdi-6br(60mg,0.042mmol)與對乙羥基苯酚(30mg,0.22mmol)加入到含有k2co3和nmp溶劑的反應瓶中115℃反應48h,反應結束,除去nmp,在正己烷中沉澱後,柱狀層析法(二氯甲烷)分離產物得到中間產物標記為qdi-4oh;
2.將步驟1)產物qdi-4oh(50mg,0.03mmol)和分子量2000的peg-cooh(240mg)混合在二氯甲烷中,在hobt和dic體系中常溫反應60h以上;冰乙醚中沉澱得到最終產物qdi-peg;
應用實施例1
取實施例1中所合成的tdi-paa溶於細胞培養基中,配置成濃度為不同濃度的溶液,和癌細胞共培育5小時,隨後用既定功率的雷射(1w/cm2)輻射5min,隨後用cck-8方法檢測這個過程中癌細胞的存活率,結果如圖6所示。
應用實施例2
小鼠體內光聲信號測試實驗:用pbs水溶液配置實施例1中所合成的tdi-paa的溶液(0.5mm),然後通過小鼠尾靜脈注射,進入小鼠血液循環系統。通過光聲儀器(msot系統)檢測光聲信號以及處理為光聲照片,結果如圖8所示。
應用實施例3
小鼠水平上光熱治療腫瘤實驗:用pbs水溶液配置實施例1中所合成的tdi-paa的溶液(15g/kg),然後通過小鼠尾靜脈注射,光熱試劑富集在腫瘤組織內部後,通過雷射定向的照射,造成腫瘤部位的高溫以及接下來的消散。並對接下來腫瘤的體積進行了檢測。
應用實施例4
取實施例2中所合成的qdi-peg溶於細胞培養基中,配置成濃度為不同濃度的溶液,和癌細胞共培育5小時,隨後用既定功率的雷射(1w/cm2)輻射5min,隨後用cck-8方法檢測這個過程中癌細胞的存活率,結果如圖14所示。
應用實施例5
小鼠體內光聲信號測試實驗:用pbs水溶液配置實施例2中所合成的qdi-peg的溶液(0.5mm),然後通過小鼠尾靜脈注射,進入小鼠血液循環系統。通過光聲儀器(msot系統)檢測光聲信號以及處理為光聲照片,結果如圖16所示。
應用實施例6
小鼠水平上光熱治療腫瘤實驗:用pbs水溶液配置實施例2中所合成的tdi-paa的溶液(10g/kg),然後通過小鼠尾靜脈注射,光熱試劑富集在腫瘤組織內部後,通過雷射定向的照射,造成腫瘤部位的高溫以及接下來的消散。並對接下來腫瘤的體積進行了檢測,結果如圖17所示。
綜上所述,本發明公開了一系列基於萊啉基化合物的水溶性聚合物及其衍生物製備及其在腫瘤光聲成像和光熱治療的醫學應用。本發明在萊啉基化合物的外圍,通過引入極性多支化或線型聚合物,使得疏水苯環骨架的水溶性大大提高,從而獲得一系列具有水溶性、功能性的螢光大分子。基於萊啉基化合物吸收光能高效地轉化為熱能的性質,實現了目標產物在小鼠活體水平的光聲成像和光熱治療應用。一系列萊啉基光熱試劑具有高生物相容性並且表現了對臟器及血液的低毒性。分子外圍水溶性聚合物能將光熱分子攜帶進入腫瘤組織深處,在定向雷射的輻射下,能高效地使腫瘤局部升溫,達到高效地熱療目的,並且對其他正常組織沒有明顯的熱傷害。結合前期的研究,這系列光熱試劑有希望實現臨床轉化,達到腫瘤以及其他疾病(如心血管類,皮膚類,腸胃類疾病)領域的應用。
雖然,上文中已經用一般性說明及具體實施方案對本發明作了詳盡的描述,但在本發明基礎上,可以對之作一些修改或改進,這對本領域技術人員而言是顯而易見的。因此,在不偏離本發明精神的基礎上所做的這些修改或改進,均屬於本發明要求保護的範圍。
