四配位氘代配體配位的鉑絡合物的製作方法
2023-05-01 00:39:36 1
本發明的公開內容是關於一種適合在顯示和照明應用中用作磷光或延遲螢光或磷光發射體的的多齒配位的鉑絡合物。
背景技術:
能夠吸收和/或發光的化合物可適用於各種光學和光電器件,包括但不限於諸如太陽能、光敏這樣的光吸收器件、有機發光二極體(oled)、光發射器件或既有光吸收又有光發射能力的器件以及用於生物標記的相關應用。為了發現用於光學和電致發光器件的有機和有機金屬材料,已專門作過很多研究。一般而言,這一領域的研究目村是實現多項目標,包括提高器件的吸收和發光效率,提高器件的穩定性,以及提高解析度等。
儘管專門為光學和光電材料(例如,紅色和綠色磷光有機金屬材料在市面上有售並且已在有機發光二極體(oled)、照明和先進顯示器中用作磷光體)所作的研究取得了顯著的進步,但許多目前可獲得的材料表現出不少缺點,包括綜合性能一般、發射或吸收不足以及穩定性不夠理想等等。
優良的藍色發射體尤其稀少,其面對的一大挑戰是藍色器件的穩定性。與紅色及綠色磷光體的最低三重激發態能量相比,藍色磷光體的最低三重激發態能量很高,這意味著藍色器件的主體材料的最低三重激發態能量甚至會更高。因此,問題之一是藍色器件可用的摻雜材料是有限的。相應地,需要能夠在光學發射和吸收應用中表現出更優性能的新材料。
在本發明的公開內容中,將氘引入鉑絡合物的配體。由於氘原子比氫原子重,與c-h鍵相比,碳-氘(c-d)鍵的振動可以減少。因此,發射光譜的振動帶將減少或削弱,而整個光譜可以變窄。這將能夠促進發射光色並改善器件的性能。更明確地說,絡合物的cie坐標將被調諧成更符合平板電視的需求。
技術實現要素:
本發明涉及適合在有機發光二極體(oled)、顯示和照明應用中的用作發射體的金屬絡合物。
此處公開的是1型分子式絡合物:
ra代表單、雙、三或四基取代,ra是獨立的氘,cdh2,cd2h,cd3,cdr1r2,cd2r1,或其他含氘的烷基芳、環烷基、環烯基、雜環基、雜芳基、烷基、烯基、炔基、氨基、單取代氨基、二烴基氨基、單氨基、二芳基胺、烷氧基、芳氧基、滷代基、芳烷基、酯、烷氧羰基、醯胺基、烷氧基羰基氨基,烷氧基碳醯基氨基、芳氧基碳醯基氨基、芳烷基、氨磺醯、氨基甲醯基、烷硫基,脲基、磷醯胺、甲矽烷基、聚合物;或其任何結合物或化合物。
rb、rc、rd和re中的每一種都是要麼獨立存在的或不存在的;如果是存在的,那麼rb、rc、rd和re中的每一種分別代表單或雙基取代,rb,rd和re也可以是三基取代,rb可以是四基取代,並且其中rb、rc、rd和re中的每一種是獨立的氘、滷素、羥基、巰基、硝基、氰基、腈、異腈、亞磺醯基、巰基、磺基、羧基、肼基;取代或未取代的:芳基、環烷基、環烯基、雜環基、雜芳基、烷基、烯基、炔基、氨基、單烷基氨基、二烷基氨基、單芳基氨基、二芳基氨基、烷氧基、芳氧基、滷代烷基、芳烷基、酯、烷氧基羰基、醯基氨基、烷氧基羰基氨基、芳基含氧羰基氨基、硫醯氨基、氨磺醯、氨基甲醯、烷硫基、脲基、磷醯胺、甲矽烷基、聚合;或其任何結合物或化合物,ra和rb可選擇性地連接形成環,rd和re可選擇性地連接形成環。
r1和r2中的每一種都是獨立的氫、氘、滷素、羥氫氧基、硫醇、硝基、氰基、腈、異腈、亞硫醯基、氫硫基、磺基、羧基、肼基;可替代或不可替代的:芳基、環烷基烷基、環烯基環烯基、雜環基、雜芳基、烷基、烯基、炔基、氨基、單烷基氨基、二烷基氨基、單芳基氨基、二芳基氨基、烷氧基、氧芳基、滷烷基、芳烷基,、酯、烷氧基羰基、醯氨基、烷氧基羰基氨基、芳氧羰氨基、硫醯氨基、氨磺醯、氨基甲醯、硫烷基、脲基、磷醯胺、甲矽烷基、聚合物;或其任何結合物或化合物。
一方面,該鉑絡合物具有分子式2、分子式3、分子式4、分子式5、分子式6或分子式7的結構。另一方面,它們也可以包含其在這沒有得到專門詳述的其他結構或部分,本發明不應局限於其那些在此得到專門詳述的結構或部分。
rb、rc、rd和re中的每一種都是要麼獨立存在的或不存在的,如果是存在的,那麼rb、rc、rd和re中的每一種分別代表單或雙基取代,rb,rd和re也可以是三基取代,rb可以是四基取代,並且其中rb、rc、rd和re中的每一種是獨立的氘、滷素、羥氫氧基、硫醇、硝基、氰基、腈、異腈、亞硫醯基、氫硫基、磺基、羧基、肼基;替代或不替代的:芳基、環烷基烷基、環烯基環烯基、雜環基、雜芳基、烷基、烯基、炔基、氨基、單烷基氨基、二烷基氨基、單芳基氨基、二芳基氨基、烷氧基、芳氧基、滷烷基、烷基、酯、烷氧基羰基、醯氨基、烷氧基羰基氨基、芳氧羰氨基、硫醯氨基、氨磺醯、氨基甲醯、烷硫基、脲基、磷醯胺、甲矽烷基、聚合;或其任何結合物或化合物,ra和rb可選擇性地連接形成熔合環,rd和re可選擇性地連接形成熔合環。
r1和r2中的每一種都是獨立的氫、氘、滷素、羥氫氧基、硫醇、硝基、氰基、腈、異腈、亞硫醯基、氫硫基、磺基、羧基、肼基;可替代或不可替代的:芳基、環烷基烷基、環烯基環烯基、雜環基、雜芳基、烷基、烯基、炔基、氨基、單烷基氨基、二烷基氨基、單芳基氨基、二芳基氨基、烷氧基、芳氧基、滷烷基、烷基、酯、烷氧基羰基、醯氨基、烷氧基羰基氨基、芳氧羰氨基、硫醯氨基、氨磺醯、氨基甲醯、烷硫基、脲基、磷醯胺、甲矽烷基、聚合;或其任何結合物或化合物。
本文還公開了包括在本文中公開的一種或多種化合物的組合物。
本文還公開了包括在本文中公開的一種或多種化合物的器件,比如有機發光二極體。
附圖說明
圖1描述了一個包含本文所公開金屬絡合物的器件。在一具體實施例中,該化合物可在有機發光二極體中使用。
圖2顯示了室溫下複合物1在ch2cl2和pmma中的發射光譜。
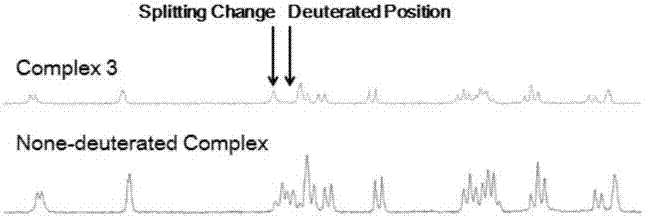
圖3顯示了在6d-dmso溶劑中含氘複合物3和不含氘複合物的1hnmr圖譜比較。
圖4顯示了室溫下複合物3在ch2cl2和pmma中的發射光譜。
圖5顯示了室溫下複合物3在ch2cl2中的含氘複合物和不含氘複合物發射光譜的比較。
圖6顯示了室溫下複合物2在pmma中的含氘複合物和不含氘複合物發射光譜的比較。
圖7顯示了室溫下複合物7在ch2cl2中的含氘複合物和不含氘複合物發射光譜的比較。
在圖片後的圖片描述中對圖片的其它方面也進行了描述。優勢是通過在權利要求中特別指出的元素和組合而實現及獲得的。需要指出的是,上面的一般說明和下面的詳細說明都只是示範性和解釋性的,不具有限定性。
具體實施方式
通過參考以下詳細說明和其中包含的示例,可以更容易地理解本發明。
在本發明化合物、器件和/或方法被公開和描述之前,應當指出的是,除非另有說明,否則它們不限於特定的合成方法,或者除非另有說明,否則它們不限於特定試劑,因為這些方法或試劑當然可以更改。還要指出的一點是,本文中所用的術語只是為了描述特定的方面,而不是為了限制。儘管與本文中所描述的那些方法或材料類似或相同的任何方法或材料都可以在實踐或測試中使用,但現在描述的是示例性方法和材料。
除非上下文另有其它明確規定,否則說明和附加權利要求中使用的單數形式「一」、「一」和「某一」包括複數指稱。因此,例如,提到「一種成分」時包括兩種或兩種以上成分的混合。
本文中使用的術語「可選的」或「可選地」指的是隨後描述的事件或情況可能會發生或可能不會發生,並且該描述包括所述事件或情況發生時的具體實施例和該事件或情況不發生時的具體實施例。
本文公開的是用於製備本文所述組合物以及在本文公開的方法中要使用的組合物本身的成分。這些和其他材料在本文中得到公開,要指出的是,當這些材料的組合、亞群、相互作用、類被公開時,雖然這些複合物的每一不同的單獨和集體組合和排列的特定引用不能得到明確公開,但每一複合物都在本文中得到特別考慮和描述。例如,如果一特定化合物得到公開和討論並且對於包含所述化合物的多個分子所能做的多種修改得到討論,除非進行了相反地特別說明,否則該化合物的每一組合和排列以及可能的修改都會得到考慮。因此,如果屬於同一類的分子a、b和c以及屬於同一類的分子d,e和f以及一種組合分子的示例得到公開,那麼a-d得到了公開,那麼這樣的話,即使不是每一分子都得到單獨詳述,每一分子都得到單獨和集體考慮的意思仍然是,a-e,a-f,b-d,b-e,b-f,c-d,c-e和c-f的組合都被認為得到了公開。同樣,這些分子的子集或組合也被認為得到了公開。因此,比如,a-e,b-f和c-e的子群會被認為得到了公開。這個概念適用於該應用的所有方面,包括,但不限於,製備和使用該組合物的方法中的步驟。因此,如果存在能夠執行的各種各樣的額外步驟,對此可以理解為,可以用這些方法的任一特定具體實施例或具體實施例組合執行這些額外步驟中的每一種。
如本文所提到的那樣,一個連接原子或基團可以連接兩個原子,比如,一個氮原子和一個碳原子。一個連接原子或集團在本文中一方面被公開為x,y,y1,y2,和/或z。如果化合價允許的話,該連接原子還可以選擇性擁有附著的其他化學基團。例如,一方面,因為如果化合價一旦被結合到兩基團上(例如,氮和碳基團),它就會飽和,所以一個氧原子不會有任何附著的其他化學基團。另一方面,當碳原子是連接原子時,可以為碳原子附著兩個額外的化學基團。合適的化學基團包括胺、醯胺、硫醇、芳基、雜芳基、環烷基烷基和雜環基基團。
術語「循環結構」或類似術語在本文中指的是任何循環化學結構,包括但不限於,芳基、雜芳基、環烷基烷基、環烯基、雜環基、碳烯和n-雜環基碳烯。
在本文中使用的「替代」一詞被設想為包括有機化合物的所有可允許取代基。在一個廣泛的方面上,可允許取代基包括有機化合物的非環狀和環狀的,支鏈和無支鏈的,碳環和雜環的,芳香族和非芳香族的取代基。說明性的取代基包括,例如,下文所描述的那些取代基。對合適的有機化合物來說,可允許取代基可以是一個或多個,可以相同或不同。為了實現本發明的目的,雜原子,如硝基,可以擁有本文所描述的滿足雜原子化合價的有機化合物的氫取代基和/或任何可允許的取代基。本發明不會以任何方式受到有機化合物的可允許取代基的限制。另外,術語「取代」或「以...取代」包括的隱含條件是,這樣的取代與取代原子和取代基的可允許化合價相一致,並且這種取代會帶來一種穩定的化合物,比如,一種不會自發通過重排、環化、消除等方式進行轉換的化合物。我們還做出的設想是,在某些方面,除非有明確相反的說明,單個取代基可以被進一步選擇性取代(即,進一步取代的或未取代的)。
為了定義不同的屬於,「a1」、「a2」、「a3」、「a4」在本文中用於作為代表各種特定取代基的通用符號。這些符號可以是任何取代基,不限於那些在本文中得到公開的取代基,如果他們在一具體實施例中被定義為特定取代基,他們能,在另一具體實施例中,被定義為一些其它取代基。
本文中使用的術語「烷基」是一種支鏈或無支鏈的由1到24個碳原子組成的飽和碳氫化合物集團,比如甲基、乙基、正丙基、異丙基、正丁基、異丁基、二丁基、叔丁基、正戊基、異戊基、二戊基、新戊基、己基、庚基、辛基、壬基、癸基、十二基、十四基、十六基、二十基、二十四基等。烷基團可以是環狀的或非環狀的。烷基團可以是支鏈或無支鏈的。烷基團也可以是可取代的或不可取代的。比如,烷基團可以用一個或多個集團取代,包括但不限於,本文所描述的烷基、環烷基烷基、烷氧基、氨基,或者,滷化物、羥基、硝基、甲矽烷基、磺氧基或硫醇。一種「低烷基」基團是一種包含從1到6(比如從1到4)個不等的碳原子的烷基團。
在本文的通篇描述中,「烷基」一般是指未取代烷基組和取代烷基組兩者;然而,在本文中,也通過特別確認烷基組上的特別取代基,提到取代烷基組。例如,術語「滷烷」或「滷代烷基」具體指一種被一個或多個滷化物,如氟、氯、溴或碘取代的烷基組。術語「烷氧基烷基」具體指被一個或多個如下文所述烷氧基團所取代的一種烷基團。術語「烷基氨基」具體指被一個或多個如下文所述烷氨基團等所取代的一種烷基團。當在一個具體實施例中使用「烷基」,而在另一個具體實施例中使用諸如「烷基乙醇」之類特定術語時,不意味著這是在暗示,「烷基」這個術語不是指的也是諸如「烷基乙醇」等之類特定術語。
這種做法也適用於本文所述的其他基組。也就是,一個諸如「環烷基」之類術語指的是非取代性和取代性環烷基烷基基團兩者,另外,取代性基團也可以在文章中得到具體確定;例如,一種特別的取代性環烷基可以北稱為,比如,一種「環烷基」。同樣,一種取代性烷氧基可以被專門稱為,例如,「滷化烷氧基」,一種特別取代性烯基可以被稱為,例如,「烯基乙醇」,或類似的術語。再次,使用諸如「環烷基」之類一般術語和諸如「烷基環烷基」之類特定術語並不意味著,一般術語不是也包括特定術語。
本文中使用的術語「環烷基」是一種至少由三個碳原子所組成的非芳香碳基環。環烷基烷基組的例子包括,但不限於,環丙烷,環丁烷,環戊烷,環己基,降冰片基,以及類似的物質。術語「雜環烷基」是一種如上文所定義的環烷基團,並包括在「環烷基「」的含義之中,在這個含義中,環上的至少一個碳原子被一個雜原子所取代,這種雜原子包括,但不限於,氮、氧、硫或磷。環烷基組和雜環烷基組可以是取代性的或非取代性的。環烷基組和雜環烷基組可以被一個或多個基組取代,包括,但不限於,本文所描述的烷基、環烷基、烷氧基、氨基、醚、滷、羥基、硝基、甲矽烷基、磺氧基,或硫醇。
本文中使用的術語「聚亞烴基組」是一種有兩個或多個彼此相連的ch2基團的基組。聚亞烴基組可由分子式—(ch2)a—表示,其中一「a」代表一個從2到500的整數。
本文中使用的術語「烷氧基的」和「烷氧基」指的是一種通過一個醚鍵相連的烷基或環烷基組;也就是,一種「烷氧基」組可以被定義為—oa1,其中a1是上文定義的烷基或環烷基。「烷氧基」也包括剛剛描述的烷氧基組的聚合物;也就是,一種烷氧基可以是一種諸如—oa1—oa2或—oa1—(oa2)a—oa3之類的聚合物,其中「a」是一個從1到200的整數,而a1、a2和a3是烷基和/或環烷基組。
本文所使用的術語「烯基」是一種包含2到24個碳原子的碳氫化合物集團,它的結構分子式至少含有一個碳碳雙鍵。諸如(a1a2)c=c(a3a4)之類的非對稱結構旨在包括e和z兩種異構體。這可以從結構分子式中推定,在結構分子式中,存在一種不對稱的烯烴,或者也可以用c=c鍵符號明確表示它。烯基團可以用一個或多個基團取代,包括但不限於,本文所描述的烷基,環烷基烷基、烷氧基、烯基、環烯基、炔基、環炔基、芳基、異芳基、乙醛、氨基、羧酸、酯、醚、滷化物、羥基、酮、疊氮化物、硝基、甲矽烷基、磺氧基或硫醇。
本文中使用的術語「環烯基」是一種由至少三個碳原子組成的非芳香碳環,並且至少含有一個碳碳雙鍵,即c=c。環烯基組的例子包括,但不限於,環丙烯基、環丁烯基、環戊烯基、環十五烯基、環己烯、環己二烯基、降冰片烯,以及類似化合物。術語「雜環烯基」是一類上文所定義的環烯基組,並且包括在術語「環烯基」的含義中,其中環上的至少一個碳原子被一雜原子所取代,該雜原子包括但不限於,氮、氧、硫、磷。環烯基組和雜環烯基組可以是取代性的和非取代性的。環烯基組和雜環烯基組可以被一種或多種組取代,包括但不限於,本文所描述的烷基、環烷基、烷氧基,、烯基、環烯基、炔基、環炔基、芳基、雜芳基、乙醛、氨基、羧酸、酯、醚、滷、羥基、酮、疊氮、硝基、甲矽烷基、磺氧基或硫醇。
本文所使用的術語「炔基」是一種包含2到24個碳原子的碳氫化合物集團,它的結構分子式至少含有一個碳碳三鍵。炔基團可以用一個或多個基團取代,包括但不限於,本文所描述的烷基、環烷基烷基、烷氧基、烯基、環烯基、炔基、環炔基、芳基、異芳基、乙醛、氨基、羧酸、酯、醚、滷化物、羥基、酮、疊氮化物、硝基、甲矽烷基、磺氧基或硫醇。
本文中使用的術語「環炔基」是一種由至少七個碳原子組成的非芳香碳環,並且至少含有一個碳碳三鍵。環炔基組的例子包括,但不限於,環庚炔基、環辛烯基、cyclonontynyl,以及類似化合物。術語「雜環炔基」是一類上文所定義的環炔基組,並且包括在術語「環炔基」的含義中,其中環上的至少一個碳原子被一雜原子所取代,該雜原子包括但不限於,氮、氧、硫或磷。環炔基組和雜環炔基組可以是取代性的和非取代性的。環炔基組和雜環炔基組可以被一種或多種組取代,包括但不限於,本文所描述的烷基、環烷基、烷氧基,、烯基、環烯基、炔基、環炔基、芳基、雜芳基、乙醛、氨基、羧酸、酯、醚、滷、羥基、酮、疊氮、硝基、甲矽烷基、磺氧基或硫醇。
本文所使用的術語「芳基」是一種包含任何碳基芳香組的組,包括但不限於,苯、萘、苯基、聯苯、苯氧基苯,及類似化合物。術語「芳基」還包括「雜芳基」,「雜芳基」被定義為一個包含芳香基團的基團,該基團至少有一個包含在芳香基團環中的雜原子。雜原子的例子包括但不限於氮、氧、硫和磷。同樣,也包含在術語「芳基」中的術語「非雜芳基」定義了一個包含以芳香基團的基團,而該芳香基團不包含雜原子。芳基組可以是取代性的和非取代性的。芳基組可以被一種或多種組取代,包括但不限於,本文所描述的烷基、環烷基、烷氧基,、烯基、環烯基、炔基、環炔基、芳基、雜芳基、乙醛、氨基、羧酸、酯、醚、滷、羥基、酮、疊氮、硝基、甲矽烷基、磺氧基或硫醇。術語「聯芳基」是一種特定類型的芳基組,並且被包括在「芳基」的定義中。聯芳基指的是通過一個稠環結構結構連接到一起的兩種芳基組,如同萘那樣,或者,通過一個或多個碳碳鍵附著到一起,如同聯苯那樣。
本文所使用術語「醛」是由分子式—c(o)h所表示的。在本文的整個描述中,「c(o)」是羰基組的一種速記符號,也就是,c=o
本文所使用的術語「胺」或「氨基」由分子式—na1a2表示,其中a1和a2可以是,獨立的,本文所描述的氫或烷基、烯基、環烯基,炔基、環炔基、芳基,或雜芳基組
本文所使用的術語「烷基氨基」由分子式—nh(-烷基)所表示,其中烷基在本文中得到了描述。有代表性的例子包括,但不限於,甲基氨基組、乙基氨基組、丙基氨基組、異丙基氨基組、丁基氨基組、異丁基氨基組、(仲丁基)氨基組、(叔丁基)氨基組、戊(烷)基氨基組、異戊基氨基組、(叔戊基)氨基組、己基氨基組,及類似化合物。
本文所使用的術語「二烷基氨基」由分子式—n(-烷基)2所表示,其中烷基在本文中得到了描述。有代表性的例子包括,但不限於,二甲基氨基組、二乙基氨基組、二丙基氨基組、二異丙基氨基組、二丁基氨基組、二異丁基氨基組、二(仲丁基)氨基組、二(叔丁基)氨基組、二戊(烷)基氨基組、二異戊基氨基組、二(叔戊基)氨基組、二己基氨基組、n-乙基-n-甲基氨基組、n-甲基-n-丙基氨基組、n-乙基-n-丙基氨基組,及類似化合物。
本文所使用的術語「羧酸」由分子式—c(o)oh所表示.
本文所使用的術語「酯」由分子式oc(o)a1或—c(o)oa1所表示,其中a1可以是,本文所述的烷基、環烷基烷基、烯基、環烯基、炔基、環炔基、芳基、雜芳基組。本文所使用的術語「聚酯」由分子式—(a1o(o)c-a2-c(o)o)a—或—(a1o(o)c-a2-oc(o))a—所表示.,其中,可以a1和a2是,獨立的,本文所描述的一種烷基、環烷基烷基、烯基、環烯基、炔基、環炔基、芳基或雜芳基組,並且「a」是一個從1到500的整數。「聚酯」作為術語用於描述由擁有至少兩個羧酸組的化合物和擁有至少兩個羥基組的化合物進行反應所產生的一種組。
本文所使用的術語「醚」由分子式oc(o)a1所表示,其中a1和a2可以是,本文所述的烷基、環烷基烷基、烯基、環烯基、炔基、環炔基、芳基、雜芳基組。本文所使用的術語「聚醚」由分子式—(a1o-a2o)a—,所表示,其中a1和a2可以是,獨立的,本文所述的烷基、環烷基、烯基、環烯基、炔基、環炔基、芳基、雜芳基組,並且「a」是一個從1到500的整數。聚醚組的例子包括聚乙烯氧化物、聚丙烯氧化物和聚丁烯氧化物。
術語「聚合的」包括聚亞烴基、聚醚、聚酯和含有重複單元的其它組,包括但不限於,-(ch2o)n-ch3、-(ch2ch2o)n-ch3、-[ch2ch(ch3)]n-ch3、-[ch2ch(cooch3)]n-ch3、-[ch2ch(cooch2ch3)]n-ch3和-[ch2ch(cootbu)]n-ch3,其中n是一個整數(比如,n>1或n>2)。
本文中使用的術語「滷化物」指的是滷族元素氟、氯、溴和碘。
本文中使用的術語「雜環基」指的是單和多環非芳香環系統,而本文中使用的「雜芳基」指的是至少一個環系統不是碳的單和多環非芳香環系統。這些術語包括氮雜環丁烷、二氧六環、呋喃、噻唑、咪唑、異惡唑、嗎啉、惡唑、吡唑,包括1,2,3-惡二唑,1,2,5-惡二唑和1,3,4-惡二唑,哌嗪、哌啶、吡嗪、吡唑、噠嗪、吡啶、嘧啶、吡咯、吡咯烷酮、四氫呋喃、四氫呋喃、四嗪,包括1,2,4,5-四嗪、四唑,包括1,2,3,4-四唑和1,2,4,5-四唑,噻重氮,包括,1,2,3-噻重氮、1,2,5-噻重氮和1,3,4-噻重氮,噻唑類、噻吩類、三嗪,包括1,3,5-三嗪和1,2,4-三嗪,三唑,包括1,2,3-三唑、1,3,4-三唑和類似化合物。
本文所使用的術語「羥氫氧基」由分子式—oh所表示。
本文所使用的術語「酮」由分子式a1c(o)a2所表示,其中a1和a2可以是,獨立的,本文所描述的一種烷基、環烷基烷基、烯基、環烯基、炔基、環炔基、芳基或雜芳基組。
本文所使用的術語「疊氮化物」由分子式—n3所表示。
本文所使用的術語「硝基」由分子式—no2所表示。
本文所使用的術語「腈」由分子式—cn所表示。
本文所使用的術語「甲矽烷基」由分子式—sia1a2a3所表示,其中a1、a2和a3可以是,獨立的,本文所描述的一種烷基、環烷基烷基、烯基、環烯基、炔基、環炔基、芳基或雜芳基組。
本文所使用的術語「氧磺基」由分子式—s(o)a1,—s(o)2a1,—os(o)2a1,或—os(o)2oa1所表示,其中a1可以是本文所描述的一種烷基、環烷基、烯基、環烯基、炔基、環炔基、芳基或雜芳基組。在本文的描述中,「s(o)」是s=o的速記簡寫。本文使用的術語「硫醯」指的是氧磺基,它由由分子式—s(o)2a1所表示,其中a1可以是本文所描述的一種烷基、環烷基、烯基、環烯基、炔基、環炔基、芳基或雜芳基組。本文所使用的術語「碸」由分子式a1s(o)2a2所表示,其中a1和a2可以是,獨立的,本文所描述的一種烷基、環烷基、烯基、環烯基、炔基、環炔基、芳基或雜芳基組。本文所使用的術語「亞碸」由分子式a1s(o)a2所表示,其中a1和a2可以是,獨立的,本文所描述的一種烷基、環烷基、烯基、環烯基、炔基、環炔基、芳基或雜芳基組。
本文所使用的術語「硫醇」由分子式—sh所表示。
本文所使用的「r1」、「r2」、「r3」和「rn」(其中n是一個整數),可以獨立地擁有上面所列出的一個或多個組。例如,如果r1是一個直鏈烷基組,烷基組的氫原子中的一個可選擇性地被一羥氫氧基組、一烷氧基組、一烷基組、一滷化物和類似物質所取代。根據所選的組,第一組可以包含在第二組中,或者,第二種選擇是,第一組可以掛到(即附到)第二組上。例如,按照「一種由氨基組組成的烷基組」這種說法,氨基組可包含到烷基組的骨幹中。另一種選擇是,氨基組可以附著到烷基組的骨幹上。所選的組的性質(s)將確定第一組是嵌入還是附著到第二組。
本文所述化合物可能含有「選擇性取代的」成分。一般來說,無論是否之前附加有「選擇性」這個術語,「取代」這個術語意味著指定成分的一個或多個氫被一個合適的取代基所取代。除非另有說明,一「選擇性取代」組可能在組的每一個可替代位置擁有一個合適的取代基,如果在任何給定結構中有多個位置可以被從特定組中選擇的數目超過一個的取代基所取代,那麼該取代基在每一個位置都可以是相同或不同的。組的取代基最好是能夠引起形成穩定或化學上可行化合物的那些取代基。也考慮到的是,在某些方面,除非有明確相反的說明,單個取代基可以被進一步選擇性取代(即,進一步被取代或未被取代)。
在一些方面,一種化合物的結構可以用下面的分子式表示:
這種分子式被理解為與下面的分子式相同:
其中n通常代表一個整數。也就是說,rn被理解為代表五種獨立的取代基,rn(a),rn(b),rn(c),rn(d),rn(e)。「獨立取代基」的意思是每個r取代基都能夠被獨立定義。例如,如果在一個具體實施例中rn(a)是滷素,那麼rn(b)在那個具體實施例中不一定是滷素。
在本文公開和描述的化學結構和成分中對r,r1,r2,r3,r4,r5,r6等提到了好幾次。在詳述中對r,r1,r2,r3,r4,r5,r6等進行的任何描述都適用於各自對r,r1,r2,r3,r4,r5,r6等進行描述的任何結構或成分。
利用有機材料的光電器器件正變得越來越受歡迎,而它們受歡迎的原因有很多。用於製造這種器件的許多材料相對便宜,因此有機光電器件相對於無機器件具有潛在的成本優勢。此外,有機材料的固有特性,如其柔韌性,可能使它們非常適合於一些特殊應用,如柔性襯底上的加工。有機光電器器件的例子包括有機發光器件(oled),有機電晶體,有機太陽能電池和有機光電探測器。對於oled來說,有機材料相比傳統材料可能有性能上的優勢。例如,有機發光層發光的波長通常可以很容易用適當的摻雜劑進行調整。
激子從單重激發態到基態的衰減產生冷光,即螢光。激子從三重激發態到基態的衰減產生冷光,即磷光。由於重金屬原子的強自旋軌道耦合能非常有效地增強單重激發態和三重激發態之間的系統間交叉(isc),磷光金屬絡合物,如鉑絡合物,已顯示了它們收穫單重和三重激發態兩者以及達到100%內部量子效率的潛力。因此,磷光金屬絡合物是作為有機發光器件(oled)發光層摻雜物的很好候選材料,它在學術和工業領域都以得到非常多的注意。並且在過去的十年中,人們已經在該技術走向高利潤商業化的道路上取得了一定成果,例如,oled已經在智慧型手機、電視機和數位相機的先進顯示器中得到應用。
然而,到目前為止,藍色電致發光器件仍然是這項技術中最具挑戰性的領域,原因至少部分是藍色器件的不穩定性。一般認為,基質材料的選擇是影響藍色器件穩定性的一個因素。但是,藍色螢光材料的最低三重態激發態(t1)的能量很高,這一般意味著藍色器件的基質材料的最低三重態激發態(t1)能量應該更高。這就給開發藍色器件基質材料帶來了困難。
本發明通過將氘原子(s)引入鉑絡合物的配體提供了一種材料設計路線。由於氘原子比氫原子重,與c-h鍵相比,碳-氘(c-d)鍵的振動可以減少。因此,發射光譜的振動帶將減少或削弱,而整個光譜可以變窄。這將能夠促進發射光色並改善器件的性能。
這裡描述的金屬絡合物可以被定製或調整以適應需要特定發射或吸收特性的特定應用。本發明中的金屬絡合物的光學性質可以通過改變圍繞金屬中心的配體的結構或通過改變配體上螢光發光體(s)的結構而進行調整。例如,具有攜帶電子供體取代基或電子吸收取代基的配體的金屬絡合物通常具有不同的光學性質,包括發射和吸收光譜。金屬絡合物的顏色可以通過更改螢光發光體和配體上的共軛基團而得到調整。
這種複合物的發射可以通過,比如,修改配體或螢光發光體的結構,而調整(例如,從紫外到近紅外)。螢光發光體是一有機分子中的一組原子,該原子可以吸收能量從而產生單重激發態。該單重激發子能產生衰減從而迅速產生及時冷光。一方面,該絡合物可以在大部分的可見光譜上發光。在具體的例子中,本文描述的絡合物可以在從400納米到700納米的範圍內發光。另一方面,絡合物提高了傳統發射絡合物的穩定性和效率。再一方面,所述絡合物可用作為,比如,生物應用、抗癌劑、有機發光二極體(oled)中的發射器或其組合,的發光標籤。最後一方面,絡合物可用於發光器件,例如,緊湊型螢光燈(cfl)、發光二極體(led)和白熾燈等。
本文公開了含有鉑、鈀或金的化合物或化合物絡合物。術語化合物、化合物絡合物和絡合物在本文中得到了交替使用。一方面,本文公開的化合物具有中性電荷。
本發明公開的化合物可以表現出理想的性質,並且具有可以通過選擇適當配體來調整的發射和/或吸收光譜。另一方面,在本文中得到特別描述的它們的化合物、結構或部分的任何一個或任何多個可能會被排除在外。
本文所公開的化合物適用於各種光學和光電器件,包括,但不限於,諸如太陽能和光敏感器件之類光吸收器件、有機發光二極體(oled)、光發射器件或既有光吸收又有光發射能力的器件以及用於生物應用的標誌物。
如上文簡單敘述,所公開的化合物是鉑絡合物。一方面,本文公開的化合物可以用作oled應用,如全彩顯示器,的基質材料。
本文公開的化合物在各種應用中都有使用價值。作為發光材料,這些化合物可用於有機發光二極體(oled)、發光器件和顯示器以及其它發光器件。
另一方面,這些化合物可以在照明器件,例如,有機發光器件中,提供比傳統材料更好的效率和/或使用壽命。
本文中所描述的化合物可以使用多種方法製成,包括,但不限於,示例中所描述的那些。
本文公開的化合物包括延遲螢光發射體、磷光發射體或它們的組合。一方面,本文公開的化合物是延遲螢光發射器。另一方面,本文公開的化合物是磷光發射體。再另一方面,本文公開的一化合物是一延遲螢光發射體和一磷光發射體兩者。
此處公開的是1型分子式絡合物:
ra代表單、雙、三或四基取代,ra是獨立的氘,cdh2,cd2h,cd3,cdr1r2,cd2r1,或其他含氘的烷基芳、環烷基、環烯基、雜環基、雜芳基、烷基、烯基、炔基、氨基、單取代氨基、二烴基氨基、單氨基、二芳基胺、烷氧基、芳氧基、滷代基、芳烷基、酯、烷氧羰基、醯胺基、烷氧基羰基氨基,烷氧基碳醯基氨基、芳氧基碳醯基氨基、芳烷基、氨磺醯、氨基甲醯基、烷硫基,脲基、磷醯胺、甲矽烷基、聚合物;或其任何結合物或化合物。
rb、rc、rd和re中的每一種都是要麼獨立存在的或不存在的,如果是存在的,那麼rb、rc、rd和re中的每一種分別代表單或雙基取代,rb,rd和re也可以是三基取代,rb可以是四基取代,並且其中rb、rc、rd和re中的每一種是獨立的氘、滷素、羥基、巰基、硝基、氰基、腈、異腈、亞磺醯基、巰基、磺基、羧基、肼基;取代或未取代的:芳基、環烷基、環烯基、雜環基、雜芳基、烷基、烯基、炔基、氨基、單烷基氨基、二烷基氨基、單芳基氨基、二芳基氨基、烷氧基、芳氧基、滷代烷基、芳烷基、酯、烷氧基羰基、醯基氨基、烷氧基羰基氨基、芳基含氧羰基氨基、硫醯氨基、氨磺醯、氨基甲醯、烷硫基、脲基、磷醯胺、甲矽烷基、聚合;或其任何結合物或化合物,ra和rb可選擇性地連接形成熔合環,rd和re可選擇性地連接形成熔合環。
r1和r2中的每一種都是獨立的氫、氘、滷素、羥氫氧基、硫醇、硝基、氰基、腈、異腈、亞硫醯基、氫硫基、磺基、羧基、肼基;可替代或不可替代的:芳基、環烷基烷基、環烯基環烯基、雜環基、雜芳基、烷基、烯基、炔基、氨基、單烷基氨基、二烷基氨基、單芳基氨基、二芳基氨基、烷氧基、氧芳基、滷烷基、芳烷基,、酯、烷氧基羰基、醯氨基、烷氧基羰基氨基、芳氧羰氨基、硫醯氨基、氨磺醯、氨基甲醯、硫烷基、脲基、磷醯胺、甲矽烷基、聚合物;或其任何結合物或化合物。
一方面,該鉑絡合物具有分子式2、分子式3、分子式4、分子式5、分子式6或分子式7的結構。另一方面,它們也可以包含其在這兒沒有得到專門詳述的其他結構或部分,本發明不應局限於其那些在此得到專門詳述的結構或部分。
rb、rc、rd和re中的每一種都是要麼獨立存在的或不存在的,如果是存在的,那麼rb、rc、rd和re中的每一種分別代表單或雙基取代,rb,rd和re也可以是三基取代,rb可以是四基取代,並且其中rb、rc、rd和re中的每一種是獨立的氘、滷素、羥氫氧基、硫醇、硝基、氰基、腈、異腈、亞硫醯基、氫硫基、磺基、羧基、肼基;替代或不替代的:芳基、環烷基烷基、環烯基環烯基、雜環基、雜芳基、烷基、烯基、炔基、氨基、單烷基氨基、二烷基氨基、單芳基氨基、二芳基氨基、烷氧基、芳氧基、滷烷基、烷基、酯、烷氧基羰基、醯氨基、烷氧基羰基氨基、芳氧羰氨基、硫醯氨基、氨磺醯、氨基甲醯、烷硫基、脲基、磷醯胺、甲矽烷基、聚合;或其任何結合物或化合物,ra和rb可選擇性地連接形成熔合環,rd和re可選擇性地連接形成熔合環。
r1和r2中的每一種都是獨立的氫、氘、滷素、羥氫氧基、硫醇、硝基、氰基、腈、異腈、亞硫醯基、氫硫基、磺基、羧基、肼基;可替代或不可替代的:芳基、環烷基、環環烯基、雜環基、雜芳基、烷基、烯基、炔基、氨基、單烷基氨基、二烷基氨基、單芳基氨基、二芳基氨基、烷氧基、芳氧基、滷烷基、烷基、酯、烷氧基羰基、醯氨基、烷氧基羰基氨基、芳氧羰氨基、硫醯氨基、氨磺醯、氨基甲醯、烷硫基、脲基、磷醯胺、甲矽烷基、聚合;或其任何結合物或化合物。
對於本文中描述的分子式1至4,它的群類可能在下文的描述中得到定義。
一方面,ra是單取代。另一方面,ra是雙取代。再另一方面,ra是三取代。最後一方面,ra是四取代。
一方面,ra是獨立氘,cdh2,cd2h,cd3,cdr1r2,cd2r1,或其它含氘烷芳基、環烷基烷基、環烯基環烯基、雜環基、雜芳基、烷基、烯基、炔基、氨基、單烷基氨基、雙烷基氨基、單芳基氨基、雙芳基氨基、烷氧基、芳氧基、滷烷基、烷基、酯、烷氧基羰基、醯氨基、烷氧基羰基氨基、芳氧基羰基氨基、硫醯氨基、氨磺醯、氨基甲醯、烷硫基、脲基、磷醯胺、甲矽烷基、聚合;或其任何結合物或化合物。
一方面,一種rb是存在的。另一方面,rb是不存在的。
一方面,rb是單取代。另一方面,rb是雙取代。再另一方面,rb是三取代。最後一方面,rb是四取代。
一方面,每一種rb都是獨立氘、滷素、羥氫氧基、硫醇、硝基、氰基、腈、異腈、亞硫醯基、氫硫基、磺基、羧基、肼基;可代替的或不科代替的:芳基、環烷基、環環烯基、雜環基、雜芳基、烷基、烯基、炔基、氨基、單烷基氨基、二烷基氨基、單芳基氨基、芳基氨基、烷氧基、芳氧基、滷烷基、烷基、酯、烷氧基羰基、醯基氨基、烷氧基羰基氨基、芳氧基羰基氨基、硫醯氨基、氨磺醯、氨基甲醯、硫烷基、脲基、磷醯胺、甲矽烷基,聚合的;或其任何結合物或化合物。
一方面,一種rc是存在的。另一方面,rc是不存在的。
一方面,rc是單取代。另一方面,rc是雙取代。
一方面,每一種rc都是獨立的氘、滷素、羥氫氧基、硫醇、硝基、氰基、腈、異腈、亞硫醯基、氫硫基、磺基、羧基、肼基;可替代或不可替代的:芳基、環烷基、環烯基、雜環基、雜芳基、烷基、烯基、炔基、氨基、單烷基氨基、二烷基氨基、單芳基氨基、二芳基氨基、烷氧基、芳氧基、滷烷基、烷基、酯、烷氧基羰基、醯氨基、烷氧基羰基氨基、芳氧羰氨基、硫醯氨基、氨磺醯、氨基甲醯、烷硫基、脲基、磷醯胺、甲矽烷基、聚合;或其任何結合物或化合物。
一方面,一種rd是存在的。另一方面,rd是不存在的。
一方面,rd是單取代。另一方面,rd是雙取代。再另一方面,rd是三取代。
一方面,每一種rd都是獨立的氘、滷素、羥氫氧基、硫醇、硝基、氰基、腈、異腈、亞硫醯基、氫硫基、磺基、羧基、肼基;可替代或不可替代的:芳基、環烷基、環烯基、雜環基、雜芳基、烷基、烯基、炔基、氨基、單烷基氨基、二烷基氨基、單芳基氨基、二芳基氨基、烷氧基、芳氧基、滷烷基、烷基、酯、烷氧基羰基、醯氨基、烷氧基羰基氨基、芳氧羰氨基、硫醯氨基、氨磺醯、氨基甲醯、烷硫基、脲基、磷醯胺、甲矽烷基、聚合;或其任何結合物或化合物。
一方面,一種re是存在的。另一方面,re是不存在的。
一方面,re是單取代。另一方面,re是雙取代。再另一方面,re是三取代。
一方面,每一種re都是獨立的氘、滷素、羥氫氧基、硫醇、硝基、氰基、腈、異腈、亞硫醯基、氫硫基、磺基、羧基、肼基;可替代或不可替代的:芳基、環烷基、環烯基、雜環基、雜芳基、烷基、烯基、炔基、氨基、單烷基氨基、二烷基氨基、單芳基氨基、二芳基氨基、烷氧基、芳氧基、滷烷基、烷基、酯、烷氧基羰基、醯氨基、烷氧基羰基氨基、芳氧羰氨基、硫醯氨基、氨磺醯、氨基甲醯、烷硫基、脲基、磷醯胺、甲矽烷基、聚合;或其任何結合物或化合物。
一方面,r、r1和r2中的每一種都是獨立的氫、滷素、羥氫氧基、硫醇、硝基、氰基、腈、異腈、亞硫醯基、氫硫基、磺基、羧基、肼基、芳基、環烷基、環烯基、雜環基、雜芳基、烷基、烯基、炔基、氨基、單烷基氨基、雙烷基氨基、單芳基氨基、雙芳基氨基、烷氧基、芳氧基、滷烷基、烷基、酯、烷氧基羰基、醯基氨基、烷氧基羰基氨基、芳氧基羰基氨基、硫醯氨基、氨磺醯、氨基甲醯、硫烷基、脲基、磷醯胺、可替代甲矽烷基、聚合,或,或其任何結合物或化合物。零一方面,r、r1和r2中的每一種都是獨立的氫、芳基、環烷基、環烯基、雜環基、雜芳基、烷基、烯基、炔基、滷素、羥氫氧基、硫醇、硝基、氰基或氨基.再一方面,r、r1和r2中的每一種都是獨立的氫、芳基、環烷基、環烯基、雜環基、雜芳基、烷基、烯基或炔基。
一方面,對於本文公開的任一種分子式,是下列結構中獨立的一種。另一方面,它們還可以包括它們的未在本文中得到具體敘述的其他結構或部分,並且本發明沒有意圖僅限於它們的那些得到特別敘述的結構或部分。
二、示例性化合物
一方面,本發明的公開內容所說明的金屬絡合物可包含以下一或多個結構。另一方面,它們也可包含本文未明確述及的其他結構或這些結構之部分,而並不意旨將本發明的公開內容限制於明確述及的該等結構或其部分。
本文還公開了包括本文所公開化合物中的一或多種的器件。
本文所公開的化合物適用於各種光學和光電器件,包括,但不限於,諸如太陽能和光敏感器件這樣的光吸收器件、有機發光二極體(oled)、光發射器件或既有光吸收又有光發射能力的器件以及用於生物應用的標誌物。
本文所說明的化合物可用在一種諸如oled之類的發光器件中。圖1說明了oled1000的斷面圖。oled1000包括基體1002、陽級1004、空穴傳輸材料(htl)1006、光處理材料1008、電子傳輸材料(etl)1010及一金屬陰極層1012。陽極1004一般是透明材料,例如氧化銦錫。光處理材料1008可以是包括一發射體和一主體的發光材料(eml)。
圖1顯示oled1000的斷面圖,其包括:具有一陽極1004的基體1002,一般是透明材料,例如氧化銦錫,;一空穴傳輸材料層(htl)1006;一發光功能材料1008,例如包括一發射體和一主體的發光材料;一電子傳輸材料層(etl)1010及一金屬陰極層1012。一方面,諸如oled之類的發光器件可包含一或多層。從各方面說,該一或該等多層的任何層均可包含氧化銦錫(ito)、moo3、ni2o3、聚(3,4-乙烯二氧噻吩)(pedot)、聚苯乙烯磺酸鈉(pss)、4,4',4」-((1e,1'e,1」e)-環丙烷-1,2,3-三亞甲基三(氰基-甲基亞基))三(2,3,5,6-四氟苯腈)(nht-49)、2,2'-(全氟萘烷-2,6-二基)丙二腈(nht-51)、2,3,5,6-四氟四氰基-對醌二甲烷(f4-tcnq)、n,n′-二-1-萘基-n,n′-聯苯-1,1′-聯苯-4,4′二胺(npd)、1,1-順((二-4-對甲苯氨基)苯基)環己烷(tapc),2,6-順(n-咔唑基)-吡啶(mcpy)、2,8-順(疊氮磷酸二苯酯)二苯並噻吩(po15)、lif、liq、cs2co3、caco3、al或其組合物。在這一具體實施方式中,光處理材料層1008可包含本發明的一或多個化合物,可選擇性地連帶一主體材料。etl層1010和1006還可包含一或多個化合物以及與電極接近的另一注入層。注入層的材料可包括(電子注入層)eil、(空穴注入層)hil和cpl(蓋層),其形式可以是單一層或分散在傳輸材料中。主體材料可以是本技術中已知的任何合適的主體材料。oled的發光顏色由光處理材料1008的發光能量(光學能隙)決定,可如上所述通過調諧發射化合物和/或主體材料的電子結構來調諧光處理材料1008的發光能量(光學能隙)。htl層1006中的空穴傳輸材料和etl層1010中的電子傳輸材料可包含本技術中已知的任何合適的空穴傳輸體。對此的選擇屬於熟悉本技術者的權限範圍。
顯然,本發明的化合物可呈現磷光。磷光oled(即,具有磷光發射體的oled)一般具有比諸如螢光oled之類的其他oled更高的器件效率。在《自然》1998年395期第151-154頁說明了基於電致磷光發射體的發光器件,因其關於oled而尤其是關於螢光oled的講授內容,以引用的方式併入於此。
從各方面說,圖1所說明的一或多層中的任何層均可包括氧化銦錫(ito)、moo3、ni2o3、聚(3,4-乙烯二氧噻吩)(pedot)、聚苯乙烯磺酸鈉(pss)、n,n′-二-1-萘基-n,n′-聯苯-1,1′-聯苯-4,4′二胺(npd)、1,1-順((二-4-對甲苯氨基)苯基)環己烷(tapc)、2,6-順(n-咔唑基)-吡啶(mcpy)、2,8-順(疊氮磷酸二苯酯)二苯並噻吩(po15)、lif、al或其組合物。
光處理層1008可包括本發明的一或多個化合物,可選擇性地連帶一主體材料。主體材料可以是本技術中已知的任何合適的主體材料。oled的發光顏色由光處理材料1008的發光能量(光學能隙)決定,可通過調諧發射化合物、主體材料或兩者的電子結構來調諧光處理材料1008的發光能量(光學能隙)。htl層1006中的空穴傳輸材料和etl層1010中的電子傳輸材料可包括本技術中已知的任何合適的空穴傳輸體。
本文所說明的化合物可呈現磷光。磷光oled(即,具有磷光發射體的oled)一般具有比諸如螢光oled之類的其他oled更高的器件效率。在wo2000/070655中更詳細地說明了基於電致磷光發射體的發光器件,因其關於oled而尤其是關於螢光oled的講授內容,以引用的方式併入於此。
以下示例的提出是為了向所屬領域的技術人員完整地公開和說明對於本文所要求保護的化合物、組成物、物件、器件和/或方法是如何製作並評估的,並且意旨純為示例性而並非作範圍限制。已盡力確保在數字方面的精確性(例如,數量、溫度等),但是對於一些誤差和偏差應加以考慮。除另有指示外,部件是按重量而論的部件,溫度是以℃為單位或者是環境溫度,而壓力是處於或接近大氣壓。
本文所說明的化合物的各種製備方法是以示例來講述。所提供的這些方法是用於說明各種製備方法,但是其意旨並非限制本文所述的任何方法。相應地,對本發明的公開內容擁有所有權的本領域技術人員可以方便地修改所述方法或者採用不同方法來製備本文所說明的化合物中的一或多種。以下方面僅作為示例,而其意旨並非作範圍限制。溫度、催化劑、濃度、反應物組成及其他工藝條件可以變化,而對本發明的公開內容擁有所有權的本領域技術人員可針對所需絡合物來方便地選擇適當的反應物和條件。
在cdcl3或dmso-d6溶液中,通過varian液態核磁共振儀記錄1hnmr(氫核磁共振)和13cnmr(碳核磁共振)光譜為300、400或500mhz,而化學位移是以殘餘的質子化溶劑為基準。如果使用cdcl3作為溶劑,則採用四甲基矽烷(δ=0.00ppm)作為內參比來記錄1hnmr(氫核磁共振)光譜;採用cdcl3(δ=77.00ppm)作為內參比來記錄13cnmr(碳核磁共振)光譜。如果使用dmso-d6作為溶劑,則採用殘餘的h2o(δ=3.33ppm)作為內參比來記錄1hnmr(氫核磁共振)光譜;採用dmso-d6(δ=39.52ppm)作為內參比來記錄13cnmr(碳核磁共振)光譜。以下縮寫詞(或其組合)是用於解說1hnmr(氫核磁共振)的多樣性:s=單線態,d=雙線態,t=三線態,q=四線態,p=五線態,m=多線態,br=寬。
鉑絡合物1是按照以下方案製備:
2-溴-4-d-吡啶的合成:向一個100ml的燒瓶添加2,6-二溴吡啶(2.36g,10mmol),在室溫下溶解於新鮮蒸餾的四氫呋喃(thf)中。然後逐滴添加i-prmgbr(8ml,12.8mmol)的正乙烷溶液。在攪拌1小時後,添加d2o(5ml)。約0.5小時後,用dcm(二氯甲烷)提取混合物,並組合各個有機相,用滷水清洗,用mg2so4乾燥。去除溶劑,得到一混合物(深褐色油質,497mg),將粗品直接用於下一步驟:
絡合物1的2-d-配體的合成:向一個15ml密封管添加1-甲基咪唑(16mg,0.2mmol),2-(3-(1h-吡唑-1-基)苯氧基)-9h-咔唑(130mg,0.4mmol),2-溴-4-d-吡啶(346mg,2mmol),k2co3(111mg,0.8mmol),甲苯(2ml)和cui(15mg,0.08mmol)。用氮讓混合物起泡10分鐘,並在120℃下攪拌3天。在冷卻後,添加水和乙酸乙酯(ea),並對混合物進行過濾。採用乙酸乙酯提取水相,並組合各個有機相,用滷水清洗,用na2so4乾燥。採用pe/ea=10:1作為洗提液,通過矽膠層析來淨化所獲得的溶液,產生目標產品(淺褐色固體,160mg,99%良率)。1hnmr(500mhz,dmso-d6):δ8.55(d,j=2.6hz,1h),8.33(d,j=8.4hz,1h),8.28(d,j=7.9hz,1h),8.13(t,j=7.8hz,1h),7.84(s,1h),7.82(s,1h),7.73(d,j=1.7hz,1h),7.64(d,j=8.5hz,1h),7.60-7.56(m,2h),7.54-7.47(m,3h),7.39(t,j=7.5hz,1h),7.14(dd,j=8.4,2.2hz,1h),6.99(dd,j=8.1,2.4hz,1h),6.56(s,1h)。ms(esi):404.2[m+h+],426.1[m+na+]
絡合物1的合成:向手套式操作箱中的一個15ml密封管添加2-d-配體(20mg,0.05mmol)、氯亞鉑酸鉀(23mg,0.055mmol)和乙酸(1ml),並在用氮讓混合物起泡15分鐘後,將混合物加熱到110℃,為時三天。在冷卻至室溫後,用水對所產生的溶液進行處理,並沉澱出少量固體。集取溶液,並採用dcm(二氯甲烷)作為洗提液,通過矽膠層析來淨化溶液,產生目標產品(黃色固體,14mg,47%良率)。1hnmr(300mhz,cdcl3):δ8.26(d,j=8.6hz,1h),8.13(d,j=2.7hz,1h),8.02(d,j=7.1hz,1h),7.98-7.88(m,2h),7.84(s,1h),7.79(d,j=8.3hz,1h),7.44-7.29(m,3h),7.21(d,j=8.0hz,1h),7.16-7.06(m,3h),6.67(s,1h)。室溫下pmma(聚甲基丙烯酸甲酯)中cie(0.156,0.124)。
鉑絡合物1是按照以下方案製備:
向手套箱中的一個15ml密封管添加配體(30mg,0.075mmol)、氯亞鉑酸鉀(31mg,0.075mmol)和乙酸(1ml),並在讓混合物起泡15分鐘後,在110℃下對混合物進行加熱,為時三天。在冷卻至室溫後,用水(10ml)對所產生的溶液進行處理,並沉澱出少量固體。集取溶液,並採用pe/dcm=1:2作為洗提液,通過矽膠層析來淨化溶液,產生目標產品(黃色固體,22mg,49%良率)。1hnmr(500mhz,dmso-d6):δ9.30(s,1h),8.92(d,j=2.7hz,1h),8.31(d,j=8.6hz,1h),8.25(dd,j=8.7,1.8hz,1h),8.20(d,j=2.2hz,1h),8.18(d,j=7.5hz,1h),8.11(d,j=8.2hz,1h),7.90(d,j=8.2hz,1h),7.53(d,j=7.6hz,1h),7.50(t,j=7.6hz,1h),7.43(t,j=7.5hz,1h),7.25(d,j=7.9hz,1h),7.24–7.22(m,1h),7.00(d,j=8.0hz,1h),6.93(t,j=3.0hz,1h)。
鉑絡合物3是按照以下方案製備:
2-(苄氧基溴)-(4-d-吡啶-2-基)-9h-咔唑的合成:向一個15ml密封管添加2-(苄氧基)-9-(4-溴吡啶-2-基)-9h-咔唑(107mg,0.25mmol)。然後在室溫下逐滴添加iprmgbr(1.5ml,1m)的四氫呋喃(thf)溶液。在攪拌1小時後,添加d2o(0.6ml)。30分鐘後,用na2so4對混合物進行乾燥。採用pe/ea=15:1作為洗提液,通過矽膠層析來淨化所產生的溶液,產生再循環的反應物(白色固體,13mg)和目標產品(淺褐色固體,75mg,85%良率)。1hnmr(300mhz,dmso-d6):δ8.77(d,j=4.9hz,1h),8.16(d,j=8.4hz,2h),7.78(d,j=8.9hz,2h),7.52(d,j=6.2hz,3h),7.40-7.36(m,5h),7.32(t,j=7.4hz,1h),7.07(dd,j=8.1,1.2hz,1h),5.22(s,2h).ms(esi):351.2[m+h+],373.1[m+na+]。
9-(4-d-吡啶-2-基)-9h-咔唑-2-丙醇的合成:向一個高壓釜添加2-(苄氧基)-9-(4-d-吡啶-2-基)-9h-咔唑(331mg,0.9mmol)、pd/c(38mg)和ea(25ml)。將混合物排空,再用氮重新填充,操作三次,並在0.8mpa和65℃下攪拌24小時。在冷卻下來後,對混合物進行過濾並用na2so4對過濾液進行乾燥。採用pe/ea=10:1,2:1作為洗提液,通過矽膠層析來淨化所獲得的溶液,產生再循環的反應物(淺褐色固體,6mg)和目標產品(白色固體,231mg,98%良率)。1hnmr(300mhz,dmso-d6):δ9.60(s,1h),8.76(d,j=4.9hz,1h),8.13-8.06(m,1h),8.03(d,j=8.4hz,1h),7.78(s,1h),7.73(d,j=8.1hz,1h),7.51(d,j=4.7hz,1h),7.41-7.32(t,j=7.7hz,1h),7.29(t,j=7.7hz,1h),7.21(d,j=2.1hz,1h),6.82(dd,j=8.4,2.1hz,1h)。ms(esi):262.1[m+h+].
絡合物1的4-d-配體的合成:向一個15ml密封管添加3-甲基咪唑(16mg,0.2mmol),4-(3-(1h-吡唑-1-基)苯氧基)-9h-咔唑(130mg,0.4mmol),2-溴-4-d-吡啶(235mg,0.9mmol),k2co3(880mg,2.7mmol),甲苯(2ml)和cui(0.18mmol,10m)。用氮讓混合物起泡10分鐘,並在120℃下攪拌3天。在冷卻後,添加水和乙酸乙酯(ea),並對混合物進行過濾。採用乙酸乙酯提取水相,並組合各個有機相,用滷水清洗,用na2so4乾燥。採用pe/ea=10:1作為洗提液,通過矽膠層析來淨化所獲得的溶液,產生目標產品(淺褐色固體,75mg,99%良率)。1hnmr(500mhz,dmso-d6):δ8.72(d,j=4.9hz,1h),8.54(d,j=8.4hz,1h),8.28(d,j=7.9hz,1h),7.13(t,j=7.8hz,1h),7.84(s,1h),7.82(s,1h),7.73(d,j=1.7hz,1h),7.64(d,j=8.5hz,1h),7.60-7.56(m,2h),7.54-7.47(m,3h),7.39(t,j=7.5hz,1h),7.14(dd,j=8.4,2.2hz,1h),7.59(dd,j=8.1,2.4hz,1h),6.55(s,1h)。ms(esi):404.2[m+h+],426.1[m+na+]。
絡合物3的合成:向一個15ml密封管添加4-d-配體(20mg,0.05mmol)、氯亞鉑酸鉀(23mg,0.055mmol)和乙酸(1ml),並在用氮讓混合物起泡15分鐘後,將混合物加熱到110℃,為時三天。在冷卻至室溫後,用水對所產生的溶液進行處理,並沉澱出少量固體。集取溶液,並採用dcm(二氯甲烷)作為洗提液,通過矽膠層析來淨化溶液,產生目標產品(黃色固體,9mg,47%良率)。1hnmr(500mhz,dmso-d6):δ9.31(d,j=5.9hz,1h),8.94(d,j=2.7hz,1h),8.32(s,1h),8.21(d,j=2.2hz,1h),8.19(d,j=6.8hz,1h),8.12(d,j=8.5hz,1h),7.91(d,j=8.3hz,1h),7.55(d,j=7.7hz,1h),7.51(t,j=7.7hz,1h),7.47-7.42(m,2h),7.28-7.23(m,2h),7.01(d,j=8.0hz,1h),6.94(t,j=2.5hz,1h)。室溫下pmma(聚甲基丙烯酸甲酯)中cie(0.155,0.117)。
鉑絡合物4是按照以下方案製備:
絡合物4的5-d-配體的合成:向一個48ml密封管添加2-溴-9-(3-d-吡啶-2-基)-9h-咔唑(196mg,0.6mmol)、n-(3-羥苯基)吡唑(80mg,0.5mmol)、n,n-二甲基甘氨酸(15mg,0.15mmol),cs2co3489mg,1.5mmol),cui(14mg,0.075mmol)和1,4-二氧六環(5ml)。用氮讓混合物起泡10分鐘,並在120℃下攪拌3天。在冷卻後,去除溶劑。用水和乙酸乙酯(ea)對混合物進行處理,並對其進行過濾。採用乙酸乙酯提取水相,並組合各個有機相,用滷水清洗,用na2so4乾燥。採用pe/ea=10:1作為洗提液,通過矽膠層析來淨化所獲得的溶液,產生目標產品(淺褐色固體,144mg,71%良率)。1hnmr(500mhz,dmso-d6):δ8.72(dd,j=4.8,2.0hz,1h),8.54(d,j=2.6hz,1h),8.32(d,j=8.4hz,1h),8.27(d,j=7.7hz,1h),8.12(dd,j=7.4,1.9hz,1h),7.83(d,j=8.3hz,1h),7.73(d,j=1.7hz,1h),7.63(dd,j=8.1,2.1hz,1h),7.59(d,j=2.2hz,1h),7.57(t,j=2.2hz,1h),7.53-7.47(m,3h),7.39(t,j=7.4hz,1h),7.13(dd,j=8.5,2.2hz,1h),6.99(dd,j=7.9,2.4hz,1h),6.55(t,j=2.2hz,1h)。
絡合物4的合成:向一個15ml密封管添加5-d-配體(40mg,0.1mmol)、氯亞鉑酸鉀(46mg,0.11mmol)和乙酸(1ml),並在用n2讓混合物起泡10分鐘後,在110℃下對混合物進行加熱,為時三天。在冷卻至室溫後,用水對所產生的溶液進行處理,並沉澱出少量固體。集取溶液,並採用pe/dcm=1:1作為洗提液,通過矽膠層析來淨化溶液,產生目標產品(黃色固體,8mg,13%良率)。1hnmr(300mhz,dmso-d6):δ9.31(d,j=5.3hz,1h),8.94(d,j=2.7hz,1h),8.27(dd,j=6.9,1.2hz,1h),8.24-8.16(m,2h),8.12(d,j=8.1hz,1h),7.91(d,j=8.3hz,1h),7.54(t,j=7.3hz,2h),7.50-7.40(m,2h),7.31-7.19(m,2h),7.01(d,j=8.0hz,1h),6.94(t,j=2.4hz,1h)。室溫下pmma(聚甲基丙烯酸甲酯)中cie(0.146,0.109)。
鉑絡合物3是按照以下方案製備:
配體絡合物7的合成:向一個15ml密封管添加4-ch3-配體(42mg,0.1mmol)、ch3ch2ona(14mg,0.2mmol)和ch3ch2od(1ml)。用氮讓混合物起泡10分鐘後,並讓混合物回流3天。在冷卻至室溫後,用乙酸乙酯來提取溶液,並組合各個有機相,用滷水清洗,用na2so4乾燥。採用pe/ea=5:1作為洗提液,通過矽膠層析來淨化所產生的溶液,產生目標產品(白色固體,42mg的4-3d-配體,100%良率)。1hnmr(300mhz,cdcl3):δ8.55(d,j=4.8hz,1h)、8.08(s,1h)、8.05(s,1h)、7.77(d,j=8.5hz,1h)、7.68(s,1h)、7.54(s,1h)、7.49-7.31(m,7h)、7.14(s,1h)、7.05(d,j=8.4hz,1h)、6.95(d,j=7.8hz,1h)、6.43(s,1h)。
絡合物7的合成:向一個15ml密封管添加4-cd3-配體(42mg,0.1mmol)、氯亞鉑酸鉀(46mg,0.11mmol)和乙酸(1ml)。用氮讓混合物起泡10分鐘,並將混合物加熱至110℃,為時三天。在冷卻至室溫後,用水對所產生的溶液進行處理,並沉澱出少量固體。集取溶液,並採用pe/dcm=1:2作為洗提液,通過矽膠層析來淨化溶液,產生目標產品(黃色固體,23mg,38%良率)。1hnmr(300mhz,cdcl3):δ9.10(d,j=5.7hz,1h),8.08-7.99(m,2h),7.92(d,j=8.0hz,1h),7.82(s,1h),7.78(d,j=8.2hz,1h),7.35(m,4h),7.20(m,1h),7.11(m,2h),6.94(d,j=6.2hz,1h),6.66(d,j=1.8hz,1h)。
發射光譜顯示在向配基添加氘原子時,三線態能隙幾乎是相同的。
發射體色純度的代表性數據是從其採用5%pmma(聚甲基丙烯酸甲酯)三氯甲烷溶液製備的薄膜發射光譜獲得。pmma(聚甲基丙烯酸甲酯)中的cie指數坐標是非氘化絡合物(0.163,0.131),絡合物1(0.156,0.124),絡合物2(0.160,0.119),絡合物3(0.155,0.117)和絡合物4(0.146,0.109)。可通過氘化來提高色純度。在圖7所示氘化甲基取代的絡合物7的情況下,與其cie坐標為(0.147,0.100)的非氘化絡合物7相比,室溫下dcm(二氯甲烷)溶液中的發射光譜在深藍色區域顯示出更佳的cie坐標(0.145,0.093)。
本領域的普通技術人員基於本說明書,會明白各方面的其他修改和替代性具體實施方式。因此,本說明書僅可解釋為是解說性的。應理解,應將本文所顯示和說明的形式作為具體實施方式的示例。本文所解說和說明者可用其他元件和材料來替代,部件和程序可以反向,並可以獨立應用特定的特徵,對於所有這些,本領域的普通技術人員在從本說明書中獲益後均會明白。可對本文說明的元件作更改,而不脫離下面權利要求書中所述的精神和範圍。
