睫狀神經營養因子突變體及其修飾型突變體和應用的製作方法
2023-05-17 14:29:41 4
本發明屬於生物醫藥領域,具體而言,涉及一種修飾型睫狀神經營養因子突變體、DNA、重組表達載體、遺傳工程宿主細胞、修飾型睫狀神經營養因子突變體、所述睫狀神經營養因子突變體以及修飾型睫狀神經營養因子突變體的應用、藥物組合物。
背景技術:
睫狀神經營養因子(Ciliary neurotrophic factor,簡稱CNTF)因為最初是從雞的睫狀體中提取出來,並可維持雞副交感神經節的存活而得名。CNTF全長由200個胺基酸組成,第17位有Cys,無分子內二硫鍵,無糖基化位點。CNTF全長分子量在23KD左右。在體內以兩個二聚體形式進行儲存,經過酶解成單體後發生生物學作用。CNTF可以促進包括:運動神經元、感覺神經元、交感神經元、海馬神經元等多種神經細胞和神經膠質細胞的生長和分化。90年代,在將CNTF用於治療肌肉萎縮性脊髓側索硬化症(ALS)的實驗研究中發現,對一組ALS患者進行臨床研究發現病人的體重大大降低,使用藥物組體重比安慰劑組明顯降低。而且這一結果持續整個研究過程。針對這一結果在肥胖症領域進行實驗,結果表明CNTF在體內可與下丘腦的特異性受體結合,激活抑制食慾的關鍵信號通路,抑制進食慾望且使機體不會產生飢餓感,從而使體重減輕。研究發現,CNTF具有多種功能,能促使多種神經細胞的存活、營養肌肉、促進糖、脂代謝和調節能量平衡以及攝食行為。在神經系統,肌肉系統,肥胖症極其相關疾病的治療中具有重要意義和廣闊的臨床前景。
CNTF是本領域技術人員所熟知的,通常使用CNTF突變體解決CNTF的生物活性不高以及表達量低的問題。因此,目前現有技術中已開發出了多種CNTF的突變體(或稱變異體),多種重組人睫狀神 經營養因子是市售的。CNTF突變體或變異體的製備方法在現有技術中也是已知的,例如中國專利CN1687413A公開了一種CNTF突變體(hCNTF),第17位的半胱氨酸突變為丙氨酸;第63位的穀氨醯胺突變為精氨酸;第64位的組氨酸突變為丙氨酸;並去除了C末端1-30個胺基酸。CN1760205A公開了一種CNTF突變體(hCNTF),第17位半胱氨酸突變為絲氨酸,並去除了C端的16個胺基酸;而且第53位的丙氨酸突變為纈氨酸,第35位的蘇氨酸突變為蛋氨酸,第178位的苯丙氨酸突變為纈氨酸。CN1844392也公開了睫狀神經營養因子的突變體。
但上述CNTF的突變體或變異體仍存在體內的作用時間短,要求反覆多次給藥;免疫原性強副反應嚴重,給病人帶來巨大的經濟壓力和精神壓力的缺點。因此,目前選擇使用PEG修飾後的蛋白,其有以下優勢:分子量增大、半衰期延長、免疫原性降低。PEG擁有獨特的親-疏水平衡:當偶聯到藥物分子表面時,將其優良性質賦予修飾後的藥物,改變它們在水溶液中的生物分配行為和溶解性,在其修飾的藥物周圍產空間屏障,減少藥物的酶解。覆蓋蛋白表面的抗原決定簇,降低蛋白的免疫原性。這樣,可以增加蛋白的分子量和體積,減少腎小球的濾過作用,使蛋白在體內作用時間更長。聚乙二醇(PEG)於1940年首次商業生產化。PEG的使用通過了美國FDA認證,符合美國藥典(USP)、國家處方集(NF)、食品化學法典(FCC)標準,被廣泛應用於食品、飼料、個人護理品、化學、醫藥化工等生產生活領域。
利用PEG類修飾劑修飾CNTF或CNTF突變體的最大的問題在於,修飾位點不穩定,如在20種構成CNTF的常見胺基酸中,具有極性的胺基酸殘基的側鏈基團都能夠進行化學修飾,包括賴氨酸、半胱氨酸、組氨酸、精氨酸、天冬氨酸、穀氨酸、絲氨酸、蘇氨酸、酪氨酸等;而且以上幾種極性胺基酸的N-端氨基和C-端羧基也可以進行修飾,這樣會使得很難獲得穩定的修飾位點和修飾方式,導致修飾的專一性降低與修飾的穩定性下降。而且修飾位點往往處於蛋白質的活性中心部位,因此修飾後蛋白活性損失較大。
另外,根據2015版藥典的質量要求,治療性蛋白的PEG修飾需專一位點的修飾。然而,無論是天然的全長CNTF還是上述專利申請開發的CNTF突變體,均無法提供唯一的修飾位點。
技術實現要素:
為解決上述現有技術中存在的問題,本發明提供了一種修飾型睫狀神經營養因子突變體、DNA、重組表達載體、遺傳工程宿主細胞、修飾型睫狀神經營養因子突變體、所述睫狀神經營養因子突變體以及修飾型睫狀神經營養因子突變體的應用、藥物組合物。
具體而言,本發明提供了:
(1)一種睫狀神經營養因子突變體,其中,所述睫狀神經營養因子突變體是在天然睫狀神經營養因子的胺基酸序列的基礎上發生突變得到的,所述突變包括:第26位的賴氨酸突變為異亮氨酸或亮氨酸、第46位的賴氨酸突變為精氨酸、第160位的賴氨酸突變為穀氨醯胺或蛋氨酸;並且其中所述睫狀神經營養因子突變體保留了天然睫狀神經營養因子第40位的賴氨酸。
(2)根據(1)所述的睫狀神經營養因子突變體,其中,所述突變包括:第26位的賴氨酸突變為亮氨酸、第46位的賴氨酸突變為精氨酸、第160位的賴氨酸突變為穀氨醯胺。
(3)根據(1)或(2)所述的睫狀神經營養因子突變體,其中,所述突變還包括:第17位半胱氨酸突變為丙氨酸、第63位穀氨醯胺突變為精氨酸、以及去除天然睫狀神經營養因子C末端的15個胺基酸。
(4)根據(1)所述的睫狀神經營養因子突變體,其中,所述的睫狀神經營養因子突變體具有SEQ ID NO:4所示的胺基酸序列。
(5)一種DNA,其中,所述DNA的核苷酸序列為編碼根據(1)至(4)中任一項所述的睫狀神經營養因子突變體的核苷酸序列。
(6)根據(5)所述的DNA,其中,所述DNA的核苷酸序列為SEQ ID NO:3所示的核苷酸序列。
(7)一種重組表達載體,其中,所述重組表達載體含有(5) 或(6)所述的核苷酸序列。
(8)根據(7)所述的重組表達載體,其中,所述重組表達載體為PET24a+/CNTFnew/Clys3表達載體。
(9)一種遺傳工程宿主細胞,其中,所述宿主細胞含有(7)或(8)所述的重組表達載體。
(10)根據(9)所述的遺傳工程宿主細胞,其中,所述宿主細胞為CNTFnew/Clys3工程菌。
(11)一種修飾型睫狀神經營養因子突變體,其中,所述的修飾型睫狀神經營養因子是通過對根據(1)至(4)中任一項所述的睫狀神經營養因子突變體的第40位賴氨酸進行定點修飾而得到的,所述定點修飾是通過在所述的第40位賴氨酸上結合化學修飾劑而實現的。
(12)根據(11)所述的修飾型睫狀神經營養因子突變體,其中,所述化學修飾劑為聚乙二醇或聚乙二醇類聚合物。
(13)根據(11)所述的修飾型睫狀神經營養因子突變體,其中,所述的化學修飾劑選自:聚乙二醇、甲氧基聚乙二醇、甲氧基聚乙二醇-琥珀醯亞胺琥珀酸酯、甲氧基聚乙二醇-琥珀醯亞胺碳酸酯、甲氧基聚乙二醇三氟乙基磺酸酯、甲氧基聚乙二醇-丙醛、甲氧基聚乙二醇-琥珀醯亞胺丙酸酯、甲氧基聚乙二醇-琥珀醯亞胺-α-甲基丁酸酯、甲氧基聚乙二醇-N-羥基琥珀醯亞胺、甲氧基聚乙二醇-馬來醯亞胺或甲氧基聚乙二醇-乙醛。
(14)根據(11)所述的修飾型睫狀神經營養因子突變體,其中,所述化學修飾劑為甲氧基聚乙二醇-乙醛。
(15)根據(1)至(4)中任一項所述的睫狀神經營養因子突變體在製備用於治療和/或預防肥胖症或與肥胖症相關的疾病的藥物中的應用。
(16)根據(11)至(14)中任意一項所述的修飾型睫狀神經營養因子突變體在製備用於治療和/或預防肥胖症或與肥胖症相關的疾病的藥物中的應用。
(17)一種用於治療和/或預防肥胖症及肥胖相關疾病的藥物組合物,其中,所述的藥物組合物包含根據(1)至(4)中任一項所述 的睫狀神經營養因子突變體和/或根據(11)至(14)中任意一項所述的修飾型睫狀神經營養因子突變體。
本發明與現有技術相比具有以下優點和積極效果:
1.本發明驚奇地發現將化學修飾劑定點修飾在CNTF第40位賴氨酸的ε氨基上,同時將CNTF第26位的賴氨酸突變為異亮氨酸或亮氨酸、將第46位的賴氨酸突變為精氨酸、以及將第160位的賴氨酸突變為穀氨醯胺或蛋氨酸,可以在保持蛋白質原有結構和生物學活性的同時,獲得修飾專一性高的修飾型睫狀神經營養因子,從而克服隨機修飾帶來的如修飾結果不穩定等一系列問題。
2.本發明的重組基因工程CNTF與原始CNTF蛋白序列與結構最為接近,使重組CNTF突變體蛋白穩定性、可溶性和生物學活性高於天然蛋白。
3.本發明獲得的CNTF突變體結構穩定,與天然蛋白相比具有更高的生物學活性和可溶性,並且修飾型CNTF與未修飾型CNTF相比具有長效作用,從而能達到治療或預防肥胖症及其相關疾病的顯著效果。
附圖說明
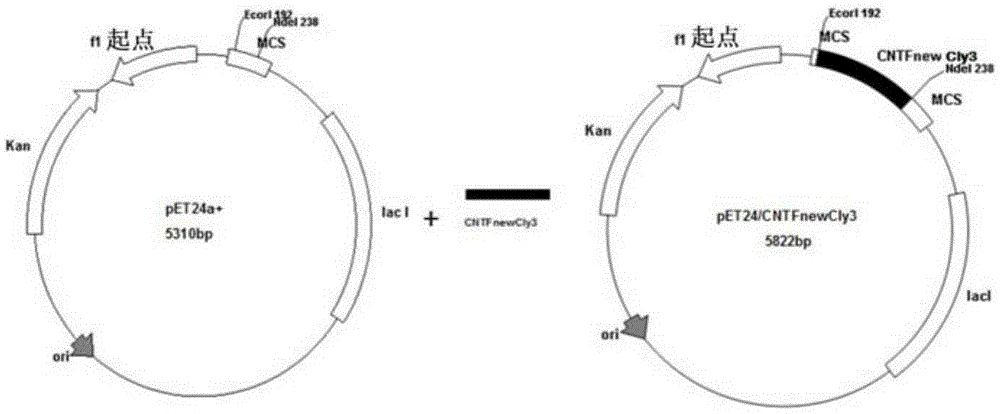
圖1為CNTF突變體表達載體PET24a+/CNTFnew/Clys3的構建圖。
圖2為CNTF突變體CNTFnew/Clys3的編碼序列PCR鑑定圖;其中,M:marker;1:陰性對照;2-6:隨機挑選的5個CNTFnew/Clys3工程菌的菌落。
圖3為NedI和EcorI雙酶切鑑定的結果圖;其中,M:marker;1-5:隨機挑選的5個CNTFnew/Clys3工程菌菌落。
圖4為CNTF突變體CNTFnew/Clys3的全基因序列測定結果圖。
圖5為目的蛋白CNTFnew/Clys3的表達結果圖;其中,M:marker;1:陰性對照;2-6:隨機挑選的5個CNTFnew/Clys3工程菌菌落。
圖6為CNTFnew/Clys3蛋白SDS-PAGE電泳圖;其中泳道M為 Marker,泳道2為CNTFnew/Clys3蛋白。
圖7為CNTFnew/Clys3蛋白的N端15個胺基酸序列的序列比對圖。
圖8為小鼠體重變化圖。
圖9為小鼠體重增長抑制率圖。
圖10為CNTFnew/Clys3蛋白與ALD-mPEG分子結合的示意圖。
圖11為用支鏈的ALD-mPEG修飾CNTFnew/Clys3的結果的電泳圖;其中,泳道M為Marker,泳道2為修飾前的CNTFnew/Clys3蛋白,泳道3為修飾反應混合液。
圖12為純化後的支鏈ALD-mPEG修飾CNTFnew/Clys3蛋白電泳圖,其中泳道M為Marker,泳道2為ALD-mPEG-CNTFnew/Clys3。
圖13為ALD-mPEG-CNTFnew/Clys3和CNTFnew/Clys3蛋白免疫印跡電泳圖,其中泳道M為Marker,泳道2為ALD-mPEG-CNTFnew/Clys3,泳道3為CNTFnew/Clys3。
具體實施方式
以下通過具體實施方式的描述並參照附圖對本發明作進一步說明,但這並非是對本發明的限制,本領域技術人員根據本發明的基本思想,可以做出各種修改或改進,但是只要不脫離本發明的基本思想,均在本發明的範圍之內。
本發明的目的在於提供一種睫狀神經營養因子突變體與一種修飾型睫狀神經營養因子,以在提高睫狀神經營養因子的治療效果的前提下,獲得修飾後性狀均一的修飾型的睫狀神經營養因子。
通過對CNTF胺基酸序列(SEQ ID NO:2)進行系統的理論分析和設計並且進行大量的試驗,本發明的發明人驚奇地發現在使用PEG或PEG類聚合物對CNTF或CNTF突變體進行修飾時,將化學修飾劑定點修飾在CNTF第40位賴氨酸上,同時將CNTF第26位的賴氨酸突變為異亮氨酸或亮氨酸、將第46位的賴氨酸突變為精氨酸、以及將第160位的賴氨酸突變為穀氨醯胺或蛋氨酸,可以在保持蛋白質原有結構和生物學活性的同時,獲得修飾專一性高的修飾型睫狀神經 營養因子,從而克服隨機修飾帶來的如修飾結果不穩定等一系列問題。
基於以上發現,本發明一個方面提供了一種睫狀神經營養因子突變體,其中,所述睫狀神經營養因子突變體是在天然睫狀神經營養因子的胺基酸序列的基礎上發生突變得到的,所述突變包括:第26位的賴氨酸突變為異亮氨酸或亮氨酸、第46位的賴氨酸突變為精氨酸、第160位的賴氨酸突變為穀氨醯胺或蛋氨酸;並且其中所述睫狀神經營養因子突變體保留了天然睫狀神經營養因子第40位的賴氨酸。
優選地,所述第26位的賴氨酸被突變為亮氨酸、第46位的賴氨酸被突變為精氨酸、第160位的賴氨酸被突變為穀氨醯胺。
本發明人通過實驗進一步發現,在上述重組基因工程CNTF的基礎上,使用常規突變CNTF的方法,例如將第17位半胱氨酸突變為丙氨酸、第63位穀氨醯胺突變成精氨酸、去除C末端的15個胺基酸等,也不會影響CNTF突變體在化學修飾中的穩定性,可以形成修飾均一的修飾型CNTF突變體,並獲得與天然蛋白相比更高的生物學活性和長效作用,從而能達到治療或預防肥胖症及其相關疾病的顯著效果。
因此,在本發明的睫狀神經營養因子突變體中,所述突變還可以包括:第17位半胱氨酸突變為丙氨酸、第63位穀氨醯胺突變為精氨酸、以及去除天然睫狀神經營養因子C末端的15個胺基酸。
優選地,所述的睫狀神經營養因子突變體具有SEQ ID NO:4所示的胺基酸序列。
本發明所述的CNTF突變體與原始CNTF蛋白序列和結構最為接近,使CNTF突變體蛋白穩定性、可溶性和生物學活性高於天然蛋白。
可以使用本領域已知的常規方法獲得CNTF突變體。這些方法在(例如)專利申請CN1687413A中有所介紹。也可以採用全基因序列合成的方法獲得本發明的CNTF突變體。
本發明第二方面提供了一種DNA,其中,所述DNA的核苷酸序列為編碼本發明所述的睫狀神經營養因子突變體的核苷酸序列。
優選的是,所述DNA的核苷酸序列為SEQ ID NO:3所示的核苷 酸序列。
本發明第三方面提供了一種重組表達載體,其中,所述重組表達載體含有本發明所述DNA的核苷酸序列。
優選的是,所述重組表達載體為如圖1所示的PET24a+/CNTFnew/Clys3表達載體。
本發明第四方面提供了一種遺傳工程宿主細胞,其中,所述宿主細胞含有本發明所述的重組表達載體。
優選的是,所述宿主細胞為CNTFnew/Clys3工程菌。
本發明第五方面提供了一種修飾型睫狀神經營養因子突變體,其中,所述的修飾型睫狀神經營養因子是通過對本發明所述的睫狀神經營養因子突變體的第40位賴氨酸進行定點修飾而得到的,所述定點修飾是通過在所述的第40位賴氨酸上結合化學修飾劑而實現的。
定點修飾的方法可採用本領域已知的方法,例如張霖琳等,聚乙二醇單修飾重組人粒細胞集落刺激因子的研究,生物工程學報,2005,21(6)中公開的方法,其在4℃條件下將待修飾蛋白置於不同pH值的緩衝液中,以保證其生物學活性。Lowry法測定蛋白濃度,將蛋白稀釋到實驗所需的各個濃度,按摩爾配比(修飾劑:蛋白質)加入修飾劑,混合均勻,按正交試驗設計的溫度進行反應,反應時間為2-16小時。
所述的化學修飾劑可以使用在蛋白質工程領域中常用的化學修飾劑(包括高分子、聚合物修飾劑等),只要能夠與賴氨酸的ε氨基相結合,獲得均一的修飾後產物即可。在本文中,「均一」是指沒有同分異構體,純度在95%以上。
優選的是,所述化學修飾劑為聚乙二醇(PEG)或聚乙二醇類聚合物。
在本文中,所述的「聚乙二醇類聚合物」指的是聚乙二醇衍生物,在聚乙二醇的應用中,端基起著決定性的作用,不同端基的聚乙二醇具有不同的用途。在實際應用中,聚乙二醇高分子鏈端不僅僅局限於鏈端羥基,其它反應性更強的功能化基團,如對甲苯磺酸酯基、氨基、羧基、醛基等亦可被引入到聚乙二醇鏈的兩端。這些功能化基團的引 入擴大了聚乙二醇的應用範圍,使它在有機合成、多肽合成、高分子合成及藥物的緩釋控釋、靶向施藥等多方面均具有廣闊的應用前景。
更優選的是,本發明的用於修飾的聚乙二醇或聚乙二醇類聚合物的分子量為20kD~40kD。
優選的是,所述的化學修飾劑選自:聚乙二醇、甲氧基聚乙二醇、甲氧基聚乙二醇-琥珀醯亞胺琥珀酸酯、甲氧基聚乙二醇-琥珀醯亞胺碳酸酯、甲氧基聚乙二醇三氟乙基磺酸酯、甲氧基聚乙二醇-丙醛、甲氧基聚乙二醇-琥珀醯亞胺丙酸酯、甲氧基聚乙二醇-琥珀醯亞胺-α-甲基丁酸酯、甲氧基聚乙二醇-N-羥基琥珀醯亞胺、甲氧基聚乙二醇-馬來醯亞胺或甲氧基聚乙二醇-乙醛。
更優選地,所述化學修飾劑為甲氧基聚乙二醇-乙醛。
本發明第六方面提供了所述的睫狀神經營養因子突變體在製備用於治療和/或預防肥胖症或與肥胖症相關的疾病(如Ⅱ型糖尿病和脂肪肝)的藥物中的應用。
本發明第七方面提供了所述的修飾型睫狀神經營養因子突變體在製備用於治療和/或預防肥胖症或與肥胖症相關的疾病(如Ⅱ型糖尿病和脂肪肝)的藥物中的應用。
本發明第八方面提供了一種用於治療和/或預防肥胖症及肥胖相關疾病的藥物組合物,其中,所述的藥物組合物包含本發明所述的睫狀神經營養因子突變體和/或本發明所述的修飾型睫狀神經營養因子突變體。
所述肥胖相關疾病包括II型糖尿病和脂肪肝。
優選的是,所述的藥物組合物還包含藥用輔料。用於本發明的藥用輔料可以為本領域常規使用的那些。
以下通過實施例的方式進一步解釋或說明本發明內容,但這些實施例不應被理解為對本發明保護範圍的限制。
實施例1.CNTF突變體的全基因序列合成
根據天然睫狀神經營養因子(CNTF)DNA序列(SEQ ID NO:1)與天然睫狀神經營養因子(CNTF)胺基酸序列(SEQ ID NO:2), 全基因序列合成重組睫狀神經營養因子(CNTF突變體)的DNA序列SEQ ID NO:3(由上海捷銳生物科技有限公司完成),其編碼的胺基酸序列為SEQ ID NO:4。
其中,CNTF突變體為將天然睫狀神經營養因子的第26位的賴氨酸突變為亮氨酸、第46位的賴氨酸突變為精氨酸、第160位的賴氨酸突變為穀氨醯胺、第17位半胱氨酸突變成丙氨酸、第63位穀氨醯胺突變成精氨酸,並且去除C末端的15個胺基酸而形成的CNTF突變體——CNTFnew/Clys3突變體。
實施例2.CNTF突變體CNTFnew/Clys3表達載體的構建與工程菌的鑑定
(1)CNTF突變體CNTFnew/Clys3表達載體的構建
全基因序列合成後,取合成片段5μL,加入限制性內切酶NedI1μL和EcorI 1μL(限制性內切酶購於TAKARA公司)。加入限制性內切酶緩衝液2μL,加雙蒸水11μL,成為20μL體系。37℃水浴,酶切1小時。同時,取pET24a+質粒(購於Novagen公司)5μL,加入相同的限制性內切酶NedI 1μL和EcorI 1μL(限制性內切酶購於TAKARA公司),加雙蒸水11μL,成為20μL體系。37℃水浴,酶切1小時,酶切載體pET24a+。
酶切完成後,進行1%的瓊脂糖凝膠電泳。切割下帶有目的條帶的膠,利用瓊脂糖凝膠回收試劑盒(購於天根生化科技有限公司)對酶切後的目的片段和載體片段進行回收。
取酶切後的合成目的片段5μL、酶切後的載體pET24a+5μL,加入1μL T4DNA連接酶(購於TAKARA公司),加入10×連接酶緩衝液2μL,加入雙蒸水7μL,成為20μL的連接反應體系。16℃連接過夜。連接成表達載體,命名為PET24a+/CNTFnew/Clys3,具體的載體構建過程可以參看圖1。
(2)將表達載體PET24a+/CNTFnew/Clys3轉化到感受態細胞BL21(DE3)(購於天根生化科技有限公司)中,製備出CNTFnew/Clys3工程菌。
具體步驟:取連接後的表達載體PET24a+/CNTFnew/Clys3共2μL,加入到一支感受態細胞BL21(DE3)中,輕敲後放置於冰上30分鐘,42℃水浴熱激60秒後,迅速至於冰上2分鐘。加入不含抗生素的LB液體培養基300μL,至於搖床中,37℃、200轉/分鐘培養1小時。經過培養後的菌液塗於含50μg/ml卡那黴素的LB固體培養基平板上,於37℃培養箱中過夜培養,得到帶有PET24a+/CNTFnew/Clys3質粒的單個菌落。
隨機挑取單個菌落,接種到5ml LB液體培養基中,37℃、200轉/分鐘過夜培養。得到工程菌,命名為CNTFnew/Clys3工程菌。
(3)經過PCR鑑定、雙酶切鑑定、全基因序列測定三種方法確定CNTFnew/Clys3工程菌中包含有目的蛋白CNTFnew/Clys3的編碼序列。
3.1)PCR鑑定過程:取過夜培養的CNTFnew/Clys3工程菌的菌液1μL,加入引物1(序列為:ATG GCT TTC ACA GAG CAT TC)1μL、引物2(序列為:GTC ATG GAT GGA CCT TAC TG)1μL、DNA Polymerase(購自TAKARA公司)1μL、2×PCR緩衝液10μL、雙蒸水6μL,成為20μL的PCR反應體系。
放入PCR儀中,溫度循環為:第一步:94℃5分鐘。第二步:94℃30秒、55℃30秒、72℃1分鐘,共30個循環。第三步:72℃10分鐘。第四步:4℃恆溫後取出。
PCR結束後對樣品進行1%的瓊脂糖凝膠電泳,觀察結果。
PCR鑑定的結果參見圖2,其中,M:marker;1:陰性對照;2-6:隨機挑選的5個CNTFnew/Clys3工程菌菌落的結果。
PCR鑑定結果為:隨機挑取的5個工程菌菌落均為陽性菌落。
3.2)雙酶切鑑定過程:
取過夜培養的CNTFnew/Clys3工程菌的菌液5ml,利用質粒小量提取試劑盒(購於Axeygen公司)提取質粒。提取的質粒取5μL,限制性內切酶NedI和EcorI各1μL,限制性內切酶緩衝液2μL,雙蒸水11μL,成為20μL的雙酶切體系,於37℃水浴,酶切1小時,之後進行1%的瓊脂糖凝膠電泳,觀察結果。
雙酶切鑑定的結果參見附圖3,其中,M:marker;1-5:隨機挑選的5個CNTFnew/Clys3工程菌菌落的結果。
雙酶切鑑定結果為:隨機挑取的5個工程菌菌落均為陽性菌落。
3.3)CNTFnew/Clys3的全基因序列測定由北京諾賽基因組研究中心完成。具體結果見圖4。
實施例3.目的蛋白CNTFnew/Clys3的表達。
1)製備LB瓊脂平板:胰蛋白腖10g、酵母提取物5g、NaCl 5g,瓊脂10g、加水定容至1L(pH為7.2±0.1),高溫高壓滅菌,當溫度降到50℃左右時加入卡那黴素,至終濃度為50μg/ml,取20ml倒培養皿,凝固後即成LB瓊脂平板。
2)培養CNTFnew/Clys3工程菌:將CNTFnew/Clys3工程菌劃線接種於LB瓊脂平板,37℃培養過夜。從培養基過夜的LB平板上挑選生長狀態良好的單個菌落,接種於含LB的試管中,37℃培養10小時。然後轉種至含有200ml LB液體培養液(胰蛋白腖10g、酵母提取物5g、NaCl 5g,加水定容至1L(pH為7.2±0.1),高壓滅菌,分裝三角瓶,每瓶200ml)的三角瓶中,37℃培養過夜製得種子液。將種子液按1%比例接種於含30L 2YT培養液的50L發酵罐中,發酵培養基為2YT(胰蛋白腖480g、酵母提取物300g、NaCl 50g,加入蒸餾水溶解,5N NaOH調節PH至7.0,定容到30L,0.12Mpa、121℃、30分鐘,高壓滅菌)。控制發酵溫度37℃、轉速250-450r/分鐘、通氣量30-50L/分鐘、pH7.3,培養至A600=1.2左右後,加入異丙基硫代-β-D-半乳糖苷(IPTG)至終濃度為1.0mM進行誘導。繼續培養4.5小時,終止發酵,收集菌體,儲存於-30℃冰箱中備用。取表達目的蛋白後的菌體,進行SDS-PAGE電泳,觀察目的蛋白CNTFnew/Clys3的表達結果見圖5,其中,M:marker;1:陰性對照;2-6:隨機挑選的5個CNTFnew/Clys3工程菌菌落的結果。
實施例4.目的蛋白CNTFnew/Clys3的復性與純化。
從-30℃冰箱中取出發酵菌體,按1%比例用0.02mol、pH7.2的 磷酸鹽溶液重新懸浮菌體,通過高壓勻漿破碎菌體,5000r/分鐘離心15分鐘,收集包涵體沉澱,再經變性〔每克包涵體使用400ml變性液(8M鹽酸胍、50mMTris-Hcl、pH8.0)處理4小時〕、復性(通過透析法復性,透析液為50mMTris-Hcl、pH8.0,透析時間為24小時)、Q-Sepharose HP(購自GE公司)層析步驟進行純化而獲得CNTFnew/Clys3。所述層析步驟簡述如下:A液50mM Tris-Hcl,pH8.0;B液50mM Tris-Hcl,1M NaCl,pH8.0;層析柱以A液平衡後,樣品以1.8mg/ml上樣,A液清洗後,用10%B洗脫,用第一個收集目的蛋白峰做SDS-PAGE,並用AlphaDigiDoc凝膠成像分析儀進行成像,用AlphaDigiDoc純度分析軟體對CNTFnew/Clys3泳道進行掃描純度分析,結果純度可達95%以上。純化結果見圖6,其中泳道M為Marker,泳道2為純化的CNTFnew/Clys3蛋白。
實施例5.CNTFnew/Clys3蛋白的N端15個胺基酸序列測定。
序列比對為將CNTFnew/Clys3蛋白的N端15個胺基酸序列與天然CNTF的N端測序結果進行比對,測定結果見圖7。結果說明CNTFnew/Clys3蛋白的N端15個胺基酸序列的測序結果與預先設計完全相同。
實施例6.CNTFnew/Clys3體外活性鑑定。
TF-1CN5a1細胞是一個依賴於GM-CSF的細胞系,其細胞表面具有rhCNTF高親和力受體,所以CNTF能促進TF-1CN5a1細胞的增殖。將不同濃度的CNTFnew/Clys3加入TF-1CN5a1細胞培養物中,觀察細胞的生長情況,以測定CNTFnew/Clys3體外活性,具體方法如下:
將TF-1CN5a1細胞(購自美國ATCC,貨號為CRL-2512TM),常規培養於GM-CSF條件(100ml RPMI1640中含有500ng的GM-CSF)的培養液中,實驗時收集對數生長期的細胞,用無血清的RPMI 1640(購自invitrogen公司)洗液洗滌3遍,然後用10%小牛血清RPMI 1640培養液調整細胞數為1.0×106,每孔加50μl細胞懸液, 使用實施例4中獲得的CNTFnew/Clys3蛋白從初始濃度200n g/ml按4倍系列稀釋後,每孔加入50μl。以50μl無血清RPMI 1640培養基作為陰性對照,以CNTF標準品(購自英國國家生物製品檢定所NIBSC,貨號:94/684)為陽性對照,初始濃度為200ng/ml,進行4倍系列稀釋後,每孔加入50μl。培養板在37℃、5%CO2條件下培養48小時後,每孔加入50mg/ml的WST-8(購自碧雲天生物技術研究所,貨號:C0038)溶液20μl,繼續培養8小時後,加入酸性異丙醇(異丙醇-HCL,pH4.0)溶液,混勻後在酶標儀上比色,測定波長為570nm,參比波長為630nm。每個實驗取3次實驗的平均結果。結果為CNTFnew/Clys3蛋白的體外活性:7.9×106IU/mg。實驗同時設置了未突變的睫狀神經營養因子對照組(購自sigma,C3710-10UG),在相同的方法和條件下測定,實驗結果證實未突變的睫狀神經營養因子的體外活性約為8.57×104IU/mg,經過定點突變的睫狀神經營養因子突變體的生物學活性高於未突變的天然分子。
實施例7.CNTFnew/Clys3在小鼠體內活性的測定。
實驗用小鼠使用雄性昆明鼠(得自北京維通利華實驗動物技術有限公司),體重18g-22g。分為陽性對照組,陰性對照組和實驗組,每組6隻。用生理鹽水溶解CNTF標準品(購自英國國家生物製品檢定所NIBSC,貨號:NIBSC94/684)作為陽性對照,樣品為CNTFnew/Clys3(實施例4所得蛋白),同樣以生理鹽水溶解並稀釋為12.5μg/ml。以每隻小鼠125μg/kg/天的量,經過計算取不同的體積進行皮下注射。陰性對照即生理鹽水。注射前分別稱量每組每隻小鼠的體重。連續五天給藥,稱量小鼠的體重,觀察小鼠的體重變化。
(1)流程:
表1.CNTF對小鼠減重作用測定流程
註:實驗時間以給藥前一天為-1天,首次給藥當天為0天。
△:根據前一操作完成情況,可提前或推後,但儘量保持每天在同一時間。
(2)測量指標:
體重增加值=某組實驗前體重-某組實驗某日體重
體重增長抑制率(%)=(對照組某日體重-對照組d0體重)-(受試組某日體重-該組d0體重)/(對照組某日體重-對照組d0體重)×100%
結果:
表2.小鼠體重變化
與表2對應的小鼠體重變化圖見圖8。
由表2可知:在給藥之後,實驗組體重一直下降,而陽性對照組和陰性對照組體重均增加,提示CNTFnew/Clys3具有很強的體重控制活性。
表3.小鼠體重增長抑制率
與表3對應的小鼠體重增長抑制率圖見圖9。
由表3可知,CNTFnew/Clys3體重增長抑制率高於陽性對照(CNTF標準品)的體重增長抑制率。
實施例8.CNTFnew/Clys3蛋白的修飾以及純化:
本實施例中利用支鏈的mPEG-ALD對上面步驟獲得的CNTFnew/Clys3蛋白進行修飾。
支鏈40KD的mPEG-ALD購於北京凱正科技有限公司,商品代號:Y-ALD-40K。分子式見下:
CNTFnew/Clys3蛋白與ALD-mPEG分子結合的示意圖見圖10。
將純化的CNTFnew/Clys3蛋白與分子量40KD的ALD-mPEG按摩爾比1:5的比例混合,反應在100mmol/L的磷酸鈉緩衝液(pH8.0,含1mmol/L的EDTA)中進行,置4℃反應16小時。修飾反應結果見圖11。泳道M為Marker,泳道2為修飾前的CNTFnew/Clys3蛋白,泳道3為修飾反應混合液。採用陰離子交換介質Q FF(購自美國GE公司,型號:Hiprep16/10 Q FF)對修飾反應混合液進行修飾劑、未修飾蛋白及修飾產物的分離。平衡緩衝液為50mM Tris-HCl,pH8.0,5個柱體積內用緩衝液B(50mM Tris-HCl,pH8.0,1M NaCl)進行梯度洗脫,收集目的蛋白洗脫峰,進行SDS-PAGE分析,結果見圖12。泳道M為Marker,泳道2為ALD-mPEG-CNTFnew/Clys3。
實施例9.修飾後蛋白體外活性的測定。
TF-1CN5a1細胞是一個依賴於GM-CSF的細胞系,其細胞表面具有rhCNTF高親和力受體,所以CNTF能促進TF-1CN5a1細胞的增殖。將不同濃度的ALD-mPEG-CNTFnew/Clys3加入TF-1CN5a1細胞培養物中,觀察細胞的生長情況,以測定ALD-mPEG-CNTFnew/Clys3體外活性,具體方法如下:
將TF-1CN5a1細胞(購自美國ATCC,貨號為CRL-2512TM),常規培養於GM-CSF條件(100ml RPMI 1640中含有500ng的GM-CSF)的培養液中,實驗時收集對數生長期的細胞,用無血清的RPMI1640(購自invitrogen公司)洗液洗滌3遍,然後用10%小牛血清RPMI1640培養液調整細胞數為1.0×106,每孔加50μl細胞懸液,使用實施例8獲得的ALD-mPEG-CNTFnew/Clys3蛋白,起始濃度為200ng/ml,按4倍系列稀釋後,每孔加入50μl。以50μl無血清RPM1640培養基作為陰性對照,以CNTF標準品(購自英國國家生物製品檢定所NIBSC,貨號:94/684)為陽性對照,初始濃度為200ng/ml,進行4倍系列稀釋後,每孔加入50μl。培養板在37℃、5%CO2條件下培養48小時後,每孔加入50mg/ml的WST-8(購自碧雲天生物技術研究所。貨號:C0038)溶液20μl,繼續培養8小時後,加入酸性異丙醇(異丙醇-HCL,pH4.0)溶液,混勻後在酶標儀上比色,測定波長為570nm,參比波長為630nm。每個實驗取3次實驗的平均結果。測定方法同實施例6的未修飾的CNTF蛋白,結果為:
支鏈40K的ALD-mPEG修飾的CNTFnew/Clys3蛋白的體外活性為:3.9×106IU/mg(為平均結果)。上述結果說明經40K的PEG修飾後,經過定點突變的睫狀神經營養因子突變體的體外生物學活性有所降低,修飾產物活性保留率為49%,但體外活性均遠高於陽性對照組8×105IU/mg(p<0.05)。
實施例10 ALD-mPEG-CNTFnew/Clys3在小鼠體內活性的測定
實驗用小鼠使用雄性昆明鼠(得自北京維通利華實驗動物技術有 限公司),體重18-22g。分為陽性對照組、陰性對照組和實驗組,每組8隻。用生理鹽水溶解CNTF標準品(購自英國國家生物製品檢定所NIBSC,貨號:NIBSC94/684)作為陽性對照,實驗組樣品為ALD-mPEG-CNTFnew/Clys3(實施例8獲得),以生理鹽水溶解並稀釋為0.5mg/ml。以每隻小鼠100μg/kg/天的量進行皮下注射。陰性對照即生理鹽水。注射前分別稱量每組每隻小鼠的體重。連續五天給藥,稱量小鼠的體重,觀察小鼠的體重變化。另同時設置每周注射組,分為修飾樣品組,未修飾樣品組,陽性對照組及陰性對照組,以每隻小鼠200μg/kg/天的量進行皮下注射。陰性對照即生理鹽水。注射前分別稱量每組每隻小鼠的體重。為了證明ALD-mPEG-CNTFnew/Clys3具有長效性,給藥方式分兩種,一種是每天給藥,連續給藥五天,另一種是每周給藥一次,並分別稱量小鼠的體重,觀察小鼠的體重變化。
(1)流程如下表4:
表4.CNTF對小鼠減重作用測定流程(每天)
註:實驗時間以給藥前一天為-1天,首次給藥當天為0天。
△:根據前一操作完成情況,可提前或推後,但儘量保持每天在同一時間。
表5.CNTF對小鼠減重作用測定流程(每周)
註:實驗時間以給藥前一天為-1天,首次給藥當天為0天。
△:根據前一操作完成情況,可提前或推後,但儘量保持每天在同一時間。
(2)測量指標:體重變化率
體重變化率=(某組給藥後體重-某組給藥前體重)/給藥前體重×100%;
體重增長抑制率(%)=(對照組某日體重-對照組d0體重)-(受試組某日體重-該組d0體重)/(對照組某日體重-對照組d0體重)×100%
小鼠體重變化結果見表6和表7:
表6小鼠體重變化表(連續5天給藥)
由表6可知:樣品ALD-mPEG-CNTFnew/Clys3,CNTFnew/Clys3 兩組注射後的小鼠,體重均有所增長,但是小鼠體重增長均小於陰性對照組(p<0.05),同時小於陽性對照(CNTF標準品)組(p<0.05)。
表7 小鼠體重變化表(每周給藥1次)
由表7可知:對於每周1次給藥組,三組注射後的小鼠,體重均有所增長,但是修飾樣品組的小鼠體重增長小於陰性對照組(p<0.05),同時小於陽性對照(CNTF標準品)組(p<0.05)。
研究證實PEG修飾藥物與未修飾藥物相比較具有長效作用。
(2)小鼠體重增長抑制率見下表8:
表8 小鼠體重增長抑制率(連續5天給藥)
由表8可知ALD-mPEG-CNTFnew/Clys3對小鼠的體重增長抑制率高於陽性對照(CNTF標準品)的體重增長抑制率(p<0.05)。
表9 小鼠體重增長抑制率(每周給藥1次)
由表9可知在每周給藥一次的情況下,ALD-mPEG-CNTFnew/Clys3對小鼠的體重增長抑制率與對照組比較有顯著差異(p<0.01),特別是ALD-mPEG-CNTFnew/Clys3樣品每周給藥一次即可達到CNTFnew/Clys3每天給藥效果,而CNTFnew/Clys3每周給藥一次不能有效抑制小鼠體重的增長。說明ALD-mPEG-CNTFnew/Clys3有長效的抑制小鼠體重的效果。
實施例11.CNTFnew/Clys3以及ALD-mPEG-CNTFnew/Clys3的免疫反應性
以CNTF的單克隆抗體作為特異性抗體進行蛋白質免疫印跡實驗,研究免疫反應性。
用CNTF的單克隆抗體(購自Abcam公司)作為一抗,以辣根過氧化物酶標記的羊抗鼠IgG作為酶標二抗。首先將CNTFnew/Clys3和ALD-mPEG-CNTFnew/Clys3做SDS-PAGE電泳,分離膠濃度為12%,濃縮膠濃度為4%,上樣量為15μl,恆壓110V,電泳1.5小時,終止電泳,將凝膠轉入NC膜上,分別與一抗和二抗孵育後顯色。具 體結果見圖13,泳道M為Marker,泳道2為ALD-mPEG-CNTFnew/Clys3,泳道3為CNTFnew/Clys3。結果顯示CNTFnew/Clyss3與ALD-mPEG-CNTFnew/Clys3均能夠與CNTF的單克隆抗體特異性結合,說明位點突變並且經過PEG修飾後仍具有與天然CNTF相似的免疫反應性,沒有改變蛋白與特異性抗體結合的能力。
以上所述僅為本發明的較佳實施例,並不用以限制本發明,凡在本發明的精神和原則之內,所作的任何修改、等同替換、改進等,均應包含在本發明的保護範圍之內。
