一種磷酸鐵鋰/碳複合材料的製備方法與流程
2023-04-23 03:52:52 3
一種磷酸鐵鋰/碳複合材料的製備方法【技術領域】本發明涉及鋰離子電池材料技術領域,尤其涉及一種磷酸鐵鋰/碳複合材料的製備方法。
背景技術:
鋰離子電池因具有工作電壓高、比熱量高、容量大、自放電小、循環性小、使用壽命長、重量輕、體積小等突出優點而成為行動電話、筆記本電腦等可攜式電子設備的理想電源;而近年來隨著環境問題的日趨嚴重,鋰離子電子競相用於電動汽車、混合動力汽車等氣體排放量少的交通工具上,這對鋰離子電池的安全性、功率及壽命提高了更高的要求。自1997年來,Padhi和Goodenough等人報導具有橄欖石相的磷酸鐵鋰(LiFePO4)可以作為鋰離子電池的正極材料以來,由於其優良的電化學性能、豐富的原料來源、較好的安全性能、可在高溫條件下使用等特點而受到廣大科研機構和商業公司的青睞。目前,合成LiFePO4一般採用固相法和液相法。其中,採用液相法製備LiFePO4,生產效率低,成本較高,導致了其產業化程度低,難以實現大規模工業生產;固相法由於其生產工藝簡單、成本較低,是目前產業化生產的主要製備方法。固相法的製備過程是將鐵源、鋰源和磷源化合物通過球磨分散,然後再通過高溫燒結得到磷酸鐵鋰正極材料。在實際製備過程中,鐵源可以為氧化鐵,該生產過程容易控制,成本較低,產品一致性較好,易產業化,但是,控制鐵的還原尤其重要,在實際生產中需要包覆大量碳源,這樣導致材料克容量低,降低了材料的容量;鐵源也可以為草酸亞鐵,材料克容量高,粒度小,易生產容量型電池,但是,材料加工過程需要多量N-甲基吡咯烷酮(N-Methylpyrrolidone;NMP),水系有可能出現果凍狀,導致其自放電過大,且生產成本高;鐵源也可以為磷酸鐵,雖然材料克容量高,但是,生產環節不好控制,前軀體在混合和燒成工藝中,溫度高或時間長都會造成材料不穩定,且生產成本高;另外,也有採用單質鐵作為鐵源,馬紫峰等在CN1581537A中採用鐵粉、磷酸鐵、磷酸鋰、摻雜元素磷酸鹽和導電劑機械固相法製備磷酸鐵鋰材料;張俊喜等在CN102244247A中將三氧化二鐵、還原劑鐵粉、輔助還原劑、磷酸、氫氧化鋰通過球磨分散後高溫燒結得到LiFePO4/C複合材料等,但是在以上已有的用單質鐵作為還原劑還原三價鐵製備磷酸鐵鋰技術中,都是以磷酸鐵以及鐵的氧化物作為鐵源,其不易與鐵粉反應,生產效率低。
技術實現要素:
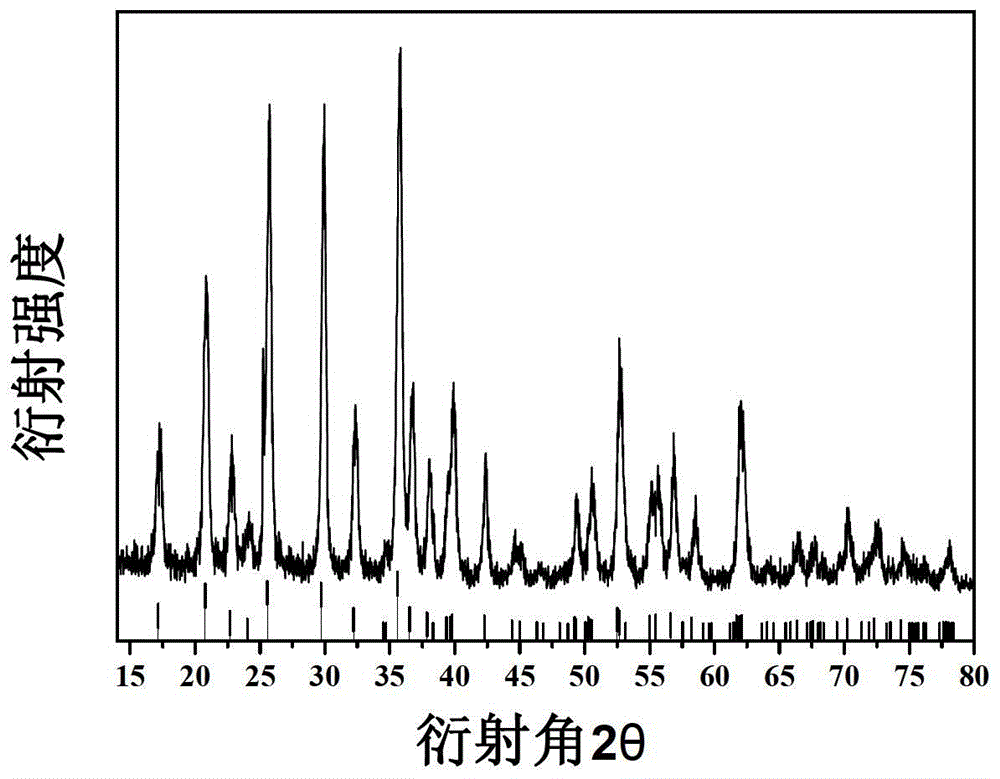
本發明要解決的技術問題在於克服現有技術製備磷酸鐵鋰/碳複合材料生產效率低、成本高、工藝複雜的缺陷,提供一種生產效率高、成本低廉、工藝簡單的磷酸鐵鋰/碳複合材料的製備方法。為解決上述技術問題,本發明採用下述技術方案:一種磷酸鐵鋰/碳複合材料的製備方法,包括下述步驟:將三價鐵鹽、鐵粉、鋰源和磷源均勻混合;在上述混合物中加入碳源、球磨劑及反應助劑,並充分球磨,其中,所述球磨劑為乙醇和去離子水的至少一種,所述反應助劑為鹽酸;將球磨後得到的前驅體,在惰性氣體環境中於600~800℃焙燒,得到所述磷酸鐵鋰/碳複合材料。在本實施中,所述三價鐵鹽為氯化鐵。在本實施中,所述鐵粉為納米級還原性鐵粉,所述鐵粉的粒徑在40~200nm。在本實施中,所述鋰源為碳酸鋰、氫氧化鋰和醋酸鋰中的一種或多種。在本實施中,所述磷源為磷酸氫二銨、磷酸二氫銨和磷酸中的一種或多種。在本實施中,所述三價鐵鹽、鐵粉、鋰源和磷源按摩爾比為Fe3+:Fe:Li:P為2:1:(3~3.05):3混合。在本實施中,所述碳源為葡萄糖、蔗糖、檸檬酸、澱粉、炭黑和乙炔黑中的一種或多種。在本實施中,所述鹽酸中的H+與所述三價鐵鹽中的Fe3+的摩爾比為1:10。在本實施中,所述球磨的時間為2h~5h。在本實施中,所述焙燒的時間為5h~10h。採用上述技術方案,本發明的有益效果在於:本發明上述實施例提供的磷酸鐵鋰/碳複合材料的製備方法,採用三價鐵鹽作為鐵源,單質鐵粉作為還原劑和鐵源之一,並加入鋰源、磷源、碳源、球磨劑以及反應助劑機械球磨後,於惰性氣體環境中焙燒,得到磷酸鐵鋰/碳複合材料。由於,採用三價鐵鹽作為鐵源,以單質鐵還原三價鐵鹽獲得二價鐵,避免了在以Fe2O3為鐵源的碳熱還原中需要加入大量碳源導致材料客容量低的缺陷;及以草酸亞鐵和磷酸鐵為鐵源的碳熱還原中成本高,工藝難控制的問題;和以單質鐵為鐵源,導致生產效率低的弊端,提高了生產效率,改善了材料的性能,工藝簡單;同時,原材料來源廣,成本低廉,降低了生產成本,適合於工業化生產。另外,在反應中還加入了反應助劑,使得反應更加完全、充分,進一步提高了生產效率。【附圖說明】圖1為本發明實施例提供的磷酸鐵鋰/碳複合材料的製備方法的步驟流程圖;圖2是本發明實施例1製備的磷酸鐵鋰/碳複合材料的XRD圖譜;圖3a是本發明實施例1製備的磷酸鐵鋰/碳複合材料放大10000倍的SEM圖;圖3b是本發明實施例1製備的磷酸鐵鋰/碳複合材料放大30000倍的SEM圖;圖4是本發明實施例1製備的的磷酸鐵鋰/碳複合材料的倍率充放電曲線圖;圖5是本發明實施例1製備的的磷酸鐵鋰/碳複合材料的1C充放電的循環性能示意圖。【具體實施方式】為了使本發明的目的、技術方案及優點更加清楚明白,以下結合附圖及具體實施例,對本發明進行進一步詳細說明。應當理解,此處所描述的具體實施例僅用以解釋本發明,並不用於限定本發明。請參閱圖1,圖1為本發明實施例提供的磷酸鐵鋰/碳複合材料的製備方法的步驟流程圖100,從圖1中可見,磷酸鐵鋰/碳複合材料的製備方法包括下述步驟:步驟S110:將三價鐵鹽、鐵粉、鋰源和磷源均勻混合。在本實施例中,三價鐵鹽優選為氯化鐵。鐵粉優選為納米級還原性鐵粉,其粒徑在40~200nm之間。鋰源優選為碳酸鋰、氫氧化鋰和醋酸鋰中的一種或多種。磷源優選為磷酸氫二銨、磷酸二氫銨和磷酸中的一種或多種。在本實施例中,上述三價鐵鹽、鐵粉、鋰源和磷源按摩爾比為Fe3+:Fe:Li:P為2:1:(3~3.05):3均勻混合。可以理解,選取合適的鐵源尤為重要,本發明提供的技術方案以三價鐵鹽作為鐵源,以單質鐵粉作為還原劑和鐵源之一,原材料來源廣,成本低廉,降低了生產成本,適合於工業化生產。步驟S120:在上述混合物中加入碳源、球磨劑及反應助劑,並充分球磨,其中,球磨劑為乙醇和去離子水的至少一種,反應助劑為鹽酸。在本實施例中,碳源優選為葡萄糖、蔗糖、檸檬酸、澱粉、炭黑和乙炔黑中的一種或多種。在本實施例中,鹽酸中的H+與三價鐵鹽中的Fe3+的摩爾比為1:10。具體地,將經步驟S110後得到的混合物置於球磨罐中,加入球磨劑和反應助劑進行充分球磨混合反應,其中,球磨的時間為2h~5h。可以理解,本實施例在反應過程中添加反應助劑,加快了反應進程,使得反應更加完全、充分,提高了生產效率。步驟S130:將球磨後得到的前驅體,在惰性氣體環境中於600~800℃焙燒,得到磷酸鐵鋰/碳複合材料。在本實施例中,惰性氣體優選為N2。具體地,將球磨後的前驅體置於燒結爐中,在惰性氣體環境的保護下於600-800℃焙燒5h~10h,即可製備所述的磷酸鐵鋰/碳複合材料。可以理解,本發明採用三價鐵鹽作為鐵源,單質鐵粉作為還原劑和鐵源之一,並加入鋰源、磷源、碳源、球磨劑以及反應助劑機械球磨後,於惰性氣體環境中焙燒,從而得到磷酸鐵鋰/碳複合材料。由於,以三價鐵鹽作為鐵源,以單質鐵還原三價鐵鹽獲得二價鐵,避免了在以Fe2O3為鐵源的碳熱還原中需要加入大量碳源導致材料客容量低的缺陷;及以草酸亞鐵和磷酸鐵為鐵源的碳熱還原中成本高,工藝難控制的問題;和以單質鐵為鐵源,導致生產效率低的弊端,提高了生產效率,改善了材料的性能,工藝簡單,適合工業化生產。以下通過實施例進一步闡述本發明,這些實施例僅用於舉例說明的目的,並沒有限制本發明的範圍。除註明的具體條件外,實施例中的試驗方法均按照常規條件進行。實施例1稱取2.694gLi2CO3、1.867g還原鐵粉、18.02gFeCl3·6H2O、0.1mol磷酸、6.25g葡萄糖,混合均勻。將其放入球磨容器中球磨4h,然後置於高溫燒結爐中,在氮氣保護下於700℃燒結10h,即可製得顆粒均勻的LiFePO4/C粉末。實施例2稱取2.394gLiOH、1.867g還原鐵粉、18.02gFeCl3·6H2O、13.105g磷酸氫二銨、6.25g葡萄糖,混合均勻;將其放入球磨容器中球磨4小時,然後置於高溫燒結爐中,在氮氣保護下700℃燒結5h,即可製得顆粒均勻的LiFePO4/C粉末。實施例3:稱取6.599g醋酸鋰、1.867g還原鐵粉、18.02gFeCl3·6H2O、11.503g磷酸二氫銨、8.33g檸檬酸,混合均勻。將其放入球磨容器中球磨4小時,然後置於高溫燒結爐中,在氮氣保護下700℃燒結5h,即可製得顆粒均勻的LiFePO4/C粉末。實施例4:稱取2.694gLi2CO3、1.867g還原鐵粉、18.02gFeCl3·6H2O、13.105磷酸氫二銨、8.33g檸檬酸,混合均勻。將其放入球磨容器中球磨4h,然後置於高溫燒結爐中,在氮氣保護下700℃燒結5h,即可製得顆粒均勻的LiFePO4/C粉末。實施例5稱取2.394gLiOH、1.867g還原鐵粉、18.02gFeCl3·6H2O、0.1mol磷酸、8.33g檸檬酸,混合均勻。將其放入球磨容器中球磨4小時,然後置於高溫燒結爐中,在氮氣保護下700℃燒結5h,即可製得顆粒均勻的LiFePO4/C粉末。實施例6稱取2.394gLiOH、1.867g還原鐵粉、18.02gFeCl3·6H2O、0.1mol磷酸、3.12g炭黑,混合均勻。將其放入球磨容器中球磨4小時,然後置於高溫燒結爐中,在氮氣保護下700℃燒結5h,即可製得顆粒均勻的LiFePO4/C粉末。實施例7稱取2.394gLiOH、1.867g還原鐵粉、18.02gFeCl3·6H2O、11.503g磷酸二氫銨、6.25g葡萄糖,混合均勻。將其放入球磨容器中球磨4小時,然後置於高溫燒結爐中,在氮氣保護下700℃燒結5h,即可製得顆粒均勻的LiFePO4/C粉末。實施例8稱取2.694gLi2CO3、1.867g還原鐵粉、18.02gFeCl3·6H2O、11.503g磷酸二氫銨、8.33g檸檬酸,混合均勻。將其放入球磨容器中球磨4小時,然後置於高溫燒結爐中,在氮氣保護下700℃燒結5h,即可製得顆粒均勻的LiFePO4/C粉末。實施例9稱取6.599g醋酸鋰、1.867g還原鐵粉、18.02gFeCl3·6H2O、13.105磷酸氫二銨、6.25g葡萄糖,混合均勻。將其放入球磨容器中球磨4小時,然後置於高溫燒結爐中,在氮氣保護下700℃燒結10h,即可製得顆粒均勻的LiFePO4/C粉末。實施例10稱取2.394gLiOH、1.867g還原鐵粉、18.02gFeCl3·6H2O、0.1mol磷酸、6.25g葡萄糖,混合均勻。將其放入球磨容器中球磨4小時,然後置於高溫燒結爐中,在氮氣保護下700℃燒結10h,即可製得顆粒均勻的LiFePO4/C粉末。實施例11稱取6.599g醋酸鋰、1.867g還原鐵粉、18.02gFeCl3·6H2O、11.503g磷酸二氫銨、8.33g檸檬酸,混合均勻。將其放入球磨容器中球磨4小時,然後置於高溫燒結爐中,在氮氣保護下700℃燒結10h,即可製得顆粒均勻的LiFePO4/C粉末。實施例12稱取6.599g醋酸鋰、1.867g還原鐵粉、18.02gFeCl3·6H2O、13.105磷酸氫二銨、8.33g檸檬酸,混合均勻。將其放入球磨容器中球磨4小時,然後置於高溫燒結爐中,在氮氣保護下700℃燒結5h,即可製得顆粒均勻的LiFePO4/C粉末。實施例13稱取2.694gLi2CO3、1.867g還原鐵粉、18.02gFeCl3·6H2O、11.503g磷酸二氫銨、8.33g檸檬酸,混合均勻。將其放入球磨容器中球磨4小時,然後置於高溫燒結爐中,在氮氣保護下700℃燒結10h,即可製得顆粒均勻的LiFePO4/C粉末。實施例14稱取2.694gLi2CO3、1.867g還原鐵粉、18.02gFeCl3·6H2O、11.503g磷酸二氫銨、3.12g炭黑,混合均勻。將其放入球磨容器中球磨4小時,然後置於高溫燒結爐中,在氮氣保護下700℃燒結5h,即可製得顆粒均勻的LiFePO4/C粉末。實施例15稱取2.694gLi2CO3、1.867g還原鐵粉、18.02gFeCl3·6H2O、13.105磷酸氫二銨、3.12g炭黑,混合均勻。將其放入球磨容器中球磨4小時,然後置於高溫燒結爐中,在氮氣保護下700℃燒結5h,即可製得顆粒均勻的LiFePO4/C粉末。實施例16稱取6.599g醋酸鋰、1.867g還原鐵粉、18.02gFeCl3·6H2O、13.105磷酸氫二銨、3.12g炭黑,混合均勻。將其放入球磨容器中球磨4小時,然後置於高溫燒結爐中,在氮氣保護下700℃燒結10h,即可製得顆粒均勻的LiFePO4/C粉末。請參閱圖2,圖2為實施例1製備的磷酸鐵鋰/碳複合材料的XRD圖譜。由圖1可知,所製得的LiFePO4/C為橄欖石正交晶系純相結構,圖譜中不存在其它雜質的峰。請參閱圖3a及圖3b,圖3a及圖3b分別為實施例1製備的磷酸鐵鋰/碳複合材料放大10000和30000倍後的掃描電鏡照片,由圖3a及圖3b可見,產物為納米材料,顆粒尺寸約為50-100nm。本實施例以實施例1製備的活性物質LiFePO4/C粉末、SP碳、PVDF以質量比8:1:1的比例共稱取2g,加入適量的1-甲基-2吡咯烷酮,充分混合均勻後成漿狀塗覆於鋁箔上真空烘乾製成正極片,烘乾後切片並準確稱量其重量,作為電池正極;同時以鋰片作為對電極,微孔狀聚乙烯為隔膜,電解液用杉杉LD-124B3,在充滿氬氣的伊特克斯手套箱中用扣式電池封口機裝配成2032扣式電池。再在2.5-4.2V電影範圍內,對電池進行恆流充放電倍率測試和循環測試。請參閱圖4,圖4為實施例1製備的磷酸鐵鋰/碳複合材料的倍率充放電曲線圖。從圖4中可以看出,0.1C,0.2C,0.5C,1C,2C,5C的充放電容量分別達到153mAh/g,143mAh/g,132mAh/g,125mAh/g,118mAh/g,103mAh/g;可見,該鋰離子電池具有良好的倍率性能。請參閱圖5,圖5為實施例1製備的磷酸鐵鋰/碳複合材料的1C充放電的循環性能示意圖。從圖5中可以看出,1C充放電100個循環後該鋰離子電池的容量保持率為97.4%。可見,該鋰離子具有優異的循環穩定性能。以上所述,僅是本發明的較佳實施例而已,並非對本發明作任何形式上的限制,雖然本發明已以較佳實施例揭露如上,然而並非用以限定本發明,任何熟悉本專業的技術人員,在不脫離本發明技術方案範圍內,當可利用上述揭示的技術內容作出些許更動或修飾為等同變化的等效實施例,但凡是未脫離本發明技術方案內容,依據本發明的技術實質對以上實施例所作的任何簡單修改、等同變化與修飾,均仍屬於本發明技術方案的範圍內。
