亞甲基橋連1,8‑萘啶配體及銅(Ⅰ)配合物、製備方法和應用與流程
2023-05-12 18:06:26 5
本發明屬於化學技術領域,涉及萘啶配合物。更具體地,涉及亞甲基橋連1,8-萘啶配體及銅(Ⅰ)配合物、製備方法和應用。
背景技術:
C―H鍵是有機化合物中最簡單、最常見的官能團,基於C―H鍵活化策略的化學合成可以簡化原料、縮短反應流程,能夠實現常規方法難以製備的目標產物,是最經濟、最簡潔、最高效的途徑,符合現代綠色合成化學的發展趨勢,因此通過C―H鍵的活化發展形成C―C、C―X鍵的合成方法學一直以來受到有機化學家們的廣泛關注。但由於C―H鍵的鍵能高,極性小,活化困難,反應活性低,非常難以實現有效地轉化,使得C―H鍵的活化成為有機化學家的一大挑戰。碳氫鍵活化是近年來發展迅速的熱門領域。碳氫鍵的直接官能團化反應由於具有多種突出的優點以及很大的挑戰性,被譽為「化學的聖杯」,吸引越來越多科學家的關注。在過去的十幾年中,經典的貴金屬催化的碳氫鍵活化已取得很大進展,但有毒有害的重金屬殘留以及較高的成本一直是難以解決的困難。最近,以廉價易得的普通過渡金屬催化的碳氫鍵活化反應,甚至是無過渡金屬催化的碳氫鍵活化反應代表了該領域未來的發展方向,具有重要的戰略意義和挑戰性,無論在有機化學理論的發展還是在化學工業的應用上都具有及其深遠的意義。同時,在實現C―H鍵活化的同時,如何利用簡單的反應物在溫和條件下,高原子經濟性的實現目標產物合成始終是有機化學家們追求的目標。
此外,有機催化反應在近幾年的研究中受到了廣泛的關注,相比金屬催化而言,它具有低成本,低負載和環境友好的特點。N-雜環化合物及其衍生物作為中間體在生物科學,天然產物和藥物中具有廣泛應用。N—芳基胺和N—芳基含氮雜環化合物廣泛存在於具有生理活性的天然產物中,並廣泛應用於醫藥、生物化學、含氮雜環碳烯化學、有機電致發光、太陽能電池光電轉化材料等領域,其合成與應用越來越受到研究者的關注。因此,發展新的方法合成這種含氮化合物在醫藥化學和有機合成中具有重要的研究意義。目前為止,已知合成C—N鍵的方法主要包括銅催化的Ullmann偶聯反應,Goldberg類型的C—N鍵形成和鈀催化的Buchwald-Hartwig胺化反應,這些反應通常在均相條件下具有較高的收率。用於催化N—芳基化反應的金屬主要有Pt、Cu、Fe、Ni、Cd等。由於銅在偶聯反應中的活性較高、價格低廉,所以以銅及其鹽或氧化物為催化劑的研究最多。
技術實現要素:
本發明要解決的第一個技術問題是在無催化劑條件下通過SP3C―H鍵活化反應得到亞甲基橋連1,8-萘啶配體及銅(Ⅰ)配合物。
本發明要解決的第二個技術問題是提供亞甲基橋連1,8-萘啶銅(Ⅰ)配合物的製備方法。
本發明要解決的第三個技術問題是提供亞甲基橋連1,8-萘啶銅(Ⅰ)配合物的應用;
為解決上述技術問題,本發明採用下述技術方案:
亞甲基橋連1,8-萘啶配體及銅(Ⅰ)配合物,分子式為:
其中:R1為氫、甲基。
本發明所述的亞甲基橋連1,8-萘啶配體及銅(Ⅰ)配合物的製備方法,包括以下步驟:
1)合成2-甲基-4-R1-7-乙醯氨基-1,8-萘啶:
在圓底燒瓶中加入7-氨基-2,4-二甲基-1,8-萘啶或7-氨基-2-甲基-1,8-萘啶,加入過量乙酸酐,氮氣保護下回流2h,薄層色譜檢測反應進程,反應液冷卻析出黃色晶體,抽濾得到7-乙醯氨基-2,4-甲基-1,8-萘啶或7-乙醯氨基-2-甲基-1,8-萘啶產物,直接用於下面的反應;
2)無催化劑SP3C―H活化合成亞甲基橋連1,8-萘啶配體:
在圓底燒瓶中將7-乙醯氨基-2,4-甲基-1,8-萘啶或7-乙醯氨基-2-甲基-1,8-萘啶和鄰醛基苯甲酸溶解在N,N-二甲基甲醯胺中,氮氣保護下升溫回流反應,薄層色譜檢測反應進程,反應完成後將產物純化,得亞甲基橋連1,8-萘啶配體;
3)合成亞甲基橋連1,8-萘啶銅(Ⅰ)配合物:
將亞甲基橋連1,8-萘啶配體溶於二氯甲烷中,得到A;
將CuI溶於甲醇中,得到B;
將B逐滴加入到A中,氮氣保護攪拌反應24小時,得到沉澱,為亞甲基橋連1,8-萘啶銅(Ⅰ)配合物;其中配體和CuI的摩爾比為1:1。
上述方法的步驟1)中,加熱回流時間為2小時,氮氣保護下繼續回流的時間為4小時,回流溫度為100-110℃。
步驟1)中,將產物純化包括:反應液冷卻析出黃色晶體或將反應液減壓旋蒸除去溶劑,固體殘留物用乙醇重結晶,得到7-乙醯氨基-2,4-甲基-1,8-萘啶或7-乙醯氨基-2-甲基-1,8-萘啶。
步驟2)中,先溶解鄰醛基苯甲酸,回流後再加入7-乙醯氨基-2,4-甲基-1,8-萘啶或7-乙醯氨基-2-甲基-1,8-萘啶;
步驟2)中,無需加入任何催化劑;
步驟2)中,升溫回流時間為24小時;
步驟2)中,回流溫度為150℃。
步驟3)中,得到的沉澱經過濾、用冰甲醇或冰乙醇洗滌、乾燥得到亞甲基橋連1,8-萘啶銅(Ⅰ)配合物。
本發明所述亞甲基橋連1,8-萘啶銅(Ⅰ)配合物的應用,將所述亞甲基橋連1,8-萘啶銅(Ⅰ)配合物用作芳基滷化物與咪唑類化合物C―N偶聯反應的催化劑。
本發明所述亞甲基橋連1,8-萘啶銅(Ⅰ)配合物用作芳基滷化物與咪唑類化合物C―N偶聯反應的催化劑的方法是:將1.0mmol得芳基滷化物、1.0mmol的咪唑、2.0mmol的氫氧化鈉、3mL的二甲基亞碸和0.01mmol的亞甲基橋連1,8-萘啶銅(Ⅰ)配合物於100℃下反應。
本領域技術人員可知,通過觀察不同條件下對比的實驗結果來判斷催化效果及催化性能。
本發明的有益效果如下:
1、本發明提供了一種無催化劑條件下通過SP3C―H鍵活化反應製備亞甲基橋連1,8-萘啶配體的方法,是目前為止發現的第一個實現無催化劑SP3C―H鍵活化構建C―C鍵的方法。
2、本發明的無催化劑SP3C―H鍵活化方法可以簡化原料、縮短反應流程,能夠實現常規方法難以製備的目標產物,是最經濟、最簡潔、最高效的途徑,符合現代綠色合成化學的發展趨勢。
3、本發明提供了一種新型的亞甲基橋連1,8-萘啶銅(Ⅰ)配合物,是目前為止發現的第一個可催化芳基滷化物與咪唑類化合物C―N偶聯反應的萘啶銅(Ⅰ)配合物。
4、本發明的配合物可催化芳基滷化物與咪唑類化合物C―N偶聯反應,使其應用在有生理活性的天然產物、醫藥、生物化學、含氮雜環碳烯化學、有機電致發光、太陽能電池光電轉化材料等的合成成為可能。
附圖說明
圖1為配體1在氘代三氯甲烷中的1H-NMR;
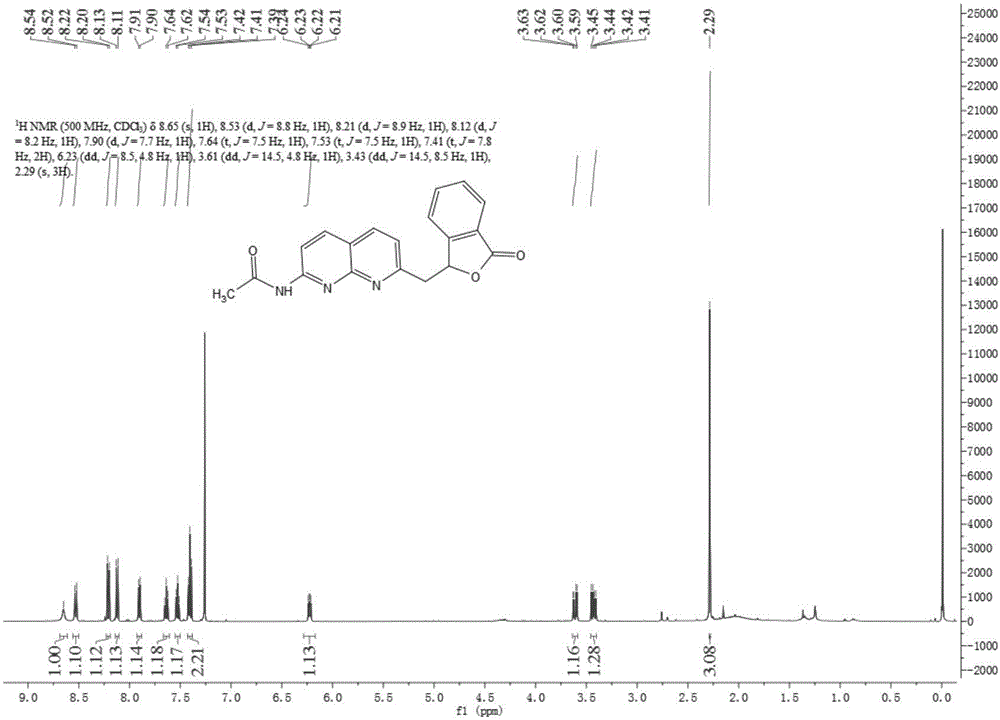
圖2為配體2在氘代三氯甲烷中的1H-NMR;
圖3為亞甲基橋連1,8-萘啶配體及銅(Ⅰ)配合物的合成路線;
圖4為亞甲基橋連1,8-萘啶銅(Ⅰ)配合物的晶體結構;
表1為咪唑和溴苯催化N―芳基化反應條件篩選結果;
表2為不同的芳基滷化物和咪唑N―芳基化配合物催化結果。
具體實施方式
為了更清楚地說明本發明,下面結合優選實施例對本發明做進一步的說明。本領域技術人員應當理解,下面所具體描述的內容是說明性的而非限制性的,不應以此限制本發明的保護範圍。
實施例
一、亞甲基橋連1,8-萘啶配體及銅(Ⅰ)配合物的合成:
1)合成2-甲基-4-R1-7-乙醯氨基-1,8-萘啶:
在100mL圓底燒瓶中加入7-氨基-2,4-二甲基-1,8-萘啶或7-氨基-2-甲基-1,8-萘啶(4.0g,23.1mmol),加入15mL乙酸酐,混合物氮氣保護下回流反應2h,反應液冷卻析出黃色晶體,抽濾得到7-乙醯氨基-2,4-甲基-1,8-萘啶或7-乙醯氨基-2-甲基-1,8-萘啶產物,直接用於下面的反應;
2)無催化劑SP3C―H活化合成亞甲基橋連1,8-萘啶配體:
將0.35g(2.33mmol)鄰醛基苯甲酸溶解在30mL N,N-二甲基甲醯胺中,氮氣保護下升溫至150℃,再加入0.50g(2.32mmol)7-乙醯氨基-2,4-二甲基-1,8-萘啶並繼續回流反應24h,停止反應,冷卻至室溫,真空旋幹得黑色固體;使用柱層析矽膠200-300目分離純化,淋洗劑V乙酸乙酯:V石油醚=1:1,得淡黃色粉末固體0.36g,產率44.4%。核磁表徵見圖1,1HNMR(500MHz,CDCl3)δ(ppm)8.58(s,1H NH),8.54(d,J=9.1Hz,1H),8.41(d,J=9.0Hz,1H),7.94(d,J=7.6Hz,1H),7.67(t,J=7.5Hz,1H),7.56(t,J=7.5Hz,1H),7.44(d,J=7.7Hz,1H),7.26(s,1H),6.25(dd,J=8.7,4.7Hz,1H CH),3.57(dd,J=14.5,4.6Hz,1H CH2),3.36(dd,J=14.5,8.8Hz,1H CH2),2.73(s,3H),2.30(s,3H).ESI-MS calcd for C20H17N3O3[M+H]+347.37,found 348.1。
另一亞甲基橋連1,8-萘啶配體合成方法同上,將0.35g(2.33mmol)鄰醛基苯甲酸溶解在30mL N,N-二甲基甲醯胺中,氮氣保護下升溫至150℃,再加入0.46g(2.32mmol)7-乙醯氨基-2-甲基-1,8-萘啶並繼續回流反應24h,停止反應,冷卻至室溫,真空旋幹得黑色固體;使用柱層析矽膠200-300目分離純化,淋洗劑V乙酸乙酯:V石油醚=1:1,得淡黃色粉末固體0.34g,產率45%。核磁表徵見圖2,1H NMR(500MHz,CDCl3)δ8.65(s,1H),8.53(d,J=8.8Hz,1H),8.21(d,J=8.9Hz,1H),8.12(d,J=8.2Hz,1H),7.90(d,J=7.7Hz,1H),7.64(t,J=7.5Hz,1H),7.53(t,J=7.5Hz,1H),7.41(t,J=7.8Hz,2H),6.23(dd,J=8.5,4.8Hz,1H),3.61(dd,J=14.5,4.8Hz,1H),3.43(dd,J=14.5,8.5Hz,1H),2.29(s,3H).ESI-MS calcd for C19H15N3O3[M+H]+334.34,found 334.1。
3)合成亞甲基橋連1,8-萘啶銅(Ⅰ)配合物:
將亞甲基橋連1,8-萘啶配體(0.072g,0.2mmol)溶於15mL二氯甲烷中,得到A;
稱取(39.5mg,0.2mmol)CuI溶於5mL甲醇中,得到B;
將B逐滴加入到A中,滴加過程中能看到溶液由澄清變為黃綠色渾濁,氮氣保護室溫攪拌反應24小時,得到的沉澱經過濾、用冰甲醇或冰乙醇洗滌,晾乾得到黃綠色固體粉末,即為亞甲基橋連1,8-萘啶銅(Ⅰ)配合物。
由於亞甲基橋連1,8-萘啶銅(Ⅰ)配合物的一價銅很容易被氧化為二價銅,二價銅配合物因為具有順磁性側不了1HNMR,所以對得到的亞甲基橋連1,8-萘啶銅(Ⅰ)配合物進行質譜和晶體表徵。ESI-MS calcd for C40H34CuIN6O6[M-I]+757.18,found 757.4.晶體結構見圖4。部分鍵長:Cu(1)-N(1),Cu(1)-N(4),Cu(1)-I(1),N(1)-C(1),N(1)-C(5),N(2)-C(8),N(2)-C(5),N(3)-C(10),N(3)-C(8),N(4)-C(21),N(4)-C(25),N(5)-C(28),N(5)-C(25),N(6)-C(30),N(6)-C(28);部分鍵角:N(1)-Cu(1)-N(4),113.22°;N(1)-Cu(1)-I(1),120.54°;N(4)-Cu(1)-I(1),126.22°;C(1)-N(1)-C(5),117.1°;C(1)-N(1)-Cu(1),126.0°;C(5)-N(1)-Cu(1),113.6°;C(8)-N(2)-C(5),117.7°;C(10)-N(3)-C(8),128.9°;C(21)-N(4)-C(25),117.2°;C(21)-N(4)-Cu(1),123.2°;C(25)-N(4)-Cu(1),115.5°;C(28)-N(5)-C(25),117.1°;C(30)-N(6)-C(28),128.7°;N(1)-C(1)-C(2),122.9°;N(1)-C(1)-C(12),116.7°。
整個反應過程如圖3所示。
二、亞甲基橋連1,8-萘啶銅(Ⅰ)配合物用作芳基滷化物與咪唑類化合物C―N偶聯反應的催化劑的方法如下:
將1.0mmol得芳基滷化物、1.0mmol的咪唑、2.0mmol的氫氧化鈉、3mL的二甲基亞碸和0.01mmol的亞甲基橋連1,8-萘啶銅(Ⅰ)配合物於100℃下反應。
亞甲基橋連1,8-萘啶銅(Ⅰ)配合物催化芳基滷化物與咪唑類化合物C―N偶聯反應實驗如下:
1、確定本發明的配合物在催化芳基滷化物與咪唑類化合物C―N偶聯反應的最佳條件,進行條件篩選。
條件篩選通過配合物催化溴苯與咪唑的C―N偶聯反應,通過改變反應條件,包括鹼的使用、溶劑使用、反應溫度、反應時間、配合物催化劑用量;考察收率,確定最佳催化條件為氫氧化鈉作鹼(2mmol)、二甲基亞碸作溶劑(3mL)、反應溫度為100℃、催化劑即本發明的亞甲基橋連1,8-萘啶銅(Ⅰ)配合物用量0.01mmol,結果見表1。二甲基亞碸作溶劑催化性能較好,收率可達96%,反應時間4h足夠,當時間降為2h,收率降至60%;此外,較低溫度80℃時,收率僅為82%,催化劑用量為0.5%(摩爾分數)時,反應收率降至70%。
表1 咪唑和溴苯催化N―芳基化反應條件篩選結果a
注:a.
反應條件:反應條件:溴苯(1.0mmol)、咪唑(1.0mmol)、鹼(2.0mmol)、配合物(0.01mmol)、溶劑(3mL)、空氣氣氛、b.分離產率;c.使用0.5%(摩爾分數)催化劑。
2、最優反應條件下,取代芳基溴化物和碘化物底物擴展實驗:
固定最佳反應條件為:氫氧化鈉作鹼(2mmol)、二甲基亞碸作溶劑(3mL)、反應溫度為100℃、催化劑即亞甲基橋連1,8-萘啶銅(Ⅰ)配合物用量0.01mmol,進行不同取代芳基溴化物和碘化物底物催化擴展實驗,結果見表2。該催化體系可容忍各種官能化的芳基滷化物的C―N偶聯反應,取代基包括腈基,硝基,乙醯基和醚基等,其中碘化物的催化收率在91%-99%之間。此外,該催化反應具有高選擇性,底物為羥基或氨基取代芳基溴化物時,能避免二芳基醚類化合物及二苯胺類化合物的形成。
表2 不同的芳基滷化物和咪唑N―芳基化配合物催化結果a
注:a.
反應條件:反應條件:芳基滷化物(1.0mmol)、咪唑(1.0mmol)、氫氧化鈉(2.0mmol)、配合物(0.01mmol)、二甲基亞碸(3mL)、100℃空氣氛圍、b.分離產率;c.2-溴吡啶芳基滷化物。
