一種聯合檢測禽流感H7N9和H9N2的四通道螢光定量PCR檢測方法及試劑盒與流程
2023-05-15 16:56:26 5
本發明屬於分子檢測技術領域,具體涉及一種聯合檢測禽流感H7N9和H9N2的四通道螢光定量PCR檢測方法及試劑盒。
背景技術:
在我國新發的人感染H7N9亞型病毒引起了廣泛的關注,病毒的常監測、早診斷、預警成為極其重要工作。研究表明,禽源H9N2亞型禽流感病毒為H7N9亞型流感這一新型重組病毒提供了內部基因。然而,雞源H9N2亞型禽流感病毒的流行和進化是如何促進新型禽流感H7N9出現的機制尚不清楚,中國農業大學劉金華教授團隊對該機制進行了研究,研究表明在過去長達10多年中,多種H9N2基因型共同存在,G57基因型出現並隨著抗體特性變化更加適應雞宿主。在2010~2013年期間,也就是新型禽流感病毒H7N9出現前期,H9N2亞型禽流感病毒G57基因型成為免疫雞農場的主要基因型,並引起了雞場禽流感的廣泛爆發,最終為新型禽流感H7N9提供了內部基因。禽農場中H9N2病毒的流行和變化監測可以為可能造成流感大流行的新型禽流感病毒出現提供重要的監測和早期診斷預警。
隨著分子生物學的快速發展,多重PCR已廣泛應用於禽病混合感染的鑑別診斷,其原理是設計能夠同時擴增出多種待測病原特定片段大小的多對引物,在PCR反應體系中加入多對引物,能夠對多種病原進行鑑別診斷。多重RT-PCR因其靈敏性、特異性和操作的簡單性被廣泛應用於禽病的多重檢測,但結果判定需要電泳,費時費力,且反應產物容易產生汙染而導致假陽性,而多重PCR是靠片段的大小來區別的,一般到了三重以上,片段大小差別大,其每種病毒的擴增效率不一樣,造成結果存在偏差。螢光定量PCR技術融合了PCR的多種優點,通過直接檢測PCR反應過程中螢光信號的變化實現對目的分子的定量,不需要電泳檢測,並且整個過程完全閉管式操作,汙染機率降低,避免了常規PCR容易造成的假陽性問題。相對常規PCR,螢光定量PCR在敏感性、特異性與速度等方面具有優勢,但實時螢光PCR技術受到螢光種類及儀器自身的限制,最多只能對5個靶標進行檢測,且實驗成功的難度極大。
技術實現要素:
本發明的一個目的在於提供一種用於聯合檢測禽流感H7N9和H9N2的螢光定量PCR引物組。
本發明的另一個目的在於提供一種用於聯合檢測禽流感H7N9和H9N2的螢光定量PCR試劑盒。
本發明的另一個目的在於提供一種用於聯合檢測禽流感H7N9和H9N2的螢光定量PCR檢測方法。
本發明所採取的技術方案是:
一種用於聯合檢測禽流感H7N9和H9N2的螢光定量PCR引物組,其包括用於檢測禽流感H7N9亞型的H7基因的引物對及螢光探針、用於檢測禽流感H7N9亞型的N9基因的引物對及螢光探針、用於檢測禽流感H9N2亞型的H9基因的引物對及螢光探針、用於檢測禽流感H9N2亞型的N2基因的引物對及螢光探針,用於檢測H7、N9、H9、N2基因的螢光探針報告基團不相同。
作為優選的,所述用於檢測禽流感H7N9亞型的H7基因的引物對及螢光探針的核苷酸序列如下所示:
H7-F:5』-TGCACTGCATGTTTCCATTCTT-3』(SEQ ID NO.1);
H7-R:5』-GGCTACAAAGATGTGATACTTTGGTTTAG-3』(SEQ ID NO.2);
H7-P:5』FAM-ATGAAAACAAGGCCCATTGCAATGGC-BHQ13』(SEQ ID NO.3)。
作為優選的,所述用於檢測禽流感H7N9亞型的N9基因的引物對及螢光探針的核苷酸序列如下所示:
N9-F:5』-TCGCGCCCTGATAAGCT-3』(SEQ ID NO.4);
N9-R:5』-GCATTCCACCCTGCTGTTG-3』(SEQ ID NO.5);
N9-P:5』VIC-CCACTATCATCACCGCCCACAGTGT-BHQ13」(SEQ ID NO.6)。
作為優選的,所述用於檢測禽流感H9N2亞型的H9基因的引物對及螢光探針的核苷酸序列如下所示:
H9-F:5』-CAATGGGGTTTGCTGCCT-3』(SEQ ID NO.7);
H9-R:5』-TTATATACAAATGTTGCATCTGC-3』(SEQ ID NO.8);
H9-P:5』TexasRed-TTCTGGGCCATGTCCAATGGTTCT-BHQ23』(SEQ ID NO.9)。
作為優選的,所述用於檢測禽流感H9N2亞型的N2基因的引物對及螢光探針的核苷酸序列如下所示:
N2-F:5』-TGACACTGCACTTCAAGCAA-3』(SEQ ID NO.10);
N2-R:5』-TTGGTTCACATGTCACTACTTGAT-3』(SEQ ID NO.11);
N2-P:5』CY5-ATGAATGCAGCATCCCCTCGAAC-BHQ23』(SEQ ID NO.12)。
一種用於聯合檢測禽流感H7N9和H9N2的螢光定量PCR試劑盒,其包含上述的螢光定量PCR引物組。
所述試劑盒還包含病毒RNA提取液、Tth DNA聚合酶、四通道螢光定量PCR Mix、陽性質控品、陰性質控品,所述四通道螢光定量PCR Mix中含有2×四通道螢光定量PCR buffer、dNTPs。
所述2×四通道螢光定量PCR buffer中含有以下成分:Tricine pH8.7、Mg(OAc)2、KOAc、甘油、DMSO、N,N,N-三甲基甘氨酸。
一種聯合檢測禽流感H7N9和H9N2的四通道螢光定量PCR檢測方法,包括如下步驟:
1)提取待測樣品中的病毒RNA;
2)以得到的總RNA為模板,使用上述的螢光定量PCR引物組進行四通道螢光定量PCR
檢測;
3)反應結束後,根據待測樣品的螢光Ct值判斷,待測樣品是否為禽流感病毒H7基因、
N9基因、H9基因、N2基因陽性。
四通道螢光定量PCR反應條件為:
95℃1分鐘;58℃20分鐘;95℃1分鐘;
95℃10秒,58℃70秒,68℃10s,採集螢光信號,40個循環。
本發明的有益效果是:
本發明方法能夠同時檢測出待測標本中禽流感病毒H7N9的H7基因和N9基因,以及禽流感病毒H9N2的H9基因和N2基因。由於該方法引入了特異性擴增引物和螢光探針,使得檢測的靈敏度和特異性得到很大程度的增強,從而避免了其他檢測方法特異性不高容易漏診和誤診的問題。同時,該試劑盒根據本方法原理製得的試劑盒,可方便地同時檢測出禽流感病毒H7N9的H7基因和N9基因,以及禽流感病毒H9N2的H9基因和N2基因,準確率高。
該方法使用Tth DNA聚合酶,代替傳統的Taq酶和MMLV酶的組合,在更高的溫度下進行逆轉錄,提升了四通道擴增這種複雜模版的擴增效果。因此該試劑盒具有廣泛的應用前景,適合在各級動物衛生監督機構、疾病控制單位等大規模篩查的推廣應用。
附圖說明
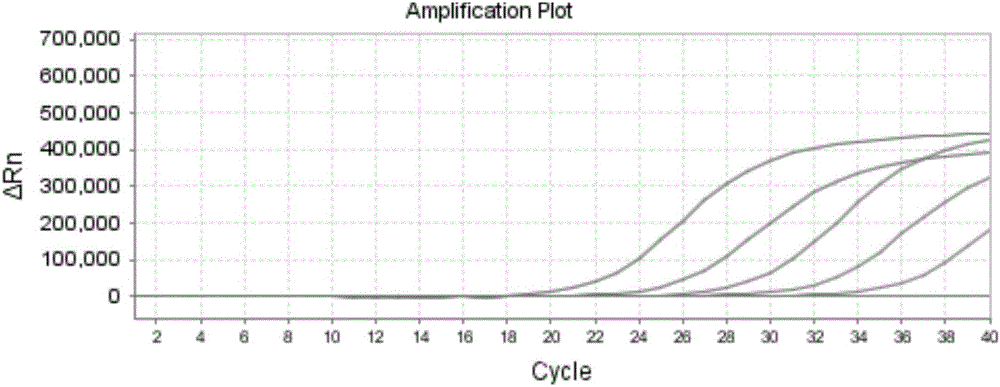
圖1為四通道螢光PCR體系中禽流感病毒H7基因檢測的靈敏度實驗,從左到右依次為1×106、1×105、1×104、1×103、1×102、1×101cp/μl的標準品的擴增結果。由圖可知,H7基因檢測的靈敏度為1×102cp/μl。
圖2為四通道螢光PCR體系中禽流感病毒N9基因檢測的靈敏度實驗,從左到右依次為1×106、1×105、1×104、1×103、1×102、1×101cp/μl的標準品的擴增結果。由圖可知,N9基因檢測的靈敏度為1×102cp/μl。
圖3為四通道螢光PCR體系中禽流感病毒H9基因檢測的靈敏度實驗,從左到右依次為1×106、1×105、1×104、1×103、1×102、1×101cp/μl的標準品的擴增結果。由圖可知,H9基因檢測的靈敏度為1×102cp/μl。
圖4為四通道螢光PCR體系中禽流感病毒N2基因檢測的靈敏度實驗,從左到右依次為1×106、1×105、1×104、1×103、1×102、1×101cp/μl的標準品的擴增結果。由圖可知,N2基因檢測的靈敏度為1×102cp/μl。
圖5為四通道螢光PCR體系中禽流感病毒H7基因檢測的特異性實驗結果,檢測哈獸研H7抗原、H7N9棉拭子標本、H7N7棉拭子標本為陽性,檢測哈獸研H5N1抗原、H5N1疫苗、H9N2棉拭子標本、廣州永順NDV疫苗及陰性質控品均為陰性。
圖6為四通道螢光PCR體系中禽流感病毒N9基因檢測的特異性實驗結果,檢測H7N9棉拭子標本為陽性,檢測H7N7棉拭子標本、哈獸研H5N1抗原、華農H5N1疫苗、H9N2棉拭子標本、廣州永順NDV疫苗及陰性質控品均為陰性。
圖7為四通道螢光PCR體系中禽流感病毒H9基因檢測的特異性實驗結果,檢測H9N2棉拭子標本為陽性,檢測H7N7棉拭子標本、哈獸研H5N1抗原、華農H5N1疫苗、H7N9棉拭子標本、廣州永順NDV疫苗及陰性質控品均為陰性。
圖8為四通道螢光PCR體系中禽流感病毒N2基因檢測的特異性實驗結果,檢測H9N2棉拭子標本為陽性,檢測H7N7棉拭子標本、哈獸研H5N1抗原、華農H5N1疫苗、H7N9棉拭子標本、廣州永順NDV疫苗及陰性質控品均為陰性。
具體實施方式
下面結合實施例對本發明做進一步的說明,但並不局限於此。
實施例1
1、特異性引物及探針的設計
根據禽流感病毒(Avian influenza virus)H1~H16的核酸序列,以及N1~N9的核酸序列,設計用於檢測禽流感病毒H7N9、H9N2基因的引物和探針(在life technology公司合成)。其序列如下:
2、標本採集和預處理
本方法及試劑盒適用標本類型包括禽類的組織、血清、咽拭子、分泌排洩物等。組織標本:無菌條件下取組織約100~200mg左右,置入1.5ml潔淨EP管中,保存待檢。血清:用一次性無菌注射器抽取受檢鳥靜脈血3-5ml,留取血清,保存待檢。咽及洩殖腔等拭子:用棉拭子取咽或洩殖腔分泌物,將拭子放入盛有1.0ml PBS的離心管中,立即送檢。分泌排洩物:無菌條件下採集,保存待檢。採集的標本應該儘快送檢,或者保存於-20℃。
3、標本RNA提取
3.1RNA提取液的組分:
裂解液
洗滌液
3.2使用杭州萊楓生物生產的RNA純化柱進行純化,以如下步驟提取:
1)200μl標本加入500μl裂解液,室溫靜止1min;
2)12000rpm離心5分鐘,棄套管中液體;
3)加入600μL洗滌液,振蕩混勻;
4)12000rpm離心5分鐘,棄套管中液體;
5)加入600μL洗滌液,振蕩混勻;
6)12000rpm離心5分鐘,棄套管,換新的1.5mL離心管;
7)加入50μL DEPC處理水,振蕩混勻;
8)12000rpm離心5分鐘,管中液體即為所提取的RNA。
4、陽性質控品的製備
H7N9假病毒陽性標準品序列如SEQ ID NO.13所示;H9N2假病毒陽性標準品序列如SEQ ID NO.14所示。
將二者分別提交廈門致善生物,合成載體、用MS2噬菌體包裝成假病毒顆粒並測定濃度。
返回的H7N9假病毒與H9N2假病毒,以1:1混合,作為試劑盒的陽性質控品,-20±5℃條件下儲存。所得假病毒顆粒擴增前需進行RNA提取實驗。
5』-GCGGTTATAAAGATGTGATACTTTGGTTTAGCTTCGGGGCATCATGTTTCATACTTCTTGCCATTGCAATGGGCCTTGTCTTCATATGTGTGAAGAATGGAAACATGCGGTGCACTATTTGTATATAATCGCGCCCTGATAAGCTGGCCACTATCATCACCGCCCACAGTATACAACAGCAGGGTGGAATGCATTGGG-3』(SEQ ID NO.13)
5』-CAATGGGGTTTGCTGCCTTCTTGTTCTGGGCCATGTCCAATGGATCATGCAGGTGCAACATTTGTATATAATGACACTGCACTTCAAGCAAAATGAATGCAGCATCCCCTCGAACAATCAAGTAGTGACATGTGAACCAA-3』(SEQ ID NO.14)
5、陰性質控品的製備
取純化水,高壓滅菌後,貯存於冷藏冰箱(2-8℃),超過7天未分裝的轉至-20±5℃條件下儲存。
6、四通道螢光定量PCR擴增
螢光定量PCR反應的反應體系總體積為25μl,組成如下:多通道螢光定量PCR Mix 20μl、DNA聚合酶1μl,以及提取標本RNA(或者陽性質控品、陰性質控品)4μl;其中四通道螢光定量PCR Mix中含有四通道螢光定量PCR buffer、dNTPs等成分。
2×四通道螢光定量PCR buffer中含有以下成分:
四通道螢光定量PCR Mix組成為:
四通道螢光定量PCR反應條件為:
95℃1分鐘;58℃20分鐘;95℃1分鐘;
95℃10秒,58℃70秒,68℃10s,採集螢光信號,40個循環。
7、結果分析和判定
7.1結果分析條件設定
1)設置基線(baseline):根據機型不同,設置3~15循環,6~15循環,特殊情況可對基線適當調整。
2)設置閾值(threshold):以閾值線剛超過陰性對照擴增曲線(無規則的噪音線)的最高點。
7.2結果判斷如下表:
實施例2靈敏度實驗
圖1為四通道螢光PCR體系中禽流感病毒H7基因檢測的靈敏度實驗,從左到右依次為1×106、1×105、1×104、1×103、1×102、1×101cp/μl的標準品的擴增結果。由圖可知,H7基因檢測的靈敏度為1×102cp/μl。
圖2為四通道螢光PCR體系中禽流感病毒N9基因檢測的靈敏度實驗,從左到右依次為1×106、1×105、1×104、1×103、1×102、1×101cp/μl的標準品的擴增結果。由圖可知,N9基因檢測的靈敏度為1×102cp/μl。
圖3為四通道螢光PCR體系中禽流感病毒H9基因檢測的靈敏度實驗,從左到右依次為1×106、1×105、1×104、1×103、1×102、1×101cp/μl的標準品的擴增結果。由圖可知,H9基因檢測的靈敏度為1×102cp/μl。
圖4為四通道螢光PCR體系中禽流感病毒N2基因檢測的靈敏度實驗,從左到右依次為1×106、1×105、1×104、1×103、1×102、1×101cp/μl的標準品的擴增結果。由圖可知,N2基因檢測的靈敏度為1×102cp/μl。
實施例3特異性實驗
圖5為四通道螢光PCR體系中禽流感病毒H7基因檢測的特異性實驗結果,檢測哈獸研H7抗原、H7N9棉拭子標本、H7N7棉拭子標本為陽性,檢測哈獸研H5N1抗原、H5N1疫苗、H9N2棉拭子標本、廣州永順NDV疫苗及陰性質控品均為陰性。
圖6為四通道螢光PCR體系中禽流感病毒N9基因檢測的特異性實驗結果,檢測H7N9棉拭子標本為陽性,檢測H7N7棉拭子標本、哈獸研H5N1抗原、華農H5N1疫苗、H9N2棉拭子標本、廣州永順NDV疫苗及陰性質控品均為陰性。
圖7為四通道螢光PCR體系中禽流感病毒H9基因檢測的特異性實驗結果,檢測H9N2棉拭子標本為陽性,檢測H7N7棉拭子標本、哈獸研H5N1抗原、華農H5N1疫苗、H7N9棉拭子標本、廣州永順NDV疫苗及陰性質控品均為陰性。
圖8為四通道螢光PCR體系中禽流感病毒N2基因檢測的特異性實驗結果,檢測H9N2棉拭子標本為陽性,檢測H7N7棉拭子標本、哈獸研H5N1抗原、華農H5N1疫苗、H7N9棉拭子標本、廣州永順NDV疫苗及陰性質控品均為陰性。
以上實驗結果表明:本發明方法及試劑盒可方便地同時檢測出禽流感病毒H7N9的H7基因和N9基因,以及禽流感病毒H9N2的H9基因和N2基因,靈敏度和特異性得到很大程度的增強。
SEQUENCE LISTING
廣東省農業科學院動物衛生研究所
一種聯合檢測禽流感H7N9和H9N2的四通道螢光定量PCR檢測方法及試劑盒
14
PatentIn version 3.5
1
22
DNA
人工序列
1
tgcactgcat gtttccattc tt 22
2
29
DNA
人工序列
2
ggctacaaag atgtgatact ttggtttag 29
3
26
DNA
人工序列
3
atgaaaacaa ggcccattgc aatggc 26
4
17
DNA
人工序列
4
tcgcgccctg ataagct 17
5
19
DNA
人工序列
5
gcattccacc ctgctgttg 19
6
25
DNA
人工序列
6
ccactatcat caccgcccac agtgt 25
7
18
DNA
人工序列
7
caatggggtt tgctgcct 18
8
23
DNA
人工序列
8
ttatatacaa atgttgcatc tgc 23
9
24
DNA
人工序列
9
ttctgggcca tgtccaatgg ttct 24
10
20
DNA
人工序列
10
tgacactgca cttcaagcaa 20
11
24
DNA
人工序列
11
ttggttcaca tgtcactact tgat 24
12
23
DNA
人工序列
12
atgaatgcag catcccctcg aac 23
13
198
DNA
H7N9
13
gcggttataa agatgtgata ctttggttta gcttcggggc atcatgtttc atacttcttg 60
ccattgcaat gggccttgtc ttcatatgtg tgaagaatgg aaacatgcgg tgcactattt 120
gtatataatc gcgccctgat aagctggcca ctatcatcac cgcccacagt atacaacagc 180
agggtggaat gcattggg 198
14
140
DNA
H7N9
14
caatggggtt tgctgccttc ttgttctggg ccatgtccaa tggatcatgc aggtgcaaca 60
tttgtatata atgacactgc acttcaagca aaatgaatgc agcatcccct cgaacaatca 120
agtagtgaca tgtgaaccaa 140
