一種胺基酸季氨基羧酸鹽的合成方法與流程
2023-04-28 13:23:36 3
本發明屬化合物合成技術領域,具體涉及一種胺基酸季氨基羧酸鹽的合成方法,合成所得的產品可用於防治微生物感染或環境消毒。
背景技術:
專利號為zl201210166719.3的中國發明專利文件公開了一種胺基酸季氨基羧酸鹽,包括胺基酸單鏈季氨基羧酸鹽和胺基酸雙鏈季氨基羧酸鹽,由帶負電荷的胺基酸陰離子和不含滷族元素的單鏈或雙鏈的季氨基陽離子構成,該化合物在低濃度時即可殺滅大多數致病細菌或病毒,無毒性。所公開的該產品合成步驟是:第一步,在具揮發性的有機溶劑中將乙醯化胺基酸用等當量的氫氧化鈉或氫氧化鉀等金屬氫氧化物中和;或在水中以冰浴或乾冰丙酮的混合物保持低溫,中和等當量的乙醯化胺基酸和氫氧化鈉或氫氧化鉀等金屬氫氧化物;第二步,去除揮發性有機溶劑或水,得到固體的胺基酸金屬鹽;第三步,將金屬陽離子、胺基酸陰離子的鹽溶於水中,與等當量的季氨基滷化銨混合;第四步,在上述水溶液中加入有機溶劑混搖,最終形成有機相和水相兩層液體,有機相裡是乙醯化胺基酸季氨基羧酸鹽;副產物金屬陽離子和無機陰離子留在水相中;第五步,將有機相和水相分離,去除有機相的溶劑;第六步,水相再次與純的有機溶劑混合提取殘存在水中的乙醯化胺基酸鹽,重複提取三次;第七步,去除有機溶劑,得到產物。此合成方法存在如下缺點:1.合成步驟相對比較複雜;2.所用的有機試劑二氯甲烷回收和處理比較麻煩且有一定毒性;3.所合成出來的物質純度不高。
技術實現要素:
本發明的目的在於克服現有合成胺基酸季氨基羧酸鹽方法的缺點,提供一種新的合成方法。
本發明合成方法為按以下步驟:
1、將1份摩爾的鹼金屬氫氧化物溶入溫度為20℃~30℃的揮發性有機溶劑中,得溶液a;
2、將1份摩爾的雙鏈季氨基滷化銨或單鏈季氨基滷化銨溶入揮發性有機溶劑中,得溶液b;
3、將上面所得到的溶液a與溶液b充分混合,其中鹼金屬的陽離子與滷族陰離子生成不溶於揮發性有機溶劑的鹽,充分過濾或離心去除不溶物,得到含雙鏈季氨基氫氧化銨或單鏈季氨基氫氧化銨的溶液c;
4、將乙醯化胺基酸溶於揮發性有機溶劑中,並讓所得溶液中含有1份摩爾的乙醯化胺基酸陰離子,得溶液d;
5、將上面所得到的溶液c與溶液d混合,去除不溶物,得到溶液e;
6、去除溶液e中的揮發性有機溶劑,得到產物胺基酸季氨基羧酸鹽。
所說胺基酸季氨基羧酸鹽,包括胺基酸單鏈季氨基羧酸鹽和胺基酸雙鏈季氨基羧酸鹽。
若需合成的是胺基酸雙鏈季氨基羧酸鹽中的雙癸基二甲基氧合脯氨酸銨dapc(proline,5-oxo-,ion(1-),n-decyl-n,n-dimethyl-1-decanaminium(1:1)),具體合成步驟可以如下:
製備溶液a:以無水乙醇為溶劑,將1份摩爾的鹼金屬氫氧化物加入其中,並加熱至20℃~30℃,充分攪拌至鹼金屬氫氧化物完全溶解,即得溶液a;
製備溶液b:以無水乙醇為溶劑,在室溫條件下將1份摩爾的雙癸基二甲基氯化銨加入其中,充分攪拌至雙癸基二甲基氯化銨完全溶解,即得溶液b;
製備溶液c:在室溫下混合溶液a和溶液b,攪拌1~10分鐘,生成不溶於無水乙醇的金屬氯化物沉澱,充分過濾或離心去除金屬氯化物沉澱,得到雙癸基二甲基氫氧化銨溶液,即得溶液c;
製備溶液d:將1份摩爾的焦穀氨酸溶於無水乙醇中,製成溶液,即得溶液d;
製備溶液e:將溶液c與溶液d充分混合,充分過濾或離心,即得溶液e;
得到產物:用旋轉蒸發儀回收溶液e的無水乙醇,得到產物dapc。
若需合成的是胺基酸雙鏈季氨基羧酸鹽中的雙癸基二甲基n-乙醯基丙氨酸銨daac(1-decanaminium,n-decyl-n,n-dimethyl-,saltwithn-acetylalanine(1:1)),具體合成步驟可以如下:
製備溶液a:以無水乙醇為溶劑,將1份摩爾的鹼金屬氫氧化物加入其中,並加熱至20℃~30℃,充分攪拌至鹼金屬氫氧化物完全溶解於無水乙醇中,即得溶液a;
製備溶液b:以無水乙醇為溶劑,在室溫條件下將1份摩爾的雙癸基二甲基氯化銨加入其中,充分攪拌至雙癸基二甲基氯化銨完全溶解於無水乙醇中,即得溶液b;
製備溶液c:在室溫下混合溶液a和溶液b,攪拌1~10分鐘,生成不溶於無水乙醇的金屬氯化物沉澱,充分過濾或離心去除金屬氯化物沉澱,得到雙癸基二甲基氫氧化銨溶液,即得溶液c;
製備溶液d:將1份摩爾的乙醯化丙氨酸溶於無水乙醇中,製成溶液,即得溶液d;
製備溶液e:將溶液c與溶液d充分混合,充分過濾或離心,即得溶液e;
得到產物:用旋轉蒸發儀回收溶液e的無水乙醇,得到產物daac。
本發明涉及一種胺基酸季氨基羧酸鹽的合成方法,該方法適用於胺基酸季氨基羧酸鹽,由帶負電荷的胺基酸陰離子和氨基陽離子構成。
所述的適用於該合成方法的胺基酸季氨基羧酸鹽具有以下通式:
其中a-coo-代表被保護的胺基酸;
其中的a代表不同的胺基酸殘基;
其中r1和r2代表直鏈、環鏈烷基或h;r1和r2可以相同,也可以不同。
所述的合成方法適用於胺基酸季氨基羧酸鹽,其結構式中r1和r2為8-18個碳原子的烷基,其中r1和r2可以相同,也可以不同的雙鏈化合物。
所述的合成方法適用於胺基酸季氨基羧酸鹽,其特徵在於結構式中r1或r2為8-18個碳原子的烷基,其中r1或r2可以是h、甲基、乙基、丙基、烷氧基、芳香基、環烷基等其它取代基的單鏈化合物。
適用於本發明所述的合成方法的胺基酸季氨基羧酸鹽中可被非環基,環基,無環基或烷氧基取代的芳香基有芐基,甲苯基,二甲苯基,萘基,吡啶基,苯亞甲基,喹啉基等。本發明所述的合成方法適用於合成:四甲基醯基胺基酸銨,三甲基乙基醯基胺基酸銨,二甲基二乙基醯基胺基酸銨,二甲基三乙基醯基胺基酸銨,四乙基醯基胺基酸銨,十六醇二甲基乙基醯基胺基酸銨,三甲基丙基醯基胺基酸銨,二甲基丙基醯基胺基酸銨,甲基三丙基醯基胺基酸銨),四丙基醯基胺基酸銨,甲基乙基丙基丁基醯基胺基酸銨,乙基丙基戊基醯基胺基酸銨,三甲基烯丙基醯基胺基酸銨,二甲基二烯丙基醯基胺基酸銨,甲基三烯丙基醯基胺基酸銨,四烯丙基醯基胺基酸銨,十八烷基三甲基醯基胺基酸銨,雙十八烷基二甲基醯基胺基酸銨,三(十八烷基)甲基醯基胺基酸銨,四(十八烷基)醯基胺基酸銨,六癸基三乙基醯基胺基酸銨,六癸基二甲基乙基醯基胺基酸銨,六癸基二乙基甲基醯基胺基酸銨,雙癸基雙辛基醯基胺基酸銨,雙癸基雙己基醯基胺基酸銨,以及癸基十八烷基十二烷基醯基胺基酸銨。
本發明所述的合成方法適用於合成含芳香基的醯基化胺基酸鹽,包括:苯十二烷基二甲基醯基胺基酸銨,o-甲苯基十二烷基二甲基醯基胺基酸銨,m-甲苯基十二烷基二甲基醯基胺基酸銨,p-甲苯基十二烷基二甲基醯基胺基酸銨,2,3-甲苯基十二烷基二甲基醯基胺基酸銨,2,4-甲苯基十二烷基二甲基醯基胺基酸銨,2,5-甲苯基十二烷基二甲基醯基胺基酸銨,3.4-甲苯基十二烷基二甲基醯基胺基酸銨,3,5-甲苯基十二烷基二甲基醯基胺基酸銨,2-氯苯基十二烷基二甲基醯基胺基酸銨,3-氯苯基十二烷基二甲基醯基胺基酸銨,4-氯苯基十二烷基二甲基醯基胺基酸銨,2,3-二氯苯基十二烷基二甲基醯基胺基酸銨,2,4-氯苯基十二烷基二甲基醯基胺基酸銨,2,5-二氯苯基十二烷基二甲基醯基胺基酸銨,2,6-二氯苯基十二烷基二甲基醯基胺基酸銨,3,4-二氯苯基十二烷基二甲基醯基胺基酸銨,3,5-二氯苯基十二烷基二甲基醯基胺基酸銨,2-氮苯基十二烷基二甲基醯基胺基酸銨,3-氮苯基十二烷基二甲基醯基胺基酸銨,4-氮苯基十二烷基二甲基醯基胺基酸銨,2,4-二氮苯基十二烷基二甲基醯基胺基酸銨,3,5-二氮苯基十二烷基二甲基醯基胺基酸銨,2-硫苯基十二烷基二甲基醯基胺基酸銨,3-硫苯基十二烷基二甲基醯基胺基酸銨,4-硫苯基十二烷基二甲基醯基胺基酸銨,2-羧苯基十二烷基二甲基醯基胺基酸銨,3-羧苯基十二烷基二甲基醯基胺基酸銨,4-羧苯基十二烷基二甲基醯基胺基酸銨,苯己基二甲基醯基胺基酸銨,苯辛基二甲基醯基胺基酸銨,苯癸基二甲基醯基胺基酸銨,苯十二烷基二甲基醯基胺基酸銨,苯十四烷基二甲基醯基胺基酸銨,苯十六烷基二甲基醯基胺基酸銨,苯十八烷基二甲基醯基胺基酸銨。
本發明所述的合成方法適用於合成胺基酸季氨基羧酸鹽,其接在四價銨離子上的脂肪或脂環可被含1-30個碳原子的直鏈烷烴或支鏈烷烴基團取代;也可被含1-30個碳原子的直鏈或支鏈烷氧基團取代。可被取代的脂環基團包括:n-己基滷化吡啶鎓(n-hexylpyridiniumhalide),n-辛基滷化吡啶鎓(n-octylpyridiniumhalide),n-癸基滷化吡啶鎓(n-decylpyridiniumhalide),n-十二烷基滷化吡啶鎓(n-dodecylpyridiniumhalide),n-十四烷基滷化吡啶鎓(n-tetradecylpyridiniumhalide),n-十六烷基滷化吡啶鎓(n-hexadecylpyridiniumhalide),己基二甲基滷化吡啶鎓(n-hexyllutidiniumhalide),辛基二甲基滷化吡啶鎓(n-octyllutidiniumhalide),癸基二甲基滷化吡啶鎓(n-decyllutidiniumhalide),十二烷基二甲基滷化吡啶鎓(n-dodecyllutidiniumhalide),十四烷基二甲基滷化吡啶鎓(n-tetradecyllutidiniumhalide),十六烷基二甲基滷化吡啶鎓(n-hexadecyllutidiniumhalide),己基甲基滷化吡啶鎓(n-hexylpicoliniumhalide),辛基甲基滷化吡啶鎓(n-octylpicoliniumhalide),癸基甲基滷化吡啶鎓(n-decylpicoliniumhalide),十二烷基甲基滷化吡啶鎓(n-dodecylpicoliniumhalide),十四烷基甲基滷化吡啶鎓(n-tetradecylpicoliniumhalide),十六烷基甲基滷化吡啶鎓(n-hexadecylpicoliniumhalide),己基滷化喹啉(n-hexylquinoliniumhalide),辛基滷化喹啉(n-octylquinoliniumhalide),癸基滷化喹啉(n-decylquinoliniumhalide),十二烷基滷化喹啉(n-dodecylquinoliniumhalide),十四烷基滷化喹啉(n-tetradecylquinoliniumhalide),十六烷基滷化喹啉(n-hexadecylquinoliniumhalide),己基滷化異喹啉(n-hexylisoquinoliniumhalide),辛基滷化異喹啉(n-octylisoquinoliniumhalide),癸基滷化異喹啉(n-decylisoquinoliniumhalide),十二烷基滷化異喹啉(n-dodecylisoquinoliniumhalide),十四烷基滷化異喹啉(n-tetradecylisoquinoliniumhalide),十六烷基滷化異喹啉(n-hexadecylisoquinoliniumhalide),己基滷化喹唑啉(n-hexylquinazoliniumhalide),辛基滷化喹唑啉(n-octylquinazoliniumhalide),癸基滷化喹唑啉(n-decylquinazoliniumhalide),十二烷基滷化喹唑啉(n-dodecylquinazoliniumhalide),十四烷基滷化喹唑啉(n-tetradecylquinazoliniumhalid),十六烷基滷化喹唑啉(n-hexadecylquinazoliniumhalide),己基滷化喹喔啉(n-hexylquinoxaliniumhalide),辛基滷化喹喔啉(n-octylquinoxaliniumhalide),癸基滷化喹喔啉(n-decylquinoxaliniumhalide),十二烷基滷化喹喔啉(n-dodecylquinoxaliniumhalide),十四烷基滷化喹喔啉(n-tetradecylquinoxaliniumhalide),十六烷基滷化喹喔啉(n-hexadecylquinoxaliniumhalide),己基滷化吡啶(n-hexylpyridopyridiniumhalide),辛基滷化吡啶(n-octylpyridopyridiniumhalide),癸基滷化吡啶(n-decylpyridopyridiniumhalide),十二烷基滷化吡啶(n-dodecylpyridopyridiniumhalide),十四烷基滷化吡啶(n-tetradecylpyridopyridininumhalide),和十六烷基滷化吡啶(n-hexadecylpyridopyridiniumhalide).
適用於本發明所述的合成方法的胺基酸季氨基羧酸鹽,其結構中的醯基胺基酸部分包括:醯基亮氨酸,醯基纈氨酸,醯基苯丙氨酸,醯基脯氨酸,醯基丙氨酸,醯基異亮氨酸,醯基酪氨酸,醯基甘氨酸,醯基蛋氨酸,醯基賴氨酸,醯基絲氨酸,醯基天門冬醯胺,醯基天門冬氨酸,醯基甲基半胱氨酸,焦穀氨酸。
為了使胺基酸成為陰離子與季銨基形成胺基酸季氨基羧酸鹽,經常採用的方法是使胺基酸乙醯化:
有些胺基酸殘基有側枝鏈,這些側枝鏈帶電荷而且具有化學活性,如胱氨酸,賴氨酸,天門冬氨酸。為了合成本發明的胺基酸季氨基羧酸鹽,須要消除側枝鏈的化學活性。對於胱氨酸,可在其巰基(–sh)上接一個甲基生成–sch3基團。巰基活性高,會引起一些共價化學反應。而-sch3基團穩定,無化學活性。
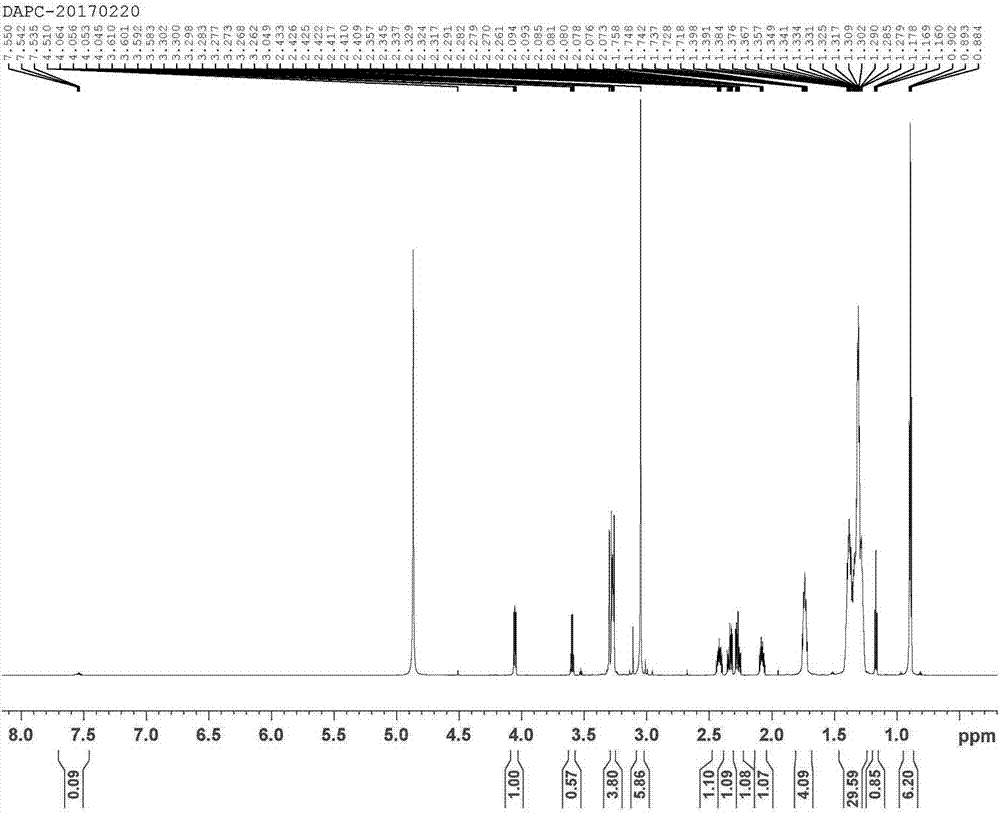
圖1是採用本發明涉合成方法合成dapc,主要衡量指標為2.0~2.5ppm處所有峰值總和與0.8~1.0ppm處峰值的比值約為4:6。
圖2是採用本發明的合成方法合成dapc,主要衡量指標為2.0~2.5ppm處所有峰值總和與0.8~1.0ppm處峰值的比值約為4:6。
圖3是採用本發明的合成方法合成daac,主要衡量指標為1.9~2.1ppm處所有峰值與0.8~1.0ppm處峰值的比值約為3:6。
圖4是按照已授權專利(專利號:zl201210166719.3)中公開的具體合成步驟合成dapc,主要衡量指標為2.0~2.5ppm處所有峰值總和與0.8~1.0ppm處峰值的比值約為2.1:6<4:6。
圖5是按照已授權專利(專利號:zl201210166719.3)中公開的具體合成步驟合成dapc,主要衡量指標為2.0~2.5ppm處所有峰值總和與0.8~1.0ppm處峰值的比值約為2.7:6<4:6。
圖6是按照已授權專利(專利號:zl201210166719.3)中公開的具體合成步驟合成dapc,主要衡量指標為2.0~2.5ppm處所有峰值總和與0.8~1.0ppm處峰值的比值約為2.3:6<4:6。
圖1、圖2、圖4、圖5、圖6中,2.0~2.5ppm處所有峰值總和與0.8~1.0ppm處峰值的比值約為4:6是指陰離子部分焦穀氨酸上3號位與4號位上的4個氫與陽離子部分雙癸基二甲基銨雙鏈末端的兩個甲基上的6個氫的比值,如果符合4:6,則說明陰離子與陽離子的比值是按照1:1的比值構成化合物,說明純度很高。如果不符合該比值,則說明陰離子與陽離子的比值不是按照1:1的比值構成化合物,說明化合物純度不高。
由此我們可以得出:採用的合成方法合成dapc,優於按照已授權專利(專利號:zl201210166719.3)公開的合成步驟合成dapc。
圖3中,1.9~2.1ppm處所有峰值與0.8~1.0ppm處峰值的比值約為1:6是指陰離子部分n-乙醯丙氨酸上乙醯基末端的甲基上的3個氫與陽離子部分雙癸基二甲基銨雙鏈末端的兩個甲基上的6個氫的比值,如果符合3:6,則說明陰離子與陽離子的比值是按照1:1的比值構成化合物,說明純度相對較高。如果不符合該比值,則說明陰離子與陽離子的比值不是按照1:1的比值構成化合物,說明化合物純度相對不高。
由此,我們可以得到採用的合成方法合成daac是符合陰陽離子1:1構成的,說明純度相對較高。
本發明的優點是克服了已授權專利(專利號:zl201210166719.3)的合成方法的缺點,實現:1.簡化了合成步驟;2.能使用毒性相對較低且較易回收、易處理的有機試劑;3.提高了胺基酸季氨基羧酸鹽的純度。
附圖說明
圖1是實施例1所得產物的nmr圖。
圖2是實施例2所得產物的nmr圖。
圖3是實施例3所得產物的nmr圖。
圖4是對比例1所得產物的nmr圖。
圖5是對比例2所得產物的nmr圖。
圖6是對比例3所得產物的nmr圖。
具體實施方式
以下用實施例和對比例對本發明做進一步的描述,但本發明的範圍不受所舉實施例的局限。
實施例1
合成雙癸基二甲基氧合脯氨酸銨dapc(proline,5-oxo-,ion(1-),n-decyl-n,n-dimethyl-1-decanaminium(1:1))的具體合成步驟如下:
製備溶液a:取無水乙醇10ml,將0.0024mol的koh溶於其中,並加熱至30℃,充分攪拌至koh完全溶解,即得溶液a;
製備溶液b:取無水乙醇10ml,在室溫條件下將0.0024mol的雙癸基二甲基氯化銨加入其中,充分攪拌至雙癸基二甲基氯化銨完全溶解,即得溶液b;
製備溶液c:在室溫下混合溶液a和溶液b,攪拌5分鐘,生成不溶於無水乙醇的氯化鉀沉澱,充分過濾或離心去除氯化鉀沉澱,得到雙癸基二甲基氫氧化銨溶液,即得溶液c;
製備溶液d:將0.0024mol的焦穀氨酸溶於無水乙醇中,製成溶液,即得溶液d;
製備溶液e:將溶液c與溶液d充分混合,即得溶液e;
得到產物:用旋轉蒸發儀回收溶液e的無水乙醇,得到產物dapc。
取適量產物做nmr(見圖1)。
實施例2
合成雙癸基二甲基氧合脯氨酸銨dapc(proline,5-oxo-,ion(1-),n-decyl-n,n-dimethyl-1-decanaminium(1:1))的具體合成步驟如下:
製備溶液a:取無水乙醇20ml,將0.005mol的koh溶於其中,並加熱至30℃,充分攪拌至koh完全溶解,即得溶液a;
製備溶液b:取無水乙醇15ml,在室溫條件下將0.005mol的雙癸基二甲基氯化銨加入其中,充分攪拌至雙癸基二甲基氯化銨完全溶解,即得溶液b;
製備溶液c:在室溫下混合溶液a和溶液b,攪拌5分鐘,生成不溶於無水乙醇的氯化鉀沉澱,充分過濾或離心去除氯化鉀沉澱,得到雙癸基二甲基氫氧化銨溶液,即得溶液c;
製備溶液d:將0.005mol的焦穀氨酸溶於無水乙醇中,製成溶液,即得溶液d;
製備溶液e:將溶液c與溶液d充分混合,即得溶液e;
得到產物:用旋轉蒸發儀回收溶液e的無水乙醇,得到產物dapc。
取適量產物做nmr(見圖2)。
實施例3
合成胺基酸雙鏈季氨基羧酸鹽是雙癸基二甲基n-乙醯基丙氨酸銨daac(1-decanaminium,n-decyl-n,n-dimethyl-,saltwithn-acetylalanine(1:1))
製備溶液a:以無水乙醇為溶劑,將0.0025mol的koh溶於其中,並加熱至20℃~30℃,充分攪拌至koh完全溶解,即得溶液a;
製備溶液b:以無水乙醇為溶劑,在室溫條件下將0.0025mol的雙癸基二甲基氯化銨加入其中,充分攪拌至雙癸基二甲基氯化銨完全溶解,即得溶液b;
製備溶液c:在室溫下混合溶液a和溶液b,攪拌1~10分鐘,生成不溶於無水乙醇的氯化鉀沉澱,充分過濾或離心去除氯化鉀沉澱,雙癸基二甲基氫氧化銨溶液,即得溶液c;
製備溶液d:將0.0025mol的n-乙醯化丙氨酸溶於無水乙醇中,製成溶液,即得溶液d;
製備溶液e:將溶液c與溶液d充分混合,即得溶液e;
得到產物:用旋轉蒸發儀回收溶液e的無水乙醇,得到產物daac。
取適量產物做nmr(見圖3)。
實施例4
其它胺基酸季氨基羧酸鹽可用同法製備,如:
脯氨酸二甲基雙癸基氨基羧酸鹽(n,n-dimethyl-n,n-di-n-decylammoniumn-acetylatedprolinecarboxylate)
苯丙氨酸二甲基雙癸基氨基羧酸鹽(n,n-dimethyl-n,n-di-n-decylammoniumn-acetylatedphenylalaninecarboxylate)
絲氨酸二甲基雙癸基氨基羧酸鹽(n,n-dimethyl-n,n-di-n-decylammoniumn-acetylatedserinecarboxylate)
異亮氨酸二甲基雙癸基氨基羧酸鹽n,n-dimethyl-n,n-di-n-decylammoniumn-acetylatedisoleucinecarboxylate
胱氨酸二甲基雙癸基羧酸鹽n,n-dimethyl-n,n-di-n-decylammoniumn-acetylateds-methylcystinecarboxylate
焦穀氨酸椰子油二甲基苄基羧酸鹽n-dodecyl-n,n-dimethyl-benzyl-ammonium-5-oxopyrrolidine-2-carboxylate
對比例1
按照已授權專利(專利號:zl201210166719.3)中公開了的合成步驟合成雙癸基二甲基氧合脯氨酸銨dapc(proline,5-oxo-,ion(1-),n-decyl-n,n-dimethyl-1-decanaminium(1:1)):
1)先稱取0.03mol的naoh,溶於去離子水中,使溶液重量為30g,並冷卻。
2)再稱取焦穀氨酸0.03mol溶於上述30g的naoh水溶液中。反應產物為焦穀氨酸鈉水溶液,得溶液a。
3)稱取0.025mol雙十烷基二甲基氯化銨溶於160g去離子水中,得溶液b。
4)將a液和b液充分混勻得到溶液c。
5)溶液c的質量約為200g。
6)取溶液c200g加入400ml二氯甲烷,並加入10克氯化鈉,充分攪勻,放入萃取瓶中再搖勻後靜置分層30分鐘。
7)取下層液抽真空旋轉蒸發30分鐘,得到產物dapc。
8)重複萃取三次。得到產物dapc。
9)取適量產物做nmr(見圖4)。
對比例2
按照已授權專利(專利號:zl201210166719.3)中公開的合成步驟合成雙癸基二甲基氧合脯氨酸銨dapc(proline,5-oxo-,ion(1-),n-decyl-n,n-dimethyl-1-decanaminium(1:1)):
1)先稱取0.025mol的naoh,溶於去離子水中,使溶液重量為20g,並冷卻。
2)再稱取焦穀氨酸0.025mol溶於上述20g的naoh水溶液中。反應產物為焦穀氨酸鈉水溶液,得溶液a。
3)稱取0.005mol雙十烷基二甲基氯化銨溶於130g去離子水中,得溶液b。
4)將a液和b液充分混勻得到溶液c。
5)溶液c的質量約為150g。
6)取溶液c150g加入400ml正丁醇,充分攪勻,放入萃取瓶中再搖勻後靜置分層30分鐘。
7)取上層液抽真空旋轉蒸發30分鐘,得到產物dapc。
8)重複萃取三次。得到產物dapc。
9)取適量產物做nmr(見圖5)。
對比例3
按照已授權專利(專利號:zl201210166719.3)中公開的合成步驟合成雙癸基二甲基氧合脯氨酸銨dapc(proline,5-oxo-,ion(1-),n-decyl-n,n-dimethyl-1-decanaminium(1:1)):
1)先稱取0.025mol的lioh,溶於去離子水中,使溶液重量為20g,並冷卻。
2)再稱取焦穀氨酸0.025mol溶於上述20g的氫氧化鋰水溶液中。反應產物為焦穀氨酸鈉水溶,得溶液a。
3)稱取0.005mol雙十烷基二甲基氯銨溶於130g去離子水中,得溶液b。
4)將a液和b液充分混勻得到溶液c。
5)溶液c的質量約為150g。
6)取溶液c150g加入400ml正丁醇,充分攪勻,放入萃取瓶中再搖勻後靜置分層30分鐘。
7)取上層液抽真空旋轉蒸發30分鐘,得到產物dapc。
8)重複萃取三次。得到產物dapc。
9)取適量產物做nmr(見圖6)。
