一種腫瘤細胞高通量分選富集微流控晶片的製作方法
2023-08-01 05:51:41 3
本發明屬於藥物傳輸系統、生物醫療診斷、集成微晶片實驗技術領域,涉及一種腫瘤細胞高通量分選富集微流控晶片,具體地說,是一種集成流量控制、癌細胞分選富集功能的微流控晶片技術。
背景技術:
癌症,亦稱惡性腫瘤,是由控制細胞生長增殖機制失常而引起的疾病。惡性腫瘤生長速度快,並且會破壞人體正常的組織與器官,最終造成患者死亡。隨著人們生活習慣和生存環境的改變,目前癌症的狀況更加嚴峻,已成為影響世界公共衛生健康最主要的問題。現代醫學發現,在癌症復發轉移早期,腫瘤細胞會從原始腫瘤灶脫落進入外周血。外周血中的腫瘤細胞(亦稱循環腫瘤細胞)常被用於預測癌症患者的生存期,也可用於指導癌症診斷和預後評估,為研製抗癌藥物提供思路。因此,能夠從外周血中快速高效地獲得腫瘤細胞將對癌症診治具有非常重要的意義。
然而截至目前,僅有美國強生公司的cellsearch系統是經過美國食品藥品監督管理局批准的用於檢測循環腫瘤細胞的儀器。該系統採用免疫磁珠標記和螢光染色的方式來捕獲和檢測腫瘤細胞,因此被捕獲的腫瘤細胞已失去生物活性,而不能用於後續的抗藥性檢測等。此外,cellsearch系統檢測費用極高,約5000元/次,因此,研發一種採用非生化標記方法的腫瘤細胞高通量分選富集微流控晶片對癌症的早期診斷、預後評估和抗癌藥物開發具有重要的價值。
技術實現要素:
為解決上述問題,本發明公開了一種腫瘤細胞高通量分選富集微流控晶片,能夠解決血液中循環腫瘤細胞密度低(1ml血液中僅1-100個)、檢測難度大等問題,實現血液中腫瘤細胞和血細胞高效、快速地分離。
為達到上述目的,本發明的技術方案如下:
一種腫瘤細胞高通量分選富集微流控晶片,包括自上而下、依次堆疊的四個功能模塊,其分別是:上導流模塊、流量調節模塊、高通量慣性分選富集模塊和下導流模塊;
所述上導流模塊上設置有生理鹽水入口、生理鹽水流道、生理鹽水出口、血液入口、血液流道和血液出口;所述生理鹽水入口與裝有生理鹽水的離心管相連;所述血液入口與裝有血液的離心管相連;使用時,生理鹽水與血液分別通過設置在上導流模塊上的生理鹽水入口和血液入口進入上導流模塊;生理鹽水和血液分別通過生理鹽水流道和血液流道導流至預設位置,並由生理鹽水出口和血液出口流出;
所述流量調節模塊上設置有生理鹽水入口、生理鹽水主流道、生理鹽水出口、生理鹽水流量控制流道、血液入口、血液主流道、血液出口、血液流量控制流道;所述上導流模塊上設置的生理鹽水出口和血液出口分別與流量調節模塊上設置的生理鹽水入口和血液入口相通;當生理鹽水流至生理鹽水主流道的中間位置時,生理鹽水流量控制流道起流量調節作用,其原理是:生理鹽水主流道與生理鹽水流量控制流道的流體壓力不同(流體壓力不同是由於流量調節閥的結構引起的,生理鹽水主流道的流體壓力從入口到出口由n逐漸衰減到0,生理鹽水流量控制流道的流體壓力始終等於入口壓力n,兩者在生理鹽水主流道中間被彈性薄膜隔開,故壓力分別為n/2和n,引起薄膜變形),引起生理鹽水主流道和生理鹽水流量控制流道之間的彈性薄膜變形;彈性薄膜通過擠壓生理鹽水主流道來調節流體流量;血液的流量調節原理與生理鹽水相同;
所述高通量慣性分選富集模塊上設置有生理鹽水入口、血液入口、慣性分選流道、血細胞出口和腫瘤細胞出口;生理鹽水和血液經過流量調節模塊調整至目標流量後,分別從生理鹽水入口和血液入口流進高通量慣性分選富集模塊;血液中的血細胞和腫瘤細胞在慣性分選流道內受到慣性升力及dean拽力的作用,並在慣性分選流道出口處分別聚焦在流道外壁面和內壁面,最終通過y形出口分離至血細胞出口和腫瘤細胞出口;
所述下導流模塊上設置有血細胞入口、血細胞流道、血細胞出口、腫瘤細胞入口、腫瘤細胞流道和腫瘤細胞出口;所述血細胞出口和腫瘤細胞出口分別與血細胞收集管和腫瘤細胞收集管相連;血液中的血細胞和腫瘤細胞最後通過下導流模塊流至不同的採樣管中。
本發明的有益效果是:
本發明所述的腫瘤細胞高通量分選富集微流控晶片,可以實現血液中腫瘤細胞和血細胞高效、快速地分離,其分離方法不影響腫瘤細胞活性,能用於後續的抗藥性檢測。
附圖說明
圖1是腫瘤細胞高通量分選富集微流控晶片功能模塊爆炸圖;
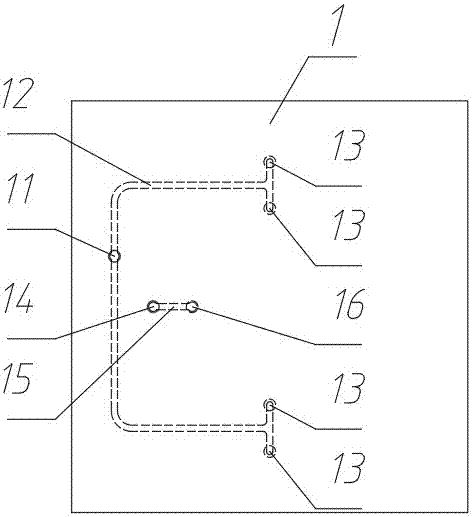
圖2是上導流模塊的俯視圖;
圖3是流量調節模塊的俯視圖;
圖4是高通量慣性分選富集模塊的俯視圖;
圖5是下導流模塊的俯視圖;
圖6是圖3中a-a剖面結構示意圖;
圖7是腫瘤細胞高通量分選富集微流控晶片的俯視圖。
其中,1為上導流模塊,11為生理鹽水入口一,12為生理鹽水流道,13為生理鹽水出口一,14為血液入口一,15為血液流道,16為血液出口一,2為流量調節模塊,21為生理鹽水入口二,22為生理鹽水主流道,23為生理鹽水出口二,24為生理鹽水上流量控制流道,25為生理鹽水下流量控制流道,26為血液入口二,27為血液主流道,28為血液出口二,29為血液上流量控制流道,210為血液下流量控制流道,3為高通量慣性分選富集模塊,31為生理鹽水入口三,32為血液入口三,33為慣性分選流道,34為血細胞出口一,35為腫瘤細胞出口一,4為下導流模塊,41為血細胞入口,42為血細胞流道,43為血細胞出口二,44為腫瘤細胞入口,45為腫瘤細胞流道,46為腫瘤細胞出口二,51為上流量控制層,52為上彈性薄膜,53為主流道層,54為下彈性薄膜,55為下流量控制層。
具體實施方式
下面結合附圖對本發明作更進一步的說明。
一種腫瘤細胞高通量分選富集微流控晶片,如圖1所示,包括由上到下依次堆疊的上導流模塊(1)、流量調節模塊(2)、高通量慣性分選富集模塊(3)和下導流模塊(4);
如圖2所示,所述上導流模塊(1)上設置有生理鹽水入口一(11)、生理鹽水流道(12)、生理鹽水出口一(13)、血液入口一(14)、血液流道(15)和血液出口一(16);所述生理鹽水入口一(11)、生理鹽水流道(12)和生理鹽水出口一(13)依次相通;所述血液入口一(14)、血液流道(15)和血液出口一(16)依次相通;所述生理鹽水入口一(11)、生理鹽水流道(12)、生理鹽水出口一(13)與血液入口一(14)、血液流道(15)、血液出口一(16)互不相通;所述生理鹽水入口一(11)和血液入口一(14)設置在上導流模塊(1)的上表面;所述生理鹽水出口一(13)與血液出口一(16)設置在上導流模塊(1)下表面;
如圖3所示,所述流量調節模塊(2)上設置有生理鹽水入口二(21)、生理鹽水主流道(22)、生理鹽水出口二(23)、生理鹽水上流量控制流道(24)、生理鹽水下流量控制流道(25)、血液入口二(26)、血液主流道(27)、血液出口二(28)、血液上流量控制流道(29)和血液下流量控制流道(210);所述生理鹽水入口二(21)、生理鹽水主流道(22)和生理鹽水出口二(23)依次相通;所述生理鹽水入口二(21)、生理鹽水主流道(22)、生理鹽水上流量控制流道(24)和生理鹽水下流量控制流道(25)在入口處相通;所述血液入口二(26)、血液主流道(27)和血液出口二(28)依次相通;所述血液入口二(26)、血液主流道(27)、血液上流量控制流道(29)和血液下流量控制流道(210)在入口處相通;所述生理鹽水入口二(21)和血液入口二(26)設置在流量調節模塊(2)上表面;所述生理鹽水出口二(23)和血液出口二(28)設置在流量調節模塊(2)下表面;
如圖6所示,所述流量調節模塊(2)包括由上到下依次堆疊的上流量控制層(51)、上彈性薄膜(52)、主流道層(53)、下彈性薄膜(54)和下流量控制層(55);所述上流量控制層(51)和主流道層(53)在生理鹽水主流道(22)和血液主流道(27)處有上彈性薄膜(52)隔開;所述主流道層(53)和下流量控制層(55)在生理鹽水主流道(22)和血液主流道(27)處有下彈性薄膜(54)隔開;
如圖7所示,所述上導流模塊(1)上設置的生理鹽水出口一(13)和血液出口一(16)分別與流量調節模塊(2)上設置的生理鹽水入口二(21)和血液入口二(26)相連;
如圖4所示,所述高通量慣性分選富集模塊(3)上設置有生理鹽水入口三(31)、血液入口三(32)、慣性分選流道(33)、血細胞出口一(34)和腫瘤細胞出口一(35);所述生理鹽水入口三(31)、血液入口三(32)、慣性分選流道(33)、血細胞出口一(34)和腫瘤細胞出口一(35)依次相通;所述生理鹽水入口三(31)和血液入口三(32)設置在高通量慣性分選富集模塊(3)上表面;所述血細胞出口一(34)和腫瘤細胞出口一(35)設置在高通量慣性分選富集模塊(3)下表面;
如圖4所示,所述生理鹽水入口三(31)、血液入口三(32)、慣性分選流道(33)、血細胞出口一(34)和腫瘤細胞出口一(35)以下總稱為「慣性分選晶片」;所述慣性分選晶片在高通量慣性分選富集模塊(3)沿x軸、y軸對稱布置4個;
如圖7所示,所述流量調節模塊(2)上設置的生理鹽水出口二(23)和血液出口二(28)分別與高通量慣性分選富集模塊(3)上設置的生理鹽水入口三(31)和血液入口三(32)相通;
如圖5所示,所述下導流模塊(4)上設置有血細胞入口(41)、血細胞流道(42)、血細胞出口二(43)、腫瘤細胞入口(44)、腫瘤細胞流道(45)和腫瘤細胞出口二(46);血細胞入口(41)、血細胞流道(42)和血細胞出口二(43)依次相通;腫瘤細胞入口(44)、腫瘤細胞流道(45)和腫瘤細胞出口二(46)依次相通;血細胞入口(41)、血細胞流道(42)、血細胞出口二(43)、腫瘤細胞入口(44)、腫瘤細胞流道(45)和腫瘤細胞出口二(46)互不相通;所述血細胞入口(41)和腫瘤細胞入口(44)設置在下導流模塊(4)的上表面;所述血細胞出口二(43)和腫瘤細胞出口二(46)設置在下導流模塊(4)的下表面;
如圖7所示,所述高通量慣性分選富集模塊(3)上設置的血細胞出口一(34)和腫瘤細胞出口一(35)分別與下導流模塊(4)上設置的血細胞入口(41)和腫瘤細胞入口(44)相連。
實施例:
如圖1所示,腫瘤細胞高通量分選富集微流控晶片由四個功能模塊堆疊組成,整體結構由上到下依次包括上導流模塊(1)、流量調節模塊(2)、高通量慣性分選富集模塊(3)和下導流模塊(4),所述上導流模塊分別與裝有生理鹽水和血液的離心管相連,用於腫瘤細胞高通量分選富集微流控晶片的生理鹽水和血液進樣,所述流量調節模塊上可設置多個被動式流量調節閥,並分別用於生理鹽水和血液的流量調節,經過實驗測試,生理鹽水和血液的流量比例為8:1時,腫瘤細胞能夠較明顯地與血細胞分離。因此,如圖3所示,本實施例中有單個被動式流量調節閥用於血液的流量調節,有8個並聯集成的被動式流量調節閥用於生理鹽水的流量調節,其目標流量大小分別是血液流量1.25ml/min及生理鹽水流量10ml/min。如圖4所示,所述高通量慣性分選富集模塊(3)上設置有螺旋狀的慣性分選流道(33)。腫瘤細胞和血細胞在慣性分選流道中因慣性升力及dean拽力的作用,分別平衡至流道的不用位置。為提高腫瘤細胞分選速度,本實施例中在同一平面內集成了4個慣性分選晶片,並在垂直方向上堆疊2層,使得腫瘤細胞的分選效率提高了8倍。如圖5所示,血細胞和腫瘤細胞由下導流模塊上設置的血細胞流道(42)和腫瘤細胞流道(45)導流至不同出口,並最終分別收集到採樣管中。
本實施例中,上導流模塊(1)、高通量慣性分選富集模塊(3)和下導流模塊(4)的材質均為pvc塑料。流量調節模塊(2)包含多種材質,具體是:上流量控制層、主流道層和下流量控制層的材質為矽膠。上彈性薄膜和下彈性薄膜的材質為聚二甲基矽氧烷pdms,為提高彈性薄膜的靈敏度,預聚體和交聯體的質量比率為20:1,使用不同材質製作時,因為材質的彈塑性與表面特性不同,會引起流量調節模塊(2)的流量調節性能差異,因此在實際加工過程中,應當根據高通量慣性分選富集模塊(3)所需求的流量調節要求選擇恰當的材質、堆疊方式及工藝參數。
本實施例中,上導流模塊(1)、高通量慣性分選富集模塊(3)和下導流模塊(4)均採用雷射加工來切割出所需的流道結構。製作時,在選取的pvc基底和塑封膜上分別用雷射器切割出所需流道結構,再使用塑封機完成封裝,流量調節模塊(2)亦可採用雷射加工技術在選取的矽膠基底上切割出所需的流道結構,再通過離子體鍵合技術完成封裝,本技術加工時間短(<1min/片),加工精度高(偏差約5μm),製作成本低,靈活性極強。
本實施例中,彈性薄膜可通過將聚二甲基矽氧烷pdms旋塗在聚醯亞胺薄膜表面獲得。本實施例中製備的彈性薄膜厚度為20μm,即上彈性薄膜(52)和下彈性薄膜(54)的厚度為20μm。
圖2為上導流模塊的俯視圖,包括生理鹽水入口一(11)、生理鹽水流道(12)、生理鹽水出口一(13)、血液入口一(14)、血液流道(15)和血液出口一(16)。
圖3為流量調節模塊的俯視圖,生理鹽水入口二(21)、生理鹽水主流道(22)、生理鹽水出口二(23)、生理鹽水上流量控制流道(24)、生理鹽水下流量控制流道(25)、血液入口二(26)、血液主流道(27)、血液出口二(28)、血液上流量控制流道(29)和血液下流量控制流道(210)。
圖4為高通量慣性分選富集模塊的俯視圖,生理鹽水入口三(31)、血液入口三(32)、慣性分選流道(33)、血細胞出口一(34)和腫瘤細胞出口一(35)。
圖5為下導流模塊的俯視圖,血細胞入口(41)、血細胞流道(42)、血細胞出口二(43)、腫瘤細胞入口(44)、腫瘤細胞流道(45)和腫瘤細胞出口二(46)。
上所述僅是本發明的優選實施方式,應當指出:對於本技術領域的普通技術人員來說,在不脫離本發明原理的前提下,還可以做出若干改進和潤飾,這些改進和潤飾也應視為本發明的保護範圍。
