檢測地西泮的酶聯免疫試劑盒及其應用的製作方法
2023-06-14 10:28:41 6
本發明涉及酶聯免疫檢測技術,具體涉及一種用於檢測地西泮的酶聯免疫試劑盒,其特別適於動物組織、尿液、飼料、水質中地西泮含量的檢測。
背景技術:
地西泮,又稱安定,是一種中樞神經系統鎮靜劑,其化學名稱為1-甲基-5-苯基-7-氯-1,3-二氫-1,4-苯並二氮卓-2-酮,它主要用於人和動物鎮靜、催眠、癲癇的治療;畜牧生產中用作動物抗運輸應激的藥物,亦被大量非法用作動物增重促進劑。當人體攝入含有地西泮殘留的食物後,肝臟負擔加重,頭腦昏昏沉沉,記憶受損,個別人出現皮疹、白細胞減少及運動神經和肌肉功能受到抑制,為此農業部規定所有食品動物中均不得檢出地西泮及其鹽和酯等。
目前,國內外已報導的地西泮及其代謝物的測定方法有HPLC、HPLC-MS/MS、GC-MS、GC-ECD、固相萃取-紫外導數光譜檢測、TLC-UV等。HPLC、TLC等方法受靈敏度限制,無法滿足目前殘留分析檢測的要求;HPLC-MS/MS作為目前報導最多的方法,可以同時進行地西泮及其代謝物的定性定量分析,但需要昂貴的儀器和專門的技術人員,樣品前處理過程複雜且花費高、費時長,難以滿足大量樣品和現場樣品快速檢測的需要。酶聯免疫吸附分析法(ELISA)具有簡便快速、特異靈敏、樣品容量大、分析成本低的特點,可以簡化甚至省去樣品淨化步驟,在大量樣本和現場樣本快速篩選檢測中顯示出獨特優勢,能夠更好地滿足我國食品企業、政府職能監管部門等開展檢測工作,極具發展潛力。
技術實現要素:
本發明的目的在於提供一種結構簡單、使用方便、價格便宜、便於攜帶的用於地西泮檢測的酶聯免疫試劑盒,並提供一種高效、準確、簡便、適於大批量樣本篩選的定性、定量檢測方法。
本發明試劑盒,它包括:包被有地西泮偶聯抗原的酶標板、地西泮單克隆抗體、酶標記抗抗體、地西泮標準品溶液、底物顯色液、終止液、洗滌液、復溶液;所述地西泮偶聯抗原是由地西泮半抗原與載體蛋白偶聯得到,所述載體蛋白為鼠血清蛋白、甲狀腺蛋白、牛血清白蛋白、兔血清蛋白、人血清白蛋白、卵清蛋白、血藍蛋白或纖維蛋白原,所述地西泮半抗原是由馬來醯亞胺基苯甲酸與草醯氯反應後,再與去甲地西泮反應得到,分子結構式為:
所述地西泮單克隆抗體是以地西泮偶聯抗原作為免疫原製備獲得。
所述酶標記抗抗體的抗抗體為羊抗鼠抗抗體。
所述酶標記抗抗體的標記酶為辣根過氧化物酶;酶標記抗抗體是採用戊二醛法或過碘酸鈉法將標記酶與抗抗體進行偶聯得到的。
為了更方便現場監控和大量樣本篩查,所述試劑盒還包括地西泮標準品溶液、底物顯色液、終止液、洗滌液、復溶液。
所述地西泮標準品溶液6瓶,濃度分別為0μg/L、0.1μg/L、0.2μg/L、0.4μg/L、0.8μg/L、1.6μg/L。
所述底物顯色液由底物液A液和底物液B液組成,底物液A液為過氧化氫或過氧化脲,底物液B液為鄰苯二胺或四甲基聯苯胺,所述終止液為1~2mol/L的硫酸溶液。
所述洗滌液優選為pH值為7.4,含有0.5%~1.0%吐溫-20、0.01‰~0.03‰疊氮化鈉、0.1~0.3mol/L的磷酸鹽緩衝液。
所述復溶液優選為pH值為7.0、0.1mol/L的磷酸鹽緩衝液。
其中在酶標板製備過程中所用到的包被緩衝液為pH值為9.6、0.05mol/L的碳酸鹽緩衝液,封閉液為pH值為7.1~7.5,含有1%~3%酪蛋白、0.1~0.3mol/L的磷酸鹽緩衝液。
本發明中酶標板的製備過程為:用包被緩衝液將包被原稀釋成20μg/mL,每孔加入100μL,37℃避光孵育2h或4℃過夜,傾去孔中液體,用洗滌液洗滌2次,每次30s,拍幹,然後在每孔中加入150~200μL封閉液,37℃避光孵育1~2h,傾去孔內液體拍幹,乾燥後用鋁膜真空密封保存。
本發明的檢測原理為:
在微孔條上預包被地西泮偶聯抗原,加入樣本溶液或標準品溶液後,再加入地西泮單克隆抗體溶液,樣本中的地西泮與酶標板上包被的地西泮偶聯抗原競爭地西泮單克隆抗體,加入酶標記抗抗體進行放大作用,用顯色液顯色,樣本吸光度值與地西泮的含量呈負相關,與標準曲線比較即可得到樣本中地西泮的殘留量;同時根據酶標板上顏色的深淺,與系列濃度的標準品溶液顏色的比較可粗略判斷樣本中地西泮殘留量的濃度範圍。
本發明還提供了一種應用上述酶聯免疫試劑盒檢測地西泮的方法,它包括步驟:
(1)樣本前處理;
(2)用試劑盒進行檢測;
(3)分析檢測結果。
本發明檢測地西泮的酶聯免疫試劑盒主要採用間接競爭ELISA方法定性或定量檢測樣本中地西泮的含量;對樣本的前處理要求低,樣本前處理過程簡單,能同時快速檢測大批量樣本;主要試劑以工作液的形式提供,檢驗方法方便易行,具有特異性高、靈敏度高、精確度高、準確度高等特點。本發明的酶聯免疫試劑盒,結構簡單、使用方便、價格便宜、攜帶便利、檢測方法高效、準確、簡便、適於大批量樣本篩選的定性、定量檢測。
附圖說明
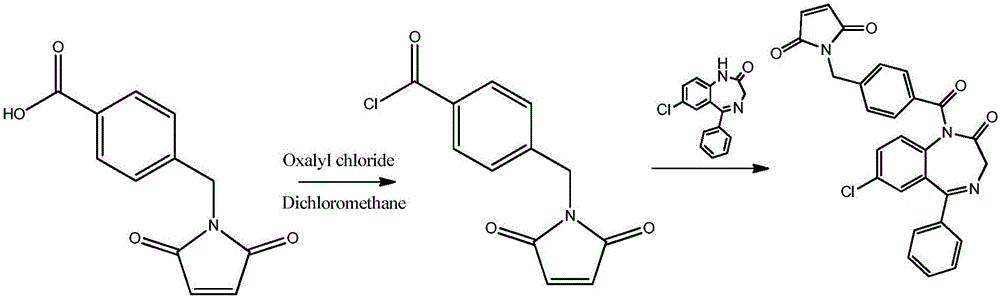
圖1:地西泮半抗原合成路線圖
圖2:試劑盒標準曲線圖
具體實施方式
下面結合具體的實施例來進一步闡述本發明。應理解,這些實施例僅用於說明本發明,而不用來限制本發明的範圍。
實施例1試劑盒組分的製備
1、地西泮半抗原的合成(合成路線見附圖1)
A、取馬來醯亞胺基苯甲酸1g,加二氯甲烷溶解,加草醯氯1.09g,室溫攪拌2h;加冰水震蕩,分層,取下層有機相用無水硫酸鈉乾燥,蒸乾,得到油狀產物,氯仿/正己烷(1/1,v/v)重結晶,得到馬來醯亞胺基苯甲醯氯產物0.93g,收率86.92%;
B、0.93g馬來醯亞胺基苯甲醯氯用吡啶溶解,加去甲地西泮1.0g,油浴加熱,回流反應4h,停止反應,TLC檢測,原料基本無剩餘;旋蒸,除去吡啶,得到紅色油狀物,1,2-二氯乙烷重結晶,得到半抗原產物馬來醯亞胺地西泮1.2g,收率66.67%。
2、地西泮偶聯抗原的合成及鑑定
免疫原製備——地西泮半抗原與牛血清白蛋白(BSA)偶聯得到免疫原。
取BSA 50mg,加5mL 0.05mol/L pH9.5的碳酸鹽緩衝液溶解,加二硫蘇糖醇10mg,室溫攪拌過夜,得到A液;取半抗原馬來醯亞胺地西泮12mg,加N,N-二甲基甲醯胺(DMF)溶解,逐滴加到活化的BSA蛋白A液中,室溫避光攪拌反應4h;用0.02mol/L PBS透析3天,每天換液3次,分裝,-20℃保存備用。
包被原製備——地西泮半抗原與人血清白蛋白(HSA)偶聯得到包被原。
取半抗原馬來醯亞胺地西泮12mg,加DMF溶解,得到A液;取HSA 50mg,加5mL 0.05mol/L pH9.5的碳酸鹽緩衝液溶解,加二硫蘇糖醇10mg,室溫攪拌過夜,將A液逐滴加到蛋白活化液中,室溫避光攪拌4h;用0.02mol/L PBS透析3天,每天換液3次,分裝,-20℃保存備用。
按合成地西泮偶聯抗原反應所用半抗原、載體蛋白與偶聯產物的比例,進行紫外(200nm~400nm)掃描測定,通過比較三者分別在260nm和280nm的吸光值計算其結合比。偶聯物地西泮半抗原-載體蛋白的最大吸收峰與地西泮半抗原、載體蛋白的最大吸收峰相比發生了明顯的變化,表明地西泮半抗原-載體蛋白的合成是成功的。
3、地西泮單克隆抗體的製備
(1)雜交瘤細胞的獲得
1)首次免疫:將地西泮半抗原-BSA偶聯物(免疫原)與等量的弗氏完全佐劑充分乳化,皮下注射6周齡的Balb/c小鼠,每隻0.2mL;
2)加強免疫兩次:從首次免疫開始,每兩周加強免疫一次,用弗式不完全佐劑代替弗氏完全佐劑,方法和劑量同首次免疫;
3)最後一次加強免疫一周後眼底靜脈採血測效價和抑制,有抑制且效價達到1:10000以上時進行如下末次免疫:腹腔注射不加任何佐劑的免疫原溶液0.1mL,三天後處死小鼠,取其脾臟與骨髓瘤細胞融合;
4)採用間接競爭酶聯免疫分析方法測定細胞上清液,篩選陽性孔。利用有限稀釋法對陽性孔進行克隆化,得到並建立穩定分泌地西泮單克隆抗體的雜交瘤細胞株,取處於對數生長期的雜交瘤細胞用凍存液製成細胞懸液,分裝於凍存管,在液氮中長期保存。
(2)單克隆抗體的製備
1)細胞復甦:取出地西泮單克隆抗體雜交瘤細胞株凍存管,立即放入37℃水浴中速融,離心去除凍存液後,移入培養瓶內培養;
2)製備腹水與抗體純化:採用體內誘生法,將Balb/c小鼠(8周齡)腹腔注入滅菌石蠟油0.5mL/只,7天後腹腔注射雜交瘤細胞5×105個/只,7天後採集腹水。用辛酸-飽和硫酸銨法進行純化,得到地西泮單克隆抗體溶液(-20℃保存)。
(3)單克隆抗體效價的測定
用間接競爭ELISA法測定抗體的效價為1:(200000~500000)。
間接競爭ELISA方法:用地西泮半抗原-HSA偶聯物包被酶標板,加入地西泮標準品溶液、地西泮單克隆抗體溶液和辣根過氧化物酶標記的羊抗鼠抗抗體溶液,25℃反應30min,倒出孔內液體,用洗滌液洗滌3~5次,用吸水紙拍幹;加入底物顯色液,25℃反應15min後,加入終止液終止反應;設定酶標儀于波長450nm處測定每孔吸光度值。
(4)單克隆抗體特異性的測定
抗體特異性是指它同特異性抗原結合的能力與同該類抗原類似物結合能力的比較,常用交叉反應率作為評價標準。交叉反應越小,抗體的特異性則越高。
本實驗將地西泮、硝西泮、奧沙西泮做系列稀釋,分別與單克隆抗體進行間接競爭ELISA,製作標準曲線,分析得到IC50,然後按下式計算交叉反應率:
結果顯示各類似物的交叉反應率為:地西泮100%、硝西泮7.6%、奧沙西泮8.8%。本發明抗體對硝西泮、奧沙西泮等類似物無交叉反應,只針對地西泮有特異性結合。
4、羊抗鼠抗抗體的製備
以羊為免疫動物,以鼠源抗體為免疫原免疫無病原體羊,得到羊抗鼠抗抗體。
5、酶標記抗抗體的製備
將羊抗鼠抗抗體與辣根過氧化物酶(HRP)採用改良後的過碘酸鈉法進行偶聯。傳統的過碘酸鈉法要求反應體系中酶與抗體的摩爾濃度比為4:1,由於辣根過氧化物酶在強氧化作用下產生許多與抗體結合的位點,這樣活化的辣根過氧化物酶分子充當了連接各分子的橋梁,降低了酶標記物的酶活性,使製備的偶聯物中混有許多聚合體。為了解決這個問題,我們將傳統的方法進行了改良,即:
(1)省去了氨基的封閉過程,因為能產生自身氨基連接的氨基實際很少;
(2)降低辣根過氧化物酶與抗體的摩爾濃度比率至2:1,改良後的方法比傳統的方法簡便,對酶活性的損失減少。
6、酶標板的製備
用包被緩衝液將包被原(地西泮半抗原-HSA偶聯物)稀釋成20μg/mL,每孔加入100μL,37℃避光孵育2h,傾去孔中液體,用洗滌液洗滌2次,每次30s,拍幹,然後在每孔中加入200μL封閉液,37℃避光孵育2h,傾去孔內液體拍幹,乾燥後用鋁膜真空密封保存。
實施例2檢測地西泮的酶聯免疫試劑盒的組建
組建檢測地西泮的酶聯免疫試劑盒,使其包含下述組分:
(1)包被地西泮偶聯抗原的酶標板;
(2)地西泮標準品溶液6瓶,濃度分別為0μg/L、0.1μg/L、0.2μg/L、0.4μg/L、0.8μg/L、1.6μg/L;
(3)地西泮單克隆抗體工作液;
(4)用辣根過氧化物酶標記的羊抗鼠抗抗體;
(5)底物顯色液由A液和B液組成,A液為過氧化脲,B液為四甲基聯苯胺;
(6)終止液為2mol/L硫酸;
(7)洗滌液為pH值為7.4,含有0.5%~1.0%吐溫-20、0.01‰~0.03‰疊氮化鈉、0.1~0.3mol/L的磷酸鹽緩衝液;
(8)復溶液為pH值為7.0、0.1mol/L的磷酸鹽緩衝液。
實施例3樣本中地西泮的檢測
1、樣本前處理
組織樣本:
稱取2.0g±0.05g均質後的組織樣本至50mL聚苯乙烯離心管中,加入8mL 0.1mol/L氫氧化鈉溶液,用振蕩器振蕩5min,3000g室溫(20~25℃)離心10min;移取1mL上清液至50mL聚苯乙烯離心管中,加入10mL正己烷,用振蕩器振蕩5min,3000g室溫(20~25℃)離心10min;移取5mL上層有機相至10mL潔淨乾燥玻璃管中,於50~60℃水浴氮氣流下吹乾;加入1mL復溶液,用渦旋儀渦動2min;取50μL用於分析。
尿液、水質樣本:
移取1mL清亮樣本至50mL聚苯乙烯離心管中,加入4mL 0.1mol/L氫氧化鈉溶液,用振蕩器振蕩2min;移取1mL混合液至50mL聚苯乙烯離心管中,加入10mL正己烷,用振蕩器振蕩5min,3000g室溫(20~25℃)離心10min;移取5mL上層有機相至10mL潔淨乾燥玻璃管中,於50~60℃水浴氮氣流下吹乾;加入1mL復溶液,用渦旋儀渦動2min;取50μL用於分析。註:若樣本不清亮,需3000g室溫(20~25℃)離心5min。
飼料樣本:
稱取1.0g±0.05g飼料樣本至50mL聚苯乙烯離心管中,分別加入1mL去離子水和3mL0.1mol/L氫氧化鈉溶液,用渦旋儀渦動1min,再加入10mL正己烷,用振蕩器振蕩10min,3000g室溫(20~25℃)離心10min;移取1mL上層有機相至10mL潔淨乾燥玻璃試管中,於50~60℃水浴氮氣流下吹乾;加入1mL復溶液,用渦旋儀渦動2min;不同飼料樣本再按如下方法進行稀釋:配合料:將樣本液與復溶液按1:9體積比進行稀釋檢測(1份樣本液+9份復溶液),濃縮料/預混料:將樣本液與復溶液按1:19體積比進行稀釋檢測(1份樣本液+19份復溶液);取50μL用於分析。
2、用試劑盒檢測
向包被有地西泮偶聯抗原的酶標板微孔中加入地西泮標準品溶液或經前處理的樣本溶液50μL/孔,然後加入地西泮單克隆抗體工作液50μL/孔,輕輕振蕩混勻,用蓋板膜蓋板後置25℃避光環境中反應30min;倒出孔內液體,每孔加入250μL洗滌液充分洗滌4~5次,每次間隔10s,用吸水紙拍幹;再加入辣根過氧化物酶標記的羊抗鼠抗抗體100μL/孔,輕輕振蕩混勻,用蓋板膜蓋板後置25℃避光環境中反應30min,取出重複洗板步驟;每孔加入底物液A液過氧化脲50μL,底物液B液四甲基聯苯胺(TMB)50μL,輕輕振蕩混勻,用蓋板膜蓋板後置25℃避光環境中反應15min,每孔加入終止液2mol/L硫酸50μL,輕輕振蕩混勻,用酶標儀波長設定在450nm處,測定每孔吸光度值(OD值)。
3、檢測結果分析
用所獲得的每個濃度的標準品溶液的吸光度平均值(B)除以第一個標準品溶液(0標準)的吸光度值(B0)再乘以100%,得到百分吸光度值。以地西泮標準品濃度(μg/L)的對數值為X軸,百分吸光度值為Y軸,繪製標準曲線,如圖2所示。用同樣的辦法計算樣本溶液的百分吸光度值,相對應每一個樣本的地西泮含量則可從標準曲線上讀出。
實施例4地西泮酶聯免疫試劑盒技術參數的確定試驗
1、試劑盒靈敏度和檢測限
按照常規方法測定試劑盒靈敏度,試劑盒標準曲線最低點為0.1μg/L,標準曲線的範圍為0.1~1.6μg/L,IC50(50%抑制濃度)浮動範圍為0.19~0.25μg/L;對空白豬肉、雞肉、尿液、水質、配合料、濃縮料、預混料樣本各20份進行檢測,從標準曲線上查出對應於各百分吸光度值的濃度,以20份樣本濃度的平均值加上3倍標準差表示檢測限,結果得該方法對組織、尿液、水質樣本的檢測限為1μg/kg,對配合料樣本的檢測限為10μg/kg,對濃縮料、預混料樣本的檢測限為20μg/kg。
2、樣本精密度和準確度試驗
以回收率作為準確度評價指標,以重複測定某一濃度樣本的檢測結果相對標準偏差(RSD%)作為精密度評價指標。計算公式為:回收率(%)=實際測定值/理論值×100%,其中理論值為樣本的添加濃度;相對標準偏差RSD%=SD/X×100%,其中SD為標準偏差,X為測定數據的平均值。
按1μg/kg、2μg/kg、4μg/kg三個濃度地西泮對空白豬肉、雞肉、尿液、水質樣本進行添加回收測定,10μg/kg、20μg/kg、40μg/kg三個濃度地西泮對空白配合料樣本進行添加回收測定,20μg/kg、40μg/kg、80μg/kg三個濃度地西泮對空白濃縮料、預混料樣本進行添加回收測定,每個樣本做4個平行,用三批不同試劑盒進行測定,計算樣本平均回收率及精密度結果見下表。
表1精密度及準確度試驗
以1、2、4μg/kg三個濃度的地西泮對空白豬肉、雞肉、尿液、水質樣本進行添加,10、20、40μg/kg三個濃度的地西泮對空白配合料樣本進行添加,20、40、80μg/kg三個濃度的地西泮對空白濃縮料、預混料樣本進行添加,平均回收率在70%~110%之間;批內、批間相對標準偏差均小於15%。
3、試劑盒穩定性試驗
試劑盒保存條件為2~8℃,經過12個月的測定,試劑盒的最大吸光度值(零標準)、50%抑制濃度、地西泮添加實際測定值均在正常範圍之內。考慮在運輸和使用過程中,會有非正常保存條件出現,將試劑盒在37℃保存條件下放置7天,進行加速老化實驗,結果表明該試劑盒各項指標完全符合要求。考慮到試劑盒冷凍情況發生,將試劑盒放入-20℃冰箱冷凍7天,測定結果也表明試劑盒各項指標完全正常。從以上結果可得出試劑盒可以在2~8℃至少保存12個月以上。
