活化人CD40的抗體和針對人PD‑L1的抗體的組合療法的製作方法
2023-06-03 23:47:31 1
本發明涉及結合人CD40的特異性抗體與結合人PD-L1的特異性抗體的組合療法。這些組合在癌症療法的領域中特別有用。
發明背景
免疫調控性抗體提供一種治療辦法且可用於直接強化抗腫瘤免疫應答或可用作抗癌疫苗的佐劑(Melero,I.,et al.Nat Rev Cancer 7,2007,95-106)。激動性抗CD40抗體構成這些試劑中的最有效類別之一。CD40是腫瘤壞死因子超家族的一個細胞表面成員,在抗原呈遞細胞(APC)諸如樹突細胞,B細胞和巨噬細胞上表達。抗CD40激動劑的臨床前研究提示用交聯性抗體觸發抗原呈遞細胞(APC)上的CD40能取代正常情況下經由CD40配體提供的CD4 T細胞幫助及推動CD8效應T細胞活化以及擴充(Li,F.et al,Science 333,2011,1030-1034)。另外,CD40活化的巨噬細胞還可以發揮直接殺腫瘤功能(Beatty,G.L.,et al.,Science 331,2011,1612-1616;Vonderheide,R.H.,et al.,Oncoimmunology 2,2013,e23033)。CD40激動劑披露於WO 2003/040170。
最近,發現了T細胞功能障礙或無反應性與抑制性受體,編程性死亡1多肽(PD-1)的誘導的且持續的表達並行發生。從而,靶向PD-1和經由與PD-1相互作用來發信號的其它分子,諸如編程性死亡配體1(PD-L1)和編程性死亡配體2(PD-L2)的治療劑是一個強烈感興趣的領域。已經提出抑制PD-L1信號傳導作為增強T細胞免疫來治療癌症(例如腫瘤免疫力)和感染(包括急性和慢性(例如持久的)感染二者)的手段。針對PD-L1的抗體記載於例如WO 2010/077634。
共刺激或對T細胞提供兩種截然不同的信號是抗原呈遞細胞(APC)對靜息T淋巴細胞的淋巴細胞活化的一種廣泛接受的模型(Lafferty,et al.,Aust.J.Exp.Biol.Med.Sci.53,1975,27-42)。在治療上對共刺激的機制感興趣,因為操作共刺激信號已經顯示出提供增強或終止基於細胞的免疫應答的手段。然而,作為一種最佳療法,共靶向CD40和PD-L1仍然有待商品化,存在尚未滿足的一項重大醫學需求。
發明概述
本發明包含結合人CD40的抗體與結合人PD-L1的抗體的組合療法,其用於治療增殖性疾病,特別是癌症。
本發明進一步包含一種藥物產品,其包含A)第一成分,該第一成分包含作為活性組分的特異性結合且活化人CD40的抗體或其抗原結合部分;和B)第二成分,該第二成分包含作為活性組分的PD-L1抗體;其用於組合,順序或同時治療增殖性疾病,特別是癌症。
本發明進一步包含特異性結合且活化人CD40的抗體或其抗原結合部分;和PD-L1抗體用於製造藥物的用途,該藥物用於組合,順序或同時治療增殖性疾病,諸如癌症,優選實體瘤。
本發明進一步包含一種試劑盒,其包含如上文限定的藥物產品。
本發明進一步包含一種治療罹患增殖性疾病,特別是癌症的患者的方法,所述方法包含組合,同時或順序施用抗CD40抗體和PD-L1抗體。
附圖簡述
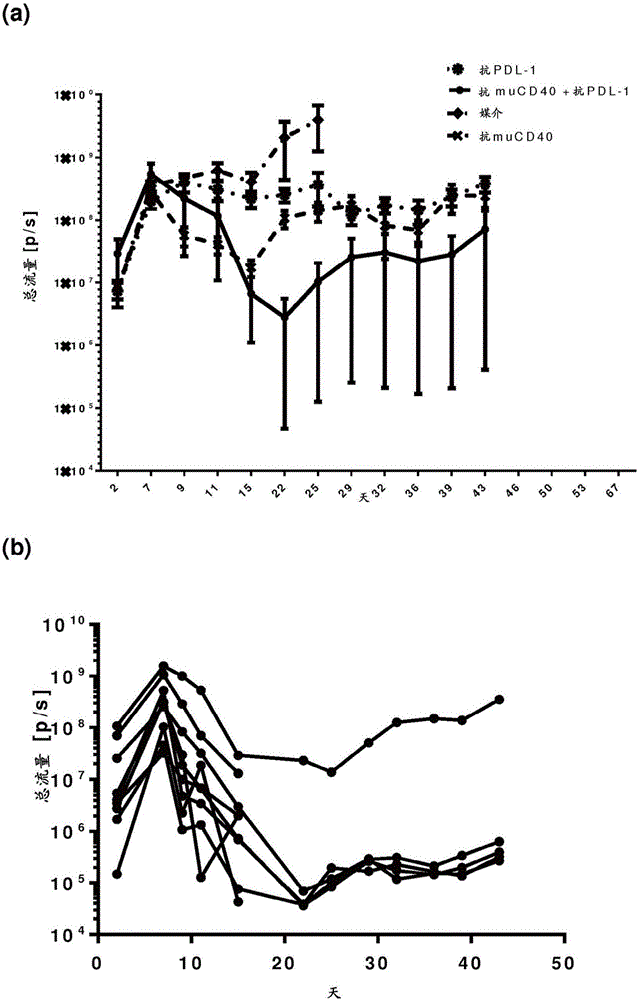
圖1:(a)同位Panc02-H7-Fluc胰腺癌模型中組合的muFGK4.5(抗CD40)和抗PD-L1較之媒介和單藥療法對照的腫瘤生長抑制的分析,(b)來自a-CD40+a-PDL1組合組的小鼠的個體腫瘤生長曲線。
圖2:在處理第22天用組合的muFGK4.5和抗PD-L1處理的小鼠個體。
圖3:同位Panc02H7-Fluc胰腺癌模型中組合的muFGK4.5和抗PD-L1抗體(「聯合」)較之對照和單藥療法的免疫藥效學(PD)分析。
圖4:牽涉人抗CD40-和抗PD-L1抗體的組合處理的臨床試驗的劑量和劑量進度表。PD-L1抗體的劑量固定於1200mg。
圖5:添加抗TNFα作為第三成分在小鼠中阻止由抗CD40/抗PD-L1組合處理誘導的重量減輕。
圖6:添加抗TNFα作為第三成分不損害抗CD40/抗PD-L1組合處理的抗腫瘤活性。
序列表簡述
SEQ ID NO 1: 人CD40
SEQ ID NO 2: 人PD-L1
SEQ ID NO 3: 依照本發明的CD40抗體的輕鏈可變域(VL)。
SEQ ID NO 4: 依照本發明的CD40抗體的重鏈可變域(VH)。
SEQ ID NO:5 重鏈可變域VH變體1,抗PD-L1 243.55
SEQ ID NO:6 重鏈可變域VH變體2,抗PD-L1 243.55
SEQ ID NO:7 重鏈可變域VH變體3,抗PD-L1 243.55
SEQ ID NO:8 輕鏈可變域VL變體1,抗PD-L1 243.55
SEQ ID NO:9 輕鏈可變域VL變體2,抗PD-L1 243.55
SEQ ID NO:10 輕鏈可變域VL變體3,抗PD-L1 243.55
SEQ ID NO:11 輕鏈可變域VL變體4,抗PD-L1 243.55
SEQ ID NO:12 輕鏈可變域VL變體5,抗PD-L1 243.55
SEQ ID NO:13 輕鏈可變域VL變體6,抗PD-L1 243.55
SEQ ID NO:14 輕鏈可變域VL變體7,抗PD-L1 243.55
SEQ ID NO:15 輕鏈可變域VL變體8,抗PD-L1 243.55
SEQ ID NO:16 輕鏈可變域VL變體9,抗PD-L1 243.55
SEQ ID NO:17 輕鏈可變域VL變體10,抗PD-L1 243.55
SEQ ID NO:18 輕鏈可變域VL變體11,抗PD-L1 243.55
SEQ ID NO:19 輕鏈可變域VL變體12,抗PD-L1 243.55
SEQ ID NO:20 輕鏈可變域VL變體13,抗PD-L1 243.55
SEQ ID NO:21 輕鏈可變域VL變體14,抗PD-L1 243.55
SEQ ID NO:22 輕鏈可變域VL變體15,抗PD-L1 243.55
SEQ ID NO:23 輕鏈可變域VL變體16,抗PD-L1 243.55
發明詳述
PD-L1(編程性死亡配體1)是結合PD-1(一種在T細胞活化後在T細胞上表達,在長期刺激的狀態下諸如在慢性感染或癌症中維持的抑制性受體)的兩種配體(PD-L1和PD-L2)之一(參見例如Blank C et al,Cancer Immunol Immunother,2005,54:307-14;及Keir ME et al,Annual Rev Immunol,2008,26:677-704)。已經報告了腫瘤細胞上PD-L1的異常表達使得它們的免疫原性低得多(Dong H et al,Nat Med,2002,8:793-800)且阻止抗腫瘤免疫力,導致免疫逃脫(Blank C et al,Cancer Immunol Immunother,2007,56:739-45)。用單克隆抗體阻斷PD-L1或PD-1在數種小鼠腫瘤模型中導致強且常常迅速的抗腫瘤效果(參見例如Iwai Y.et al,Proc Natl Acad Sci USA,2002,99:12293-7;及Strome SE et al,Cancer Res 2003,63:6501-5),提示腫瘤特異性T細胞可能以無活性或受阻抑狀態存在於腫瘤微環境中,而且抑制PD-1/PD-L1途徑可能重新激勵腫瘤特異性T細胞應答。基於該實驗數據,預期阻斷PD-L1或PD-1增強正在發生的針對腫瘤抗原的免疫應答(Merelli B et al,Crit Rev Oncol Hematol.,2014,89:140-65)。例如,對PD-L1的抗體記載於例如WO 2010/077634。
經由它在抗原呈遞細胞(APC)(包括B淋巴細胞,樹突細胞(DC),和單核細胞)上的表達,CD40(腫瘤壞死因子受體(TNFR)超家族的一個成員)是抗腫瘤免疫應答的一種至關重要調節物(參見例如Grewal IS et al,Ann Rev Immunol,1998,16:111-35;Van Kooten C et al,J Leukoc.Biol,2000,67:2-17;及O'Sullivan B et al,Crit Rev Immunol.2003,23(1 2):83-107)。經CD40刺激的DC上調抗原加工和呈遞途徑並遷移至淋巴結以活化幼稚T細胞。在鼠模型中顯示了激動性CD40抗體替代CD4+淋巴細胞的功能,導致細胞毒性T淋巴細胞(CTL)擴充,能夠清除已建立的淋巴瘤(參見例如Sotomayor EM et al,Nature Medicine,1999,5(7):780-7;及Gladue RP et al,Cancer Immunol Immunother,2011,60(7):1009-17)。CD40激動劑通過活化宿主APC,然後宿主APC驅動針對腫瘤的T細胞應答來觸發免疫刺激(參見例如Vonderheide RH,Clin Cancer Res,2007,13:1083-8)。
CD40激動劑和PD-L1抑制劑的組合如此可經由CD40激動活性觸發次級淋巴器官中抗腫瘤T細胞的引發和擴充,同時去除PD-1/PD-L1介導的抗腫瘤T細胞免疫遏制。然而,免疫療法和更具體而言T細胞介導的免疫應答還可能導致嚴重的不利事件(AE),諸如輸注相關反應,細胞因子釋放(CRS,「細胞因子風暴」或「高細胞因子血症」),和免疫相關毒性。
依照本發明,現在已經發現CD40激動劑和PD-L1抑制劑的組合,順序或同時應用在體內導致超過疊加的(即協同性的)腫瘤生長抑制和甚至個別腫瘤消除。在一個優選實施方案中,這兩種成分(即CD40激動劑和PD-L1抑制劑)的施用是順序的。
因此,在一個實施方案中,本發明提供包含CD40激動劑和PD-L1抑制劑的協同性組合。
在另一個實施方案中,本發明提供所述CD40激動劑和所述PD-L1抑制劑在人中的可接受的(即可耐受的)應用的劑量和劑量方案。對於當前組合治療,這些劑量和劑量方案降低或消除免疫相關毒性的風險且提高安全性概況和耐受性。
人CD40抗原是一種50kDa細胞表面糖蛋白,它屬於腫瘤壞死因子受體(TNF-R)家族(Stamenkovic et al.,EMBO J.8:1403-10(1989))。它也稱作「腫瘤壞死因子受體超家族成員5」。備選名稱包括B細胞表面抗原40,Bp50,CD40L受體,CDw40,CDW40,MGC9013,p50或TNFRSF5。它以例如UniProt編目號P25942登記。在一個實施方案中,人CD40抗原具有依照SEQ ID NO:1的序列(見表1)。
表1:人CD40抗原的蛋白質序列
人PD-L1(或PDL1)抗原也稱作「編程性細胞死亡1配體1」或CD274分子。備選名稱包括B7-H,B7H1,B7-H1,B7同系物1,MGC142294,MGC142296,PDCD1L1,PDCD1LG1,PDCD1配體1,PDL1,PD-L1,編程性死亡配體1。在一個實施方案中,人PD-L1抗原具有SEQ ID NO:2的序列(表2),如例如以UniProt編目號Q9NZQ7登記的。
表2:人PD-L1抗原的蛋白質序列
依照本發明,「抗CD40抗體」(或「CD40抗體」,「a-CD40抗體」)是結合,或特異性結合且活化人CD40的抗體。在一個實施方案中,人CD40具有依照SEQ ID NO:1的序列。如本文中使用的,「結合人CD40」或「特異性結合人CD40」或「結合人CD40的」或「抗CD40抗體」指以1.0x10-8mol/l或更小的KD值,在一個實施方案中,1.0x10-9mol/l或更小的KD值的結合親和力特異性結合人CD40抗原的抗體。結合親和力用標準結合測定法,諸如表面等離振子共振技術(GE-Healthcare Uppsala,Sweden)來測定。如此,如本文中使用的,「結合且活化人CD40的抗體」指以1.0x10-8mol/l或更小(在一個實施方案中,1.0x10-8mol/l-1.0x10-13mol/l)的KD,在一個實施方案中,1.0x10-9mol/l或更小(在一個實施方案中,1.0x10-9mol/l-1.0x10-13mol/l)的KD的結合親和力特異性結合人CD40抗原的抗體。在另一個實施方案中,依照本發明的抗CD40抗體以4x10-10M或更小的KD結合人CD40。
在本發明的一個實施方案中,結合人CD40的抗體是激動劑(「CD40激動劑」)。「激動劑」與細胞上的受體結合併啟動與該受體的天然配體所啟動的相似或相同的反應或活性。「CD40激動劑」誘導任何或所有,但不限於下述應答:B細胞增殖和/或分化;經由諸如ICAM-1,E-選擇蛋白,VC-AM,等等分子的細胞間粘附的上調;促炎性細胞因子諸如IL-1,IL-6,IL-8,IL-12,TNF,等等的分泌;通過諸如TRAF(例如TRAF2和/或TRAF3),MAP激酶諸如NIK(NF-kB誘導性激酶),I-κB激酶(IKK/.β.),轉錄因子NF-kB,Ras和MEK/ERK途徑,PI3K AKT途徑,P38MAPK途徑,等等途徑的經由CD40受體的信號轉導;通過諸如XIAP,mcl-1,bcl-x,等等分子的抗凋亡信號的轉導;B和/或T細胞記憶產生;B細胞抗體生成;B細胞同種型轉換,MHC II類和CD80/86的細胞表面表達的上調,等等。
激動劑活性意圖是比由陰性對照誘導的激動劑活性大至少30%,35%,40%,45%,50%,60%,70%,75%,80%,85%,90%,95%,或100%的激動劑活性,如在B細胞應答的測定法測量的。
在另一個實施方案中,CD40激動劑具有比由陰性對照誘導的激動劑活性大至少2倍或大至少3倍的激動劑活性,如在B細胞應答的測定法測量的。
如此,例如,在感興趣的B細胞應答是B細胞增殖的情況中,激動劑活性會是誘導比由陰性對照誘導的B細胞增殖水平大至少2倍或大至少3倍的B細胞增殖水平。
如本文中使用的,「CD40激動劑」包括激動CD40/CD40L相互作用的任何模塊。典型地,這些模塊會是激動性CD40抗體或激動性CD40L多肽。舉例而言,這些抗體包括特異性激動CD40/CD40L結合相互作用的人抗體,嵌合抗體,人源化抗體,雙特異性抗體,scFv,和抗體片段。在一個實施方案中,激動性CD40抗體會包含嵌合的,完全人的或人源化的CD40抗體。在另一個優選實施方案中,激動性CD40抗體會包含嵌合的,完全人的或人源化的CD40抗體。
在一個實施方案中,所述CD40抗體是IgG2亞類的完全人抗體。在還有另一個實施方案中,所述抗體是WO2003/040170中具體披露的任何抗CD40抗體。在仍有另一個實施方案中,依照本發明的CD40激動劑選自下組:依照WO2003/040170的稱作3.1.1,7.1.2,10.8.3,15.1.1,21.4.1,21.2.1,22.1.1,23.5.1,23.25.1,23.29.1和24.2.1的抗體。分泌那些抗體的雜交瘤已經依照布達佩斯條約保藏。保藏號可見WO2003/040170的段落[0250]。在另一個實施方案中,依照本發明的CD40抗體包含抗體21.4.1(ATCC保藏號PTA-3605)的重鏈可變域胺基酸序列和輕鏈可變域胺基酸序列。在還有另一個實施方案中,依照本發明的CD40抗體由抗體21.4.1(ATCC保藏號PTA-3605)的重鏈胺基酸序列和輕鏈胺基酸序列組成。
在一個實施方案中,依照本發明的人抗CD40抗體包含胺基酸SEQ ID NO:3的輕鏈可變域和胺基酸SEQ ID NO:4的重鏈可變域(表3)。
表3:依照本發明的CD40激動劑的輕鏈可變域(VL)和重鏈可變域(VH)的胺基酸序列。
依照本發明,「PD-L1抗體」是結合或特異性結合人PD-L1的抗體。在一個實施方案中,人PD-L1具有依照SEQ ID NO:2的序列。如本文中使用的,「結合人PD-L1」或「特異性結合人PD-L1」或「結合人PD-L1的」或「抗PD-L1抗體」指以1.0x10-8mol/l或更低的KD值,在一個實施方案中,1.0x10-9mol/l或更低的KD值的結合親和力特異性結合人PD-L1抗原的抗體。結合親和力用標準結合測定法,諸如表面等離振子共振技術(GE-Healthcare Uppsala,Sweden)來測定。如此,如本文中使用的,「結合人PD-L1的抗體」指以1.0x10-8mol/l或更低(在一個實施方案中,1.0x10-8mol/l-1.0x10-13mol/l)的KD,在一個實施方案中,1.0x10-9mol/l或更多(在一個實施方案中,1.0x10-9mol/l-1.0x10-13mol/l)的KD的結合親和力特異性結合人PD-L1抗原的抗體。
在一個實施方案中,本文所述組合療法中使用的結合人PD-L1的抗體選自下組:243.55.S70,243.55.H1,243.55.H12,243.55.H37,243.55.H70,243.55.H89,243.55.S1,243.55.5,243.55.8,243.55.30,243.55.34,243.55.S37,243.55.49,243.55.51,243.55.62,和243.55.84。
這些抗體記載於WO 2010/77634(序列顯示於WO 2010/77634的圖11)且特徵在於包含下述重鏈可變域(VH)和輕鏈可變域(VL)序列(表4):
表4:選定PD-L1抗體的VH和VL的組合
表5:依照表4的SEQ ID NO的序列
因此,依照本發明,結合人PD-L1的抗體(即成分B的抗體)特徵在於
a)SEQ ID NO:5的重鏈可變域VH和SEQ ID NO:8的輕鏈可變域VL,或
b)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:9的輕鏈可變域VL,或
c)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:10的輕鏈可變域VL,或
d)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:11的輕鏈可變域VL,或
e)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:12的輕鏈可變域VL,或
f)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:13的輕鏈可變域VL,或
g)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:14的輕鏈可變域VL,或
h)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:15的輕鏈可變域VL,或
i)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:16的輕鏈可變域VL,或
j)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:17的輕鏈可變域VL,或
k)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:18的輕鏈可變域VL,或
l)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:19的輕鏈可變域VL,或
m)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:20的輕鏈可變域VL,或
n)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:21的輕鏈可變域VL,或
o)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:22的輕鏈可變域VL,或
p)SEQ ID NO:7的重鏈可變域VH和SEQ ID NO:23的輕鏈可變域VL。
因此,在一個實施方案中,本發明提供一種藥物產品,其包含A)第一成分,該第一成分包含作為活性組分的特異性結合且活化人CD40的抗體或其抗原結合部分;和B)第二成分,該第二成分包含作為活性組分的PD-L1抗體;其用於組合,順序或同時治療增殖性疾病,特別是癌症。
在這個實施方案內,A)中的抗體是以4x10-10M或更小的KD結合人CD40的IgG2亞類的完全人抗體;或包含SEQ ID NO:3的VL和SEQ ID NO:4的VH的抗體;或包含抗體21.4.1(ATCC保藏號PTA-3605)的重鏈可變域胺基酸序列和輕鏈可變域胺基酸序列的抗體;或包含抗體21.4.1(ATCC保藏號PTA-3605)的重鏈胺基酸序列和輕鏈胺基酸序列的抗體;且B)中的抗體是本文中之前a)至p)中提到的任何PD-L1抗體。
在還有另一個實施方案中,本發明提供一種藥物產品,其包含A)第一成分,該第一成分包含作為活性組分的以4x10-10M或更小的KD結合人CD40的IgG2亞類的完全人抗體;和B)第二成分,該第二成分包含作為活性組分的選自包含下述各項的抗體的PD-L1抗體:
a)SEQ ID NO:5的重鏈可變域VH和SEQ ID NO:8的輕鏈可變域VL,或
b)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:9的輕鏈可變域VL,或
c)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:10的輕鏈可變域VL,或
d)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:11的輕鏈可變域VL,或
e)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:12的輕鏈可變域VL,或
f)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:13的輕鏈可變域VL,或
g)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:14的輕鏈可變域VL,或
h)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:15的輕鏈可變域VL,或
i)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:16的輕鏈可變域VL,或
j)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:17的輕鏈可變域VL,或
k)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:18的輕鏈可變域VL,或
l)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:19的輕鏈可變域VL,或
m)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:20的輕鏈可變域VL,或
n)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:21的輕鏈可變域VL,或
o)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:22的輕鏈可變域VL,或
p)SEQ ID NO:7的重鏈可變域VH和SEQ ID NO:23的輕鏈可變域VL;
其用於組合,順序或同時治療增殖性疾病,特別是癌症。
在還有另一個實施方案中,本發明提供一種藥物產品,其包含A)第一成分,該第一成分包含作為活性組分的包含SEQ ID NO:3的VL和SEQ ID NO:4的VH的抗體;和B)第二成分,該第二成分包含作為活性組分的選自包含下述各項的抗體的PD-L1抗體:
a)SEQ ID NO:5的重鏈可變域VH和SEQ ID NO:8的輕鏈可變域VL,或
b)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:9的輕鏈可變域VL,或
c)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:10的輕鏈可變域VL,或
d)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:11的輕鏈可變域VL,或
e)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:12的輕鏈可變域VL,或
f)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:13的輕鏈可變域VL,或
g)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:14的輕鏈可變域VL,或
h)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:15的輕鏈可變域VL,或
i)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:16的輕鏈可變域VL,或
j)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:17的輕鏈可變域VL,或
k)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:18的輕鏈可變域VL,或
l)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:19的輕鏈可變域VL,或
m)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:20的輕鏈可變域VL,或
n)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:21的輕鏈可變域VL,或
o)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:22的輕鏈可變域VL,或
p)SEQ ID NO:7的重鏈可變域VH和SEQ ID NO:23的輕鏈可變域VL;
其用於組合,順序或同時治療增殖性疾病,特別是癌症。
在還有另一個實施方案中,本發明提供一種藥物產品,其包含A)第一成分,該第一成分包含作為活性組分的包含抗體21.4.1(ATCC保藏號PTA-3605)的重鏈可變域胺基酸序列和輕鏈可變域胺基酸序列的抗體;和B)第二成分,該第二成分包含作為活性組分的選自包含下述各項的抗體的PD-L1抗體:
a)SEQ ID NO:5的重鏈可變域VH和SEQ ID NO:8的輕鏈可變域VL,或
b)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:9的輕鏈可變域VL,或
c)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:10的輕鏈可變域VL,或
d)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:11的輕鏈可變域VL,或
e)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:12的輕鏈可變域VL,或
f)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:13的輕鏈可變域VL,或
g)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:14的輕鏈可變域VL,或
h)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:15的輕鏈可變域VL,或
i)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:16的輕鏈可變域VL,或
j)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:17的輕鏈可變域VL,或
k)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:18的輕鏈可變域VL,或
l)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:19的輕鏈可變域VL,或
m)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:20的輕鏈可變域VL,或
n)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:21的輕鏈可變域VL,或
o)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:22的輕鏈可變域VL,或
p)SEQ ID NO:7的重鏈可變域VH和SEQ ID NO:23的輕鏈可變域VL;
其用於組合,順序或同時治療增殖性疾病,特別是癌症。
在還有另一個實施方案中,本發明提供一種藥物產品,其包含A)第一成分,該第一成分包含作為活性組分的包含抗體21.4.1(ATCC保藏號PTA-3605)的重鏈胺基酸序列和輕鏈胺基酸序列的抗體;和B)第二成分,該第二成分包含作為活性組分的選自包含下述各項的抗體的PD-L1抗體:
a)SEQ ID NO:5的重鏈可變域VH和SEQ ID NO:8的輕鏈可變域VL,或
b)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:9的輕鏈可變域VL,或
c)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:10的輕鏈可變域VL,或
d)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:11的輕鏈可變域VL,或
e)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:12的輕鏈可變域VL,或
f)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:13的輕鏈可變域VL,或
g)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:14的輕鏈可變域VL,或
h)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:15的輕鏈可變域VL,或
i)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:16的輕鏈可變域VL,或
j)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:17的輕鏈可變域VL,或
k)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:18的輕鏈可變域VL,或
l)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:19的輕鏈可變域VL,或
m)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:20的輕鏈可變域VL,或
n)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:21的輕鏈可變域VL,或
o)SEQ ID NO:6的重鏈可變域VH和SEQ ID NO:22的輕鏈可變域VL,或
p)SEQ ID NO:7的重鏈可變域VH和SEQ ID NO:23的輕鏈可變域VL;
其用於組合,順序或同時治療增殖性疾病,特別是癌症。
在還有另一個實施方案中,本發明提供一種藥物產品,其包含A)第一成分,該第一成分包含作為活性組分的包含SEQ ID NO:3的VL和SEQ ID NO:4的VH的抗體;和B)第二成分,該第二成分包含作為活性組分的包含SEQ ID NO:8的VL和SEQ ID NO:5的VH的抗體;其用於組合,順序或同時治療增殖性疾病,特別是癌症。
在還有另一個實施方案中,本發明提供一種藥物產品,其包含A)第一成分,該第一成分包含作為活性組分的包含抗體21.4.1(ATCC保藏號PTA-3605)的重鏈可變域胺基酸序列和輕鏈可變域胺基酸序列的抗體;和B)第二成分,該第二成分包含作為活性組分的包含抗體243.55.S70的重鏈可變域胺基酸序列和輕鏈可變域胺基酸序列的抗體;其用於組合,順序或同時治療增殖性疾病,特別是癌症。
在還有另一個實施方案中,本發明提供一種藥物產品,其包含A)第一成分,該第一成分包含作為活性組分的包含抗體21.4.1(ATCC保藏號PTA-3605)的重鏈胺基酸序列和輕鏈胺基酸序列的抗體;和B)第二成分,該第二成分包含作為活性組分的包含抗體243.55.S70的重鏈胺基酸序列和輕鏈胺基酸序列的抗體;其用於組合,順序或同時治療增殖性疾病,特別是癌症。
在一個實施方案中,成分A)和B)是分開施用的,優選時間相差1,或2,或3,或4,或5,或6,或7天。在另一個實施方案中,成分A)和B)的施用之間的差異可以是介於1天和21天之間,優選介於1天和14天,或1天和10天,或1天和7天之間的任何時間。
在另一個實施方案中,本發明提供特異性結合且活化人CD40的抗體,或其抗原結合部分;和PD-L1抗體用於製造藥物的用途,該藥物用於組合,順序或同時治療增殖性疾病,諸如癌症,優選實體瘤。
本發明進一步包括一種用於治療需要療法的患者的方法,其特徵在於對該患者施用治療有效量的依照本發明的抗體。本發明包括依照本發明的抗體用於所描述的療法的用途。
如此,本發明的一個實施方案是本文所述CD40抗體或其抗原結合部分,其用於與本文所述抗PD-L1抗體組合治療癌症。如本文中使用的,術語「癌症」可以是例如肺癌,非小細胞肺(NSCL)癌,支氣管肺泡細胞肺癌,骨癌,胰腺癌,皮膚癌,頭或頸癌,皮膚或眼內黑素瘤,子宮癌,卵巢癌,直腸癌,肛門區癌,胃癌,胃的癌,結腸癌,乳腺癌,子宮癌,輸卵管,子宮內膜癌,宮頸癌,陰道癌,外陰癌,何杰金氏病,食管癌,小腸癌,內分泌系統癌,甲狀腺癌,甲狀旁腺癌,腎上腺癌,軟組織肉瘤,尿道癌,陰莖癌,前列腺癌,膀胱癌,腎或輸尿管癌,腎細胞癌,腎盂癌,間皮瘤,肝細胞癌,膽管癌,中樞神經系統(CNS)贅生物,脊髓軸腫瘤,腦幹膠質瘤,多形性成膠質細胞瘤,星形細胞瘤,許旺細胞瘤,室管膜瘤,成神經管細胞瘤,腦膜瘤,鱗狀細胞癌,垂體腺瘤,淋巴瘤,淋巴細胞性白血病,包括任何上述癌症的難治性形式,或一種或多種上述癌症的組合。在一個優選實施方案中,此類癌症是乳腺癌,結直腸癌,黑素瘤,頭和頸癌,肺癌或前列腺癌。在一個實施方案中,此類癌症是選自乳腺癌,肺癌,結腸癌,卵巢癌,黑素瘤癌症,膀胱癌,腎的癌,腎癌,肝癌,頭和頸癌,結直腸癌,胰腺癌,胃的癌瘤癌,食管癌,間皮瘤或前列腺癌的實體瘤。在另一個實施方案中,此類癌症是血液學腫瘤,諸如例如白血病(諸如AML,CLL),淋巴瘤,骨髓瘤。在仍有另一個實施方案中,該癌症是乳腺癌,肺癌,結腸癌,結直腸癌,胰腺癌,胃的癌或前列腺癌。
在一個實施方案中,當前組合療法用於預防或治療轉移。
在一個實施方案中,當前組合療法用於治療免疫相關疾病諸如腫瘤免疫或延遲免疫相關疾病諸如腫瘤免疫的進展。
在一個實施方案中,當前組合療法用於刺激免疫應答或功能,諸如T細胞活性。
術語「表位」表示人CD40或PD-L1中能夠特異性結合抗體的蛋白質決定簇。表位通常由諸如胺基酸或糖側鏈等分子的化學活性表面編組組成,而且表位通常具有特定三維結構特徵,以及特定電荷特徵。構象和非構象表位的區別在於在變性溶劑存在下喪失對前者而非後者的結合。
如本文中使用的,「可變域」(輕鏈可變域VL,重鏈可變域VH)表示直接牽涉抗體結合抗原的輕和重鏈域對中的每一個。可變輕和重鏈域具有相同的整體結構且每個域包含四個框架(FR)區,其序列廣泛保守,通過三個「高變區」(或互補決定區,CDR)連接。框架區採取β-片層構象,而CDR可形成連接β-片層結構的環。每條鏈中的CDR通過框架區保持它們的三維結構且與來自另一條鏈的CDR一起形成抗原結合位點。抗體的重和輕鏈CDR3區在依照本發明的抗體的結合特異性/親和力中發揮特別重要的作用且因此提供本發明的又一個目標。
在本文中使用時,術語「抗體的抗原結合部分」指抗體中負責抗原結合的胺基酸殘基。抗體的抗原結合部分包含來自「互補決定區」或「CDR」的胺基酸殘基。「框架」或「FR」區是可變域中除如本文中定義的高變區殘基以外那些區域。因此,抗體的輕和重鏈可變域自N端至C端包含域FR1,CDR1,FR2,CDR2,FR3,CDR3,和FR4。尤其,重鏈的CDR3是對抗原結合貢獻最大的區域且限定抗體的特性。CDR和FR區依照Kabat et al.,Sequences of Proteins of Immunological Interest,5th ed.,Public Health Service,National Institutes of Health,Bethesda,MD(1991)的標準定義來確定和/或是那些來自「高變環」的殘基。
在本發明的一個實施方案中,特異性結合且活化人CD40的抗體的「抗原結合部分」包含抗體21.4.1(ATCC保藏號PTA-3605)的重鏈可變域和輕鏈可變域的CDR1,CDR2和CDR3。
如本文中使用的,術語「核酸」或「核酸分子」意圖包括DNA分子和RNA分子。核酸分子可以是單鏈的或雙鏈的,但是優選是雙鏈DNA。
如本申請內使用的,術語「胺基酸」表示天然發生羧基α-胺基酸的組,包括丙氨酸(三字母代碼:ala,單字母代碼:A),精氨酸(arg,R),天冬醯胺(asn,N),天冬氨酸(asp,D),半胱氨酸(cys,C),穀氨醯胺(gln,Q),穀氨酸(glu,E),甘氨酸(gly,G),組氨酸(his,H),異亮氨酸(ile,I),亮氨酸(leu,L),賴氨酸(lys,K),甲硫氨酸(met,M),苯丙氨酸(phe,F),脯氨酸(pro,P),絲氨酸(ser,S),蘇氨酸(thr,T),色氨酸(trp,W),酪氨酸(tyr,Y),和纈氨酸(val,V)。
抗體的「Fc部分」沒有直接牽涉抗體結合抗原,但是展現各種效應器功能。「抗體的Fc部分」是熟練技術人員熟知的術語且基於抗體的木瓜蛋白酶切割來定義。根據它們的重鏈的恆定區的胺基酸序列,抗體或免疫球蛋白分成類:IgA,IgD,IgE,IgG和IgM,而且這些中的數種可進一步細分成亞類(同種型),例如IgG1,IgG2,IgG3,和IgG4,IgA1,和IgA2。依照重鏈恆定區,不同類的免疫球蛋白分別稱作α,δ,ε,γ,和μ。抗體的Fc部分直接牽涉ADCC(抗體依賴性細胞介導的細胞毒性)和CDC(補體依賴性細胞毒性),其基於補體活化,C1q結合和Fc受體結合。補體活化(CDC)通過補體因子C1q結合至大多數IgG抗體亞類的Fc部分來啟動。雖然抗體對補體系統的影響取決於某些條件,但是結合至C1q是由Fc部分中限定的結合位點引起的。此類結合位點是現有技術已知的且記載於例如Boackle,R.J.,et al.,Nature 282(1979)742-743;Lukas,T.J.,et al.,J.Immunol.127(1981)2555-2560;Brunhouse,R.,and Cebra,J.J.,Mol.Immunol.16(1979)907-917;Burton,D.R.,et al.,Nature 288(1980)338-344;Thommesen,J.E.,et al.,Mol.Immunol.37(2000)995-1004;Idusogie,E.E.,et al.,J.Immunol.164(2000)4178-4184;Hezareh,M.,et al.,J.Virology 75(2001)12161-12168;Morgan,A.,et al.,Immunology 86(1995)319-324;EP 0 307 434。此類結合位點是例如L234,L235,D270,N297,E318,K320,K322,P331和P329(編號方式依照Kabat,E.A.的EU索引,見下文)。亞類IgG1,IgG2和IgG3的抗體通常顯示補體活化和C1q和C3結合,而IgG4不活化補體系統且不結合C1q和C3。
在一個實施方案中,依照本發明的抗體可包含自人起源衍生的Fc部分和優選人恆定區的所有其它部分。如本文中使用的,術語「自人起源衍生的Fc部分」表示如下的Fc部分,它是亞類IgG1,或IgG2,或IgG3或IgG4的人抗體的Fc部分,優選來自人IgG1或IgG2亞類的Fc部分,來自人IgG1或IgG2亞類的突變Fc部分(在一個實施方案中,具有L234A+L235A上的突變),來自人IgG4亞類的Fc部分或來自人IgG4亞類的突變Fc部分,在一個更加具體的實施方案中,具有S228P上的突變。在另一個實施方案中,所述抗體可具有降低的或最小限度的效應器功能。在一個實施方案中,最小限度的效應器功能可源自無效應器性(effectorless)Fc突變。在一個實施方案中,無效應器性Fc突變是L234A/L235A或L234A/L235A/P329G或N297A或D265A/N297A。在一個實施方案中,對於彼此獨立的每種抗體,無效應器性Fc突變可選自包含L234A/L235A,L234A/L235A/P329G,N297A和D265A/N297A的組。
在一個實施方案中,依照本發明的抗體是單克隆抗體。在另一個實施方案中,依照本發明的抗體是人IgG類的(即IgG1,或IgG2,或IgG3或IgG4亞類的)。在還有另一個實施方案中,一種抗體優選是IgG2亞類的且另一種是IgG1或IgG4亞類的。
在一個實施方案中,本文所述抗體特徵在於人起源的恆定鏈。此類恆定鏈是現有技術公知的且記載於例如Kabat,E.A.(參見例如Johnson,G.and Wu,T.T.,Nucleic Acids Res.28(2000)214-218)。
本文所述抗體優選是通過重組手段生成的。此類方法是現有技術廣泛知道的且包括在原核和真核細胞中表達蛋白質及隨後分離抗體多肽並通常純化至藥學可接受的純度。對於蛋白質表達,通過標準方法將編碼輕和重鏈或其片段的核酸插入表達載體。在適宜的原核或真核宿主細胞(諸如CHO細胞,NS0細胞,SP2/0細胞,HEK293細胞,COS細胞,酵母,或大腸桿菌細胞)中實施表達,並自細胞(自上清液或在細胞裂解後)回收抗體。
抗體的重組生成是現有技術公知的且記載於例如綜述性文章Makrides,S.C.,Protein Expr.Purif.17(1999)183-202;Geisse,S.,et al.,Protein Expr.Purif.8(1996)271-282;Kaufman,R.J.,Mol.Biotechnol.16(2000)151-161;Werner,R.G.,Drug Res.48(1998)870-880。
抗體可以存在於完整細胞中,細胞裂解物中,或經部分純化的,或實質性純的形式。實施純化是為了清除其它細胞成分或其它汙染物,例如其它細胞核酸或蛋白質,其通過標準技術進行,包括鹼/SDS處理,CsCl成帶,柱層析,瓊脂糖凝膠電泳,和本領域公知的其它技術。參見Ausubel,F.,et al.,ed.Current Protocols in Molecular Biology,Greene Publishing and Wiley Interscience,New York(1987)。
NS0細胞中的表達記載於例如Barnes,L.M.,et al.,Cytotechnology 32(2000)109-123;Barnes,L.M.,et al.,Biotech.Bioeng.73(2001)261-270。瞬時表達記載於例如Durocher,Y.,et al.,Nucl.Acids.Res.30(2002)E9。可變域的克隆記載於Orlandi,R.,et al.,Proc.Natl.Acad.Sci.USA 86(1989)3833-3837;Carter,P.,et al.,Proc.Natl.Acad.Sci.USA 89(1992)4285-4289;Norderhaug,L.,et al.,J.Immunol.Methods 204(1997)77-87。一種優選的瞬時表達系統(HEK 293)記載於Schlaeger,E.-J.and Christensen,K.,in Cytotechnology 30(1999)71-83及Schlaeger,E.-J.,in J.Immunol.Methods 194(1996)191-199
將依照本發明的重和輕鏈可變域與啟動子,翻譯起始,恆定區,3'非翻譯區,聚腺苷酸化,和轉錄終止的序列組合以形成表達載體構建物。可以將重和輕鍊表達構建物組合成單一載體,共轉染,連續轉染,或分開轉染入宿主細胞,然後融合宿主細胞以形成表達這兩條鏈的單一宿主細胞。
例如,對於原核生物合適的控制序列包括啟動子,任選的操縱基因序列,和核糖體結合位點。已知真核細胞利用啟動子,增強子和聚腺苷酸化信號。
當核酸放置成與另一核酸序列處於功能性關係時,它是「可操作連接的」。例如,如果前序列(presequence)或分泌前導的DNA表達成參與多肽的分泌的前蛋白(preprotein),那麼它與多肽的DNA可操作連接;如果啟動子或增強子影響編碼序列的轉錄,那麼它與該序列可操作連接;或者如果核糖體結合位點的定位推動翻譯,那麼它與編碼序列可操作連接。通常,「可操作連接」意味著所連接的DNA序列是毗鄰的,而且在分泌前導的情況中是毗鄰且同框的。然而,增強子不必是毗鄰的。連接通過方便的限制性位點處的連接來實現。如果不存在此類位點,那麼依照常規實踐使用合成寡核苷酸銜接頭或接頭。
通過常規免疫球蛋白純化規程將單克隆抗體與培養液恰當分開,諸如例如蛋白A-Sepharose,羥磷灰石層析,凝膠電泳,透析,或親和層析。編碼單克隆抗體的DNA和RNA易於使用常規規程來分離和測序。雜交瘤細胞可充當此類DNA和RNA的來源。一旦分離,就可以將DNA插入表達載體,然後將表達載體轉染入其它情況下不生成免疫球蛋白蛋白質的宿主細胞(諸如HEK293細胞,CHO細胞,或骨髓瘤細胞),以在宿主細胞中獲得重組單克隆抗體的合成。
如本文中使用的,表述「細胞」,「細胞系」,和「細胞培養物」可互換使用,而且所有此類名稱包括後代。如此,詞語「轉化子」和「經轉化細胞」包括原代主題細胞及自其衍生的培養物,不管傳代的次數。還要理解的是,由於有意或無意的突變,所有後代在DNA內容方面可以不是精確相同的。包括具有與初始轉化細胞中所篩選的相同的功能或生物學活性的變體後代。
用於生成依照本發明使用的特定抗體的方法還披露於WO2003/040170(關於抗CD40抗體)和WO2010/77634(關於PD-L1抗體)。
在另一個方面,本發明提供含有一種或一組本發明的單克隆抗體或其抗原結合部分,與藥學可接受載劑一起配製的組合物,例如藥物組合物。
如本文中使用的,「藥學可接受載劑」包括任何和所有生理學相容的溶劑,分散介質,塗層,抗細菌和抗真菌劑,等張和吸收/再吸收延遲劑,等等。優選的是,載劑適合於注射或輸注。
本發明的組合物可以通過多種本領域已知方法來施用。正如技術人員會領會的,施用路徑和/或模式會根據期望結果而變化。
藥學可接受載劑包括無菌含水溶液或分散體和用於製備無菌可注射溶液或分散體的無菌粉末。此類介質和藥劑對於藥學活性物質的用途是本領域已知的。在水以外,載劑還可以是例如等張緩衝鹽水溶液。
不管所選擇的施用路徑,通過本領域技術人員知道的常規方法將可以以合適水合形式使用的本發明的化合物和/或本發明的藥物組合物配製成藥學可接受劑量形式。
依照本發明使用的特定抗體的藥物組合物可以是技術人員知道的標準製劑,而且披露於例如WO2003/040170(關於抗CD40抗體)和WO2010/77634(關於PD-L1抗體)。
本發明的藥物組合物中活性組分的實際劑量水平可以變化,從而獲得活性組分對特定患者,組合物,和施用模式有效實現期望治療性響應,對患者無毒的量(有效量)。所選擇的劑量水平會取決於多種藥動學因素,包括所採用的本發明特定組合物或其酯,鹽或醯胺的活性,施用路徑,施用時間,所採用的特定化合物的排洩速率,與所採用的特定組合物組合使用的其它藥物,化合物和/或材料,所治療的患者的年齡,性別,重量,狀況,整體健康和在先醫學史,及醫學領域公知的類似因素。
術語「方法治療」或其等同語在應用於例如癌症時指設計成減少或消除患者中癌細胞的數目,或減輕癌症的症狀的規程或作用過程。癌症或其它增殖性病症的「治療方法」並非必然意味著癌細胞或其它病症事實上會消除,細胞或病症的數目事實上會減少,或癌症或其它病症的症狀事實上會減輕。通常,即使成功的可能性較低,但是鑑於患者的醫學史和估算存活預期,仍然認為誘導總體有益作用過程,也會實施治療癌症的方法。
術語「組合施用」或「共施用」,「組合療法」或「組合治療」指例如作為分開的配製劑/應用(或作為單一配製劑/應用)施用本文所述抗CD40抗體和抗PD-L1抗體。共施用可以是同時的或者是任意次序順序的,其中優選有一段時間所有活性劑同時發揮它們的生物學活性。在一個實施方案中,本文中使用的成分A和B任一可以使用靜脈內路徑(i.v.),例如經由連續輸注,或皮下路徑(s.c.)通過它自己的,分開的藥物製劑來施用。在一個實施方案中,成分A和B通過靜脈內路徑/製劑分開共施用。在另一個實施方案中,成分A和B通過皮下路徑/製劑分開共施用。在仍有另一個實施方案中,成分A和B分開共施用,一個通過皮下路徑/製劑,另一個通過靜脈內路徑/製劑。
不言自明的是,以「治療有效量」(或簡單的說,「有效量」)將抗體施用於患者,該量的相應化合物或組合會引發研究人員,獸醫,醫生或其他臨床醫師尋求的組織,系統,動物或人的生物學或醫學應答。
共施用的每種成分的劑量和共施用的時機會取決於所治療的患者的類型(物種,性別,年齡,重量,等)和狀況及所治療的疾病或疾患的嚴重程度。特別地,基於免疫系統活化的治療一般可能攜帶壓倒性免疫應答(有時稱作細胞因子釋放症候群(CRS))或抗藥物抗體(ADA)應答的風險。找到牽涉CD40激動劑的治療性臨床相關治療方案(即可耐受的且有效的劑和劑量進度表)構成一項當前未滿足的醫學需求。
如此,在一個實施方案中,順序共施用成分(A和B),其中或是在同一天在兩次分開的施用(i.v.或s.c.)中施用每種單一成分的劑量,或是在第1天施用一種並在第2天和第42天之間,或第2天和第21天之間,或第2天和第14天之間,或第2天和第7天之間的任何一天共施用第二種成分。在另一個實施方案中,在施用第一種成分之後在第2,或7,或14,或21天共施用第二種成分。在另一個實施方案中,在施用第一種成分之後在第2天或第21天共施用第二種成分。
在另一個實施方案中,第一個施用的成分是成分A,即如本文中限定的抗CD40抗體。在這個實施方案內,以介於4mg和16mg之間,優選4mg,或8mg,或16mg的固定劑量施用成分A。
在另一個實施方案中,在第1天以16mg的劑量施用成分A一次,接著是第42天的成分B的給藥以及每3周,或每14或7天的成分B的進一步維持給藥。
在另一個實施方案中,在第1天以16mg的劑量施用成分A一次,接著是第21天的成分B的第一次給藥以及每3周,或每14或7天的成分B的進一步維持給藥。
在另一個實施方案中,在第1天以4mg的劑量施用成分A一次,接著是第21天的成分B的第一次給藥以及每3周,或每14或7天的成分B的進一步維持給藥。
在另一個實施方案中,在第1天以4mg的劑量施用成分A一次,接著是第14天的成分B的第一次給藥以及每3周,或每14或7天的成分B的進一步維持給藥。
在另一個實施方案中,在第1天以4mg的劑量施用成分A一次,接著是第7天的成分B的第一次給藥以及每3周,或每14或7天的成分B的進一步維持給藥。
在另一個實施方案中,在第1天以16mg的劑量施用成分A一次,接著是第14天的成分B的第一次給藥以及每3周,或每14或7天的成分B的進一步維持給藥。
在另一個實施方案中,在第1天以16mg的劑量施用成分A一次,接著是第7天的成分B的第一次給藥以及每3周,或每14或7天的成分B的進一步維持給藥。
在另一個實施方案中,在第1天施用成分B,接著是第2天成分A以介於4mg和16mg之間的固定劑量的單次施用;再接著是每3周,或每14或7天的成分B的維持給藥。在這個實施方案內,成分A的固定劑量優選選自4mg,8mg,14mg,15mg或16mg。
在還有另一個實施方案中,在治療的第1天施用成分B,接著是每3周(21天)的進一步施用,並且在治療的第2天施用成分A,接著是3次另外的施用,每次間隔在6周(42天)內。在這個實施方案內,以介於4mg和16mg之間,優選4mg,8mg,14mg,15mg或16mg的固定劑量施用成分A。
在還有另一個實施方案中,在治療的第1天施用成分B,接著是每3周(21天)的進一步施用,並且在治療的第2天施用成分A,接著是3次另外的施用,每次間隔在3周(21天)內。在這個實施方案內,以介於4mg和16mg之間,優選4mg,8mg,14mg,15mg或16mg的固定劑量施用成分A。
在涉及施用/劑量方案的所有上述實施方案內,以1200mg的固定劑量施用成分B(即抗PD-L1抗體)。繼續成分B的治療或「維持給藥」直至疾病進展。
在還有另一個實施方案中,本發明提供牽涉抗CD40抗體和抗PD-L1抗體的組合療法的任何劑量進度表,如圖4中所示。
如此,在一個實施方案中,本發明提供一種藥物產品,其包含如本文中限定的成分A和B,其中成分A)和B)是分開施用的。
在另一個實施方案中,本發明提供所述藥物產品,其中成分A和/或B是靜脈內(i.v.)或皮下(s.c.)施用的。
在還有另一個實施方案中,本發明提供所述藥物產品,其中成分A是以介於4和16mg之間的固定劑量施用的,且成分B是以1200mg的固定劑量施用的。
在仍有另一個實施方案中,本發明提供所述藥物產品,其中成分A和B的施用隔開1至42天,優選1,或7,或14或21或42天。
在仍有另一個實施方案中,本發明提供所述藥物產品,其中成分A與成分B一起施用1至4次,隨後只用成分B繼續治療直至疾病進展。
在另一個更加具體的實施方案中,本發明提供任何上述劑量方案,其中成分A是如下的成分,其包含作為活性組分的包含SEQ ID NO:3的VL和SEQ ID NO:4的VH的抗體;且成分B是如下的成分,其包含作為活性組分的包含SEQ ID NO:8的VL和SEQ ID NO:5的VH的抗體。
在另一個實施方案中,本發明提供特異性結合且活化人CD40的抗體或其抗原結合部分;和PD-L1抗體用於製造藥物的用途,該藥物用於組合,順序或同時治療增殖性疾病,諸如癌症,優選實體瘤。
在與抗PD-L1抗體組合的抗CD40抗體以外,還可以涵蓋別的治療選項,諸如化療劑或放療。
在一個實施方案中,此類可以與本文所述抗CD40抗體和本文所述抗PD-L1抗體一起施用的別的化療劑包括但不限於抗腫瘤劑,包括烷化劑,包括:氮芥,諸如二氯甲基二乙胺(mechlorethamine)、環磷醯胺(cyclophosphamide)、異環磷醯胺(ifosfamide)、美法侖(melphalan)和苯丁酸氮芥(chlorambucil);亞硝基脲(nitrosourea),諸如卡莫司汀(carmustine)(BCNU)、洛莫司汀(lomustine)(CCNU)、和司莫司汀(semustine)(甲基-CCNU);TemodalTM(替莫唑胺(temozolamide))、乙撐亞胺/甲基蜜胺諸如三乙撐蜜胺(TEM)、三乙烯硫代磷醯胺(塞替派(thiotepa))、六甲基蜜胺(HMM,六甲蜜胺(altretamine));烴基磺酸酯,諸如白消安(busulfan);三嗪,諸如達卡巴嗪(dacarbazine)(DTIC);抗代謝物,包括葉酸類似物,諸如甲氨喋呤(methotrexate)和三甲曲沙(trimetrexate),嘧啶類似物,諸如5-氟尿嘧啶(5FU)、氟脫氧尿苷、吉西他濱(gemcitabine)、胞嘧啶阿拉伯糖苷(AraC,阿糖胞苷(cytarabine))、5-氮胞苷、2,2'-二氟脫氧胞苷,嘌呤類似物,諸如6-巰基嘌呤、6-硫鳥嘌呤、硫唑嘌呤(azathioprine)、T-脫氧柯福黴素(噴司他丁(pentostatin))、赤式羥基壬基腺嘌呤(erythrohydroxynonyladenine,EHNA)、磷酸氟達拉濱(fludarabine phosphate)、和2-氯脫氧腺苷(克拉屈濱(cladribine),2-CdA);天然產物,包括抗有絲分裂藥物,諸如帕利他賽(paclitaxel)、長春花生物鹼(包括長春鹼(vinblastine)(VLB)、長春新鹼(vincristine)、和長春瑞濱(vinorelbine))、泰索帝(taxotere)、雌莫司汀(estramustine)、和磷酸雌莫司汀;表鬼臼毒素(pipodophylotoxin),諸如依託泊苷(etoposide)和替尼泊苷(teniposide);抗生素,諸如放線菌素D(actinomycin D)、道諾黴素(daunomycin)(柔紅黴素(rubidomycin))、多柔比星(doxorubicin)、米託蒽醌(mitoxantrone)、伊達比星(idarubicin)、博來黴素(bleomycin)、普卡黴素(plicamycin)(光輝黴素(mithramycin))、絲裂黴素C(mitomycin C)、和放線菌素(actinomycin);酶,諸如L-天冬醯胺酶;生物學應答改性劑,諸如幹擾素-α、IL-2、G-CSF和GM-CSF;包括鉑配位複合物的混雜劑,諸如奧沙利鉑(oxaliplatin)、順鉑(cisplatin)和卡鉑(carboplatin),蒽二酮,諸如米託蒽醌(mitoxantrone),取代的脲,諸如羥基脲、甲基肼衍生物,包括N-甲基肼(MIH)和丙卡巴肼(procarbazine)、腎上腺皮質阻抑劑,諸如米託坦(mitotane)(o、p-DDD)和氨魯米特(aminoglutethimide);激素和拮抗劑,包括腎上腺皮質類固醇拮抗劑,諸如強的松(prednisone)及等效物、地塞米松(dexamethasone)和氨魯米特(aminoglutethimide);GemzarTM(吉西他濱(gemcitabine))、妊娠素,諸如己酸羥基孕酮(hydroxyprogesterone caproate)、乙酸甲羥孕酮(medroxyprogesterone acetate)和乙酸甲地孕酮(megestrol acetate);雌激素,諸如己烯雌酚(diethylstilbestrol)和乙炔雌二醇等效物;抗雌激素,諸如他莫昔芬(tamoxifen);雄激素,包括丙酸睪酮(testosterone propionate)和氟甲睪酮(fluoxymesterone)/等效物;抗雄激素,諸如氟他胺(flutamide)、促性腺激素釋放激素類似物和亮丙瑞林(leuprolide);和非類固醇抗雄激素,諸如氟他胺(flutamide)。靶向後成機制的療法包括但不限於組蛋白脫乙醯基酶抑制劑,脫甲基化劑(例如Vidaza)和釋放轉錄阻抑(ATRA)療法也可以與抗原結合蛋白組合。在一個實施方案中,化療劑選自下組:紫杉烷(像例如帕利他賽(泰素(Taxol))、多西他賽(泰索帝(Taxotere))、經修飾的帕利他賽(例如Abraxane和Opaxio)、多柔比星、舒尼替尼(Sutent)、索拉非尼(Nexavar)、和其它多激酶抑制劑、奧沙利鉑、順鉑和卡鉑、依託泊苷、吉西他濱、和長春鹼。在一個實施方案中,化療劑選自下組:紫杉烷(像例如帕利他賽(Taxol)、多西他賽(Taxotere)、經修飾的帕利他賽(例如Abraxane和Opaxio)。在一個實施方案中,別的化療劑選自5-氟尿嘧啶(5-FU)、亞葉酸、伊立替康、或奧沙利鉑。在一個實施方案中,化療劑為5-氟尿嘧啶、亞葉酸和伊立替康(FOLFIRI)。在一個實施方案中,化療劑為5-氟尿嘧啶和奧沙利鉑(FOLFOX)。
與別的化療劑的組合療法的具體例子包括例如有紫杉烷(例如多西他賽或帕利他賽)或經過修飾的帕利他賽(例如Abraxane或Opaxio),多柔比星,卡培他濱和/或貝伐珠單抗(Avastin)的療法,用於治療乳腺癌;有卡鉑,奧沙利鉑,順鉑,帕利他賽,多柔比星(或經過修飾的多柔比星(Caelyx或Doxil)),或託泊替康(Hycamtin)的療法,用於卵巢癌;有多激酶抑制劑,MKI(Sutent,Nexavar,或706)和/或多柔比星的療法,用於治療腎癌;有奧沙利鉑,順鉑和/或放射的療法,用於治療鱗狀細胞癌;有泰素和/或卡鉑的療法,用於治療肺癌。
本發明進一步提供一種用於製造藥物的方法,該藥物包含與藥學可接受載劑一起的有效量的依照本發明的抗CD40抗體和/或PD-L1抗體。
本發明進一步提供一種試劑盒,該試劑盒包含一種藥物產品,其包含A)特異性結合且活化人CD40的抗體或其抗原結合部分;和B)PD-L1抗體,以及告知技術人員(例如內科醫師,腫瘤學家或其他醫學從業人員)如何使用所述藥物產品作為用於組合,順序或同時治療增殖性疾病(諸如癌症,優選實體瘤)的藥物的說明書。
在仍有另一個實施方案中,依照本發明的藥物產品,即包含本文中公開的成分A和B的產品,可以與第三成分(C)一起施用,其中所述第三成分是抗細胞因子(細胞因子抑制劑),諸如例如抗IL6(a-IL6)和/或抗TNFα(a-TNFα,抗TNFα)。已經發現添加所述細胞因子抑制劑提高可耐受性同時維持上文公開的成分A和B治療的功效(見實施例2)。
因此,在另一個實施方案中,提供一種藥物產品,其包含A)第一成分,該第一成分包含作為活性組分的特異性結合且活化人CD40的抗體或其抗原結合部分;和B)第二成分,該第二成分包含作為活性組分的PD-L1抗體;和C)第三成分,該第三成分包含作為活性組分的細胞因子抑制劑;其用於組合,順序或同時治療增殖性疾病,特別是癌症。
在這個實施方案內,所述細胞因子抑制劑是抑制TNFα的分子。多種TNFα抑制劑,小分子和抗體批准用於人中的療法。關於它們的可應用藥物製劑,施用路徑和劑量的信息因而是本領域技術人員公知的。在一個依照本發明的特定實施方案中,TNFα抑制劑是抗體,優選稱作TN3-19.12的抗體的人類似物。可以依照本發明使用的其它TNFα抑制劑包括(英夫利昔單抗(infliximab)),(依那西普(etanercept)),(阿達木單抗(adalimumab)),(塞妥珠單抗(certolizumab pegol))和(戈利木單抗(golimumab))。還有,在這個實施方案內,成分C可以與成分A和B同時或分開施用。本文中關於成分A和B的施用公開的任何劑量方案也適用於該三重組合。成分C優選與成分A和/或B同時施用,或是在相同的藥物製劑中或是在不同的藥物中。本文中關於成分A和B公開的任何劑量方案與成分C一起形成依照本發明的另一個實施方案。在這個實施方案內,在施用成分A或B時還總是施用成分C。
在另一個實施方案中,成分C的施用在成分A和B的施用之前開始。優選地,成分C的施用在治療的第1天開始,並自第2天起依照本文中之前關於成分A和B限定的劑量方案給予成分A和B。
在另一個實施方案中,優選在治療的第1,2,3和4天施用成分C;在第2天施用成分A;並在第2天施用成分B,接著是單獨的或與成分C組合的成分B的每周施用。
在還有另一個實施方案中,優選在治療的第1,2,3和4天施用成分C;在第2天施用成分A;並在第9天施用成分B,接著是單獨的或與成分C組合的成分B的每周施用。
在還有另一個實施方案中,優選在治療的第1,2,3和4天施用成分C;在第2天施用成分A;並在第16天施用成分B,接著是單獨的或與成分C組合的成分B的每周施用。
提供以下實施例以幫助理解本發明,其真正的範圍在所附權利要求書中列出。應當理解,可以在不背離本發明精神的前提下對列出的規程做出修改。
實施例
實施例1
此實施例證明抗鼠CD40與抗PDL-1組合在同位Panc02-Fluc胰腺同基因癌症模型中的治療功效。在這項研究中,會經由一周兩次生物發光成像來評估腫瘤生長。
實驗進度表:
研究組
當達到終止標準時會處死每個組的動物。會使用來自媒介組的2隻scouts動物來評估療法啟動時的腫瘤負荷。
材料和方法
細胞培養和應用
Panc-02-Fluce細胞克隆(人胰腺癌細胞)最初是自ATCC(美國典型培養物保藏中心)獲得的並在擴充後保藏於Roche-Glycart內部細胞庫。在含有10%FCS(Sigma)和1%Glutamax+500ug/ml潮黴素的RPMI培養基中培養Panc-02-Fluc細胞。在5%CO2的水飽和氣氛中於37℃培養細胞。在麻醉的C57BL/6小鼠的腹部左側做一小切口。打開腹膜壁並用鑷子小心分離胰。將10微升(0.2x106個細胞,在RPMI培養基中)細胞懸浮液注射入胰尾。使用5/0可吸收縫合線閉合腹膜壁和皮膚傷口。
動物
依照提交的指導方針(GV-Solas;Felasa;TierschG)在無特定病原體的條件下以12小時明亮/12小時黑暗的日周期維持60隻黑色6雌性小鼠;實驗開始時8-9周齡(購自Charles Rivers,Germany)。實驗性研究方案得到地方政府審查和批准(P 2011-128)。到達後,將動物維持1周以適應新環境和進行觀察。定期進行連續健康監測。
處理
在研究第0天對小鼠胰內注射RPMI中的2x105個Panc02-Fluc細胞(傳代18,存活力95.9%)。在第7天對小鼠i.v.注射媒介(15隻動物),10mg/kg a-CD40(15隻動物),10mg/kg a-PD-L1,10mg/kg a-CD40+10mg/kg a-PD-L1。進度表為a-PD-L1和媒介一周一次達3周。a-CD40抗體只在第7天施用一次。
測試化合物(抗體)
化合物的規格
抗體保存於4℃。
對所有小鼠i.v.注射200μL適宜溶液。對媒介組的小鼠注射組氨酸緩衝液並對治療組注射抗體。為了獲得適當量的抗體,在必要時用組氨酸緩衝液稀釋抗體溶液。對小鼠進行處理的最大數目是3次。
抗體製備:
10mg/kg等於200μg/小鼠:
下面計算每隻小鼠需要的構建物的體積:
調查
監測
每天對動物管理臨床症狀和不利影響檢測。動物的終止標準為臨床病態,運動受損,毛皮不潔。
用於腫瘤標誌物分析的血清提取
在注射腫瘤細胞之前3天,第一次抗體處理之後24小時和處死當天收集來自所有經處理動物的血清樣品。樣品保存於-20℃。
屍檢
依照終止標準處死小鼠。自所有動物收集脾和肝腫瘤用於隨後的組織病理學分析(PFA,冷凍)。
樣品加工
切出胰腫瘤,立即在福馬林溶液中固定,隨後為石蠟包埋(Leica自動組織加工儀TP1020,Germany)和微分4μm切片(Leica RM2235旋轉切片機,Germany)加工。使用標準方案實施蘇木精和曙紅染色。使用大鼠抗小鼠CD68(AbD Serotec,Switzerland)依照製造商的說明書檢測鼠免疫細胞。
生物化學分析
大鼠IgG-ELISA和mEGFR IgG ELISA
在第一次抗體處理後24小時(研究第8天)對小鼠採血並對血清分析人IgG濃度。使用用於針對CD20的單克隆抗體的量化的ELISA(Roche Pharma Penzberg;TR-TNA5,Germany)依照方案測試血清中的治療性抗體濃度。試劑單抗IgG-Bi(M-R10Z8E9;Ch.02GG);單抗rH-IgG(RO5072759);單抗<hfcy>IgG-Dig(XOSU-Sux)(M-R10Z8E9;Ch.03)由J.Schleypen(Roche Penzberg)饋贈。以連續稀釋液(1:2000;1:20000;1:200000)分析血清樣品。使用測量波長405nm和參考波長492nm(VersaMax可調式微量板讀數儀,Molecular Devices)測量吸光度。
結果
在同基因同位Panc02模型中,與媒介和抗PD-L1相比,muFGK4.5與抗PD-L1抗體的組合展現顯著的腫瘤生長抑制。此外,muFGK4.5和抗PD-L1抗體一起在體內協同性增強效應T細胞的擴充,這轉化成此模型中9隻小鼠中4隻中腫瘤的完全消除(圖1和2)。
免疫藥效學(PD)分析證明了muFGK4.5將小鼠脾和血液中以及淋巴結中活化的T細胞(CD4和CD8)的數目提高大約2倍。有趣的是,9天起動療法之後muFGK4.5與抗PD-L1抗體的組合將小鼠脾中活化的T細胞的數目進一步提高大約6至7倍(圖3)。
實施例2
此實施例證明a-PDL-1和a-CD40與兩種不同抗細胞因子(a-IL6和a-TNFa,單獨的或一起的)的組合的功效。此信息是有用的,因為那些抗體可用於在a-CD40注射後中和細胞因子釋放。
材料和方法
細胞培養和應用
Panc-02-Fluc細胞克隆H7(人胰腺癌細胞)最初是自ATCC(美國典型培養物保藏中心)獲得的並在擴充後保藏於內部細胞庫。在含有10%FCS(Sigma)和1%Glutamax+500ug/ml潮黴素的RPMI培養基中培養Panc-02-Fluc細胞。在5%CO2的水飽和氣氛中於37℃培養細胞。
在麻醉的C57BL/6小鼠的腹部左側做一小切口。打開腹膜壁並用鑷子小心分離胰。將10微升(0.2x106個細胞,在RPMI培養基中)細胞懸浮液注射入胰尾。使用5/0可吸收縫合線閉合腹膜壁和皮膚傷口。
動物
依照提交的指導方針(GV-Solas;Felasa;TierschG)在無特定病原體的條件下以12小時明亮/12小時黑暗的日周期維持60隻C57BL/6雌性小鼠;實驗開始時8-9周齡(購自Charles Rivers,Germany)。實驗性研究方案得到地方政府審查和批准(P 2011-128)。到達後,將動物維持1周以適應新環境和進行觀察。之後對它們在背部右側皮下植入發射機應答器進行鑑別並再維持1周進行恢復。定期進行連續健康監測。
處理
在研究第0天對小鼠胰內注射RPMI中的2x105個Panc02-Fluc細胞(傳代16,存活力90.5%)。
在第6,7,8,和9天,對12隻小鼠/組i.p.注射不同化合物。在第7,14和21天,對10隻小鼠/組i.p.注射不同化合物(見研究組)。
測試化合物(抗體)
化合物的規格
對所有小鼠注射200μL適宜溶液。i.p.注射所有抗體。對媒介組的小鼠注射組氨酸緩衝液並對治療組注射抗體。為了獲得適當量的抗體/200μL,在必要時用組氨酸緩衝液稀釋抗體溶液。對小鼠進行處理的最大數目是4次。
調查
監測
每天對動物管理臨床症狀和不利影響檢測。動物的終止標準為臨床病態,運動受損,毛皮不潔。
用於化合物分析的血清提取
在第2次,第5次和第6次抗體處理之後1小時收集來自一半經處理動物的血清樣品,並在第2次,第5次和第6次抗體處理之後24小時收集來自另一半經處理動物的血清樣品。在處死當天對所有動物採血。樣品保存於-20℃。
屍檢
依照終止標準處死小鼠。自4隻小鼠/組收集脾,肝和胰腫瘤用於隨後的組織病理學分析(4%甲醛,閃凍)。
樣品加工
切出胰腫瘤,肝和脾,立即在10%福馬林溶液中固定,隨後為石蠟包埋(Leica自動組織加工儀TP1020,Germany)和微分4μm切片(Leica RM2235旋轉切片機,Germany)加工。使用標準方案實施蘇木精和曙紅染色。使用大鼠抗小鼠CD68(AbD Serotec,Switzerland)依照製造商的說明書檢測鼠免疫細胞。
生物化學分析
mCD40IgG-ELISA和mPDL-1IgG ELISA
使用用於抗CD40的量化的CD40/Fc嵌合物(R&D,1215-CD-050)ELISA依照方案(Roche-Glycart,Switzerland)測試血清中抗CD40濃度。使用試劑;捕捉蛋白質:6xHis標籤生物素(Abcam,ab27025)和CD40/Fc嵌合物(R&D,1215-CD-050),檢測抗體:抗小鼠IgG(HRP),(Abcam,ab98808)。以連續稀釋液(1:300,1:1500,1:7500)分析血清樣品。使用測量波長405nm和參考波長490nm(VersaMax可調式微量板讀數儀,Molecular Devices)測量吸光度。
使用用於抗PD-L1的量化的鼠PD-L1(R&D,1019-B7-100)ELISA依照方案(Roche-Glycart,Switzerland)測試血清中的抗PD-L1濃度。使用試劑;捕捉蛋白質:IgG-FC生物素(Abcam ab98561)和鼠B7-H1/PD-L1(R&D,1019-B7-100),檢測抗體:抗小鼠IgG(HRP),(Abcam,ab98808)。以連續稀釋液(1:2500,1:12500,1:62500)分析血清樣品。使用測量波長405nm和參考波長490nm(VersaMax可調式微量板讀數儀,Molecular Devices)測量吸光度。
細胞因子分析
通過Luminex測定法(Bio-Plex Pro小鼠細胞因子23路測定法)依照製造商的說明書測量細胞因子。
結果
與單獨的CD40激動劑和PD-L1抑制劑(分別為成分A和B)雙藥相比,添加抗細胞因子作為第三成分導致可耐受性提高,表現為體重減輕更少。特別是,添加抗TNFα作為第三成分(成分C)導致可耐受性提高,如例如通過監測治療期間的體重減輕而證明的(見圖5)。同時,CD40/PD-L1組合的活性在與作為第三成分的抗細胞因子一起注射時得到保留(見圖6)。
序列表
豪夫邁·羅氏有限公司(F. Hoffmann-La Roche AG)
活化人CD40的抗體和針對人PD-L1的抗體的組合療法
P32260-EP-1
23
PatentIn version 3.5
1
277
PRT
人(Homo sapiens)
1
Met Val Arg Leu Pro Leu Gln Cys Val Leu Trp Gly Cys Leu Leu Thr
1 5 10 15
Ala Val His Pro Glu Pro Pro Thr Ala Cys Arg Glu Lys Gln Tyr Leu
20 25 30
Ile Asn Ser Gln Cys Cys Ser Leu Cys Gln Pro Gly Gln Lys Leu Val
35 40 45
Ser Asp Cys Thr Glu Phe Thr Glu Thr Glu Cys Leu Pro Cys Gly Glu
50 55 60
Ser Glu Phe Leu Asp Thr Trp Asn Arg Glu Thr His Cys His Gln His
65 70 75 80
Lys Tyr Cys Asp Pro Asn Leu Gly Leu Arg Val Gln Gln Lys Gly Thr
85 90 95
Ser Glu Thr Asp Thr Ile Cys Thr Cys Glu Glu Gly Trp His Cys Thr
100 105 110
Ser Glu Ala Cys Glu Ser Cys Val Leu His Arg Ser Cys Ser Pro Gly
115 120 125
Phe Gly Val Lys Gln Ile Ala Thr Gly Val Ser Asp Thr Ile Cys Glu
130 135 140
Pro Cys Pro Val Gly Phe Phe Ser Asn Val Ser Ser Ala Phe Glu Lys
145 150 155 160
Cys His Pro Trp Thr Ser Cys Glu Thr Lys Asp Leu Val Val Gln Gln
165 170 175
Ala Gly Thr Asn Lys Thr Asp Val Val Cys Gly Pro Gln Asp Arg Leu
180 185 190
Arg Ala Leu Val Val Ile Pro Ile Ile Phe Gly Ile Leu Phe Ala Ile
195 200 205
Leu Leu Val Leu Val Phe Ile Lys Lys Val Ala Lys Lys Pro Thr Asn
210 215 220
Lys Ala Pro His Pro Lys Gln Glu Pro Gln Glu Ile Asn Phe Pro Asp
225 230 235 240
Asp Leu Pro Gly Ser Asn Thr Ala Ala Pro Val Gln Glu Thr Leu His
245 250 255
Gly Cys Gln Pro Val Thr Gln Glu Asp Gly Lys Glu Ser Arg Ile Ser
260 265 270
Val Gln Glu Arg Gln
275
2
290
PRT
人(Homo sapiens)
2
Met Arg Ile Phe Ala Val Phe Ile Phe Met Thr Tyr Trp His Leu Leu
1 5 10 15
Asn Ala Phe Thr Val Thr Val Pro Lys Asp Leu Tyr Val Val Glu Tyr
20 25 30
Gly Ser Asn Met Thr Ile Glu Cys Lys Phe Pro Val Glu Lys Gln Leu
35 40 45
Asp Leu Ala Ala Leu Ile Val Tyr Trp Glu Met Glu Asp Lys Asn Ile
50 55 60
Ile Gln Phe Val His Gly Glu Glu Asp Leu Lys Val Gln His Ser Ser
65 70 75 80
Tyr Arg Gln Arg Ala Arg Leu Leu Lys Asp Gln Leu Ser Leu Gly Asn
85 90 95
Ala Ala Leu Gln Ile Thr Asp Val Lys Leu Gln Asp Ala Gly Val Tyr
100 105 110
Arg Cys Met Ile Ser Tyr Gly Gly Ala Asp Tyr Lys Arg Ile Thr Val
115 120 125
Lys Val Asn Ala Pro Tyr Asn Lys Ile Asn Gln Arg Ile Leu Val Val
130 135 140
Asp Pro Val Thr Ser Glu His Glu Leu Thr Cys Gln Ala Glu Gly Tyr
145 150 155 160
Pro Lys Ala Glu Val Ile Trp Thr Ser Ser Asp His Gln Val Leu Ser
165 170 175
Gly Lys Thr Thr Thr Thr Asn Ser Lys Arg Glu Glu Lys Leu Phe Asn
180 185 190
Val Thr Ser Thr Leu Arg Ile Asn Thr Thr Thr Asn Glu Ile Phe Tyr
195 200 205
Cys Thr Phe Arg Arg Leu Asp Pro Glu Glu Asn His Thr Ala Glu Leu
210 215 220
Val Ile Pro Glu Leu Pro Leu Ala His Pro Pro Asn Glu Arg Thr His
225 230 235 240
Leu Val Ile Leu Gly Ala Ile Leu Leu Cys Leu Gly Val Ala Leu Thr
245 250 255
Phe Ile Phe Arg Leu Arg Lys Gly Arg Met Met Asp Val Lys Lys Cys
260 265 270
Gly Ile Gln Asp Thr Asn Ser Lys Lys Gln Ser Asp Thr His Leu Glu
275 280 285
Glu Thr
290
3
107
PRT
人(Homo sapiens)
3
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Tyr Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Asn Leu Leu Ile
35 40 45
Tyr Thr Ala Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Asn Ile Phe Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
4
126
PRT
人(Homo sapiens)
4
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asp Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Asn Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Gln Pro Leu Gly Tyr Cys Thr Asn Gly Val Cys Ser Tyr
100 105 110
Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120 125
5
118
PRT
人(Homo sapiens)
5
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Ser
20 25 30
Trp Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Trp Ile Ser Pro Tyr Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg His Trp Pro Gly Gly Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ala
115
6
118
PRT
人(Homo sapiens)
6
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Ser
20 25 30
Trp Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Trp Ile Ser Pro Tyr Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg His Trp Pro Gly Gly Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ala
115
7
118
PRT
人(Homo sapiens)
7
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Gly Ser
20 25 30
Trp Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Trp Ile Leu Pro Tyr Gly Gly Ser Ser Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg His Trp Pro Gly Gly Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ala
115
8
108
PRT
人(Homo sapiens)
8
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Ser Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Leu Tyr His Pro Ala
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
9
108
PRT
人(Homo sapiens)
9
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Ser Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Asn Val Pro Trp
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
10
108
PRT
人(Homo sapiens)
10
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Ser Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ala Pro Pro Trp
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
11
108
PRT
人(Homo sapiens)
11
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Ser Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Thr Val Pro Trp
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
12
108
PRT
人(Homo sapiens)
12
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Val Ile Asn Thr Phe
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Thr Val Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
13
108
PRT
人(Homo sapiens)
13
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Ser Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Tyr Gly Val Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
14
108
PRT
人(Homo sapiens)
14
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Ser Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Leu Phe Thr Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
15
108
PRT
人(Homo sapiens)
15
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Ser Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Phe Ile Thr Pro Thr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
16
108
PRT
人(Homo sapiens)
16
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Ser Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Tyr Thr Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
17
108
PRT
人(Homo sapiens)
17
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Ser Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Phe Phe Tyr Thr Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
18
108
PRT
人(Homo sapiens)
18
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Ser Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Leu Phe Thr Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
19
108
PRT
人(Homo sapiens)
19
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Ser Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Leu Tyr Thr Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
20
108
PRT
人(Homo sapiens)
20
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Ser Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Trp Tyr His Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
21
108
PRT
人(Homo sapiens)
21
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Ser Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Phe Tyr Ile Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
22
108
PRT
人(Homo sapiens)
22
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Ser Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Trp Tyr Thr Pro Thr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
23
107
PRT
人(Homo sapiens)
23
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Ser Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Ser
50 55 60
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
65 70 75 80
Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Phe Ile Pro Pro Thr
85 90 95
Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
