一種用於治療心肌梗死的細胞製劑及製備方法與應用與流程
2023-06-21 09:27:41 3
本發明屬於生物醫藥領域,特別涉及一種用於治療心肌梗死的細胞製劑及製備方法與應用。
背景技術:
目前無論基礎和臨床,儘管近幾十年對心肌梗死的治療有了很大的進步,目前尚沒有任何能夠根治心肌梗死的藥物和療法。細胞治療被認為是治療心肌梗死最有希望的方法之一。無論是基礎和臨床研究均證明:骨髓間充質幹細胞(BMSCs)對梗死心肌的細胞治療,被證明是可行和安全的。但其療效只體現在減小梗死面積,提高射血分數,改善心功能,及改善病理性左心室重構,但上述療效還不能完全治癒心肌梗死。因此,目前研發瓶頸和前沿是:研發對於有效減小梗死面積,改善心功能,改善缺血心肌纖維化、以改善梗死心臟病理重構療效更佳的細胞療法及細胞治療製劑。
技術實現要素:
本發明的首要目的在於克服現有使用BMSCs對梗死心肌細胞治療的缺點與不足,提供一種用於治療心肌梗死的細胞製劑。該細胞製劑的主要成分為心臟Telocytes(簡稱為CTs)和骨髓間充質幹細胞(BMSCs)。
本發明的另一目的在於提供所述用於治療心肌梗死的細胞製劑的製備方法。
本發明的再一目的在於提供所述用於治療心肌梗死的細胞製劑的應用。
本發明的目的通過下述技術方案實現:一種用於治療心肌梗死的細胞製劑,主要成分為CTs和BMSCs。
所述的CTs和所述的BMSCs按細胞數1:1配比。
所述的CTs的純度優選為在95%以上。
所述的CTs在所述的用於治療心肌梗死的細胞製劑中的濃度為至少5×106個細胞/mL。
所述的BMSCs的純度優選為在95%以上。
所述的BMSCs在所述的用於治療心肌梗死的細胞製劑中的濃度為至少5×106個細胞/mL。
所述的用於治療心肌梗死的細胞製劑還包括溶劑。也就是說,所述的用於治療心肌梗死的細胞製劑優選由CTs、BMSCs和溶劑組成。
所述的溶劑是維持細胞生理狀態的溶液,如生理鹽水、PBS或含血清的培養液;優選為含血清的培養液。
所述的血清優選為胎牛血清。
所述的血清的濃度優選為體積百分比20%。
所述的培養液優選為DMEM培養液。
所述的用於治療心肌梗死的細胞製劑還可以包括上述CTs和BMSCs分別分泌的功能因子和小RNA中的一種或兩種。即所述的用於治療心肌梗死的細胞製劑優選由如下成分組成:CTs和BMSCs分別分泌的功能因子和小RNA中的一種或兩種、CTs、BMSCs和溶劑。兩種細胞與及其分泌的功能因子、小RNA經混合培養,彼此相互作用對該兩種細胞本身的表型和分泌表型改變,使其在增殖能力、移行能力、抗細胞死亡、存活能力、抗缺血與缺氧能力、抗炎症反應能力、促進血管新生能力、抗纖維化能力的增強,以及該兩種細胞及分泌功能分子彼此協同作用,在上述特性而獲得的提高。
所述的功能因子優選為能促進經移植細胞、心肌細胞、心臟血管內皮細胞、心臟CTs,心臟內源性幹細胞的增殖和分化、移行、存活,抗死亡、抗缺血與缺氧、抗炎症,及促進心肌血管新生,抗心肌纖維化,及其彼此的協同作用。
所述的小RNA包括microRNA、LncRNA和piRNA等,其作用也是對心肌細胞、心臟血管內皮細胞、心臟CTs,心臟內源性幹細胞和內外源性骨髓間充質幹細胞的抗死亡與促進存活、促進增殖和誘導分化。
所述的用於治療心肌梗死的細胞製劑的製備方法,包括如下步驟:將CTs和BMSCs混勻,得到用於治療心肌梗死的細胞製劑;優選為將CTs和BMSCs在溶劑中混勻,得到用於治療心肌梗死的細胞製劑;更優選為將如下成分混勻:CTs和BMSCs分別分泌的功能因子和小RNA中的一種或兩種、CTs、BMSCs和溶劑,得到用於治療心肌梗死的細胞製劑。
所述的CTs和所述的BMSCs按細胞數1:1配比。
所述的CTs的純度優選為在95%以上。
所述的CTs在所述的用於治療心肌梗死的細胞製劑中的濃度為至少5×106個細胞/mL。
所述的BMSCs的純度優選為在95%以上。
所述的BMSCs在所述的用於治療心肌梗死的細胞製劑中的濃度為至少5×106個細胞/mL。
所述的用於治療心肌梗死的細胞製劑的應用,是將其直接用於治療心肌梗死或是將其製備成用於治療心肌梗死的藥物或醫療器械進行應用;具體包括如下方式與途徑:可通過對缺血心肌的缺血區和邊緣區同時進行注射,或通過介入的方式對缺血心肌的缺血區和邊緣區同時進行注射,但實施治療的途徑不僅限於上述兩種方式,還包括與不同生物體內可降解材料相混合,製備成含不同濃度該細胞製劑的各種細胞製片,通過手術覆蓋在缺血心肌缺血區,以發揮治療作用;也可以把該細胞製劑中的細胞使用各類特異性靶向心臟的靶向子(如:抗體或短肽等)進行表面修飾,然後通過靜脈注射使用,以實施經靜脈使用的心臟靶向細胞治療。
所述的細胞製劑發揮療效實現途徑包括但不限於如下闡述:①促進缺血心肌梗死區CTs構成網狀結構的修復與再生;②促進缺血心肌缺血區和邊緣區的血管新生;③改善缺血心肌纖維化、及改善梗死心臟的病理重構;④減小缺血心肌的梗死面積,改善心功能,及有效減小心梗後心衰的發生率,從而實現有效促進心梗心臟缺血區和邊緣區的心肌層的再生。
本發明相對於現有技術具有如下的優點及效果:
(1)本發明提供的細胞製劑經心肌內直接注射或介入心肌內注射,對急性心肌梗死心臟的缺血區和缺血邊緣區實施該細胞製劑移植,能有效修復與再生缺血心肌缺血區嚴重受損的由CTs構成的細胞網絡,以修復有利於梗死心肌再生的細胞結構微環境,從而有利於梗死心肌的再生。
(2)該細胞製劑對急性心肌梗死實施移植治療後,在減小梗死面積,改善心梗心臟心功能方面的療效要優於目前常用的單獨使用BMSCs的治療。
(3)該細胞製劑對急性心肌梗死實施移植治療後,在改善缺血心肌纖維化、促進缺血區和邊緣區血管新生,以及改善梗死心臟病理重構,減小心梗後心衰發生率方面的療效要優於目前常用的BMSCs。
附圖說明
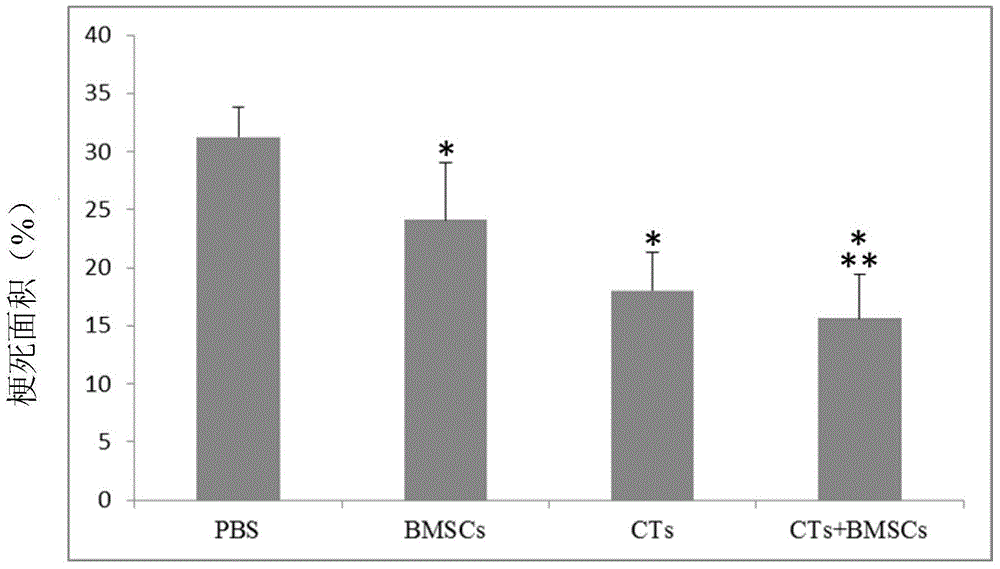
圖1是使用PBS和不同的細胞製劑注射心肌梗死模型4周後的心臟梗死面積統計結果圖;其中,*表示CTs+BMSCs組,CTs組和BMSCs組分別相對於 PBS組,p<0.01;**表示CTs+BMSCs組相對於BMSCs組,p<0.01。
圖2是使用PBS和不同的細胞製劑注射心肌梗死模型4周後的心功能檢測結果圖;其中,圖(A)為各組細胞治療梗死心臟的射血分數圖,心功能越好,其值就越大;圖(B)為各組細胞治療梗死心臟的收縮末期的左心室最小直徑結果圖,心功能越好,其值就越小;圖(C)為各組細胞治療梗死心臟的舒張末期的左心室最小直徑結果圖,心功能越好,其值就越小;*表示CTs+BMSCs組,CTs組和BMSCs組分別相對於PBS組,p<0.05;**表示CTs+BMSCs組相對於BMSCs組,p<0.05。
圖3是使用PBS和不同的細胞製劑注射心肌梗死模型4周後的心肌層纖維化程度結果圖;其中,圖(A)為梗死區纖維化面積結果圖,圖(B)為非梗死區血管周邊纖維化面積結果圖;*表示CTs+BMSCs組,CTs組和BMSCs組分別相對於PBS組,p<0.05;**表示CTs+BMSCs組相對於BMSCs組,p<0.05。
圖4是使用PBS和不同的細胞製劑注射心肌梗死模型4周後的肌成纖維細胞數目檢測結果圖;其中,*表示CTs+BMSCs組,CTs組和BMSCs組分別相對於PBS組,p<0.01;**表示CTs+BMSCs組相對於BMSCs組和CTs組,p<0.01。
圖5是使用PBS和不同的細胞製劑注射心肌梗死模型4周後的心肌層血管單位密度結果圖;其中,圖(A)為梗死區陽性血管密度的半定量分析結果圖,圖(B)為邊緣區陽性血管密度的半定量分析結果圖;*表示CTs+BMSCs組,CTs組和BMSCs組分別相對於PBS組,p<0.05。
圖6是使用PBS和不同的細胞製劑注射心肌梗死模型4周後的梗死區CTs檢測結果圖;其中,*表示CTs+BMSCs組,CTs組和BMSCs組分別相對於PBS組,p<0.01。
具體實施方式
下面結合實施例及附圖對本發明作進一步詳細的描述,但本發明的實施方式不限於此。
實施例1
(一)CTs的製備
1、SD雌性大鼠(250-300g)(廣東省醫學實驗動物中心)乙醚麻醉後拉頸處死,在70(v/v)%乙醇中浸泡消毒5min,迅速轉移至生物安全櫃內。
2、無菌條件下迅速剪開胸腔取出心臟,將心臟放入無菌PBS溶液(0.01M, pH7.4)中清洗3次,除去心臟中殘餘的血液,在無菌平皿中剪碎心臟組織(1-2mm3),然後將心臟組織塊轉移至50ml無菌離心管,加入37℃預熱的經過濾除菌的消化酶液[0.05(w/v)%膠原酶+0.1(w/v)%胰酶,下同]2.5ml,密閉管蓋後,於37℃水浴搖床內(300rpm)消化10min,然後在生物安全櫃內靜置2min,棄上層懸液。
3、在生物安全櫃內,往沉澱組織塊中加入消化酶液2.5ml,密閉管蓋後,於37℃水浴搖床(300rpm)內再消化15min,然後在生物安全櫃內使用移液槍充分吹打經消化的組織塊,至細胞充分分離,離心管靜置2min後,取上層懸液置於一支新的15mL無菌離心管,並加入等體積的含20%胎牛血清的DMEM培養液混勻終止酶消化反應。
4、往沉澱組織中再重新加入消化酶液2.5ml,密閉管蓋後轉移至37℃水浴搖床(300rpm)內消化15min,重複步驟3、4,收集含經分離細胞的懸液,直至組織完全消化。
5、將所有經分離細胞的懸液收集,分別使用無菌孔徑為100μm和40μm的尼龍膜濾過,去除體積大組織碎片,然後將細胞懸液置50×g離心力下離心2min,將上層細胞懸液轉移至一新的15ml無菌離心管,在458×g離心力下離心5min,棄上清,收集經分離細胞。
6、往含細胞沉澱的離心管內加入5ml無菌PEB液[稱取牛血清白蛋白(BSA)1.00g、乙二胺四乙酸(EDTA)0.12g,溶於200ml PBS緩衝液中,溶解混勻後調節pH值至7.2,用0.22μm無菌濾膜過濾除菌,分裝於無菌瓶中,4℃冰箱中保存)重懸細胞沉澱,並將懸液在38×g離心力下離心2min,將上層細胞懸液轉移至新的15ml無菌離心管,在200×g離心力下離心10min,收集細胞,然後加入1ml PEB液混勻細胞,獲得目標分離單細胞懸液。
7、向所獲目標分離單細胞懸液中加入兔抗大鼠c-Kit抗體5μl(終濃度為體積比稀釋1:200),混勻後密閉管蓋,4℃旋轉孵育40min後,向細胞懸液中加入2ml PEB液輕微吹打,洗去未結合抗體,然後在458×g離心力下離心5min,棄上清。
8、向離心管內加入180μl PEB液並混勻細胞,然後加入羊抗兔lgG免疫磁珠20μl,密閉管蓋置4℃孵育25min後,往細胞懸液中加入2ml PEB液輕微吹打,洗去未結合二抗磁珠,然後在458×g離心力下離心5min,以收集細胞,然後加入500μl PEB混懸細胞。
9、使用磁珠分選系統,按陽性分選獲得C-kit+的CTs。
10、經分離的CTs在含20%胎牛血清的DMEM培養液,37℃、5%CO2、95%空氣的無菌培養箱進行培養,對經分離的細胞CTs進行傳代擴增,經該法分離的細胞近95%的細胞為c-Kit+/CD34+,達到較高的純度。按步驟1~10,能重複得到CTs。
11、所有用於細胞治療製劑製備的CTs均為傳代低於五代,以確保細胞核型沒有發生改變。
(二)BMSCs的製備
1、SD雌性大鼠(250-300g)(廣東省醫學實驗動物中心),乙醚麻醉後拉頸處死,放入70(v/v)%酒精中浸泡5min。
2、在生物安全櫃中,剪開大鼠股骨外面的皮膚、剔除肌肉,收集股骨。
3、剪開股骨兩端露出骨髓腔,用無菌注射器吸取4ml含10(v/v)%FBS的L-DMEM培養液,插入骨髓腔一端將骨髓衝出。收集液用200無菌目尼龍膜過濾,然後加入4ml Tris-NH4Cl(稱取3.735g氯化銨、三羥甲基氨基甲烷(Tris)1.3g加水溶解並稀釋至500ml。0.22μm濾膜過濾除菌,4℃保存)溶液吹打均勻,靜置5min。
4、在458×g離心力下離心4min,棄上清液,用2ml含10(v/v)%FBS的L-DMEM重懸經收集的細胞,並接種到35mm培養皿中,置於37℃、5%CO2、95%空氣的無菌培養箱進行培養,48小時換液除去未貼壁細胞,以後每隔一天換液一次。
5、待細胞生長至90%融合時用0.25(w/v)%胰酶消化,將細胞按照5×105個/ml的密度接種到35mm培養皿進行擴增培養,以獲得足夠數量的BMSCs以進行下一步實驗。經該法分離擴增得到的細胞超過97%為CD90+、CD73+和CD105+陽性,低於0.5%的細胞為CD45+、CD14+和CD34+陽性,純度達到95%的BMSCs。
6、所有用於製備細胞製劑的BMSCs均為傳代低於五代,以確保細胞核型沒有發生改變。
(三)CTs和BMSCs混合細胞治療用製劑的製備
1、將經製備的CTs和BMSCs使用含20(v/v)%胎牛血清(FBS)的無菌DMEM培養液混勻,並按2.5×105:2.5×105的比例將兩種細胞均勻混合,製備成細胞總量為5×105的細胞混合液(濃度為1×104/μl,共50μl)。
2、經製備的上述混合細胞治療用製劑置於無菌的器皿,在4℃保存備用,供移植使用。
(四)CTs和BMSCs混合細胞治療用製劑對心肌梗死實施移植治療
使用雌性(250克)S.D.大鼠,行冠狀動脈前降支(LAD)結紮術致左心室前壁缺血,進行心肌梗死建模,LAD結紮後30分鐘後,左心室前壁缺血區和缺血邊緣區分別行心肌內注射步驟(三)製備好的CTs+BMSCs混合細胞治療製劑,其中,在缺血區注射10μl,且分別在缺血邊緣區的12點、3點、6點和9點位置各注射10μl。其中同等體積PBS(pH=7.4)、CTs(濃度為1×104/μl,細胞總量為5×105)和BMSCs(濃度為1×104/μl,細胞總量為5×105)分別按相同的注射方法進行心肌內注射作為對照組,每組動物為5-9隻。
(五)檢測指標
所有上述經心肌內細胞移植組別的模型鼠,於注射後4周使用B超(超聲心動圖技術)對其進行心功能指標進行測定後,取出心臟,進行常規的石蠟包埋和組織切片,並使用Massion Trichrome染色對梗死面積進行染色(藍色是梗死心肌,紅色部分是活心肌)對纖維化進行染色(藍色是纖維化,紅色部分是非纖維化的心肌組織),對不同組別梗死面積和纖維化進行比較分析;使用抗vWF(血管內皮細胞標記物)抗體進行免疫組化染色,以對不同組別的缺血區和缺血邊緣區的血管密度進行比較分析,使用c-Kit/CD34抗體(CTs的標記物)對不同組別的缺血區的CTs進行比較分析(上述方法學均是領域廣泛認可的常規方法學)。
(六)檢測結果
1、CTs+BMSCs混合細胞治療用製劑對心肌梗死治療的療效
對各組梗死面積進行半定量比較柱狀圖(如圖1所示),PBS:PBS對照組;BMSCs:骨髓間充質幹細胞組;CTs:心臟CTs組;CTs+BMSCs:心臟CTs+骨髓間充質幹細胞組(如下其它部分的均使用該相同的簡寫符號)。CTs+BMSCs混合細胞治療用製劑組,CTs組和BMSCs組梗死面積均顯著性小於PBS對照組,差異有顯著性統計學意義(p<0.01)。CTs+BMSCs混合細胞治療用製劑組的梗死面積,顯著性小於BMSCs組的梗死面積,差異有顯著性統計學意義(p<0.01)。CTs+BMSCs混合細胞治療用製劑組梗死面積的均值小於CTs組的梗死面積。上述結果表明,CTs+BMSCs混合細胞治療用製劑能顯著性減小缺血心肌的梗死面積,且其療效優於單獨使用BMSCs和CTs。
2、CTs+BMSCs混合細胞治療用製劑能顯著性改善缺血梗死心臟的心功能
左心室射血分數,左心室收縮末期直徑,左心室舒張末期直徑是衡量心臟功能的常用主要指標。檢測結果如圖2所示:
①左心室射血分數指標的研究發現(如圖2(A)所示):CTs+BMSCs混合細胞治療用製劑組,CTs組和BMSCs組的左心室射血分數均顯著性大於PBS對 照組,差異有顯著性統計學意義(p<0.05)。CTs+BMSCs混合細胞治療用製劑組的左心室射血分數顯著性大於BMSCs組,差異有顯著性統計學意義(p<0.05)。CTs+BMSCs混合細胞治療用製劑組左心室射血分數的均值大於CTs組。上述結果證明:使用CTs,BMSCs和CTs+BMSCs混合細胞治療用製劑均能顯著性改善缺血心臟的射血分數,且CTs+BMSCs混合細胞治療用製劑療效優於單獨使用BMSCs。CTs+BMSCs混合細胞治療用製劑療效也顯示優於單獨使用CTs的趨勢。
②對左心室收縮末期直徑指標的研究發現(如圖2(B)所示):CTs+BMSCs混合細胞治療用製劑組,CTs組和BMSCs組的左心室收縮末期直徑均顯著性小於PBS對照組,差異有顯著性統計學意義(p<0.05)。CTs+BMSCs混合細胞治療用製劑組的左心室收縮末期直徑的均值小於CTs和BMSCs組。上述結果證明:使用CTs,BMSCs和CTs+BMSCs混合細胞治療用製劑均能顯著性改善缺血心臟的左心室收縮末期直徑,且CTs+BMSCs混合細胞治療用製劑療效也顯示優於單獨使用CTs或BMSCs的趨勢。
③對左心室舒張末期直徑指標的研究發現(如圖2(C)所示):CTs+BMSCs混合細胞治療用製劑組,CTs組和BMSCs組的左心室舒張末期直徑均顯著性小於PBS對照組,差異有顯著性統計學意義(p<0.05)。CTs+BMSCs混合細胞治療用製劑組的左心室舒張末期直徑的均值小於CTs和BMSCs組。上述結果證明:使用CTs、BMSCs和CTs+BMSCs混合細胞治療用製劑均能顯著性改善缺血心臟的左心室舒張末期直徑,且CTs+BMSCs混合細胞治療用製劑療效也顯示優於單獨使用CTs或BMSCs的趨勢,但差異沒有顯著性統計學意義。
綜合上述三個指標證明:CTs+BMSCs混合細胞治療用製劑能顯著性改善缺血梗死心臟的心功能,且其療效優於單獨使用BMSCs。
3、CTs+BMSCs混合細胞治療用製劑能顯著性改善缺血梗死心臟的纖維化,且其療效優於單獨使用BMSCs。檢測結果如圖3所示:
梗死區纖維化面積,及非梗死區血管周邊纖維化面積是衡量心肌層纖維化程度的常用主要指標。
①梗死區纖維化面積指標的研究發現(如圖3(A)所示):CTs+BMSCs混合細胞治療用製劑組,CTs組和BMSCs組的梗死區纖維化面積均顯著性小於PBS對照組,差異有顯著性統計學意義(p<0.05)。CTs+BMSCs混合細胞治療用製劑組的梗死區纖維化面積顯著性小於BMSCs組,差異有顯著性統計學意義(p<0.01)。CTs+BMSCs混合細胞治療用製劑組的梗死區纖維化面積的均值小於CTs組。上述結果證明:使用CTs,BMSCs和CTs+BMSCs混合細胞治療用製劑 均能顯著性改善缺血心臟的梗死區纖維化面積,且CTs+BMSCs混合細胞治療用製劑療效優於單獨使用BMSCs。CTs+BMSCs混合細胞治療用製劑療效也顯示優於單獨使用CTs的趨勢。
②非梗死區血管周邊纖維化面積指標的研究發現(如圖3(B)所示):CTs+BMSCs混合細胞治療用製劑組,CTs組和BMSCs組的非梗死區血管周邊纖維化面積均顯著性小於PBS對照組,差異有顯著性統計學意義(p<0.05)。CTs+BMSCs混合細胞治療用製劑組的非梗死區血管周邊纖維化面積的均值小於BMSCs組。上述結果證明:使用CTs,BMSCs和CTs+BMSCs混合細胞治療用製劑均能顯著性改善缺血心臟的非梗死區血管周邊纖維化面積,且CTs+BMSCs混合細胞治療用製劑療效也顯示優於單獨使用BMSCs。
綜合上述二個指標證明:CTs+BMSCs混合細胞治療用製劑能顯著性改善缺血梗死心臟的纖維化,且其療效優於單獨使用BMSCs。
4、CTs+BMSCs混合細胞治療用製劑能顯著性減小缺血心肌梗死區,產生膠原纖維的來源細胞――肌成纖維細胞的數目,從而有效改善缺血心肌的纖維化,且其療效優於單獨使用BMSCs和CTs。
心肌缺血缺氧會誘導心肌層的成纖維細胞分化成為肌成纖維細胞,該細胞能大量合成膠原纖維,導致心肌層纖維化。因此,評價心肌層肌成纖維細胞的單位密度,是目前常用的改善心肌纖維化的一個指標。使用抗α平滑肌肌動蛋白(肌成纖維細胞的標記物)抗體對各組心臟切片進行免疫組化染色。該指標的研究發現(如圖4所示):CTs+BMSCs混合細胞治療用製劑組,CTs組和BMSCs組的梗死區的肌成纖維細胞密度均顯著性小於PBS對照組,差異有顯著性統計學意義(p<0.01)。CTs+BMSCs混合細胞治療用製劑組的肌成纖維細胞密度,顯著性小於BMSCs組和CTs,差異有顯著性統計學意義(p<0.01)。上述結果證明:使用CTs,BMSCs和CTs+BMSCs混合細胞治療用製劑均能顯著性減少缺血心肌梗死區肌型成纖維細胞密度,且CTs+BMSCs混合細胞治療用製劑療效優於單獨使用BMSCs和CTs。
5、CTs+BMSCs混合細胞治療用製劑能促進缺血心肌梗死區和邊緣區的血管新生。
心肌層血管單位密度是評價心肌層血管新生的一個常用指標。使用抗vWF(血管內皮細胞的標記物)抗體對各組心臟切片進行免疫組化染色(陽性血管呈褐色)。對該指標研究發現(如圖5所示):CTs+BMSCs混合細胞治療用製劑組,CTs組和BMSCs組的梗死邊緣區的血管密度均顯著性高於PBS對照組,差異有 顯著性統計學意義(p<0.05)。CTs+BMSCs混合細胞治療用製劑組和CTs組梗死區的血管密度均顯著性高於PBS對照組,差異有顯著性統計學意義(p<0.05),BMSCs組的梗死區的血管密度顯高於PBS對照組。CTs+BMSCs混合細胞治療用製劑組的梗死區和邊緣區的血管密度的均值均大於BMSCs組。上述結果證明:CTs+BMSCs混合細胞治療用製劑均能顯著性改善缺血心臟的缺血區和邊緣區的血管新生。
6、CTs+BMSCs混合細胞治療用製劑能促進缺血心肌梗死區CTs的再生。
缺血心肌的梗死區的CTs在心肌梗死時大部分死亡,影響缺血梗死心肌的結構完整和缺血心肌的再生。使用抗c-Kit/CD34(CTs標記物)抗體對各細胞治療組心臟切片進行免疫組化染色,對該指標研究發現(如圖6所示):CTs+BMSCs混合細胞治療用製劑組,CTs組和BMSCs組的梗死區的CTs密度均顯著性高於PBS對照組,差異有顯著性統計學意義(p<0.05)。CTs+BMSCs混合細胞治療用製劑組的梗死區CTs密度的均值均大於BMSCs組和CTs組。上述結果證明:CTs+BMSCs混合細胞治療用製劑能顯著性改善缺血心臟的梗死區CTs的再生。
上述1~6的結果綜合證明:使用CTs+BMSCs混合細胞治療用製劑對缺血梗死心肌實施移植治療,能顯著減小缺血心肌的梗死面積,改善缺血心臟的心功能,及減少心肌梗死後心衰的風險,實現上述療效的部分機理是,有效減小梗死區產生膠原纖維來源細胞――肌成纖維細胞的數目,減小梗死區和邊緣區的纖維化,以減小缺血心臟的不良左心室重構,及促進梗死區和邊緣區的血管新生,促進梗死區CTs的再生,從而促進梗死心肌的修復及減少心梗死後心衰的風險。CTs+BMSCs混合細胞治療用製劑對缺血梗死心肌的上述指標的綜合療效優於單獨使用BMSCs。
上述實施例為本發明較佳的實施方式,但本發明的實施方式並不受上述實施例的限制,其他的任何未背離本發明的精神實質與原理下所作的改變、修飾、替代、組合、簡化,均應為等效的置換方式,都包含在本發明的保護範圍之內。
