一種葡萄糖氧化酶活性快速測定試劑盒及其檢測方法與流程
2023-07-04 05:44:41 2
本發明涉及實驗室檢驗領域中的一種分析試劑盒及其檢測方法,具體涉及一種用於快速測定葡萄糖氧化酶活性的檢測試劑盒及其檢測方法。
背景技術:
葡萄糖氧化酶(Glucose oxidase,GOD),其系統命名為β-D-葡萄糖氧化還原酶(EC1.1.3.4),它能高度專一性地催化β-D-葡萄糖與氧反應,使葡萄糖氧化成為葡萄糖酸和過氧化氫。該酶廣泛分布於動物、植物及微生物體內。1928年Muller首先在黑麴黴的無細胞提取液中發現葡萄糖氧化酶。1960年Kusai等、1964年Pazurp和Swoboddas分別從青黴素和黑麴黴中提純葡萄糖氧化酶。1995年Petruccioli等用青黴素的突變株生產出葡萄糖氧化酶。我國自1986年開始研究葡萄糖氧化酶的製備提純工藝,1998年正式投入生產。1999年農業部將其定為12種允許使用的飼料酶製劑添加劑之一。
葡萄糖氧化酶催化葡萄糖氧化生成過氧化氫(H2O2),H2O2在過氧化物酶催化下可將4-氨基安替比林和苯酚氧化縮合生成粉紅色醌亞胺,基本反應如下:
測定時,在第一步的反應中,葡萄糖底物要求相對葡萄糖氧化酶絕對過量,從而催化反應為準一級反應,反應速率與加入的酶量成正比,而與底物濃度無關。第二步的反應目的是精確地測定第一步反應所釋放的H2O2的量,這一步反應需要過氧化物酶相對H2O2絕對過量,使生成的H2O2迅速參加反應,以達到實時測定第一步反應速率的目的。反應液顏色的深度與過氧化物酶催化產生的醌亞胺的量成正比,而醌亞胺的的生成量與H2O2生成量成正比,H2O2生成量則與反應液中葡萄糖氧化酶的活力成正比。
如何將上述的測定原理通過對吸收波長,緩衝液類型、pH值,反應時間等進行優化,製造出一種結構簡單、使用方便的葡萄糖氧化酶活性快速測定試劑盒是技術人員要解決的問題。
技術實現要素:
本發明需要解決的技術問題是提供一種快速測定葡萄糖氧化酶活性的檢測試劑盒及其檢測方法,旨在解決上述問題。
為了達到上述目的,本發明的技術方案是:一種葡萄糖氧化酶活性快速測定方法,其特徵在於,包括以下步驟;
將液體酶液通過1000~3000RCF離心10~20min,所獲得的上清液用緩衝液進行適當稀釋;
吸取1.0mL磷酸鹽緩衝液,置於37℃水浴保溫5~10min;
吸取1.0mL經過適當稀釋的酶液,置於37℃水浴保溫5~10min;
吸取磷酸鹽緩衝液20.0mL、苯酚溶液2.0mL、4-氨基安替比林溶液1.0mL、過氧化物酶溶液1.0mL和葡萄糖底物溶液6.0mL,總計30.0mL混勻作為測定試劑,取混合液適量置於37℃水浴保溫5~10min;
取一乾淨比色杯,吸取3.0mL經過37℃水浴保溫的測定試劑加入比色杯中,將比色杯放入分光光度計中,在波長500nm處調零,隨後向比色杯中加入0.1mL經過37℃水浴保溫的待測酶液,加入比色杯中同時計時,並立即吹吸使之混合均勻,以後每隔1min記錄吸光值,連續記錄10min;
按照公式計算酶稀釋液中葡萄糖氧化酶的活力:
公式中,XD:酶稀釋液中葡萄糖氧化酶的活力,單位為U/mL;ΔA500:一定時間內在波長500nm處溶液吸光值變化;Δt:吸光值變化對應的反應時間,單位為min;1:比色皿厚度,單位為cm;12.9:生成顯色物醌亞胺的毫摩爾吸光係數,單位為L·mmol-1.cm-1;1/2:每1mol過氧化氫生成醌亞胺物質的量;V總:反應混合液總體積,單位為mL;:V酶酶溶液的體積,單位為mL;
按照公式計算葡萄糖氧化酶樣品的酶活力,固體樣品單位為酶活性單位每克(U/g),其計算公式為:液體樣品單位酶活性單位每毫升(U/mL)其計算公式為: 公式中,X:葡萄糖氧化酶樣品的酶活力,單位為U/g(或U/mL);Df:所取酶樣品全部稀釋到合適濃度對應的緩衝液體積,單位為mL;m:稱取的固體酶樣品質量,單位為g;V:量取的液體酶樣品體積,單位為mL。
一種葡萄糖氧化酶活性快速測定試劑盒,期特徵在於,包括R1、R2、R3、R4和R5試劑,各試劑組分與配比為:
R1:緩衝液100-200mmol/L;
R2:葡萄糖水溶液1000mmol/L;
R3:過氧化物酶溶液125KU/L;
R4:4-氨基安替比林溶液4mg/mL(19.68mmol//L);
R5:苯酚溶液1.5mg/mL(15.9mmol//L);
緩衝液pH5.0-7.0,
所述的緩衝液可以為但不限於磷酸鹽緩衝液、乙酸鹽緩衝液、Tris緩衝液、McIlvaine緩衝液,其pH為5.0-7.0。試劑盒還進一步含有非離子表面活性劑,其中非離子表面活性劑可以是吐溫系列、TritonX非離子表面活性劑,用量可以是0.01-1%,主要起到增溶、澄清作用。
附圖說明
圖1為酶活測定線性範圍回歸直線
圖2為酶活測定線性範圍回歸直線
具體實施方式
下面結合實施例對本發明進行進一步說明。
實施例1
本實施例中的一種葡萄糖氧化酶快速定量檢測試劑盒為五種試劑,包括R1、R2、R3、R4和R5試劑,各試劑組分與配比為:
R1試劑:pH6.0磷酸鹽緩衝液100mmol/L;
R2試劑:葡萄糖水溶液1000mmol/L;
R3試劑:過氧化物酶溶液0.5mg/L;
R4試劑:4-氨基安替比林溶液4mg/mL;
R5試劑:苯酚溶液1.5mg/mL;
上述試劑溶解後,分裝入瓶,製成液體五試劑,直接按特定比例混合即可使用。
實施例2
利用實施例1中的葡萄糖氧化酶快速定量檢測試劑盒檢測發酵液中葡萄糖氧化酶的活性,具體操作步驟如下:
1)樣品的製備
將發酵液通過2000RCF離心10min,所獲得的上清液既是,然後取上清液用緩衝液進行適當稀釋;
2)吸取1.0mL磷酸鹽緩衝液,置於37℃水浴保溫5min;
3)吸取1.0mL經過適當稀釋的酶液,置於37℃水浴保溫5min;
4)吸取磷酸鹽緩衝液20.0mL、苯酚溶液2.0mL、4-氨基安替比林溶液1.0mL、過氧化物酶溶液1.0mL和葡萄糖底物溶液6.0mL,總計30.0mL混勻作為測定試劑,取混合液適量置於37℃水浴保溫5min;
5)取一乾淨比色杯,吸取3.0mL測定試劑(經過37℃水浴保溫)加入比色杯中,將比色杯放入分光光度計中,在波長500nm處調零;
6)隨後向比色杯中加入0.1mL待測酶液(經過37℃水浴保溫),加入比色杯中同時計時,並立即吹吸使之混合均勻,以後每隔1min記錄吸光值,連續記錄10min;根據公式
和公式進行計算葡萄糖氧化酶的活性。
實施例3
利用實施例1中的葡萄糖氧化酶快速定量檢測試劑盒檢測純酶溶液葡萄糖氧化酶的活性,具體操作步驟如下:
1)樣品製備:將酶樣品稱取試樣兩份,精確至0.001g,置於100mL容量瓶中,加入約40mL磷酸鹽緩衝液,在電磁振蕩器或恆溫振蕩器震蕩30min,或者用磁力攪拌器攪拌30min,取出用磷酸鹽緩衝液定容並搖勻,取搖勻的貯存液上離心機以4000r/min離心10min,然後取上清液用磷酸鹽緩衝液進行適當稀釋。液體樣品可以直接用磷酸鹽緩衝液進行稀釋、定容;
2)吸取1.0mL磷酸鹽緩衝液,置於37℃水浴保溫5min;
3)吸取1.0mL經過適當稀釋的酶液,置於37℃水浴保溫5min;
4)吸取磷酸鹽緩衝液20.0mL、苯酚溶液2.0mL、4-氨基安替比林溶液1.0mL、過氧化物酶溶液1.0mL和葡萄糖底物溶液6.0mL,總計30.0mL混勻作為測定試劑,取混合液適量置於37℃水浴保溫5min;
5)取一乾淨比色杯,吸取3.0mL測定試劑(經過37℃水浴保溫)加入比色杯中,將比色杯放入分光光度計中,在波長500nm處調零;
6)隨後向比色杯中加入0.1mL待測酶液(經過37℃水浴保溫),加入比色杯中同時計時,並立即吹吸使之混合均勻,以後每隔1min記錄吸光值,連續記錄10min;
7)固體樣品單位為酶活性單位每克(U/g),按公式和公式進行計算;
液體樣品單位酶活性單位每毫升(U/mL),按公式和公式進行計算。
酶活力單位U定義:在上述反應條件下,每分鐘使1μmol葡萄糖氧化為葡萄糖酸和H2O2所需要的酶量,定義為一個酶活力單位。
實施例4
利用實施例1中的葡萄糖氧化酶快速定量檢測試劑盒檢測葡萄糖氧化酶純酶溶液稀釋液的活性,結果如下:
將葡萄糖氧化酶純酶製劑溶解於pH7.0磷酸鹽緩衝液中,適當稀釋得到酶液A(0.66U),再進一步進行梯度稀釋,按照連續分光光度法連續測定1-10min的吸光度變化。每個濃度重複兩次,取每個時間點吸光度的平均值進行線性回歸分析,利用回歸分析所得直線斜率計算酶活力。結果如表1所示。
表1吸光值變化速率回歸分析與檢驗
從表1中可以看出,酶稀釋液在不同的濃度下的線性相關係數均較高,基本呈隨酶液濃度增大而減小趨勢,主要原因是隨著酶活增大,底物對於酶活不再絕對過量,反應對一級反應動力學有所偏離。p值均小於0.01,因此在各個濃度下10min內吸光值的變化均為嚴格的線性變化,因此只從吸光度隨時間變化難以判斷酶活測定線性範圍,需要進一步分析。
利用所得回歸直線的斜率計算出酶活,以酶活對相對濃度進行線性回歸分析,並對相對酶液A濃度0.1~0.5的範圍結果作圖,見說明書附圖1。
表2酶活測定線性範圍回歸分析與檢驗
從表2可以看出,在相對酶液A的濃度為0.1~0.5的範圍內相關係數與R2值最大,因此在這個濃度範圍內酶活測定值與濃度呈嚴格的線性關係。濃度範圍的上限增加後,雖然均有很小的p值,但是從相關係數上看,從0.1~0.5的濃度範圍內線性關係更加嚴格,說明書附圖1也印證了這一點,因此可以確定0.055~0.207U/mL在該測定方法的線性範圍內。實際應用中,可以用每分鐘吸光值變化的大小來方便地判定酶液濃度是否在線性範圍內,從表1可看出對應的每分鐘吸光值變化為0.011~0.042。
由於用線性回歸的方法計算ΔA/Δt比較麻煩,降低了連續分光光度法的實用性,因此嘗試對線性範圍內的點採取兩點法進行計算。分別選取第一組(2min和6min)、第二組(2min和8min)和第三組(2min和10min)兩組吸光值進行分析,結果如表3、表4和表5所示。
表3兩點法和標準方法測定結果比較(第一組)
表4兩點法和標準方法測定結果比較(第二組)
表5兩點法和標準方法測定結果比較(第三組)
經過分析,在線性範圍內的各濃度點,取第三組的吸光值用兩點法得到的酶活與標準方法測得的酶活相當接近,最大相對誤差僅為0.85%,第二組測得的酶活值相對誤差最大不超過1.36%,可以替代標準方法的測定值。第一組測得的酶活值相對誤差最大不超過3.70%,對於要求不甚嚴格的分析也可以接受,並且更加快捷。因此,對於標準的連續分光光度法,兩點法更加實用。
選取不同來源的3種葡萄糖氧化酶樣品,適當稀釋後4000rpm/min離心10min,取上清液測定酶活力。記錄1~10min的吸光值,每分鐘記錄一次。通過公式(1)可以看出,在計算酶活力是不需要時間點和吸光值嚴格的對應關係,只需要一個時間段的吸光值變化數據,且ΔA/Δt在方法允許的線性範圍內即可。取2~10min時的吸光值進行線性回歸分析,同時用標準方法計算酶活力,並選擇2min和10min時的吸光值用兩點法進行計算,如表6所示。
表6樣品酶活測定吸光值變化速率回歸分析與酶活計算
表6表明樣品酶活測定吸光值在2~10min線性關係良好,並且標準方法與兩點法結果高度一致,可以直接使用兩點法測定,後續工作可以以此進行。
實施例5
利用實施例1中的葡萄糖氧化酶快速定量檢測試劑盒檢測純酶溶液葡萄糖氧化酶的活性,結果如下:
將葡萄糖氧化酶純酶製劑溶解於pH6.0磷酸鹽緩衝液中,適當稀釋得到酶液酶液B(0.59U),再進一步進行梯度稀釋,按照連續分光光度法連續測定1-10min的吸光度變化。每個濃度重複兩次,取每個時間點吸光度的平均值進行線性回歸分析,利用回歸分析所得直線斜率計算酶活力。結果如表7所示。
表7吸光值變化速率回歸分析與檢驗
在不同的濃度下的線性相關係數均較高,基本呈隨酶液濃度增大而減小趨勢,主要原因是隨著酶活增大,底物對於酶活不再絕對過量,反應對一級反應動力學有所偏離。p值均小於0.01,因此在各個濃度下10min內吸光值的變化均為嚴格的線性變化,因此只從吸光度隨時間變化難以判斷酶活測定線性範圍,需要進一步分析。
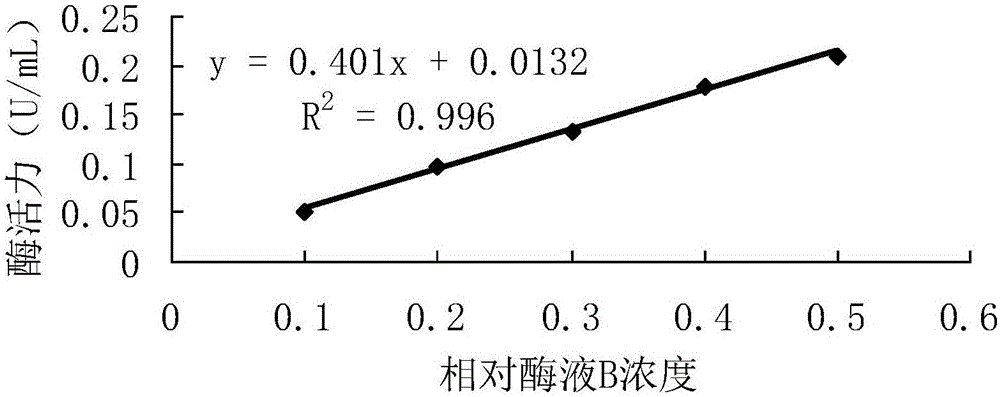
利用所得回歸曲線的斜率計算出酶活,以酶活對相對濃度進行線性回歸分析,並對相對酶液B濃度0.1~0.5的範圍結果作圖。
表8酶活測定線性範圍回歸分析與檢驗
從表8可以看出,在相對酶液B的濃度為0.1~0.5的範圍內相關係數與R2值最大,因此在這個濃度範圍內酶活測定值與濃度呈嚴格的線性關係。濃度範圍的上限增加後,雖然均有很小的p值,但是從相關係數上看,從0.1~0.5的濃度範圍內線性關係更加嚴格,說明書附圖2也印證了這一點,因此可以確定0.050~0.209U/mL在該測定方法的線性範圍內。實際應用中,可以用每分鐘吸光值變化的大小來方便地判定酶液濃度是否在線性範圍內,從表7可看出上述範圍對應的每分鐘吸光值變化約為0.010~0.042。
由於用線性回歸的方法計算ΔA/Δt比較麻煩,降低了連續分光光度法的實用性,因此嘗試對線性範圍內的點採取兩點法進行計算。分別選取第一組(2min和6min)、第二組(2min和8min)和第三組(2min和10min)兩組吸光值進行分析,結果如表9、表10和表11所示。
表9兩點法和標準方法測定結果比較(第一組)
表10兩點法和標準方法測定結果比較(第二組)
表11兩點法和標準方法測定結果比較(第三組)
經過分析,在線性範圍內的各濃度點,取第二組的吸光值用兩點法得到的酶活與標準方法測得的酶活相當接近,最大相對誤差僅為1.68%,第三組測得的酶活值相對誤差最大不超過2.15%,可以替代標準方法的測定值。第一組測得的酶活值相對誤差最大不超過8.32%,對於要求不甚嚴格的分析也可以接受,並且更加快捷。因此,對於標準的連續分光光度法,兩點法更加實用。
選取不同來源的3種葡萄糖氧化酶樣品,適當稀釋後4000rpm/min離心10min,取上清液測定酶活力。記錄1~10min的吸光值,每分鐘記錄一次。通過公式可以看出,在計算酶活力是不需要時間點和吸光值嚴格的對應關係,只需要一個時間段的吸光值變化數據,且ΔA/Δt在方法允許的線性範圍內即可。取2~8min時的吸光值進行線性回歸分析,同時用標準方法計算酶活力,並選擇2min和8min時的吸光值進行計算,如表12所示。
表12樣品酶活測定吸光值變化速率回歸分析與酶活計算
表12表明樣品酶活測定吸光值變化,在2~8min線性關係良好,並且標準方法與兩點法結果高度一致,可以直接使用兩點法測定。
