一種嵌合抗原受體T細胞及其製備方法與應用與流程
2023-05-31 10:27:01 2
本發明涉及一種嵌合抗原受體T細胞及其製備方法與應用。
背景技術:
嵌合抗原受體T細胞(Chimeric Antigen Receptor T cells,CART)是通過基因修飾的手段,使能特異性識別靶抗原的單克隆抗體的單鏈可變區
(scFv)表達在T細胞表面,同時scFv通過跨膜區與人工設計的T細胞胞內的活化增殖信號域相耦連。這樣,單克隆抗體對靶抗原的特異性識別與T細胞的功能相結合,產生特異性的殺傷作用,而且CART能夠以非MHC限制性的方式殺傷靶細胞。現CAR-T淋巴細胞技術已發展到了第三代。1989年,科學家Zelig Eshhar提出了CART的構想,在隨後的CART技術發展中,主要經過了3代的演化,第一代CAR由識別腫瘤表面抗原的單鏈抗體(scFv)抗原結合部和免疫受體酪氨酸活化基序構成,胞外通過單鏈抗體(scFv)識別腫瘤標誌分子,如CD19,胞內利用CD3分子ζ鏈傳遞信號,由於沒有協同刺激信號,T細胞增殖時間短,細胞因子分泌低,在臨床試驗中,效果不理想。2011年,Carl June教授利用二代CART技術治療3例慢性淋巴細胞性白血病取得了非常好的效果,2例完全緩解,1例部分緩解;二代CART技術根據選用的協同刺激分子不同分為兩類,一種為協同刺激分子CD28+CD3ζ,一種為協同刺激分子4-1BB+CD3ζ,即引入了共刺激的信號序列,可提高T細胞的細胞獨活性、增殖性與存活時間、促進細胞因子的釋放,這兩類CART在臨床治療急性淋巴細胞性白血病時都取得了成功。CD28協同刺激信號促使T細胞快速擴增,4-1BB信號促使T細胞擴增、存活、持續存活時間更長,結合CD28和4-1BB兩個分子在一個CAR分子結構上的CART,稱為三代CART,即同時在胞漿區串聯排列了CD28、4-1BB協同刺激分子和CD3ζ分子,基本模擬了T細胞正常發揮作用時受到的刺激信號,和二代載體相比,引入了雙共刺激的信號序列將具有更好的效果。
CART是近兩年取得顯著進展的治療腫瘤的技術,該技術首先在治療以CD19為靶點的急性淋巴細胞性白血病和淋巴瘤上取得了成功,據諾華公司報導的臨床數據,利用CD19CART治療兒童B細胞性急性淋巴細胞性白血病,可達到93%的完全緩解率。目前,在臨床廣泛應用中,用於治療白血病和淋巴瘤的CART載體結構設計皆為二代載體的結構。儘管臨床治療中尤其是用於治療白血病時取得了非常好的效果,但是這些患者的入組條件較為嚴苛,對於病情非常嚴重的患者仍不能入組治療;另外,針對CD19的CART治療淋巴瘤時的完全緩解率約為30%-47%,仍存在繼續改進提高的空間。因此,亟待進一步增加CAR分子結構胞漿區內協同刺激分子的數量,以能更好模擬T細胞在生理和病理情況下自然活化的機制,促使細胞擴增,殺傷腫瘤細胞,延長體內持續存活時間,提高CD19CART治療效果。
技術實現要素:
本發明的目的是通過以下技術方案實現的,一種嵌合抗原受體T細胞,表面表達嵌合抗原受體CD19CAR基因,其鹼基序列如SEQ ID NO:3所示。
進一步,所述嵌合抗原受體CD19CAR基因是由合成ScFV基因和合成3代CAR結構基因通過重疊PCR進行拼接。
進一步,所述合成ScFV基因是通過PCR方法獲得編碼CD8信號肽、序列號CAA74659.1的重鏈胺基酸密碼子優化為核苷酸、(G4S)3鉸鏈區和序列號為
CAA74660.1的輕鏈胺基酸密碼子優化為核苷酸序列的CD19單鏈抗體的ScFV基因的核苷酸片段,其鹼基序列如SEQ ID NO:1所示。
進一步,所述合成3代CAR結構基因是通過PCR方法獲得編碼CD8鉸鏈區、CD28跨膜區、胞漿區、4-1BB胞漿區和CD3ζ胞漿區的核苷酸片段的CAR結構基因的核苷酸片段,其鹼基序列如SEQ ID NO:2所示。
本發明進一步的目的是通過以下技術方案實現的,一種嵌合抗原受體T細胞的製備方法,包括以下步驟:
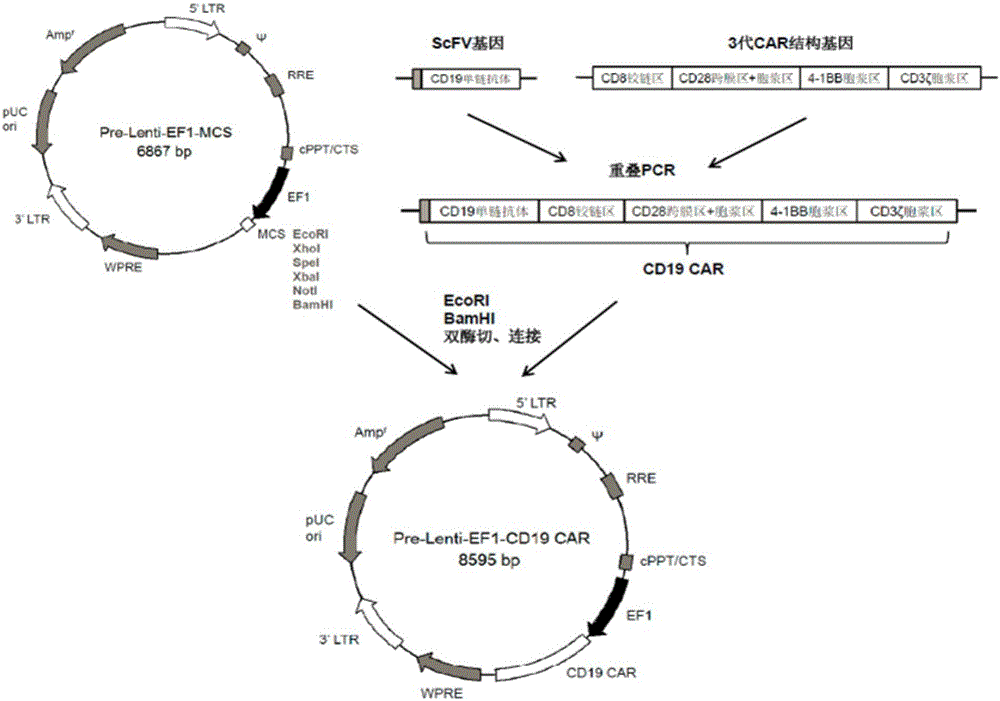
(1)構建3代慢病毒CAR載體:首先將合成ScFV基因或合成3代CAR結構基因分別擴增PCR,得到合成ScFV基因片段的PCR產物和合成3代CAR結構基因片段的PCR產物;然後進行重疊PCR將這兩個基因片段的PCR產物連接在一起,得到3代CAR結構的CD19CAR基因;最後通過Pre-Lenti-EF1-MCS載體對CD19CAR基因酶切,連接,轉化,挑克隆,提質粒,測序,得到序列正確的表達CD19CAR的慢病毒載體Pre-Lenti-EF1-CD19CAR;
(2)包裝CD19CAR慢病毒,感染T細胞,製備得到CART。
進一步,步驟(1)中,用於所述擴增PCR的引物為EcoRI-up序列如SEQ ID NO:4所示和BamHI-down序列如SEQ ID NO:5所示。
進一步,步驟(1)中,用於所述重疊PCR的引物為Middle-R如SEQ ID NO:6所示和Middle-F如SEQ ID NO:7所示。
進一步,步驟(1)中,測序引物為Pre-up-Seq,如SEQ ID NO:8所示和Pre-down-Seq,如SEQ ID NO:9所示。
進一步,步驟(1)中,步驟(1)中,所述雙酶選自EcoRI-HF限制性內切酶和BamHI-HF限制性內切酶。
本發明進一步的目的是通過以下技術方案實現的,一種嵌合抗原受體T細胞在製備抗白血病和淋巴瘤藥物中的應用。
本發明在3代CD19CAR載體的結構中加入了兩種協同刺激信號,構建了慢病毒載體,並在細胞和動物實驗中觀察了三代CD19CART的效果,證實了三代CD19CART能夠有效殺死腫瘤細胞。
附圖說明
通過閱讀下文優選實施方式的詳細描述,各種其他的優點和益處對於本領域普通技術人員將變得清楚明了。附圖僅用於示出優選實施方式的目的,而並不認為是對本發明的限制。而且在整個附圖中,用相同的參考符號表示相同的部件。在附圖中:
圖1為CART載體設計的演化。
圖2為CD19CAR慢病毒載體構建流程圖
圖3為ScFV基因和3代CAR結構基因PCR產物電泳圖。其中,左邊為ScFV基因,中間為Marker(1000,2000,3000,4000,5000,6000,8000,10000bp),右邊為3代CAR結構基因。
圖4為重疊PCR產物電泳圖。其中,左邊為Marker(1000,2000,3000,4000,5000,6000,8000,10000bp),右邊為CD19CAR基因(1728bp)。
圖5為CD19-CART的殺傷效果。
圖6為注射Raji淋巴瘤細胞後分別注射Control或CD19CART兩周後的小鼠肝臟表現。
圖7為小鼠生存曲線。
具體實施方式
下面將參照附圖更詳細地描述本公開的示例性實施方式。雖然附圖中顯示了本公開的示例性實施方式,然而應當理解,可以以各種形式實現本公開而不應被這裡闡述的實施方式所限制。相反,提供這些實施方式是為了能夠更透徹地理解本公開,並且能夠將本公開的範圍完整的傳達給本領域的技術人員。
實施例1:Pre-Lenti-EF1-CD19CAR載體構建
1、合成ScFV基因:通過PCR方法獲得編碼CD8信號肽、序列號CAA74659.1的重鏈胺基酸密碼子優化為核苷酸、(G4S)3鉸鏈區和序列號為CAA74660.1的輕鏈胺基酸密碼子優化為核苷酸序列的CD19單鏈抗體的ScFV基因的核苷酸片段,其鹼基序列如SEQ ID NO:1所示。
2、合成3代CAR結構基因,通過PCR方法獲得編碼CD8鉸鏈區、CD28跨膜區、胞漿區、4-1BB胞漿區和CD3ζ胞漿區的核苷酸片段的CAR結構基因的核苷酸片段,其鹼基序列如SEQ ID NO:2所示。
3、將合成ScFV基因和3代CAR結構基因通過重疊PCR進行拼接,得到CD19CAR基因,如SEQ ID NO:3所示。具體過程如下:
(1)引物設計:使用序列分析軟體pDRAW32分析CD19CAR基因序列,單酶切位點EcoRI、BamHI適合用於基因克隆,能夠和Pre-Lenti-EF1-MCS載體的MCS(多克隆位點)匹配,設計兩端引物如下:
EcoRI-up序列:CGGAATTC GCCACCATGGCCTTACCAGTGACCGC,如SEQ ID NO:4所示;
BamHI-down序列:CGGGATCC TTAGCGAGGGGGCAGGGCCTG,如SEQ ID NO:5所示。用於重疊PCR的引物為:
Middle-R,GTCGTGGTGGGCTTCGCTGGTGAGGAGACGGTGACTGAGG,如SEQ ID NO:6所示。
Middle-F,CCTCAGTCACCGTCTCCTCACCAGCGAAGCCCACCACGAC,如SEQ ID NO:7所示。
(2)PCR重疊延伸:收到合成的基因和引物後,進行PCR重疊延伸。
PCR體系如下(使用Toyobo的KOD Fx酶):
PCR反應程序為:
PCR產物電泳:見圖3,對PCR產物進行凝膠電泳,膠回收(Biomiga,貨號:DC-3511-01),定量PCR片段濃度後,進行重疊PCR。
PCR體系見下:
PCR程序為:
PCR產物電泳:見圖4,PCR產物凝膠電泳,膠回收,進行後續克隆實驗。
(3)酶切:
酶切反應體系如下:
(4)回收酶切後產物:Biomiga膠回收試劑盒(貨號:DC-3511-01)。
(5)連接反應:
根據載體nmole數:片段nmole數=1:3,即
配製連接體系:
上述內容各組分加至1.5mL離心管中,充分混勻;22℃水浴30min;
(5)轉化,塗氨苄平板:冰上將上述連接產物加入50μL感受態中,輕彈,靜置20min;42℃水浴熱激90秒;冰上5min;加500μL LB,37℃復甦1h;4000rpm離心5min,留適量上清液,加樣槍重懸,塗氨苄抗性平板;37℃溫箱過夜。10、挑克隆,搖菌:連接反應時設置一不加連接片段的陰性對照,第二日觀察可見加入CD19CAR片段的平板內克隆數約50個左右,明顯比未加片段的克隆數(10個)多,因此判斷連接成功。隨機挑取6個克隆,搖菌擴增。
(6)質粒提取:Biomiga無內毒素質粒提取試劑盒(貨號:PD1220-02)。
(7)測序:選取濃度較高質粒測序,引物為:
Pre-up-Seq:GGAGCCTACCTAGACTCAGC,如SEQ ID NO:8所示,
Pre-down-Seq:CAACCAGGATTTATACAAGG,如SEQ ID NO:9所示,
測序結果經比對,完全正確,得到了表達CD19CAR基因的慢病毒載體Pre-Lenti-EF1-CD19CAR,結構見圖2。
實施例2:細胞殺傷實驗
1、慢病毒包裝
(1)293T細胞培養於37℃,5%CO2孵箱內,培養基為DMEM/10%FBS。
(2)包裝病毒前一天,胰酶消化293T細胞,1×107細胞/孔種植10cm培養皿。
(3)轉染細胞時,除了Pre-Lenti-EF1-MCS-CD19CAR質粒外,每種質粒還要和包裝質粒psPAX2、pMD2.0G共轉染。其中Pre-Lenti-EF1-MCS-CD19CAR使用5μg,psPAX2使用3.75μg,pMD2.0G使用1.25μg。轉染時,將以上三種質粒的混合物加入500μl opti-MEM培養基內,在另一個微型離心管內將25μl Lipofectamine 2000試劑加入500μl opti-MEM培養基內,然後將稀釋的轉染試劑逐滴加入稀釋的質粒上方,混勻,離心,室溫靜置20min,最後將質粒和轉染試劑的混合物加入10cm培養皿內,輕晃、混勻,放入孵箱。
(4)細胞轉染3天後,可以收穫病毒,將10ml含病毒培養基轉入50ml離心管內,4℃,1250rpm,5min,去除漂浮死亡的293T細胞,然後將含病毒培養基過濾,濃縮,分裝,-80℃凍存,和留存部分病毒測定滴度。
2、淋巴細胞分離
(1)抽血:在無菌的條件下抽取人體的靜脈血10ml。
(2)稀釋:將獲得的血液用相同體積的1640培養基10ml稀釋。
(3)在離心管中加入10ml人淋巴細胞分離液(達科為生物工程有限公司)。
(4)用電動移液槍將血液貼壁緩慢加入離心管中。
(5)將離心管放入離心機中,以700g,22℃離心25min。
(6)離心結束後,淋巴細胞在上層血漿層和分離液之間的白膜層中。
(7)用84滴管儘量將白膜層吸到另一支離心管中(加入30ml 1640培養基),注意不要吸到分離液。
(8)250g,22℃,10分鐘。
(9)棄掉上層液體,用含IL2、滅活血清的1640培養基重懸,計數。
3、T細胞純化
(1)淋巴細胞計數,取1x107個淋巴細胞於微型離心管中。
(2)250g,22℃,10分鐘。
(3)棄掉上層液體,80μL磁珠分離緩衝液重懸細胞沉澱,加入20μl的CD3MicroBeads(美天旎)。
(4)4℃冰箱中放置1小時,保證充分結合。
(5)1小時後,在微型離心管中加入1mL的磁珠分離緩衝液,250g,5℃離心10分鐘。期間準備過濾柱子,將過濾柱安放在磁鐵上,用500μl的緩衝液潤洗(緩衝液隨著重力留下)。
(6)離心後細胞棄上清,500μl的緩衝液重懸,加入柱子,緩衝液隨著重力向下,細胞懸液流出後,柱子用500μl的緩衝液洗四次。
(7)將柱子從磁鐵上卸掉,用1mL緩衝液將T細胞衝出,至1ml離心管。
(8)250g,5℃離心10分鐘。
(9)含IL2、含滅活血清的1640培養基重懸,計數。
4、T細胞慢病毒感染
(1)純化T計數,2×106個T細胞/孔(6孔板)種植,培養過夜後,加入MOI為2的對照病毒液(空載體包裝,Control)和Pre-Lenti-EF1-MCS-CD19CAR病毒液,感染過夜。
(2)感染第二天,補加1ml新鮮培養基。
(3)感染第三天,T細胞已充分活化,增殖旺盛,此時將T細胞轉入25cm 2培養瓶。
(4)感染5天後,進行殺傷實驗。
5、殺傷實驗
計數表達CD19分子的K562細胞(K562-CD19,通過慢病毒感染的方法建立的穩定細胞系),1×104個K562-CD19細胞/孔(96孔板);計數病毒感染的T細胞(Control病毒液感染的Control T細胞和Pre-Lenti-EF1-MCS-CD19CAR病毒液感染的CD19CAR-T細胞),按照效靶比10:1,5:1,2.5:1的比例加入K562-CD19細胞上層,實驗設計見表1。
表1.殺傷實驗設計表(靶細胞:K562.CD19)
6、殺傷測量:通過測量死亡細胞釋放入細胞培養上清的LDH,來確定CAR-T細胞殺死K562-CD19靶細胞的效果。
(1)操作按照Promega試劑盒說明書(CytoTox 96非放射性細胞毒性檢測,貨號:G1780)。
(2)步驟5中殺傷實驗孵育過夜,約18h後,最大釋放孔加入10×細胞裂解液。
(3)2小時後,每孔取50μl上清,再加入50μl LDH酶底物,室溫靜置20分鐘後,酶標儀測量492nm處吸光度OD492。
(4)殺傷率計算,計算公式為
實驗孔為不同效靶比得到的OD492,效應細胞自發為Control T細胞或CD19CAR-T細胞的OD492,靶細胞自發為K562-CD19最小釋放,靶細胞最大為K562-CD19最大釋放。計算得到的殺傷率見圖5,靶細胞為K562表達CD19的細胞,效應細胞為對照(Control)T細胞和CD19-CART細胞,從圖5可知,CD19-CART細胞可以特異性殺傷表達CD19的K562細胞,表明Pre-Lenti-EF1-MCS-CD19CAR-T構建成功。
實施例3:動物實驗
1、小鼠品系:為NSG免疫缺陷小鼠品系(缺乏T細胞、B細胞和NK細胞功能)。2、腫瘤接種:採用Raji淋巴瘤細胞系,1x106細胞/200ul PBS尾靜脈注射(6隻小鼠)。
3、CART注射:Raji腫瘤細胞接種2天後,尾靜脈注射Control或CD19CART細胞(1x107細胞/200ul PBS,一組3隻小鼠),見圖6。由圖6可知,對照CART不能有效抑制淋巴瘤細胞在肝臟的生長(白色斑塊為淋巴瘤細胞形成的腫瘤),CD19CART能有效抑制淋巴瘤。
4、每隔2天觀察,測量小鼠體重,直至CART細胞注射2周後,對照組(Control)小鼠開始出現後肢癱瘓,陸續死亡,解剖觀察,記錄死亡時間,整理生存曲線,見圖7。由圖7可知,CD19CART明顯延長了小鼠生存時間。
以上所述,僅為本發明較佳的具體實施方式,但本發明的保護範圍並不局限於此,任何熟悉本技術領域的技術人員在本發明揭露的技術範圍內,可輕易想到的變化或替換,都應涵蓋在本發明的保護範圍之內。因此,本發明的保護範圍應以所述權利要求的保護範圍為準。
SEQUENCE LISTING
北京普瑞金科技有限公司
一種嵌合抗原受體T細胞及其製備方法與應用
2016
9
PatentIn version 3.5
1
789
DNA
ScFV基因
1
atggccttac cagtgaccgc cttgctcctg ccgctggcct tgctgctcca cgccgccagg 60
ccggacatcc agatgacaca gactacatcc tccctgtctg cctctctggg agacagagtc 120
accatcagtt gcagggcaag tcaggacatt agtaaatatt taaattggta tcagcagaaa 180
ccagatggaa ctgttaaact cctgatctac catacatcaa gattacactc aggagtccca 240
tcaaggttca gtggcagtgg gtctggaaca gattattctc tcaccattag caacctggag 300
caagaagata ttgccactta cttttgccaa cagggtaata cgcttccgta cacgttcgga 360
ggggggacca agctggagat cacaggtggc ggtggctcgg gcggtggtgg gtcgggtggc 420
ggcggatctg aggtgaaact gcaggagtca ggacctggcc tggtggcgcc ctcacagagc 480
ctgtccgtca catgcactgt ctcaggggtc tcattacccg actatggtgt aagctggatt 540
cgccagcctc cacgaaaggg tctggagtgg ctgggagtaa tatggggtag tgaaaccaca 600
tactataatt cagctctcaa atccagactg accatcatca aggacaactc caagagccaa 660
gttttcttaa aaatgaacag tctgcaaact gatgacacag ccatttacta ctgtgccaaa 720
cattattact acggtggtag ctatgctatg gactactggg gccaaggaac ctcagtcacc 780
gtctcctca 789
2
939
DNA
CAR結構基因
2
ccagcgaagc ccaccacgac gccagcgccg cgaccaccaa caccggcgcc caccatcgcg 60
tcgcagcccc tgtccctgcg cccagaggcg tgccggccag cggcgggggg cgcagtgcac 120
acgagggggc tggacttcgc cccacgcaaa attgaagtta tgtatcctcc tccttaccta 180
gacaatgaga agagcaatgg aaccattatc catgtgaaag ggaaacacct ttgtccaagt 240
cccctatttc ccggaccttc taagcccttt tgggtgctgg tggtggttgg tggagtcctg 300
gcttgctata gcttgctagt aacagtggcc tttattattt tctgggtgag gagtaagagg 360
agcaggctcc tgcacagtga ctacatgaac atgactcccc gccgccccgg gcccacccgc 420
aagcattacc agccctatgc cccaccacgc gacttcgcag cctatcgctc caaacggggc 480
agaaagaaac tcctgtatat attcaaacaa ccatttatga gaccagtaca aactactcaa 540
gaggaagatg gctgtagctg ccgatttcca gaagaagaag aaggaggatg tgaactgaga 600
gtgaagttca gcaggagcgc agacgccccc gcgtaccagc agggccagaa ccagctctat 660
aacgagctca atctaggacg aagagaggag tacgatgttt tggacaagag acgtggccgg 720
gaccctgaga tggggggaaa gccgcagaga aggaagaacc ctcaggaagg cctgtacaat 780
gaactgcaga aagataagat ggcggaggcc tacagtgaga ttgggatgaa aggcgagcgc 840
cggaggggca aggggcacga tggcctttac cagggtctca gtacagccac caaggacacc 900
tacgacgccc ttcacatgca ggccctgccc cctcgctaa 939
3
1728
DNA
CD19 CAR基因
3
atggccttac cagtgaccgc cttgctcctg ccgctggcct tgctgctcca cgccgccagg 60
ccggacatcc agatgacaca gactacatcc tccctgtctg cctctctggg agacagagtc 120
accatcagtt gcagggcaag tcaggacatt agtaaatatt taaattggta tcagcagaaa 180
ccagatggaa ctgttaaact cctgatctac catacatcaa gattacactc aggagtccca 240
tcaaggttca gtggcagtgg gtctggaaca gattattctc tcaccattag caacctggag 300
caagaagata ttgccactta cttttgccaa cagggtaata cgcttccgta cacgttcgga 360
ggggggacca agctggagat cacaggtggc ggtggctcgg gcggtggtgg gtcgggtggc 420
ggcggatctg aggtgaaact gcaggagtca ggacctggcc tggtggcgcc ctcacagagc 480
ctgtccgtca catgcactgt ctcaggggtc tcattacccg actatggtgt aagctggatt 540
cgccagcctc cacgaaaggg tctggagtgg ctgggagtaa tatggggtag tgaaaccaca 600
tactataatt cagctctcaa atccagactg accatcatca aggacaactc caagagccaa 660
gttttcttaa aaatgaacag tctgcaaact gatgacacag ccatttacta ctgtgccaaa 720
cattattact acggtggtag ctatgctatg gactactggg gccaaggaac ctcagtcacc 780
gtctcctcac cagcgaagcc caccacgacg ccagcgccgc gaccaccaac accggcgccc 840
accatcgcgt cgcagcccct gtccctgcgc ccagaggcgt gccggccagc ggcggggggc 900
gcagtgcaca cgagggggct ggacttcgcc ccacgcaaaa ttgaagttat gtatcctcct 960
ccttacctag acaatgagaa gagcaatgga accattatcc atgtgaaagg gaaacacctt 1020
tgtccaagtc ccctatttcc cggaccttct aagccctttt gggtgctggt ggtggttggt 1080
ggagtcctgg cttgctatag cttgctagta acagtggcct ttattatttt ctgggtgagg 1140
agtaagagga gcaggctcct gcacagtgac tacatgaaca tgactccccg ccgccccggg 1200
cccacccgca agcattacca gccctatgcc ccaccacgcg acttcgcagc ctatcgctcc 1260
aaacggggca gaaagaaact cctgtatata ttcaaacaac catttatgag accagtacaa 1320
actactcaag aggaagatgg ctgtagctgc cgatttccag aagaagaaga aggaggatgt 1380
gaactgagag tgaagttcag caggagcgca gacgcccccg cgtaccagca gggccagaac 1440
cagctctata acgagctcaa tctaggacga agagaggagt acgatgtttt ggacaagaga 1500
cgtggccggg accctgagat ggggggaaag ccgcagagaa ggaagaaccc tcaggaaggc 1560
ctgtacaatg aactgcagaa agataagatg gcggaggcct acagtgagat tgggatgaaa 1620
ggcgagcgcc ggaggggcaa ggggcacgat ggcctttacc agggtctcag tacagccacc 1680
aaggacacct acgacgccct tcacatgcag gccctgcccc ctcgctaa 1728
4
34
DNA
人工合成
4
cggaattcgc caccatggcc ttaccagtga ccgc 34
5
29
DNA
人工合成
5
cgggatcctt agcgaggggg cagggcctg 29
6
40
DNA
人工合成
6
gtcgtggtgg gcttcgctgg tgaggagacg gtgactgagg 40
7
40
DNA
人工合成
7
cctcagtcac cgtctcctca ccagcgaagc ccaccacgac 40
8
20
DNA
人工合成
8
ggagcctacc tagactcagc 20
9
20
DNA
人工合成
9
caaccaggat ttatacaagg 20
