聚乙二醇化包裹聚多巴胺載藥磁性納米顆粒的製備方法與流程
2023-05-29 16:19:06 2
本發明涉及化學藥物領域,具體涉及具有靶向作用及協同療法的聚乙二醇化包裹多巴胺的載藥磁性納米顆粒製備與用途。
背景技術:
阿黴素(doxorubicin,dox,別稱:多柔比星;亞法裡亞黴素等,化學結構式:c27h29no11,cas號:23214-92-8,相對分子量:543.52)是由波賽鏈黴菌青灰亞種產生的一種蒽環類抗腫瘤抗生素,是細胞周期非特異性藥物(ccnsa),對s及m期較敏感。鹽酸鹽為橘紅色針狀結晶。熔點204~205℃。易溶於水、乙醇、甲醇。是從放線菌屬培養液中分離出的一種抗腫瘤抗生素。作用機制與柔紅黴素相似,其抗瘤譜較廣,治療指數較高。臨床應用於急、慢性淋巴細胞白血病及實體性腫瘤白血病、淋巴瘤、乳腺癌、卵巢癌、軟組織肉瘤、成骨肉瘤、橫紋肌肉瘤、尤文氏肉瘤、腎母細胞瘤、神經母細胞癌、胃癌、胰腺癌、肝癌、前列腺癌、頭頸部鱗癌、睪丸癌、肺癌、膀胱癌、甲狀腺髓樣癌和肉瘤的治療。
光熱治療是一種純物理治療方法。主要利用物理能量對人體進行整體或局部加熱,通過產熱量使得腫瘤組織區域的溫度上升到有效治療溫度,並維持一段時間,從而改變腫瘤細胞所處的微環境,抑制腫瘤血管形成和腫瘤細胞轉移,並使其調亡、壞死,最終達到治療腫瘤的目的。多巴胺(da)是一種典型的神經遞質,在大腦中自然存在,在鹼性條件下可以自發聚合成聚多巴胺(pda),而不需要額外的氧化劑。pda具有優良的生物相容性和生物可降解性,在實際應用中可防止長期毒性。最重要的是pda具有顯著的光熱轉換效率,具有出色的光熱穩定性,這表明有很大的潛力作為近紅外驅動的光熱製劑。然而,單一的治療方法很難徹底的消滅腫瘤細胞,因此,由於協同作用,光熱療法與化療的結合很有希望獲得一種增強的抗腫瘤功效。
為了進一步提高治療效果和減少不良副作用,針對腫瘤部位的特異性靶向作用也極具吸引性。磁靶向技術是一種已被證實的技術,可以將納米複合材料傳送到由外部磁場引導的腫瘤區域。超順磁性fe3o4納米粒子被廣泛應用於各種藥物的磁性運輸,以到達單個腫瘤細胞。因此,從pda、fe3o4和dox合成的納米複合材料被認為是一個用於臨床應用很有前景的藥物遞送平臺。
技術實現要素:
由於目前用於治療腫瘤的藥物遞送載體其作用單一,生物相容性、降解性較差,本發明旨在合成一種具有較好生物相容性和可降解性同時又能在磁靶向的作用下結合傳統化療方法和光熱療法的新型藥物遞送平臺。
本發明的技術方案具體如下:
聚乙二醇化包裹聚多巴胺載藥磁性納米顆粒,製備方法包括以下步驟:
(1)將二價鐵鹽和三價鐵鹽溶於去離子水中,加入濃鹽酸;
(2)將步驟(1)得到的混合溶液逐滴加到氫氧化鈉溶液中攪拌半個小時,用一塊強磁鐵磁性分離得到的四氧化三鐵磁性納米顆粒,用去離子水洗滌三次;
(3)將步驟(2)所得到的四氧化三鐵磁性納米顆粒分散在三羥甲基氨基甲烷(tris)緩衝溶液中,加入鹽酸多巴胺,在室溫下機械攪拌12小時,磁鐵分離,用去離子水洗滌,得到多巴胺包裹的磁性納米顆粒(fe3o4@pda);
(4)將步驟(3)得到的fe3o4@pda納米顆粒分散在去離子水中得到fe3o4@pda納米顆粒懸浮液,將硫醇聚乙二醇加入到fe3o4@pda納米顆粒懸浮液中,攪拌5min後加入氨水繼續攪拌一個小時,磁鐵磁性分離洗滌三次,得到聚乙二醇化包裹多巴胺的磁性納米顆粒(fe3o4@pda/peg);
(5)將步驟(4)得到的fe3o4@pda/peg磁性納米顆粒分散在磷酸鹽緩衝溶液中,加入鹽酸阿黴素,避光下攪拌6h,磁鐵磁性分離用去離子水洗滌三次。
進一步的,所述步驟(1)中的二價鐵鹽為七水合硫酸亞鐵、氯化亞鐵的一種或幾種;所述步驟(1)中的三價鐵鹽是六水合三氯化鐵、硫酸鐵的一種或幾種;所述步驟(1)中的二價鐵鹽與三價鐵鹽的摩爾比是1:1-1:3;所述步驟(1)中的濃鹽酸摩爾濃度為12m,並與鐵離子摩爾比為1:1-1:2。
進一步的,所述步驟(2)中的氫氧化鈉溶液摩爾濃度為1.5m,體積為50ml。
進一步的,所述步驟(3)中的tris緩衝溶液ph=8.5,摩爾濃度為10mm;所述步驟(3)中的四氧化三鐵磁性納米顆粒濃度為2mg/ml,多巴胺濃度為2-4mg/ml。
進一步的,所述步驟(4)中的fe3o4@pda納米顆粒與硫醇聚乙二醇質量比為1:2-1:3;氨水質量分數為28-30%,在整個體系中體積分數為0.5%。
進一步的,所述步驟(5)中的磷酸鹽緩衝溶液摩爾濃度為20mm,ph=8;所述步驟(5)中的fe3o4@pda/peg磁性納米顆粒濃度為1mg/ml;所述步驟(5)中的fe3o4@pda/peg磁性納米顆粒與阿黴素質量比為1:2-1:3。
本發明主要優點有:
針對目前納米藥物載體存在的問題,本項目創造性地提出能夠實現多種治療方法協同治療同時又具有較好生物相容性及靶向性的納米藥物遞送平臺。本項目中,四氧化三鐵具有磁靶向功能,pda用於光熱治療,peg能顯著提高納米遞送系統的生物相容性,整個納米藥物遞送系統能有效提高治療效果,解決納米遞送系統的靶向性和協同性等問題,推動腫瘤的高效治療。
附圖說明
為了使本發明的目的、技術方案和有益效果更加清楚,本發明提供如下附圖。
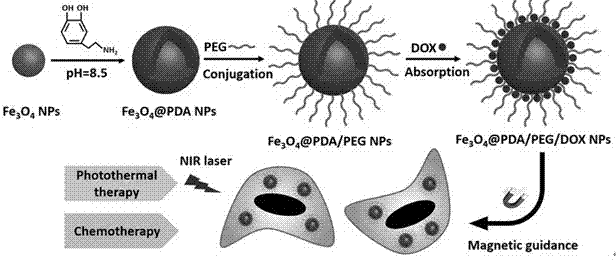
圖1為本發明實施例1磁性複合納米顆粒(fe3o4@pda/peg/dox)的合成示意圖。
圖2為本發明實施例1中磁性複合納米顆粒紅外圖。
圖3為本發明實施例1中磁性複合納米顆粒的tem圖。
圖4為本發明實施例1中fe3o4及fe3o4@pda/peg/dox磁性複合納米顆粒298k的磁化曲線圖。
圖5為本發明實施例1中磁性複合納米顆粒對hela癌細胞24h的體外毒性圖。
圖6為本發明實施例1中磁性複合納米顆粒對hela癌細胞48h的體外毒性圖。
具體實施方式
以下實施例用於說明本發明,但不用來限制本發明的範圍。
實施例1製備聚乙二醇化包裹聚多巴胺的載藥磁性納米顆粒
(1)fe3o4@pda磁性複合材料的製備:將0.556g七水合硫酸亞鐵和1.04g六水合三氯化鐵溶於5ml去離子水中,加入0.17ml濃鹽酸,將混合溶液逐滴加到50ml1.5m氫氧化鈉溶液中80℃氮氣保護下劇烈攪拌半個小時,自然冷卻到室溫後磁性分離用去離子水洗滌3遍,將fe3o4納米顆粒分散在ph=8.5,10mm三羥甲基氨基甲烷緩衝液中,室溫下機械攪拌12小時,磁性分離,用去離子水洗滌三遍。
(2)peg化的fe3o4@pda的製備:將100mg硫醇聚乙二醇加入到40ml1mg/mlfe3o4@pda納米顆粒懸浮液中,攪拌5分鐘後加入0.2ml氨水(28-30%)繼續攪拌一個小時,磁性分離後用去離子水洗滌幾遍。
(3)fe3o4@pda/peg/dox的製備:將20mg鹽酸阿黴素加入到20ml1mg/ml的fe3o4@pda/peg磷酸鹽緩衝溶液中(ph=8,20×10−3m),避光條件下攪拌6小時後,磁性分離用去離子水洗滌3遍。其紅外光譜見圖2,結果顯示fe3o4、pda、peg、dox的特徵峰在fe3o4@pda/peg/dox上均存在,說明fe3o4@pda/peg/dox已成功的合成。其透射電鏡(tem)見圖3,tem結果顯示納米顆粒直徑約為16.2±2.6nm。圖5、圖6分別是所得納米顆粒對hela腫瘤細胞24h和48h的體外毒性示意圖,顯示隨著時間的增加(從24小時到48小時),對hela腫瘤細胞的毒性一直持續增加。
最後說明的是,以上優選實施例僅用以說明本發明的技術方案而非限制,儘管通過上述優選實施例已經對本發明進行了詳細的描述,但本領域技術人員應當理解,可以在形式上和細節上對其做出各種各樣的改變,而不偏離本發明權利要求書所限定的範圍。
