一種十四面體形納米鎳錳酸鋰的製備方法與流程
2023-06-05 11:25:31 3
本發明涉及一種用作電池正極材料的鎳錳酸鋰的製備方法,特別是涉及一種十四面體形的納米鎳錳酸鋰的製備方法。
背景技術:
近年來,各種電子設備飛速發展,對於電池的要求越來越高,而鋰離子電池被視作最好的新型能源,大到電動汽車,小到筆記本、手機,都離不開鋰電池。
錳酸鋰(LiMn2O4)由於具有電壓高、價格低廉、資源豐富、與環境友好等特點,成為最有前途的鋰離子電池正極材料之一,得到廣泛的研究與應用。但是錳酸鋰在循環過程中容量有較大的衰減,嚴重阻礙了其商業化的應用。經研究發現,影響錳酸鋰的容量衰減的因素主要在於:(1)相結構的純度及穩定性、微觀形貌的不規則;(2)材料在深度放電時產生Jahn-Teller效應;(3)錳酸鋰在充放電時容易發生歧化反應,產生三價錳離子溶解到電解液中等。
相比於LiFePO4、LiCoO2等正極材料,錳酸鋰由於原材料豐富,價格優勢明顯,並且其製備工藝相對簡單,安全性能高。因此,目前對該材料的研究只要集中在摻雜改性等方面,以提高其循環性能。其中,用Fe、Co、Ni、Zn等金屬摻雜以穩定尖晶石結構、提高循環性能是較為有效的方法。
目前,合成鎳錳酸鋰的方法主要有高溫固相法、共沉澱法、溶膠凝膠法等、噴霧乾燥法等。其中,利用共沉澱法製備得到的鎳錳酸鋰電化學性能指標較好,但是在製備過程中難以實現分子水平的均勻混合,一定程度上影響到其電化學性能。
作為電池正極材料,鎳錳酸鋰的電化學性能與錳離子的價態(+3價和+4價)、Mn/Ni比例、顆粒形貌、表面位面、表面組成等相關。
納米材料是近年來研究的熱點,納米正極材料具有大的比表面積,增大了材料與電解液的接觸程度,小粒徑也縮短了鋰離子固相擴散的路徑,都有利於提高材料的功率密度。另外,不同的形貌以及結晶度及規則程度,也會對電化學性能帶來較大的影響,規則的微粒可以減小團聚和粒子架橋現象,降低顆粒堆積填充時的粒子鹼洗,進而有利於鋰離子電池比容量的提高。
技術實現要素:
本發明的目的在於提供一種十四面體形的納米鎳錳酸鋰,作為鋰離子電池正極材料時,由於其獨特的形貌而有助於提高電池的功率密度和電池比容量。
本發明的目的通過以下技術方案實現:
一種十四面體形納米鎳錳酸鋰的製備方法,其特徵在於,包括如下步驟:
(1)微波法製備晶種:將可溶性鋰化合物、可溶性鎳化合物和可溶性錳化合物分別溶解於去離子水中,形成濃度均為0.05-0.07mol/L的鋰離子溶液、鎳離子溶液和錳離子溶液,然後按照鋰離子、鎳離子和錳離子的摩爾比為1∶x∶(2-x)的比例將三種溶液混合併攪拌均勻,然後再加入濃度為0.1mol/L的尿素水溶液,攪拌10-30min得到混合溶液,將上述混合溶液經微波加熱,得到晶種溶液;其中,微波加熱功率為5kW,頻率為2450MHz,時間為2~5分鐘,尿素與鋰離子的摩爾比為6-8∶1;
(2)鎳錳酸鋰的製備:將可溶性鋰化合物、可溶性鎳化合物和可溶性錳化合物分別溶解於去離子水中,形成濃度均為0.1-0.3mol/L的鋰離子溶液、鎳離子溶液和錳離子溶液,然後按照鋰離子、鎳離子和錳離子的摩爾比為1∶x∶(2-x)的比例將三種溶液混合併攪拌均勻,再加入步驟(1)得到的晶種溶液充分攪拌至混合均勻,最後再加入0.2mol/L的胺基酸水溶液,將得到的混合反應物放入水熱反應釜中在120-160℃下水熱反應2~3h,取出反應產物,過濾,洗滌,並在50-60℃下乾燥,得到十四面體形納米鎳錳酸鋰;
其中,步驟(1)和(2)中所述的可溶性鋰化合物為硝酸鋰或醋酸鋰、所述的可溶性鎳化合物為硝酸鎳或醋酸鎳,所述的可溶性錳化合物為硝酸錳或醋酸錳,0.3≤x≤0.7;步驟(2)中所述的胺基酸溶液為L-精氨酸水溶液或L-賴氨酸水溶液,L-精氨酸或L-賴氨酸與鋰離子的摩爾比為7-10∶1。
本發明公開的鎳錳酸鋰的製備方法,通過兩步法製備得產物,其原理如下:
第一步為晶種的製備,即對製備好的反應原料採用微波的方法進行加熱得到顆粒細小的晶種。由於選用的微波加熱設備頻率為2450MHz,原料中的極性分子在其作用下每秒鐘變換方向2.45×109次,分子來迴轉動,與周圍分子相互碰撞摩擦,迅速升溫,原料中的尿素作為沉澱劑釋放出OH-,與鋰離子和鎳離子、錳離子快速反應得到晶種,另一方面,由於微波加熱的均勻性並通過控制反應時間以及反應原料的濃度,有效地避免了晶種的長大,得到大量細小的鎳錳酸鋰晶種顆粒。
第二步為納米鎳錳酸鋰產物的製備,即利用上一步驟中得到的晶種,與反應原料混合,在常規的水熱反應釜中進行反應,得到產物十四面體形的納米鎳錳酸鋰。該步驟在大量細小的晶種作為生長基點的基礎上,通過傳統的水熱法,將原料鋰離子、鎳離子和錳離子反應,得到產物納米級的鎳錳酸鋰,其粒徑分布均勻。該步驟中,將鋰離子和錳離子的濃度適當提高,加快其反應與晶體生長速度,而水溶性的胺基酸L-精氨酸或L-賴氨酸一方面作為具有緩釋效果的沉澱劑保證反應的進行,另一方面,L-精氨酸或L-賴氨酸也作為軟模板劑,促進鎳錳酸鋰晶體結構的發育,形成十四面體形。至於得到十四面體形的機理,發明人猜測可能是由於L-精氨酸或L-賴氨酸的位阻效應,或者是由於其上的基團,如-COOH、-NH2,與水中氫鍵、範德華力,共同促進納米鎳錳酸鋰的組裝與成形。
本發明得到的十四面體形納米鎳錳酸鋰作為鋰離子電池正極材料,由於其特殊的形貌對離子擴散的影響以及對顆粒堆積的影響,提高了功率密度和電池比容量,具有廣闊的應用前景。
附圖說明
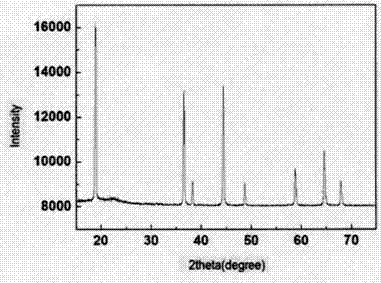
圖1是實施例1得到的十四面體形納米鎳錳酸鋰的XRD圖;
圖2是實施例1得到的十四面體形納米鎳錳酸鋰的SEM圖。
具體實施方式
以下為本發明的具體實施方式,用以對本發明進行解釋和說明。
實施例1
一種十四面體形納米鎳錳酸鋰的製備方法,其特徵在於,包括如下步驟:
(1)微波法製備晶種:將硝酸鋰、硝酸鎳和醋酸錳分別溶解於去離子水中,形成濃度均為0.05mol/L的鋰離子溶液、鎳離子溶液和錳離子溶液,然後按照鋰離子、鎳離子和錳離子的摩爾比為1∶0.5∶1.5的比例將三種溶液混合併攪拌均勻,然後再加入濃度為0.1mol/L的尿素水溶液,攪拌30min得到混合溶液,將上述混合溶液經微波加熱,得到晶種溶液;其中,微波加熱功率為5kW,頻率為2450MHz,時間為5分鐘,尿素與鋰離子的摩爾比為6∶1;
(2)鎳錳酸鋰的製備:將硝酸鋰、醋酸鎳和醋酸錳分別溶解於去離子水中,形成濃度均為0.1mol/L的鋰離子溶液、鎳離子溶液和錳離子溶液,然後按照鋰離子、鎳離子和錳離子的摩爾比為1∶0.5∶1.5的比例將三種溶液混合併攪拌均勻,再加入步驟(1)得到的晶種溶液充分攪拌至混合均勻,最後再按照L-賴氨酸與鋰離子的摩爾比為8∶1,加入0.2mol/L的L-賴氨酸水溶液,將得到的混合反應物放入水熱反應釜中在160℃下水熱反應2h,取出反應產物,過濾,洗滌,並在60℃下乾燥,得到十四面體形納米鎳錳酸鋰LiNi0.5Mn1.5O4。
圖1和2分別為製備出的十四面體形納米鎳錳酸鋰的XRD和SEM圖,從中可以確定,製備出的產物為鎳錳酸鋰LiNi0.5Mn1.5O4晶體,晶粒尺寸分布均勻,形貌統一。
實施例2
一種十四面體形納米鎳錳酸鋰的製備方法,其特徵在於,包括如下步驟:
(1)微波法製備晶種:將醋酸鋰、醋酸鎳和醋酸錳分別溶解於去離子水中,形成濃度均為0.07mol/L的鋰離子溶液、鎳離子溶液和錳離子溶液,然後按照鋰離子、鎳離子和錳離子的摩爾比為1∶0.3∶1.7的比例將三種溶液混合併攪拌均勻,然後再加入濃度為0.1mol/L的尿素水溶液,攪拌30min得到混合溶液,將上述混合溶液經微波加熱,得到晶種溶液;其中,微波加熱功率為5kW,頻率為2450MHz,時間為2分鐘,尿素與鋰離子的摩爾比為8∶1;
(2)鎳錳酸鋰的製備:將醋酸鋰、醋酸鎳和醋酸錳分別溶解於去離子水中,形成濃度均為0.3mol/L的鋰離子溶液、鎳離子溶液和錳離子溶液,然後按照鋰離子、鎳離子和錳離子的摩爾比為1∶0.3∶1.7的比例將三種溶液混合併攪拌均勻,再加入步驟(1)得到的晶種溶液充分攪拌至混合均勻,最後再按照L-精氨酸與鋰離子的摩爾比為10∶1,加入0.2mol/L的L-精氨酸水溶液,將得到的混合反應物放入水熱反應釜中在120℃下水熱反應3h,取出反應產物,過濾,洗滌,並在50℃下乾燥,得到十四面體形納米鎳錳酸鋰LiNi0.3Mn1.7O4。
