基於計算流體力學優化的個體化自體組織工程補片的製作方法
2023-06-18 20:27:57 2
本發明涉及醫療器械技術領域,具體地說,是基於計算流體力學優化的個體化自體組織工程補片。
背景技術:
補片是心臟外科,尤其是小兒心臟外科的重要手術材料。補片不僅可用於血管成型(血管補片),也可用作心內分割板障。臨床上常用的補片包括自體心包補片、牛心包補片或Gore-Tex補片。儘管目前這些補片仍然具有極普遍的使用性,但依然存在不同的缺點:新鮮的自體心包補片極柔軟易皺褶,力學強度差,常需要在術中用0.6%戊二醛交聯固定;但處理後的心包易鈣化,同時將失去組織活性。異種心包補片,如牛心包補片,雖然來源廣泛,但同樣需經過交聯劑處理,也容易引發機體對異種組織的排斥反應,最終出現嚴重鈣化。Gore-Tex補片的缺點類似其血管制品,且不具有組織活性。因此,構建新型自體血管補片具有必要性。本發明的目的之一,即製備一種具有自體細胞和生物活性的組織工程補片。
然而,一種優良的組織工程血管補片並不是組織工程血管的簡化——血管補片在用於狹窄血管的補片擴大後,需要協同周圍自體血管,長期穩定地發揮生理功能。因此,在構建組織工程血管補片時,還要求個體化設計出補片的三維形態,使其整合到原有血管段後,能相互配合併發揮出最優化的血流特性。
以法洛四聯症(ToF)右室流出道補片擴大術為例,補片植入後的肺動脈形態對患兒術後肺動脈發育具有直接的影響:ToF伴左右肺動脈分支狹窄的患兒,直接補片擴大左右肺動脈並不利於術後肺分支血管的發育。相反,通過合理的肺動脈總幹補片擴大,使肺血流恢復正常後,發育不良的肺分支血管可恢復其生長潛能。在實際臨床應用中,肺動脈跨瓣補片擴大術是糾治ToF患兒肺動脈瓣狹窄的常用方法,然而,肺動脈補片的裁剪、縫合依靠手術醫生長期的手術經驗和術中對患兒肺動脈解剖的判斷,標準的補片成型方法有利於提高患兒中遠期預後。因此,本發明的另一個目的,是結合一種科學的分析、評價手段,在術前即針對患者的個體特徵,找到最佳的補片形態和手術植入方法。
計算流體力學(computational fluid dynamics,CFD)是利用數字分析和算法來分析、解決流體相關問題的的科學。通過傳統的影像數據(CT、MRI)以及心臟都卜勒超聲數據,我們可以重建出符合患者肺動脈解剖的三維圖形,並模擬每次心臟搏動肺動脈管腔中的血流速度等指標。已有研究證實CFD在個體化ToF術前規劃中具有參考價值。因此,本發明中,我們主要結合計算流體技術,通過設計得到血流最優化的補片形態和植入方法,製備出個體化的、具有特定三維形態的自體組織工程補片。
中國專利文獻CN103860291A公開了一種法洛氏四聯症室間隔缺損補片的製作方法,包括以下步驟:1)製作三維實體模型:採集心臟數據後,用後處理工作站對原始數據進行數位化三維重建,獲得心臟外形三維圖像,並採用外科手術進路方式於右心室游離壁進一步切割,獲得室間隔缺損三維圖像;然後將所述兩個圖象通過數控轉換,生成STL格式文件;接著將該STL數據輸入選擇性雷射燒結成型設備中,進行燒結成型,製作帶有室間隔缺損的心臟1:1的三維實體模型;2)製作補片:在上述製得的三維實體模型上對照室間隔缺損形狀裁剪出手術補片。但是關於本發明的基於計算流體力學優化的個體化自體組織工程補片目前還未見報導。
技術實現要素:
本發明的目的是針對現有技術中的不足,提供一種基於計算流體力學優化的個體化自體組織工程補片及其製備方法。
為實現上述目的,本發明採取的技術方案是:一種基於計算流體力學優化的組織工程血管補片的製備方法,所述的製備方法包括以下步驟:
1)通過計算流體力學優化(和虛擬手術)設計血管補片;
2)將計算流體力學優化的設計模型製備出來,以製備的模型為內核,將電紡絲包裹於模型表面,然後進行組織工程構建,撤去模型即獲得有自體細胞和組織的血管補片。
步驟1)為:以心血管影像數據對血管進行三維重建,設計不同的血管補片,在計算機系統進行虛擬手術規劃,通過流體力學分析選擇最佳的血管補片。或直接通過計算流體力學分析生成最佳的補片設計。
血管三維重建的方法為:術前獲取患者心血管影像圖像,通過醫學圖像三維重建軟體標記每層圖像中肺動脈的位置,重建後獲得肺動脈三維圖像;直接重建出的圖像表面粗糙,在儘量減少處理對圖像精確度帶來損失的前提下,對肺動脈表面作光滑處理,完成肺動脈的三維重建。
所述的心血管影像圖像為MRI、CT或三維超聲。
根據臨床經驗公式設計血管補片,並以臨床經驗公式設計的血管補片為基礎進一步設計不同的血管補片。
計算流體力學優化的設計模型通過3D列印製得。
所述的電紡絲為聚己內酯電紡絲。
所述的聚己內酯電紡絲由聚己內酯的三氟乙醇溶液進行靜電紡絲製得。
所述的聚己內酯電紡絲以質量體積比≥25%的聚己內酯的三氟乙醇溶液進行靜電紡絲製得,靜電紡絲過程中電紡絲的接收距離≤10cm,接收裝置為轉動的鏤空骨架滾筒。所述的聚己內酯電紡棉具有微米級直徑和高孔隙率的特徵,在體內外均有利於細胞向電紡棉深層長入。
所述的組織工程構建的方法為:將包裹或不包裹生物材料的模型(實施例展示包裹聚己內酯電紡膜的方式)移植到皮下。
所述的組織工程構建的方法為:將包裹聚己內酯電紡絲的模型移植皮下。
以上製備方法製得的血管補片。
本發明優點在於:
1、本發明提供了一種基於計算流體力學優化的個體化自體組織工程補片的製備方法,與傳統的二維補片相比,本發明的補片經過了計算流體力學優化,為個體化的具有三維形態的血管補片。
2、補片中的細胞和細胞外基質來源於自體,且具有組織活性,自體移植後不發生免疫排斥反應,也不易引起鈣化。
3、以法洛四聯症為例,通過本發明的方法製備的肺動脈補片的大小和成角均進行了優化,患者肺動脈總幹流速及左右肺血流分配比均接近於正常生理條件。
附圖說明
附圖1:靜電紡絲裝置的搭建。
附圖2:無細胞聚己內酯(PCL)電紡棉的形態和二維自體血管補片的構建。
附圖3:患者肺動脈三維重建。獲取患者心血管MRI圖像,在Mimics 17.0軟體中用黃色蒙版標記每層圖像中肺動脈的位置(A和B),重建後獲得肺動脈三維圖像(C)。直接重建出的圖像表面粗糙,在儘量減少處理對圖像精確度帶來損失的前提下,對肺動脈表面作光滑處理,完成肺動脈的三維重建模型(D)。
附圖4:肺動脈補片的大小設計、虛擬手術規劃和流體分析。患者術前肺動脈及左右分支情況被用於模擬補片植入手術(A),利用計算血流動力學可分析得到肺動脈血流速度和左右肺動脈血流分配(D)。補片①依據臨床經驗公式計算的肺動脈瓣環直徑的150%設計,用於單純瓣環擴大(B,白色顯示補片設計);補片②單純瓣環擴大則依據採用臨床經驗公式計算的瓣環直徑(C,白色顯示補片設計)。兩種補片的計算流體分析結果分別為E和F。
附圖5:肺動脈補片的成角設計、虛擬手術規劃和流體分析。補片②在設計時僅考慮了擴大肺動脈瓣環,因此虛擬手術規劃後可看出該設計不影響肺動脈總幹與左右肺動脈之間的成角關係,主肺動脈依然偏向左肺動脈(A)。補片③採取折中的做法,使虛擬手術植入後肺動脈總幹與左右肺動脈間成角大小相當(B)。補片④在虛擬手術植入後肺動脈總幹偏向左肺動脈(C)。上述3種補片的虛擬手術計算流體力學分析分別為圖D,E和F。
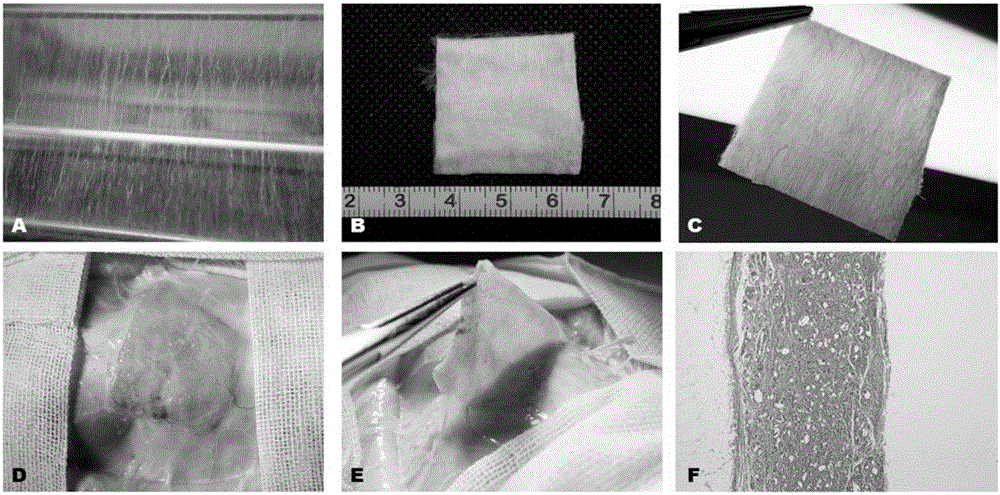
附圖6:個體化組織工程肺動脈補片的構建。3D列印出優化的補片模型作為組織工程肺動脈補片的三維形態支撐(A),大孔徑PCL電紡棉被包繞於3D列印補片模型的表面(B)。將其整體移植到大鼠皮下。4周後取材(C)並撥出3D列印模型表面的組織,可得到與優化補片相同三維結構的組織工程肺動脈補片(D,E)。組織切片HE染色證實細胞長入和組織形成(F)。標尺:F-框圖=100μm。
具體實施方式
下面結合附圖對本發明提供的具體實施方式作詳細說明。
實施例1大孔徑聚己內酯(PCL)電紡纖維的製備和二維血管補片的構建
原料:聚己內酯(PCL),三氟乙醇(TFE)
設備:高壓電源,微量注射泵、靜電紡接收裝置(鏤空四骨架滾筒)
方法:
(1)溶液的配置——35%PCL靜電紡溶液
以TFE為溶劑,用電子天平稱取PCL顆粒,按35%(m/v)的溶質比例稱量後轉入可密封玻璃瓶。按1.386g/ml的密度用電子天平量取相應體積的TFE轉入對應溶解瓶中。室溫下反覆翻轉玻璃瓶促進PCL均勻溶解。持續翻轉溶解3天後用於靜電紡。配製好的溶液應於1周內用完。
(2)靜電紡PCL纖維的製備
用10mL注射器吸取35%PCL靜電紡溶液,換14G平口點膠針頭。將注射器裝載於微量注射泵,並安置使之懸於鏤空四骨架滾筒接收裝置的上方。調節高度,使針尖與接收裝置之間的距離為6cm。將高壓電源地極端連接於滾筒接收裝置,電源高壓端夾於針頭金屬部分。調節高壓電源,使高壓輸出為16kV。調節微量注射泵注射速率為5ml/h。調節滾筒控制器,使滾筒旋轉速率為2000rpm。靜電紡初期,由於出絲尚不穩定,這部分電紡絲可收集於滾筒一端。待出絲穩定後,於滾筒中部接收電紡絲。接收過程中應不斷緩慢左右移動滾動,使電紡絲在滾筒上以均勻的密度分布。本例收集1ml PCL/TFE溶液。
(3)一般的組織工程血管補片
為了探索上述PCL電紡纖維是否可以作為一般組織工程血管補片的支架,我們首先將上述PCL纖維沿同一方向反覆層疊10次(層),製備出「無細胞PCL電紡棉」。將PCL電紡棉用75%乙醇和紫外照射滅菌處理後,移植到大鼠皮下,待細胞長入和組織形成。4周後取出,得到自體血管補片。
無細胞PCL電紡棉片直接移植於大鼠背部皮下4周後,取材可見新生皮下組織形成。組織肉紅色,質地均一,富有彈性,與周圍其他組織靠疏鬆結締組織分界。組織石蠟切片HE染色證明細胞已完全長入電紡棉片,並分泌大量細胞外基質,形成緻密緊實的自體組織片。
實施例2患者血管補片的設計、虛擬手術和計算流體優化
以一例法洛四聯症(ToF)患者為例說明(本例中,採用補片大小優化和成角優化):
患兒一般情況:男,入院時11月齡,身長75cm,體重8.8kg。術前心臟超聲顯示ToF,其中肺動脈瓣及瓣下狹窄。瓣環直徑0.61cm,總幹內徑0.63cm,流速5.23m/s。
患兒心血管MRI圖像被用於肺動脈三維重建。蒙版的作用是指導計算機層疊圖像蒙版所在的圖像區域以完成三維重建,這裡肺動脈所在部位被黃色蒙版標記。因為直接重建的圖像表面粗糙,在儘量減少圖像精度損失的前提下,完成重建圖像的光滑處理。
根據臨床經驗公式計算出的瓣環擴大直徑為10.7mm,首先設計出下列兩種補片設計:補片①:按經驗公式計算值的150%,即以16.0mm的瓣環直徑作瓣環擴大;補片②:按肺動脈瓣環經驗公式計算值10.7mm為直徑作瓣環擴大。結合患者原始肺動脈形態進行流體計算。分析後可知,患者術前肺動脈瓣環較臨床經驗公式計算值小43%,肺總幹血流流速總體高於4m/s,左右肺血流分配比約30:70。經過補片①擴大後,患者肺動脈總幹流速降低,平均<2.0m/s,左右肺血流分配比約32:68。以補片②作虛擬手術計算結果顯示,肺總幹血流高於補片①組,低於術前組;然而,左右肺血流分配比保持不變,依然為32:68。
在確認以補片設計的基礎上,為了研究肺動脈總幹與左右肺血流分配比之間的關係,在補片②依據臨床經驗公式計算瓣環擴大直徑的基礎上,進一步設計出兩種補片設計:補片③:肺動脈總幹與左右肺動脈分支角度相當;補片④:肺動脈總幹稍偏向右肺動脈。其中,原有補片②血管夾角關係與患者術前動脈間夾角關係一致,即肺動脈總幹稍偏向左肺動脈。以上述補片設計為模板,整合入患者術前肺動脈完成虛擬手術規劃。通過計算流體力學分析可以看出,三種針對角度的補片設計基本不影響肺動脈血流流速。然而,補片③行虛擬手術後左右肺動脈血流比例為40:60,補片④行虛擬手術後左右肺血流比例為43:57。
綜合上述對瓣環補片擴大大小和肺動脈成角的虛擬手術及對應計算流體分析,我們認為補片④的設計是上述方案中的最優設計,因為不僅可以降低肺動脈血流速度,緩解肺動脈梗阻,還使左右肺血流分配比接近正常生理條件下的分配比例(45:55)。此後以補片④的設計方案完成實驗。
實施例3基於計算流體力學優化的個體化組織工程血管補片的構建
將上述計算流體力學分析優化的瓣膜設計模型(即補片④)用3D印表機列印出來,作為個體化組織工程肺動脈補片構建的內核。由於本例實驗中以大鼠為移植對象,因此列印的補片模型等比例縮小至長軸為2.0cm。將靜電紡PCL電紡絲包裹於3D列印補片表面,大鼠皮下移植4周可見3D列印表面已完全包裹自體組織。撤去3D列印補片內核,可見基於PCL電紡棉支架形成的組織完全按照3D列印補片的形態生長,初步實現了個體化組織工程補片的構建。
此外,為了實現個體化組織工程血管補片的構建,還可以使用自體細胞接種、幹細胞接種等方法,在體內外培養實現組織形成,最終構建出具有優化三維形態特徵的補片組織。
以上所述僅是本發明的優選實施方式,應當指出,對於本技術領域的普通技術人員,在不脫離本發明方法的前提下,還可以做出若干改進和補充,這些改進和補充也應視為本發明的保護範圍。
