控制水稻葉綠素合成的基因YL‑1及其應用的製作方法
2023-06-04 10:49:01 1
本發明涉及分子生物技術領域,具體來說是一種控制水稻葉綠素合成的基因YL-1及其應用。
背景技術:
葉片是植物進行光合作用的主要器官,水稻籽粒中2/3以上的乾物質是開花後通過光合作用獲得的(王旭軍,徐慶國,楊知建(2005)水稻葉片衰老生理的研究進展.中國農學通報21:187-190)。光合作用的效率與葉綠體結構和功能是否完整、光合作用複合體的穩定性、葉綠素含量的高低都有著複雜的關係。近年來,水稻葉色的應用價值備受關注,葉色變異可以作為標記性狀,在水稻雜交育種和良種繁育中發揮重要作用,不但可以用於苗期剔除受外源花粉汙染的種子和假雜種,還可以用於快速測定種子純度(章志興,陳善福(2001)葉色標記技術在雜交水稻種子生產中的應用.種子科技19:33-34)。另外,葉色突變體的研究對於利用基因工程有效提高水稻的光合能力,培育高光效水稻品種,增加水稻產量具有重要的理論意義和應用價值。
目前,利用水稻葉色突變體,已經克隆出多個參與或調控葉綠素代謝和葉綠體發育的基因,通過分析基因功能、表達模式、基因間互作以及核-質信號傳導,初步了解了水稻葉色形成及調控機理。截止目前,在擬南芥中葉綠素合成過程的關鍵酶都已鑑定出來(Nagata N(2005)Identification of a Vinyl Reductase Gene for Chlorophyll Synthesis in Arabidopsis thaliana and Implications for the Evolution of Prochlorococcus Species.The Plant Cell Online 17:233-240),但在水稻中只有部分基因被鑑定出來,其他基因還有待進一步發掘。此外,葉綠素降解的調控機制尚未明朗,核-質互作的機理尚不清晰,都有待深入進一步研究。
植物鎂原卟啉IX單甲脂環化酶基因(Magnesium protoporphyrin IX monomethyl ester cyclase)是植物葉綠素合成過程中的關鍵酶,其功能是將鎂原卟啉IX單甲脂轉化成二乙烯基原葉綠素酸脂。該酶複合體是由催化亞基,輔因子調節亞基,降解亞基組合而成。在細菌和海藻類生物體內,其同源基因編碼起催化作用的亞基已被鑑定。在單子葉模式植物水稻中,該基因的克隆及其功能研究還未見報導。
技術實現要素:
本發明要解決的問題是提供一種從水稻黃葉突變體中克隆新基因YL-1,該基因編碼一個鎂原卟啉IX單甲脂環化酶,調控葉綠素的合成。
為實現上述目的,本發明採用的技術方案是:一種控制水稻葉綠素合成的基因YL-1,所述基因YL-1的核苷酸序列如SEQ ID NO:1所示。
進一步的是:所述基因YL-1的核苷酸序列還包括在SEQ ID NO:1所示的核苷酸序列中添加、取代,插入或缺失一個或多個核苷酸而生成的突變體、等位基因或衍生物。
本發明還提供一種由控制水稻葉綠素合成的基因YL-1編碼的蛋白,所述蛋白質的胺基酸序列如SEQ ID NO:3所示。
進一步的是:所述蛋白胺基酸序列還包括在SEQ ID NO:3所示的胺基酸序列中添加、取代、插入或缺失一個或多個胺基酸或其他物種的同源序列而生成的胺基酸序列或衍生物。
本發明還提供一種含有植物葉綠素合成相關蛋白編碼基因的轉基因細胞系。
本發明還提供一種含有植物葉綠素合成相關蛋白編碼基因的轉基因重組菌。
本發明的另一個目的是提供一種用YL-1基因進行高效的植物轉化方法,具體地說,本發明提供了具有SEQ ID NO:1所示的序列片段載體。
本發明的有益技術效果是:本發明利用水稻黃葉突變體,通過圖位克隆法克隆到了YL-1基因,該基因編碼葉綠素合成相關鎂原卟啉IX單甲脂環化酶蛋白,通過轉基因過表達驗證實驗鑑定了YL-1基因的功能,因而本發明能調節水稻葉綠素的合成,進而獲得苗期黃化表型,為該基因的進一步利用打下基礎。
附圖說明
為了更清楚地說明本發明實施例或現有技術中的技術方案,下面將對實施例或現有技術描述中所需要使用的附圖作簡單地介紹,顯而易見地,下面描述中的附圖僅僅是本發明的一些實施例,對於本領域普通技術人員來講,在不付出創造性勞動性的前提下,還可以根據這些附圖獲得其他的附圖。
圖1野生型YK17和突變體yl-1幼苗期葉片和抽穗期劍葉,稻穗葉綠素a、葉綠素b、葉綠素a/b對比分析;
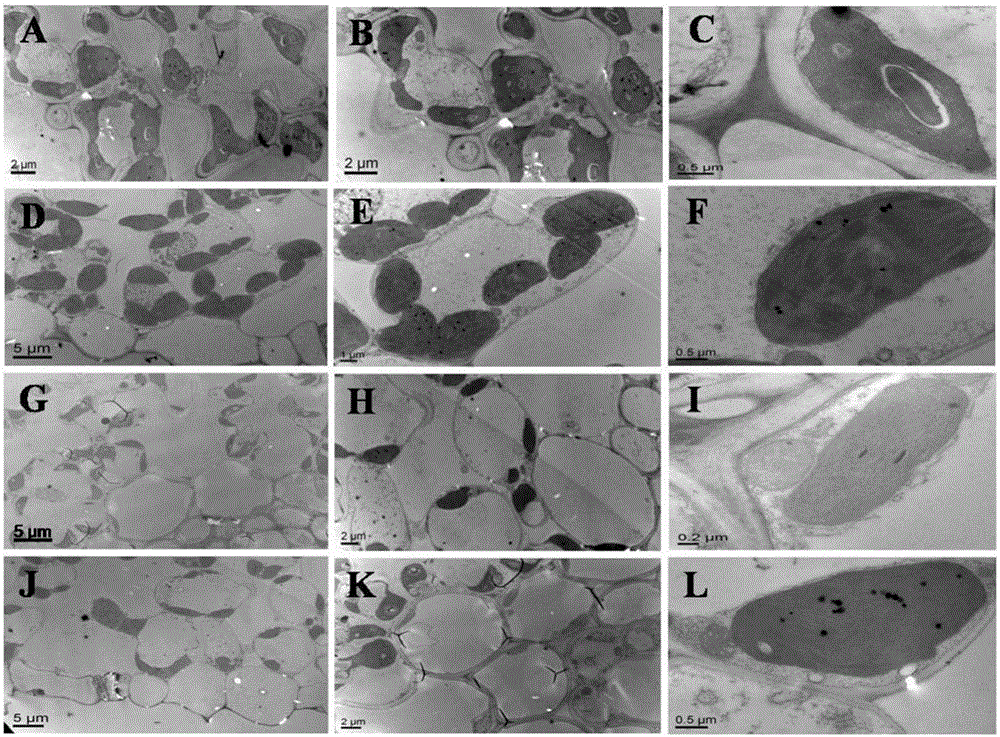
圖2苗期和抽穗期yl-1突變體和野生型中嘉早17葉片透射電鏡葉綠體亞顯微結構觀察,A、B、C苗期野生型中嘉早17葉片葉綠體亞顯微結構,D、E、F、抽穗期野生型中嘉早17葉片葉綠體亞顯微結構,G、H、I苗期yl-1葉片葉綠體亞顯微結構,J、K、L抽穗期yl-1葉片葉綠體亞顯微結構;
圖3 YL-1在水稻第1染色體上的精細定位;
圖4野生型YK17(左),突變體yl-1(中),T0轉基因過表達植株(右)整體植株,劍葉,稻穗表型;
圖5野生型YK17,突變體yl-1,轉基因過表達植株YL-1基因(LOC_OS01g17170)相對表達量分析。YK17,野生型中嘉早17;yl-1,突變體;YL-1E,轉基因過表達植株。
具體實施方式
下面將結合本發明實施例中的附圖,對本發明實施例中的技術方案進行清楚、完整地描述,顯然,所描述的實施例僅僅是本發明一部分實施例,而不是全部的實施例。基於本發明中的實施例,本領域普通技術人員在沒有作出創造性勞動前提下所獲得的所有其他實施例,都屬於本發明保護的範圍。
實施例1
一、水稻黃葉突變體yl-1的分離和遺傳分析
本研究突變體yl-1來源於超級早稻品種中嘉早17(YK17)的EMS誘變突變體庫,田間表型觀察發現該突變體的主要特徵是:該突變體從苗期至成熟期葉片、莖稈、稻穗均表現為黃色;其它農藝性狀方面:株高,yl-1(72.88cm)略矮於YK17(84.80cm);分櫱數,yl-1(12.5)遠高於YK17(7.00);每穗粒數,yl-1(118.50)低於YK17(209.20);結實率,yl-1(85%)高於YK17(75%);淨光合速率,yl-1(25.31)低於YK17(32.96)。葉綠素測定結果表明yl-1主要表現為葉綠素b較野生型嚴重缺乏(圖1)。利用透射電鏡(TEM)觀察幼苗期和抽穗期野生型YK17和yl-1的葉片葉綠體超微結構,發現在幼苗期和抽穗期野生型的葉肉細胞含有較多的葉綠體,且葉綠體含有正常的片層結構;而yl-1含有較少的葉綠體,且葉綠體片層堆積較少,模糊,含有較多的嗜鋨小體(圖2)。用突變體分別與水稻品種D50,Dular和02428進行正反交,得到的F1後代均表現為正常綠化,在其自交F2群體中正常植株與突變植株分離比接近3:1(表2),表明此性狀由一對隱性核基因控制。
表1.突變體yl-1與野生型中嘉早17(YK17)農藝性狀比較
表2.突變植株與正常植株在不同F2群體中的分離
二、圖位克隆YL-1基因
1.YL-1基因的分子定位:
為了分離YL-1基因,本發明首先建立了一個大的多態性高的F2定位群體,由熱帶粳稻品種D50為父本,突變體yl-1為母本,掛牌收穫F2單株鑑定後代基因型,對獲得的F2群體中有表型分離的群體選取其中的隱性黃葉極端個體進行基因定位,利用SSR分子標記對YL-1位點進行初步定位,將其初步定位在第1染色體的短臂上,並介於RM10551和RM10748兩SSR標記之間。然後通過對RM10622和RM10644兩標記之間的BAC序列進行分析,發展了新的Indel標記,將YL-1精細定位於PAC克隆P0025D05的RM10622和Indel8之間44.8kb的範圍之內(圖3),通過分析此區段開放閱讀框(ORF)推測候選基因並基因測序分析,尋找突變位點。
2.YL-1基因的鑑定和功能分析
根據精細定位的結果,在44.8kb範圍內根據RiceGAAS(Rice Automat ed Systrm,http://ricegaas.dna.affrc.go.jp/)和TIGR(http://rice.plantbiology.msu.edu/)的預測,發現在此區間內共有4個候選基因,我們設計了各基因的測序引物,採用PCR的方法分別從yl-1突變體和野生型YK17基因組中擴增出所有候選基因進行測序分析。發現其中1個基因的DNA片段中,突變體擴增的產物與野生型品種比較發生了單鹼基突變,造成胺基酸的突變。野生型品種YK17擴增的基因序列為SEQ ID NO.1,命名為YL-1基因。為了確證突變體表型是由YL-1基因突變引起的,我們對突變體進行了轉基因恢復驗證實驗。轉基因恢復驗證主要是將野生型YL-1基因全長基因組序列克隆並構建到雙元植物轉基因載體pUbi-1390的多克隆位點KpnI/BamHI處,得到過量表達載體。將構建好的過量表達載體通過農桿菌介導的遺傳轉化系統轉化突變體愈傷,經過抗性愈傷誘導進而分化成轉基因苗。轉化了外源YL-1基因的突變體(即轉基因陽性株系)幼苗顏色復綠,YL-1表達量明顯增高,圖4為野生型、突變體以及T0轉基因過表達植株的表型。圖5為野生型、突變體、轉基因過表達植株的YL-1表達量分析。轉基因過表達恢復試驗確證了突變體表型是由YL-1基因突變引起的,表明本發明獲得了使突變體恢復正常功能的轉基因水稻。
實施例2YL-1基因的克隆
a)水稻材料
水稻(Oryza sativa L)突變體yl-1(yellow leaves 1),原始野生型材料為超級早稻品種中嘉早17(YK17).
b)電鏡觀察
利用透射電鏡(TEM)觀察苗期和抽穗期野生型和yl-1葉片的葉綠體超微結構,發現野生型的葉綠體含有正常的片層結構和澱粉粒,而yl-1的葉肉細胞含有較少的葉綠體,且葉綠體片層堆積疏鬆較模糊,嗜鋨小體較多(圖3)。
c)遺傳分析和定位群體
利用正反雜交確定yl-1為隱性突變體,選取突變體和D50進行雜交,F1代自交,單株收種種植F2群體,從有分離的群體中選出1500個隱性個體(幼苗黃色)作為定位群體。在四葉期每株取1克左右的嫩葉,用來提取總DNA進行基因定位。
d)YL-1基因的初步定位和精細定位
採用水稻微量DNA的快速提取方法從水稻葉片中提取用於基因定位的基
組DNA,該DNA抽提的方法為SDS法(Dellaporta SL,Wood J,Hicks JB(1983)A plant DNA minipreparation:version II.Plant Mol Biol Rep 1:19-21)。取大約100mg水稻葉片剪碎後放入2ml離心管,加入鋼珠經液氮冷凍後,在磨樣機上粉碎,然後提取DNA,獲得的DNA沉澱溶解於400μL超純水中,每一個PCR反應用1μLDNA樣品。在YL-1基因的初步定位中,採用由30個具有突變表型的F2極端個體進行SSR分析。首先根據公布的粳稻和秈稻創建的分子遺傳圖譜,選取近似均勻分布於各染色體上的SSR引物進行PCR擴增(反應體系如下)。通過8%的聚丙烯醯胺凝膠(凝膠配置方法如下)電泳分離,通過檢測條帶的多態性,將基因初步定位到第1染色體的短臂上,並介於RM10551和RM10748兩SSR標記之間。
PCR反應體系:
8%聚丙烯醯胺凝膠配方:
聚丙烯醯胺凝膠顯色液配方:
註:甲醛是臨用前現加,其他三個按相應量提前配好。
然後通過對RM10622和RM10644兩標記之間的BAC序列進行分析,發展了新的Indel標記,最後將F2定位群體擴大到1500個進行精細定位,將YL-1精確定位於BAC克隆P0481E12的RM10622和Indel8之間44.8kb的範圍之內,(圖3),通過分析此區段開放閱讀框(ORF)推測候選基因並基因測序分析,尋找突變位點。
Indel標記引物序列:
Indel4-F ACAATCAACTCTAAATGGATAACTAC(SEQ ID NO.6)
Indel4-R GCCTATGCTTTGCTACGGA(SEQ ID NO.7)
Indel8-F CCATTAGGTCTTTCTTGTGCC(SEQ ID NO.8)
Indel8-R GTCCGTAGGTGGTGTTGG(SEQ ID NO.9)
e)基因預測和比較分析
根據精細定位的結果,在44.8kb範圍內根據RiceGAAS(Rice Automat ed Systrm,http://ricegaas.dna.affrc.go.jp/)和TIGR(http://rice.plantbiology.msu.edu/)的預測,發現在此區間內共有4個候選基因,我們設計了各基因的測序引物,採用PCR的方法分別從yl-1突變體和野生型品種基因組中擴增出所有候選基因進行測序分析。發現其中1個基因(LOC-Os01g17170)的DNA片段中,突變體擴增的產物與野生型品種比較發生了單鹼基突變(CDS 515位鹼基C突變成T),造成胺基酸的突變(絲氨酸Ser突變成苯丙氨酸Phe)。野生型品種擴增的基因序列為SEQ ID NO.1,命名為YL-1基因,其編碼的蛋白質測序得到的核苷酸序列為SEQ ID NO.2.
實施例3轉基因實驗
1、載體構建
設計一對完全覆蓋整個YL-1基因ORF的引物,並在引物上分別設計酶切位點KpnI和BamHI位點,PCR擴增野生型基因組DNA,電泳檢測切膠回收,回收產物用KpnI和BamHI酶切,連接至同樣酶切的pUbi-1390載體上,測序確認沒有發生鹼基突變,構建後的載體結構圖為pUbi1390-YL-1,把構建好的載體通過電擊的方法轉入農桿菌(A grobacterium tumefaciens)菌株中。
擴增ORF序列的引物序列為:
OG2-KpnI:5』-TTACTTCTGCACTAGGTACCTCTCGCCACCTTATCTCATC-3』(SEQ ID NO.4)
OG2-BamHI:5』-GAATTCCCGGGGATCCTAACCACCCATCATCTCACC-3』(SEQ ID NO.5)
2、遺傳轉化:
(1)轉化受體的選擇
將yl-1種子成熟胚誘導愈傷組織,經過誘導培養基誘導2周後將胚芽剪下,繼續培養1周,挑選生長旺盛的愈傷用作轉化的受體。
(2)遺傳轉化
採用農桿菌介導的遺傳轉化方法(Hiei Y,Ohta S,Komari T,Kumashiro T(1994)Efficient transformation of rice(Oryza sativa L.)mediated by Agrobacterium and sequence analysis of the boundaries of the T‐DNA.The Plant Journal 6:271-282),將pUbi-1390空載體和pUbi1390-YL-1載體的EHA105菌株侵染水稻愈傷,在黑暗、25℃條件下共培養3天後,在含有120mg/L G418的篩選培養基上培養。篩選抗性愈傷在含有120mg/L預分化培養基上培養10-13天。將預分化的愈傷轉至分化培養基上在光照條件下培養。一個月左右得到抗性轉基因植株。對植株進行鑑定和連續的觀察,發現轉空載體的轉基因植株表型與yl-1相比不發生變化,即苗期黃化,而pUbi1390-YL-1載體的陽性轉基因植株與野生型表現一致,表現為綠色,即恢復了yl-1的突變表型,見圖4。
本技術領域技術人員可以理解,除非另外定義,這裡使用的所有術語(包括技術術語和科學術語)具有與本發明所屬領域中的普通技術人員的一般理解相同的意義。還應該理解的是,諸如通用字典中定義的那些術語應該被理解為具有與現有技術的上下文中的意義一致的意義,並且除非像這裡一樣定義,不會用理想化或過於正式的含義來解釋。
最後所應說明的是:以上實施例僅用以說明而非限制本發明的技術方案,儘管參照上述實施例對本發明進行了詳細說明,本領域的普通技術人員應該理解:依然可以對本發明進行修改或者等同替換,而不脫離本發明的精神和範圍的任何修改或局部替換,其均應涵蓋在本發明的權利要求範圍當中。
