對咽拭子樣本或鼻咽拭子直接實時定量的PCR的方法與流程
2023-10-09 08:48:49 2
本發明屬於分子診斷生物學技術領域,具體涉及對咽拭子樣本或鼻咽拭子樣本直接實時定量的PCR的方法。
背景技術:
聚合酶鏈式反應(Polymerase Chain Reaction PCR)是在模板DNA、引物和四種脫氧核糖核苷酸存在下,依賴於DNA聚合酶的酶促合成反應技術。該技術自從美國Cetus公司人類遺傳室Kary Mullis及同事於1958年發明以來,相關的衍生技術就快速開發出來,並在微生物學,遺傳病學和法醫等領域中得到廣泛應用。尤其在病原體檢測方面,當知道某一病原體的一段基因時,根據該段基因設計特異性的引物然後進行PCR擴增,使其達到檢測量,然後通過合適的檢測手段,即可以確定樣本中是否存在該病原體。
實時螢光定量PCR技術是1996年由美國Applied Biosystems公司推出的,該技術是指在PCR反應體系中加入螢光基團或螢光染料,利用螢光信號積累實時監測整個PCR進程,最後通過標準曲線對未知模板進行定量分析。與普通的PCR相比,螢光定量PCR技術檢測具有特異性強,靈敏度高,重複性好,速度快,全封閉反應等優點,使其在醫學、農學和臨床檢測學中得廣泛使用。在進行螢光定量PCR檢測時,首先要進行樣本的核酸提取,目前核酸提取的方法主要有鹼裂解法、層析柱法和磁珠法,前兩種方法操作比較複雜且需要用離心機等大型設備;磁珠法操作簡便,但存在多次洗脫操作導致核酸損失且存在汙染風險,因此需要尋找不需要核酸提取直接PCR的方法對提高檢測質量具有重要意義。
技術實現要素:
本發明的目的在於提供對咽拭子樣本或鼻咽拭子樣本直接實時定量的PCR的方法,以克服現有檢測技術的不足,為咽拭子樣本或鼻咽拭子樣本提供一種快速、簡便、高效、實用的檢測方法,不要核酸提取過程,簡化了操作過程,節約了時間和成本,且能大量處理樣本,操作檢測時可防止汙染。
為達到上述目標提供了對咽拭子樣本或鼻咽拭子直接實時定量的PCR的方法,包括以下步驟:
(1)製備裂解液和PCR反應液;
(2)將咽拭子樣本或鼻咽拭子樣本加入到含有步驟(1)中裂解液的PCR擴增管中,再加入磁珠到PCR擴增管中,振蕩搖勻混合;
(3)將步驟(2)中的PCR擴增管在80-100℃高溫處理10min後冷卻到室溫,然後在18-28℃反應5-10min;
(4)將PCR擴增管瞬時離心後放入到磁力架中,待磁珠吸附到磁力架一側後將上清吸出;
(5)在PCR擴增管內加入配置好的PCR反應液,進行實時定量PCR反應;
所述步驟(1)中裂解液的成分為0-2M的NaCl、0-0.3%的Triton-X和0-0.2M的KCl。
所述步驟(2)樣本與裂解液的體積比為1:3—1:10。
所述步驟(3)中的高溫為100℃。
所述磁珠為市售的核酸提取使用的羥基磁珠,即超順磁性核心及無機氧化矽的外殼,優選的,平均粒徑為≤1000nm的單分散性羥基磁珠。
所有反應步驟都在同一個試管內進行,本發明所述方法可以手動操作以及機械自動化操作,且不要核酸提取過程,簡化了操作過程,節約了時間以及成本。
本發明的有益效果是:為咽拭子樣本或鼻咽拭子樣本提供一種快速、簡便、高效、實用的檢測方法,不要核酸提取過程,簡化了操作過程,節約了時間和成本,且能大量處理樣本,操作檢測時可防止汙染。
附圖說明
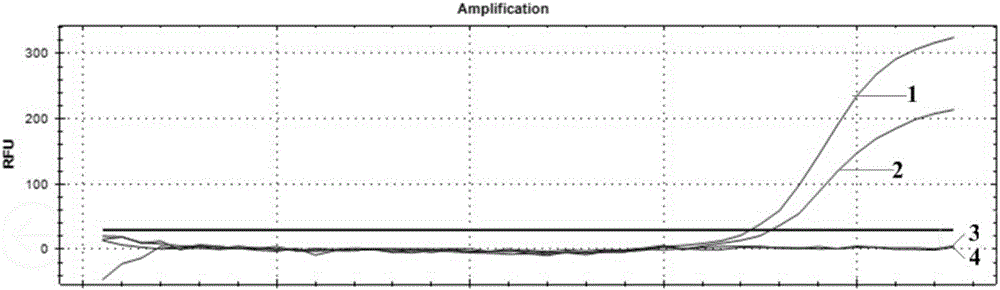
圖1為實施例1的本發明方法應用於乙流臨床樣本的實時螢光定量PCR檢測結果圖,圖中標號為1、2、3和4的四條曲線分別為1號樣本、2號樣本、3號樣本和4號樣本的實驗結果;
圖2為實施例2的本發明方法檢測陰性的乙流咽拭子樣本的敏感性結果圖,圖中標號為1、2、3和4的四條曲線分別為2.0×104TCID50/L,2.0×103TCID50/L,2.0×102TCID50/L,2.0×101TCID50/L的樣本的實驗結果;
圖3為實施例3的本發明方法檢測陰性的乙流咽拭子樣本的重複性結果圖,圖中標號為1、2、3、4和5的五條曲線分別是5個孔內樣本的實驗結果;
圖4為實施例5的本發明方法檢測RSV的結果圖,圖中標號為1、2、3和4的四條曲線分別是2.0×104TCID50/L,2.0×103TCID50/L,2.0×102TCID50/L,2.0×101TCID50/L樣本的檢測結果;
圖5為實施例5的廣東華銀醫藥科技有限公司的RSV核酸檢測試劑盒(包含核酸提取試劑)檢測RSV的結果圖,圖中標號為1、2、3和4的四條曲線分別是2.0×104TCID50/L,2.0×103TCID50/L,2.0×102TCID50/L,2.0×101TCID50/L樣本的檢測結果。
具體實施方式
以下結合附圖和具體實施方式對本發明作進一步詳細說明,實施例提供的方案為優選方案,但不作為對本申請的限定,實施例中所用的PCR擴增儀器為Bio-RAD CFX96和ABI 7500。
實施例1
本發明方法應用於乙流臨床樣本的實時螢光定量PCR檢測
(1)配置成分為1MNaCl、0.01%Triton-X和0.01MKCl的裂解液100ml,按照磁珠和裂解液1:200的體積比加0.5ml磁珠到上述配好的裂解液中混勻,取4個相同的專用PCR管,每管分裝80ul配置好的混有磁珠的裂解液;
(2)從紹興疾控中心提供的2例乙流陽性和2例乙流陰性咽拭子四個樣本中均取20ul分別加入到步驟(1)中的四個PCR管中分別作為1號樣本、2號樣本、3號樣本和4號樣本,蓋好管蓋;
(3)將步驟(2)中的四個PCR管放入在95℃中加熱5min後室溫(室溫為18-28℃)放置10min;
(4)將步驟(3)中的四個PCR管放入到磁珠架上靜置2min,然後用移液器在磁珠對側吸棄液體,保留磁珠;
(5)在四個PCR管中均加入0.5ul(200U/ul)單位的逆轉錄酶和24.5ul的反應液(所述反應液包含濃度為30nmol/L的乙流的上下引物、30nmol/L乙流的探針、水和商業的一步法RT-QPCR試劑盒的buffer,推薦使用TAKARA和全式金公司的該試劑盒),封蓋後渦旋振蕩搖勻30s,確保磁珠和PCR反應混合均勻;
(6)將步驟(5)中的四個PCR管瞬時離心使PCR管中液體都在底部;
(7)將上述步驟(6)得到的四個PCR管放置在PCR擴增儀器(選用的為Bio-RAD CFX96)中進行擴增,45℃,10min;95℃,10min;進行40-45循環的95℃,15S和60℃,45S,在60℃檢測螢光信號。
實驗結果如圖1所示,1號、2號、3號和4號曲線分別為1號樣本、2號樣本、3號樣本和4號樣本的實驗結果,結果表明,按照本實施例的方法進行操作,可以有效準確的檢測出乙流的咽拭子樣本。
實施例2
本發明方法的敏感性測試
用實施例1步驟(2)中的陰性的乙流咽拭子樣本作為稀釋液,將中國藥品生物製品檢定所的甲乙流國家標準中的乙流最低檢測限參考品S2 2.0×106TCID50/L進行稀釋,分別獲得2.0×104TCID50/L,2.0×103TCID50/L,2.0×102TCID50/L,2.0×101TCID50/L的四個樣本,利用與實施1相同的方法對以上四個稀釋樣本進行實時螢光PCR檢測(選用ABI7500進行PCR擴增)。
實驗結果如圖2所示:圖中標號為1、2、3和4的四條曲線分別為濃度為2.0×104TCID50/L,2.0×103TCID50/L,2.0×102TCID50/L,2.0×101TCID50/L的樣本的實驗結果,結果表明,本發明可檢測出的乙流的最低濃度為2.0×102TCID50/L,符合國家參考品的要求最低檢測2.0×103TCID50/L的濃度要求。
實施例3
本發明方法的螢光PCR檢測的重複性測試
用實施例1中的陰性的乙流咽拭子樣本作為稀釋液,將中國藥品生物製品檢定所的甲乙流國家標準中的乙流最低檢測限參考品S2 2.0×106TCID50/L進行稀釋,獲得2.0×103TCID50/L的樣本。利用與實施1相同的方法對樣本進行5孔復檢實時螢光PCR檢測(Bio-RAD CFX96進行擴增),圖中標號為1、2、3、4和5的五條曲線分別是5個孔內樣本的實驗結果。
檢測結果如圖3和如下表:
結果表明,本發明方法的檢測可重複。
實施例4
本發明方法檢測乙流與上海之江核酸提取試劑盒以甲、乙型流感病毒聯合測定試劑盒中檢測乙流比較
取紹興疾控中心給予的2例陽性的乙流咽拭子樣本分別作為5號樣本和6號樣本,利用與實施例1相同的方法(Bio-RAD CFX96進行擴增)和上海之江核酸提取試劑(磁珠柱法)以及甲、乙型流感病毒聯合測定試劑盒進行檢測,
結果如下表:
結果表明,本方法檢測的結果與上海之江試劑盒檢測的結果無顯著差異。
實施例5
本發明方法檢測RSV與廣東華銀醫藥科技有限公司的RSV核酸檢測試劑盒(包含核酸提取試劑)檢測RSV的比較
用實施例1中的陰性的乙流的咽拭子樣本(經廣東華銀醫藥科技有限公司的RSV核酸檢測試劑盒檢測RSV為陰性)作為稀釋液,將紹興疾控中心提供的RSV的2.0×105TCID50/L進行稀釋,分別獲得2.0×104TCID50/L,2.0×103TCID50/L,2.0×102TCID50/L,2.0×101TCID50/L的四個樣本,利用與實施例1相同的方法(採用Bio-RAD CFX96進行擴增,其中引物和探針換成RSV的引物和探針)和廣東華銀醫藥科技有限公司的RSV核酸檢測試劑盒(包含核酸提取試劑)對四個樣本分別檢測,結果如圖4、圖5和下表:
圖4為本發明方法檢測的結果,圖4中的標號為1、2、3和4的四條曲線分別是2.0×104TCID50/L,2.0×103TCID50/L,2.0×102TCID50/L,2.0×101TCID50/L樣本的檢測結果。
圖5為廣東華銀醫藥科技有限公司的RSV核酸檢測試劑盒的檢測結果,圖5中的標號為1、2、3和4的四條曲線分別是2.0×104TCID50/L,2.0×103TCID50/L,2.0×102TCID50/L,2.0×101TCID50/L樣本的檢測結果。
