具有水平電場驅動型液晶顯示元件用液晶取向膜的基板的製造方法與流程
2023-12-01 04:38:51 5
本發明涉及具有水平電場驅動型液晶顯示元件用液晶取向膜的基板的製造方法。更詳細而言,涉及用於製造燒屏特性優異的液晶顯示元件的新方法。
背景技術:
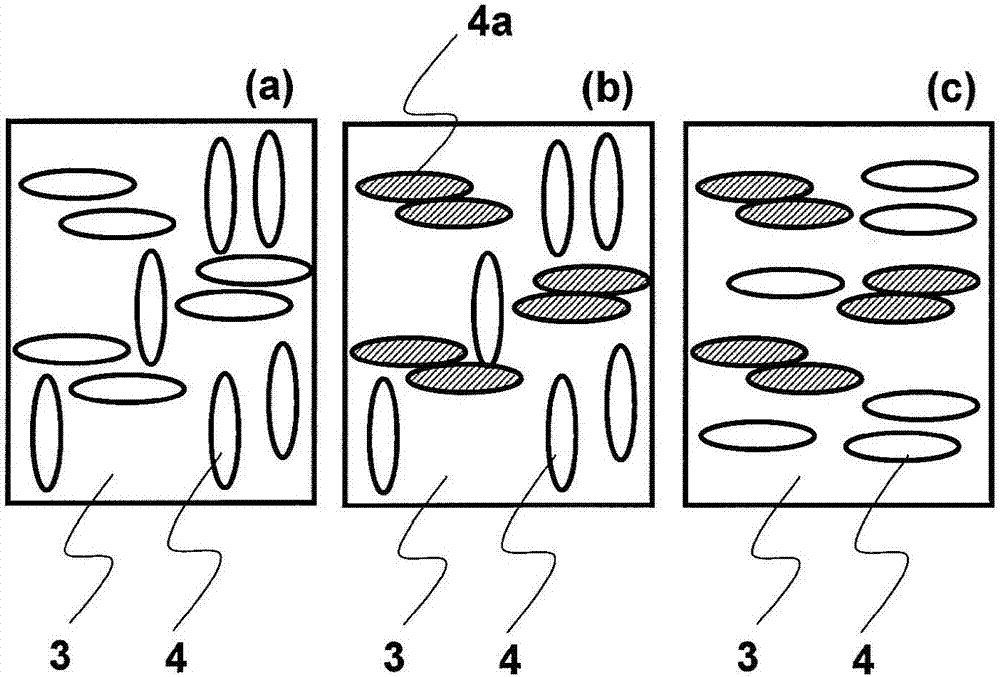
液晶顯示元件作為輕量、薄型且低能耗的顯示器件而被知曉,近年來,被用於大型的電視機用途等,取得了突飛猛進的發展。液晶顯示元件通過例如用具備電極的透明的一對基板夾持液晶層來構成。此外,液晶顯示元件中,以使液晶在基板間達到所需的取向狀態的條件,使用由有機材料構成的有機膜作為液晶取向膜。即,液晶取向膜是液晶顯示元件的構成構件,且形成於夾持液晶的基板與液晶接觸的面,起到在該基板間使液晶朝一定的方向取向的作用。而且,對於液晶取向膜,除了要求使液晶朝例如與基板平行的方向等的一定方向取向的作用外,有時還要求控制液晶的預傾角的作用。這樣的液晶取向膜中的控制液晶取向的能力(以下稱為取向控制能力)可通過對構成液晶取向膜的有機膜進行取向處理而賦予。作為用於賦予取向控制能力的液晶取向膜的取向處理方法,一直以來已知摩擦法。摩擦法是指,對於基板上的聚乙烯醇、聚醯胺或聚醯亞胺等有機膜,用棉、尼龍、聚酯等的布對其表面沿一定方向擦拭(摩擦),使液晶沿擦拭的方向(摩擦方向)取向的方法。該摩擦法能夠簡便地實現比較穩定的液晶的取向狀態,所以被利用在現有的液晶顯示元件的製造工藝中。此外,作為液晶取向膜所用的有機膜,主要選擇耐熱性等的可靠性及電特性優異的聚醯亞胺類的有機膜。但是,對由聚醯亞胺等構成的液晶取向膜的表面進行擦拭的摩擦法,存在揚塵及產生靜電的問題。此外,由於近年來的液晶顯示元件的高精細化、和因對應的基板上的電極或液晶驅動用的開關有源元件所產生的凹凸,有時無法用布對液晶取向膜表面進行均勻地摩擦,無法實現均勻的液晶取向。於是,作為無法進行摩擦的液晶取向膜的其他取向處理方法,正在積極地研究光取向法。光取向法有各種方法,利用直線偏振或準直後的光在構成液晶取向膜的有機膜內形成各向異性,根據該各向異性使液晶取向。作為主要的光取向法,已知分解型的光取向法。例如,對聚醯亞胺膜照射偏振紫外線,利用分子結構的紫外線吸收的偏振方向依賴性使其發生各向異性分解。接著,利用未分解而殘留的聚醯亞胺使液晶取向(例如參照專利文獻1)。此外,還已知光交聯型及光異構化型的光取向法。例如,使用聚肉桂酸乙烯酯,照射偏振紫外線,使與偏振光平行的兩個側鏈的雙鍵部分發生二聚化反應(交聯反應)。接著,使液晶在與偏振方向正交的方向上取向(例如參照非專利文獻1)。此外,使用側鏈具有偶氮苯的側鏈型高分子的情況下,照射偏振紫外線,使與偏振光平行的側鏈的偶氮苯部分發生異構化反應,使液晶在與偏振方向正交的方向上取向(例如參照非專利文獻2)。如以上的例那樣,採用光取向法的液晶取向膜的取向處理方法中,不需要摩擦,沒有揚塵及產生靜電之虞。於是,即使對於表面有凹凸的液晶顯示元件的基板也能實施取向處理,是適合於工業領域的生產工藝的液晶取向膜的取向處理方法。現有技術文獻專利文獻專利文獻1:日本專利特許第3893659號公報非專利文獻非專利文獻1:M.Shadt等,日本,《應用物理學雜誌(J.Appl.Phys.)》31,2155(1992).非專利文獻2:K.Ichimura等,《化學評論(Chem.Rev.)》,100,1847(2000).
技術實現要素:
發明所要解決的技術問題如上所述,光取向法與一直以來作為液晶顯示元件的取向處理方法在工業領域應用的摩擦法相比,不需要摩擦工序本身,因此具有很大優點。而且,與通過摩擦而進行的取向控制能力大致恆定的摩擦法相比,光取向法能改變偏振光的照射量來控制取向控制能力。但是,光取向法的情況下,在想要實現與通過摩擦法而進行的情況相同程度的取向控制能力時,有時需要大量的偏振光的照射量,或無法實現穩定的液晶取向。例如,上述的專利文獻1中記載的分解型的光取向法中,需要對聚醯亞胺膜照射60分鐘的來自輸出功率500W的高壓汞燈的紫外光等的需要長時間和大量的紫外線照射。此外,在二聚化型和光異構化型的光取向法的情況下,有時也需要幾J(焦耳)~幾十J程度的大量的紫外線照射。還有,光交聯型及光異構化型的光取向法的情況下,由於液晶取向的熱穩定性及光穩定性差,所以製成液晶顯示元件後,存在發生取向不良或顯示燒屏的問題。特別是水平電場驅動型的液晶顯示元件中,因為在平面內驅動液晶分子,所以容易發生液晶驅動後的液晶的取向偏差,由AC驅動引起的顯示燒屏成為較大的技術問題。因此,光取向法中,要求實現取向處理的高效率化及穩定的液晶取向,要求能高效地對液晶取向膜賦予高的取向控制能力的液晶取向膜及液晶取向劑。本發明的目的在於提供具有以高效率被賦予了取向控制能力的、燒屏特性優異的水平電場驅動型液晶顯示元件用液晶取向膜的基板,以及具有該基板的水平電場驅動型液晶顯示元件。解決技術問題所採用的技術方案本發明人為了解決上述技術問題進行了認真研究,結果發現了以下的發明。具有液晶取向膜的基板的製造方法,該液晶取向膜為通過下述方法得到的被賦予了取向控制能力的水平電場驅動型液晶顯示元件用液晶取向膜,該方法包括:[I]將含有(A)在規定的溫度範圍內呈現液晶性的感光性的側鏈型高分子、和(B)有機溶劑的聚合物組合物塗布在具有水平電場驅動用的導電膜的基板上以形成塗膜的工序;[II]對由[I]得到的塗膜照射偏振紫外線的工序;以及[III]對由[II]得到的塗膜進行加熱的工序。上述中,(A)成分可以具有發生光交聯、光異構化、或光弗利斯重排的感光性側鏈。上述或中,(A)成分可以具有選自下述式(1)~(6)的任一種感光性側鏈,[化1]式中,A、B、D分別獨立地表示單鍵、-O-、-CH2-、-COO-、-OCO-、-CONH-、-NH-CO-、-CH=CH-CO-O-、或-O-CO-CH=CH-;S是碳數1~12的亞烷基,它們所結合的氫原子可以被滷素基團取代;T是單鍵或碳數1~12的亞烷基,它們所結合的氫原子可以被滷素基團取代;Y1表示選自1價的苯環、萘環、聯苯環、呋喃環、吡咯環和碳數5~8的脂環式烴的環,或者是選自這些取代基的相同或不同的2~6個環通過連結基團B結合而成的基團,它們所結合的氫原子分別獨立地可以被-COOR0(式中,R0表示氫原子或碳數1~5的烷基)、-NO2、-CN、-CH=C(CN)2、-CH=CH-CN、滷素基團、碳數1~5的烷基、或碳數1~5的烷氧基取代;Y2是選自2價的苯環、萘環、聯苯環、呋喃環、吡咯環、碳數5~8的脂環式烴、以及它們的組合的基團,它們所結合的氫原子分別獨立地可以被-NO2、-CN、-CH=C(CN)2、-CH=CH-CN、滷素基團、碳數1~5的烷基、或碳數1~5的烷氧基取代;R表示羥基、碳數1~6的烷氧基,或表示與Y1相同的定義;X表示單鍵、-COO-、-OCO-、-N=N-、-CH=CH-、-C≡C-、-CH=CH-CO-O-、或-O-CO-CH=CH-,在X的數量為2時,X彼此可以相同或不同;Cou表示香豆素-6-基或香豆素-7-基,它們所結合的氫原子分別獨立地可以被-NO2、-CN、-CH=C(CN)2、-CH=CH-CN、滷素基團、碳數1~5的烷基、或碳數1~5的烷氧基取代;q1和q2中的一方為1,另一方為0;q3為0或1;P和Q分別獨立地為選自2價的苯環、萘環、聯苯環、呋喃環、吡咯環、碳數5~8的脂環式烴、以及它們的組合的基團;但是,X為-CH=CH-CO-O-、-O-CO-CH=CH-的情況下,-CH=CH-所結合的一側的P或Q為芳香環,P的數量為2以上時,P彼此可以相同或不同,Q的數量為2以上時,Q彼此可以相同或不同;l1為0或1;l2為0~2的整數;l1和l2均為0時,T為單鍵時A也表示單鍵;l1為1時,T為單鍵時B也表示單鍵;H和I分別獨立地為選自2價的苯環、萘環、聯苯環、呋喃環、吡咯環、和它們的組合的基團。上述或中,(A)成分可以具有選自下述式(7)~(10)的任一種感光性側鏈,[化2]式中,A、B、D、Y1、X、Y2、及R具有與上述相同的定義;l表示1~12的整數;m表示0~2的整數,m1、m2表示1~3的整數;n表示0~12的整數(其中n=0時B為單鍵)。上述或中,(A)成分可以具有選自下述式(11)~(13)的任一種感光性側鏈,[化3]式中,A、X、l、m、m1及R具有與上述相同的定義。上述或中,(A)成分可以具有以下述式(14)或(15)表示的感光性側鏈,[化4]式中,A、Y1、l、m1及m2具有與上述相同的定義。上述或中,(A)成分可以具有以下述式(16)或(17)表示的感光性側鏈,[化5]式中,A、X、l及m具有與上述相同的定義。上述或中,(A)成分可以具有以下述式(18)或(19)表示的感光性側鏈,[化6]式中,A、B、Y1、q1、q2、m1、及m2具有與上述相同的定義。R1表示氫原子、-NO2、-CN、-CH=C(CN)2、-CH=CH-CN、滷素基團、碳數1~5的烷基、或碳數1~5的烷氧基。上述或中,(A)成分可以具有以下述式(20)表示的感光性側鏈,[化7]式中,A、Y1、X、l及m具有與上述相同的定義。上述~的任一項中,(A)成分可以具有選自下述式(21)~(31)的任一種液晶性側鏈,[化8]式中,A、B、q1及q2具有與上述相同的定義;Y3是選自1價的苯環、萘環、聯苯環、呋喃環、含氮雜環和碳數5~8的脂環式烴、以及它們的組合的基團,它們所結合的氫原子分別獨立地可以被-NO2、-CN、滷素基團、碳數1~5的烷基、或碳數1~5的烷氧基取代;R3表示氫原子、-NO2、-CN、-CH=C(CN)2、-CH=CH-CN、滷素基團、1價的苯環、萘環、聯苯環、呋喃環、含氮雜環、碳數5~8的脂環式烴、碳數1~12的烷基、或碳數1~12的烷氧基;l表示1~12的整數,m表示0~2的整數,但是,式(23)~(24)中,全部的m的合計在2以上,式(25)~(26)中,全部的m的合計在1以上,m1、m2和m3分別獨立地表示1~3的整數;R2表示氫原子、-NO2、-CN、滷素基團、1價的苯環、萘環、聯苯環、呋喃環、含氮雜環和碳數5~8的脂環式烴、以及烷基、或烷氧基;Z1、Z2表示單鍵、-CO-、-CH2O-、-CH=N-、-CF2-。基板,其具有由上述~中任一項製造的水平電場驅動型液晶顯示元件用液晶取向膜。水平電場驅動型液晶顯示元件,其具有上述的基板。液晶顯示元件的製造方法,其為通過具有下述工序來得到水平電場驅動型液晶顯示元件的方法,該方法具有:準備上述的基板(第1基板)的工序;通過具有[I』]在第2基板上塗布含有(A)在規定的溫度範圍內呈現液晶性的感光性的側鏈型高分子、和(B)有機溶劑的聚合物組合物,以形成塗膜的工序;[II』]對由[I』]得到的塗膜照射偏振紫外線的工序;以及[III』]對由[II』]得到的塗膜進行加熱的工序而得到被賦予了取向控制能力的液晶取向膜,並得到具有該液晶取向膜的第2基板的工序;以及[IV]以使第1基板和第2基板的液晶取向膜介以液晶相對的方式,相向配置第1基板和第2基板,得到液晶顯示元件的工序。由上述製造的水平電場驅動型液晶顯示元件。水平電場驅動型液晶顯示元件用液晶取向膜的製造用組合物,其含有:(A)在規定的溫度範圍呈現液晶性的感光性的側鏈型高分子,以及(B)有機溶劑。以下述式(1)(式中,R表示氫原子或甲基;S表示碳數2~10的亞烷基)表示的化合物。[化9]以下述式(2)(式中,R表示氫原子或甲基;R10表示Br或CN;S表示碳數2~10的亞烷基)表示的化合物。[化10]以下述式(3)(式中,R表示氫原子或甲基;S表示碳數2~10的亞烷基)表示的化合物。[化11]以下述式(4)(式中,R表示氫原子或甲基;S表示碳數2~10的亞烷基;u表示0或1)表示的化合物。[化12]以下述式(5)(式中,R表示氫原子或甲基;S表示碳數2~10的亞烷基;u表示0或1)表示的化合物。[化13]以下述式(6)(式中,R表示氫原子或甲基;S表示碳數2~10的亞烷基)表示的化合物。[化14]以下述式(7)(式中,R表示氫原子或甲基;S表示碳數2~10的亞烷基)表示的化合物。[化15]以下述式(8)(式中,R表示氫原子或甲基;S表示碳數2~10的亞烷基)表示的化合物。[化16]以下述式(9)(式中,R表示氫原子或甲基;S表示碳數2~10的亞烷基)表示的化合物。[化17]以下述式(10)(式中,R表示氫原子或甲基;S表示碳數2~10的亞烷基)表示的化合物。[化18]以下述式(11)(式中,R表示氫原子或甲基;S表示碳數2~10的亞烷基;Py表示2-吡啶基、3-吡啶基或4-吡啶基;u表示0或1)表示的化合物。[化19]以下述式(12)(式中,S表示碳數2~9的亞烷基;v表示1或2)表示的化合物。[化20]以下述式(13)(式中,S表示碳數2~10的亞烷基;u表示0或1)表示的化合物。[化21]以下述式(14)(式中,S表示碳數1~10的亞烷基;u表示0或1)表示的化合物。[化22]以下述式(15)(式中,S表示碳數2~10的亞烷基)表示的化合物。[化23]以下述式(16)(式中,R表示氫原子或甲基;S表示碳數2~10的亞烷基)表示的化合物。[化24]以下述式(17)(式中,R表示氫原子或甲基;S表示碳數2~10的亞烷基)表示的化合物。[化25]1.水平電場驅動型液晶顯示元件的製造方法,其特徵是,經過下述工序:在具有水平電場驅動用的導電膜的基板上塗布含有(A)在規定的溫度範圍內呈現液晶性的感光性的側鏈型高分子、以及(B)有機溶劑的聚合物組合物,形成塗膜,通過紫外線的照射和其後的加熱得到被賦予了取向控制能力的一對帶塗膜的基板,將所得到的一對帶塗膜的基板以介以液晶分子層、使上述塗膜相對的方式相向配置,形成液晶晶胞。2.如1所述的方法,其特徵是,(A)成分具有發生光交聯、光異構化、或光弗利斯重排的側鏈。3.如1或2所述的方法,其特徵是,(A)成分具有下述式(1)~(8)的感光性側鏈,[化26]其中,A、B、D分別獨立地表示單鍵、-O-、-CH2-、-COO-、-OCO-、-CONH-、-NH-CO-;Y1是選自1價的苯環、萘環、聯苯環、呋喃環、吡咯環、碳數5~8的環狀烴、以及它們的組合的基團,它們所結合的氫原子分別獨立地可以被-NO2、-CN、-CH=C(CN)2、-CH=CH-CN、滷素基團、烷基、或烷氧基取代;X表示單鍵、-COO-、-OCO-、-N=N-、-CH=CH-、-C≡C-;l表示1~12的整數;m表示0~2的整數;m1、m2表示1~3的整數;n表示0~12的整數(其中n=0時B為單鍵);Y2為選自2價的苯環、萘環、聯苯環、呋喃環、吡咯環、碳數5~8的環狀烴、以及它們的組合的基團,它們所結合的氫原子分別獨立地可以被-NO2、-CN、-CH=C(CN)2、-CH=CH-CN、滷素基團、烷基、或烷氧基取代;R表示氫原子、及碳數1~6的烷基;R1表示氫原子-NO2、-CN、-CH=C(CN)2、-CH=CH-CN、滷素基團、烷基、或烷氧基。4.如1~3中任一項所述的方法,其特徵是,(A)成分具有下述式(5)~(13)的液晶性的側鏈,[化27]其中,A、B、Y1、R、l、m、m1、m2、及R1具有與上述相同的定義;Z1、Z2表示-CO-、-CH2O-、-C=N-、-CF2-。5.聚合物組合物,其特徵是,其為含有(A)在規定的溫度範圍內體現液晶性的感光性的側鏈型高分子,以及(B)有機溶劑的聚合物組合物,在1~4中任一項記載的水平電場驅動型液晶顯示元件的製造方法中,用於形成塗膜,該製造方法經過下述工序:在具有水平電場驅動用的導電膜的基板上形成塗膜,通過紫外線的照射和其後的加熱得到被賦予了取向控制能力的一對帶塗膜的基板,將所得到的一對帶塗膜的基板以介以液晶分子層、使上述塗膜相對的方式相向配置,形成液晶晶胞。6.液晶顯示元件,其特徵是,通過1~4中任一項所述的液晶顯示元件的製造方法製得。7.以下述式(1)表示的液晶性化合物,[化28]式中,R表示氫原子或甲基,S表示碳原子數2~10的亞烷基。發明效果根據本發明,能提供具有以高效率被賦予了取向控制能力的、燒屏特性優異的水平電場驅動型液晶顯示元件用液晶取向膜的基板,以及具有該基板的水平電場驅動型液晶顯示元件。根據本發明的方法製造的水平電場驅動型液晶顯示元件被高效地賦予了取向控制能力,所以即使長時間連續驅動也不會損害顯示特性。附圖說明圖1是示意地說明本發明中使用的液晶取向膜的製造方法中的各向異性導入處理的一個例子的圖,是在感光性的側鏈上使用交聯性的有機基團所導入的各向異性小的情況下的圖。圖2是示意地說明本發明中使用的液晶取向膜的製造方法中的各向異性導入處理的一個例子的圖,是在感光性的側鏈上使用交聯性的有機基團所導入的各向異性大的情況下的圖。圖3是示意地說明本發明中使用的液晶取向膜的製造方法中的各向異性導入處理的一個例子的圖,是在感光性的側鏈上使用發生弗利斯重排或異構化的有機基團所導入的各向異性小的情況下的圖。圖4是示意地說明本發明中使用的液晶取向膜的製造方法中的各向異性導入處理的一個例子的圖,是在感光性的側鏈上使用發生弗利斯重排或異構化的有機基團所導入的各向異性大的情況下的圖。具體實施方式本發明人進行了認真研究,結果獲得以下發現,從而完成了本發明。本發明的製造方法中所用的聚合物組合物具有能呈現液晶性的感光性的側鏈型高分子(以下也簡稱為側鏈型高分子),使用上述聚合物組合物而得的塗膜是具有能呈現液晶性的感光性的側鏈型高分子的膜。對於該塗膜無需進行摩擦處理,通過偏振光照射來進行取向處理。接著,偏振光照射後,經過對該側鏈型高分子膜進行加熱的工序,形成被賦予了取向控制能力的塗膜(以下也稱為液晶取向膜)。此時,通過偏振光照射而呈現的微小的各向異性成為驅動力,液晶性的側鏈型高分子自身通過自組織化而高效地再取向。其結果是,作為液晶取向膜,可得到實現高效率的取向處理、被賦予了高取向控制能力的液晶取向膜。下面,對本發明的實施方式進行詳細說明。及具有本發明的液晶配向膜的基板的製造方法包括:[I]將含有(A)在規定的溫度範圍內呈現液晶性的感光性的側鏈型高分子、和(B)有機溶劑的聚合物組合物塗布在具有水平電場驅動用的導電膜的基板上以形成塗膜的工序;[II]對由[I]得到的塗膜照射偏振紫外線的工序;以及[III]對由[II]得到的塗膜進行加熱的工序。通過上述工序,可得到被賦予了取向控制能力的水平電場驅動型液晶顯示元件用液晶取向膜,可得到具有該液晶取向膜的基板。此外,通過除了上述得到的基板(第1基板)之外還準備第2基板,可得到水平電場驅動型液晶顯示元件。第2基板除了使用不具有水平電場驅動用的導電膜的基板來代替具有水平電場驅動用的導電膜的基板以外,通過採用上述工序[I]~[III](因為使用不具有水平電場驅動用的導電膜的基板,所以方便起見,本申請中,有時也簡記為工序[I』]~[III』]),可得到具有被賦予了取向控制能力的液晶取向膜的第2基板。水平電場驅動型液晶顯示元件的製造方法包括[IV]:以使第1基板和第2基板的液晶取向膜介以液晶相對的方式,相向配置上述得到的第1基板和第2基板,得到液晶顯示元件的工序。藉此,可得到水平電場驅動型液晶顯示元件。以下,對本發明的製造方法所具有的[I]~[III]、以及[IV]的各工序進行說明。工序[I]中,在具有水平電場驅動用的導電膜的基板上塗布含有在規定的溫度範圍內呈現液晶性的感光性的側鏈型高分子和有機溶劑的聚合物組合物,形成塗膜。對於基板沒有特別限定,所製造的液晶顯示元件是透射型的情況下,優選使用透明性高的基板。該情況下,沒有特別限定,可使用玻璃基板、或丙烯酸基板、聚碳酸酯基板等的塑料基板等。此外,考慮到在反射型的液晶顯示元件中的應用,也可使用矽晶片等不透明的基板。基板具有水平電場驅動用的導電膜。作為該導電膜,在液晶顯示元件為透射型的情況下,可例舉ITO(IndiumTinOxide:氧化銦錫)、IZO(IndiumZincOxide:氧化銦鋅)等,但不局限於此。此外,反射型的液晶顯示元件的情況下,作為導電膜,可例舉鋁等反射光的材料等,但不局限於此。在基板上形成導電膜的方法可使用目前公知的方法。在具有水平電場驅動用的導電膜的基板上、特別是導電膜上,塗布聚合物組合物。本發明的製造方法中所用的該聚合物組合物含有(A)在規定的溫度範圍內呈現液晶性的感光性的側鏈型高分子;及(B)有機溶劑。<>(A)成分是在規定的溫度範圍內呈現液晶性的感光性的側鏈型高分子。(A)側鏈型高分子可以在250nm~400nm的波長範圍的光的作用下反應,且在100℃~300℃的溫度範圍內呈現出液晶性。(A)側鏈型高分子優選具有在250nm~400nm的波長範圍的光作用下反應的感光性側鏈。(A)側鏈型高分子優選為了在100℃~300℃的溫度範圍內呈現出液晶性而具有介晶基團(日文:メソゲン基)。(A)側鏈型高分子在主鏈結合有具有感光性的側鏈,能夠對光產生感應而發生交聯反應、異構化反應、或光弗利斯重排。對具有感光性的側鏈的結構沒有特別限定,理想的是對光產生感應而發生交聯反應、或光弗利斯重排的結構,更理想的是發生交聯反應的結構。該情況下,即使暴露於熱等外部應力,也能夠長時間穩定地保持所實現的取向控制能力。能呈現出液晶性的感光性的側鏈型高分子膜的結構只要滿足該特性就沒有特別限定,優選側鏈結構中具有剛性的介晶成分(日文:メソゲン成分)。該情況下,將該側鏈型高分子製成液晶取向膜後,能得到穩定的液晶取向。該高分子的結構可以是例如下述結構:具有主鏈和該主鏈所結合的側鏈,該側鏈具有聯苯基、三聯苯基、苯基環己基、苯甲酸苯酯、偶氮苯基等介晶成分,和前端部所結合的對光產生感應而發生交聯反應或異構化反應的感光性基團;或具有主鏈和該主鏈所結合的側鏈,該側鏈也構成介晶成分,且具有發生光弗利斯重排反應的苯甲酸苯酯。作為能呈現液晶性的感光性的側鏈型高分子膜的結構更具體的例子,優選具有下述的主鏈和側鏈的結構;主鏈由選自烴、(甲基)丙烯酸酯、衣康酸酯、富馬酸酯、馬來酸酯、α-亞甲基-γ-丁內酯、苯乙烯、乙烯基、馬來醯亞胺、降冰片烯等自由基聚合性基團和矽氧烷的至少一種構成;側鏈由選自下述式(1)~(6)的至少一種構成。[化29]式中,A、B、D分別獨立地表示單鍵、-O-、-CH2-、-COO-、-OCO-、-CONH-、-NH-CO-、-CH=CH-CO-O-、或-O-CO-CH=CH-;S是碳數1~12的亞烷基,它們所結合的氫原子可以被滷素基團取代;T是單鍵或碳數1~12的亞烷基,它們所結合的氫原子可以被滷素基團取代;Y1表示選自1價的苯環、萘環、聯苯環、呋喃環、吡咯環和碳數5~8的脂環式烴的環,或是選自這些取代基的相同或不同的2~6的環通過連結基團B結合而成的基團,它們所結合的氫原子分別獨立地可以被-COOR0(式中,R0表示氫原子或碳數1~5的烷基)、-NO2、-CN、-CH=C(CN)2、-CH=CH-CN、滷素基團、碳數1~5的烷基、或碳數1~5的烷氧基取代;Y2是選自2價的苯環、萘環、聯苯環、呋喃環、吡咯環、碳數5~8的脂環式烴、和它們的組合的基團,它們所結合的氫原子分別獨立地可以被-NO2、-CN、-CH=C(CN)2、-CH=CH-CN、滷素基團、碳數1~5的烷基、或碳數1~5的烷氧基取代;R表示羥基、碳數1~6的烷氧基,或表示與Y1相同的定義;X表示單鍵、-COO-、-OCO-、-N=N-、-CH=CH-、-C≡C-、-CH=CH-CO-O-、或-O-CO-CH=CH-,X的數量為2時,X彼此可以相同或不同;Cou表示香豆素-6-基或香豆素-7-基,它們所結合的氫原子分別獨立地可以被-NO2、-CN、-CH=C(CN)2、-CH=CH-CN、滷素基團、碳數1~5的烷基、或碳數1~5的烷氧基取代;q1和q2中的一方為1,另一方為0;q3是0或1;P和Q分別獨立地為選自2價的苯環、萘環、聯苯環、呋喃環、吡咯環、碳數5~8的脂環式烴、和它們的組合的基團;其中,X為-CH=CH-CO-O-、-O-CO-CH=CH-時,-CH=CH-所結合的一側的P或Q是芳香環,P的數量為2以上時,P彼此可以相同或不同,Q的數量為2以上時,Q彼此可以相同或不同;l1為0或1;l2為0~2的整數;l1和l2都為0時,T為單鍵時A也表示單鍵;l1為1時,T為單鍵時B也表示單鍵;H和I分別獨立地為選自2價的苯環、萘環、聯苯環、呋喃環、吡咯環、和它們的組合的基團。側鏈可以是選自下述式(7)~(10)的任一種感光性側鏈。式中,A、B、D、Y1、X、Y2、及R具有與上述相同的定義;l表示1~12的整數;m表示0~2的整數,m1、m2表示1~3的整數;n表示0~12的整數(其中,n=0時B為單鍵)。[化30]側鏈可以是選自下述式(11)~(13)的任一種感光性側鏈。式中,A、X、l、m、m1及R具有與上述相同的定義。[化31]側鏈可以是以下述式(14)或(15)表示的感光性側鏈。式中,A、Y1、l、m1及m2具有與上述相同的定義。[化32]側鏈可以是以下述式(16)或(17)表示的感光性側鏈。式中,A、X、l、及m具有與上述相同的定義。[化33]此外,側鏈可以是以下述式(18)或(19)表示的感光性側鏈。式中,A、B、Y1、q1、q2、m1、及m2具有與上述相同的定義。R1表示氫原子、-NO2、-CN、-CH=C(CN)2、-CH=CH-CN、滷素基團、碳數1~5的烷基、或碳數1~5的烷氧基。[化34]側鏈可以是以下述式(20)表示的感光性側鏈。式中,A、Y1、X、l及m具有與上述相同的定義。[化35]此外,(A)側鏈型高分子可以具有選自下述式(21)~(31)的至少一種液晶性側鏈。式中,A、B、q1及q2具有與上述相同的定義。Y3是選自1價的苯環、萘環、聯苯環、呋喃環、含氮雜環、和碳數5~8的脂環式烴、以及它們的組合的基團,它們所結合的氫原子分別獨立地可以被-NO2、-CN、滷素基團、碳數1~5的烷基、或碳數1~5的烷氧基取代;R3表示氫原子、-NO2、-CN、-CH=C(CN)2、-CH=CH-CN、滷素基團、1價的苯環、萘環、聯苯環、呋喃環、含氮雜環、碳數5~8的脂環式烴、碳數1~12的烷基、或碳數1~12的烷氧基。l表示1~12的整數,m表示0~2的整數,但是,式(23)~(24)中,全部的m的合計在2以上,式(25)~(26)中,全部的m的合計在1以上,m1、m2和m3分別獨立地表示1~3的整數;R2表示氫原子、-NO2、-CN、滷素基團、1價的苯環、萘環、聯苯環、呋喃環、含氮雜環、和碳數5~8的脂環式烴、以及烷基、或烷氧基;Z1、Z2表示單鍵、-CO-、-CH2O-、-CH=N-、-CF2-。[化36]<>上述能呈現液晶性的感光性的側鏈型高分子可通過使具有上述的感光性側鏈的光反應性側鏈單體和液晶性側鏈單體進行聚合而得到。[光反應性側鏈單體]光反應性側鏈單體是指形成高分子的情況下,在高分子的側鏈部位可形成具有感光性側鏈的高分子的單體。作為側鏈所具有的光反應性基團,優先下述的結構及其衍生物。[化37]作為光反應性側鏈單體的更具體的例子,優選具有下述聚合性基團和感光性側鏈的結構;所述聚合性基團由選自烴、(甲基)丙烯酸酯、衣康酸酯、富馬酸酯、馬來酸酯、α-亞甲基-γ-丁內酯、苯乙烯、乙烯、馬來醯亞胺、降冰片烯等的自由基聚合性基團和矽氧烷的至少一種構成;所述感光性側鏈為由上述式(1)~(6)的至少一種構成的感光性側鏈,優選例如由上述式(7)~(10)的至少一種構成的感光性側鏈,由上述式(11)~(13)的至少一種構成的感光性側鏈,以上述式(14)或(15)表示的感光性側鏈,以上述式(16)或(17)表示的感光性側鏈,以上述式(18)或(19)表示的感光性側鏈,以上述式(20)表示的感光性側鏈。本申請中,作為光反應性和/或液晶性側鏈單體,提供以下的新型化合物。以下述式(1)(式中,R表示氫原子或甲基;S表示碳數2~10的亞烷基)表示的化合物,[化38]以下述式(2)(式中,R表示氫原子或甲基;R10表示Br或CN;S表示碳數2~10的亞烷基)表示的化合物,[化39]以下述式(3)(式中,R表示氫原子或甲基;S表示碳數2~10的亞烷基)表示的化合物,[化40]以下述式(4)(式中,R表示氫原子或甲基;S表示碳數2~10的亞烷基;u表示0或1)表示的化合物,[化41]以下述式(5)(式中,R表示氫原子或甲基;S表示碳數2~10的亞烷基;u表示0或1)表示的化合物,[化42]以下述式(6)(式中,R表示氫原子或甲基;S表示碳數2~10的亞烷基)表示的化合物,[化43]以下述式(7)(式中,R表示氫原子或甲基;S表示碳數2~10的亞烷基)表示的化合物,[化44]以下述式(8)(式中,R表示氫原子或甲基;S表示碳數2~10的亞烷基)表示的化合物,[化45]以下述式(9)(式中,R表示氫原子或甲基;S表示碳數2~10的亞烷基)表示的化合物,[化46]以下述式(10)(式中,R表示氫原子或甲基;S表示碳數2~10的亞烷基)表示的化合物,[化47]以下述式(11)(式中,R表示氫原子或甲基;S表示碳數2~10的亞烷基;Py表示2-吡啶基、3-吡啶基或4-吡啶基;u表示0或1)表示的化合物,[化48]以下述式(12)(式中,S表示碳數2~9的亞烷基;v表示1或2)表示的化合物,[化49]以下述式(13)(式中,S表示碳數2~10的亞烷基;u表示0或1)表示的化合物,[化50]以下述式(14)(式中,S表示碳數1~10的亞烷基;u表示0或1)表示的化合物,[化51]以下述式(15)(式中,S表示碳數2~10的亞烷基)表示的化合物,[化52]以下述式(16)(式中,R表示氫原子或甲基;S表示碳數2~10的亞烷基)表示的化合物,[化53]以下述式(17)(式中,R表示氫原子或甲基;S表示碳數2~10的亞烷基)表示的化合物,[化54][液晶性側鏈單體]液晶性側鏈單體是指下述單體:來源於該單體的高分子呈現液晶性,該高分子在側鏈部位可形成介晶基團的單體。作為側鏈所具有的介晶基團,可以是聯苯或苯甲酸苯酯等單獨形成介晶結構的基團,也可以是苯甲酸等那樣的側鏈之間通過氫鍵形成介晶結構的基團。作為側鏈所具有的介晶基團,優選下述的結構。[化55]作為液晶性側鏈單體的更具體的例子,優選具有聚合性基團和由上述式(21)~(31)的至少一種構成的側鏈的結構,所述聚合性基團由選自烴、(甲基)丙烯酸酯、衣康酸酯、富馬酸酯、馬來酸酯、α-亞甲基-γ-丁內酯、苯乙烯、乙烯基、馬來醯亞胺、降冰片烯等的自由基聚合性基團和矽氧烷的至少一種構成。(A)側鏈型高分子可通過上述的呈現液晶性的光反應性側鏈單體的聚合反應而得到。此外,可通過不呈現液晶性的光反應性側鏈單體和液晶性側鏈單體的共聚,或呈現液晶性的光反應性側鏈單體和液晶性側鏈單體的共聚而得到。還有,可以在不損害呈現液晶性的能力的範圍內與其他單體共聚。作為其他單體,可例舉例如能工業上獲得的能進行自由基聚合反應的單體。作為其他單體的具體例,可例舉不飽和羧酸、丙烯酸酯化合物、甲基丙烯酸酯化合物、馬來醯亞胺化合物、丙烯腈、馬來酸酐、苯乙烯化合物及乙烯基化合物等。作為不飽和羧酸的具體例,可例舉丙烯酸、甲基丙烯酸、衣康酸、馬來酸、富馬酸等。作為丙烯酸酯化合物,例如可例舉丙烯酸甲酯、丙烯酸乙酯、丙烯酸異丙酯、丙烯酸苄酯、丙烯酸萘酯、丙烯酸蒽酯、丙烯酸蒽基甲酯、丙烯酸苯酯、丙烯酸2,2,2-三氟乙酯、丙烯酸叔丁酯、丙烯酸環己酯、丙烯酸異冰片酯、丙烯酸2-甲氧基乙酯、丙烯酸甲氧基三乙二醇酯、丙烯酸2-乙氧基乙酯、丙烯酸四氫糠基酯、丙烯酸3-甲氧基丁酯、丙烯酸2-甲基-2-金剛烷基酯、丙烯酸2-丙基-2-金剛烷基酯、丙烯酸8-甲基-8-三環癸酯和丙烯酸8-乙基-8-三環癸酯等。作為甲基丙烯酸酯化合物,例如可例舉甲基丙烯酸甲酯、甲基丙烯酸乙酯、甲基丙烯酸異丙酯、甲基丙烯酸苄酯、甲基丙烯酸萘酯、甲基丙烯酸蒽酯、甲基丙烯酸蒽基甲酯、甲基丙烯酸苯酯、甲基丙烯酸2,2,2-三氟乙酯、甲基丙烯酸叔丁酯、甲基丙烯酸環己酯、甲基丙烯酸異冰片酯、甲基丙烯酸2-甲氧基乙酯、甲基丙烯酸甲氧基三乙二醇酯、甲基丙烯酸2-乙氧基乙酯、甲基丙烯酸四氫糠基酯、甲基丙烯酸3-甲氧基丁酯、甲基丙烯酸2-甲基-2-金剛烷基酯、甲基丙烯酸2-丙基-2-金剛烷基酯、甲基丙烯酸8-甲基-8-三環癸酯和甲基丙烯酸8-乙基-8-三環癸酯等。也可以使用(甲基)丙烯酸縮水甘油酯、(甲基)丙烯酸(3-甲基-3-氧雜環丁烷基)甲酯、以及(甲基)丙烯酸(3-乙基-3-氧雜環丁烷基)甲酯等具有環狀醚基的(甲基)丙烯酸酯化合物。作為乙烯基化合物,可例舉例如乙烯基醚、甲基乙烯基醚、苄基乙烯基醚、2-羥乙基乙烯基醚、苯基乙烯基醚、及丙基乙烯基醚等。作為苯乙烯化合物,可例舉例如苯乙烯、甲基苯乙烯、氯苯乙烯、溴苯乙烯等。作為馬來醯亞胺化合物,可例舉例如馬來醯亞胺、N-甲基馬來醯亞胺、N-苯基馬來醯亞胺、及N-環己基馬來醯亞胺等。對於本實施方式的側鏈型高分子的製造方法沒有特別限定,可以使用工業上採用的通用的方法。具體而言,可通過利用液晶性側鏈單體及光反應性側鏈單體的乙烯基的陽離子聚合、自由基聚合、陰離子聚合來製造。其中,從反應控制的容易度等的觀點考慮,特別優選自由基聚合。作為自由基聚合的聚合引發劑,可使用自由基聚合引發劑、可逆的加成-斷裂型鏈轉移(RAFT)聚合試劑等的公知化合物。自由基熱聚合引發劑是通過加熱到分解溫度以上而產生自由基的化合物。作為這樣的自由基熱聚合引發劑,可例舉例如過氧化酮類(過氧化甲乙酮、過氧化環己酮等)、過氧化二醯類(過氧化乙醯、過氧化苯甲醯等)、過氧化氫類(過氧化氫、過氧化叔丁基、氫過氧化枯烯等)、過氧化二烷基類(過氧化二叔丁基、過氧化二枯基、過氧化二月桂醯等)、過氧化縮酮類(二丁基過氧化環己酮等)、烷基過氧化酯類(過氧化新癸酸叔丁酯、過氧化叔戊酸叔丁酯、過氧化2-乙基環己酸叔戊酯等)、過硫酸鹽類(過硫酸鉀、過硫酸鈉、過硫酸銨等)、偶氮類化合物(偶氮二異丁腈、及2,2′-二(2-羥乙基)偶氮二異丁腈等)。這樣的自由基熱聚合引發劑可單獨使用1種,或者也可將2種以上組合使用。自由基光聚合引發劑只要是通過光照射而引發自由基聚合的化合物,就沒有特別限定。作為這樣的自由基光聚合引發劑,可例舉二苯酮、米蚩酮、4,4』-雙(二乙基氨基)二苯酮、呫噸酮、噻噸酮、異丙基呫噸酮、2,4-二乙基噻噸酮、2-乙基蒽醌、苯乙酮、2-羥基-2-甲基苯丙酮、2-羥基-2-甲基-4』-異丙基苯丙酮、1-羥基環己基苯基酮、異丙基苯偶姻醚、異丁基苯偶姻醚、2,2-二乙氧基苯乙酮、2,2-二甲氧基-2-苯基苯乙酮、樟腦醌、苯並蒽酮、2-甲基-1-[4-(甲硫基)苯基]-2-嗎啉基丙烷-1-酮、2-苄基-2-二甲基氨基-1-(4-嗎啉基苯基)-丁酮-1、4-二甲基氨基苯甲酸乙酯、4-二甲基氨基苯甲酸異戊酯、4,4』-二(叔丁基過氧化羰基)二苯酮、3,4,4』-三(叔丁基過氧化羰基)二苯酮、2,4,6-三甲基苯甲醯基二苯基氧化膦、2-(4』-甲氧基苯乙烯基)-4,6-雙(三氯甲基)-s-三嗪、2-(3』,4』-二甲氧基苯乙烯基)-4,6-雙(三氯甲基)-s-三嗪、2-(2』,4』-二甲氧基苯乙烯基)-4,6-雙(三氯甲基)-s-三嗪、2-(2』-甲氧基苯乙烯基)-4,6-雙(三氯甲基)-s-三嗪、2-(4』-戊氧基苯乙烯基)-4,6-雙(三氯甲基)-s-三嗪、4-[對N,N-二(乙氧基羰基甲基)]-2,6-二(三氯甲基)-s-三嗪、1,3-雙(三氯甲基)-5-(2』-氯苯基)-s-三嗪、1,3-雙(三氯甲基)-5-(4』-甲氧基苯基)-s-三嗪、2-(對二甲基氨基苯乙烯基)苯並唑、2-(對二甲基氨基苯乙烯基)苯並噻唑、2-巰基苯並噻唑、3,3』-羰基雙(7-二乙基氨基香豆素)、2-(鄰氯苯基)-4,4』,5,5』-四苯基-1,2』-聯咪唑、2,2』-雙(2-氯苯基)-4,4』,5,5』-四(4-乙氧基羰基苯基)-1,2』-聯咪唑、2,2』-雙(2,4-二氯苯基)-4,4』,5,5』-四苯基-1,2』-聯咪唑、2,2』雙(2,4-二溴苯基)-4,4』,5,5』-四苯基-1,2』-聯咪唑、2,2』-雙(2,4,6-三氯苯基)-4,4』,5,5』-四苯基-1,2』-聯咪唑、3-(2-甲基-2-二甲基氨基丙醯基)咔唑、3,6-雙(2-甲基-2-嗎啉基丙醯基)-9-正十二烷基咔唑、1-羥基環己基苯基酮、雙(5-2,4-環戊二烯-1-基)-雙(2,6-二氟-3-(1H-吡咯-1-基)-苯基)鈦、3,3』,4,4』-四(叔丁基過氧化羰基)二苯酮、3,3』,4,4』-四(叔己基過氧化羰基)二苯酮、3,3』-二(甲氧基羰基)-4,4』-二(叔丁基過氧化羰基)二苯酮、3,4』-二(甲氧基羰基)-4,3』-二(叔丁基過氧化羰基)二苯酮、4,4』-二(甲氧基羰基)-3,3』-二(叔丁基過氧化羰基)二苯酮、2-(3-甲基-3H-苯並噻唑-2-亞基)-1-萘-2-基-乙酮、或2-(3-甲基-1,3-苯並噻唑-2(3H)-亞基)-1-(2-苯甲醯基)乙酮等。這些化合物可單獨使用,也可以將2種以上混合使用。自由基聚合法沒有特別限定,可以使用乳液聚合法、懸浮聚合法、分散聚合法、沉澱聚合法、本體聚合法、溶液聚合法等。作為能呈現液晶性的感光性的側鏈型高分子的聚合反應中使用的有機溶劑,只要是能溶解生成的高分子的溶劑就沒有特別限定。下面例舉其具體例。可例舉N,N-二甲基甲醯胺、N,N-二甲基乙醯胺、N-甲基-2-吡咯烷酮、N-乙基-2-吡咯烷酮、N-甲基己內醯胺、二甲亞碸、四甲基脲、吡啶、二甲碸、六甲亞碸、γ-丁內酯、異丙醇、甲氧基甲基戊醇、二戊烯、乙基戊基酮、甲基壬基酮、甲基乙基酮、甲基異戊基酮、甲基異丙基酮、甲基溶纖劑、乙基溶纖劑、甲基溶纖劑乙酸酯、乙基溶纖劑乙酸酯、丁基卡必醇、乙基卡必醇、乙二醇、乙二醇單乙酸酯、乙二醇單異丙基醚、乙二醇單丁基醚、丙二醇、丙二醇單乙酸酯、丙二醇單甲基醚、丙二醇叔丁基醚、二丙二醇單甲基醚、二乙二醇、二乙二醇單乙酸酯、二乙二醇二甲基醚、二丙二醇單乙酸酯單甲基醚、二丙二醇單甲基醚、二丙二醇單乙基醚、二丙二醇單乙酸酯單乙基醚、二丙二醇單丙基醚、二丙二醇單乙酸酯單丙基醚、3-甲基-3-甲氧基丁基乙酸酯、三丙二醇甲基醚、3-甲基-3-甲氧基丁醇、二異丙醚、乙基異丁基醚、二異丁烯、乙酸戊酯、丁酸丁酯、丁醚、二異丁酮、甲基環己烯、丙醚、二己醚、二烷、正己烷、正庚烷、正辛烷、二乙醚、環己酮、碳酸亞乙酯、碳酸亞丙酯、乳酸甲酯、乳酸乙酯、乙酸甲酯、乙酸乙酯、乙酸正丁酯、乙酸丙二醇酯單乙基醚、丙酮酸甲酯、丙酮酸乙酯、3-甲氧基丙酸甲酯、3-乙氧基丙酸甲乙酯、3-甲氧基丙酸乙酯、3-乙氧基丙酸、3-甲氧基丙酸、3-甲氧基丙酸丙酯、3-甲氧基丙酸丁酯、二甘醇二甲醚、4-羥基-4-甲基-2-戊酮、3-甲氧基-N,N-二甲基丙醯胺、3-乙氧基-N,N-二甲基丙醯胺、3-丁氧基-N,N-二甲基丙醯胺等。這些有機溶劑可以單獨使用,也可以混合使用。此外,即使是不溶解生成的高分子的溶劑,只要是在生成的高分子不析出的範圍內,也可以混合在上述有機溶劑中使用。此外,自由基聚合中,有機溶劑中的氧是阻礙聚合反應的原因,所以有機溶劑優選使用儘可能地脫氣後的有機溶劑。自由基聚合時的聚合溫度可選擇30℃~150℃的任意溫度,但優選50℃~100℃的範圍。此外,反應能以任意的濃度進行,但如果濃度過低則難以得到高分子量的聚合物,如果濃度過高則反應液的粘性過高,難以進行均勻的攪拌,所以單體濃度優選1質量%~50質量%,更優選5質量%~30質量%。也可以反應初期在高濃度下進行,之後追加有機溶劑。上述的自由基聚合反應中,自由基聚合引發劑的比率相對於單體如果較多則所得的高分子的分子量變小,如果較少則所得的高分子的分子量變大,所以自由基引發劑的比率相對於進行聚合的單體優選為0.1摩爾%~10摩爾%。此外,聚合時還可以追加各種單體成分、溶劑、引發劑等。[聚合物的回收]從通過上述的反應得到的能呈現液晶性的感光性的側鏈型高分子的反應溶液回收生成的高分子的情況下,將反應溶液投入不良溶劑,使這些聚合物沉澱即可。作為沉澱中使用的不良溶劑,可例舉甲醇、丙酮、己烷、庚烷、丁基溶纖劑、庚烷、甲基乙基酮、甲基異丁基酮、乙醇、甲苯、苯、二乙醚、甲基乙基醚、水等。投入到不良溶劑中而沉澱的聚合物可以在過濾回收之後,在常壓或減壓下、常溫或加熱下進行乾燥。另外,如果重複進行2~10次使沉澱回收的聚合物再溶解於有機溶劑並再沉澱回收的操作,則可以減少聚合物中的雜質。作為此時的不良溶劑,可例舉例如醇類、酮類、烴類等,如果使用選自這些溶劑的3種以上的不良溶劑,則由於純化效率進一步提高而優選。關於本發明的(A)側鏈型高分子的分子量,在考慮所得的塗膜的強度、塗膜形成時的作業性、以及塗膜的均勻性的情況下,通過GPC(GelPermeationChromatography:凝膠滲透色譜)法測得的重均分子量優選2000~1000000,更優選5000~100000。[聚合物組合物的製備]本發明中所用的聚合物組合物優選以適合形成液晶取向膜的方式製備成塗布液。即,本發明中使用的聚合物組合物優選製備成用於形成樹脂被膜的樹脂成分溶解於有機溶劑中而得的溶液。這裡,該樹脂成分是包含已說明的能呈現液晶性的感光性的側鏈型高分子的樹脂成分。此時,樹脂成分的含量優選1質量%~20質量%,更優選1質量%~15質量%,特別優選1質量%~10質量%。本實施方式的聚合物組合物中,上述的樹脂成分可以全部都是上述的能呈現液晶性的感光性的側鏈型高分子,但在不損害液晶呈現能力和感光性能力的範圍內也可以混合除此以外的其他聚合物。此時,樹脂成分中的其他聚合物的含量為0.5質量%~80質量%,優選1質量%~50質量%。這樣的其他聚合物可由例如聚(甲基)丙烯酸酯、聚醯胺酸及聚醯亞胺等構成,可例舉不是能呈現液晶性的感光性的側鏈型高分子的聚合物等。本發明所用的聚合物組合物中使用的有機溶劑,只要是能夠溶解樹脂成分的有機溶劑即可,無特別限定。下面例舉其具體例。可例舉N,N-二甲基甲醯胺、N,N-二甲基乙醯胺、N-甲基-2-吡咯烷酮、N-甲基己內醯胺、2-吡咯烷酮、N-乙基吡咯烷酮、N-乙烯基吡咯烷酮、二甲亞碸、四甲基脲、吡啶、二甲碸、六甲亞碸、γ-丁內酯、3-甲氧基-N,N-二甲基丙醯胺、3-乙氧基-N,N-二甲基丙醯胺、3-丁氧基-N,N-二甲基丙醯胺、1,3-二甲基-咪唑啉酮、乙基戊基酮、甲基壬基酮、甲基乙基酮、甲基異戊基酮、甲基異丙基酮、環己酮、碳酸亞乙酯、碳酸亞丙酯、二甘醇二甲醚、4-羥基-4-甲基-2-戊酮、丙二醇單乙酸酯、丙二醇單甲基醚、丙二醇叔丁基醚、二丙二醇單甲基醚、二乙二醇、二乙二醇單乙酸酯、二乙二醇單甲基醚、二丙二醇單乙酸酯單甲基醚、二丙二醇單甲基醚、二丙二醇單乙基醚、二丙二醇單乙酸酯單乙基醚、二丙二醇單丙基醚、二丙二醇單乙酸酯單丙基醚、3-甲基-3-甲氧基丁基乙酸酯、三丙二醇甲基醚等。這些溶劑可以單獨使用,也可以混合使用。本發明中使用的聚合物組合物可以含有上述(A)和(B)成分以外的成分。作為其例子,可例舉能提高塗布聚合物組合物時的膜厚均勻性或表面平滑性的溶劑及化合物、能提高液晶取向膜和基板的密合性的化合物等,但不限定於此。作為能提高膜厚的均勻性或表面平滑性的溶劑(不良溶劑)的具體例,可例舉以下物質。例如,可例舉異丙醇、甲氧基甲基戊醇、甲基溶纖劑、乙基溶纖劑、丁基溶纖劑、甲基溶纖劑乙酸酯、乙基溶纖劑乙酸酯、丁基卡必醇、乙基卡必醇、乙基卡必醇乙酸酯、乙二醇、乙二醇單乙酸酯、乙二醇單異丙基醚、乙二醇單丁基醚、丙二醇、丙二醇單乙酸酯、丙二醇單甲基醚、丙二醇叔丁基醚、二丙二醇單甲基醚、二乙二醇、二乙二醇單乙酸酯、二乙二醇二甲醚、二丙二醇單乙酸酯單甲基醚、二丙二醇單甲基醚、二丙二醇單乙基醚、二丙二醇單乙酸酯單乙基醚、二丙二醇單丙基醚、二丙二醇單乙酸酯單丙基醚、3-甲基-3-甲氧基丁基乙酸酯、三丙二醇甲基醚、3-甲基-3-甲氧基丁醇、二異丙醚、乙基異丁基醚、二異丁烯、乙酸戊酯、丁酸丁酯、丁醚、二異丁酮、甲基環己烯、丙醚、二己醚、1-己醇、正己烷、正戊烷、正辛烷、二乙醚、乳酸甲酯、乳酸乙酯、乙酸甲酯、乙酸乙酯、乙酸正丁酯、乙酸丙二醇酯單乙基醚、丙酮酸甲酯、丙酮酸乙酯、3-甲氧基丙酸甲酯、3-乙氧基丙酸甲乙酯、3-甲氧基丙酸乙酯、3-乙氧基丙酸、3-甲氧基丙酸、3-甲氧基丙酸丙酯、3-甲氧基丙酸丁酯、1-甲氧基-2-丙醇、1-乙氧基-2-丙醇、1-丁氧基-2-丙醇、1-苯氧基-2-丙醇、丙二醇單乙酸酯、丙二醇二乙酸酯、丙二醇-1-單甲基醚-2-乙酸酯、丙二醇-1-單乙基醚-2-乙酸酯、二丙二醇、2-(2-乙氧基丙氧基)丙醇、乳酸甲酯、乳酸乙酯、乳酸正丙酯、乳酸正丁酯、乳酸異戊酯等具有低表面張力的溶劑等。這些不良溶劑可以使用1種,或將多種混合使用。使用上述的溶劑的情況下,以不顯著降低聚合物組合物中所含的溶劑整體的溶解性的條件,優選為全部溶劑的5質量%~80質量%,更優選20質量%~60質量%。作為能提高膜厚的均勻性或表面平滑性的化合物,可例舉氟類表面活性劑、矽氧烷類表面活性劑、及非離子型表面活性劑等。更具體而言,可例舉例如、エフトップ(註冊商標)301、EF303、EF352(託凱姆產品株式會社(トーケムプロダクツ社)制)、メガファック(註冊商標)F171、F173、R-30(DIC株式會社制)、フロラードFC430、FC431(住友3M株式會社(住友スリーエム社)制)、アサヒガード(註冊商標)AG710(旭硝子株式會社(旭硝子社)制)、サーフロン(註冊商標)S-382、SC101、SC102、SC103、SC104、SC105、SC106(AGC清美化學株式會社(AGCセイミケミカル社)制)等。這些表面活性劑的使用比例相對於聚合物組合物中所含有的樹脂成分100質量份,優選為0.01質量份~2質量份,更優選0.01質量份~1質量份。作為能提高液晶取向膜和基板的密合性的化合物的具體例,可例舉以下所示的含官能性矽烷的化合物等。例如,可例舉3-氨基丙基三甲氧基矽烷、3-氨基丙基三乙氧基矽烷、2-氨基丙基三甲氧基矽烷、2-氨基丙基三乙氧基矽烷、N-(2-氨基乙基)-3-氨基丙基三甲氧基矽烷、N-(2-氨基乙基)-3-氨基丙基甲基二甲氧基矽烷、3-脲基丙基三甲氧基矽烷、3-脲基丙基三乙氧基矽烷、N-乙氧基羰基-3-氨基丙基三甲氧基矽烷、N-乙氧基羰基-3-氨基丙基三乙氧基矽烷、N-三乙氧基甲矽烷基丙基三亞乙基三胺、N-三甲氧基甲矽烷基丙基三亞乙基三胺、10-三甲氧基甲矽烷基-1,4,7-三氮雜癸烷、10-三乙氧基甲矽烷基-1,4,7-三氮雜癸烷、9-三甲氧基甲矽烷基-3,6-二氮雜壬基乙酸酯、9-三乙氧基甲矽烷基-3,6-二氮雜壬基乙酸酯、N-苄基-3-氨基丙基三甲氧基矽烷、N-苄基-3-氨基丙基三乙氧基矽烷、N-苯基-3-氨基丙基三甲氧基矽烷、N-苯基-3-氨基丙基三乙氧基矽烷、N-雙(氧乙烯基)-3-氨基丙基三甲氧基矽烷、N-雙(氧乙烯基)-3-氨基丙基三乙氧基矽烷等。此外,為了提高基板和液晶取向膜的密合性,以及防止構成液晶顯示元件時的由背光源引起的電特性的下降等的目的,也可以使聚合物組合物中含有如下所述的酚醛塑料類及含環氧基的化合物的添加劑。下面示出具體的酚醛塑料類添加劑,但不局限於這些結構。[化56]作為具體的含環氧基的化合物,可例舉乙二醇二縮水甘油基醚、聚乙二醇二縮水甘油基醚、丙二醇二縮水甘油基醚、三丙二醇二縮水甘油基醚、聚丙二醇二縮水甘油基醚、新戊二醇二縮水甘油基醚、1,6-己二醇二縮水甘油基醚、甘油二縮水甘油基醚、2,2-二溴新戊二醇二縮水甘油基醚、1,3,5,6-四縮水甘油基-2,4-己二醇、N,N,N』,N』,-四縮水甘油基-間二甲苯二胺、1,3-雙(N,N-二縮水甘油基氨基甲基)環己烷、N,N,N』,N』,-四縮水甘油基-4、4』-二氨基二苯基甲烷等。使用能提高與基板的密合性的化合物的情況下,其使用量相對於聚合物組合物所含有的樹脂成分100質量份,優選為0.1質量份~30質量份,更優選1質量份~20質量份。如果使用量不足0.1質量份,則無法期待密合性提高的效果,如果多於30質量份,則有時液晶的取向性變差。作為添加劑,還可使用光敏劑。優選無色敏化劑及三重態敏化劑。作為光敏劑,有芳香族硝基化合物、香豆素(7-二乙基氨基-4-甲基香豆素、7-羥基4-甲基香豆素)、氧代香豆素、羰基雙香豆素、芳香族2-羥基甲酮、以及氨基取代後的芳香族2-羥基甲酮(2-羥基二苯酮、一或二-對(二甲基氨基)-2-羥基二苯酮)、苯乙酮、蒽醌、呫噸酮、噻噸酮、苯並蒽酮、噻唑啉(2-苯甲醯基亞甲基-3-甲基-β-萘並噻唑啉、2-(β-萘甲醯基亞甲基)-3-甲基苯並噻唑啉、2-(α-萘甲醯基亞甲基)-3-甲基苯並噻唑啉、2-(4-聯苯基亞甲基)-3-甲基苯並噻唑啉、2-(β-萘甲醯基亞甲基)-3-甲基-β-萘並噻唑啉、2-(4-聯苯基亞甲基)-3-甲基-β-萘並噻唑啉、2-(對氟苯甲醯基亞甲基)-3-甲基-β-萘並噻唑啉)、唑啉(2-苯甲醯基亞甲基-3-甲基-β-萘並唑啉、2-(β-萘甲醯基亞甲基)-3-甲基苯並唑啉、2-(α-萘甲醯基亞甲基)-3-甲基苯並唑啉、2-(4-聯苯基亞甲基)-3-甲基苯並唑啉、2-(β-萘甲醯基亞甲基)-3-甲基-β-萘並唑啉、2-(4-聯苯基亞甲基)-3-甲基-β-萘並唑啉、2-(對氟苯甲醯基亞甲基)-3-甲基-β-萘並唑啉)、苯並噻唑、硝基苯胺(間或對硝基苯胺、2,4,6-三硝基苯胺)或硝基苊(5-硝基苊)、(2-[(m-羥基-p-甲氧基)苯乙烯基]苯並噻唑、苯偶姻烷基醚、N-烷基化弗他酮(日文:N-アルキル化フタロン)、苯乙酮縮酮(2,2-二甲氧基苯乙酮)、萘、蒽(2-萘甲醇、2-萘甲酸、9-蒽甲醇、以及9-蒽甲酸)、苯並吡喃、咪唑[1,5-A]吡啶、梅洛香豆素(日文:メロクマリン)等。優選芳香族2-羥基甲酮(二苯酮)、香豆素、氧代香豆素、羰基雙香豆素、苯乙酮、蒽醌、呫噸酮、噻噸酮、以及苯乙酮縮酮。在聚合物組合物中,除上述的物質外,只要是在不損害本發明效果的範圍內,可以改變液晶取向膜的介電常數和導電性等電特性為目的而添加電介質和導電物質,還可以提高製成液晶取向膜後的膜的硬度及緻密度為目的而添加交聯性化合物。對於將上述的聚合物組合物塗布在具有水平電場驅動用的導電膜的基板上的方法沒有特別限定。塗布方法是工業領域通常通過絲網印刷、膠版印刷、柔版印刷或噴墨法等進行塗布的方法。作為其它塗布方法,還有浸塗法、輥塗法、狹縫塗布法、旋塗法(旋轉塗布法)、或噴塗法等,可以根據目的使用這些方法。在具有水平電場驅動用的導電膜的基板上塗布聚合物組合物後,可以通過加熱板、熱循環式爐或IR(紅外線)型爐等加熱裝置在50~200℃、優選50~150℃下使溶劑蒸發,從而得到塗膜。此時的乾燥溫度優選比側鏈型高分子的液晶相呈現溫度低。塗膜的厚度如果過厚,則在液晶顯示元件的耗電方面不利;如果過薄,則有時液晶顯示元件的可靠性降低,因此優選5nm~300nm,更優選10nm~150nm。此外,也可以在[I]工序之後,接著的[II]工序之前,設置將形成有塗膜的基板冷卻至室溫的工序。在工序[II]中,對工序[I]中得到的塗膜照射偏振紫外線。對塗膜的膜面照射偏振紫外線時,從相對於基板為一定的方向、介由偏振板照射經偏振的紫外線。作為使用的紫外線,可使用波長在100nm~400nm的範圍的紫外線。優選根據使用的塗膜的種類,介由濾波器等選擇最佳的波長。而且,例如可以以選擇性地引起光交聯反應的條件,選擇使用波長290nm~400nm的範圍的紫外線。作為紫外線,可使用例如從高壓汞燈放射的光。偏振紫外線的照射量取決於使用的塗膜。照射量優選設為實現該塗膜中的ΔA的最大値(以下也稱為ΔAmax)的偏振紫外線的量的1%~70%的範圍內,更優選設在1%~50%的範圍內,該ΔA是與偏振紫外線的偏振方向平行的方向的紫外線吸光度和與偏振方向垂直的方向的紫外線吸光度的差。在工序[III]中,對工序[II]中照射了偏振紫外線的塗膜進行加熱。通過加熱,可賦予塗膜取向控制能力。加熱可使用加熱板、熱循環式爐或IR(紅外線)型爐等加熱裝置。加熱溫度可考慮使所用的塗膜呈現液晶性的溫度來決定。加熱溫度優選在側鏈型高分子呈現液晶性的溫度(以下稱為液晶性呈現溫度)的溫度範圍內。預想在塗膜那樣的薄膜表面的情況下的塗膜表面的液晶性呈現溫度低於以塊狀觀察能呈現液晶性的感光性的側鏈型高分子的情況下的液晶性呈現溫度,因此加熱溫度更優選在塗膜表面的液晶性呈現溫度的溫度範圍內。即,偏振紫外線照射後的加熱溫度的溫度範圍,優選是以比使用的鏈型高分子的液晶性呈現溫度的溫度範圍的下限低10℃的溫度作為下限,以比該液晶溫度範圍的上限低10℃的溫度作為上限的範圍的溫度。如果加熱溫度低於上述溫度範圍,則塗膜中的由熱引起的各向異性的增大效果有可能不充分,此外,如果加熱溫度比上述溫度範圍過高,則塗膜的狀態有可能接近各向同性的液體狀態(各向同性相),該情況下,通過自組織化在一方向上再取向會變得困難。另外,液晶性呈現溫度是指在側鏈型高分子或塗膜表面自固體相向液晶相發生相轉變的玻璃化溫度(Tg)以上、且在自液晶相向各向同性相(各向同性相)發生相轉變的各向同性相轉變溫度(Tiso)以下的溫度。關於加熱後所形成的塗膜的厚度,由於工序[I]中記載的相同的理由,優選5nm~300nm,更優選50nm~150nm。通過具有以上的工序,根據本發明的製造方法,能夠實現高效的、對塗膜的各向異性的導入。而且,能高效地製造帶液晶取向膜的基板。[IV]工序是下述工序:將[III]中得到的在水平電場驅動用的導電膜上具有液晶取向膜的基板(第1基板)、和同樣地在上述[I』]~[III』]中得到的不具有導電膜的帶液晶取向膜的基板(第2基板)介以液晶,以雙方的液晶取向膜相對的方式相向配置,通過公知的方法製作液晶晶胞,製作水平電場驅動型液晶顯示元件的工序。另外,工序[I』]~[III』],除了在工序[I]中使用不具有水平電場驅動用導電膜的基板來代替具有水平電場驅動用的導電膜的基板以外,可與工序[I]~[III]同樣地實施。工序[I]~[III]與工序[I』]~[III』]的不同點僅在於有無上述的導電膜,因此省略對工序[I』]~[III』]的說明。若例舉液晶晶胞或液晶顯示元件的製作的一例,可例示下述方法:準備上述的第1基板和第2基板,在一片基板的液晶取向膜上散布間隔物,以液晶取向膜面成為內側的方式貼合另一片基板,減壓注入液晶並密封的方法;或在散布有間隔物的液晶取向膜面上滴加液晶之後,將基板貼合進行密封的方法等。此時,一側的基板優選使用具有水平電場驅動用的梳齒狀結構的電極的基板。此時的間隔物的直徑優選1μm~30μm,更優選2μm~10μm。該間隔物直徑決定夾持液晶層的一對基板間距離、即液晶層的厚度。本發明的帶塗膜的基板的製造方法是,將聚合物組合物塗布在基板上,形成塗膜後,照射偏振紫外線。接著,通過進行加熱,實現對側鏈型高分子膜的高效的各向異性的導入,製造具備液晶的取向控制能力的帶液晶取向膜的基板。本發明中使用的塗膜中,利用由側鏈的光反應和基於液晶性的自組織化引起的分子再取向的原理,實現對塗膜的高效的各向異性的導入。本發明的製造方法中,側鏈型高分子在具有光交聯性基團作為光反應性基團的結構的情況下,在使用側鏈型高分子在基板上形成塗膜後,照射偏振紫外線,接著進行加熱後,製成液晶顯示元件。以下,將使用具有光交聯性基團作為光反應性基團的結構的側鏈型高分子的實施方式稱為第1形態;將使用具有光弗利斯重排基團或引起異構化的基團作為光反應性基團的結構的側鏈型高分子的實施方式稱為第2形態,並進行說明。圖1是本發明的第1形態中,對使用具有光交聯性基團作為光反應性基團的結構的側鏈型高分子的液晶取向膜的製造方法中的各向異性的導入處理進行示意說明的一個例子的圖。圖1(a)是示意地示出偏振光照射前的側鏈型高分子膜的狀態的圖;圖1(b)是示意地示出偏振光照射後的側鏈型高分子膜的狀態的圖;圖1(c)是示意地示出加熱後的側鏈型高分子膜的狀態的圖;特別是所導入的各向異性小的情況下,即,本發明的第1形態中,[II]工序的紫外線照射量在ΔA達到最大的紫外線照射量的1%~15%的範圍內時的示意圖。圖2是本發明的第1形態中,對使用具有光交聯性基團作為光反應性基團的結構的側鏈型高分子的液晶取向膜的製造方法中的各向異性的導入處理進行示意說明的一個例子的圖。圖2(a)是示意地示出偏振光照射前的側鏈型高分子膜的狀態的圖;圖2(b)是示意地示出偏振光照射後的側鏈型高分子膜的狀態的圖;圖2(c)是示意地示出加熱後的側鏈型高分子膜的狀態的圖;特別是所導入的各向異性大的情況下,即,本發明的第1形態中,[II]工序的紫外線照射量在ΔA達到最大的紫外線照射量的15%~70%的範圍內時的示意圖。圖3是本發明的第2形態中,對使用具有光異構化性基團或以上述式(18)表示的光弗利斯重排基團作為光反應性基團的結構的側鏈型高分子的液晶取向膜的製造方法中的各向異性的導入處理進行示意說明的一個例子的圖。圖3(a)是示意地示出偏振光照射前的側鏈型高分子膜的狀態的圖;圖3(b)是示意地示出偏振光照射後的側鏈型高分子膜的狀態的圖;圖3(c)是示意地示出加熱後的側鏈型高分子膜的狀態的圖;特別是所導入的各向異性小的情況下,即,本發明的第2形態中,[II]工序的紫外線照射量在ΔA達到最大的紫外線照射量的1%~70%的範圍內時的示意圖。圖4是本發明的第2形態中,對使用具有以上述式(19)表示的光弗利斯重排基團作為光反應性基團的結構的側鏈型高分子的液晶取向膜的製造方法中的各向異性的導入處理進行示意說明的一個例子的圖。圖4(a)是示意地示出偏振光照射前的側鏈型高分子膜的狀態的圖;圖4(b)是示意地示出偏振光照射後的側鏈型高分子膜的狀態的圖;圖4(c)是示意地示出加熱後的側鏈型高分子膜的狀態的圖;特別是所導入的各向異性大的情況下,即,本發明的第2形態中,[II]工序的紫外線照射量在ΔA達到最大的紫外線照射量的1%~70%的範圍內時的示意圖。本發明的第1形態中,在對塗膜的各向異性的導入處理中,[II]工序的紫外線照射量在ΔA達到最大的紫外線照射量的1%~15%的範圍內時,首先在基板上形成塗膜1。如圖1(a)所示,在基板上所形成的塗膜1中,側鏈2具有無規排列的結構。伴隨著塗膜1的側鏈2的無規排列,側鏈2的介晶成分和感光性基團也無規地取向,該塗膜1為各向同性。本發明的第1形態中,在對塗膜的各向異性的導入處理中,[II]工序的紫外線照射量在ΔA達到最大的紫外線照射量的15%~70%的範圍內時,首先在基板上形成塗膜3。如圖2(a)所示,在基板上所形成的塗膜3中,側鏈4具有無規排列的結構。伴隨著塗膜3的側鏈4的無規排列,側鏈4的介晶成分和感光性基團也無規地取向,該塗膜2為各向同性。本發明的第2形態中,在對塗膜的各向異性的導入處理中,在使用通過使用具有光異構化性基團或以上述式(18)表示的光弗利斯重排基團的結構的側鏈型高分子而得的液晶取向膜的場合下,[II]工序的紫外線照射量在ΔA達到最大的紫外線照射量的15%~70%的範圍內時,首先在基板上形成塗膜5。如圖3(a)所示,在基板上所形成的塗膜5中,側鏈6具有無規排列的結構。伴隨著塗膜5的側鏈6的無規排列,側鏈6的介晶成分和感光性基團也無規地取向,該側鏈型高分子膜5為各向同性。本發明的第2形態中,在對塗膜的各向異性的導入處理中,在使用通過使用具有上述式(19)表示的光弗利斯重排基團的結構的側鏈型高分子而得的液晶取向膜的情況下,[II]工序的紫外線照射量在ΔA達到最大的紫外線照射量的1%~70%的範圍內時,首先在基板上形成塗膜7。如圖4(a)所示,在基板上所形成的塗膜7中,側鏈8具有無規排列的結構。伴隨著塗膜7的側鏈8的無規排列,側鏈8的介晶成分和感光性基團也無規地取向,該塗膜7為各向同性。本實施方式的第1形態中,[II]工序的紫外線照射量在ΔA達到最大的紫外線照射量的1%~15%的範圍內時,對於該各向同性的塗膜1照射偏振紫外線。於是,如圖1(b)所示,在與紫外線的偏振方向平行的方向上排列的側鏈2中的具有感光性基團的側鏈2a的感光性基團優先發生二聚化反應等的光反應。其結果是,發生光反應的側鏈2a的密度在照射紫外線的偏振方向上稍微增大,結果對塗膜1賦予非常小的各向異性。本實施方式的第1形態中,[II]工序的紫外線照射量在ΔA達到最大的紫外線照射量的15%~70%的範圍內時,對於該各向同性的塗膜3照射偏振紫外線。於是,如圖2(b)所示,在與紫外線的偏振方向平行的方向上排列的側鏈4中的具有感光性基團的側鏈4a的感光性基團優先發生二聚化反應等的光反應。其結果是,發生光反應的側鏈4a的密度在照射紫外線的偏振方向上增大,結果對塗膜3賦予小的各向異性。本實施方式的第2形態中,使用通過使用具有光異構化性基團或以上述式(18)表示的光弗利斯重排基團的結構的側鏈型高分子而得的液晶取向膜,[II]工序的紫外線照射量在ΔA達到最大的紫外線照射量的1%~70%的範圍內時,對於該各向同性的塗膜5照射偏振紫外線。於是,如圖3(b)所示,在與紫外線的偏振方向平行的方向上排列的側鏈6中的具有感光性基團的側鏈6a的感光性基團優先發生光弗利斯重排等的光反應。其結果是,發生光反應的側鏈6a的密度在照射紫外線的偏振方向上稍微增大,結果對塗膜5賦予非常小的各向異性。本實施方式的第2形態中,使用通過使用具有以上述式(19)表示的光弗利斯重排基團的結構的側鏈型高分子而得的塗膜,[II]工序的紫外線照射量在ΔA達到最大的紫外線照射量的1%~70%的範圍內時,對於該各向同性的塗膜7照射偏振紫外線。於是,如圖4(b)所示,在與紫外線的偏振方向平行的方向上排列的側鏈8中的具有感光性基團的側鏈8a的感光性基團優先發生光弗利斯重排等的光反應。其結果是,發生光反應的側鏈8a的密度在照射紫外線的偏振方向上增大,結果對塗膜7賦予小的各向異性。接著,本實施方式的第1形態中,[II]工序的紫外線照射量在ΔA達到最大的紫外線照射量的1%~15%的範圍內時,對於偏振光照射後的塗膜1進行加熱,達到液晶狀態。於是,如圖1(c)所示,塗膜1中,在與照射紫外線的偏振方向平行的方向和與偏振方向垂直的方向之間發生的交聯反應的量不同。該情況下,在與照射紫外線的偏振方向平行的方向上產生的交聯反應的量非常小,所以該交聯反應部位起到增塑劑的作用。因此,與照射紫外線的偏振方向垂直的方向的液晶性比平行方向的液晶性更高,在與照射紫外線的偏振方向平行的方向上自組織化而使包含介晶成分的側鏈2進行再取向。其結果是,由光交聯反應引發的塗膜1的非常小的各向異性通過熱而增大,對塗膜1賦予更大的各向異性。同樣地,本實施方式的第1形態中,[II]工序的紫外線照射量在ΔA達到最大的紫外線照射量的15%~70%的範圍內時,對於偏振光照射後的塗膜3進行加熱,達到液晶狀態。於是,如圖2(c)所示,側鏈型高分子膜3中,在與照射紫外線的偏振方向平行的方向和與偏振方向垂直的方向之間發生的交聯反應的量不同。因此,在與照射紫外線的偏振方向平行的方向上自組織化而使包含介晶成分的側鏈4進行再取向。其結果是,由光交聯反應引發的塗膜3的小的各向異性通過熱而增大,對塗膜3賦予更大的各向異性。同樣地,本實施方式的第2形態中,使用通過使用具有光異構化性基團或以上述式(18)表示的光弗利斯重排基團的結構的側鏈型高分子而得的塗膜,[II]工序的紫外線照射量在ΔA達到最大的紫外線照射量的1%~70%的範圍內時,對偏振光照射後的塗膜5加熱,使其達到液晶狀態。於是,如圖3(c)所示,塗膜5中,在與照射紫外線的偏振方向平行的方向和與偏振方向垂直的方向之間發生的光弗利斯重排反應的量不同。該情況下,在與照射紫外線的偏振方向垂直的方向上產生的光弗利斯重排物的液晶取向力比反應前的側鏈的液晶取向能力更強,所以在與照射紫外線的偏振方向垂直的方向上自組織化而使包含介晶成分的側鏈6進行再取向。其結果是,由光弗利斯重排反應引發的塗膜5的非常小的各向異性通過熱而增大,對塗膜5賦予更大的各向異性。同樣地,本實施方式的第2形態中,使用通過使用具有以上述式(19)表示的光弗利斯重排基團的結構的側鏈型高分子而得的塗膜,[II]工序的紫外線照射量在ΔA達到最大的紫外線照射量的1%~70%的範圍內時,對偏振光照射後的塗膜7加熱,使其達到液晶狀態。於是,如圖4(c)所示,側鏈型高分子膜7中,在與照射紫外線的偏振方向平行的方向和與偏振方向垂直的方向之間發生的光弗利斯重排反應的量不同。光弗利斯重排體8(a)的錨固力比重排前的側鏈8更強,所以如果產生一定量以上的光弗利斯重排體,則在與照射紫外線的偏振方向平行的方向上自組織化而使包含介晶成分的側鏈8進行再取向。其結果是,由光弗利斯重排反應引發的塗膜7的小的各向異性通過熱而增大,對塗膜7賦予更大的各向異性。因此,本發明的方法中使用的塗膜可通過依次進行對塗膜照射偏振紫外線和加熱處理,高效地導入各向異性,製成取向控制能力優異的液晶取向膜。此外,本發明的方法所用的塗膜中,將對塗膜照射的偏振紫外線的照射量和加熱處理中的加熱溫度最優化。籍此,可實現高效的對塗膜的各向異性的導入。最適合於本發明中所用的塗膜的高效的各向異性的導入的偏振紫外線的照射量,對應於該塗膜中感光性基團發生光交聯反應、光異構化反應、或者光弗利斯重排反應的量達到最佳的偏振紫外線的照射量。如果對本發明中所用的塗膜照射偏振紫外線的結果是進行光交聯反應、光異構化反應或光弗利斯重排反應的側鏈的感光性基團少,則達不到足夠的光反應量。該情況下,其後即使加熱,也不會進行充分的自組織化。另一方面,本發明中所用的塗膜中,如果對具有光交聯性基團的結構照射偏振紫外線的結果是是進行交聯反應的側鏈的感光性基團過量,則不會過度進行側鏈間的交聯反應。該情況下,所得的膜變得剛性,有時會妨礙其後的藉由加熱而發生的自組織化的進行。此外,本發明中所用的塗膜中,如果對具有光弗利斯重排基團的結構照射偏振紫外線的結果是進行光弗利斯重排反應的側鏈的感光性基團過量,則塗膜的液晶性會過度降低。該情況下,所得的膜的液晶性也降低,有時會妨礙其後的藉由加熱而發生的自組織化的進行。此外,如果對具有光弗利斯重排基團的結構照射偏振紫外線時紫外線的照射量過多,則側鏈型高分子會光分解,有可能妨礙其後的藉由加熱而發生的自組織化的進行。因此,本發明中所用的塗膜中,通過偏振紫外線的照射而使側鏈的感光性基團進行光交聯反應、光異構化反應、或者光弗利斯重排反應的最佳的量優選為該側鏈型高分子膜所具有的感光性基團的0.1摩爾%~40摩爾%,更優選0.1摩爾%~20摩爾%。通過使進行光反應的側鏈的感光性基團的量在該範圍內,隨後的藉由加熱處理的自組織化高效地進行,能高效地在膜中形成各向異性。本發明的方法中所用的塗膜中,通過偏振紫外線的照射量的最優化,將側鏈型高分子膜的側鏈中的感光性基團的光交聯反應、光異構化反應、或光弗利斯重排反應的量最優化。接著,結合其後的加熱處理,實現高效的、對本發明中所用的塗膜的各向異性的導入。該情況下,對於優選的偏振紫外線的量,可以基於本發明所使用的塗膜的紫外吸收的評價來進行。即,對於本發明所使用的塗膜,分別測定偏振紫外線照射後的與偏振紫外線的偏振方向平行的方向的紫外線吸收、和與偏振方向垂直的方向的紫外線吸收。根據紫外吸收的測定結果,評價該塗膜中的與偏振紫外線的偏振方向平行的方向的紫外線吸光度和與偏振方向垂直的方向的紫外線吸光度的差、即ΔA。接著,算出本發明所用的塗膜中所實現的ΔA的最大值(ΔAmax)和實現該最大值的偏振紫外線的照射量。本發明的製造方法中,以實現該ΔAmax的偏振紫外線照射量作為基準,確定液晶取向膜的製造中照射的優選量的偏振紫外線量。本發明的製造方法中,優選將對本發明中所用的塗膜照射的偏振紫外線的照射量設在實現ΔAmax的偏振紫外線的量的1%~70%的範圍內,更優選在1%~50%的範圍內。本發明中所用的塗膜中,實現ΔAmax的偏振紫外線的量的1%~50%的範圍內的偏振紫外線的照射量相當於使該側鏈型高分子膜所具有的全部感光性基團的0.1摩爾%~20摩爾%進行光交聯反應的偏振紫外線的量。根據以上所述,本發明的製造方法中,為了實現對塗膜的高效的各向異性的導入,可以以該側鏈型高分子的液晶溫度範圍作為基準,確定如上所述的合適的加熱溫度。因此,例如,本發明中所用的側鏈型高分子的液晶溫度範圍為100℃~200℃的情況下,優選將偏振紫外線照射後的加熱溫度設為90℃~190℃。籍此,在本發明中所用的塗膜中,賦予更大的各向異性。籍此,由本發明提供的液晶顯示元件對於光、熱等外部應力顯示出高的可靠性。通過如上操作,由本發明的方法製造的水平電場驅動型液晶顯示元件用基板或具有該基板的水平電場驅動型液晶顯示元件的可靠性優異,適合用於大畫面且高清晰的液晶電視機等。實施例實施例中使用的縮寫如下所述。(甲基丙烯酸酯單體)[化57][化58][化59]MA1通過專利文獻(WO2011-084546)記載的合成法合成。MA2通過專利文獻(日本專利特開平9-118717)記載的合成法合成。MA3通過非專利文獻(《大分子(Macromolecules)》2002,35,706-713)記載的合成法合成。MA4是文獻等未公開的新型化合物,在以下的合成例1中詳述其合成法。MA5通過專利文獻(日本專利特開2010-18807)記載的合成法合成。MA6~MA9是文獻等未公開的新型化合物,在以下的合成例2~5中詳述其合成法。MA10使用能從市場購入的M6BC(綠色化學株式會社(みどり化學株式會社)制)。MA11~13是文獻等未公開的新型化合物,在以下的合成例6~8中詳述其合成法。MA14~18分別使用能從市場購入的M4CA、M4BA、M2CA、M3CA、及M5CA(這些全都是綠色化學株式會社制)。MA19~23是文獻等未公開的新型化合物,在以下的合成例9~13中詳述其合成法。MA24通過非專利文獻(《聚合物雜誌(PolymerJournal)》,第29卷,第4期,第303-308頁(1997))記載的合成方法進行合成。MA25是文獻等未公開的新型化合物,在以下的合成例14中詳述其合成法。MA26和MA27分別通過非專利文獻(《大分子(Macromolecules)》(2012),45(21),8547-8554)、非專利文獻(《液晶(LiquidCrystals)》(1995),19(4),433-40)中記載的合成方法進行合成。MA28~33是文獻等未公開的新型化合物,在以下的合成例15~20中詳述其合成法。MA34~39是文獻等未公開的新型化合物,在以下的合成例21~26中詳述其合成法。MA40和41通過專利文獻(日本專利特表2009-511431號)中記載的合成方法進行合成。MA42是文獻等未公開的新型化合物,在以下的合成例27中詳述其合成法。MA43通過專利文獻(WO2012-115129)中記載的合成方法進行合成。MA44通過專利文獻(WO2013-133078)中記載的合成方法進行合成。MA45通過專利文獻(WO2008-072652)中記載的合成方法進行合成。MA46是文獻等未公開的新型化合物,在以下的合成例28中詳述其合成法。化合物[MA4]的合成[化60]在3L四口燒瓶中添加4-溴-4』-羥基聯苯[MA4-1](150g、0.60mol)、丙烯酸叔丁酯[MA4-2](162g、1.3mol)、乙酸鈀(2.7g、12mmol)、三(鄰甲苯基)膦(7.3g、24mmol)、三丁胺(334g、1.8mol)、N,N-二甲基乙醯胺(750g),於100℃進行加熱攪拌。通過HPLC進行反應追蹤,確認反應結束後,將反應溶液冷卻至室溫附近後,注入1M鹽酸水溶液1.8L中。向其中添加乙酸乙酯(1L),通過分液操作除去水層。將有機層用10%鹽酸水溶液1L清洗2次,用飽和食鹽水1L清洗3次後,將有機層用硫酸鎂乾燥。之後,通過過濾、用蒸發器蒸餾除去溶劑,得到作為油狀化合物的174g化合物[MA4-3](收率98%)。1H-NMR(400MHz,DMSO-d6,δppm):9.68(1H,s),7.72(2H,d),7.63(2H,d),7.59-7.55(9H,m),6.87-6.85(2H,m),1.44(9H,s).在裝備有機械攪拌器、攪拌葉片的2L四口燒瓶中添加上述得到的化合物[MA4-3](174g、0.59mol)、6-氯-1-己醇(96.7g、0.71mol)、碳酸鉀(163g、1.2mol)、碘化鉀(9.8g、59mmol)、N,N-二甲基甲醯胺(1600g),於80℃進行加熱攪拌。通過HPLC進行反應追蹤,確認反應結束後,將反應溶液冷卻至室溫附近後,將反應溶液注入2L蒸餾水中。過濾分離析出的固體後,注入甲醇/蒸餾水(1:1)溶液中,再次過濾分離。通過將得到的固體減壓乾燥,得到221g的化合物[MA4-4](收率95%)。1H-NMR(400MHz,CDCl3,δppm):7.61(1H,d),7.56-7.52(6H,m),6.98-6.95(2H,m),6.38(1H,d),4.02(2H,t),3.67(2H,t),1.84-1.44(17H,m).在3L四口燒瓶中添加上述得到的化合物[MA4-4](221g、0.56mol)、三乙胺(67.7g、0.67mol)、四氫呋喃(1800g),冷卻反應溶液。向其中滴加甲基丙烯醯氯(70.0g、0.67mmol)的四氫呋喃(200g)溶液,同時注意內溫不要超過10℃。滴加結束後,使反應溶液為23℃,進一步進行反應。通過HPLC進行反應追蹤,確認反應結束後,將反應溶液注入6L蒸餾水中,添加2L乙酸乙酯,通過分液操作除去水層。然後,用5%氫氧化鉀水溶液、1M鹽酸水溶液、飽和食鹽水依次清洗有機層,將有機層用硫酸鎂乾燥。然後,過濾,用蒸發器蒸餾除去溶劑,得到粗產物。將得到的粗產物用100g的2-丙醇清洗,通過過濾、乾燥,得到127g化合物[MA4-5](收率49%)。1H-NMR(400MHz,DMSO-d6,δppm):7.73(2H,d),7.70-7.63(4H,m),7.58(1H,d),7.02-7.00(2H,m),6.53(1H,d),6.03-6.02(1H,m),5.67-5.66(1H,m),4.11(2H,t),4.00(2H,t),1.88-1.87(3H,m),1.79-1.25(17H,m).在1L四口燒瓶中添加上述得到的化合物[MA4-5](81g、0.17mol)、甲酸(400g),於40℃進行加熱攪拌。通過HPLC進行反應追蹤,確認反應結束後,將反應溶液注入3L蒸餾水中進行過濾。將得到的固體用200g甲醇清洗,使固體乾燥,得到56g化合物[MA4](收率79%)。1H-NMR(400MHz,CDCl3,δppm):7.81(1H,d),7.60(4H,s),7.55(2H,d),6.97(2H,d),6.47(2H,d),6.11-6.10(1H,m),5.56-5.52(1H,m),4.17(2H,t),4.00(2H,t),1.95-1.94(2H,m),1.85-1.82(3H,m),1.75-1.71(2H,m),1.55-1.48(4H,m).化合物[MA6]的合成[化61]在1L四口燒瓶中添加甲基丙烯酸2-羥基乙酯[MA6-1](63.42g、487mmol)、異煙酸鹽酸鹽[MA6-2](50.00g、406mmol)、1-(3-二甲基氨基丙基)-3-乙基碳二亞胺鹽酸鹽(以下簡稱為EDC)(93.43g、487mmol)、4-二甲基氨基吡啶(以下簡稱為DMAP)(4.96g、40.6mmol)、THF(500g),於23℃進行反應。通過HPLC進行反應追蹤,確認反應結束後,將反應溶液注入蒸餾水(3L)中,添加乙酸乙酯(1L),通過分液操作除去水層。將有機層用蒸餾水(1L)清洗2次後,將有機層用硫酸鎂乾燥。之後,通過過濾、用蒸發器蒸餾除去溶劑,得到作為油狀化合物的86.3g化合物[MA6](收率93%)。1H-NMR(400MHz,CDCl3,δppm):8.80(2H,dd),7.85(2H,dd),6.14-6.12(1H,m),5.62-5.60(1H,m),4.63-4.61(2H,m),4.52-4.50(2H,m),1.96-1.95(3H,m).化合物[MA7]的合成[化62]在200mL四口燒瓶中添加化合物[MA7-1](20.00g、86.9mmol)、4-羥基吡啶(8.26g、86.9mmol)、EDC(20.00g、104mmol)、DMAP(1.06g、8.7mmol)、THF(80g),於23℃進行反應。通過HPLC進行反應追蹤,確認反應結束後,將反應溶液注入蒸餾水(800mL)中,添加乙酸乙酯(500mL),通過分液操作除去水層。將有機層用蒸餾水(300mL)清洗3次後,將有機層用硫酸鎂乾燥。之後,通過過濾、用蒸發器蒸餾除去溶劑,得到作為油狀化合物的23.1g化合物[MA6](收率87%)。1H-NMR(400MHz,CDCl3,δppm):8.50-8.48(1H,m),8.44-8.43(1H,m),7.51-7.48(1H,m),7.35-7.32(1H,m),6.18-6.12(1H,m),5.91-5.58(1H,m),4.41-4.35(4H,m),2.95-2.92(2H,m),2.81-2.78(2H,m),2.05-1.93(3H,m)化合物[MA8]的合成[化63]除了將合成例2中使用的異煙酸鹽酸鹽[MA6-2]改為煙酸鹽酸鹽[MA8-1]以外,進行與合成例2同樣的操作,得到作為油狀化合物的80.13g化合物[MA8](收率86%)。1H-NMR(400MHz,CDCl3,δppm):9.24-9.23(1H,m),8.80(1H,dd),8.32-8.29(1H,m),7.43-7.40(1H,m),6.16-6.14(1H,m),5.62-5.60(1H,m),4.64-4.61(2H,m),4.52-4.51(2H,m),1.97-1.95(3H,m).化合物[MA9]的合成[化64]在500mL四口燒瓶中添加化合物[MA2](20.00g、65.3mmol)、化合物[MA9-1](14.09g、71.8mmol)、EDC(15.02g、78.4mmol)、DMAP(0.80g、6.53mmol)、THF(200g),於23℃進行反應。通過HPLC進行反應追蹤,確認反應結束後,將反應溶液注入蒸餾水(1.2L)中,添加乙酸乙酯(2L),通過分液操作除去水層。將有機層用蒸餾水(500mL)清洗3次後,將有機層用硫酸鎂乾燥。之後,通過過濾、用蒸發器蒸餾除去溶劑,得到作為油狀化合物的化合物[MA9-2]。接著,在得到的化合物[MA9-2]中添加對甲苯磺酸吡啶鎓(記為PPTS)(1.59g、6.3mmol)、乙醇(100g),於60℃進行加熱攪拌。通過HPLC進行反應追蹤,確認反應結束後,將反應溶液用冰浴冷卻,過濾析出的固體,用乙醇清洗。通過將得到的固體減壓乾燥,得到19.2g的化合物[MA9](收率69%)。1H-NMR(400MHz,CDCl3,δppm):8.22-8.18(2H,m),8.17-8.14(2H,m),7.36-7.32(2H,m),7.00-6.96(2H,m),6.12-6.11(1H,m),5.57-5.55(1H,m),4.20-4.16(2H,m),4.06(2H,t),1.96-1.95(3H,m),1.90-1.46(8H,m).化合物[MA11]的合成[化65]在2L四口燒瓶中添加化合物[MA11-1](50.00g、256mmol)、6-氯-1-己醇(36.74g、268mmol)、碳酸鉀(106.2g、768mmol)、碘化鉀(21.3g、128mmol)、DMF(500g),於85℃進行加熱反應。通過HPLC進行反應追蹤,確認反應結束後,將反應溶液注入蒸餾水(3L)中,進行過濾,用蒸餾水進行清洗,得到粗產物。之後,將所得的粗產物用甲醇進行清洗,過濾,減壓乾燥,得到61.9g化合物[MA11-2](收率82%)。1H-NMR(400MHz,DMSO-d6,δppm):7.89-7.84(4H,m),7.72-7.68(2H,m),7.07-7.03(2H,m),4.37(1H,brs),4.07-4.00(2H,m),3.42-3.38(2H,m),1.77-1.29(8H,m).在2L四口燒瓶中添加上述得到的化合物[MA11-2](61.9g、210mol)、三乙胺(25.45g、252mol)、THF(520g),冷卻反應溶液。向其中滴加甲基丙烯醯氯(26.3g、252mmol)的THF(120g)溶液,同時注意內溫不要超過10℃。滴加結束後,使反應溶液為23℃,進一步進行反應。通過HPLC進行反應追蹤,確認反應結束後,將反應溶液注入蒸餾水4L中,過濾分離析出的固體。將得到的粗產物用甲醇清洗後,進行減壓乾燥,得到47.5g化合物[MA11](收率77%)。1H-NMR(400MHz,DMSO-d6,δppm):7.89-7.86(2H,m),7.84-7.82(2H,m),7.72-7.68(2H,m),7.07-7.03(2H,m),6.02-6.01(1H,m),5.67-5.66(1H,m),4.11(2H,t),4.03(2H,t),1.88-1.87(3H,m),1.76-1.41(8H,m).化合物[MA12]的合成[化66]在2L四口燒瓶中添加化合物[MA4-1](4-溴-4』-羥基聯苯)(50.00g、201mmol)、6-氯-1-己醇(32.90g、241mmol)、碳酸鉀(83.2、602mmol)、碘化鉀(16.7g、100mmol)、DMF(500g),於85℃進行加熱反應。通過HPLC進行反應追蹤,確認反應結束後,將反應溶液注入蒸餾水(3L)中,進行過濾,用蒸餾水進行清洗,得到粗產物。之後,將得到的粗產物用甲醇進行清洗,過濾,減壓乾燥,得到化合物[MA12-1]的粗產物。1H-NMR(400MHz,DMSO-d6,δppm):7.62-7.56(6H,m),7.02-6.98(2H,m),4.00(2H,t),3.44(2H,t),1.76-1.26(8H,m).在2L四口燒瓶中添加上述得到的化合物[MA12-1](70.10g、201mol)、三乙胺(28.43g、281mol)、THF(950g),冷卻反應溶液。向其中滴加甲基丙烯醯氯(29.37g、281mmol)的THF(100g)溶液,同時注意內溫不要超過10℃。滴加結束後,使反應溶液為23℃,進一步進行反應。通過HPLC進行反應追蹤,確認反應結束後,將反應溶液注入5L蒸餾水中。向其中添加乙酸乙酯(2L),通過分液操作除去水層後、將有機層用飽和食鹽水(500g)清洗3次。將有機層用硫酸鎂乾燥後,進行過濾,用蒸發器蒸餾除去溶劑,得到粗產物。通過將得到的粗產物用甲醇清洗,減壓乾燥,得到68.4g化合物[MA12](收率82%)。1H-NMR(400MHz,DMSO-d6,δppm):7.61-7.56(6H,m),7.02-6.99(2H,m),6.02-6.01(1H,m),5.67-5.62(1H,m),4.09(2H,t),4.00(2H,t),1.99-1.85(3H,m),1.77-1.32(8H,m).化合物[MA13]的合成[化67]在500mL四口燒瓶中,將[MA2](38.6g、126mmol)、4-氟-4'-羥基聯苯[MA13-1](25g、136mmol)、EDC(31g、151mmol)、DMAP(630mg、6.3mmol)溶解於THF(200g)中,在室溫下進行攪拌。通過HPLC進行反應追蹤,確認反應結束後,將反應溶液注入蒸餾水3L中。通過過濾分離析出的固體,將得到的固體用IPA(300g)和甲醇(300g)清洗,使固體乾燥,得到50g化合物[MA13](收率83%)。1H-NMR(400MHz,DMSO-d6,δppm):8.08(2H,d),7.74(4H,m),7.37-7.29(4H,m),7.12(2H,d),6.03-6.02(1H,m),5.68-5.66(1H,m),4.11(2H,t),4.09(2H,t),1.88(3H,s),1.79-1.73(2H,m),1.69-1.62(2H,m),1.49-1.40(4H,m)化合物[MA19]的合成[化68]在500mL四口燒瓶中添加[MA1](30.00g、98mmol)、化合物[MA19-1](23.91g、98mmol)、EDC(20.65g、108mmol)、DMAP(1.2g、9.8mmol)、THF(300g),於23℃進行反應。通過HPLC進行反應追蹤,確認反應結束後,在蒸餾水1.5L中注入反應溶液,過濾析出的固體。接著,將得到的固體懸濁於IPA(400g)中,在40℃進行加熱攪拌後,將反應溶液冷卻至室溫,進行過濾、減壓乾燥,從而得到41g化合物[MA19](收率75%)。1H-NMR(400MHz,DMSO-d6,δppm):8.21-8.18(2H,m),7.87(1H,d),7.77(1H,d),7.46-7.43(2H,m),7.23-7.20(2H,m),7.03-7.00(4H,m),6.74(1H,m),6.02-6.01(1H,m),5.68-5.66(1H,m),4.11(2H,t),4.06(2H,t),4.03(3H,s),1.88-1.87(3H,m),1.76-1.40(8H,m).化合物[MA20]的合成[化69]除了將合成作為化合物[MA4]的中間體的化合物[MA4-4]時使用的6-氯-1-己醇改為8-氯-1-辛醇以外,進行與合成例1相同的操作,得到40.82g化合物[MA20]。1H-NMR(400MHz,DMSO-d6,δppm):7.70-7.56(7H,m),6.97(2H,d),6.51(1H,d),5.98(1H,s),5.62(1H,s),4.04(2H,t),3.94(2H,t),1.83(3H,s),1.70-1.10(12H).化合物[MA21]的合成[化70]在2L四口燒瓶中添加4-溴苯基-4』-反-羥基環己酮[MA21-1](500g、2.21mol)、丙烯酸叔丁酯[MA4-2](598g、4.66mol)、乙酸鈀(9.92g、44mmol)、三(鄰甲苯基)膦(26.91g、88mmol)、三丙胺(950g、6.63mol)、DMAc(2500g),於100℃進行加熱攪拌。通過HPLC進行反應追蹤,確認反應結束後,將反應溶液冷卻至室溫附近後,注入6L的1M鹽酸水溶液中。向其中添加乙酸乙酯(3L),通過分液操作除去水層。將有機層用10%鹽酸水溶液1L清洗2次,用飽和食鹽水1L清洗3次後,將有機層用硫酸鎂乾燥。之後,通過過濾、用蒸發器蒸餾除去溶劑,得到561.9g化合物[MA21-2](收率84%)。1H-NMR(400MHz,CDCl3,δppm):7.56(1H,d),7.45-7.43(2H,m),7.22-7.19(2H,m),6.32(1H,d),3.78-3.65(1H,m),2.58-2.44(1H,m),2.13-2.09(2H,m),1.96-1.91(2H,m),1.60-1.41(13H,m).在2L四口燒瓶中添加上述得到的化合物[MA21-2](100g、331mmol)、叔-4-甲氧基-桂皮酸(58.92g、331mol)、EDC(76.07g、397mol)、DMAP(4.04g、33mmol)、THF(885g),於23℃進行攪拌。通過HPLC進行反應追蹤,確認反應結束後,將反應溶液注入蒸餾水8L中,過濾析出的固體,用蒸餾水進行清洗,得到粗產物。接著,使粗產物懸濁於甲醇(3L)中,攪拌一段時間後,再次過濾、減壓乾燥,從而得到82.17g化合物[MA21-3](收率54%)。1H-NMR(400MHz,CDCl3,δppm):7.64(1H,d),7.56(1H,d),7.51-7.48(2H,m),7.46-7.44(2H,m),7.23-7.21(2H,m),6.92-6.90(2H,m),6.34(1H,d),6.30(1H,d),4.95-4.89(1H,m),3.84(3H,s),2.59-2.54(1H,m),2.20-2.18(2H,m),2.00-1.97(2H,m),1.69-1.37(13H,m).(9H,m),6.87-6.85(2H,m),1.44(9H,s).在2L四口燒瓶中添加上述得到的化合物[MA21-3](82.17g、178mmol)、甲酸(410g),於40℃進行加熱攪拌。通過HPLC進行反應追蹤,確認反應結束後,將反應溶液冷卻至室溫附近後,將反應溶液注入3L蒸餾水中。將析出的固體過濾分離後,用乙酸乙酯清洗,進行減壓乾燥,從而得到54.4g化合物[MA21-4](收率75%)。1H-NMR(400MHz,DMSO-d6,δppm):7.70-7.68(2H,m),7.62(1H,d),7.60(2H,s),7.56(2H,d),7.31(2H,d),7.00-6.97(2H,m),6.50(1H,d),6.46(1H,d),4.91-4.82(1H,m),3.80(3H,s),2.62-2.48(1H,m),2.10-2.07(2H,m),1.87-1.84(2H,m),1.65-1.48(4H,m).在1L四口燒瓶中添加上述得到的化合物[MA21-5](30.00g、73.8mmol)、甲基丙烯酸2-羥基乙酯[MA6-1](10.57g、81.2mmol)、EDC(17.0g、88.6mmol)、DMAP(0.90g、7.38mmol)、THF(450g),於23℃進行攪拌。通過HPLC進行反應追蹤,確認反應結束後,將反應溶液注入蒸餾水2L中,用乙酸乙酯(600g)進行萃取。將有機層用蒸餾水(500g)清洗2次,將有機層用硫酸鎂脫水、過濾,蒸餾除去溶劑,得到32.8g化合物[MA21](收率86%)。1H-NMR(400MHz,DMSO-d6,δppm):7.70-7.68(2H,m),7.7.67(2H,s),7.65-7.63(1H,m),7.60(1H,d),7.32(2H,d),7.00-6.97(2H,m),6.62(1H,d),6.50(1H,d),6.05-6.04(1H,m),5.71-5.70(1H,m),4.87-4.81(1H,m),4.43-4.36(4H,m),3.80(3H,s),2.62-2.58(1H,m),2.10-2.06(2H,m),1.89-1.88(5H,m),1.66-1.48(4H,m).化合物[MA22]的合成[化71]在1L四口燒瓶中添加化合物[MA2](50.00g、163mmol)、化合物[MA22-1](39.90g、180mmol)、EDC(37.54g、196mmol)、DMAP(1.99g、16.3mmol)、THF(500g),於23℃進行反應。通過HPLC進行反應追蹤,確認反應結束後,將反應溶液注入蒸餾水(3L)中,添加乙酸乙酯(1L),通過分液操作除去水層。將有機層用蒸餾水(1L)清洗3次後,將有機層用硫酸鎂乾燥。之後,通過過濾、用蒸發器蒸餾除去溶劑,得到作為油狀化合物的74.95g化合物[MA22-2](收率90%)。1H-NMR(400MHz,CDCl3,δppm):8.13(2H,d),7.74(1H,d),7.60(2H,d),7.25(2H,d),7.00-6.96(2H,m),6.43(2H,d),6.11-6.10(1H,m),5.96-5.54(1H,m),5.44(2H,s),4.17(2H,t),4.06(2H,t),3.79-3.73(2H,m),1.95-1.94(3H,m),1.85-1.43(8H,m),1.25(3H,t).在上述得到的化合物[MA22-2](74.95g、147mmol)中添加PPTS(3.69g、14.7mmol)、乙醇(480g),於60℃進行加熱攪拌。通過HPLC進行反應追蹤,確認反應結束後,將反應溶液用冰浴冷卻,過濾析出的固體,用乙醇清洗。通過將得到的固體減壓乾燥,得到44.9g的化合物[MA22](收率68%)。1H-NMR(400MHz,CDCl3,δppm):8.14(2H,d),7.79(1H,d),7.61(2H,d),7.26(2H,d),6.97(2H,d),6.43(1H,d),6.11-6.09(1H,m),5.56-5.55(1H,m),4.16(2H,t),4.06(2H,t),1.95(3H,s),1.88-1.43(8H,m).化合物[MA23]的合成[化72]在1L四口燒瓶中添加化合物[MA1](50.00g、150mmol)、化合物[MA9-1](32.46g、166mmol)、EDC(34.6g、181mmol)、DMAP(1.84g、15.0mmol)、THF(500g),於23℃進行反應。通過HPLC進行反應追蹤,確認反應結束後,將反應溶液注入蒸餾水(3L)中,添加乙酸乙酯(1L),通過分液操作除去水層。將有機層用蒸餾水(1L)清洗3次後,將有機層用硫酸鎂乾燥。之後,通過過濾、用蒸發器蒸餾除去溶劑,得到作為油狀化合物的76.5g化合物[MA23-1](收率99%)。1H-NMR(400MHz,CDCl3,δppm):8.14(2H,d),7.84(1H,d),7.55-7.53(2H,m),7.28-7.26(2H,m),6.95-6.92(2H,m),6.48(1H,d),6.11-6.10(1H,m),5.56-5.55(3H,m),4.18-4.10(2H,m),4.01(2H,t),3.82-3.74(2H,m),1.95(3H,s),1.86-1.43(8H,m),1.26(3H,t).在上述得到的化合物[MA23-1](76.5g、150mmol)中添加PPTS(3.77g、15.0mmol)、乙醇(540g),於60℃進行加熱攪拌。通過HPLC進行反應追蹤,確認反應結束後,將反應溶液用冰浴冷卻,過濾析出的固體,用乙醇清洗。通過將得到的固體減壓乾燥,得到16.9g的化合物[MA23](收率48%)。1H-NMR(400MHz,CDCl3,δppm):8.18(2H,d),7.84(1H,d),7.54(2H,d),7.29(2H,d),6.93(2H,d),6.49(1H,d),6.11-6.10(1H,m),5.56-5.55(1H,m),4.17(2H,t),4.01(2H,t),1.95-1.94(3H,m),1.88-1.43(8H,m).化合物[MA25]的合成[化73]在2L四口燒瓶中添加4-溴苯甲酸叔丁酯[MA25-1](126.0g、488mmol)、丙烯酸(73.86g、1.03mol)、乙酸鈀(2.19g、9.77mmol)、三(鄰甲苯基)膦(5.94g、19.53mmol)、三丁胺(271.5g、1.46mol)、DMAc(630g),於100℃進行加熱攪拌。通過HPLC進行反應追蹤,確認反應結束後,將反應溶液冷卻至室溫附近後,注入4L的1M鹽酸水溶液中。過濾析出的固體,依次用蒸餾水、甲醇進行清洗,自乙酸乙酯/己烷重結晶,從而得到116.1g化合物[MA25-2](收率96%)。1H-NMR(400MHz,DMSO-d6,δppm):10.01(1H,s),12.49(1H,brs),7.92-7.90(2H,m),7.82-7.80(2H,m),7.63(1H,d),6.65(1H,d),1.55(9H,s).在裝備有機械攪拌器、攪拌葉片的2L四口燒瓶中添加上述得到的化合物[MA25-2](50.00g、201mmol)、6-氯-1-己醇(30.27g、222mol)、碳酸鉀(30.63g、222mmol)、碘化鉀(3.34g、20.14mmol)、DMF(250g),於80℃進行加熱攪拌。通過HPLC進行反應追蹤,確認反應結束後,將反應溶液注入蒸餾水1.5L中,用乙酸乙酯(500mL)進行2次清洗。使有機層合併後,用5%氫氧化鉀水溶液(300g)、飽和食鹽水(300g)清洗2次,用硫酸鎂乾燥有機層,過濾後,蒸餾除去溶劑,得到62.5g化合物[MA25-3](收率89%)。1H-NMR(400MHz,DMSO-d6,δppm):7.92-7.90(2H,m),7.86-7.84(2H,d),7.68(1H,d),6.76(1H,d),4.16(2H,t),3.39(2H,t),1.65-1.28(15H,d).在2L四口燒瓶中添加上述得到的化合物[MA25-3](62.5g、179mmol)、三乙胺(21.78g、215mmol)、THF(400g),冷卻反應溶液。向其中滴加甲基丙烯醯氯(20.63g、197mmol)的THF(100g)溶液,同時注意內溫不要超過10℃。滴加結束後,使反應溶液為23℃,進一步進行反應。通過HPLC進行反應追蹤,確認反應結束後,將反應溶液注入4L蒸餾水中,添加1L乙酸乙酯,通過分液操作除去水層。然後,用5%氫氧化鉀水溶液、1M鹽酸水溶液、飽和食鹽水依次清洗有機層,將有機層用硫酸鎂乾燥。之後,進行過濾,用蒸發器蒸餾除去溶劑,得到65.19g化合物[MA25-4](收率87%)。1H-NMR(400MHz,DMSO-d6,δppm):7.92-7.90(2H,m),7.87-7.84(2H,m),7.68(2H,d),6.75(1H,d),6.02-6.01(1H,m),5.67-5.65(1H,m),4.16(2H,t),4.06-4.00(2H,m),1.88-1.87(3H,m),1.66-1.36(15H,m).在2L四口燒瓶中添加上述得到的化合物[MA25-4](65.19g、157mmol)、甲酸(325g),於40℃進行加熱攪拌。通過HPLC進行反應追蹤,確認反應結束後,將反應溶液注入2L蒸餾水中進行過濾。將得到的固體用甲醇清洗,使固體乾燥,從而得到26.8g化合物[MA25](收率48%)。1H-NMR(400MHz,DMSO-d6,δppm):13.1(1H,brs),7.97-7.95(2H,m),7.86-7.84(2H,m),7.69(1H,d),6.75(1H,d),6.02-6.01(1H,m),5.68-5.65(1H,m),4.16-4.03(4H,m),1.88-1.87(3H,m),1.68-1.32(8H,m).化合物[MA28]的合成[化74]添加上述合成例11中合成的化合物[MA21-2](50.00g、165mmol)、4-甲氧基苯甲酸(25.16g、165mol)、EDC(38.0g、198mol)、DMAP(2.02g、16.5mmol)、THF(380g),於23℃進行攪拌。通過HPLC進行反應追蹤,確認反應結束後,將反應溶液注入2.5L蒸餾水中,添加乙酸乙酯,通過分液操作分離有機層。將得到的有機層用蒸餾水(1L)清洗3次後,將有機層用硫酸鎂乾燥。之後,通過過濾、用蒸發器蒸餾除去溶劑,得到作為油狀化合物的65.5g化合物[MA28-1](收率91%)。1H-NMR(400MHz,CDCl3,δppm):8.10(2H,d),7.56(1H,d),7.45-7.43(2H,d),7.22-7.19(2H,m),7.00-6.97(2H,m),6.33(1H,d),3.90(3H,s),3.73-3.66(1H,m),2.58-2.42(1H,m),2.12-1.43(17H,m).在2L四口燒瓶中添加上述得到的化合物[MA28-1](65.5g、150mmol)、甲酸(650g),於40℃進行加熱攪拌。通過HPLC進行反應追蹤,確認反應結束後,將反應溶液冷卻至室溫附近後,將反應溶液注入4L蒸餾水中。將析出的固體過濾分離後,用乙酸乙酯清洗,進行減壓乾燥,從而得到29.9g化合物[MA28-2](收率52%)。1H-NMR(400MHz,DMSO-d6,δppm):7.94-7.88(2H,m),7.62-7.54(3H,m),7.33-7.79(2H,m),7.07-7.01(2H,m),6.48(1H,d),4.95-4.92(1H,m),4.84-4.77(1H,m),3.83(3H,s),2.65-1.48(8H).在1L四口燒瓶中添加上述得到的化合物[MA28-2](29.9g、78.6mmol)、甲基丙烯酸2-羥基乙酯(12.27g、94.3mmol)、EDC(21.1g、110mmol)、DMAP(0.96g、7.86mmol)、THF(450g),於23℃進行攪拌。通過HPLC進行反應追蹤,確認反應結束後,將反應溶液注入蒸餾水2.7L中,用乙酸乙酯(600g)進行萃取。將有機層用蒸餾水(500g)清洗2次,將有機層用硫酸鎂脫水、過濾,蒸餾除去溶劑,得到23.6g化合物[MA28](收率56%)。1H-NMR(400MHz,DMSO-d6,δppm):8.08-8.02(2H,m),7.68(1H,d),7.48-7.46(2H,m),7.24-7.22(2H,m),6.92(2H,d),6.42(1H,d),6.16(1H,s),5.61-5.60(1H,m),5.12-4.93(2H,m),4.47-4.22(4H,m),3.86(3H,s),2.60-1.43(11H).化合物[MA29]的合成[化75]在2L四口燒瓶中添加6-溴-2-萘酚[MA29-1](150g、672mol)、丙烯酸叔丁酯[MA4-2](103.4g、807mmol)、乙酸鈀(3.02g、13.5mmol)、三(鄰甲苯基)膦(8.19g、26.9mmol)、三丙胺(289.0g、2.02mol)、DMAc(700g),於100℃進行加熱攪拌。通過HPLC進行反應追蹤,確認反應結束後,將反應溶液冷卻至室溫附近後,注入3L的1M鹽酸水溶液中。向其中添加乙酸乙酯(2L),通過分液操作除去水層。將有機層用10%鹽酸水溶液1L清洗2次,用飽和食鹽水1L清洗3次後,將有機層用硫酸鎂乾燥。之後,通過過濾、用蒸發器蒸餾除去溶劑,得到181g化合物[MA29-2](收率99%)。1H-NMR(400MHz,DMSO-d6,δppm):10.01(1H,s),8.04(1H,s),7.81-7.74(2H,m),7.70-7.63(2H,m),7.14-7.10(2H,m),6.54(1H,d),1.51-1.48(9H,m).在裝備有機械攪拌器、攪拌葉片的2L四口燒瓶中添加上述得到的化合物[MA29-2](181g、672mmol)、6-氯-1-己醇(110.2g、806mol)、碳酸鉀(111.5g、806mmol)、碘化鉀(1.12g、6.7mmol)、DMF(900g),於80℃進行加熱攪拌。通過HPLC進行反應追蹤,確認反應結束後,將反應溶液注入2L蒸餾水中,添加乙酸乙酯(2L),通過分液操作除去水層。之後,將有機層用飽和食鹽水(1L)清洗2次,用硫酸鎂乾燥有機層,過濾後,蒸餾除去溶劑,得到粗產物。將得到的粗產物用乙酸乙酯/己烷混合溶劑重結晶,得到185g化合物[MA29-3](收率74%)。1H-NMR(400MHz,DMSO-d6,δppm):8.06(1H,s),7.80(1H,d),7.77-7.76(2H,m),7.62(1H,d),7.34(1H,d),7.15(1H,dd),6.53(1H,d),4.34(1H,t),4.05(2H,t),3.39-3.33(2H,m),1.73(2H,t),1.46-1.31(15H,m).在3L四口燒瓶中添加上述得到的化合物[MA29-3](130.5g、352mmol)、三乙胺(42.76g、423mmol)、THF(950g),冷卻反應溶液。向其中滴加甲基丙烯醯氯(44.2g、423mmol)的THF(100g)溶液,同時注意內溫不要超過10℃。滴加結束後,使反應溶液為23℃,進一步進行反應。通過HPLC進行反應追蹤,確認反應結束後,將反應溶液注入6L蒸餾水中,添加2L乙酸乙酯,通過分液操作除去水層。然後,用5%氫氧化鉀水溶液、1M鹽酸水溶液、飽和食鹽水依次清洗有機層,將有機層用硫酸鎂乾燥。之後,進行過濾,用蒸發器蒸餾除去溶劑,得到140.9g化合物[MA29-4](收率92%)。1H-NMR(400MHz,DMSO-d6,δppm):8.09(1H,s),7.83(1H,d),7.80-7.79(2H,m),7.66(1H,d),7.33(1H,d),7.18(1H,dd),6.57(1H,d),6.02-6.01(1H,m),5.66-5.65(1H,m),4.12-4.06(4H,m),1.88-1.87(3H,m),1.84-1.42(15H,m).在3L四口燒瓶中添加上述得到的化合物[MA29-4](140.9g、321mmol)、甲酸(700g),於40℃進行加熱攪拌。通過HPLC進行反應追蹤,確認反應結束後,將反應溶液注入4.5L蒸餾水中,進行過濾。將得到的固體用IPA/己烷混合溶劑進行清洗,使固體乾燥,從而得到95.9g化合物[MA29](收率78%)。1H-NMR(400MHz,DMSO-d6,δppm):12.4(1H,brs),8.10(1H,s),7.84(1H,d),7.81-7.80(2H,m),7.70(1H,d),7.35(1H,d),7.19(1H,dd),6.59(1H,d),6.03-6.02(1H,m),5.67-5.65(1H,m),4.13-4.07(4H,m),1.88-1.87(3H,m),1.83-1.41(8H,m).化合物[MA30]的合成[化76]除了在合成例16中,將合成化合物[MA29-3]時使用的6-氯-1-己醇改為8-氯-1-辛醇以外,進行與合成例16相同的操作,得到171g化合物[MA30]。1H-NMR(400MHz,CDCl3,δppm):12.4(1H,brs),7.94-7.88(2H,m),7.77-7.71(2H,m),7.70-7.63(1H,m),7.17(1H,dd),7.12-7.11(1H,m),6.51(1H,d),6.11-6.10(1H,m),5.55-5.54(1H,m),4.17-4.06(4H,m),1.95-1.94(3H,m),1.87-1.40(12H,m).化合物[MA31]的合成[化77]在2L四口燒瓶中添加6-羥基-2-萘甲酸[MA31-1](300g、1.59mol)、氫氧化鉀(205g、3.66mol)、蒸餾水(1200g),於100℃進行加熱攪拌。向其中滴加6-氯-1-己醇(261g、1.91mol)。滴加結束後,通過HPLC進行反應追蹤,確認反應結束後,將反應溶液冷卻至室溫附近後,將反應溶液注入冰水(3L)中,添加35%鹽酸進行中和。之後,將析出的固體過濾,用蒸餾水清洗後,對固體進行減壓乾燥,從而得到275g化合物[MA31-2](收率60%)。1H-NMR(400MHz,DMSO-d6,δppm):8.53-8.52(1H,m),8.06-7.87(3H,m),7.40(1H,d),7.27-7.23(1H,m),4.32(1H,t),4.12(2H,m),3.44-3.33(2H,m),1.82-1.76(2H,m),1.51-1.3(6H).在2L四口燒瓶中添加上述得到的化合物[MA31-2](50.00g、173mmol)、二甲基氨基苯酚(46.23g、382mmol)、硝基苯(2.13g、17.3mmol)、THF(500g),進行氮置換後,在加熱回流下進行攪拌。向其中慢慢滴加甲基丙烯醯氯(38.1g、361mmol)的THF(100g)溶液。滴加結束後,通過HPLC進行反應追蹤,確認反應結束後,將反應溶液冷卻至室溫。之後,將反應溶液注入3L的1M鹽酸水溶液中,過濾析出的固體,得到粗產物。接著,將得到的粗產物用乙醇/己烷混合溶劑、接著用丙酮清洗後,進行減壓乾燥,從而得到38.4g化合物[MA31](收率62%)。1H-NMR(400MHz,DMSO-d6,δppm):8.63(1H,s),8.08(1H,dd),7.87(1H,d),7.76(1H,d),7.22-7.19(1H,m),7.16-7.15(1H,m),6.11-6.10(1H,m),5.56-5.54(1H,m),4.20-4.10(4H,m),1.97-1.95(3H,m),1.92-1.85(2H,m),1.78-1.71(2H,m),1.60-1.47(4HH,m).化合物[MA32]的合成[化78]在1L四口燒瓶中添加化合物[MA1](50.00g、150mmol)、化合物[MA22-1](37.10g、165mmol)、EDC(34.6g、181mmol)、DMAP(1.89g、15.0mmol)、THF(500g),於23℃進行反應。通過HPLC進行反應追蹤,確認反應結束後,將反應溶液注入蒸餾水(3L)中,過濾析出的固體,依次用蒸餾水、甲醇進行清洗,將得到的固體減壓乾燥,從而得到79.8g化合物[MA32-1](收率99%)。1H-NMR(400MHz,CDCl3,δppm):7.83(1H,d),7.73(1H,d),7.60-7.57(2H,m),7.56-7.53(2H,m),7.23-7.21(2H,m),6.94-6.92(2H,m),6.48(1H,d),6.42(1H,d),6.11-6.10(1H,m),5.57-5.55(1H,m),5.43(2H,s),4.17(2H,t),4.01(2H,t),3.76(2H,q),1.95(3H,s),1.85-1.43(6H,m),1.26(3H,t).在上述得到的化合物[MA32-1](79.8g、150mmol)中添加PPTS(3.78g、15.0mmol)、乙醇(565g),於60℃進行加熱攪拌。通過HPLC進行反應追蹤,確認反應結束後,將反應溶液用冰浴冷卻,過濾析出的固體,用乙醇清洗。通過將得到的固體減壓乾燥,得到63.0g的化合物[MA32](收率88%)。1H-NMR(400MHz,CDCl3,δppm):7.83(1H,d),7.78(1H,d),7.62-7.59(2H,m),7.55-7.53(2H,m),7.24-7.22(2H,m),6.94-6.91(2H,m),6.48(1H,d),6.43(1H,d),6.11-6.10(1H,m),5.56-5.55(1H,m),4.18(2H,t),4.01(2H,t),1.95-1.94(3H,m),1.85-1.45(6H,m).化合物[MA33]的合成[化79]在500mL四口燒瓶中添加化合物[MA2](20.00g、65.3mmol)、4-羥基吡啶(6.83g、71.8mmol)、EDC(15.02g、78.4mmol)、DMAP(0.80g、6.53mmol)、THF(200g),於23℃進行反應。通過HPLC進行反應追蹤,確認反應結束後,將反應溶液注入蒸餾水(1.2L)中,添加乙酸乙酯(1L),通過分液操作除去水層。將有機層用蒸餾水(500mL)清洗3次後,將有機層用硫酸鎂乾燥。之後,通過過濾、用蒸發器蒸餾除去溶劑,得到24.31g化合物[MA33](收率97%)。1H-NMR(400MHz,CDCl3,δppm):8.66(2H,d),8.15-8.11(2H,m),7.24-7.23(2H,m),7.00-6.96(2H,m),6.10-6.11(1H,m),5.57-5.56(1H,m),4.19-4.16(2H,m),4.06(2H,t),1.96-1.95(3H,m),1.90-1.46(8H,m).化合物[MA34]的合成[化80]在2L四口燒瓶中添加化合物[MA34-1](264g、1.0mol)、三乙胺(111g、1.1mol)、THF(1300g),將反應溶液冷卻至0℃。向其中滴加氯甲基乙基醚(103g、1.1mol),之後於25℃進行攪拌。反應結束後,將反應溶液注入乙酸乙酯(2L)中,用蒸餾水(1L)清洗3次後,將有機層用硫酸鈉乾燥。之後,進行過濾,用蒸發器蒸餾除去溶劑,將得到的粗產物用己烷(1L)進行再漿化(repulp)清洗,通過進行過濾、乾燥,得到212g化合物[MA34-2](收率65%)。1H-NMR(400MHz,DMSO-d6,δppm):7.64-7.70(3H,m),6.95-6.99(2H,d),6.48-6.52(1H,d),5.34(2H,s),4.34-4.37(1H,t),3.99-4.03(2H,t),3.64-3.69(2H,t),3.37-3.41(2H,m),1.68-1.73(2H,m),1.31-1.45(6H,m),1.11-1.17(3H,t).在1L四口燒瓶中添加化合物[MA34-2](54.5g、0.17mol)、4-乙烯基苯甲酸(25.0g、0.17mol)、EDC(48.7g、0.25mol)、DMAP(2.1g、17mmol)、THF(250g),於25℃進行攪拌。反應結束後,將反應溶液注入乙酸乙酯(250mL)中,用飽和食鹽水(200mL)清洗3次後,將有機層用硫酸鈉乾燥。之後,進行過濾,用蒸發器蒸餾除去溶劑,在得到的殘渣中添加對甲苯磺酸吡啶鎓(記作PPTS)(4.3g、34mmol)、乙醇(375g),於65℃進行加熱攪拌。確認反應結束後,將反應溶液用冰浴冷卻,過濾析出的固體,用乙腈進行清洗。將得到的粗產物用乙酸乙酯/己烷=1/1溶液(250g)進行再漿化清洗,進行過濾、乾燥,從而得到46.6g化合物[MA34](收率70%)。1H-NMR(400MHz,DMSO-d6,δppm):12.23(1H,s),7.92-7.94(2H,d),7.52-7.61(5H,m),6.94-6.96(2H,m),6.78-6.85(1H,m),6.35-6.39(1H,d),5.97-6.01(1H,d),5.42-5.44(1H,d),4.26-4.30(2H,m),3.98-4.02(2H,m),1.72-1.75(4H,m),1.46-1.48(4H,m).化合物[MA35]的合成[化81]在3L四口燒瓶中添加化合物[MA35-1](402g、1.7mol)、三乙胺(188g、1.9mol)、THF(2000g),將反應溶液冷卻至0℃。向其中滴加氯甲基乙基醚(176g、1.9mol),之後於25℃進行攪拌。反應結束後,將反應溶液注入乙酸乙酯(1L)中,用飽和食鹽水(500mL)清洗3次後,用硫酸鈉乾燥有機層。之後,進行過濾,用蒸發器蒸餾除去溶劑,將得到的粗產物用異丙醇/己烷=1/2(300g)進行再漿化清洗,通過進行過濾、乾燥,得到505g化合物[MA35-2](收率99%)。1H-NMR(400MHz,DMSO-d6,δppm):7.92-7.94(2H,d),7.03-7.06(2H,d),5.45(2H,s),4.37(1H,s),4.01-4.07(2H,t),3.69-3.74(2H,t),3.41-3.52(2H,m),1.70-1.75(2H,m),1.32-1.46(6H,m),1.14-1.20(3H,t).在1L四口燒瓶中添加化合物[MA35-2](45.6g、0.15mol)、4-乙烯基苯甲酸(29.6g、0.20mol)、EDC(50.3g、0.26mol)、DMAP(2.9g、24mmol)、THF(250g),於25℃進行攪拌。反應結束後,將反應溶液注入乙酸乙酯(250mL)中,用飽和食鹽水(200mL)清洗3次後,用硫酸鈉乾燥有機層。之後,進行過濾,用蒸發器蒸餾除去溶劑,在得到的殘渣中添加對甲苯磺酸吡啶鎓(記作PPTS)(3.9g、16mmol)、乙醇(350g),於65℃進行加熱攪拌。確認反應結束後,將反應溶液用冰浴冷卻,過濾析出的固體,用乙腈進行清洗。將得到的粗產物用乙酸乙酯(300g)進行再漿化清洗,進行過濾、乾燥,從而得到24.5g的化合物[MA35](收率43%)。1H-NMR(400MHz,DMSO-d6,δppm):12.66(1H,s),7.86-7.94(4H,m),7.59-7.61(2H,d),6.98-7.00(2H,d),6.78-6.85(1H,m),5.97-6.01(1H,d),5.42-5.45(1H,d),4.26-4.29(2H,m),4.03-4.06(2H,m),1.74-1.76(4H,m),1.48-1.50(4H,m).化合物[MA36]的合成[化82]在1L四口燒瓶中添加化合物[MA36-1](52.0g、0.24mol)、6-馬來醯亞胺己烷酸(50.0g、0.24mol)、EDC(67.9g、0.35mol)、DMAP(2.9g、24mmol)、THF(250g),於25℃進行攪拌。反應結束後,將反應溶液注入乙酸乙酯(2L)中,用飽和食鹽水(200mL)清洗3次後,用硫酸鈉乾燥有機層。之後,進行過濾,用蒸發器蒸餾除去溶劑,向得到的殘渣中添加甲酸(280g),於50℃進行加熱攪拌。確認反應結束後,用冰浴冷卻反應溶液,之後,將反應溶液注入蒸餾水(1.5L)中,過濾析出的固體,用乙腈進行清洗。將得到的粗產物用乙酸乙酯(90g)進行再漿化清洗,進行過濾、乾燥,從而得到24.5g化合物[MA36](收率43%)。1H-NMR(400MHz,DMSO-d6,δppm):12.43(1H,s),7.73-7.76(2H,d),7.57-7.61(1H,d),7.14-7.17(2H,d),7.02(2H,s),6.50-6.54(1H,d),3.40-3.43(2H,t),2.56-2.59(2H,t),1.60-1.68(2H,m),1.50-1.58(2H,m),1.27-1.34(2H,m).化合物[MA37]的合成[化83]在1L四口燒瓶中添加化合物[MA37-1](39.5g、0.20mol)、6-馬來醯亞胺己烷酸(50.0g、0.24mol)、EDC(56.9g、0.30mol)、DMAP(2.4g、20mmol)、THF(500g),於25℃進行攪拌。反應結束後,將反應溶液注入乙酸乙酯(2L)中,用飽和食鹽水(200mL)清洗3次後,用硫酸鈉乾燥有機層。之後,進行過濾,用蒸發器蒸餾除去溶劑,向得到的殘渣中添加甲酸(200g),於50℃進行加熱攪拌。確認反應結束後,用冰浴冷卻反應溶液,之後,將反應溶液注入蒸餾水(1L)中,過濾析出的固體。將得到的粗產物用乙酸乙酯/己烷=2/1溶液(90g)進行再漿化清洗,進行過濾、乾燥,從而得到29.8g化合物[MA37](收率45%)。1H-NMR(400MHz,DMSO-d6,δppm):13.04(1H,s),7.97-8.00(2H,d),7.22-7.26(2H,d),7.02(2H,s),3.40-3.44(2H,t),2.58-2.61(2H,t),1.61-1.68(2H,m),1.50-1.58(2H,m),1.27-1.35(2H,m).化合物[MA38]的合成[化84]在1L四口燒瓶中添加化合物[MA38-1](20.0g、0.06mol)、衣康酸單甲酯(13.4g、0.09mol)、EDC(23.8g、0.12mol)、DMAP(0.8g、6.0mmol)、CH2Cl2(200g),於25℃進行攪拌。反應結束後,將反應溶液注入乙酸乙酯(500mL)中,用飽和食鹽水(200mL)清洗3次後,用硫酸鈉乾燥有機層。之後,進行過濾,用蒸發器蒸餾除去溶劑,向得到的殘渣中添加甲酸(150g),於50℃進行加熱攪拌。確認反應結束後,用冰浴冷卻反應溶液,之後,將反應溶液注入蒸餾水(700ml)中,過濾析出的固體,用乙腈進行清洗。將得到的粗產物用乙酸乙酯(100g)進行再漿化清洗,進行過濾、乾燥,從而得到10.7g化合物[MA38](收率44%)。1H-NMR(400MHz,DMSO-d6,δppm):12.21(1H,s),7.61-7.63(2H,d),7.51-7.55(1H,d),6.94-6.97(2H,d),6.35-6.39(1H,d),6.20(1H,s),5.82(1H,s),4.08-4.11(2H,t),3.99-4.02(2H,t),3.59(3H,s),3.37(2H,s),1.70-1.74(2H,m),1.59-1.63(2H,m),1.37-1.44(4H,m).化合物[MA39]的合成[化85]在2L四口燒瓶中添加化合物[MA2](75.6g、0.25mol)、傘形酮(40.0g、0.09mol)、EDC(70.93g、0.25mol)、DMAP(3.0g、25mmol)、THF(750g),於25℃進行攪拌。反應結束後,將反應溶液注入蒸餾水(3L)中,過濾析出的固體,用異丙醇進行清洗,並進行乾燥,從而得到91.9g化合物[MA39](收率83%)。1H-NMR(400MHz,DMSO-d6,δppm):8.08-8.12(3H,m),7.81-7.83(1H,d),7.45(1H,s),7.30-7.32(1H,d),7.12-7.14(2H,d),6.49-6.52(1H,d),6.02(1H,s),5.67(1H,s),4.09-4.13(4H,m),1.88(3H,s),1.75-1.79(3H,m),1.64-1.67(2H,m),1.41-1.47(4H,m).化合物[MA42]的合成[化86]在帶冷卻管的100ml茄型燒瓶中添加4-羥基肉桂酸甲酯3.6g(20.0mmol)、2-(4-溴-1-丁基)-1,3-二氧戊環4.2g(20.0mmol)、碳酸鉀5.5g(40mmol)、以及丙酮50ml以形成混合物,一邊在溫度64℃下攪拌24小時一邊使其反應。反應結束後,將反應液注入純水500ml中,得到白色的固體6.0g。將該固體用NMR進行測定,測定的結果如下所示。根據該結果,確認該白色固體是中間體化合物[MA42-1](收率98%)。1HNMR(CDCl3)δ:1.62(m,2H),1.76(m,2H),1.87(m,2H),3.79(s,3H),3.85(m,2H),4.00(m,4H),4.90(m,1H),6.29(d,1H),6.90(d,2H),7.45(d,2H),7.64(d,1H).[化87]接著,在帶冷卻管的200ml茄型燒瓶中添加上述得到的中間體化合物[MA42-1]6.0g(20mmol)、2-(溴甲基)丙烯酸3.3g(20mmol)、THF55.0ml、氯化錫(II)4.3g(23mmol)、及10質量%HCl水溶液17.0ml以形成混合物,一邊在溫度70℃下攪拌20小時一邊使其反應。反應結束後、將反應液減壓過濾,與純水40ml混合,在其中添加氯仿50ml,進行萃取。萃取進行3次。在萃取後的有機層中添加無水硫酸鎂進行乾燥,從減壓過濾後的溶液蒸餾除去溶劑,得到粘稠性液體4.3g。將該黏稠性液體用NMR進行測定,測定的結果如下所示。根據該結果,確認該黏稠性液體是中間體化合物[MA42-2](收率65%)。1HNMR(CDCl3)δ:1.5-1.9(m,6H),2.63(m,1H),3.07(s,1H),3.80(s,3H),4.03(t,2H),4.58(m,1H),5.64(m,1H),6.23(m,1H),6.30(d,1H),6.90(d,2H),7.45(d,2H),7.64(d,1H).[化88]在帶冷卻管的200ml茄型燒瓶中添加乙醇60ml、上述得到的化合物[MA42-2]4.3g(13mmol)、以及10%氫氧化鈉水溶液15ml以形成混合物,一邊在溫度85℃下攪拌5小時一邊使其反應。反應結束後,在500ml的燒杯中添加水300ml和反應液,在室溫下攪拌30分鐘後,滴加10質量%的HCl水溶液15ml後,進行過濾,得到白色固體。接著,在帶冷卻管的50ml茄型燒瓶中,添加得到的白色固體、10質量%HCl水溶液15ml、和四氫呋喃60.0ml以形成混合物,在溫度70℃下攪拌5小時使其反應。反應結束後,將反應液注入純水500ml中,得到白色的固體。將該白色固體通過重結晶(己烷/四氫呋喃=2/1)進行純化後,得到白色固體3.0g。將該固體用NMR進行測定,測定的結果如下所示。根據該結果,確認該白色固體是目標的聚合性液晶化合物[MA42](收率73%)。1HNMR(DMSO-d6)δ:1.45(m,2H),1.53(m,2H),1.74(m,2H),2.62(m,1H),3.12(m,1H),4.04(m,2H),4.60(m,1H),5.70(s,1H),6.03(s,1H),6.97(d,2H),7.52(d,1H),7.63(d,2H),12.22(s,1H).化合物[MA46]的合成[化89]在6-氯己醇(544g,4000mmol)和PPTS(1.01g,4mmol)的二氯甲烷(1632g)溶液中,用3小時滴加二氫吡喃(403g,480mmol),在室溫下攪拌18小時。在該溶液中添加純水(1500g),將有機相清洗3次後,用硫酸鎂進行乾燥。通過過濾除去硫酸鎂後,進行濃縮,得到無色油狀的[MA46-1](收量:870g,收率:98.5%)。1H-NMR(400MHz,CDCl3,δppm):4.59-4.56(1H,m),3.89-3.84(1H,m),3.78-3.71(1H,m),3.56-3.47(3H,m),3.42-3.36(1H,m),1.88-1.35(14H,m).將添加有4-反-4-羥基環己基苯酚(96.1g,500mol)、MAX-1(121g,550mmol)、碳酸鉀(89.8g,650mmol)和碘化鉀(8.33g,50mmol)的DMF(二甲基甲醯胺)溶液(288g)在80℃下攪拌18小時。之後,通過過濾除去碳酸鉀,用乙酸乙酯(1400g)稀釋後,使用純水(840g),將有機相清洗3次,用硫酸鎂進行乾燥。通過過濾除去硫酸鎂後,進行濃縮,從而得到粗產物[MA46-2](粗收量:232g、粗收率:123%)。得到的粗產物[MA46-2]不用純化,用於接下來的反應。1H-NMR(400MHz,CDCl3,δppm):7.10(2H,d),6.82(2H,m),4.59-4.56(1H,m),3.93-3.84(3H,m),3.78-3.62(2H,m),3.56-3.49(1H,m),3.41-3.38(1H,m),2.48-2.41(1H,m),2.10-2.04(1H,m),1.92-1.29(20H,m).添加[MA46-2](116g、250mmol)、4-甲氧基桂皮酸(49.0g、275mmol)、1-(3-二甲基氨基丙基)-3-乙基碳二亞胺(57.5g、300mmol)、4-二甲基氨基吡啶(36.7g、30mmol)、THF(575g),在室溫下反應24小時。通過過濾除去反應液中析出的粘性物質,用乙酸乙酯(2000g)稀釋後,用水(1000g)清洗3次,用硫酸鎂進行乾燥。通過過濾除去硫酸鎂後,進行濃縮,在得到的殘渣中添加PPTS(12.6g,50mmol)、乙醇(862g),在70℃下攪拌18小時。將得到的反應液注入水(4000g)中,攪拌2小時。將析出的固體通過過濾回收後,用2-丙醇進行重結晶,得到[MA46-3](收量:93.3g、收率:82.4%)。1H-NMR(400MHz,DMSO,δppm):7.59(2H,d),7.61(1H,d),7.15(2H,d),6.97(2H,d),6.83(2H,d),6.49(1H,d),4.84-4.78(1H,m),4.34(1H,t),3.91(2H,t),3.80(3H,s),3.41-3.36(2H,m),2.07-2.04(2H,m),1.84-1.81(2H,m),1.81-1.30(13H,m).在[MA46-3](81.5g、180mmol)、三乙胺(23.7g、234mol)的THF(407g)溶液中用1小時滴加甲基丙烯醯氯(20.5g、196mmol),之後在室溫下攪拌18小時。將得到的反應液用乙酸乙酯(2500g)稀釋,用水(1500g)清洗3次,用硫酸鎂進行乾燥。通過過濾除去硫酸鎂後,進行濃縮,將得到的粗產物用THF(1000g)再溶解,添加活性炭(8.15g),在室溫下攪拌2小時。之後通過過濾除去活性炭,濃縮後,用2-丙醇(400g)進行清洗,得到目標化合物[MA46](收量:52.0g、收率:55.5%)。1H-NMR(400MHz,CDCl3,δppm):7.65(1H,d),7.49(2H,d),7.12(2H,d),6.91(2H,d),6.83(2H,d),6.32(1H,d),6.01(1H,s),5.55(1H,s),4.93-4.88(m,1H),4.15(2H,t),3.94(2H,t),3.85(3H,s),2.51-2.47(1H,m),2.18-2.15(2H,m),1.97-1.91(5H,m),1.83-1.42(12H,m).(有機溶劑)THF:四氫呋喃NMP:N-甲基-2-吡咯烷酮BC:丁基溶纖劑CH2Cl2:二氯甲烷(聚合引發劑)AIBN:2,2』-偶氮二異丁腈[相轉移溫度的測定]由實施例得到的聚合物的液晶性呈現溫度使用差示掃描量熱測定儀(DSC)DSC3100SR(馬可賽恩斯公司(マック·サイエンス社)制)進行測定。將MA1(9.97g、30.0mmol)溶解於THF(92.0g)中,用隔膜泵進行脫氣後,添加AIBN(0.246g、1.5mmol),再次進行脫氣。之後,在50℃下使其反應30小時,得到甲基丙烯酸酯的聚合物溶液。將該聚合物溶液滴加到二乙醚(1000ml)中,過濾得到的沉澱物。將該沉澱物用二乙醚進行清洗,在40℃的爐中進行減壓乾燥,得到甲基丙烯酸酯聚合物粉末(A)。該聚合物的數均分子量為16000,重均分子量為32000。得到的甲基丙烯酸酯聚合物的液晶性呈現溫度為145℃~190℃。在得到的甲基丙烯酸酯聚合物粉末(A)(6.0g)中添加NMP(29.3g),在室溫下攪拌5小時以使其溶解。通過在該溶液中添加NMP(24.7g)、BC(40.0g),進行攪拌,得到液晶取向劑(A1)。[液晶晶胞的製作]使用上述得到的液晶取向劑(A1),按照下述所示的步驟進行液晶晶胞的製作。基板使用30mm×40mm的尺寸、厚度為0.7mm的玻璃基板,其配置有將ITO膜圖案化而形成的梳齒狀的像素電極。像素電極具有將多個中央部分彎曲的「く」字形狀的電極元件排列而構成的梳齒狀的形狀。各電極元件的短邊方向寬度為10μm,電極元件間的間隔為20μm。形成各像素的像素電極由多個中央部分彎曲的、「く」字形狀的電極元件排列而構成,所以各像素的形狀不是長方形狀,而是具有與電極元件同樣地中央部分彎曲的、類似粗「く」字的形狀。於是,各像素以其中央的彎曲部分為界被上下分割,具有彎曲部分上側的第一區域和下側的第二區域。對各像素的第一區域和第二區域進行比較時,發現構成它們的像素電極的電極元件的形成方向是不同的。即、將後述的液晶取向膜的取向處理方向作為基準的情況下,像素的第一區域中,像素電極的電極元件以呈+15°的角度(順時針方向)的方式形成,像素的第二區域中,像素電極的電極元件以呈-15°的角度(順時針方向)的方式形成。即、各像素的第一區域和第二區域中,以由像素電極和對置電極之間的電壓施加而引發的液晶在基板面內的旋轉動作(平面內切換)的方向為彼此相反的方向的方式構成。將上述得到的液晶取向劑(A1)旋塗在準備好的上述帶電極的基板上。接著,用70℃的加熱板乾燥90秒,形成膜厚100nm的液晶取向膜。接著,對於塗膜面隔著偏振片以5mJ/cm2照射313nm的紫外線後,用150℃的加熱板加熱10分鐘,得到帶液晶取向膜的基板。另外,在作為相向基板的未形成有電極的具有高度為4μm的柱狀間隔物的玻璃基板上也同樣形成塗膜,實施取向處理。在一塊基板的液晶取向膜上印刷密封劑(協立化學株式會社(協立化學)制XN-1500T)。接著,將另一塊的基板以使液晶取向膜的相對取向方向為0°的條件進行貼合後,熱固化密封劑,製得空晶胞。在該空晶胞中通過減壓注入法注入液晶MLC-2041(默克公司(メルク株式會社)制),密封注入口,得到具備IPS(In-PlanesSwitching:面內轉換)模式液晶顯示元件的構成的液晶晶胞。(殘影評價)將實施例1中準備的IPS模式用液晶晶胞設置在以偏光軸正交的方式配置的兩塊偏振片之間,在未施加電壓的狀態下使背光源發光,調整液晶晶胞的配置角度以使透射光的亮度達到最小。接著,將從像素的第二區域為最暗的角度到第一區域為最暗的角度旋轉液晶晶胞時的旋轉角度作為初期取向方位角而算出。接著,在60℃的爐中,以頻率30Hz施加168小時的16VPP的交流電壓。之後,使液晶晶胞的像素電極和對置電極之間處於短路的狀態,保持該狀態下於室溫放置1小時。放置後,同樣地測定取向方位角,將交流驅動前後的取向方位角的差作為角度Δ(deg.)算出。將MA1(4.99g、15.0mmol)、MA2(4.60g、15.0mmol)溶解於THF(88.5g)中,用隔膜泵進行脫氣後,添加AIBN(0.246g、1.5mmol),再次進行脫氣。之後,在50℃下使其反應30小時,得到甲基丙烯酸酯的聚合物溶液。將該聚合物溶液滴加到二乙醚(1000ml)中,過濾得到的沉澱物。將該沉澱物用二乙醚進行清洗,在40℃的爐中進行減壓乾燥,得到甲基丙烯酸酯聚合物粉末(B)。該聚合物的數均分子量為14000,重均分子量為29000。得到的甲基丙烯酸酯聚合物的液晶性呈現溫度為135℃~180℃。在得到的甲基丙烯酸酯聚合物粉末(B)(6.0g)中添加NMP(29.29g),在室溫下攪拌5小時以使其溶解。通過在該溶液中添加NMP(24.7g)、BC(450.0g),進行攪拌,得到液晶取向劑(B1)。對於液晶取向劑(B1),除了將紫外線的照射量改為20mJ、將使用加熱板的加熱溫度改為140℃以外,通過與實施例1相同的步驟製作液晶晶胞後,進行殘影評價。將MA3(10.29g、20.0mmol)溶解於NMP(94.1g)中,用隔膜泵進行脫氣後,添加AIBN(0.164g、1.0mmol),再次進行脫氣。之後,在50℃下使其反應30小時,得到甲基丙烯酸酯的聚合物溶液。將該聚合物溶液滴加到甲醇(1000ml)中,過濾得到的沉澱物。將該沉澱物用甲醇進行清洗,在40℃的爐中進行減壓乾燥,得到甲基丙烯酸酯聚合物粉末(C)。該聚合物的數均分子量為19000,重均分子量為39000。得到的甲基丙烯酸酯聚合物的液晶性呈現溫度為150℃~300℃。在得到的甲基丙烯酸酯聚合物粉末(C)(1.0g)中添加CH2Cl2(99.0g),在室溫下攪拌5小時使其溶解,得到液晶取向劑(C1)。對於液晶取向劑(C1),除了將紫外線的照射量改為300mJ、將使用加熱板的加熱溫度改為180℃以外,通過與實施例1相同的步驟製作液晶晶胞後,進行殘影評價。將MA4(8.16g、20.0mmol)溶解於NMP(75.0g)中,用隔膜泵進行脫氣後,添加AIBN(0.164g、1.0mmol),再次進行脫氣。之後,在70℃下使其反應30小時,得到甲基丙烯酸酯的聚合物溶液。將該聚合物溶液滴加到甲醇(1000ml)中,過濾得到的沉澱物。將該沉澱物用甲醇進行清洗,在40℃的爐中進行減壓乾燥,得到甲基丙烯酸酯聚合物粉末(D)。該聚合物的數均分子量為18000,重均分子量為29000。得到的甲基丙烯酸酯聚合物的液晶性呈現溫度為225℃~290℃。在得到的甲基丙烯酸酯聚合物粉末(D)(6.0g)中添加NMP(29.29g),在室溫下攪拌5小時以使其溶解。通過在該溶液中添加NMP(24.7g)、BC(40.0g),進行攪拌,得到液晶取向劑(D1)。對於液晶取向劑(D1),除了將紫外線的照射量改為30mJ、將使用加熱板的加熱溫度改為240℃以外,通過與實施例1相同的步驟製作液晶晶胞後,進行殘影評價。將MA5(8.66g、25.0mmol)溶解於NMP(79.8g)中,用隔膜泵進行脫氣後,添加AIBN(0.205g、1.3mmol),再次進行脫氣。之後,在70℃下使其反應30小時,得到甲基丙烯酸酯的聚合物溶液。將該聚合物溶液滴加到甲醇(1000ml)中,過濾得到的沉澱物。將該沉澱物用甲醇進行清洗,在40℃的爐中進行減壓乾燥,得到甲基丙烯酸酯聚合物粉末(E)。該聚合物的數均分子量為16000,重均分子量為31000。得到的甲基丙烯酸酯聚合物在30℃~300℃的溫度範圍內沒有呈現出液晶性。在得到的甲基丙烯酸酯聚合物粉末(E)(6.0g)中添加NMP(29.29g),在室溫下攪拌5小時以使其溶解。通過在該溶液中添加NMP(24.7g)、BC(40.0g),進行攪拌,得到液晶取向劑(E1)。對於液晶取向劑(E1),除了將紫外線的照射量改為500mJ、將照射後使用加熱板的加熱溫度改為150℃以外,通過與實施例1相同的步驟製作液晶晶胞後,進行殘影評價。除了使用液晶取向劑(A1),將紫外線照射量改為5mJ/cm2、50mJ/cm2或500mJ/cm2,以及在照射後沒有進行使用加熱板的加熱以外,與實施例1同樣地製作了液晶晶胞。[表1]表1.如表1所示,實施例1~4中均表現出良好的取向性,交流驅動前後的取向方位角的差、即角度Δ(deg.)也在0.1以下,極為良好。另一方面,比較例1中,沒有呈現出液晶性,沒有再取向,結果角度Δ(deg.)高達1.4度。此外,沒有進行光照射後的再加熱的比較例2~4中,液晶沒有取向,無法測定角度Δ(deg.)。將MA1(1.99g、6.0mmol)、MA2(7.35g、24.0mmol)溶解於THF(85.5g)中,用隔膜泵進行脫氣後,添加AIBN(1.48g、3.0mmol),再次進行脫氣。之後,在50℃下使其反應30小時,得到甲基丙烯酸酯的聚合物溶液。將該聚合物溶液滴加到二乙醚(1000ml)中,過濾得到的沉澱物。將該沉澱物用二乙醚進行清洗,在40℃的爐中進行減壓乾燥,得到甲基丙烯酸酯聚合物粉末。得到的甲基丙烯酸酯聚合物的液晶性呈現溫度為140℃~182℃。在得到的甲基丙烯酸酯聚合物粉末(6.0g)中添加NMP(29.3g),在室溫下攪拌5小時以使其溶解。通過在該溶液中添加NMP(24.7g)、BC(40.0g),進行攪拌,得到液晶取向劑(T1)。[液晶晶胞的製作]除了使用實施例5中得到的液晶取向劑(T1)來代替實施例1的液晶取向劑(A1)以外,通過與實施例1中的「液晶晶胞的製作」相同的方法,得到液晶晶胞。(殘影評價)除了使用實施例5中準備的IPS模式用液晶晶胞以外,通過與實施例1的(殘像評價)同樣的方法,算出角度Δ(deg.)。根據表2所示的組成,使用與上述實施例5同樣的方法合成了實施例6~51的液晶取向劑(T2~T48)。對於得到的液晶取向劑(T2~T30和T42~48),除了紫外線的照射量和使用加熱板的加熱的溫度以外,通過與實施例5相同的步驟製作了液晶晶胞。將各液晶晶胞的製作條件和殘影評價結果示於表3中。[表2]表2.[表3]表2.續[表4]表2.續[表5]表3.如表1和表3所示,通過對呈現液晶性的側鏈型高分子膜照射紫外線後,在液晶性呈現溫度範圍內進行加熱,從而高分子整體通過自組織化被高效地賦予液晶取向能力,所以即使在長期的AC驅動後,也幾乎沒有觀測到取向方位的偏差。另一方面,如比較例那樣,可知在使用不呈現液晶性的側鏈型高分子的情況下,由於長期的AC驅動,會導致取向方位發生偏差。可認為其原因是,僅在膜中的發生光反應的部分進行液晶取向,高分子和液晶的相互作用弱。由此,確認了通過本發明的方法製造的液晶顯示元件表現出非常優異的殘影特性。符號說明圖11側鏈型高分子膜2、2a側鏈圖23側鏈型高分子膜4、4a側鏈圖35側鏈型高分子膜6、6a側鏈圖47側鏈型高分子膜8、8a側鏈
