β‑葡聚糖與影響腫瘤微環境的抗癌劑的組合的製作方法
2023-05-22 09:29:37 4
本申請要求於2014年7月10日提交的序列號為62/022,754、2014年11月6日提交的序列號為62/076,094、2015年2月13日提交的序列號為62/115,895和2015年4月20日提交的序列號為62/149,892的美國臨時專利申請的優先權,所有這些申請都通過引用而併入本文。
背景技術:
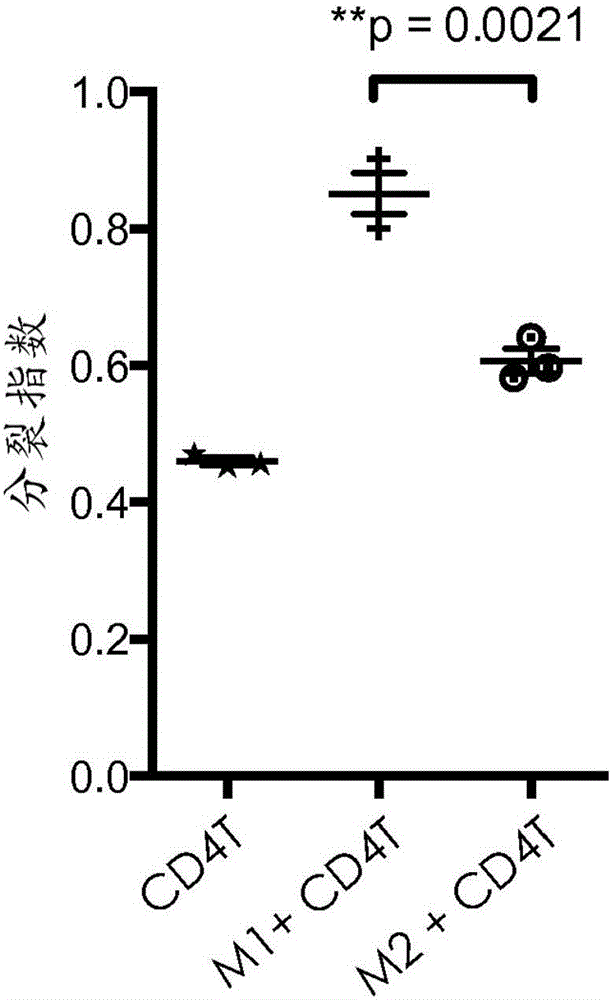
:本發明涉及可溶性β-葡聚糖與包括減輕免疫抑制的抗癌劑在內的影響腫瘤微環境的抗癌劑的組合。β-葡聚糖為真菌PAMP,並且被血清中的模式識別分子C3以及在包括嗜中性粒細胞和單核細胞在內的先天性免疫細胞上的模式識別受體——補體受體3(CR3)識別。來源於酵母的多糖β-葡聚糖——β-葡聚糖(β(1,6)-[聚-(1,3)-D-吡喃葡萄糖基]-聚-β(1,3)-D-吡喃葡萄糖)正在作為與抗腫瘤單克隆抗體組合用於治療若干種癌症的免疫治療劑進行研發。β-葡聚糖使得先天性免疫效應細胞能夠通過補體CR3依賴性機制殺死補體包被的腫瘤細胞。許多動物腫瘤模型已經證明,與單獨的任一藥劑相比,可溶性β-葡聚糖與補體激活性、腫瘤靶向性抗體的聯合施用導致顯著降低的腫瘤生長和改善的總體存活率。然而,癌症不僅僅是大量的惡性細胞,其還是募集並利用許多其他非轉化細胞的複雜「器官」。惡性細胞與非轉化細胞之間的相互作用產生腫瘤微環境(TME)。TME中的非惡性細胞在癌發生的各個階段具有動態且多為腫瘤促進性的功能。細胞因子、趨化因子、生長因子和炎症因子以及基質重塑酶的複雜且動態的網絡驅動受影響組織內的細胞間通訊。因此,為了有效對抗癌症,必須開發出抑制TME的腫瘤促進性質的療法。技術實現要素:在一個方面,本公開內容描述了可溶性β-葡聚糖與影響腫瘤微環境的抗癌劑組合的用途和組合物。以上對本發明的概述並非旨在描述本發明的每一個公開的實施方案或每一次實施。下面的描述更具體地舉例說明了說明性的實施方案。在整個申請中的若干部分,通過實例列表提供了指導,這些實例可以以各種組合的方式來使用。在每種情況下,所記載的列表僅用作代表性的組,而不應被解釋為排他性列表。附圖說明圖1A-1D.體外培養的人M1和M2巨噬細胞的形態和功能表徵。圖2A-2D.可溶性β-葡聚糖處理的M2巨噬細胞的形態、表型和功能表徵。圖3A-3D.在β-葡聚糖處理的來自強結合者和弱結合者的M1和M2巨噬細胞中,CD4T細胞增殖以及對IFN-γ和IL-4產生的調節的評估。圖4.在免疫抑制條件下,β-葡聚糖處理的M2和M2a巨噬細胞中的T細胞增殖和IFN-γ調節的評估。圖5A-5E.在Treg的存在下β-葡聚糖對CD4/CD8T細胞增殖和活化作用的評估。圖6A-6B.體外培養的人未成熟單核細胞來源的樹突細胞(imMoDC)和成熟單核細胞來源的樹突細胞(mMoDC)的表徵。圖7A-7D.β-葡聚糖對MoDC成熟的影響的評估。圖8A-8C.由於細胞-細胞接觸而導致的M2-β-葡聚糖增加CD4T細胞增殖的結果。圖9.由於可溶性因子而導致的M2-β-葡聚糖增加CD4T細胞增殖的結果。圖10.強結合者與弱結合者中β-葡聚糖處理的M2巨噬細胞的分析。圖11A-11B.在來自強結合者的血清的存在下,來源於弱結合者的單核細胞的M2-β-葡聚糖的功能評估結果。圖12A-12B.在免疫抑制細胞因子(TCM)的存在下培養的β-葡聚糖處理的M2巨噬細胞上的PD-L1上調。圖13.MiaPaCa中的PD-L1上調。圖14A-14B.可溶性β-葡聚糖對骨髓來源的抑制細胞(MDSC)的影響。圖15.腫瘤細胞上的β-葡聚糖誘導的PD-L1表達的評估。圖16.採用IMPRIMEPGG與DC101抗體組合的小鼠研究的結果。圖17A-17C.可溶性β-葡聚糖和貝伐珠單抗(bevicizumab)對腫瘤微環境的體內影響。具體實施方式β-葡聚糖是來源於包括例如酵母、細菌、藻類、海藻、蘑菇、燕麥和大麥在內的多種微生物和植物源的葡萄糖聚合物。其中,已經對酵母β-葡聚糖就其免疫調節性質進行了廣泛研究。酵母β-葡聚糖可以以多種形式存在,例如,完整酵母、酵母聚糖、純化的全葡聚糖顆粒、溶解的酵母聚糖多糖或不同分子量的高度純化的可溶性β-葡聚糖。在結構上,酵母β-葡聚糖由排列為β-(1,3)-連接的吡喃葡萄糖骨架的葡萄糖單體和經由β-(1,6)糖苷鍵連接至該骨架上的周期性β-(1,3)吡喃葡萄糖分支構成。不同形式的酵母β-葡聚糖可以彼此不同地發揮作用。酵母β-葡聚糖發揮其免疫調節作用的機制可受到不同形式的β-葡聚糖之間的結構差異例如其顆粒或可溶性性質、三級構象、主鏈長度、側鏈長度和側鏈頻率的影響。酵母β-葡聚糖的免疫刺激功能還依賴於在不同物種的不同細胞類型中所涉及的受體,該受體也可依賴於β-葡聚糖的結構性質。通常,β-葡聚糖免疫療法可包括向受試者施用任何適宜形式的β-葡聚糖或兩種或更多種形式的β-葡聚糖的任意組合。適宜的β-葡聚糖以及適宜的β-葡聚糖從其天然來源的製備在例如公開號為US2008/0103112A1的美國專利申請中描述。在一些情況下,β-葡聚糖可以來源於酵母,例如釀酒酵母(Saccharomycescerevisiae)。在某些情況下,β-葡聚糖可以是或衍生自β(1,6)-[聚-(1,3)-D-吡喃葡萄糖基]-聚-β(1,3)-D-吡喃葡萄糖,其在本文中也稱為PGG(IMPRIMEPGG,Biothera,Eagan,MN),為酵母來源的可溶性β-葡聚糖的一種高度純化且充分表徵的形式。此外,基於β-葡聚糖的免疫療法可涉及使用例如修飾的和/或衍生的β-葡聚糖,如申請號為PCT/US12/36795的國際專利申請中描述的那些。在其他情況下,β-葡聚糖免疫療法可涉及施用例如顆粒狀可溶性β-葡聚糖或顆粒狀可溶性β-葡聚糖製品,它們在例如第7,981,447號美國專利中均有描述。抗癌免疫治療藥物通過多種方式殺死癌細胞:1)先天性免疫細胞的直接激活,2)適應性免疫細胞的直接激活,3)通過使腫瘤細胞更具免疫原性或通過摧毀腫瘤誘導的免疫抑制而對先天性和適應性免疫細胞的間接激活。越來越多的證據表明,腫瘤微環境(TME)下的骨髓細胞,包括M2巨噬細胞、N2嗜中性粒細胞和骨髓來源的抑制細胞(MDSC),通過直接引起細胞毒性T細胞的功能性耗竭或通過間接增加T調節細胞(Treg)的抑制能力而在免疫抑制中起到關鍵作用。這導致TME中免疫刺激與免疫抑制平衡出現偏移。TME的免疫刺激環境主要受細胞毒性T細胞和NK細胞、細胞溶解和誘導吞噬的M1巨噬細胞、細胞毒性N1嗜中性粒細胞、誘導體液應答的B細胞以及抗原呈遞免疫原性樹突細胞(DC)的存在而影響。免疫刺激細胞因子和趨化因子如幹擾素γ(IFN-γ)、白介素-12(IL-12)、腫瘤壞死因子-α(TNF-α)等是免疫刺激活性的關鍵協調物。使得TME的免疫抑制性質發生偏移的重要參與者為抗炎Th2細胞、N2嗜中性粒細胞、M2巨噬細胞、Treg和致耐受性DC。免疫抑制性細胞因子和趨化因子如轉化生長因子-β(TGF-β)、白介素-10(IL-10)、巨噬細胞集落刺激因子(M-CSF)、白介素-4(IL-4)等是免疫抑制活性的關鍵協調物。憑藉與骨髓來源的細胞(即嗜中性粒細胞和單核細胞)上的CD11b結合的病原體相關分子模式(PAMP),可溶性β-葡聚糖與N1嗜中性粒細胞和M1巨噬細胞結合併增加它們的免疫刺激功能,並且降低MDSC、N2嗜中性粒細胞和M2巨噬細胞的免疫抑制功能。這種調節導致TME中不同的先天性和適應性細胞亞群之間的交互(cross-talk),並最終使平衡朝免疫刺激方向傾斜。更具體地,一旦與外周血單核細胞結合,可溶性β-葡聚糖就在M1/抗致瘤性極化相比M2/促致瘤性極化條件下調節單核細胞向巨噬細胞的分化,使得M1極化得到增強從而增加巨噬細胞免疫刺激功能,而M2極化得到抑制從而降低巨噬細胞免疫抑制功能。可溶性β-葡聚糖直接影響M2復極化為M1表型並驅動Th1極化,並且即使在Treg的存在下,可溶性β-葡聚糖引發的先天性免疫細胞產生細胞因子以間接影響CD4和CD8T細胞增殖,並最終驅動Th1極化。可溶性β-葡聚糖通過已知將先天性和適應性免疫應答聯繫起來的兩個先天性細胞亞群(單核細胞來源的巨噬細胞和樹突細胞)而引發適應性免疫應答,並將會上調在單核細胞來源的巨噬細胞和樹突細胞兩者上的PD-L1表達。儘管PD-L1上調,但可溶性β-葡聚糖處理的單核細胞來源的巨噬細胞和樹突細胞使T細胞活化和增殖增強,並且由可溶性β-葡聚糖引發的協調的免疫應答引起類似於適應性免疫抗性的腫瘤反應,即PD-L1表面表達的上調。可溶性β-葡聚糖可與非補體激活性、腫瘤靶向性減輕免疫抑制的MAb組合。例如,可溶性β-葡聚糖可在包括黑素瘤、腎細胞癌、肺癌等若干種癌症的治療中與抗PD-L1免疫檢查點抑制劑(Fc-工程化的IgG1MAb)進行組合。已報導,抗-PD1/PD-L1抗體的效力依賴於腫瘤上PD-L1的表達水平。腫瘤上PD-L1表達的機制之一被稱為適應性免疫抗性,其中由於腫瘤微環境內的免疫應答(例如,活化T細胞的幹擾素γ產生)而適應性地誘導PD-L1表達。可溶性β-葡聚糖直接或間接誘導Th1極化。這種作用使PD-L1在腫瘤細胞上的表達上調,從而增強抗-PD1/PD-L1抗體的抗腫瘤活性。檢驗點抑制劑的實例為納武單抗(nivolumab)和派姆單抗(pembrolizumab)。可溶性β-葡聚糖可與增強免疫共刺激的非補體激活性、非腫瘤靶向性MAb組合。例如,a)靶向樹突細胞的抗-CD40MAb(IgG2MAb),b)若干種癌症治療中T細胞共刺激的增強劑:抗-OX40、抗-41BB。可溶性β-葡聚糖還可與非補體激活性、非腫瘤靶向性減輕免疫抑制的小分子以及非補體激活性、腫瘤靶向性減輕免疫抑制的小分子進行組合。其可用作癌症疫苗中的佐劑以驅動Th1極化。其可在治療上用來減弱慢性疾病(即,TB)中的抑制機制,以加速感染的完全清除。最後,其可用來使Th2佔優勢的自身免疫性疾病(變態反應、哮喘、特應性疾病)中的Th2-Th1平衡向Th1極化環境方向偏移。雖然非補體激活性免疫抑制減輕劑可能是優選的,特別是對於非腫瘤靶向劑而言,但本發明也可利用補體激活性免疫抑制減輕劑來進行。一個實例可為巴維昔單抗(bavituximab)。本發明部分地包括共施用β-葡聚糖與另一種藥劑,如本文所用的,該藥劑可為抗體製品或小分子製品或為了影響TME而施用的任何製品。如本文所用的,「共施用」是指兩種或更多種組分的組合施用,使得該組合的治療或預防效果可大於任一組分單獨施用時的治療或預防效果。兩種組分可以同時共施用或順序地共施用。同時共施用的組分可以在一個或多個藥物組合物中提供。兩種或更多種組分的順序共施用包括這樣的情況,其中施用這些組分使得所有組分在施用後是同時生物可利用的。無論組分是同時共施用還是順序地共施用,組分均可在單一部位或在不同部位處共施用。在另一方面,所述方法包括向受試者施用組合物,該組合物包含與抗體、治療性抗體、抗腫瘤抗體或抗體片段如抗體的Fc部分綴合的β-葡聚糖部分。申請號為PCT/US12/36795的國際專利申請中描述了修飾的和/或衍生的可溶性β-葡聚糖,包括β-葡聚糖部分與抗體的β-葡聚糖綴合物,這也可應用於抗體片段的綴合物。β-葡聚糖部分可以是或衍生自β-1,3/1,6葡聚糖。在這種語境中,「衍生自」表示綴合物可能必須通過產生替換β-葡聚糖的一個或多個原子的共價鍵來製備。如本文所用的,「衍生自β-1,3/1,6葡聚糖」是指在替換β-葡聚糖的一個或多個原子以形成綴合物的共價鍵之後作為該綴合物的一部分而保留的β-葡聚糖的一部分。可將β-葡聚糖、抗體或小分子製品和/或兩種組分的組合與「載體」一起配製於組合物中。如本文所用的,「載體」包括任何溶劑、分散介質、媒介物、塗料、稀釋劑、抗細菌劑和/或抗真菌劑、等滲劑、吸收延遲劑、緩衝液、載體溶液、懸浮液、膠體等。這類介質和/或試劑作為藥物活性物質的應用是本領域公知的。除非任何常規介質或試劑均與β-葡聚糖或抗體不相容,否則將涵蓋其在治療組合物中的應用。補充的活性成分也可摻入組合物中。「藥學上可接受的」意指在生物學上或在其他方面並非不期望的物質,即,該物質可與β-葡聚糖和/或藥劑一起施用至個體,而不會引起任何不期望的生物效應或不會以有害的方式與包含它的藥物組合物中的任何其他組分相互作用。可將β-葡聚糖、藥劑和/或兩種組分的組合配製成藥物組合物。在一些實施方案中,β-葡聚糖和藥劑可以在單一製劑中提供。在其他實施方案中,β-葡聚糖和藥劑可以在分開的製劑中提供。可將藥物組合物配製成適應於一種或多種優選的給藥途徑的各種和/或多種形式。因此,藥物組合物可經由一種或多種已知的途徑來施用,包括例如口服、腸胃外(例如,皮內、經皮、皮下、肌內、靜脈內、腹膜內等)或局部(例如,鼻內、肺內、乳房內、陰道內、子宮內、皮內、經皮、直腸等)給藥途徑。可以將藥物組合物或其部分施用於黏膜表面,例如通過向例如鼻或呼吸道黏膜(例如,通過噴霧或氣霧劑)施用。還可經由持續或延遲釋放來施用藥物組合物或其部分。製劑可以方便地以單位劑型提供,並且可通過藥學領域公知的方法來製備。製備具有藥學上可接受的載體的組合物的方法包括使β-葡聚糖和/或藥劑與構成一種或多種輔助成分的載體相結合的步驟。通常,可通過使活性化合物與液體載體、精細粉碎的固體載體或兩者均勻和/或緊密地結合,並且如果需要,然後將產物成形為所需的製劑而製備該製劑。β-葡聚糖、藥劑和/或兩種組分的組合可以以任何合適的形式提供,包括但不限於溶液、懸浮液、乳液、噴霧劑、氣霧劑或任何形式的混合物。該組合物可以與任何藥學上可接受的賦形劑、載體或媒介物一起在製劑中遞送。例如,該製劑可以以常規的局部劑型來遞送,例如乳膏、軟膏、氣霧製劑、非氣霧噴霧劑、凝膠、洗劑等。該製劑可進一步包含一種或多種添加劑,包括例如佐劑、皮膚滲透促進劑、著色劑、香料、調味劑、保溼劑、增稠劑等。在一些實施方案中,β-葡聚糖可來源於酵母,例如釀酒酵母。在一些實施方案中,β-葡聚糖可包括β-1,3/1,6葡聚糖,例如,β(1,6)-[聚-(1,3)-D-吡喃葡萄糖基]-聚-β(1,3)-D-吡喃葡萄糖。在一些實施方案中,所述方法可包括施用足夠的β-葡聚糖以向受試者提供例如約100ng/kg至約50mg/kg的劑量,但在一些實施方案中,可通過以該範圍之外的劑量施用β-葡聚糖來實施該方法。在一些實施方案中,所述方法包括施用足夠的β-葡聚糖以向受試者提供約10μg/kg至約5mg/kg的劑量,例如約4mg/kg的劑量。或者,可採用在治療過程臨開始前獲得的實際體重來計算劑量。對於以這種方式計算的劑量,利用Dubois方法在治療過程開始前計算體表面積(m2):m2=(體重kg0.425×身高cm0.725)×0.007184。因此,在一些實施方案中,所述方法可包括施用足夠的β-葡聚糖以提供例如約0.01mg/m2至約10mg/m2的劑量。在一些實施方案中,所述方法可包括施用足夠的能與β-葡聚糖特異性結合的抗體,以向受試者提供例如約100ng/kg至約50mg/kg的劑量,但在一些實施方案中,可通過以該範圍之外的劑量施用該抗體來實施該方法。在一些實施方案中,所述方法包括施用足夠的抗體以向受試者提供約10μg/kg至約5mg/kg的劑量,例如約100μg/kg至約1mg/kg的劑量。或者,可採用在治療過程臨開始前獲得的實際體重來計算劑量。對於以這種方式計算的劑量,利用Dubois方法在治療過程開始前計算體表面積(m2):m2=(體重kg0.425×身高cm0.725)×0.007184。因此,在一些實施方案中,所述方法可包括施用足夠的抗體以提供例如約0.01mg/m2至約10mg/m2的劑量。在一些實施方案中,β-葡聚糖和藥劑可以例如以每周單劑量到多劑量來共施用,但在一些實施方案中,可以通過以該範圍之外的頻率來共施用β-葡聚糖和藥劑而實施該方法。在某些實施方案中,β-葡聚糖和藥劑可以大約每年施用一次至每周施用一次。術語「和/或」意指所列出的要素的一個或全部,或任意兩個或更多個所列出的要素的組合;術語「包括」及其變化形式在說明書和權利要求中出現時不具有限制性含義;除非另有說明,否則「一個」、「一種」、「該」和「至少一個」可互換使用,並且意指一個或超過一個;並且利用端點對數值範圍的表述包括包含在該範圍內的所有數值(例如,1至5包括1、1.5、2、2.75、3、3.80、4、5等)。在前面的描述中,為清楚起見,可以單獨地描述特定的實施方案。除非另外明確說明特定實施方案的特徵與另一實施方案的特徵不兼容,否則某些實施方案可包括本文關於一個或多個實施方案所描述的兼容特徵的組合。對於包括離散步驟的本文公開的任何方法,這些步驟可以以任何可行的順序進行。並且根據需要,可以同時進行兩個或更多個步驟的任何組合。本發明通過以下實施例予以說明。應當理解,特定的實施例、材料、量和程序應根據本文所述的本發明的範圍和精神而進行寬泛地解釋。實施例實施例1體外培養的人M1和M2巨噬細胞的建立和表徵:採用Ficoll梯度和磁珠分離來富集來自人全血的CD14+單核細胞。然後將所富集的單核細胞(5×105個細胞/mL)於M1-極化(補充有5%自體血清和100ng/mL重組人粒細胞巨噬細胞集落刺激因子(rhGM-CSF)(R&DSystems)的XVivo10培養基(LonzaGroup))或M2-極化(補充有10%自體血清和50ng/mL重組人巨噬細胞集落刺激因子(rhM-CSF)(R&DSystems)的XVivo10培養基)條件下培養6天。在為了評價β-葡聚糖的作用而進行的實驗中,首先將全血與媒介物(檸檬酸鈉緩衝液)或25μg/mL可溶性β-葡聚糖在37℃下溫育2小時,然後分離單核細胞並使其分化。在收集巨噬細胞以供表型分析之前檢查其形態。收集第6天巨噬細胞培養物(MCM)的培養基,離心(spundown)以除去汙染的細胞沉澱,然後冷凍以供隨後通過ELISA進行細胞因子分析或用來建立與CD3和CD28刺激的CD4T細胞的共培養物(MCM-CD4T)以用於評估表面標誌物或CD4T細胞增殖。在第6天,利用巨噬細胞建立與CD3和CD28刺激或僅CD3刺激的CD4T細胞(Mac-CD4T)的共培養物,以用於評估表面標誌物調節或對CD4T細胞增殖的影響。對於Mac-CD4T細胞增殖研究,以1:10比例將M1或M2巨噬細胞與CD3和CD28刺激或僅CD3刺激的、CFSE標記的自體CD4T細胞一起培養。在實驗結束時(第9天至第11天)通過流式細胞術測量T細胞增殖,並且結果以圖形表示為CFSE-稀釋峰。始終在第11天進行僅CD3刺激的T細胞的評估。定量結果被報告為在每個培養條件下針對三個重複孔中的每一個計算的分裂指數(群體經歷的細胞分裂的平均次數)。收集Mac-CD4T共培養物的培養上清液用於隨後的細胞因子分析。為了評估Mac-CD4T細胞表面標誌物調節,如上所述將M2巨噬細胞與T細胞一起共培養,並在第8天、第9天和第10天收穫細胞以對M2巨噬細胞和T細胞二者進行表面受體染色。對於MCM-CD4T細胞增殖研究,用50%MCM來培養CD3和CD28刺激的CFSE標記的CD4T細胞。如上所述在第11天測量T細胞增殖。收集MCM-CD4T細胞共培養物的培養上清液用於隨後的細胞因子分析。如上所述進行MCM-CD4T細胞表面標誌物評估。對於如上所述製備和表徵的M1和M2巨噬細胞,表徵了A)形態,B)表型,C)Mac-CD4T細胞增殖的功能評價,和D)共培養物中的細胞因子分析。圖1A-圖1C包括來自5個不同實驗的代表性結果。根據文獻所述,M1的形態似乎更圓,而M2則更類似於細長的成纖維細胞(圖1A)。通過流式細胞術評估M1/M2特異性標誌物的表達。計算了同種型對照染色和表面抗原染色的MFI中值,該結果示於表1中。表1與關於表型的文獻一致,M1巨噬細胞通常表達更高水平的HLA-DR和CD274(PD-L1),而M2巨噬細胞則表達更高水平的CD163和CD14。此外,如圖1B所示,與體外分化的M2巨噬細胞相比,M1巨噬細胞還明顯有助於CD4T細胞增殖。隨著增殖增強,在M1和CD4T細胞共培養物的上清液中觀察到幹擾素γ(IFN-γ)的產生增加(圖1C)。用於體外培養和表徵人巨噬細胞的備選方法的步驟(包括M1和M2巨噬細胞的活化(稱為M1a和M2a巨噬細胞))概述如下。該方法在以下一系列實驗中使用。表徵了如上所述製備和表徵的活化M1a和M2s巨噬細胞的形態和表型。在此示出了來自5個不同實驗的代表性結果。圖1D示出了M1a和M2a巨噬細胞的形態。通過流式細胞術評估M1a/M2a特異性標誌物的表達。計算了同種型對照染色和表面抗原染色的MFI中值,該結果示於表2中。表2實施例2β-葡聚糖對M2至M1復極化的影響:如上所述製備來自媒介物處理的或β-葡聚糖處理的全血的M1和M2巨噬細胞。通過流式細胞術測量一組M1/M2特異性標誌物(包括HLA-DR、CD163、CD206、CD209、CD80、CD86和PD-L1)的表達。β-葡聚糖預處理不影響M1巨噬細胞表型,但的確影響M2巨噬細胞表型。如圖2A所示,CD163的平均螢光強度(MFI)在β-葡聚糖處理的M2巨噬細胞中下調。此外,CD86的表面表達以及PD-L1的蛋白質和mRNA水平都得到增強(圖2B)。接下來,將媒介物處理的或β-葡聚糖處理的M1或M2巨噬細胞與CD3和CD28刺激的、羧基螢光素二乙酸琥珀醯亞胺酯(CFSE)標記的自體CD4T細胞一起培養,並在實驗結束時通過流式細胞術來測量T細胞增殖,並將結果定量地報告為分裂指數(群體已經經歷的細胞分裂的平均次數)。圖2C是通過將T細胞與β-葡聚糖處理的M2巨噬細胞共培養而進行的代表性CFSE稀釋T細胞增殖試驗,並且結果顯示出β-葡聚糖處理的M2巨噬細胞增強CD4T細胞增殖的能力。還通過ELISA測量了來自CFSE稀釋T細胞增殖試驗(圖2B)的培養上清液的IFN-γ水平。圖2D是IFN-γ水平的代表圖,其顯示出IFN-γ產生的伴隨增加。因此,β-葡聚糖影響M2至M1復極化並驅動抗腫瘤發生的Th1極化。實施例3在來自強結合受試者和弱結合受試者的細胞中,β-葡聚糖對M2至M1復極化的影響:評估可溶性β-葡聚糖與嗜中性粒細胞和單核細胞的結合的早期研究揭示,受試者具有不同的結合能力。進一步的研究發現,可溶性β-葡聚糖與至少一些強結合受試者的免疫細胞結合,並且強結合受試者還具有更高水平的天然抗β-葡聚糖抗體。功能研究鑑定了結合的總體截止值和抗體水平,用其將受試者鑑別為強結合者(對β-葡聚糖具有高反應)和弱結合者(對β-葡聚糖具有低反應)。為此,對來源於可溶性β-葡聚糖處理的來自強結合者和弱結合者的單核細胞的M1/M2巨噬細胞進行了評估。隨後評估來自強結合者和弱結合者的M1和M2巨噬細胞的A)表型,B)CD4T細胞增殖的增強,和C)IFN-γ和IL-4產生的調節。圖3A-圖3C示出了來自4個不同實驗的代表性結果。通過流式細胞術評估了對媒介物處理的和β-葡聚糖處理的、來源於強結合者的M1和M2巨噬細胞的一組標誌物的表達(對CD163評估兩次)。計算了同種型對照染色和表面抗原染色的MFI中值,該結果示於表3中。表3-強結合者通過流式細胞術評估了媒介物處理的和β-葡聚糖處理的、來源於弱結合者的M1和M2巨噬細胞的CD163和CD86。計算了同種型對照染色和表面抗原染色的MFI中值,結果示於表4中。表4-弱結合者關鍵的結果是β-葡聚糖處理的M2巨噬細胞具有更低的CD163表達,CD163是關鍵的M2標誌物之一。有趣的是,該結果對強結合者是特異的,因為CD163的表達在媒介物處理的和β-葡聚糖處理的M2巨噬細胞之間保持相同。接下來,評估了來源於可溶性β-葡聚糖處理的來自強結合者和弱結合者的單核細胞的M1/M2巨噬細胞增強CD3和CD28刺激的CD4T細胞增殖的能力。圖3A顯示了強結合者中CD4T細胞增殖試驗的結果,而圖3B則示出了弱結合者中的結果。在強結合者中與採用媒介物處理的M2巨噬細胞觀察到的相比,β-葡聚糖處理的M2巨噬細胞具有顯著更高的增強CD3和CD28刺激的CD4T細胞增殖的能力,而在弱結合者中增殖沒有增強。此外,無論在強結合者中還是在弱結合者中,與媒介物處理的M2巨噬細胞相比,β-葡聚糖處理的M1巨噬細胞在該功能能力方面沒有顯示出差異。然後評估了對媒介物處理的和β-葡聚糖處理的M2巨噬細胞的IFN-γ和IL-4產生的調節。隨著增殖增強,在強結合者(圖3C)而非弱結合者(圖3D)中的β-葡聚糖處理的M2巨噬細胞和CD4T細胞的共培養物中觀察到IFN-γ產生顯著增加,但IL-4並非如此。因此,來源於β-葡聚糖處理的單核細胞的M2巨噬細胞在強結合受試者中是M1樣的。實施例4免疫抑制條件下β-葡聚糖對M2至M1復極化的影響:在免疫抑制細胞因子的存在下,對β-葡聚糖處理的M2a巨噬細胞和β-葡聚糖處理的M2巨噬細胞進行了表型和功能評估。如上所述製備M2或M2a巨噬細胞。在第3天,向M2巨噬細胞培養物添加腫瘤條件培養基(TCM)直到佔培養物體積的70%,然後在第6天評估CD163表達和功能活性。已證明,來自BxPC3(一種胰腺癌細胞系)的TCM含有若干種免疫抑制細胞因子,包括M-CSF、TGF-β、IL-4等。如上所述在IL-4中培養M2a巨噬細胞。首先評估了在IL-4中培養的β-葡聚糖處理的M2a巨噬細胞和在TCM中培養的M2巨噬細胞的CD163和CD86表達。通過流式細胞術評估CD163和CD86,並計算同種型對照染色和表面抗原染色的MFI中值,該結果示於表5中。表5-免疫抑制條件如在先前使用M-CSF的M2分化實驗中所見,在TCM中培養的β-葡聚糖處理的單核細胞也顯示出CD163的顯著下調。此外,β-葡聚糖處理的M2巨噬細胞具有更高的HLA-DR表達(數據未示出)。然後通過CD4T細胞增殖試驗(每個條件重複三次或六次)對調節CD4T細胞增殖的能力進行功能評估。與採用媒介物處理的M2和M2a巨噬細胞觀察到的相比,在TCM中培養的β-葡聚糖處理的M2巨噬細胞和在IL-4中培養的M2a巨噬細胞保持增強CD4T細胞增殖的能力。隨著增殖增強,在巨噬細胞和CD4T細胞的共培養物中觀察到IFN-γ產生的顯著增加(圖4)。上述實施例證明,如通過CD163表達降低、CD86表達增加以及通過M2抑制CD4T細胞增殖的能力受到抑制所證明的,可溶性β-葡聚糖具有抑制M2極化並誘導更類似於M1的細胞的能力。即使在通過存在IL-4與M-CSF或腫瘤條件培養基(TCM)的組合而模擬的免疫抑制條件下,可溶性β-葡聚糖也能夠抑制M2極化並增強其幫助CD4T細胞增殖的能力。M2-可溶性β-葡聚糖對CD4T細胞增殖的增強伴隨著促炎性Th1極化細胞因子IFN-γ的增加,而免疫抑制性細胞因子IL-4的產生沒有變化。實施例5在Treg的存在下β-葡聚糖對CD4/CD8T細胞增殖和活化的影響:為獲得血漿,用25μg/mLβ-葡聚糖或媒介物處理全血6小時、離心並取出血漿。在50,000個T細胞活化CD3/28珠子(用於T細胞擴充和活化的DYNABEADS人T-激活劑CD3/CD28)的存在下,將50,000個自體CFSE標記的PBMC於處理的血漿中培養3天。在培養結束時,用CD4和CD8將PBMC染色,並通過CFSE稀釋測量T細胞增殖。如圖5A中的代表性CFSE稀釋圖所示,與媒介物處理的對照相比,來自β-葡聚糖處理的全血的血漿提供了CD4和CD8兩者增殖的顯著增強。接下來,為了顯示可溶性β-葡聚糖對CD4和CD8細胞活化的影響,再次進行了上述的T細胞增殖試驗。但是在第3天,針對包括粒酶B產生和CD25上調在內的激活標誌將細胞染色。圖5B中示出的圖形證明,β-葡聚糖處理的血漿增強了CD4和CD8細胞活化。當在血漿分離前將全血處理6小時的溫育期時,對增殖的增強最大,表明對T細胞增殖的這種影響是間接機制(即由先天性免疫細胞的細胞因子釋放)的結果。為了確定β-葡聚糖對T細胞增殖的增強是直接還是間接的,除了在添加至自體PBMC之前將來自未處理的(媒介物)全血的血漿用β-葡聚糖或媒介物處理之外,如上所述進行T細胞增殖試驗。利用FLOWJO軟體通過分裂指數對CFSE稀釋進行定量,並以相對於媒介物對照的倍數變化作圖。圖5C中所示的結果表明,β-葡聚糖的增強效應由間接機製造成。由於這些PBMC培養物含有Treg,因此Treg的抑制能力似乎在可溶性β-葡聚糖的存在下而改變,並進行研究以確定β-葡聚糖是否影響了Treg抑制。將來自β-葡聚糖處理的或媒介物處理的全血的血漿(如上所述)與數目逐漸增加的分離的自體Treg(CD4+CD25+)一起添加至25,000個分離的CFSE標記的自體CD4T細胞(CD4+CD25-),產生具有逐漸提高的比例的孔。然後用50,000個T細胞活化CD3/28珠子刺激細胞3天。隨後通過CFSE稀釋測量增殖,並通過分裂指數將其定量,該分裂指數用來計算共培養物中Treg的%抑制。%抑制=100-(Treg孔的分裂指數/1:0孔的分裂指數)/100。結果示於圖5D中。與來自媒介物處理的全血的血漿相比,來自β-葡聚糖處理的全血的血漿顯示出Treg的抑制能力的顯著降低。β-葡聚糖對Treg的抑制還導致增強的IFN-γ產生。如上所述進行Treg抑制試驗,並且在共培養3天後,分析上清液的IFN-γ產生。圖5E顯示了來自以8:1的T細胞:Treg比培養的孔的IFN-γ產生的結果。總之,這些結果顯示,β-葡聚糖影響CD4和CD8增殖以及Treg功能,導致抗腫瘤適應性效應子功能的增強。實施例6體外培養的人未成熟單核細胞來源的樹突細胞(imMoDC)和成熟單核細胞來源的樹突細胞(mMoDC)的建立和表徵:鑑於巨噬細胞和樹突細胞是將先天性和適應性免疫聯繫起來的兩種關鍵的抗原呈遞細胞類型,因此還在人單核細胞來源的樹突細胞(MoDC)上評估了可溶性β-葡聚糖的表型效果和功能效果。將從可溶性β-葡聚糖處理的或媒介物處理的全血中富集的單核細胞在含有適當細胞因子GM-CSF加IL-4的培養基中培養以供樹突細胞的分化。用於體外培養和表徵人MoDC的方法中包括的步驟概述如下。如上所述製備的imMoDC和mMoDC於圖6A中示出。mMoDC形態的特徵在於存在長突起或樹突。通過流式細胞術對mMoDC的CD80、CD83、CD86和HLA-DR表達進行了評估,並計算了同種型對照染色和表面抗原染色的MFI中值,該結果示於表6中。表6mMoDC顯示成熟和共刺激標誌物CD80、CD83、CD86以及HLA-DR的表面表達增加。此外,這些mMoDC還在同種異體混合淋巴細胞反應中顯示出免疫原性(每個條件重複四次),觸發CD4和CD8T細胞擴充的增加(圖6B)。實施例7β-葡聚糖對MoDC成熟的影響:進行了由可溶性β-葡聚糖處理的強結合者和弱結合者的全血製備的mMoDC的表型和功能評估。如上所述製備來自強結合者和弱結合者的mMoDC。通過流式細胞術對mMoDC的CD80、CD83、CD86和HLA-DR表達進行了評估,並計算了同種型對照染色和表面抗原染色的MFI中值,該結果示於表7中。表7-mMoDCβ-葡聚糖處理的來源於強結合者的mMoDC上CD80、CD86、CD83和HLA-DR的表達增加表明這些mMoDC比來源於弱結合者的那些更成熟。β-葡聚糖處理的來源於強結合者的mMoDC還在allo-MLR中顯示出免疫原性的增加(每個條件重複四次),從而再次觸發相對於來源於弱結合者的細胞(圖7B)增加的CD4和CD8T細胞擴充(圖7A)。此外,相對來源於弱結合者的細胞和媒介物處理的mMoDC,β-葡聚糖處理的來源於強結合者的mMoDC能夠調節IFN-γ產生(圖7C)。來源於β-葡聚糖處理的單核細胞的MoDC即使在免疫抑制條件下也是更成熟的。如上所述製備MoDC。在第0天添加TCM直到佔培養物體積的70%,並且TCM在整個培養期間都存在。隨後評估在TCM存在下培養的mMoDC的表型改變。計算同種型對照染色和表面抗原染色的MFI中值,該結果示於表8中。表8-免疫抑制條件實施例8細胞-細胞接觸和可溶性因子增加由β-葡聚糖處理的M2巨噬細胞引起的CD4T細胞增殖:利用CD4T細胞增殖作為讀出(read-out),研究了在由β-葡聚糖處理的M2巨噬細胞引發增殖中對細胞-細胞接觸或可溶性因子的要求。為了研究巨噬細胞與T細胞之間的細胞-細胞接觸,當在不存在CD28共刺激的情況下與β-葡聚糖處理的M2巨噬細胞共培養時測量了CD4T細胞增殖,並在共培養物中的β-葡聚糖處理的M2巨噬細胞和T細胞二者上研究了表面活化標誌物的調節。細胞-細胞接觸的評估如下進行:將媒介物處理的和β-葡聚糖處理的M2巨噬細胞以及CD3和CD28刺激與僅CD3刺激的CD4T細胞共培養物用於測量CD4T細胞增殖和IFN-γ產生。如圖8A所示,在不存在外源CD28抗體的情況下與CD4T細胞一起培養的β-葡聚糖處理的M2巨噬細胞表現出顯著更高的增強CD4T細胞增殖的能力。隨著增殖增強,在β-葡聚糖處理的M2巨噬細胞與CD4T細胞的共培養物中觀察到顯著增加的IFN-γ產生(圖8B)。還測量了巨噬細胞以及CD3和CD28刺激的T細胞二者上表面標誌物表達的變化。通過流式細胞術評估了來自共培養物的媒介物處理的和β-葡聚糖處理的M2巨噬細胞和CDT細胞對於共刺激分子或共抑制分子的調節。圖8C和表9為來自2個不同實驗的代表性結果。表9表面標誌物巨噬細胞上MFI的變化*T細胞上MFI的變化*HLA-DR無變化NACD86增加NACD80無變化NACD28NA無變化CTLA-4NA無變化CD40無變化NACD40LNA無變化4-1BBL無變化NA4-1BBNA無變化OX40無變化NAPD1(CD279)NA增加PD-L1(CD274)增加NACD209無變化NACD172無變化NA*β-葡聚糖處理的M2巨噬細胞/T細胞上的MFI相對於在媒介物處理的M2巨噬細胞/T細胞中觀察到的MFI的變化在所有測試的表面標誌物中,與媒介物處理的M2巨噬細胞上所觀察到的相比,在β-葡聚糖處理的M2巨噬細胞的表面上觀察到CD86(第8天)和PD-L1(第9天)的表面表達的相對增加。在與β-葡聚糖處理的M2巨噬細胞共培養的T細胞的表面上觀察到PD-1(第9天)表達的增加。為了確定是否需要由β-葡聚糖處理的M2巨噬細胞分泌的可溶性因子,對與β-葡聚糖處理的M2巨噬細胞MCM(50%體積)共培養的CD4T細胞增殖進行了測量,並觀察了與MCM一起溫育的T細胞上的表面活化標誌物調節。圖9代表2個不同的實驗。當通過CD4T細胞增殖試驗評估時,與媒介物處理的M2巨噬細胞MCM相比,與CD4T細胞一起培養的β-葡聚糖處理的M2巨噬細胞MCM表現出顯著更高的增強CD4T細胞增殖的能力(圖9)。此外,評估了在媒介物處理的和β-葡聚糖處理的M2巨噬細胞MCM中培養的CD4T細胞對共刺激或共抑制分子(CD80、CD28、CTLA-4、4-1BB和PD-1)的調節。令人驚訝的是,未觀察到任何T細胞標誌物的變化(數據未示出)。實施例9強結合者與弱結合者中β-葡聚糖處理的M2巨噬細胞的分析:如前所述,已顯示,受試者中的抗β-葡聚糖抗體(ABA)閾值對β-葡聚糖免疫療法是重要的。因此,研究了ABA閾值對β-葡聚糖調節M1/M2極化的能力的重要性。通過表型評估和功能評估確定了β-葡聚糖調節強結合者與弱結合者中的M1/M2極化的能力。製備了來自4位強結合者和4位弱結合者的M2巨噬細胞,並評估了它們調節CD4T細胞增殖的能力。通過ELISA來測量來自各種CD4T細胞增殖條件的上清液的IFN-γ。圖10所示的結果是來自4個不同實驗的代表。針對4位供體中的每一位,以相對於在媒介物處理的M2巨噬細胞和CD4T細胞的共培養物中產生的IFN-γ水平的倍數變化進行繪圖。在弱結合者中,β-葡聚糖在M1/M2極化條件下未調節單核細胞來源的巨噬細胞上的任何表型標誌物(數據未示出),並且在通過CD4T細胞增殖試驗對弱結合者的功能評估中,β-葡聚糖處理的M2巨噬細胞既未增強CD4T細胞增殖也未增加IFN-γ產生。實施例10血清交叉研究:因為β-葡聚糖未能在弱結合者中顯示出M1/M2極化的調節,所以在含有更高水平ABA的血清的存在下(來自強結合者的血清交叉),評估了採用來自弱結合者的單核細胞由β-葡聚糖引起的調節。為檢驗這一點,在進行了少許修改的情況下如上所述製備M2巨噬細胞。將弱結合者的全血離心以去除血漿,然後用從強結合者中獲得的血清來重建細胞。在37℃下用媒介物或β-葡聚糖(25μg/mL)將重建的血液處理2小時。通過採用抗β-葡聚糖特異性單克隆抗體及隨後採用流式細胞術來評估單核細胞的結合。然後分離全血中媒介物處理的或β-葡聚糖處理的單核細胞,並使其分化成M2巨噬細胞,並且採用上述方法使用M2細胞(數據未示出)或MCM來評估它們增強CD4T細胞增殖(每個條件重複六次)和增加IFN-γ產生的能力。弱結合者的全血中的單核細胞未與β-葡聚糖結合,但當將含有更高水平ABA的強結合者的血清添加至弱結合者的全血中時,顯示出顯著更高的結合(圖11A)。此外,與採用媒介物處理的M2巨噬細胞上所觀察到的相比,來自與強結合者的血清交叉的β-葡聚糖處理的弱結合者M2巨噬細胞的MCM具有顯著更高的增強CD4T細胞增殖的能力。隨著增殖增強,在β-葡聚糖處理的M2巨噬細胞與CD4T細胞的共培養物中觀察到顯著增加的IFN-γ產生(圖11B)。實施例11在免疫抑制細胞因子(TCM)的存在下培養的β-葡聚糖處理的M2巨噬細胞上的PD-L1上調:如上所述製備單核細胞或M2巨噬細胞。在第3天,添加TCM直到佔培養物體積的70%,然後評估TCM下的PD-L1表達,然後在與CD4T細胞共培養時再次評估PD-L1表達。在TCM中培養的β-葡聚糖處理的M2巨噬細胞具有更高的PD-L1表面表達(圖12A)。在與CD4T細胞共培養時,表達也增加(圖12B)。利用上述系統,如通過關鍵M2標誌物CD163的表達降低以及通過M2抑制CD4T細胞增殖的能力受到抑制所證明的,確定了β-葡聚糖具有抑制M2極化的能力。即使在通過存在IL-4與M-CSF(數據未示出)或腫瘤條件培養基(TCM)的組合而模擬的免疫抑制環境下,β-葡聚糖也能夠抑制M2極化並增強其幫助CD4T細胞增殖的能力。M2-β-葡聚糖對CD4T細胞增殖的增強伴隨著促炎性Th1極化細胞因子IFN-γ的增加,而免疫抑制性細胞因子IL-4的產生沒有變化。如隨著T細胞活化和IFN-γ產生增加所預期的,觀察到PD-L1在β-葡聚糖處理的M2巨噬細胞上的表面表達和PD-1在T細胞上的表面表達的增加。β-葡聚糖處理的M2巨噬細胞本身以及由該細胞分泌的可溶性因子對於增強CD4T細胞增殖是重要的。最後,β-葡聚糖僅在來自具有更高水平ABA的健康供體的細胞中抑制M2極化。實施例12MiaPaCa中的PD-L1上調:用強結合者血清和弱結合者血清培養β-葡聚糖處理的和媒介物處理的M2巨噬細胞和β-葡聚糖處理的M2巨噬細胞+ABA,以評估腫瘤細胞上的PD-L1表達。圖13顯示,β-葡聚糖處理的M2巨噬細胞使強結合者中的腫瘤細胞上的PD-L1表達增加,並且隨著ABA的添加,β-葡聚糖處理的M2巨噬細胞還使弱結合者中的腫瘤細胞上的PD-L1表達增加。實施例13可溶性β-葡聚糖對骨髓來源的抑制細胞(MDSC)的影響:MDSC積聚在大多數患有癌症的患者和實驗動物的血液、淋巴結和骨髓中以及腫瘤部位處,並且既抑制適應性免疫又抑制先天性免疫。MDSC由腫瘤分泌的因子和宿主分泌的因子誘導,其中許多因子都是促炎分子。促炎介質對MDSC的誘導產生以下假說:炎症促進使免疫監視和抗腫瘤免疫下調的MDSC的積聚,從而促進腫瘤生長。在不同時間從進行MPRIMEPGG治療的病例研究受試者中抽取血液,並分析MDSC的存在。第一次抽血在輸注前,第8循環,第1天進行。如圖14A所示,外周血中存在大量的CD33+MDSC。第二次抽血在輸注後,第8循環,第1天進行。如圖14A中的第二幅圖所示,在輸注後的幾小時內,MDSC短暫消失。最後一個血液樣品在在輸注前,第8循環,第15天抽取。CD33+MDSC再次出現在外周血中。在另一項研究中,將人臍帶血經針對CD34+細胞進行富集,並培養9天以產生CD33+CD11b+細胞(MDSC)。然後用可溶性β-葡聚糖或檸檬酸鹽緩衝液(對照)處理MDSC,並評估其抑制T細胞增殖的能力。在CD8T細胞與處理或未處理的MDSC的比例為2:1的條件下進行T細胞增殖試驗。如圖14B所示,β-葡聚糖處理的MDSC對T細胞增殖的抑制性較低。這些結果表明,β-葡聚糖調節MDSC群體,使它們短暫地離開外周血液循環並且對T細胞增殖的抑制性較低。因此,如果一種或多種癌症免疫治療藥物或化療藥物與可溶性β-葡聚糖聯合施用(特別是在CD33+細胞群體短暫缺失期間),那麼該療法將對腫瘤更加有效。實施例14來自β-葡聚糖處理的M2巨噬細胞/MoDC和T細胞共培養物的上清液誘導腫瘤細胞上的PD-L1表達:M2巨噬細胞和MoDC如上所述製備。隨後將巨噬細胞和MoDC如前所述用於T細胞增殖試驗。收穫來自這些增殖試驗的上清液,並將其與包括NSCLC、乳腺癌、胰腺癌、結腸癌和B細胞淋巴瘤在內的各種腫瘤細胞系一起溫育。在48小時後通過流式細胞術評估PD-L1在這些腫瘤細胞系上的表達。圖15示出了來自3個不同實驗的代表性結果。T細胞的效應機理需要三種信號。信號1是在抗原呈遞細胞(APC)上的MHC分子的背景下呈遞的抗原,信號2由APC上的膜共刺激分子提供,而信號3則為在效應子功能的環境中產生的細胞因子。共抑制分子如PD-L1可以抑制T細胞的效應子功能。來源於β-葡聚糖處理的單核細胞的巨噬細胞和樹突細胞在體外具有更高的PD-L1表達水平,但該處理也增加了共刺激分子CD86(信號2)和細胞因子(信號3)的表達,從而使得T細胞效應子功能增強。由β-葡聚糖引起的更廣泛的先天性和適應性免疫應答也增強了腫瘤細胞系上的PD-L1表達。這些結果證明,免疫細胞和腫瘤細胞兩者上由β-葡聚糖誘導的PD-L1表達上調使其成為檢查點抑制劑癌症免疫療法的有希望的組合配偶體。同樣重要的是注意到,β-葡聚糖還具有通過補償機制如增加共刺激分子的表達和免疫刺激性細胞因子的產生而抵消對PD-L1上調的抑制作用的能力。實施例15可溶性β-葡聚糖與抗血管生成劑組合對TME的影響:腫瘤血管生成改變TME中的免疫功能,從而導致免疫抑制環境。已經證明抗血管生成劑如抗VEGFR2抗體DC101(小鼠雷莫蘆單抗(ramucirumab)在癌症治療中有用。因為可溶性β-葡聚糖可使TME傾向於更為抗腫瘤的環境,所以將其與DC101組合用於治療小鼠中的NCI-H441非小細胞肺癌(NSCLC)皮下異種移植物,以增加DC101抗體的有效性。6至8周齡的雌性無胸腺裸鼠在脅腹皮下注射0.2ml體積的5×106個H441腫瘤細胞。當平均腫瘤體積達到約150mm3時,每兩周一次給予小鼠以下藥劑:·0.2ml/小鼠媒介物·1.2mg/小鼠IMPRIMEPGG(Biothera,Inc.)·10mg/kg或20mg/kgDC101(克隆:DC101目錄號:BE0060)在第10天和最後一次給藥後2小時收集血液樣品。處理組包括媒介物(PBS對照)、單獨的IMPRIMEPGG、單獨的DC101和DC101+IMPRIMEPGG。一旦腫瘤大小達到組平均值150mm3,則將腫瘤隨機分入處理組。10mg/kg處理組的結果在圖16中示出。從圖中可見,IMPRIMEPGG+DC101(補體激活性、非腫瘤靶向性抗體)協同作用而使腫瘤的生長降至最低。因此,可溶性β-葡聚糖與抗血管生成劑(其可以是或可以不是補體激活性、非腫瘤靶向性抗體)組合是有效的癌症療法。實施例16可溶性β-葡聚糖與抗PD-L1抗體組合提高無腫瘤存活率:在另一項動物研究中,向小鼠注射MC38腫瘤細胞並將其隨機分入處理組。8至12周齡的雌性C57BL/6小鼠在脅腹皮下注射0.1ml體積的1×106個MC38腫瘤細胞(表達低水平PD-L1的結腸腺癌)。在第3天開始每兩周一次給予小鼠以下藥劑:·0.2ml/小鼠媒介物·1.2mg/小鼠IMPRIMEPGG(Biothera,Inc.)·100μg/小鼠抗-PDL-1克隆:10F.9G2BioXcell目錄號:BE0101在第1次給藥前1小時、第3次給藥後2小時、終點和最後一次給藥後2小時(第20天)收集血液樣品。處理組包括媒介物(PBS對照)、單獨的IMPRIMEPGG、單獨的抗PD-L1抗體和抗PD-L1+IMPRIMEPGG。一旦腫瘤大小達到組平均值150mm3,則將腫瘤隨機分入處理組。該結果示於表10中。表10處理組無腫瘤存活者(第29天)媒介物1/18IMPRIMEPGG2/18抗-PD-L16/18抗-PD-L1+IMPRIMEPGG14/17再次,抗PD-L1抗體+可溶性β-葡聚糖的組合協同作用,以有效地提高無腫瘤存活率。還應注意,腫瘤上的PD-L1表達是抗PD-1抗體反應性的生物標誌。因此,由於可溶性β-葡聚糖誘導腫瘤上的PD-L1表達,因此可溶性β-葡聚糖還將增強抗PD-1抗體的有效性。這通過上述可溶性β-葡聚糖處理誘導的PD-1表達增加而得到證實。實施例17可溶性β-葡聚糖和抗血管生成劑對TME的體內影響:如上文針對其他小鼠研究所描述的,向攜帶H1299NSCLC腫瘤的小鼠施用貝伐珠單抗(bevacizumab)(一種抗血管生成抗體)和IMPRIMEPGG。如圖17A所示,施用貝伐珠單抗與IMPRIMEPGG的組合的處理組顯示出PD-L1表達的增加,圖17B顯示精氨酸酶1的下調,而圖17C顯示與單獨施用貝伐珠單抗的組相比,TME的C11b陽性先天性免疫浸潤物中的iNOS表達增加。iNOS增加和精氨酸酶1減少是指示M1免疫刺激環境的標誌。該數據清楚地說明,可溶性β-葡聚糖增強了抗血管生成劑的有效性並在體內調節TME。本文引用的所有專利、專利申請和出版物以及可通過電子方式獲得的材料(例如,包括例如GenBank和RefSeq形式的核苷酸序列提交材料,以及例如SwissProt、PIR、PRF、PDB形式的胺基酸序列提交材料,以及GenBank和RefSeq形式的來自注釋編碼區的翻譯)的完整公開內容通過引用整體併入本文。在本申請的公開內容與通過引用而併入本文的任何文獻的公開內容之間存在任何不一致的情況下,應以本申請的公開內容為準。前面的詳述和實施例僅僅是為了清楚理解的目的而提供的。不應從中得出不必要的限制。本發明不限於所示出和描述的確切細節,因為對於本領域技術人員顯而易見的變化將包括在由權利要求限定的發明內。除非另有說明,否則在說明書和權利要求書中使用的表示組分的量、分子量等的全部數字應被理解為在所有情況下均被術語「約」修飾。因此,除非另有相反的指示,否則說明書和權利要求書中所述的數值參數為近似值,其可以根據本發明所尋求獲得的預期性質而變化。至少,並且並非試圖將等同原則限制於權利要求的範圍,每個數值參數均應當至少根據所報告的有效數字的位數以及通過應用普通的捨入技術來解釋。儘管闡述本發明的寬範圍的數值範圍和參數是近似值,但在具體實施例中闡述的數值是儘可能精確地報告的。然而,所有數值都固有地包括必定由在其各自的測試量度中出現的標準偏差導致的範圍。所有標題均是為了方便讀者,並且不應被用來限制標題後的正文的含義,除非是如此規定的。權利要求書(按照條約第19條的修改)1.一種組合物,其包含:可溶性β-葡聚糖;以及減輕免疫抑制的抗癌劑。2.如權利要求1所述的組合物,其中所述減輕免疫抑制的抗癌劑為檢查點抑制劑。3.如權利要求2所述的組合物,其中所述檢查點抑制劑為抗-PD-L1抗體。4.如權利要求1-3中任一項所述的組合物,其進一步包含:增強免疫共刺激的非腫瘤靶向性抗體。5.如權利要求1-3中任一項所述的組合物,其進一步包含:抗血管生成劑。6.如權利要求5所述的組合物,其中所述抗血管生成劑為抗血管生成抗體。7.如權利要求1-6中任一項所述的組合物,其中所述可溶性β-葡聚糖來源於酵母。8.如權利要求7所述的組合物,其中所述可溶性β-葡聚糖包含β-1,3/1,6葡聚糖。9.在單一製劑中提供的任何前述權利要求的組合物。10.如任何前述權利要求所述的組合物,其中所述可溶性β-葡聚糖組分和所述減輕免疫抑制的抗癌劑組分在分開的製劑中提供。11.可溶性β-葡聚糖和抗-PD-L1抗體在可溶性β-葡聚糖免疫療法中的用途。12.如權利要求11所述的用途,其中所述抗-PD-L1抗體為非補體激活性抗體。13.如權利要求11-12中任一項所述的用途,其進一步包括增強免疫共刺激的非腫瘤靶向性抗體。14.如權利要求11所述的用途,其中所述可溶性β-葡聚糖來源於酵母。15.如權利要求11所述的用途,其中所述可溶性β-葡聚糖包含β-1,3/1,6葡聚糖。16.如權利要求11所述的用途,其中所述可溶性β-葡聚糖和抗-PD-L1抗體協同作用以提高無腫瘤存活率。17.可溶性β-葡聚糖和抗-VEGFR2抗體在可溶性β-葡聚糖免疫療法中的用途。18.如權利要求17所述的用途,其中所述抗-VEGFR2抗體為非補體激活性抗體。19.如權利要求17所述的用途,其中所述可溶性β-葡聚糖和抗-VEGFR2抗體協同作用以使腫瘤生長降至最低。20.如權利要求17所述的用途,其中所述可溶性β-葡聚糖來源於酵母。21.如權利要求17所述的用途,其中所述可溶性β-葡聚糖包含β-1,3/1,6葡聚糖。22.如權利要求17所述的用途,其中所述可溶性β-葡聚糖包含β(1,6)-[聚-(1,3)-D-吡喃葡萄糖基]-聚-β(1,3)-D-吡喃葡萄糖。23.一種治療癌症的方法,該方法包括共施用包含可溶性β-葡聚糖和減輕免疫抑制的抗癌劑的組合物。24.如權利要求23所述的方法,其中所述可溶性β-葡聚糖和所述減輕免疫抑制的抗癌劑同時共施用。25.如權利要求23所述的方法,其中所述可溶性β-葡聚糖和所述減輕免疫抑制的抗癌劑在不同時間共施用。26.如權利要求23-25中任一項所述的方法,其中與所述癌症有關的腫瘤細胞在所述組合物共施用之前表達低水平的PD-L1。27.如權利要求23所述的方法,其中所述減輕免疫抑制的抗癌劑為抗-PD-L1抗體。28.如權利要求23所述的方法,其中所述癌症為非小細胞肺癌、乳腺癌、胰腺癌、結腸癌、B細胞淋巴瘤、黑素瘤和腎細胞癌中的一種。當前第1頁1 2 3 
