用於治療心力衰竭的方法與流程
2023-08-07 11:48:21 3
對相關申請的引用
本申請要求2015年12月23日提交的澳大利亞專利申請號2014905243的優先權,其全部內容通過引用併入。
公開領域
本公開涉及用於治療或預防具有升高的左心室收縮末期容積(lvesv)的受試者的心力衰竭的方法。
背景技術:
由於心肌梗死(mi)所致的心力衰竭仍然是發達國家中的死亡率和發病率的主要原因之一。已經公布了美國醫療保險記錄的最近更新,其評估了牽涉>65歲的患者中350,509例急性mi住院的數據,所述患者在其事件後活著出院(schuster等人(2004)physiolheartcircaphysiol.,287(2):525-32)。在指數事件後的第一年內,25.9%的mi患者死亡,50.5%重新住院。在mi後的一個月中,死亡的可能性比普通醫療保險年齡人群中高21倍,並且住院的可能性高12倍。
具有mi後的較大梗死和更多的梗死後lv功能障礙的患者處於經歷中長期心臟事件和死亡的顯著升高的風險。具體來說,在梗死後期前壁梗死、較大的梗死、和更多的lv功能障礙處於經歷中長期心臟事件和死亡的顯著升高的風險(eitel等人(2010)jamcollcardiol.,55:2470-9)。
本領域中強烈需要用於預防和治療心力衰竭的新的且有效的方法,特別是避免對心臟移植物(其中器官的可用性罕見)的需要的治療方法。特別是下述系統,其允許在不呈現與全身麻醉和開放心臟手術有關的風險和潛在併發症的情況下逆轉心臟組織損傷或者修復心臟組織缺陷。
公開內容
出乎意料地,用間充質譜系前體細胞進行的臨床前心臟研究已經證明了在最大量的心肌損傷的背景中產生最佳結果。這產生了下述的可能性:來自受損心肌的信號對於根本的生物化學/生理學紊亂和間充質譜系前體細胞之間的組織水平上的「串擾(cross-talk)」是必需的,以使間充質譜系前體細胞釋放其「有效負載」,即旁分泌因子。此觀察已經得到研究支持,所述研究證明了在將細胞注射到健康心肌組織中時沒有顯著的間充質譜系前體細胞介導的效應。
本公開基於下述觀察:具有由於顯著的左心室收縮異常(即收縮功能障礙)所致的晚期慢性心力衰竭的患者中間充質前體細胞(mpc)的心肌施用增強mpc的效力信號。特別地,本公開基於下述發現,即具有中等嚴重左心室收縮損傷的受試者良好響應mpc的經心內膜遞送,並且具有由於左心室收縮功能異常所致的慢性心力衰竭的患者中基線左心室收縮異常的幅度越大,mpc相關心臟保護效果的益處越大。
更特別地,發明人已經發現了使用心力衰竭受試者中的基線左心室收縮末期容積(lvesv)截止值鑑定了有主要不良心臟事件(mace)的高風險的晚期心力衰竭的受試者群體,並且鑑定了最佳響應mpc施用的受試者群體。
本公開提供了用於治療或預防受試者的心力衰竭的方法,其包括向受試者施用間充質譜系前體細胞或幹細胞的群體和/或其後代和/或自其衍生的可溶性因子,所述受試者具有大於70ml的升高的左心室收縮末期容積(lvesv)。
在一個實例中,升高的lvesv是由於急性心肌梗死。在另一個實例中,升高的lvesv是由於慢性充血性心力衰竭。
在另一個實例中,方法包括以下步驟:
i)選擇具有大於70ml的升高的lvesv的受試者,並且
ii)向所述受試者施用間充質譜系前體細胞或幹細胞的群體和/或其後代和/或自其衍生的可溶性因子。
在另一個實例中,方法包括以下步驟:
i)診斷具有心力衰竭的受試者;
ii)選擇具有大於70ml的升高的lvesv的診斷受試者的群組;並且
iii)向受試者施用間充質譜系幹細胞或前體細胞的群體和/或其後代和/或自其衍生的可溶性因子。
在一個實例中,lvesv大於80ml、大於90ml、大於100ml、大於100ml、大於110ml、大於120ml或大於130ml。在另一個實例中,lvesv大於80ml/m2、大於90ml/m2、大於100ml/m2、大於110ml/m2、大於120ml/m或大於130ml/m2。
在一個實例中,通過基於導管的系統向所述受試者施用所述細胞和/或其後代和/或可溶性因子。在另外的實例中,使用插入受試者的靜脈系統中的導管在組織損傷處或附近向受試者的心肌施用所述細胞和/或其後代和/或可溶性因子。在另一個實例中,可以全身施用所述細胞和/或其後代和/或可溶性因子。可以在鑑定需要治療的心肌區域後進行細胞和/或其後代和/或可溶性因子的遞送。
在另外的實例中,通過經心內膜注射、冠狀動脈內輸注或經心外膜注射向所述受試者施用所述細胞和/或其後代和/或可溶性因子。
在另外的實例中,受試者的特徵為具有小於或等於約35%的左心室射血分數(lvef)。在另一個實例中,受試者具有小於約35%、小於約30%、小於約25%、或小於約20%的lvef。
在一個實例中,心力衰竭是由於高血壓、心肌病(缺血性或非缺血性)、心肌炎、肥胖症或糖尿病。在另外的實例中,在診斷心力衰竭後向受試者施用間充質譜系幹細胞或前體細胞和/或其後代和/或自其衍生的可溶性因子。
在一個實例中,受試者具有急性心肌病。在另外的實例中,受試者具有缺血性心肌病。在另外的實例中,受試者具有非缺血性心肌病。在另外的實例中,受試者具有擴張性或充血性心肌病。在另外的實例中,受試者具有限制型心肌病。
在另一個實例中,在急性心肌梗死後向受試者施用間充質譜系幹細胞或前體細胞和/或其後代和/或自其衍生的可溶性因子。在另外的實例中,在診斷心力衰竭後約1-7天向受試者施用間充質譜系幹細胞或前體細胞和/或其後代和/或自其衍生的可溶性因子。在另外的實例中,在心肌梗死後約1-7天向受試者施用間充質譜系幹細胞或前體細胞和/或其後代和/或自其衍生的可溶性因子。在另外的實例中,在診斷心力衰竭後,或在心肌梗死後約3-5天向受試者施用間充質譜系幹細胞或前體細胞和/或其後代和/或自其衍生的可溶性因子。
在另一個實例中,受試者具有約5%-30%,或約10%-20%左心室的梗死大小。
用於診斷心力衰竭的方法會是本領域技術人員熟悉的。實例包括受試者的身體檢查、心電圖、胸部x-射線、通過血液測試測定bnp和/或肌鈣蛋白水平、超聲心動圖顯象、都卜勒超聲、霍爾特監護儀(holstermonitor)、核子心臟掃描、心導管插入術、應激測試或心臟磁共振成像(心臟mri)。
根據本公開的用於選擇具有大於70ml的升高的lvesv的受試者的方法是本領域技術人員熟悉的。例如,可以通過本領域中已知的設備測量受試者的lvesv,包括但不限於二維超聲心動圖顯象、磁共振斷層攝影術、心臟計算機斷層攝影術(ct)或雙平面左心室電影造影術。另外,本領域技術人員會熟悉術語「升高的lvesv」的界限和邊界,如該術語在本領域中理解以及如本文中其它地方描述。
可以對接受用於心力衰竭和/或其症狀的藥物或其它治療的受試者進行根據本公開的間充質譜系幹細胞或前體細胞和/或其後代的施用。或者,它可以對未接受用於心力衰竭的其它藥物或治療的受試者進行。在一些實例中,對先前已經經歷冠狀動脈旁路移植(cabg)或左心室輔助裝置(lvad)植入的受試者進行根據本公開的間充質譜系幹細胞或前體細胞和/或其後代的施用。受試者經歷的cabg或lvad植入方案可以伴隨或可以不伴隨根據本公開的間充質譜系幹細胞或前體細胞和/或其後代的同時施用。在一些實例中,對正在經歷cabg或lvad植入的個體進行根據本公開的間充質譜系幹細胞或前體細胞和/或其後代的施用。在其它實例中,對尚未接受和/或不會接受用於治療受損/缺陷的心臟組織的任何療法的受試者進行根據本公開的間充質譜系幹細胞或前體細胞和/或其後代的施用。
本公開還提供了用於治療或預防具有大於70ml的升高的lvesv的心臟中的心力衰竭的方法,其包括向心臟施用間充質譜系幹細胞或前體細胞的群體和/或其後代和/或自其衍生的可溶性因子。
在一個實例中,lvesv大於80ml、大於90ml、大於100ml、大於100ml、大於110ml或大於120ml。在另一個實例中,lvesv大於80ml/m2、大於90ml/m2、大於100ml/m2、大於110ml/m2或大於120ml/m2。
在另一個實例中,本公開提供了用於降低具有大於70ml的lvesv的心臟中的升高的左心室收縮末期容積(lvesv)的方法,其包括向心臟施用間充質譜系幹細胞或前體細胞的群體和/或其後代和/或自其衍生的可溶性因子。
在一個實例中,lvesv大於80ml、大於90ml、大於100ml、大於100ml、大於110ml或大於120ml。在另一個實例中,lvesv大於80ml/m2、大於90ml/m2、大於100ml/m2、大於110ml/m2或大於120ml/m2。
在另一個實例中,與尚未施用間充質譜系幹細胞或前體細胞和/或其後代和/或自其衍生的可溶性因子的相同心臟相比,lvesv的降低是至少20%、至少15%、至少10%、至少5%、或至少2%。
在另一個實例中,在施用間充質譜系幹細胞或前體細胞和/或其後代和/或自其衍生的可溶性因子後約6個月、約12個月、約24個月、或約36個月時測量lvesv。
在一個實例中,通過基於導管的系統向心臟施用所述細胞和/或其後代和/或可溶性因子。在另外的實例中,在組織損傷位置處或附近向心肌施用細胞和/或其後代和/或可溶性因子。可以在鑑定需要治療的心肌的區域後進行細胞和/或其後代和/或可溶性因子的遞送。
在另外的實例中,通過經心內膜注射、冠狀動脈內輸注或經心外膜注射向心臟施用所述細胞和/或其後代和/或可溶性因子。
在另外的實例中,心臟的特徵進一步為具有小於約55%的左心室射血分數(lvef)。在另外的實例中,心臟的特徵進一步為具有小於或等於約35%的左心室射血分數(lvef)。在另一個實例中,心臟具有小於約35%、小於約30%、小於約25%或小於約20%的lvef。
在一個實例中,升高的lvesv是由於急性心肌梗死。在另外的實例中,升高的lvesv是由於慢性充血性心力衰竭。
在另外的實例中,在診斷心力衰竭後向心臟施用間充質譜系幹細胞或前體細胞和/或其後代和/或自其衍生的可溶性因子。在另一個實例中,在急性心肌梗死後向心臟施用間充質譜系幹細胞或前體細胞和/或其後代和/或自其衍生的可溶性因子。在另外的實例中,在診斷心力衰竭後約1-7天向心臟施用間充質譜系幹細胞或前體細胞和/或其後代和/或自其衍生的可溶性因子。在另外的實例中,在急性心肌梗死後約1-7天向心臟施用間充質譜系幹細胞或前體細胞和/或其後代和/或自其衍生的可溶性因子。在另外的實例中,在診斷心力衰竭後或在心肌梗死後約3-5天向心臟施用間充質譜系幹細胞或前體細胞和/或其後代和/或自其衍生的可溶性因子。
在另一個實例中,心臟具有約10%-35%、或約11–34%、約12–33%、約13–32%、約14–31%、約15–30%、約16–29%或約17–28%左心室的左心室梗死大小。
在一些實施方案中,本公開的方法還包括向心臟或向受試者施用針對stro-1+細胞富集的間充質譜系幹細胞或前體細胞的群體和/或其後代和/或自其衍生的可溶性因子。在另一個實例中,本公開的方法包括向心臟或向受試者施用針對stro-1亮細胞富集的間充質譜系幹細胞或前體細胞的群體和/或其後代和/或自其衍生的可溶性因子。
在另一個實例中,間充質譜系幹細胞或前體細胞的群體表達組織非特異性鹼性磷酸酶(tnap),和/或後代細胞和/或可溶性因子衍生自表達tnap的間充質譜系細胞。在另一個實例中,間充質譜系幹細胞或前體細胞的群體以至少0.1μg/106個細胞的量表達血管生成素-1(ang1)和/或後代細胞和/或可溶性因子衍生自以至少0.1μg/106個細胞的量表達ang1的間充質譜系前體細胞。在另一個實例中,間充質譜系幹細胞或前體細胞的群體以至少0.5μg/106個細胞的量表達ang1。在另一個實例中,間充質譜系幹細胞或前體細胞的群體以至少1μg/106個細胞的量表達ang1。在另一個實例中,間充質譜系幹細胞或前體細胞的群體以小於約0.05μg/106個細胞的量表達血管內皮生長因子(vegf)和/或後代細胞和/或可溶性因子衍生自以小於約0.05μg/106個細胞和/或後代細胞的量表達vegf的間充質譜系前體細胞。在另一個實例中,間充質譜系幹細胞或前體細胞的群體以小於約0.03μg/106個細胞的量表達vegf。在另一個實例中,間充質譜系幹細胞或前體細胞的群體以至少約2:1的比率表達ang1:vegf和/或後代細胞和/或可溶性因子衍生自以至少約2:1的比率表達ang1:vegf的間充質譜系幹細胞或前體細胞。在另一個實例中,間充質譜系幹細胞或前體細胞的群體以至少約10:1的比率表達ang1:vegf。在另一個實例中,間充質譜系幹細胞或前體細胞的群體以至少約20:1的比率表達ang1:vegf。在另一個實例中,間充質譜系幹細胞或前體細胞的群體以至少約30:1的比率表達ang1:vegf。
在一個實例中,以治療有效量向心臟或受試者施用間充質譜系幹細胞或前體細胞的群體和/或其後代。
在一個實例中,以多劑向心臟或受試者施用所述間充質譜系幹細胞或前體細胞的群體和/或其後代。在另外的實例中,本公開的方法包括施用1x106至8x108個細胞。在另一個實例中,本公開的方法包括施用約1.5x108個細胞。
在一個實例中,以組合物形式施用間充質譜系幹細胞或前體細胞和/或其後代細胞和/或自其衍生的可溶性因子,所述組合物包含間充質譜系幹細胞或前體細胞和/或其後代細胞和/或自其衍生的可溶性因子和藥學上可接受載體和/或賦形劑。在另外的實例中,在施用前和/或在獲得所述可溶性因子前已經培養擴增了間充質譜系幹細胞或前體細胞的群體和/或其後代。
本公開還提供了間充質譜系幹細胞或前體細胞的群體和/或其後代和/或自其衍生的可溶性因子或本文中所述的組合物用於治療具有大於70ml的升高的lvesv的受試者的心力衰竭的用途。
本公開還提供了間充質譜系幹細胞或前體細胞的群體和/或其後代和/或自其衍生的可溶性因子或本文中所述的組合物用於治療具有大於70ml的升高的lvesv的心臟的用途。
在根據本文中所述的任何用途的一個實例中,升高的lvesv是由於急性心肌梗死。在根據本文中所述的任何用途的另一個實例中,升高的lvesv是由於慢性充血性心力衰竭。
本公開還提供了間充質譜系幹細胞或前體細胞的群體和/或其後代和/或自其衍生的可溶性因子,其用在製造用於治療具有大於70ml的升高的左心室收縮末期容積(lvesv)的受試者的心力衰竭的藥物中。
本公開還提供了間充質譜系幹細胞或前體細胞的群體和/或其後代和/或自其衍生的可溶性因子,其用在製造用於治療具有大於70ml的升高的左心室收縮末期容積(lvesv)的心臟的藥物中。
本公開還提供了間充質譜系幹細胞或前體細胞的群體和/或其後代和/或自其衍生的可溶性因子或本文中所述的組合物,其用於治療具有大於70ml的升高的lvesv的受試者的心力衰竭。
本公開還提供了間充質譜系幹細胞或前體細胞的群體和/或其後代和/或自其衍生的可溶性因子或本文中所述的組合物,其用於治療具有大於70ml的升高的左心室收縮末期容積(lvesv)的心臟。
在另一個實例中,本公開提供了間充質譜系幹細胞或前體細胞的群體和/或其後代和/或自其衍生的可溶性因子或本文中所述的組合物用於降低具有大於70ml的升高的lvesv的心臟中的左心室收縮末期容積(lvesv)的用途。
在另一個實例中,本公開提供了間充質譜系幹細胞或前體細胞的群體和/或其後代和/或自其衍生的可溶性因子或本文中所述的組合物,用於降低具有大於70ml的升高的lvesv的心臟中的左心室收縮末期容積(lvesv)。
在根據本文中所述的任何群體或用途的一個實例中,lvesv大於80ml、大於90ml、大於100ml、大於110ml或大於120ml。在另一個實例中,lvesv大於80ml/m2、大於90ml/m2、大於100ml/m2、大於110ml/m2、或大於120ml/m2。
在根據本文中所述的任何方法或用途的另外的實例中,間充質譜系前體細胞的群體和/或其後代是分離的或純化的。
在另外的實例中,間充質譜系幹細胞或前體細胞的群體和/或其後代衍生自供體受試者。供體受試者可以是接受細胞、和/或其後代和/或自其衍生的可溶性因子施用的相同受試者,在該情況下細胞是自體的。在另一個實例中,供體受試者是接受細胞、和/或其後代和/或自其衍生的可溶性因子施用的不同受試者,在該情況中細胞是同種異體的。
在另外的實例中,受試者具有小於約55%的左心室射血分數(lvef)。在根據本文中所述的任何用途的另一個實例中,受試者具有小於或等於約35%的lvef。在另一個實例中,受試者具有小於約35%、小於約30%、小於約25%或小於約20%的lvef。
在根據本文中所述的任何用途的另一個實例中,心臟具有約5%-30%,或約10%-20%的左心室梗死大小。在根據本文中所述的任何用途的另一個實例中,受試者具有約5%-30%,或約10%-20%的左心室梗死大小。
在另一個實例中,本公開提供了間充質幹細胞或譜系前體細胞的群體和/或其後代和/或自其衍生的可溶性因子,其用在製造用於降低具有大於70ml的升高的lvesv的心臟中的左心室收縮末期容積(lvesv)的藥物中。
本公開還提供了試劑盒,其包括間充質譜系幹細胞或前體細胞的群體和/或其後代和/或自其衍生的可溶性因子或本文中所述的組合物和用於施用所述細胞、和/或其後代和/或可溶性因子的遞送裝置。在一個實例中,遞送裝置是導管。
在另一個實例中,根據本公開的受試者是哺乳動物。在另外的實例中,受試者是人,包括青少年或小兒。在具體的實例中,受試者大於或等於18歲。
在另外的實例中,受試者在施用間充質譜系幹細胞或前體細胞的群體和/或其後代和/或自其衍生的可溶性因子前12個月內已經具有心力衰竭事件。
在另外的實例中,受試者分類為紐約心臟學會(nyha)ii、iii或iv類。ii類定義為輕度,其中受試者經歷中等身體活動期間疲勞和呼吸短促。ii類定義為中等,其中患者即使在輕度身體活動期間經歷呼吸短促。iv類或末期定位為嚴重,其中患者即使在休息時也是精疲力竭的。
在另外的實例中,受試者具有降低的基線6分鐘步行測試(6mwt),意味著受試者在6分鐘時段內穿行的距離相對於非心力衰竭受試者降低。
在另一個實例中,受試者具有大於150ml左室舒張末期容積(lveds)。在另一個實例中,受試者具有大於170ml的lvesv。
在另一個實例中,還對受試者同時施用常規的心力衰竭藥物。在另外的實例中,心力衰竭藥物包括但不限於下列一種或多種:β阻斷劑、ace抑制劑或血管緊張素受體阻斷劑。
在另一個實例中,受試者具有較高的主要不良心臟事件(mace)率。在另外的實例中,受試者在36個月內具有>50%心力衰竭-mace(hf-mace)率。在另一個實例中,受試者在36個月內具有>60%hf-mace率、或>65%hf-mace率、或>70%hf-mace率。
附圖說明
圖1顯示基於左心室(lv)容積在心臟重塑中mpc的劑量依賴性效果。
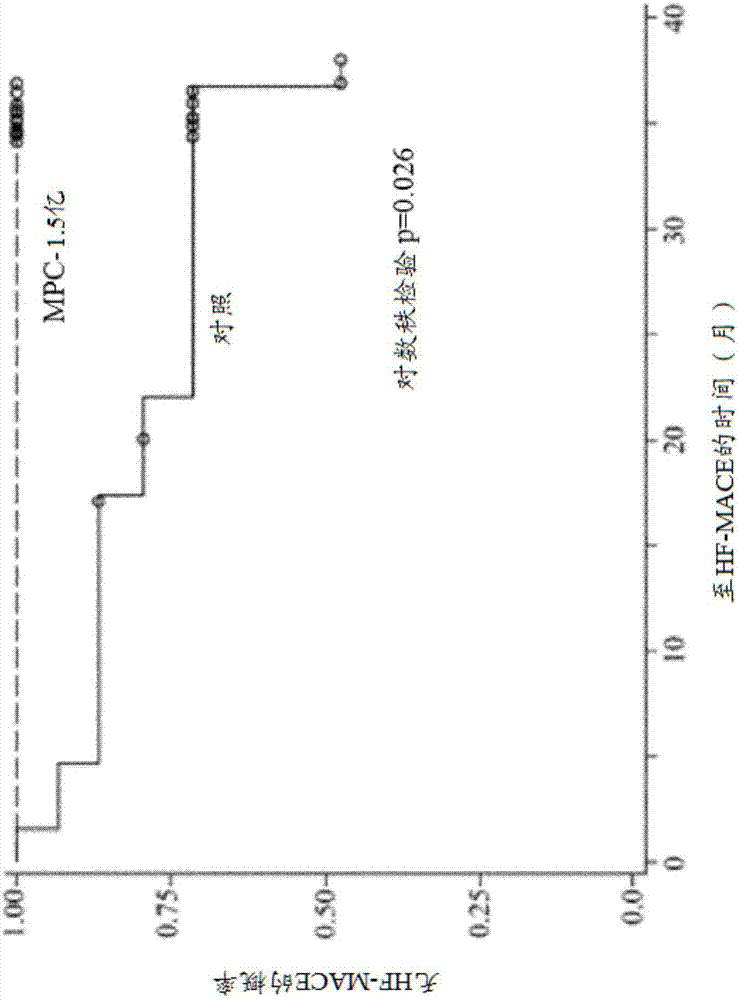
圖2顯示用1.5億個mpc處理後36個月通過kaplan-meier曲線得到的hf-mac。
圖3-1顯示根據小於或等於100ml或大於100ml的lvesv分層的施用了安慰劑(對照)和間充質前體細胞(mpc)的受試者(1.5億個細胞)中的基線左心室收縮末期容積(lvesv)值。
圖3-2顯示根據小於或等於100ml或大於100ml的lvesv分層的施用了安慰劑(對照)和mpc的受試者(1.5億個細胞)中的6個月時lvesv值的變化。
圖4-1顯示根據小於或等於100ml或大於100ml的lvesv分層的施用了安慰劑(對照)和mpc的受試者(1.5億個細胞)中的基線左心室收縮末期容積(lvedv)值。
圖4-2顯示根據小於或等於100ml或大於100ml的lvesv分層的施用了安慰劑(對照)和mpc的受試者(1.5億個細胞)中的6個月時lvedv值的變化。
圖5-1顯示根據小於或等於100ml或大於100ml的lvesv分層的施用了安慰劑(對照)和mpc的受試者(1.5億個細胞)中的基線左心室射血分數(lvef)值。
圖5-2顯示根據小於或等於100ml或大於100ml的lvesv分層的施用了安慰劑(對照)和mpc的受試者(1.5億個細胞)中的6個月時lvef值的變化。
圖6顯示根據大於70ml的lvesv分層的施用了安慰劑(對照)和mpc的受試者(1.5億個細胞)中的6個月時lvesv值的變化。
圖7顯示根據大於80ml的lvesv分層的施用了安慰劑(對照)和mpc的受試者(1.5億個細胞)中的6個月時lvesv值的變化。
圖8顯示根據大於90ml的lvesv分層的施用了安慰劑(對照)和mpc的受試者(1.5億個細胞)中的6個月時lvesv值的變化。
圖9顯示根據大於100ml的lvesv分層的施用了安慰劑(對照)和mpc的受試者(1.5億個細胞)中的6個月時lvesv值的變化。
圖10顯示根據大於110ml的lvesv分層的施用了安慰劑(對照)和mpc的受試者(1.5億個細胞)中的6個月時lvesv值的變化。
圖11顯示根據大於120ml的lvesv分層的施用了安慰劑(對照)和mpc的受試者(1.5億個細胞)中的6個月時lvesv值的變化。
圖12顯示具有lvesv>100ml的患者中治療後36個月時mf-macekaplan-meier曲線。
具體實施方式
在整個本說明書中,除非另有明確說明或上下文另有要求,否則提及單個步驟、物質組成、步驟組或物質組成組應當理解為涵蓋那些步驟、物質組成、步驟組或物質組成組的一個和多個(即一個或多個)。
本領域技術人員將理解,除了具體描述的那些之外,本文所述的公開內容易於進行變化和修改。應當理解,本公開包括所有這些變化和修改。本公開還包括在本說明書中單獨或共同地引用或指出的所有步驟、特徵、組合物和化合物,以及任何和所有組合或所述步驟或特徵中的任何兩種或更多種。
本公開的範圍不限於本文所述的具體實施方案,所述具體實施方案僅意圖為了舉例的目的。如本文所述,功能上等同的產品、組合物和方法顯然在本公開的範圍內。
除非另有明確說明,否則本文公開的任何實例應當視為作必要的修正適用於任何其它實例。
除非另有特別限定,本文使用的所有技術和科學術語應被視為具有與本領域(例如,在細胞培養、分子遺傳學、幹細胞分化、免疫學、免疫組織化學、蛋白質化學和生物化學中)普通技術人員通常理解的相同的含義。
除非另有說明,本公開中使用的外科技術是本領域技術人員熟知的標準程序。
獲得和富集間充質譜系幹細胞或前體細胞群體的方法是本領域已知的。例如,可以通過使用流式細胞術和細胞分選程序,基於使用在間充質譜系幹細胞或前體細胞上表達的細胞表面標誌物來獲得間充質譜系幹細胞或前體細胞的富集群體。
本文引用或提到的所有文件以及本文引用的文件中引用或提到的所有文件,連同本文提及的任何產品的任何製造商的說明書、說明、產品規格和產品表,或通過引用併入本文的任何文件在此通過引用完整併入本文。
選擇的定義
術語「和/或」,例如「x和/或y」應理解為「x和y」或「x或y」,並且應當視為提供對這兩種含義或任一含義的明確支持。
如本文所用,除非另有說明,術語「約」是指指定值的+/-10%,更優選+/-5%。
在整個說明書中,詞語「包括/包含」或變型將理解為暗示包括所述元素、整數或步驟,或元素、整數或步驟的組,但是不排除任何其它元素、整數或步驟,或元素、整數或步驟的組。
如本文中所用,單數形式「一個」、「一種」和「該/所述」包括單數和複數提及物,除非上下文另有指示。
如本文中所用,術語「心力衰竭」可以與術語「充血性心力衰竭(chf)」互換使用,並且是指心臟由於例如心肌功能失常、心肌衰弱(稱為「心肌病」)和其它心肌相關原因而不能將足夠的血液泵送到身體的其它器官的狀況。除了其它效應外,充血性心力衰竭的特徵在於左心室(lv)室擴張、lv收縮力降低和循環兒茶酚胺水平升高。在另一個實例中,由於缺血和其它再灌注以及其它非缺血因素而發生心力衰竭。心力衰竭包括但不限於單獨或共同的以下症狀或體徵:心臟再灌注損傷、補償性肥大、人末期心力衰竭、高血壓性心肌病、左心室高血壓、左心室或右心室擴張、左心室或右心室衰竭、適應不良性肥大,心肌結構紊亂(凋亡和心肌細胞的喪失)和心肌功能障礙(收縮和/或鬆弛的損失)和壓力超負荷的心臟。
所謂「分離的」或「純化的」是指已經與其自然環境的至少一些成分分離的細胞。該術語包括細胞與其天然環境的粗略的物理分離(例如從供體去除)。術語「分離的」包括通過例如解離來改變細胞與其直接相鄰的細胞的關係。術語「分離的」不是指組織切片中的細胞。當用於指細胞群體時,術語「分離的」包括由本公開的分離的細胞的增殖引起的細胞群。
如本文中所用,術語「左心室高血壓(lvh)」是其中心肌通過變大響應增加的循環阻力的狀況。然而,隨著時間的推移,肥大的心肌的纖維變厚並縮短,因此不太能鬆弛。高血壓使心肌更努力運行。所產生的肥大是心臟的肌肉纖維增厚或縮短的產物。在這些狀況下,心臟鬆弛和經歷正常的收縮和鬆弛周期變得更加困難。膠原中出現心肌變化,導致僵硬度增加。此過程的結果是不太能滿足正常循環的輸出需求的心臟。
如本文中所用,術語「左心室擴張」是指左心室擴大,其可以增加從心室噴射的血液的體積,暫時改善心輸出量。然而,心室的尺寸增加也導致了招致的血液左心室容積百分比(稱為射血分數)降低,並具有顯著的生理學意義。左心室擴張是心肌梗死後心臟功能障礙和充血性心力衰竭的公認前兆和體徵。類似地,右心室擴張是指右心室擴大和相關的體徵或病症。
如本文中所用,術語「左心室衰竭」是指心臟左側不能有效泵送血的病症。這導致血液進入肺的逆流、壓力和/或充血。指示左心室衰竭的體徵包括橫向位移心尖搏動。可以聽到奔馬律作為增加血流量或增加心臟內壓力的標誌。
如本文所用,術語「心肌病」是指心臟肌肉(心肌)變得發炎和擴大的病狀。幾種不同類型的心肌病在本領域中是已知的,包括其中心肌被拉伸並變薄的擴張型心肌病,其中心肌細胞擴大並導致心臟壁增厚的肥大性心肌病,以及其中心臟由於異常組織(例如疤痕組織)變硬和僵硬的限制型心肌病。
如本文中所用,術語「心肌梗死」也被理解為指心臟病發作。當血液停止正常流動到心臟的一部分,並且心臟肌肉由於其未接受足夠的氧氣而受損傷時,發生心臟病發作。這可以在將血液供應給心臟的冠狀動脈之一發生阻塞時發生。
如本文中所用,術語「左心室收縮末期容積」(lvesv)是指在收縮結束,或心縮期,和填充(filing)開始或心舒期的左心室中的血液容積。它指心臟周期中的任何點時的心室中的最低血液容積。男性的正常值的範圍通常為22-58ml,對於女性為19-49ml。作解釋,lvesv值在本文中是指基線lvesv值,即在向受試者施用間充質譜系前體細胞或幹細胞和/或其後代和/或自其衍生的可溶性因子前確定的lvesv值。
本領域技術人員將理解術語「升高的lvesv」。通常,應理解為意指高於對於男性或女性的正常lvesv範圍的數值。在一個實例中,升高的lvesv將理解為意指大於70ml的值。在另一個實例中,它理解為意指大於100ml的lvesv值。
如本文中所用,術語「左心室收縮末期容積指數」(lvesvi)是指指數化的左心室收縮末期容積。該值通常表示為ml/m2。術語lvesv和lvesvi可以在本文中互換使用。
如本文中所用,術語「左心室射血分數」(lvef)是指心臟每次收縮泵送多好。射血分數(ef)通常以百分比表示,即每次收縮時離開心臟的血液百分比。正常lvef範圍為55-70%。65%的lvef例如意味著每次心跳泵送出來左心室中的血液總量的65%。由於左心室是心臟的主要泵送室,ef通常僅在左心室(lv)中測量。55%以上的lvef認為是正常的。50%以下的lvef認為是降低的。專家在其關於50%和55%之間的ef的意見上有變化,並且有些認為這是一個邊界範圍。
如本文中所用,術語「左心室舒張末期容積」(lvedv)是指在收縮結束,或心縮期,和填充開始或心舒期的右心室中的血液容積。它指心臟周期中的任何點時的心室中的最低血液容積。通常,正常健康受試者的lvedv是約120ml。作解釋,lvedv值在本文中是指基線lvedv值,即在向受試者施用間充質譜系前體細胞和/或其後代和/或自其衍生的可溶性因子前確定的lvedv值。
如本文所用,術語「治療(treating)」、「治療(treat)」或「治療(treatment)」包括施用間充質譜系幹細胞或前體細胞的群體和/或其後代和/或自其衍生的可溶性因子,從而減少或消除心力衰竭至少一種症狀。在一個具體實例中,相比於基線值(即施用間充質譜系幹細胞或前體細胞的群體和/或其後代和/或自其衍生的可溶性因子前),治療將lvesv值降低至少5%、至少10%、至少15%、至少20%、至少25%、至少30%、至少35%、至少40%、至少45%、或至少50%。
如本文所用,術語「預防(prevent)」或「預防(preventing)」包括施用間充質譜系幹細胞或前體細胞的群體和/或其後代和/或自其衍生的可溶性因子,從而停止或阻礙心力衰竭的至少一種症狀的發展。
如本文所用,術語「受試者」是指哺乳動物,包括但不限於鼠、大鼠、猿、人、家畜和農場動物。
間充質譜系前體細胞
如本文所用,術語「間充質譜系前體細胞或幹細胞」是指具有自我更新的能力,同時維持多能性和分化成間充質來源(例如成骨細胞、軟骨細胞、脂肪細胞、基質細胞、成纖維細胞和肌腱),或非中胚層來源(例如肝細胞、神經細胞和上皮細胞)的多種細胞類型的能力的未分化的多能細胞。為了避免疑問,「間充質譜系前體細胞」是指可以分化成間質細胞如骨、軟骨、肌肉和脂肪細胞以及纖維結締組織的細胞。
術語「間充質譜系前體細胞或幹細胞」包括親本細胞及其未分化後代二者。該術語還包括間充質前體細胞、多能基質細胞、間充質幹細胞(msc)、血管周圍間充質前體細胞及其未分化後代。
間充質譜系前體細胞或幹細胞可以是自體的、異種的、同系的或同基因的。自體細胞從將接受它們再植入的同一個體分離。從相同物種的供體分離同種異體細胞。從另一物種的供體分離異種細胞。從遺傳相同的生物體(如雙胞胎、克隆、或高度近交的研究動物模型)分離同系的或同基因的細胞。
間充質譜系前體細胞或幹細胞主要駐留於骨髓中,但也顯示存在於多種宿主組織中,包括例如臍帶血和臍帶、成人外周血、脂肪組織、小梁骨和牙髓。
在一個實例中,間充質譜系前體細胞是stro-1+間充質前體細胞(mpc)。如本文所用,短語「stro-1+多能細胞」應當視為指能夠形成多能細胞集落的stro-1+和/或tnap+祖細胞。
stro-1+多能細胞是在骨髓、血液、牙髓細胞、脂肪組織、皮膚、脾臟、胰腺、腦、腎、肝臟、心臟、視網膜、腦、毛囊、腸、肺、淋巴結、胸腺、骨、韌帶、肌腱、骨骼肌、真皮和骨膜中發現;並且能夠分化成種系,如中胚層和/或內胚層和/或外胚層的細胞。因此,stro-1+多能細胞能夠分化成大量的細胞類型,包括但不限於脂肪組織、骨組織、軟骨組織、彈性組織、肌肉組織和纖維結締組織。這些細胞進入的具體譜系定向和分化途逕取決於機構影響和/或內源性生物活性因子,如生長因子、細胞因子和/或由宿主組織建立的局部微環境條件的各種影響。
間充質譜系前體細胞或幹細胞可以從宿主組織中分離,並通過選擇stro-1+細胞進行富集。例如,來自受試者的骨髓抽吸物可以用針對stro-1或tnap的抗體進一步處理,以使得能夠選擇間充質譜系前體細胞或幹細胞。在一個實例中,間充質譜系前體細胞或幹細胞可以通過使用(simmons&torok-storb,1991)中描述的stro-1抗體來富集。
術語「富集」或其變型在本文中用於描述當與未處理的細胞群體(例如,其天然環境中的細胞)相比,一種特定細胞類型的比例或多種特定細胞類型的比例增加的細胞群體。在一個實例中,針對stro-1+細胞富集的群體包含至少約0.1%或0.5%或1%或2%或5%或10%或15%或20%或25%或30%或50%或75%stro-1+細胞。在這方面,術語「針對stro-1+細胞富集的細胞群體」應當視為提供對術語「包含x%stro-1+細胞的細胞群體」的明確支持,其中x%是如本文所述的百分比。在一些實例中,stro-1+細胞可以形成克隆形成集落,例如,cfu-f(成纖維細胞)或其子集(例如50%或60%或70%或70%或90%或95%)可以具有這種活性。
在一個實例中,以可選擇形式從包含stro-1+細胞的細胞製備物富集細胞群體。在這方面,術語「可選擇形式」將理解為意味著細胞表達允許stro-1+細胞選擇的標誌物(例如,細胞表面標誌物)。標誌物可以是stro-1,但不需要如此。例如,如本文中描述和/或示例,表達stro-2和/或stro-3(tnap)和/或stro-4和/或vcam-1和/或cd146和/或3g5的細胞(例如間充質前體細胞)也表達stro-1(並且可以是stro-1亮)。因此,細胞是stro-1+的指示並不意味著僅通過stro-1表達來選擇細胞。在一個實例中,基於至少stro-3表達來選擇細胞,例如它們是stro-3+(tnap+)。
提及細胞或其群體的選擇不一定需要從特定組織來源進行選擇。如本文所述,可以從極其多種來源中選擇或分離或富集stro-1+細胞。也就是說,在一些實例中,這些術語提供了對從包含stro-1+細胞(例如間充質前體細胞)的組織或血管化組織或包含周細胞(例如,stro-1+周細胞)的組織或任何一種或多種的本文所述的組織選擇的支持。
在一個實例中,本公開中使用的細胞表達單獨或共同選自由以下組成的組的一種或多種標誌物:tnap+、vcam-1+、thy-1+、stro-2+、stro-4+(hsp-90β)、cd45+、cd146+、3g5+或其任何組合。
「單獨地」是指本公開單獨涵蓋所述標誌物或標誌物組,並且儘管單獨的標誌物或標誌物組可以不在本文中單獨列出,但是所附權利要求書可以彼此分開且可分地定義此類標誌物或標誌物組。
「共同地」是指本公開涵蓋所述標誌物或標誌物組的任何數量或組合,並且儘管標誌物或標誌物組的這種數目或組合可能在本文中沒有明確列出,但是所附權利要求書可以與標誌物或標誌物組的任何其它組合分開且可分地定義此類組合或亞組合。
在一個實例中,stro-1+細胞是stro-1亮(同義詞stro-1bri)。在另一個實例中,相對於stro-1暗或stro-1中間細胞優先富集stro-1bri細胞。
在另一個實例中,stro-1bri細胞另外是tnap+、vcam-1+、thy-1+、stro-2+、stro-4+(hsp-90β)和/或cd146+中的一種或多種。例如,細胞針對一種或多種前述標誌物進行選擇和/或顯示以表達一種或多種前述標誌物。在這方面,顯示表達標誌物的細胞不需要明確測試,而是可以測試先前富集或分離的細胞,隨後使用,分離或富集的細胞可以合理地假定也表達相同的標誌物。
在一個實例中,間充質前體細胞(mpc)是如wo2004/85630中定義的血管周圍間充質前體細胞,其特徵在於存在血管周圍標誌物3g5。例如,mpc表達血管周圍細胞的標誌物,例如細胞是stro-1+或stro-1bri和/或3g5+。在一個實例中,細胞是或先前是或是從血管化組織或器官或其部分分離的細胞或者是該細胞的後代。
對於給定的標誌物稱為「陽性」的細胞可以根據標誌物存在於細胞表面上的程度而表達低(lo或暗)或高(亮,bri)水平的所述標誌物的,其中該術語與細胞分選過程中使用的螢光強度或其它標誌物有關。在被分類的特定細胞群體上使用的標誌物的上下文中將理解lo(或暗或暗淡)和bri的區別。對於給定的標誌物稱為「陰性」的細胞不一定完全不存在於該細胞中。該術語意味著標誌物由該細胞以相對非常低的水平表達,並且它在可檢測標記時產生非常低的信號或在背景水平,例如使用同種型對照抗體檢測的水平以上檢測不到。
如本文所用,術語「亮」或「bri」是指在被可檢測地標記時產生相對較高信號的細胞表面上的標誌物。雖然不希望被理論限制,但是提出「亮」細胞比樣品中的其它細胞表達更多的靶標誌物蛋白(例如由stro-1識別的抗原)。例如,如通過螢光激活細胞分選(facs)分析確定,當用fitc綴合的stro-1抗體標記時,與非亮細胞(stro-1暗淡/暗)相比,stro-1bri細胞產生更大的螢光信號。在一個實例中,「亮」細胞構成起始樣品中包含的最亮標記的骨髓單核細胞的至少約0.1%。在其它實例中,「亮」細胞構成起始樣品中包含的最明亮標記的骨髓單核細胞的至少約0.5%、至少約1%、至少約1.5%或至少約2%。在一個實例中,stro-1亮細胞相對於「背景」,即stro-1-的細胞,具有stro-1表面表達的高2個對數量級的表達。相比之下,stro-1暗淡和/或stro-1中間細胞比「背景」具有stro-1表面表達的高小於2個對數量級的表達,通常為約1個對數或更小。
如本文所用,術語「tnap」意在涵蓋組織非特異性鹼性磷酸酶的所有同種型。例如,該術語包括肝同種型(lap)、骨同種型(bap)和腎同種型(kap)。在一個實例中,tnap是bap。在一個實例中,如本文所用,tnap是指可以結合stro-3抗體的分子,所述stro-3抗體由在2005年12月19日根據布達佩斯條約的規定在保藏登錄號pta-7282下保藏於atcc的雜交瘤細胞系產生。
此外,在一個實例中,stro-1+細胞能夠產生克隆形成cfu-f。
在一個實例中,相當大比例的stro-1+細胞能夠分化為至少兩個不同的種系。可以定向stro-1+細胞的譜系的非限制性實例包括骨前體細胞;肝細胞祖細胞,其對於膽管上皮細胞和肝細胞是多能性的;神經受限細胞,其可以產生進展為少突膠質細胞和星形膠質細胞的神經膠質細胞前體;進展為神經元的神經元前體;心肌和心肌細胞的前體、葡萄糖反應性胰島素分泌胰腺β細胞系。其它譜系包括但不限於成牙本質細胞、產生牙本質的細胞和軟骨細胞,以及以下的前體細胞:視網膜色素上皮細胞、成纖維細胞、皮膚細胞如角質形成細胞、樹突狀細胞、毛囊細胞、腎管上皮細胞、平滑和骨骼肌細胞、睪丸祖細胞、血管內皮細胞、腱、韌帶、軟骨、脂肪細胞、成纖維細胞、骨髓基質、心肌、平滑肌、骨骼肌、周細胞、血管、上皮、膠質細胞、神經元、星形膠質細胞和少突膠質細胞。
在本公開的一個實例中,間充質譜系前體細胞或幹細胞是間充質幹細胞(msc)。msc可以是同質的組合物,或者可以是富含msc的混合細胞群體。可以通過培養貼壁的骨髓或骨膜細胞獲得同質msc組合物,並且可以通過用獨特的單克隆抗體鑑定的特異性細胞表面標誌物鑑定msc。用於獲得富集msc的細胞群的方法描述於例如美國專利no.5,486,359中。msc的替代來源包括但不限於血液、皮膚、臍帶血、肌肉、脂肪、骨骼和軟骨膜。
在另一個實例中,間充質譜系前體細胞或幹細胞是cd29+、cd54+、cd73+、cd90+、cd102+、cd105+、cd106+、cd166+、mhc1+msc(例如remestemcel-l)。
分離或富集的間充質譜系前體細胞或幹細胞可以通過培養進行體外擴增。分離或富集間充質譜系前體細胞或幹細胞可以冷凍保存,解凍,隨後通過培養進行體外擴增。
在一個實例中,將分離或富集的間充質譜系前體細胞或幹細胞以50,000個活細胞/cm2接種在培養基(無血清或血清補充),例如補充有5%胎牛血清(fbs)和穀氨醯胺的α最小必需培養基(αmem)中,並使其在37℃,20%o2下貼壁到培養容器過夜。隨後根據需要更換和/或改變培養基,並將細胞在37℃,5%o2下再培養68至72小時。
如本領域技術人員將理解的,培養的間充質譜系前體細胞或幹細胞與體內細胞表型不同。例如,在一個實施方案中,它們表達一種或多種以下標誌物:cd44、ng2、dc146和cd140b。培養的間充質譜系前體細胞或幹細胞在與體內細胞在生物學上不同,與體內大部分非循環(靜止)細胞相比,具有較高的增殖速率。
也可以在向受試者施用前冷凍保存間充質譜系前體細胞或幹細胞。
細胞的修飾
在一個實例中,本公開的間充質譜系前體細胞或幹細胞可以經遺傳修飾或遺傳未修飾,並且以至少0.1μg/106個細胞的量表達ang1。然而,在多個實例中,設想本公開的間充質幹細胞或前體細胞可以以至少0.2μg/106個細胞、0.3μg/106個細胞、0.4μg/106個細胞、0.5μg/106個細胞、0.6μg/106個細胞、0.7μg/106個細胞、0.8μg/106個細胞、0.9μg/106個細胞、1μg/106個細胞、1.1μg/106個細胞、1.2μg/106個細胞、1.3μg/106個細胞、1.4μg/106個細胞、1.5μg/106個細胞的量表達ang1。
在一個實例中,本公開的間充質譜系前體細胞或幹細胞是遺傳未修飾的,並且以至少0.1μg/106個細胞的量表達ang1。然而,在本實例的多個實施方案中,設想間充質譜系前體細胞或幹細胞可以以至少0.2μg/106個細胞、0.3μg/106個細胞、0.4μg/106個細胞、0.5μg/106個細胞、0.6μg/106個細胞、0.7μg/106個細胞、0.8μg/106個細胞、0.9μg/106個細胞、1μg/106個細胞、1.1μg/106個細胞、1.2μg/106個細胞、1.3μg/106個細胞、1.4μg/106個細胞、1.5μg/106個細胞的量表達ang1。
在另一個方面,本公開的間充質譜系前體細胞或幹細胞以小於約0.05μg/106個細胞的量表達vegf。然而,在多個實施方案中,設想本公開的間充質譜系幹細胞或前體細胞可以以小於約0.05μg/106個細胞、0.04μg/106個細胞、0.03μg/106個細胞、0.02μg/106個細胞、0.01μg/106個細胞、0.009μg/106個細胞、0.008μg/106個細胞、0.007μg/106個細胞、0.006μg/106個細胞、0.005μg/106個細胞、0.004μg/106個細胞、0.003μg/106個細胞、0.002μg/106個細胞、0.001μg/106個細胞的量表達vegf。
在一個實例中,本公開的間充質譜系前體細胞或幹細胞是遺傳未修飾的,並且以小於約0.05μg/106個細胞的量表達vegf。然而,在本實例的多個實施方案中,設想本公開的間充質譜系前體細胞或幹細胞可以以小於約0.05μg/106個細胞、0.04μg/106個細胞、0.03μg/106個細胞、0.02μg/106個細胞、0.01μg/106個細胞、0.009μg/106個細胞、0.008μg/106個細胞、0.007μg/106個細胞、0.006μg/106個細胞、0.005μg/106個細胞、0.004μg/106個細胞、0.003μg/106個細胞、0.002μg/106個細胞、0.001μ/106個細胞的量表達vegf。
間充質譜系前體細胞或幹細胞的組合物或培養物中表達的細胞ang1和/或vegf的量可以通過本領域技術人員已知的方法測定。此類方法包括但不限於定量測定,如定量elisa測定,例如或螢光連接免疫吸附測定(flisa)、western印跡、競爭測定、放射免疫測定、側流免疫測定、穿流免疫測定、電化學發光測定、基於濁度的測定(nephelometric-basedassay)、基於濁度的測定(turbidometric-basedassay)、基於螢光激活細胞分選(facs)的測定(用於檢測培養間充質譜系前體細胞或幹細胞的培養基中的ang-1或vegf)、表面等離子共振(spr或biacore)。
然而,應當理解,本公開的範圍不限於用於確定在本公開的間充質譜系前體細胞或幹細胞中表達的ang1或vegf的量或水平的任何具體方法。
在一個實例中,通過elisa測定來確定由間充質譜系前體細胞或幹細胞的組合物或培養物表達的ang1或vegf的水平。在此類測定中,將來自間充質譜系前體細胞或幹細胞的培養物的細胞裂解物添加到elisa板的孔中。該孔可以用針對ang1或vegf的一抗(單克隆抗體或多克隆抗體)包被。然後,將孔清洗,然後與針對一抗的二抗(單克隆抗體或多克隆抗體)接觸。例如,將二抗與適當的酶綴合,如辣根過氧化物酶。可以孵育孔,然後在孵育期後清洗。然後,使孔與合適於與二抗綴合的酶的底物接觸,所述底物如一種或多種色原體。可以使用的色原體包括但不限於過氧化氫和四甲基聯苯胺。在添加底物之後,將孔孵育適當的時間段。孵育完成後,向孔中添加「停止」溶液,以便停止酶與底物的反應。然後測量樣品的光密度(od)。樣品的光密度與含有已知量的ang1或vegf的樣品的光密度相關,以確定由正在測試的間充質譜系前體細胞或幹細胞的培養物表達的ang1或vegf的量。
在另一個方面,本公開的間充質譜系前體細胞或幹細胞以至少約2:1的比率表達ang1:vegf。然而,在多個實施方案中,設想本公開的間充質譜系前體細胞或幹細胞可以以至少約10:1、15:1、20:1、21:1、22:1、23:1、24:1、25:1、26:1、27:1、28:1、29:1、30:1、31:1、32:1的比率表達ang1:vegf。
在一個實例中,本公開的間充質譜系前體細胞或幹細胞是遺傳未修飾的,並且以至少約2:1的比率表達ang1:vegf。然而,在多個實施方案中,設想本公開的間充質譜系前體細胞或幹細胞可以以至少約10:1、15:1、20:1、21:1、22:1、23:1、24:1、25:1、26:1、27:1、28:1、29:1、30:1、31:1、32:1的比率表達ang1:vegf。
用於測定ang1:vegf表達比率的方法對於本領域技術人員將是顯而易見的。在確定ang1和vegf表達比率的方法的實例中,通過如上所述的定量elisa來定量ang1和vegf表達水平。在此類實例中,在定量ang1和vegf的水平之後,基於ang1和vegf的定量水平的比率可以表示為:(ang1的水平/vegf的水平)=ang1:vegf比率。
本公開的間充質譜系前體細胞或幹細胞可以以如下的方式改變,使得在施用時,細胞的裂解被抑制。抗原的改變可以誘導免疫學的非響應性或耐受性,從而防止最終造成正常免疫應答中的外源細胞排斥的免疫應答的效應階段(例如細胞毒性t細胞產生,抗體產生等)的誘導。可以改變以實現該目標的抗原包括例如mhci類抗原、mhcii類抗原、lfa-3和icam-1。
在另一個實例中,間充質譜系前體細胞或幹細胞可以經遺傳修飾以表達供應給接受移植的受試者的基因產物。可以通過遺傳修飾的間充質譜系前體細胞遞送到受試者的基因產物的實例包括可以預防未來心臟病症的基因產物,例如促進血管侵入心肌的生長因子(例如血管內皮生長因子(vegf)、成纖維細胞生長因子(fgf)、轉化生長因子β(tgf-β)和血管緊張素)。
間充質譜系前體細胞或幹細胞也可以經遺傳修飾以表達對條紋骨骼肌細胞的分化和/或維持重要的蛋白質。示例性蛋白質包括生長因子(tgf-β,胰島素樣生長因子1(igf-1),fgf),肌原性因子(例如,myod、成肌素、肌原性因子5(myf5)、肌原性調節因子(mrf)、轉錄因子(例如gata-4)、細胞因子(例如心肌營養蛋白-1)、神經調節蛋白家族的成員(例如神經調節蛋白1、2和3)和同源盒基因(例如csx、tinman和nkx家族)。
心力衰竭
當心臟不能充分泵送以維持血液流動來滿足身體的需要時,心力衰竭發生。心力衰竭的一個原因是心肌梗死(mi)。當血液停止正常流動到心臟的一部分時,發生mi。缺乏供血導致稱為梗死或梗死形成的局部心肌壞死區域。梗死的心臟不能充分泵送以維持血液流動來滿足身體的需要,導致心力衰竭。在mi後,啟動一系列補償機制,用於緩解心輸出量的下降,並協助維持足夠的血壓來灌注重要的器官。因此,心力衰竭患者可能長時間不進展。然而,補償機制最終無法補償受損心臟,導致心輸出量逐漸下降,稱為「進行性心力衰竭」。
通過整合呈現疾病和身體檢查的歷史與心電圖發現和心臟標誌物產生mi的診斷。可以進行冠狀動脈血管造影,其允許在心臟血管上顯現狹窄或阻塞。根據2000年修訂的who標準(alpertjs,thygesenk,antmane,bassandjp.(2000)."myocardialinfarctionredefined--aconsensusdocumentofthejointeuropeansocietyofcardiology/americancollegeofcardiologycommitteefortheredefinitionofmyocardialinfarction".jamcollcardiol36(3):959–69),心臟肌鈣蛋白升高伴有典型症狀、病理性q波、st升高或抑制或冠狀動脈幹預是mi的診斷。
70多年來,12導聯心電圖(ecg)仍然是確定mi的存在和位置的標準。它是普遍可用的、非侵入的、便宜的且可易於重複的。通過計算機模擬設計的定量selvesterqrs評分系統(selvesterrh等人(1985)archinternmed145(10):1877-1881)利用ecg上的信息來估計mi大小。selvester評分系統是基於標準12導聯心電圖中q-和r-波持續時間和r/q和r/s振幅比的觀察的50個標準的31點qrs評分系統。用於確定梗死大小的方法,包括但不限於qrs評分是本領域技術人員熟知的。
還可以測量心臟標誌物以確定mi的發生。此類標誌物包括肌鈣蛋白t和i、肌酸酐激酶、肌紅蛋白水平、利尿鈉肽(例如b型利尿鈉肽)、c-反應蛋白(crp),紅細胞沉降率(esr),心臟型脂肪酸結合蛋白以及和肽素(copeptin)、中間區域性房前利尿鈉肽原、st2,c-末端內皮素原1和中間區域性腎上腺髓質素原。
肌鈣蛋白是當發生不可逆的心肌損傷時從肌細胞釋放的蛋白質。它對心臟組織高度特異性,並準確診斷具有缺血性疼痛或反映缺血的ecg變化的病史的心肌梗死。心臟肌鈣蛋白水平依賴梗死大小,因此為梗死後預後提供指示。
本公開的方法涉及進行性心力衰竭的心輸出量特徵的逐漸下降的治療。
因此,在本公開的上下文中,「治療(treat和treatment)」是指治療性治療和預防性或防範性措施。
在一個實例中,治療減少心臟衰竭相關主要不良心臟事件(hf-mace)的機率或風險,所述hf-mace被定義為心臟相關死亡或復甦的心臟死亡或非致命失代償性心力衰竭事件的複合。在一個實例中,hf-mace的風險機率在至少6個月、至少12個月、至少24個月、至少36個月內減少。
在本公開的背景下,設想術語慢性心力衰竭,充血性心力衰竭,充血性心力衰竭可以與「進行性心力衰竭」互換使用。
心肌梗死誘發性心力衰竭
眾所周知,患者預後(progmosis)和心臟功能與梗死的左心室(lv)的量有關。
術語「心肌梗死誘發性心力衰竭」是指心肌梗死(mi)是心力衰竭的原因的受試者子集。設想本公開的方法可用於治療mi受試者的特定群體中的進行性心力衰竭。
特別地,mi受試者的群體是那些具有大於70ml的lvesv的群體。在其它實例中,lvesv大於80ml、大於90ml、大於100ml、大於110ml或大於120ml。在一個實例中,受試者具有近端左前降支(lad)動脈病變。在本公開的上下文中,術語「動脈病變」涵蓋阻塞性病變,其阻塞心臟的lad;或先前阻塞已經例如通過經皮冠狀動脈介入(pci),也稱為血管成形術治療的lad的動脈病變。
mi可導致持續性左心室功能障礙。左心室功能障礙的特徵在於心肌收縮力的降低。當心肌收縮力在整個左心室內降低時產生左心室射血分數(lvef)的降低。因此,lvef提供了一種確定左心室功能障礙的方式。lvef可以通過本領域已知的多種方法測量,例如但不限於二維超聲心動圖顯象(ecg)、磁共振斷層攝影術、心臟計算機斷層攝影術(ct)、放射性核素血管造影術、門控心肌灌注單光子發射計算機斷層攝影術(spect)、門控心肌灌注正電子發射斷層攝影術(pet)或雙平面左心室電影造影。
lvef可以使用以下公式測量:lvef=中風體積(edv-esv)/edv。lvef變化5-10%可能代表lvef的真正下降。
在一個實例中,lvef小於約55%的受試者具有左心室功能障礙。在其它實例中,lvef低於約54%、53%、52%、51%、50%、49%、48%、47%、46%的受試者具有左心室功能障礙。在另一個實例中,lvef小於約45%的受試者具有左心室功能障礙。在其它實例中,lvef小於約44%、43%、42%、41%的受試者具有左心室功能障礙。在另一個實例中,lvef小於約40%的受試者具有左心室功能障礙。在其它實例中,lvef小於約39%、38%、37%、36%、35%、34%、33%、32%、31%、30%的受試者具有左心室功能障礙。
在本公開的上下文中,術語「持續性左心室功能障礙」用於定義在一段時間或一系列測量中持續的左心室功能障礙。例如,「持續性左心室功能障礙」可以包括mi後約1至約14天之間或更長持續的左心室功能障礙。例如,持續性左心室功能障礙可以包括mi後約1至約10之間、約1至約9之間、約2至約8之間、約2至約7天之間的左心室功能障礙。在另一個實例中,「持續性左心室功能障礙」可以包括在約1至10次或更多次測量中持續的左心室功能障礙。
mi後心肌壞死的大小或量臨床上稱為梗死大小。設想本公開的方法涉及治療具有大梗死大小的mi受試者。例如,使用本公開的方法治療的受試者具有大於約10-35%左心室的梗死大小。在其它實例中,受試者具有大於約11-34%、約12-33%、約13-32%、約14-31%、約15-30%、約16-29%、約17-28%左心室的梗死大小。在另一個實例中,受試者具有大於約18.5%左心室的梗死大小。在其它實例中,受試者具有約19-27%、約20-26%、約21-25%、約22-24%、約23%左心室的梗死大小。
可以通過本領域已知的多種方法來測量梗死大小。這些方法的實例包括使用血清標誌物如肌酸激酶(ck)、ck-mb、肌鈣蛋白i和腦利鈉肽肌鈣蛋白。
在一個實例中,用本公開的方法治療的受試者具有至少約2x正常上限(ulm)的肌鈣蛋白水平。
在另一個實例中,受試者具有至少約3x、約4x、約5x、約6xulm的肌鈣蛋白水平。
在一個實例中,用本公開的方法治療的受試者具有至少約2x正常上限(ulm)的肌酸激酶-mb水平。
在另一個實例中,受試者具有至少約3x、約4x、約5x、約6xulm的肌酸激酶-mb水平。
測量梗死大小的其它實例包括sestamibi單光子發射計算機斷層掃描(spect)心肌灌注成像、磁共振成像。在一個實例中,使用cmri測量梗死大小。幾種心臟磁共振成像(cmri)技術可用於診斷梗死大小。最準確和最有效的技術之一是延遲增強心臟磁共振成像(de-cmr)技術。在一個實例中,cmri包括延遲增強心臟磁共振成像(de-cmr)。
當使用de-cmr的適當設置時,正常的心肌顯示為黑色或無效,而非活區域表現為明亮或過度增強。因此,在一個實例中,梗死大小可以通過明亮和超增強區域的視覺評估來確定。確定梗死大小的其它實例是本領域已知的(sievers等人(2007),circulation,115,236-244;kim等人(2000),nengljmed,343,1445-1453)。簡而言之,在17段模型上用每個區段的5點量表對超增強進行評分(0=無過度增強,1=1%至25%,2=26%至50%,3=51%至75%,4=76%至100%)。完全包含在超增強的心肌內的黑色區域被解釋為微血管損傷(無回流)的區域,並被包括在梗死的一部分中。通過對區域評分進行求和將梗死大小計算為lv心肌的百分比,每個區域通過超增強範圍中點加權(即1=13%,2=38%,3=63%,4=88%),並除以17。在另一個實例中,梗死大小可以通過在短軸圖像堆棧上的超增強區域的測面積法來量化。
在一個實例中,在mi後約1天和40天之間測量梗死大小。
在其它實例中,在mi後約1至40天之間、約2至35天之間、約3至30天之間、約4至25天之間、約5至20天之間、約6至15天之間、約6至15天之間測量梗死大小。
在一個實例中,可以在mi後約30天測量梗死大小。
在本公開的上下文中,「梗死大小」是指左心室梗死大小。換句話說,左心室梗死大小是指梗死的左心室的量。
設想本公開的方法可以用於治療具有心臟衰竭的各種階段或分類的心肌梗死受試者的進行性心力衰竭。
在一個實例中,心力衰竭分期是基於美國心臟病學會(acc)和美國心臟協會(aha)分期標準。在另一個具體的實例中,受試者根據acc或aha標準具有a、b、c或d期心力衰竭。在另一個實例中,受試者具有b或c期心力衰竭。
在另一個實例中,心力衰竭分類是基於紐約心臟協會(nyha)分類量表。在另一個具體的實例中,受試者具有i、ii、iii或iv類心力衰竭。在另一個實例中,受試者具有ii或iii期心力衰竭。
基於導管的遞送系統
任何基於導管的遞送系統可以用於實施本公開的方法,所述遞送系統允許將間充質譜系前體細胞或幹細胞和/或其後代和/或由其衍生的可溶性因子或包含其的組合物注射到受試者的心肌或心臟組織損傷區域附近的位置。在某些實例中,將導管經皮引入(例如,進入股動脈或另一血管),並通過血管系統引導到受試者的心肌,在心肌中它用於經由從導管末端擠出的針遞送間充質譜系前體細胞或幹細胞和/或其後代和/或由其衍生的可溶性因子,或包含其的組合物。在其它實例中,導管通過最小的手術切口(例如,限制性胸廓切開術,其涉及肋骨之間的切口)到達心臟。
已經設計了若干導管,以便精確地將藥劑遞送到心臟內的受損區域,例如梗死區域(參見例如美國專利號6,102,926;6,120,520;6,251,104;6,309,370;6,432,119和6,485,481,每篇的全部內容通過引用併入本文)。導管可以通過向下傳導具有容納腔的可導向或可導引的導管(參見例如美國專利號5,030,204)或通過固定構造導嚮導管(參見例如,美國專利號5,104,393)引導到指定位置。或者,導管可以通過可偏轉的探針(參見例如wo93/04724)或可偏轉的導絲(例如參見美國專利號5,060,660)行進到心臟內的期望位置。
導管可以耦合到心臟定位系統,其允許確定損壞/缺陷區的位置和程度(如上所述)。一旦鑑定了需要治療的區域,則可以拉出轉向引導件,在注射部位留下針頭。部分或全部間充質譜系前體細胞或幹細胞和/或其後代和/或其衍生的可溶性因子向下傳送至導管的內腔並注射入心肌。當已經進行了所有注射時從受試者縮回導管。
在將導管引導到受試者的心臟中時,針元件可以通常在鞘內縮回,以避免損傷靜脈系統和/或心肌。在注射時,針從導管的尖端擠出。在注射期間,針向成人心肌壁中伸出小於10mm、小於7.5mm或小於5mm。取決於注射部位,可以改變最大長度。對於嬰兒和兒童,伸出深度相應地較小,如通過實際或估計的壁厚所確定。用於移植細胞的針規格可以是例如25至30。
在一個實例中,用於將間充質譜系前體細胞或幹細胞和/或其後代和/或由其衍生的可溶性因子遞送至心肌的導管被配置為包括用於定位穿透深度和針插入的位置的反饋傳感器。反饋傳感器的使用提供了準確靶向注射位置的優點。用於遞送細胞組合物的靶位置可以變化。例如,最佳治療可以需要在沒有兩次注射穿透相同部位的損傷/缺陷區域內進行多次小的注射。或者,靶位置可以在連續的細胞施用程序中保持相同。
可用於本公開的合適的導管是nogatm注射導管系統(biosensewebster,inc.)。該導管是具有可偏轉尖端和設計成將藥劑注射到心肌中的注射針的多電極經皮導管。注射導管的尖端配備有biosense位置傳感器和可伸縮的中空的27號針,用於流體遞送。注射部位在心臟圖上實時指示,允許精確分配注射。獲得局部電信號以最小化導管尖端創傷。
本公開的組合物
在本公開的一個實例中,間充質譜系前體細胞或幹細胞和/或其後代和/或由其衍生的可溶性因子以組合物的形式施用。在一個實例中,這種組合物包含藥學上可接受的載體和/或賦形劑。
術語「載體」和「賦形劑」是指本領域常規用於促進活性化合物的儲存、施用和/或生物活性的物質組合物(參見例如remington'spharmaceuticalsciences,第16版,macpublishingcompany(1980))。載體也可以減少活性化合物的任何不期望的副作用。合適的載體例如是穩定的,例如不能與載體中的其它成分反應。在一個實例中,載體在用於治療的劑量和濃度下不會在接受者中產生顯著的局部或全身不利反應。
用於本公開的合適的載體包括常規使用的那些,例如水、鹽水、右旋糖水溶液、乳糖、林格氏溶液、緩衝溶液、透明質酸和二醇是示例性液體載體,特別是(當等張時)用於溶液。合適的藥物載體和賦形劑包括澱粉、纖維素、葡萄糖、乳糖、蔗糖、明膠、麥芽、米、麵粉、白堊、矽膠、硬脂酸鎂、硬脂酸鈉、單硬脂酸甘油酯、氯化鈉、甘油、丙二醇、水、乙醇,等。
在另一個實例中,載體是培養基組合物,例如其中培養或懸浮細胞。例如,此類培養基組合物不誘導其施用的受試者產生任何不利影響。
示例性載體和賦形劑不會不利地影響細胞的存活力和/或細胞減少、預防或延遲代謝症候群和/或肥胖症的能力。
在一個實例中,載體或賦形劑提供緩衝活性以將細胞和/或可溶性因子維持在合適的ph,從而發揮生物活性,例如載體或賦形劑是磷酸鹽緩衝鹽水(pbs)。pbs代表有吸引力的載體或賦形劑,因為它與細胞和因子最小程度地相互作用並允許細胞和因子的快速釋放,在這種情況下,本公開的組合物可以作為液體生產以供例如通過注射直接應用於血液或應用入組織或組織周圍或附近的區域。
也可以將間充質譜系前體細胞或幹細胞和/或其後代和/或自其衍生的可溶性因子摻入或嵌入受體相容並且降解成對接受者無害的產物的支架內。這些支架為要移植到接受者受試者的細胞提供支持和保護。天然和/或合成的可生物降解的支架是這種支架的實例。
在本公開的實踐中可以成功使用多種不同的支架。示例性支架包括但不限於生物的、可降解的支架。天然可生物降解支架包括膠原、纖連蛋白和層粘連蛋白支架。用於細胞移植支架的合適的合成材料應該能夠支持廣泛的細胞生長和細胞功能。這種支架也可以是可再吸收的。合適的支架包括聚乙醇酸支架(例如,如vacanti等人j.ped.surg.23:3-91988;cima等人biotechnol.bioeng.38:1451991;vacanti等人plast.reconstr.surg.88:753-91991所述);或合成聚合物如聚酐、聚原酸酯和聚乳酸。
在另一個實例中,間充質譜系前體細胞或幹細胞和/或其後代和/或自其衍生的可溶性因子可以在凝膠支架(如來自upjohncompany的gelfoam)中施用。
本文所述的組合物可以單獨施用或作為與其它細胞的混合物施用。不同類型的細胞可以在施用前立即或不久與本公開的組合物混合,或者它們可以在施用前一起共培養一段時間。
在一個實例中,組合物包含有效量或治療或預防有效量的間充質譜系前體細胞或幹細胞和/或其後代和/或自其衍生的可溶性因子。例如,組合物包含約1x105個幹細胞至約1x109個幹細胞或約1.25x103個幹細胞至約1.25x107個幹細胞/kg(80kg受試者)。要施用的細胞的確切量取決於多種因素,包括受試者的年齡、體重和性別以及所治療的病症的程度和嚴重程度。
示例性的劑量包括至少約1.2x108至約8x1010個細胞,如約1.3x108至約8x109個細胞、例如約1.4x108至約8x108個細胞、例如約1.5x108至約7.2x108個細胞、約1.6x108至約6.4x108個細胞、如約1.7x108至約5.6x108個細胞、例如約1.8x108至約4.8x108個細胞、例如約1.9x108至約4x108個細胞、約2.0x108至約3.2x108個細胞、約2.1x108至約2.4x108個細胞。例如,劑量可以包括至少約2.0x108個細胞。例如,劑量可以包括至少約1.5x108個細胞。
換言之,示例性的劑量包括至少約1.5x106個細胞/kg。例如,劑量可以包括約1.5x106至約1x109個細胞/kg、如約1.6x106至約1x108個細胞/kg、如約1.8x106至約1x107個細胞/kg、例如約1.9x106至約9x106個細胞/kg、約2.0x106至約8x106個細胞/kg、如約2.1x106至約7x106個細胞/kg、例如約2.3x106至約6x106個細胞/kg、例如約2.4x106至約5x106個細胞/kg、例如約2.5x106至約4x106個細胞/kg、例如約2.6x106至約3x106個細胞/kg。例如,劑量可以包括至少約2.5x106個細胞/kg。
在一個實例中,間充質譜系前體細胞或幹細胞組成組合物的細胞群體的至少約5%、至少約10%、至少約15%、至少約20%、至少約25%、至少約30%、至少約35%、至少約40%、至少約45%、至少約50%、至少約55%、至少約60%、至少約65%、至少約70%、至少約75%、至少約80%、至少約85%、至少約90%、至少約95%、至少約99%。
可以冷凍保存本公開的組合物。間充質譜系前體細胞或幹細胞的冷凍保存可以使用本領域已知的慢速冷卻方法或「快速」冷凍方案進行。優選地,與未冷凍的細胞相比,冷凍保存的方法維持類似的表型、細胞表面標誌物和冷凍保存的細胞的生長速率。
冷凍保存的組合物可以包含冷凍保存溶液。冷凍保存溶液的ph通常為6.5至8,優選7.4。
靜脈注射溶液(cyropreservationsolution)可以包括無菌、非致熱原性等張溶液,例如plasmalyteatm。100ml的plasmalyteatm含有526mg氯化鈉,usp(nacl);502mg葡萄糖酸鈉(c6h11nao7);368mg三水合乙酸鈉,usp(c2h3nao2·3h2o);37mg氯化鉀,usp(kcl);和30mg氯化鎂,usp(mgcl2·6h2o)。它不含抗菌劑。用氫氧化鈉調節ph。ph為7.4(6.5至8.0)。
冷凍保存溶液可以包括profreezetm。冷凍保存溶液可以另外或可選地包括培養基,例如αmem。
為了便於冷凍,通常將冷凍保護劑,如例如二甲基亞碸(dmso)添加到冷凍保存溶液。理想地,冷凍保護劑應對細胞和患者無毒、非抗原性、化學惰性,解凍後提供高存活率,並且允許在不清洗的情況下移植。然而,最常用的冷凍保護劑dmso表現出一些細胞毒性。羥乙基澱粉(hes)可用作替代物或與dmso組合以降低冷凍保存溶液的細胞毒性。
冷凍保存溶液可以包含dmso、羥乙基澱粉、人血清組分和其它蛋白質填充劑中的一種或多種。在一個實例中,冷凍保存的溶液包含約5%人血清白蛋白(hsa)和約10%dmso。冷凍保存溶液還可以包含甲基纖維素、聚乙烯吡咯烷酮(pvp)和海藻糖中的一種或多種。
在一個實施方案中,將細胞懸浮於42.5%profreezetm/50%αmem/7.5%dmso中,並在受控速率冷凍機中冷卻。
可以解凍冷凍保存的組合物並直接施用於受試者,或添加到另一種溶液(例如包含ha)中。或者,可以解凍冷凍保存的組合物,並且在施用前將間充質質系系前體或幹細胞重懸於替代載體中。
在一個實例中,可以在mi後約1至約10天施用本文所述的組合物。
在其它實例中,可以在mi後約1至9天、約1至8天、約2至7天、約2至6天、約3至5天施用本文所述的組合物。例如,可以在pci後約5天施用本文所述的組合物。
在一個實例中,可以在皮冠狀動脈幹預(pci)後約1至約10天施用本文所述的細胞組合物。
在其它實例中,可以在pci後約1至9天、約1至8天、約2至7天、約2至6天、約3至5天施用本文所述的組合物。例如,可以在pci後約5天施用本文所述的組合物。
在一個實例中,本文所述的組合物可以以單次劑量施用。
在一些實例中,可以以多劑施用本文中所述的組合物。例如,至少2,至少3,至少4,至少5,至少6,至少7,至少8,至少9,至少10劑。
在一個實例中,可以在施用前培養擴增間充質譜系前體細胞或幹細胞。細胞培養的各種方法是本領域已知的。
在一個實例中,在施用前在無血清培養基中培養擴增間充質譜系前體細胞或幹細胞。
在一些實例中,細胞被包含在室內,所述室不允許細胞離開受試者的循環,然而,允許細胞分泌的因子進入循環。以這種方式,可以通過允許細胞將因子分泌到受試者的循環中而將可溶性因子施用於受試者。這樣的室可以同樣植入受試者的部位,以增加可溶性因子的局部水平,例如植入在心臟中或附近。
可以全身施用間充質譜系前體細胞或幹細胞和/或其後代和/或由細胞衍生的可溶性因子,如例如通過靜脈內、動脈內或腹腔內施用。也可以通過肌肉內或心臟內施用來施用間充質譜系前體細胞或幹細胞和/或其後代和/或自其衍生的可溶性因子。
在一個實例中,將間充質譜系前體細胞或幹細胞和/或其後代和/或由細胞衍生的可溶性因子直接施用到心肌中。例如,可以將間充質譜系前體細胞或幹細胞和/或其後代和/或由細胞衍生的可溶性因子直接施用到左心室的心肌中。
在一個實例中,通過心臟內膜導管如j&jmyostartm注射導管施用間充質譜系前體細胞或幹細胞和/或其後代和/或由細胞衍生的可溶性因子。
在一個實例中,將間充質譜系前體細胞或幹細胞和/或其後代和/或由細胞衍生的可溶性因子施用於有活力的心肌。
在一個實例中,將間充質譜系前體細胞或幹細胞和/或其後代和/或由細胞衍生的可溶性因子施用於冬眠心肌。
本領域技術人員將能夠使用本領域已知的方法鑑定有活力的心肌和/或冬眠心肌。例如,可以使用諸如nogastartm映射導管系統的映射導管系統來鑑定有活力的心肌和/或冬眠心肌。
在另一個實例中,通過冠狀動脈內輸注施用間充質譜系前體細胞或幹細胞和/或其後代和/或由細胞衍生的可溶性因子。例如,可以將間充質譜系前體細胞或幹細胞和/或其後代和/或由細胞衍生的可溶性因子施用於左前降支(lad)動脈。
在一個實例中,通過pci在lad血運重建後立即將間充質譜系前體細胞或幹細胞和/或其後代和/或由細胞衍生的可溶性因子施用到lad動脈中。
6分鐘步行測試(6mwt)
6分鐘步行測試(6mwt)於1963年開發(balkeb等人(1963)repcivaeromedresinstus53:1-8),以評估慢性呼吸系統疾病和心力衰竭中的運動耐力。測試測量受試者在總共6分鐘內在堅硬、平坦的表面上行走的距離。目標是在六分鐘內儘可能地步行。允許受試者自行踱步,並且當他們沿著標記人行道來回行走時根據需要休息。
本領域技術人員將理解,在不脫離本公開的廣泛的總體範圍的情況下,可以對上述實施方案進行許多變化和/或修改。因此,本實施方案在所有方面都認為是說明性的而不是限制性的。
以下具體實施例將被解釋為僅僅是說明性的,而不是以任何方式限制本公開的其餘部分。沒有進一步的闡述,認為本領域技術人員可以基於本文的描述,最大程度地利用本發明。
實施例
實施例1:研究設計
進行了一項研究,以評估由於缺血性或非缺血性病因學的左心室收縮功能異常所致的心力衰竭受試者中3種增加劑量(2500、7500萬或1.5億個細胞)的間充質前體細胞(mpc)的安全性和可耐受性。次要目標是通過多個參數來觀察功效,並鑑定mpc治療的最佳有效劑量和最佳目標群體。
心力衰竭受試者年齡為>18歲;由缺血性或非缺血性心肌病引起的心力衰竭,通過在放射性核素心室造影術、二維超聲心動圖顯象或核磁共振成像上檢測的射血分數(ef)3.2cm/m2或>6cm;呼吸困難或休息或最小限度盡力時疲勞的症狀(紐約心臟協會(nyha)ii類或iii類)>2個月;在篩查前12個月內需要靜脈利尿或血管擴張劑治療的至少一次住院或兩次門診訪視;以及最佳藥物治療,包括利尿劑、β阻斷劑和血管緊張素轉換酶(ace)抑制劑或血管緊張素受體阻斷劑(arb)),除非不耐受或禁忌。
在前90天內,根據急性心肌梗死排除受試者,血清鉀5.5meq/l,地高辛水平>1.2ng/ml,鎂水平2.0mg/dl和血清膽紅素>3.0mg/dl。
根據在導管插入實驗室中的心內膜心肌導管或編寫的模擬注射(對照組),將受試者隨機化為2500萬、7500萬或1.5億個mpc的注射。使用j&jmyostartm注射導管和nogastartm映射導管系統將mpc施用於左心室(約15-20次注射0.2ml/注射),所述系統基於電壓鑑定活力/冬眠心肌,理論上使健康但有風險的組織的靶向更容易。該導管具有該應用的最大安全性概況,並且已經在多次試驗的超過1,000名患者中使用。功能效力的測量涉及左心室收縮末期容積或lvesv、左心室舒張末期容積或lvedv、測量以及左心室射血分數或lvef。進行了與心力衰竭相關的主要不良心臟事件或hf-mace的第一次事件前時間的另外的分析。hf-mace被定義為心臟相關死亡或復甦心臟死亡或非致命失代償心力衰竭事件的複合。
慢性心力衰竭患者中mpc的心內膜心肌注射是可行和安全的。不利事件的發生率在所有組中相似,並且在接受mpc的任何患者中沒有臨床顯著的免疫應答。
1.5億細胞劑量顯示對左心室重塑和功能能力的最大影響和對於減少長期hf-mace的閾值益處(圖1)。
更具體地,在lvesv和lvedv兩者之間存在劑量相關的效果,其中與治療後6個月時lv重塑的對照(lvesv和lvedv兩者p100的受試者的比較的分析。意圖治療分析是一個統計概念。根據fisher等人(fisherld,dixondo,hersonj,frankowskirk,hearronms,peaceke.intentiontotreatinclinicaltrials.於:peaceke編statisticalissuesindrugresearchanddevelopment.newyork:marceldekker;1990.第331–50頁(1990)),itt分析包括他們被隨機化分配的組中的所有隨機化患者,無論其是否遵守入選標準,無論其實際接受的治療,以及無論隨後從治療中退出或偏離方案。換言之,itt分析包括根據隨機化治療分配隨機化的每個受試者。它忽略不順從、方案偏差、撤藥以及隨機化後發生的任何事情。itt分析通過接受在實際臨床實踐中可能發生不順從和方案偏差來避免源自除去非順從者的幹預的功效的過於樂觀的評估。
表1全部受試者與lvesv>100ml的受試者(itt,或意圖治療)的比較
此分析表明,通過聚焦於具有實質性基線lv收縮異常和晚期心力衰竭(lvesv大於100ml)的目標群體明顯放大1.5萬劑量對lv重塑的參數的治療益處。
實施例3:mpc施用對lvesv的治療益處
對共計30名受試者(心力衰竭和非心力衰竭受試者的混合)評估基線lvesv水平。在表2中顯示受試者的分布。受試者分類為安慰劑組或mpc細胞組(其施用1.5x108個間充質前體細胞(mpc))。使用j&jmyostar注射導管和基於電壓鑑定活力/冬眠心肌的nogastar映射導管系統注射入左心室(約15-20次注射0.2ml/注射)。受試者基於他們的左心室收縮末期容積(lvesv)值100ml分層。
表2根據基線lvesv值的受試者分層
在對研究評估的30名受試者中,18名受試者具有基線lvesv值>100ml。將七(7)名受試者分配到安慰劑,並且將11名分配到mpc。
圖3-1顯示了受試者組的基線lvesv值。根據小於或等於(≤)100ml的lvesv分層的受試者具有平均基線lvesv值為81ml。根據其大於(>)100ml的lvesv值分層的受試者具有平均基線值136ml。
在施用安慰劑或1.5x108個間充質前體細胞(mpc)後6個月時間點對受試者進行重新評估。對於基於lvesv值分層的受試者確定主要不良心臟事件(mace)率。在圖3-2中顯示結果,表示基線和6個月時間點之間lvesv值的變化。施用了安慰劑組(對照)和mpc的受試者之間的lvesv值的變化是統計學顯著的。
表3顯示了以數字和百分比數值表示的心力衰竭mace率(hf-mace)。
表3根據基線lvesv值分層的受試者中的lvesv值的變化
基線lvesv值≤100ml的受試者在6個月評估期未形成主要不良心臟事件,這與受試者是否施用安慰劑或1.5x108個間充質前體細胞(mpc)無關。hf-mace只發生在安慰劑受試者(對照)中,所述安慰劑受試者具有較大的基線心臟功能障礙的證據,如通過lvesv>100ml評估。相比之下,施用了mpc的具有如通過lvesv>100ml評估的基線心臟功能障礙的受試者無一形成hf-mace。
表2中的數據表明,用安慰劑治療的心臟衰竭受試者將經歷高mace率(即6個月時期時71%)。特別地,高mace率僅在具有基線lvesv值>100ml的受試者中觀察到。
數據顯示,基線lvesv值>100ml的心力衰竭受試者從mpc的施用中獲得最佳治療益處。換言之,疾病進展風險最高的受試者從mpc的施用中獲得最大的益處。
實施例4:mpc施用對lvedv和lvef的治療益處
還在已經根據lvesv值小於或等於(≤)100ml或>100ml分層的受試者中評估左心室舒張末期容積(lvedv)。
圖4-1顯示了受試者的基線lvedv值。基線lvesv≤100ml的受試者的平均基線lvedv為128ml。基線lvesv值>100ml的受試者的平均基線lvedv值為198ml。
受試者分布按照表1。
圖4-2顯示了根據基線lvesv≤100ml和基線lvesv>100ml分層的受試者之間施用安慰劑(對照)或mpc後6個月的lvedv值的變化。該圖顯示,mace率最高的心力衰竭受試者達到來自mpc施用的治療益處,如lvedv值的改善證明。根據lvesv值≤100ml或>100ml分層的受試者之間的差異是統計學顯著的。
也在按照lvesv值分層的受試者中評估左心室射血分數(lvef)值。圖5-1顯示了受試者的基線lvef值。基線lvesv≤100ml的受試者具有35-40%的平均基線lvef。基線lvesv值>100ml的受試者的平均基線lvef值為約32%。
受試者分布按照表1。
圖5-2顯示了根據基線lvesv≤100ml和基線lvesv>100ml分層的受試者之間施用安慰劑(對照)或mpc後6個月時lvef值的變化。該圖顯示了具有最高的mace率的心力衰竭受試者達到來自mpc施用的治療益處,如通過lvef值的改善所證明的。根據lvesv值≤100ml或>100ml分層的受試者之間的差異是統計學顯著的。
實施例5:疾病嚴重性和mpc對lvesv的治療益處之間的關聯
在70ml和120ml之間基線lvesv的每十分位數間的進一步靈敏度分析證實了在使用大於100ml的lvesv的分層中看到的發現。
圖6至圖11顯示了在施用安慰劑(對照)或mpc(1.5x108個間充質前體細胞)後6個月評價的受試者lvesv的變化。lvesv的降低與心力衰竭的水平(如通過基線lvesv的測量確定)相關。將受試者根據lvesv分層,如下表4所示。
表4lvesv的變化
實施例6:lvesv>100ml的患者中的hf-mace。
在對照組和接受1.5億個mpc的受試者中治療後36個月檢查hf-mace。在36個月隨訪內的所有hf-mace事件都僅僅發生在具有晚期心力衰竭的對照組中(圖12)。
與所有對照中的11%相比,這些快速進展者的按年計算的hf-mace率為24%。
更具體地,在18名基線lvesv>100ml的ii/iii類chf患者中,5/7(71%)安慰劑處理者對0/111.5億個mpc治療者在36個月內經歷了一次或多次hf-mace事件(p=0.0007)。
因此,在晚期心力衰竭和高進展率的那些患者中,1.5億mpc劑量對整體hf-mace的影響顯著放大,並且這可以代表mpc療法的最佳目標患者群體。
評述
本文中顯示的數據表明,由於左心室收縮功能障礙引起的慢性心力衰竭受試者的基線左心室收縮異常的量級越大,在6個月隨訪期內觀察到的mpc相關心臟保護效果越有益。數據進一步表明,通過用mpc治療可以有益地改變與晚期慢性心力衰竭有關的進行性不利天然病史。不希望受理論束縛,發現支持旁分泌串擾假設,其中組織水平的生物化學/生理紊亂產生促進mpc釋放有益的旁分泌介質的局部環境。因此,在具有最高疾病進展風險的受試者,即基線lvesv>70ml的受試者中觀察到通過在心力衰竭受試者中施用mpc所獲得的最佳效果。
基線lvesv>70ml鑑定了經歷高hf-mace的慢性心力衰竭和左心室收縮功能異常受試者的快速進展的亞組。
在基線lvesv>70ml、>80ml、>90ml、>100ml、>110ml或>120ml的受試者中,用高劑量(1.5億)mpc的治療導致比對照受試者中的所見更大的心臟重塑變量和hf-mace的改善。
本文呈現的結果鑑定了細胞療法的心臟保護益處的最佳目標群體,並且促進具有由於左心室收縮功能異常所致的心力衰竭的受試者的試驗設計的改進。
對於lvesv和lvedv體積顯著惡化以及lvef損失,具有晚期心力衰竭(基線lvesv>100ml)的對照患者是6個月內最快的進展者。在6個月的隨訪期內,1.5億mpc劑量對具有實質性基線lv收縮異常的ii/iii類患者(即具有基線lvesv>100ml的那些患者)中的lvesv(p<0.02)、lvedv(p<0.03)和lvef(p100ml的那些患者)中的lvesv(p<0.02)、lvedv(p<0.03)和lvef(p<0.05)具有顯著的心臟保護作用。
