菊苣酸在製備抗呼吸道合胞病毒的藥物中的應用的製作方法
2023-05-26 18:33:21 3
本發明涉及菊苣酸在製備抗呼吸道合胞病毒的藥物中的應用。
背景技術:
紫錐菊又名紫錐花、紫松果菊,為多年生草本植物,菊科松果菊屬。上個世紀70年代,紫錐菊引入我國,作為觀賞性植物栽培;90年代,肖培根院士首先將紫錐菊作為免疫調節劑介紹到國內,國內各地開始將其作為藥用植物引種,並逐漸投入gap標準化生產,從而保證研究與開發的原料安全問題。近年來國內已有數種紫錐菊製劑得到開發並應用於臨床,如「金屏風膠囊」(浙江正大青春寶藥業有限公司)、「紫黃精」(成都地奧製藥集團有限公司)等,均為紫錐菊與補氣中藥黃芪的複方製劑。
紫錐菊的應用非常廣泛,主要用途有提高機體免疫水平、抗炎、清除氧自由基以抗氧化、抗腫瘤、抗病毒等。國外對紫錐菊抗病毒作用的研究中,wacker採用小鼠l-929細胞培養的方法證實紫錐菊提取物能間接的抑制流感病毒、皰疹病毒與水泡性口炎病毒的活性;may發現松果菊的水提取物可明顯抑制流感病毒、皰疹病毒與脊髓灰質炎病毒活性。目前,國內對紫錐菊抗病毒作用的研究還處在起步階段,文獻報導多集中在畜牧業。馮善祥考察了紫錐菊複合物對感染雞新城疫病毒雛雞、人工感染傳染性法氏囊病毒雛雞的保護作用,並指出紫錐菊複合物可用於雞新城疫、雞傳染性法氏囊的預防以及治療。在細胞水平上,紫錐菊複方製劑對ndv有明顯的抑制作用,效果優於紫錐菊。
在紫錐菊的抗病毒研究中,已證實其提取物對流感病毒、柯薩奇b族病毒、皰疹病毒、hsv-ⅱ引起的細胞病變具有不同程度的抑制作用,對ard3、ard7、副流感病毒、echo11及hsv-ⅰ等的體外實驗則無明顯效果。目前我國對引種紫錐菊藥理活性的研究還局限在刺激免疫水平方面,人用抗病毒製劑尚未全面開發。在實現將紫錐菊用於人類病毒性疾病的治療過程中,仍然有藥材標準缺失、抗病毒活性成分不詳、抗病毒作用機理及靶點不清等問題橫亙眼前。因此對紫錐菊進行全面質量評價研究及藥理活性研究是其在我國得到全面開發應用的前提。
紫錐菊作為一種良好的免疫促進草藥,其化學成分及成分活性已有較多報導。目前在紫錐菊屬植物及其製劑的化學成分及結構研究中,已分離出咖啡酸類衍生物、烷基醯胺類、多糖類、揮髮油類、生物鹼、黃酮、多炔類及其它類化學成分等。菊苣酸是紫錐菊中極為重要的免疫活性成分之一,近年來的藥理研究表明,菊苣酸具有增強免疫功能和抗炎作用,並能抑制透明質酸酶,保護膠原蛋白免受可導致降解的自由基的影響。現有技術中尚未見到關於菊苣酸在抗呼吸道合胞病毒方面的相關報導。
技術實現要素:
針對上述現有技術,本發明經研究,發現了菊苣酸的新用途——在製備抗呼吸道合胞病毒的藥物中的應用。
本發明是通過以下技術方案實現的:
本發明的發明人應用中藥化學方法對植物紫錐菊中的抗病毒成分進行篩選,並通過體外抗病毒藥效實驗發現了最佳抗病毒活性成分——菊苣酸,並發現菊苣酸對呼吸道合胞病毒(rsv)的體外抗病毒活性最強,優於對照藥利巴韋林,因此,可以以菊苣酸為活性成分用於製備抗呼吸道合胞病毒的藥物,具體應用時,可適量添加藥劑學上可接受的基質或輔料,也可以與適當的藥物聯合應用。
紫錐菊中藥物活性成分複雜,有咖啡酸類衍生物、烷基醯胺類、多糖類、揮髮油類、生物鹼、黃酮、多炔類及其它類化學成分等,本發明不但發現了紫錐菊提取物對呼吸道合胞病毒有抑制作用,還明確了菊苣酸為體外抗呼吸道合胞病毒的有效成分,對紫錐菊的抗病毒研究、紫錐菊成方製劑的進一步研究等具有重要意義。
附圖說明
圖1::正常細胞及病毒病變細胞,其中,a:正常vero細胞(4×40);b:hsv-ⅰ病毒病變(4×10);c:正常vero細胞(4×10);d:rsv病毒病變(4×10);e:正常rd細胞(4×10);f:ev71病毒病變(4×10)。
圖2:紫錐菊體外抗病毒譜的篩選結果柱狀圖。
圖3:紫錐菊提取方法優化結果柱狀圖。
圖4:紫錐菊水提物d101型大孔樹脂洗脫物抗病毒結果柱狀圖。
圖5:d101大孔樹脂柱分離樣品pad監測圖。
圖6:d101大孔樹脂柱分離有效部位液相色譜圖。
圖7:快速製備化合物高效液相檢測色譜圖。
圖8:菊苣酸對照品裂解碎片信息。
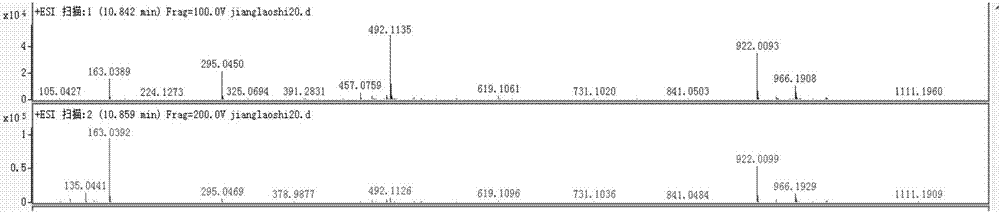
圖9:製備純品化合物裂解碎片信息。
圖10:紫錐菊製備純品抗病毒實驗結果柱狀圖。
具體實施方式
下面結合實施例對本發明作進一步的說明。
下述實施例中所涉及的儀器、試劑、材料等,若無特別說明,均為現有技術中已有的常規儀器、試劑、材料等,可通過正規商業途徑獲得。下述實施例中所涉及的實驗方法,檢測方法等,若無特別說明,均為現有技術中已有的常規實驗方法,檢測方法等。
實驗一紫錐菊體外抗病毒譜的篩選
1.實驗儀器與材料
1.1藥品紫錐菊乾燥地上部分藥材購自安徽省桐城市維慶藥用植物有限公司,粉碎機粉碎,備用;利巴韋林注射液(齊魯製藥有限公司,規格為50mg/ml,批號:1501166141)。
1.2細胞非洲綠猴腎細胞(vero,為hsv-ⅰ、rsv的敏感細胞株,由山東省醫學科學院微生物實驗室保存);橫紋肌瘤細胞(rd,為ev71的敏感細胞株,由山東省醫學科學院微生物實驗室保存)。
1.3病毒毒種hsv-ⅰ:f株,1996年引自山東醫科大學微生物學教研室,由山東省醫學科學院微生物實驗室保存;rsv:long株,2000年10月引自中國預防醫學科學院病毒所毒種室,本科室保存;ev71,分離自濟南市兒童醫院icu病房病死患兒(genbank登記號:hq825317)。
1.4試劑正丁醇、石油醚、乙酸乙酯、丙酮、乙醇、二甲基亞碸(天津富宇精細化工有限公司產品,均為分析純);細胞培養液(1640細胞培養液,gibco產品,含11%新生牛血清及100u/ml青黴素和鏈黴素,置4℃備用);細胞維持液(1640細胞培養液,gibco產品,含2%新生牛血清及100u/ml青黴素和鏈黴素);pbs(ph7.2,含nacl8g、kcl0.2g、kh2po40.2g、na2hpo42.9g,加雙蒸水至1000ml,過濾除菌,分裝置4℃備用);細胞消化液(0.25%胰酶,macgene公司產品,分裝至青黴素瓶,置-20℃冰箱備用)。
1.5儀器co2恆溫培養箱(日本三洋公司產品);生物安全櫃(濟南鑫貝西公司產品);超淨工作檯(濟南隆宏淨化設備有限公司);高壓滅菌鍋(上海博訊實業有限公司醫療設備廠);雙人雙面淨化工作檯(蘇州淨化儀器廠);倒置顯微鏡(olympus公司產品);臺式自動平衡離心機(長沙湘智離心機有限公司);離心機(賀立氏臺式低溫離心機);超低溫冰箱(-80℃,725型,thermoforma公司);低溫冰箱(-40℃,日本三洋公司;–20℃,中科美菱公司產品;4℃,海爾兄弟公司產品);液氮罐(四川液氮罐廠產品);96孔細胞培養板(美國gibco公司產品);除菌針頭濾器(美國頗爾公司pallcorporation,孔徑:0.22μm,直徑13mm);移液器(德國eppendorf產品,型號:20-200μl;100-1000μl);移液器吸頭(德國eppendorf產品,與移液器配套);超聲振蕩清洗儀(崑山市超聲儀器有限公司);高速萬能粉碎機(北京市永光明醫療儀器有限公司,fw-100);水浴鍋(上海樹立儀器儀表有限公司)電熱鼓風乾燥箱(天津市萊玻特瑞儀器設備有限公司,gfl-230)。
2.實驗方法
2.1製備不同極性溶劑紫錐菊提取物
取紫錐菊藥材粉末40g,加入8倍量的蒸餾水進行煎煮2h,抽濾;取過濾後藥渣加同樣量蒸餾水繼續煎煮2h,抽濾;將兩次濾液合併,水浴揮幹。分別更換80%乙醇、100%乙醇、石油醚、乙酸乙酯、正丁醇重複上述工藝步驟,製備紫錐菊不同極性部位提取物。水提物以細胞維持液溶解,其它提取物以dmso溶解,0.22μm濾頭過濾除菌,備用。
取紫錐菊粉末40g,加8倍量的50%丙酮超聲提取1h,抽濾,濾渣再加8倍量50%丙酮重複超聲1h,抽濾;兩次濾液合併,水浴揮幹,用dmso溶解適量,0.22μm濾頭過濾除菌,備用。
2.2不同極性溶劑紫錐菊提取物體外抗病毒實驗
2.2.1細胞的復甦與傳代
從液氮中取出凍存的vero、rd細胞,均投放於37℃溫水中迅速搖晃,在1min內迅速解凍。800rpm離心5min,棄去上清液,使用細胞培養液將細胞懸浮,轉移至含有細胞培養液的細胞培養瓶中,37℃、5%co2培養箱中靜止培養。2d後細胞長成單層,0.25%胰酶消化並1:2傳代,至細胞長成單層時可用於試驗。
2.2.2病毒的擴增
取上述已長至單層的細胞,棄去上清液,將存放於-80℃條件下的hsv-ⅰ、rsv、ev71病毒解凍後分別接種於對應的敏感細胞上。於35℃,5%co2條件下的培養箱中孵育1h,取出加入細胞維持液後,繼續放置培養箱中進行培養。逐日鏡下觀察細胞病變(cytopathiceffect,cpe),當cpe達到90%,於超低溫冰箱反覆凍融3次,吹打離心(20000r/min,15min),取上清分裝,做好標記,–40℃冰箱凍存備用。
2.2.3病毒毒力的測定
用細胞維持液將單純皰疹ⅰ型病毒液、呼吸道合胞病毒液做10倍比系列稀釋,橫向依次接種在96孔板內長成單層的vero細胞上,縱向重複3孔,同時設正常細胞對照,置35℃、5%co2培養箱中培養;用同樣方法取ev71病毒液做十倍比系稀釋後,種在長成單層的rd細胞上。48h後倒置顯微鏡下觀察,細胞出現病變,視為病毒毒性,終止培養,觀察並記錄細胞病變率。
運用reed-muench兩氏法,即公式(1)、(2),計算各病毒的半數細胞感染量tcid50(50%tissuecultureinfectivedose)。
公式(2)········tcid50=antilog(logc+pd×logcm)
其中:pd=細胞比距;p1=高於50%病變百分數;p2=低於50%病變百分數;c=高於50%病變率的稀釋度;cm=倍比稀釋係數。
2.2.4藥物細胞毒性的測定
取2.1項下備用不同極性提取物適量,用細胞維持液做2倍比系列稀釋,共12個稀釋度,分別加樣於96孔板中已經長成單層的vero、rd細胞上,各稀釋度縱向重複3孔,37℃、5%co2培養箱中培養。24小時後顯微鏡下觀察病變情況,待病毒對照病變率達到90%,終止培養,觀察並記錄每種提取物的細胞病變(cpe)百分率,應用reed-muench方法計算藥物半數中毒濃度(tc50),並確定最大無毒濃度(tc0)。
2.2.5藥物對病毒致細胞病變作用的影響
取2.1項下備用的不同極性提取物用細胞維持液做2倍比系列,稀釋共12個稀釋度,分別按100μl/孔依次加樣於96孔板內的單層rd、vero細胞上,每個稀釋度重複3孔,設利巴韋林注射液原液為陽性對照,並設細胞對照、病毒對照。除細胞對照加100μl細胞維持液外,各孔加2.2.3項下測得tcid50濃度的病毒液100μl。置35℃、5%co2培養箱中培養,每日顯微鏡下觀察細胞病變,待病毒對照出現90%細胞病變後終止培養。鏡下觀察其cpe。應用reed-muench方法計算藥物半數有效濃度(ec50)(concentrationfor50%ofmaximaleffect,ec50)。根據2.2.4項下的藥物半數中毒濃度(tc50)及藥物半數有效濃度(ec50),計算藥物的抑毒指數(ti)。
公式(3)…tc50=[antilog(log高於50%病變率藥物稀釋度值-pd)]×初始濃度
細胞存活率大於50%最後一個濃度為ec50
公式(4)…ec50=[antilog(log高於50%存活率藥物稀釋度值-pd)]×初始濃度
3實驗結果
3.1病毒毒力測定的結果
觀察病毒所致細胞的病變情況,按reed·muench法計算hsv-ⅰ型病毒(f株)的tcid50=10-3.33/100μl,rsv病毒株的tcid50為10-2.50/100μl,ev71病毒株的tcid50為10-4.33/100μl。
3.2藥物對病毒的抑制作用結果
結果如圖1所示。通過記錄的cpe百分率,應用reed-muench方法計算藥物半數中毒濃度(tc50)及藥物半數有效濃度(ec50),並確定抑毒指數(ti=tc50/ec50)。結果見表1、圖2。
表1紫錐菊體外抗病毒譜的篩選結果
注:—表示無效,ti值大於4視為有效。
4.討論
本實驗同時考察了紫錐菊不同極性部位對hsv-ⅰ、rsv、ev71所致細胞病變的效果,使抗病毒譜的結果更加準確全面。結果表明,紫錐菊不同提取物對hsv-ⅰ、rsv、ev71所致細胞病變均有不同程度的抑制作用。通過檢測紫錐菊不同極性提取物對hsv-ⅰ、rsv、ev71的抗病毒效果發現,80%醇回流、水煎煮部位對三種病毒均有較好的抑制活性。通過比較各有效ti值發現,80%醇回流部位對rsv、ev71的抑制效果、水煎煮部位對hsv、rsv、ev71的抑制效果均大於陽性對照藥利巴韋林的抗病毒效果。本課題的目的是尋找紫錐菊的抗病毒有效成分,且水煎煮部位對抗rsv的效果最佳(ti值已達到196,遠大於陽性對照的31),因此選擇紫錐菊水部位對rsv的效果作為跟蹤依據,作為後續實驗方向。
實驗二紫錐菊提取方法的優化
實驗一中已明確紫錐菊的水煎煮部位對rsv所致細胞病變比其他極性部位有更好的抑制效果,因此在水提取的基礎上進行優化以確定一個更好的提取方案。
由於本研究的主要目的為定性,因此僅選擇對提取效果影響較大的溫度作為考察因素,分別設水煎煮提取與水超聲提取兩種提取方法,通過體外實驗考察溫度因素對提取效果的影響,從而確定最佳提取方案。
1實驗儀器與材料
1.1藥品紫錐菊乾燥地上部分藥材購自安徽省桐城市維慶藥用植物有限公司,粉碎機粉碎,備用;利巴韋林注射液(齊魯製藥有限公司,規格為50mg/ml,批號1501166141)。
1.2細胞非洲綠猴腎細胞(vero,rsv的敏感細胞株,由山東省醫學科學院微生物實驗室保存。
1.3病毒毒種rsv:long株,2000年10月引自中國預防醫學科學院病毒所毒種室,本科室保存。
1.4試劑蒸餾水;細胞培養液(1640細胞培養液,gibco產品,含11%新生牛血清及100u/ml青黴素和鏈黴素,置4℃備用);細胞維持液(1640細胞培養液,gibco產品,含2%新生牛血清及100u/ml青黴素和鏈黴素);pbs(ph7.2,含nacl8g、kcl0.2g、kh2po40.2g、na2hpo42.9g,加雙蒸水至1000ml,過濾除菌,分裝置4℃備用);細胞消化液(0.25%胰酶,macgene公司產品,分裝至青黴素瓶,置-20℃冰箱備用)。
1.5儀器同實驗一。
2.實驗方法
2.1不同極性紫錐菊提取物的提取
(1)水超聲提取法取紫錐菊粉末40g,加8倍量的蒸餾水超聲提取2h,抽濾;濾渣再加8倍量蒸餾水重複提取,抽濾;兩次濾液合併,100℃水浴揮幹,細胞維持液溶解適量,0.22μm濾頭過濾除菌,備用。
(2)水煎煮提取法取紫錐菊藥材粉末40g,加入8倍量的蒸餾水進行煎煮2h,抽濾;取過濾後藥渣加同樣量蒸餾水繼續煎煮2h,抽濾;將兩次濾液合併,水浴揮幹。以細胞維持液溶解適量,0.22μm濾頭過濾除菌,備用。
2.2體外抗病毒實驗
2.2.1藥物細胞毒性的測定
取紫錐菊水超聲提取物、水煎煮提取物適量,用細胞維持液做2倍比系列稀釋,共12個稀釋度,加樣於多孔板中已經長成單層的vero細胞上,每個稀釋度重複3孔,於37℃、5%co2培養箱中培養。24小時後顯微鏡下觀察病變情況,待病毒對照病變率達到90%,終止培養,觀察並記錄細胞病變(cpe)百分率,應用reed-muench方法計算藥物半數中毒濃度(tc50),並確定最大無毒濃度(tc0)。
2.2.2藥物對病毒致細胞病變作用的影響
取紫錐菊水煎煮提取物、水超聲提取物用細胞維持液做2倍比系列稀釋,共12個稀釋度,依次加入96孔板內的單層vero細胞上(100μl/孔),每個稀釋度重複3孔,設利巴韋林注射液原液為陽性對照,並設細胞對照、病毒對照。除細胞對照加100μl維持液外,各孔加100個tcid50的病毒100μl。置35℃、5%co2培養箱中培養,每日顯微鏡下觀察細胞病變,待病毒對照出現90%細胞病變後終止培養。鏡下觀察並記錄其cpe。應用reed-muench方法計算藥物半數有效濃度(ec50)(concentrationfor50%ofmaximaleffect,ec50)。根據上述藥物半數中毒濃度(tc50)及藥物半數有效濃度(ec50),計算藥物抑毒指數(ti)。
3實驗結果(見表2、圖3)。
表2紫錐菊提取方法優化結果
4.討論
溫度會影響受熱易變性成分的溶出效率,實驗中的兩種提取方法主要考察溫度因素對活性成分提取效率的影響。本實驗結果顯示,水煎煮提取的抑毒指數大於水超聲提取的抑毒指數,同時水提取物的效果遠大於陽性對照藥利巴韋林的效果。由此得出結論:抑制rsv所致細胞病變的有效成分在加熱條件下仍有存在,且高溫條件有利於其溶出,因此確定水煎煮提取法為最終的提取方法。
實驗三紫錐菊抗病毒有效部位的分離與純化
大孔吸附樹脂的應用出現在二十世紀六十年代,是繼離子交換法之後的又一分離純化方法,七十年代開始應用於中藥的分離純化。大孔吸附樹脂通過分子間作用力、氫鍵的吸附作用及多孔結構的分子篩作用發揮作用,待分離物質因吸附力及分子量大小的差異在洗脫過程中達到分離與純化的目的。按其極性大小和所選用的單體分子結構不同,可分為非極性、中極性和極性三種類型,對各種不同極性的藥物均具有較好的分離效果。d101型大孔吸附樹脂是苯乙稀型非極性共聚體,是一種多孔海綿狀結構的人工合成的聚合物吸附劑,適用範圍比較廣譜。
紫錐菊的水溶性部位主要為咖啡酸類衍生物、多糖類、蛋白質等大極性物質,成分種類繁多且極性相近,分離難度較大。已有文獻報導,咖啡酸衍生物類為紫錐菊重要的刺激機體免疫力的活性成分,在擬將其作為目標組分的情況下,選擇d101型大孔吸附樹脂,能將大極性成分快速洗脫下來,做到有效物質少損失,從而達到較理想的分離純化目的。
1實驗儀器與材料
乙醇(天津富宇精細化工有限公司產品,分析純);d101型大孔吸附樹脂(滄州寶恩化工有限公司);玻璃層析柱(φ4.5×85cm)。其餘儀器與材料同實驗二。
2.實驗方法
2.1樣品溶液製備
取紫錐菊粉末50g,加入8倍量的蒸餾水進行煎煮2h,抽濾;取過濾後藥渣加同樣量蒸餾水繼續煎煮2h,抽濾;將兩次濾液合併,100℃水浴揮幹。取上述水煎煮提取物超聲溶於400ml水中,備用
2.2大孔樹脂的預處理
取一定量的d101型大孔吸附樹脂,用100%乙醇浸泡24h,充分溶脹後的體積約為1l。取潔淨的玻璃層析柱(φ4.5×85cm),溼法裝柱,至樹脂高度約為柱高的2/3處,用乙醇進行衝洗。隨時檢測柱下端流出液體,即將液體與水按1:5混合,若混合後所得溶液澄清透明時,改用蒸餾水衝洗,至柱中流出的液體無乙醇味,靜置樹脂柱床備用。
2.3上樣
將2.1中的樣品溶液用玻璃棒緩慢引流上樣於處理好的的大孔樹脂柱中,打開層析柱下端的閥門,讓樣品溶液緩緩流動,最後保持液面高出樹脂柱床2~3cm處,關閉閥門,靜置12小時。
2.4洗脫
依次用水、25%乙醇、50%乙醇、75%乙醇進行梯度洗脫。控制流出液流出速度約為1滴/秒,每200ml收集為一段,每個洗脫梯度衝至無色換下一個梯度。將洗脫液按收集順序編號,並分別水浴蒸乾,備用。
2.5體外抗病毒實驗
2.5.1藥物細胞毒性的測定
取紫錐菊大孔樹脂洗脫物適量,分別用細胞維持液溶解,並做2倍比系列稀釋,共12個稀釋度,加樣於96孔板中已經長成單層的vero細胞上,每個稀釋度縱向重複3孔,於37℃、5%co2培養箱中培養。24小時後顯微鏡下觀察病變情況,待病毒對照的病變率達到90%,終止培養,觀察並記錄細胞病變(cpe)百分率,應用reed-muench方法計算藥物半數中毒濃度(tc50)。
2.5.2藥物對病毒致細胞病變作用的影響
取紫錐菊大孔樹脂洗脫物溶解並用細胞維持液做2倍比系列稀釋,共12個稀釋度,依次加樣於96孔板內的單層vero細胞上(100μl/孔),每個稀釋度重複3孔,設利巴韋林注射液原液為陽性對照,並設細胞對照、病毒對照。除細胞對照加100μl維持液外,各孔加100個tcid50的rsv病毒液100μl。置35℃、5%co2培養箱中培養,每日顯微鏡下觀察細胞病變,待病毒對照出現90%細胞病變後終止培養。鏡下觀察並記錄其cpe。應用reed-muench方法計算藥物半數有效濃度(ec50)(concentrationfor50%ofmaximaleffect,ec50)。根據上述藥物半數中毒濃度(tc50)及藥物半數有效濃度(ec50),計算藥物抑毒指數(ti)。
3實驗結果(見表3、圖4)
表3紫錐菊水提物d101型大孔樹脂洗脫物的抗病毒作用結果
4.討論
在洗脫過程中,為保證成分不損失,最初流出、未被大孔樹脂吸附部分也等體積分段收集;收集過程中設200ml為一個收集體,以保證更好的分離效果。表3中的洗脫物序號為抗病毒實驗驗證後,按順序將相鄰十個效果相近的收集段合併的結果。
圖表中結果顯示,水2、水3、水4、水5、水6的抑毒指數大於d101型大孔樹脂分離純化前的抑毒指數(ti=235),並且仍然優於利巴韋林(ti=32),說明用d101大孔吸附樹脂作為紫錐菊水煎煮提取物的分離純化方法切實可行。
縱觀本部分體外抗呼吸道合胞病毒結果發現,基本各洗脫部位的抗病毒效果均優於利巴韋林,針對這種情況有兩種猜想:①本實驗所採用的分離純化方法對活性成分的富集效果不理想;②紫錐菊中有多種抗呼吸道合胞病毒活性成分,並且強活性成分主要集中在大極性的水部位。本實驗無論符合哪種猜想,均說明,除優選出的效果集中部位外,其它洗脫部位仍有繼續開發的價值,不可忽視。
實驗四紫錐菊抗病毒有效成分的分析及結構鑑定
1實驗儀器與材料
1.1藥品取實驗三中水2、水3、水4、水5、水6合併,4000rpm離心15min,上清、沉澱分別100℃水浴揮幹,備用。
1.2試劑乙醇、乙酸丁酯、甲酸、磷酸(天津富宇精細化工有限公司產品,分析純);乙腈(tediacompany,禹王集團,色譜純);
1.3儀器pad紫外檢測器;高效液相色譜儀;agilent1260系列高效液相色譜儀(美國安捷倫公司,配有在線脫氣機,四元泵,自動進樣器,柱溫箱,二極體陣列檢測器);agilent6230tof質譜儀(美國安捷倫公司,配有標準電噴霧離子源,masshunlerdataacquisition在線工作站和qualiatiseanalysis離線分析軟體);cheetahtmmp100中壓快速純化製備系統(天津博納艾傑爾科技有限公司)。餘同實驗三。
2.實驗方法與結果
2.1檢測波長的選擇
取本實驗1.1中離心上清樣品適量,用蒸餾水稀釋至接近無色,經pad紫外檢測器全波長掃描,結果如圖5。
由圖5可知,pad的監測波長範圍為200~500,樣品的最大吸收波長為330nm,將其作為應用高效液相分析的參考條件。
2.2高效液相色譜檢測
2.2.1樣品處理取本章中離心上清樣品適量,超聲溶於超純水,0.45μm微孔濾膜濾過,得供試樣品,備用。
2.2.2色譜條件
查閱文獻並結合實驗摸索,確定樣品的hplc檢測條件為:syncronisc18色譜柱(250mm×4.6mm,5μm);柱溫35℃;流速1ml/min;檢測波長330nm;進樣量20μl;流動相條件乙腈(a)-0.3%磷酸溶液(b)=10(a):90(b),等度洗脫。
2.2.3hplc檢測結果
由圖6可知,d101大孔吸附樹脂分離所得樣品在2.2.2色譜條件下分離結果成分簡單,分離度好,因此將此樣品在半製備液相繼續純化精製。
2.3中壓快速製備色譜條件
本實驗採用sq230020-0flash球形aqc18(球形20~35μm,20g)色譜柱,在中壓快速製備液相上,以乙腈-0.3%磷酸作為流動相;流速:15ml/min;柱溫:室溫;收集波長:325nm。
表4快速製備液相的洗脫梯度
2.4化合物的製備
稱取1.1中的上清樣品0.0972g,於1ml蒸餾水中超聲溶解,進樣。按2.3項下的快速製備色譜條件製備,按峰收集製備產物,並編號。
將製備產物分別過0.45μm微孔濾膜,按2.2.2項下的色譜條件,進樣高效液相色譜進行檢測,得單峰物質,見圖7。
根據高效液相色譜檢測結果,合併譜圖相同組分,40℃恆溫水浴揮幹,得白色針狀結晶。2.5化合物的結構鑑定
菊苣酸對照品:esi-ms:492.1135[m+h2o]+,分子量374.1,分子式為c22h18o12。裂解電壓為100v時的碎片:135.0431,163.0384,224.1249,295.0446,325.0710,391.2831,492.1139,619.1109,767.1069,841.0523,922.0092,966.1917,1109.1847;裂解電壓為200v時的裂解碎片有:135.0441,163.0390,295.0454,378.9861,492.1132,569.0255,691.0268,767.1098,841.0469,922.0094,966.1924,1109.1796。如圖8所示。
相同實驗條件下,所得純品化合物的離解碎片:裂解電壓為100v時,碎片有:163.0389,224.1273,295.0450,325.0694,391.2831,457.0759,492.1135,619.1061,731.1020,841.0503,922.0093,966.1908,1111.1960;裂解電壓為200v時,碎片有:135.0441,163.0392,295.0469,378.9877,492.1126,619.1096,731.1036,841.0484,922.0099,966.1929,1111.1909。如圖9所示。與菊苣酸對照品的離解碎片基本一致,故可判斷所得到的白色針狀結晶為菊苣酸。
3純品化合物的體外藥效實驗
3.1藥物細胞毒性的測定
取製備純品,用細胞維持液溶解,過0.45μm微孔濾膜,做2倍比系列稀釋,共12個稀釋度,加樣於多孔板中已經長成單層的vero細胞上,每個稀釋度重複3孔,於37℃、5%co2培養箱中培養。24小時後顯微鏡下觀察病變情況,待病毒對照的病變率達到90%,終止培養,觀察並記錄細胞病變(cpe)百分率,應用reed-muench方法計算藥物半數中毒濃度(tc50)。3.2藥物對病毒致細胞病變作用的影響
取1.1中的上清樣品及製備純品適量,用細胞維持液溶解,過0.45μm微孔濾膜,用細胞維持液溶解並做2倍比系列稀釋,共12個稀釋度,依次加樣於96孔板內的單層vero細胞上(100μl/孔),每個稀釋度重複3孔,設利巴韋林注射液原液為陽性對照,並設細胞對照、病毒對照。除細胞對照加100μl維持液外,各孔加100個tcid50的rsv病毒液100μl。置35℃、5%co2培養箱中培養,每日顯微鏡下觀察細胞病變,待病毒對照出現90%細胞病變後終止培養。鏡下觀察並記錄其cpe。應用reed-muench方法計算藥物半數有效濃度(ec50)(concentrationfor50%ofmaximaleffect,ec50)。根據上述藥物半數中毒濃度(tc50)及藥物半數有效濃度(ec50),計算藥物抑毒指數(ti)。
3.3實驗結果(如表5、圖10所示)
表5紫錐菊製備純品抗病毒實驗結果
4.討論
本實驗中製備所得化合物菊苣酸對呼吸道合胞病毒所致細胞病變的抑制指數為4272,是製備前上清液的9倍,是陽性對照藥的256倍,抑毒效果突出,因此是體外抗呼吸道合胞病毒的有效成分。
由實驗三中圖4可知,體外抗病毒實驗優選出的水2、水3、水4、水5、水6部位的抗病毒效果差別較大,由於每個部位樣品量較少,為使後續實驗順利進行,本實驗中使用的樣品為各部位的合併物。
由於大孔樹脂洗脫物中仍有多糖、蛋白質、鞣質等大分子物質,本實驗採用離心後取上清的方式去除大分子雜質,以降低純化難度。
對比製備前樣品與製備產物的hplc圖譜發現,製得化合物為總樣品中的第4個峰,其在總樣中的含量最高,因此較易分得。
總結
本研究補充與完善了三種不同來源紫錐菊的性狀、顯微鑑別資料;建立了紫錐菊的體外抗病毒譜;通過體外藥理活性追蹤發現了活性成分菊苣酸。本研究的實驗成果為紫錐菊抗病毒的進一步研究及三種不同來源紫錐菊的準確使用提供了科學數據和資料。
本實驗在抗病毒活性成分的篩選工作中,採取了「篩選範圍由寬至窄、由淺入深、逐步鎖定目標」的實驗方案。首先選定具有不同遺傳物質的不同類型病毒,結合不同極性部位提取物做廣譜篩選,綜合分析篩選結果,確定效果最佳極性部位及病毒種類,進而以有效部位的分離、純化、精製作為跟蹤方向,以所選病毒的體外藥效作為篩選依據,層層推進,進而得到抗病毒活性物質。
當今針對呼吸道合胞病毒所引發疾病的治療並無特效藥,利巴韋林為臨床常用藥。本實驗中,選定利巴韋林為抗病毒實驗的陽性對照藥,雖然其體外抑制效果並不突出,但並不能否定其在臨床應用中的地位。為保證實驗結果的一致性,應繼續將利巴韋林作為考察菊苣酸抗病毒效果的陽性對照藥應用於體內藥理實驗,亦可考慮增添其它陽性對照藥。
紫錐菊中的菊苣酸是不穩定成分,其在紫錐菊的製劑商品中含量不穩定或並不存在,因此質量控制中常以多糖類成分或醯胺類成分作為質量標準。本實驗結果顯示,菊苣酸體外抑制rsv效果突出,表明其藥理活性得到了肯定,因而其在治療性藥物中的含量會對某些疾病的療效會產生一定影響。因此,在後續的體內藥理實驗中、在紫錐菊成方製劑的進一步研究中,針對菊苣酸的有效利用量及其作用效果,亦可做進一步考察。
在實現將紫錐菊用於人類病毒性疾病的治療過程中,仍然有藥材標準缺失、抗病毒活性成分不詳、抗病毒作用機理、靶點不清等問題橫亙眼前。因此對紫錐菊進行藥理活性研究、尋找可靠活性成分並進行全面質量評價是其在我國得到進一步開發應用的前提。
