豬圓環病毒II型口服病毒樣顆粒疫苗及其製備方法和應用與流程
2023-11-02 22:48:55 5
本發明涉及一種口服疫苗及其製備方法和應用,尤其涉及一種口服豬圓環病毒疫苗及其製備方法和應用
背景技術:
豬圓環病毒(Porcine circovirus,PCV)是迄今發現最小的動物病毒之一,屬於圓環病毒科圓環病毒屬,是無囊膜的單股環狀負鏈DNA病毒,20面體對稱,直徑17-20nm,已知PCV具有兩個血清型,即豬圓環I型病毒(PCV1)和豬圓環II型病毒(PCV2),其中,PCV 1為非致病性病毒,PCV2為致病性的病毒。
儘管豬圓環病毒基因組結構簡單,但對畜牧業的危害巨大,豬圓環病毒病是近幾年影響世界養豬業的最重要的病毒性傳染病之一。
我國豬圓環II型病毒(PCV2)的感染具有以下三大特徵:
1)感染率高,感染面廣:個體陽性率為21.7-87.3%,豬場陽性率為38.2-100%;
2)PCV2的感染率逐年上升:2003年為21.7%,2006年為38.3%,2008年為70.9%,2012年為83.2%;
3)PCV2與其他病原的混合感染嚴重:在感染PCV2病毒的血清中,經常能夠檢測到混合感染的藍耳病毒PRRSV、偽狂犬病毒PRV、細小病毒PPV、肺炎支原體、多殺性巴氏桿菌、流行性腹瀉病毒PEDV、豬流感病毒SIV等;有統計報導表明PCV2病毒二重感染率超過50%,與藍耳病毒PRRSV共感染率為51.9%、偽狂犬病毒PRV共感染率為62.44%、細小病毒PPV共感染率為56.9%。
更為嚴峻的是,我國養豬業中的PVC2已呈現感染日齡早(產房哺乳仔豬即可感染)的狀況。因此PCV2已被認為是世界養豬業的重要病原,能引起豬的免疫抑制,造成二重或者三重感染,發病率和死亡率高,給養豬業帶來重大危害、和嚴重的經濟損失。目前,PCV2疫苗已經成為繼豬瘟、口蹄疫、藍耳病和偽狂犬等疫苗後用量最大、用量最多的豬病疫苗品種,市場需求量大。
PCV2疫苗主要分為三類:全病毒滅活苗,PCV1-2重組病毒滅活疫苗,和類病毒顆粒亞單位疫苗。其中,PCV2亞單位疫苗(主要是類病毒顆粒疫苗),已經證實免疫效果要優於全病毒滅活苗,比滅活疫苗在安全性、有效性和製造工藝上都有了很大改進,正在成為新一代基因工程疫苗發展的新趨勢。
目前市場上銷售的PCV-2Cap蛋白類病毒顆粒疫苗有兩類:
A)一類是大腸桿菌製備的PCV2類病毒顆粒(原核表達),PCV-2的ORF2基因(Cap蛋白)插入大腸桿菌原核載體中去,利用大腸桿菌表達PCV-2Cap蛋白,製備亞單位疫苗。大腸桿菌表達系統具有生長速度快、易培養、表達蛋白產量高等特點,但其表達的蛋白大多以無活性的包涵體形式存在,經過蛋白變性復性等一系列操作後,可以得到可溶性蛋白。但是原核表達容易出現不具備活性的包涵體,需要進行蛋白復性來提高疫苗效果,成本高,生產周期長(每批次耗時約2-3個月)、效率低,獲得的蛋白免疫原性較差;特別是大腸桿菌表達的蛋白雖然經過純化,依然有可能殘留內毒素,免疫動物會產生副反應。
B)另一類由杆狀病毒/昆蟲細胞表達系統表達制PCV2類病毒顆粒疫苗由杆狀病毒/昆蟲細胞表達系統表達的類病毒顆粒(真核表達),用PCV-2的ORF2基因(Cap蛋白)插入到昆蟲杆狀病毒,用昆蟲細胞培養,獲得重組的PCV-2Cap蛋白,經純化、與免疫佐劑混合後獲得,在臨床上以注射方式免疫,真核表達的工藝要求較高,產品中可能會混有杆狀病毒顆粒,產生副反應,存在一定的生物安全風險。
另外,目前PCV2疫苗以注射為主,可用於口服的疫苗尚未見有報導。
技術實現要素:
針對目前PCV2疫苗存在的生產效率低、副反應大、不能口服等缺陷,本發明提供了一種可口服的PCV2疫苗。
本發明第一個方面是提供一種重組馬克斯克魯維酵母營養缺陷型菌株,由重組載體轉化馬克斯克魯維酵母營養缺陷型菌株製備。
所述重組載體通過將編碼豬圓環病毒衣殼蛋白(本發明下文中也稱為「豬圓環病毒衣殼蛋白Cap」或「Cap蛋白」)的核苷酸插入到馬克斯克魯維酵母表達載體所構建。
在一種優選實施例中,所述豬圓環病毒衣殼蛋白優選為豬圓環病毒II型病毒衣殼蛋白。
本發明第二個方面是提供一種製備所述豬圓環病毒II型病毒樣顆粒的方法,包括:
所述重組馬克斯克魯維酵母重組工程菌培養發酵,在細胞內組裝成豬圓環病毒II型病毒樣顆粒;
收集培養發酵的菌,獲得豬圓環病毒II型病毒樣顆粒。
或者所述方法還包括如下構建所述重組馬克斯克魯維酵母重組工程菌的步驟:
將編碼豬圓環病毒衣殼蛋白的核苷酸插入到馬克斯克魯維酵母表達載體,構建重組載體;
將重組載體轉化馬克斯克魯維酵母營養缺陷型菌株,構建得到所述重組馬克斯克魯維酵母重組工程菌。
在一種優選實施例中,所收集的培養發酵的菌,可以單獨作為豬圓環病毒II型病毒樣顆粒產品,或者破裂後收集釋放的病毒樣顆粒作為豬圓環病毒II型病毒樣顆粒產品,或破裂後的細胞破碎液或破碎液乾燥產物作為豬圓環病毒II型病毒樣顆粒產品。
本發明第三個方面是提供一種豬圓環病毒II型病毒樣顆粒口服藥物和/或疫苗,包括所述的豬圓環病毒II型病毒樣顆粒。
本發明第四個方面提供了一種製備豬圓環病毒II型病毒樣顆粒藥物和/或疫苗的方法,尤其是製備豬圓環病毒II型口服病毒樣顆粒藥物和/或疫苗(豬圓環病毒II型病毒引發的疾病的口服藥物和/或疫苗)的方法,包括以所收集的培養發酵的菌或破裂後獲得病毒樣顆粒,作為活性成分或作為活性成分之一,製備豬圓環病毒II型病毒樣顆粒疫苗。
在一種優選實施例中,收集菌體後,直接破壁,所得產物作為口服疫苗。
在一種優選實施例中,所收集的培養發酵的菌破裂後釋放病毒樣顆粒,加入保護劑製備豬圓環病毒II型病毒樣顆粒疫苗。
其中,所述保護劑可以是蔗糖、乳糖、海藻糖中的一種或多種。
在另一種優選實施例中,所收集的培養發酵的菌破裂後,將細胞破碎液噴霧乾燥製備豬圓環病毒II型病毒樣顆粒疫苗。
本發明第六個方面是提供一種所述豬圓環病毒II型病毒樣顆粒或豬圓環病毒II型病毒樣顆粒的應用,優選為製備預防和/或治療豬圓環病毒II型病毒引發的疾病的藥物和/或疫苗。
在一種優選實施例中,所述豬圓環病毒衣殼蛋白胺基酸序列包括(優選地,為):
1)SEQ ID No.1胺基酸序列;或
2)SEQ ID No.1胺基酸序列經過取代、缺失或添加一個或幾個胺基酸且具有豬圓環病毒核衣殼Cap蛋白活性的由SEQ ID No.1胺基酸序列衍生的蛋白質。
在一種優選實施例中,所述SEQ ID No.1所示豬圓環病毒衣殼蛋白中第226位苯丙氨酸被亮氨酸取代,如包括(並優選為):SEQ ID No.2胺基酸序列。
在一種優選實施例中,編碼所述豬圓環病毒衣殼蛋白的核苷酸系列包括、並優選為SEQ ID No.3所示序列
在一種優選實施例中,所述方法中,根據馬克斯克魯維酵母的密碼子偏好性,對編碼所述豬圓環病毒衣殼蛋白的核苷酸進行密碼子優化,更優選為在保證編碼豬圓環病毒衣殼蛋白序列相同的條件下進行密碼子優化。
在一種優選實施例中,所述馬克斯克魯維酵母表達載體包括馬克斯克魯維酵母菊粉酶啟動子基因和終止子基因序列,並優選為不含有無抗性基因序列、大腸桿菌起始複製序列。更優選地,所述馬克斯克魯維酵母表達載體包括、並優選組成為SEQ ID No.6所示核苷酸序列。
在一種優選實施例中,所述馬克斯克魯維酵母表達載體營養缺陷篩選標記基因。
在本發明的更一種優選實施例中,所述重組載體包括馬克斯克魯維酵母自主複製序列、馬克斯克魯維酵母菊粉酶啟動子基因序列、編碼豬圓環病毒衣殼蛋白的基因序列、馬克斯克魯維酵母菊粉酶終止子基因序列、營養缺陷篩選標記基因序列;更優選地,不含有無抗性基因序列、大腸桿菌起始複製序列。
本發明所述馬克斯克魯維酵母的營養缺陷型菌株,為馬克斯克魯維酵母敲除部分或全部特定營養基因所得。所述特定營養基因優選為選自URA3基因、HIS3基因、ADE2基因中的任意一種或幾種,並優選為URA3基因。
其中,在一種更優選實施例中,所述馬克斯克魯維酵母營養缺陷型菌株在Uracil營養缺陷培養基中不能生長。
在本發明的優選實施例中,上述的馬克斯克魯維酵母優選為CGMCC No.10621。該菌株保藏於中國微生物菌種保藏管理委員會普通微生物中心,保藏單位地址:北京市朝陽區北辰西路1號院3號中國科學院微生物研究所,保藏日期為2015年3月13日。
在本發明的一種優選實施例中,所述轉化可以是電轉化或化學轉化中的任意一種或幾種。
在本發明的一種優選實施例中,所述重組酵母培養所用培養基中含有葡萄糖、硫酸銨、硫酸鎂、磷酸二氫鉀。
其中,所述豬圓環病毒II型病毒樣顆粒或豬圓環病毒II型病毒樣顆粒疫苗優選為用於製備預防和/或治療豬圓環病毒II型病毒引發的疾病的藥物和/或疫苗。
所述應用優選為包括、但不限於用作口服疫苗、作為飼料添加劑、飲用水添加劑中的任意一種或幾種。
其中,所述豬圓環病毒II型病毒引發的疾病包括、但不限於斷奶仔豬多系統衰竭綜合症、豬皮炎腎病綜合症、仔豬先天性震顫和母豬繁殖障礙中的任意一種或幾種。
在本發明的一種優選實施例中,所述任意疫苗可以是優選為固體製劑、液體製劑、半固體製劑、氣體製劑中的任意一種或幾種,並優選為固體製劑。
其中,所述任意疫苗可以是、但不限於乾粉、顆粒、片劑、膠囊、膏劑、氣霧劑、噴霧劑、溶液、懸液、乳液中的任意一種或幾種。
在本發明的一種優選實施例中,所述任意疫苗也可以包括輔料,輔料優選為可以是、但不限於矯味劑、防腐劑、保溼劑、崩解劑、潤滑劑、潤溼劑、填充劑、粘合劑或抗粘結劑、助懸劑、顏料、釋放阻滯劑、稀釋劑、增溶劑、溶劑、絮凝劑或反絮凝劑、消泡劑或發泡劑、增稠劑、增塑劑、緩衝劑、pH值調節劑、乳化劑中的任意一種或幾種。
在本發明的一種優選實施例中,所述任意疫苗也可以包括佐劑,佐劑優選為可以是、但不限於水包油、油包水、水包油包水佐劑中的任意一種或幾種。
本發明上述各個方面以及各個實施例可以由本領域技術人員進行相互組合,各種組合也在本發明內容的範圍之內。
本發明提供的豬圓環病毒II型病毒樣顆粒或豬圓環病毒II型病毒樣顆粒疫苗、優選為口服疫苗,能夠減少和預防感染PCV2所引起相關性臨床症狀,具有可口服、免疫效果好、安全性高、培養操作簡單,產量高、生產成本低以及可大規模放大生產等優點。
附圖說明
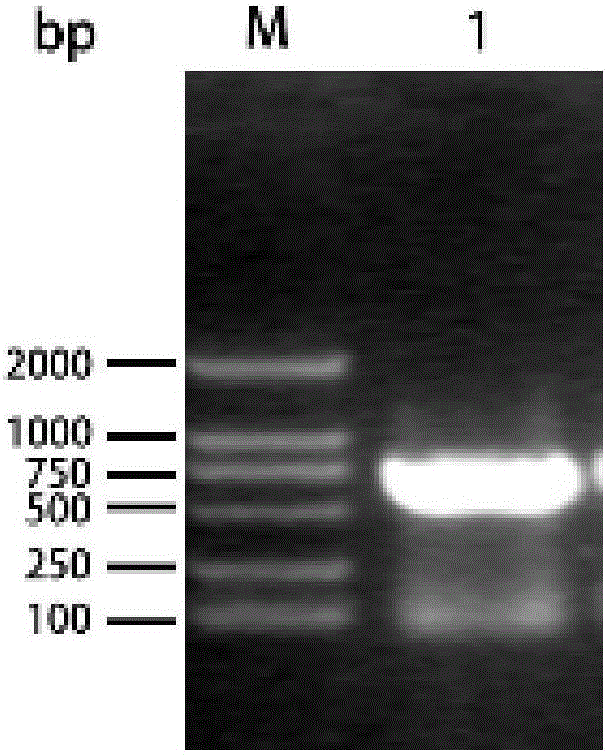
圖1為Cap基因的PCR擴增DNA電泳圖;
圖2為Cap蛋白馬克斯克魯維酵母重組載體pUKD-N125/Cap示意圖;
圖3為豬圓環病毒II Cap蛋白在馬克斯克魯維酵母中的表達;其中,泳道1:Fim-1ura3Δ;泳道2:Fim-1ura3Δ-pUKD-N125/Cap重組酵母全細胞裂解液;泳道3:Fim-1ura3Δ-pUKD-N125/Cap重組酵母解液上清;
圖4為馬克斯克魯維酵母表達豬圓環病毒II Cap蛋白的免疫印跡Western Blot檢測達;其中,泳道1:Fim-1ura3Δ;泳道2:Fim-1ura3Δ-pUKD-N125/Cap重組酵母;
圖5為馬克斯克魯維酵母表達PCV病毒樣顆粒電子顯微鏡觀察;
圖6為Fim-1ura3Δ-pUKD-N125/Cap重組酵母中試發酵生長曲線;
圖7為Fim-1ura3Δ-pUKD-N125/Cap重組酵母中試發酵過程中相同菌量下Cap蛋白表達水平;
圖8為口服圓環病毒疫苗與注射進口疫苗免疫小鼠後血清中Cap IgG抗體水平比較;
圖9為小鼠餵食口服圓環病毒疫苗的糞便中產生的Cap IgA抗體水平。
具體實施方式
實施例1,PCV衣殼蛋白重組表達載體pUKD-N125/Cap的構建
本實施例中,編碼豬圓環病毒衣殼蛋白(上下文中也稱為「豬圓環病毒衣殼Cap蛋白」、或「Cap蛋白」)的胺基酸序列的基因具有SEQ ID No.3的序列。根據馬克斯克魯維酵母的密碼子偏好性,對Cap基因序列進行密碼子優化,並將優化後的Cap基因序列進行人工合成。
所編碼的Cap蛋白胺基酸序列可以是如SEQ ID No.1所示,或者SEQ ID No.1中226位的苯丙氨酸由亮氨酸替代(如SEQ ID No.2)。
利用PCR擴增的方法,以PCVN125-F(5'-TTTTTTTGTTAGATCCGCGGATGACATATCCAAGGAGGCGTTTC-3')和PCVN125-R(5'-AGCTTGCGGCCTTAACTAGTTCA CTTAGGGTTAAGTGGAGGGTCCTTAAG-3')為引物擴增Cap基因。經1%瓊脂糖凝膠電泳後用DNA凝膠試劑盒回收700kb左右的片段(如圖1)。
提供pUKD-N125載體(SEQ ID No.6),該載體由PUKD-N118載體(參照中國發明專利申請201510562564.9實施例中PUKDN118)構建,構建方法如下:
正向引物5'-ACTAGTTAAGGCCGCAAGCTTTGATCTGATCTGC-3'和反向引物5'-TCCCCCGCGGATCTAACAAAAAAAAAATTAAATG-3'對PUKDN118質粒進行PCR擴增,擴增片段中包括了菊粉酶終止子、KmURA3啟動子、KmURA3ORF、酵母自主複製序列和菊粉酶啟動子;
利用Taq酶多擴增片段進行加A處理,然後將回收產物與PMD18-T載體連接;測序後,SacII和SpeI進行酶切得到pUKD-N125載體。
pUKD-N125載體中,包括馬克斯克魯維酵母自主複製序列、馬克斯克魯維酵母菊粉酶啟動子序列、馬克斯克魯維酵母菊粉酶終止子序列、馬克斯克魯維酵母的營養缺陷篩選標記基因URA3(KmURA3ORF),不含有大腸桿菌序列。
採用Sac II和Spe II兩個限制性酶切pUKD-N125載體,1%瓊脂糖凝膠電泳,用DNA凝膠試劑盒回收8kb左右的載體片段
Cap基因片段與載體片段的連接採用Gibson Assembly的方法,用NEB公司的Gibson Assembly無痕連接系統(產品編號E2611S/L),構建重組載體pUKD-N125/Cap,如圖2所示,編碼Cap蛋白的基因序列(PCV2CAP)插入到載體內。
實施例2,PCV衣殼蛋白Cap蛋白在馬克斯克魯維酵母基因工程菌Fim-1ura3Δ-pUKD-N125/Cap的構建及Cap表達分析
提供馬克斯克魯維酵母尿嘧啶營養缺陷型菌株Fim-1ura3Δ,該菌株的製備方法可參考中國專利公布文件CN105112313A實施例1公開的Fim-1(ura3Δ)的菌株的構建方法。
Fim-1ura3Δ接種於含3mL YEPD培養基的玻璃試管中,30℃搖床過夜培養至OD600為12-15。收集菌體,LiAc-TE溶液(100mM LiAc,10mM Tris-HCl,1mM EDTA)洗滌。
在菌體中依次加入carrier DNA,重組載體pUKD-N125/Cap,PEG溶液(40%PEG 4000、100m M LiAc、10mM Tris-HCl pH 7.5、1mM EDTA)和終濃度為10mM DTT,充分混勻後,30℃水浴15min,47℃水浴15min,8000rpm瞬離,棄上清,加100μL無菌水懸浮菌體,塗SD平板(0.67%無氨基酵母氮源YNB、2%葡萄糖、2%瓊脂),30℃培養2-4天直至克隆形成。
重組菌的鑑定通過提取基因組,用Cap基因特異性PCVN125-F和PCVN125-R引物進PCR驗證,擴增出700bp左右的條帶的為陽性克隆,即為轉入pUKD-N125/Cap重組載體的基因工程菌Fim-1ura3Δ-pUKD-N125/Cap。
實施例3,馬克斯克魯維酵母基因工程菌Fim-1ura3Δ-pUKD-N125/Cap表達Cap蛋白及病毒樣顆粒的組裝
PCR驗證陽性的克隆接種於裝有50ml的YP培養基(1%酵母抽提物(Yeast Extract),2%葡萄糖)的三角搖瓶中,30℃、220rpm培養96h後離心收集細胞,採用高壓均質的方法破碎細胞,細胞裂解液進行聚丙烯醯胺凝膠蛋白電泳SDS-PAG(polyacrylamide gel electrophoresis,PAGE)和PCV抗體免疫印跡Western Blot檢測豬圓環病毒(PCV)Cap蛋白在克魯維酵母的表達。
與對照菌Fim-1ura3Δ(第1泳道)對比,基因工程菌Fim-1ura3Δ-pUKD-N125/Cap的全細胞裂解液及上清(第2和第3泳道)中35-40kD大小多了一條蛋白條帶(如圖3),該蛋白條帶是豬圓環病毒的Cap蛋白,並且獲得了可溶性表達。
進一步利用Western Blot驗證Fim-1ura3Δ-pUKD-N125/Cap表達的Cap蛋白。實驗步驟如下:將細胞裂解液樣品經蛋白質電泳SDS-PAGE後,使用Bio-Rad公司的Trans-Blot將蛋白轉移至硝酸纖維素膜上(220mA,100min),然後將膜在含5%的脫脂奶粉的TBST緩衝液(20mM Tris-HCl pH 8.0、137mM NaCl、0.1%Tween 20)中的室溫孵育2h,抗PCV抗體豬血清多抗1︰400稀釋,4度過夜孵育後,TBST洗3遍,羊抗豬HRP酶標二抗1︰2500倍稀釋,室溫孵育1.5h,TBST洗3遍後,加入豬圓環病毒抗體A、B等量混合的顯色液,觀察結果。
結果:Fim-1ura3Δ(第1泳道)沒有免疫印跡條帶,而Fim-1ura3Δ-pUKD-N125/Cap樣品(第2泳道)中25-35kD的條帶免疫印跡,與Cap蛋白的理論分子量28kD基本一致,證實蛋白條帶為圓環病毒的Cap蛋白(圖4)。
利用電子顯微鏡成像技術,觀察Fim-1ura3Δ-pUKD-N125/Cap表達圓環病毒的Cap蛋白是否完成自我組裝成病毒樣顆粒VLPs,發現搖瓶培養92h後Fim-1ura3Δ-pUKD-N125/Cap存在大小約17-20nm左右的病毒顆粒(如圖5)。
實施例4,馬克斯克魯維酵母基因工程菌Fim-1ura3Δ-pUKD-N125/Cap發酵與口服疫苗的製備
馬克斯克魯維酵母基因工程菌Fim-1ura3Δ-pUKD-N125/Cap在5升的發酵罐中進行高密度發酵,利用合成培養基(含葡萄糖、硫酸銨、硫酸鎂、磷酸二氫鉀等成分),通過流加補料發酵,發酵48h後菌體密度OD600達271(如圖6),生物量達102g/L(細胞乾重),通過電泳檢測與灰度掃描,PCV2Cap蛋白的產量達2g/L(如圖7)。
發酵48小時後收集菌體,用去離子水洗滌3次,用磷酸緩衝液PBS重懸後,採用高壓均質的方法破碎細胞,加入保護劑蔗糖或直接噴霧乾燥制的口服豬圓環病毒II型口服病毒樣顆粒疫苗。
實施例5,口服馬克斯克魯維酵母製備的圓環病毒疫苗免疫小鼠
選用6周齡健康雌性SPF級Balb/c小鼠,隨機分組,每組各7隻。第一組為空白組,餵食PBS(PBS)不做免疫;第二組為對照組,注射進口某公司圓環病毒II型疫苗(0.3mL/只),第三組為免疫組:餵食本發明提供的豬圓環病毒II型口服病毒樣顆口服疫苗(KM口服),每隻小鼠餵食劑量100μg Cap蛋白/次,首免1周後,按相同途徑和劑量重複餵食4次(餵食時間:0天、7天、14天、21天、28天)。
餵食前小鼠眼眶後靜脈叢取血,採取的血液放到37度培養箱中1h,然後4℃、3000rpm離心4min,用10μl的移液器吸取血清到新的EP內,放-20℃冰箱保存。採集的糞便稱重,加入十倍的TBST(含有0.01%的疊氮化鈉),渦旋振蕩混勻後,14000rpm離心10min,取上清於新的EP管內,做好標記,放-20℃冰箱。
小鼠血清中抗PCV cap IgG抗體的含量的檢測採用武漢科前生物製品有限公司豬圓環病毒II型ELISA抗體檢測試劑盒,檢測步驟如下:
1)取抗原包被板,每孔加入TBST 200ul,靜止3min後倒掉,在吸水紙上拍幹,洗滌兩次。
2)加入1︰100稀釋的待檢血清,37度培養箱內靜止45min。
3)棄去孔中的樣品,用吸水紙拍幹後加入200ul TBST,靜止3min後倒掉,拍幹,共計洗滌5次。
4)每孔加入1︰33000稀釋的羊抗鼠IgG酶標二抗,37度靜置30min。
5)棄去板中的液體,清洗,方法同3)
6)加入100ul等量混合的底物液A和B,室溫下避光顯色10min。
7)每孔中加入硫酸反應終止液50ul,用酶標儀檢測450nm下的吸光值。
小鼠餵食本發明製備的口服圓環病毒II型疫苗2周血清中產生抗體,小鼠血清產生抗PCV Cap IgG抗體(如圖8)。免疫6周後,小鼠血清中的PCV Cap IgG抗體達到峰值,平均滴度達到10000以上,與進口注射疫苗(純化PCV Cap蛋白)抗體水平相當,但本發明更早產生抗體。此外,口服本發明提供的圓環病毒疫II型疫苗產生的抗體能持續20周以上,並且抗體滴度保持在10000以上,說明本發明製備的口服圓環病毒具有很好的免疫效果。
糞便中抗PCV Cap IgA抗體含量的檢測採用酶標二抗使用羊抗鼠IgAα鏈-HRP(英國abcam公司,貨號ab97235),操作方法同血清中抗PCV Cap IgG抗體的檢測。參照圖9,小鼠餵口服本發明圓環病毒疫苗(KM口服)28和35天後,糞便中的IgA抗體顯著高於空白對照組(PBS),說明本發明製備的圓環病毒口服疫苗能顯著提高小鼠的黏膜免疫效果,產生PCV Cap IgA抗體。
以上對本發明的具體實施例進行了詳細描述,但其只是作為範例,本發明並不限制於以上描述的具體實施例。對於本領域技術人員而言,任何對本發明進行的等同修改和替代也都在本發明的範疇之中。因此,在不脫離本發明的精神和範圍下所作的均等變換和修改,都應涵蓋在本發明的範圍內。
