一種芹菜籽提取物及其製劑和製法的製作方法
2023-10-08 11:29:49 5
本發明屬於藥物製劑領域,特別涉及一種芹菜籽提取物及其製劑和製法。
背景技術:
芹菜籽,為傘形科植物芹菜Apium graveolens L.的種子,芹菜籽治療關節疼痛在澳洲已有百年的歷史,被視為傳統民間偏方,芹菜籽提取物具有降尿酸、降血壓、血脂等多種功效,以降尿酸的功效最為顯著。國內大多數研究人員針對芹菜的根、莖、葉提取物及芹菜籽精油進行相關的研究和報導,但較少涉及到芹菜籽提取物的相關研究;中國專利CN100569241C公開了一種芹菜籽乙酸乙酯萃取物,製備方法如下:芹菜乾燥種子10kg,以15~20倍量75~95%(V/V)乙醇滲漉提取或以4~5倍量75~95%(V/V)乙醇加熱提取3~4次,每次加熱1~1.5小時;提取液於55℃減壓濃縮至近無乙醇,得濃縮液;於濃縮液中加1~2倍量水稀釋混懸後,用稀釋液三分之一體積的60~90℃沸程的石油醚,萃取2~3次,分出石油醚層並回收石油醚,得石油醚萃取物;水層再用三分之一體積乙酸乙酯萃取4次,分出乙酸乙酯層並回收乙酸乙酯得芹菜籽乙酸乙酯萃取物,並公開所述提取物用於製備防治痛風藥物、抗炎藥物或保健食品藥物中的應用。現有芹菜籽提取物的提取方法存在提取步驟複雜、生藥率低、基本沒有精製方法、重複性差等諸多不足,難以工業化生產。
技術實現要素:
本發明的特徵在於提供一種芹菜籽提取物及其製備方法,得到的芹菜籽提取物具有較佳的藥學性能,能有效降低尿酸;製備方法工藝簡單,產率高,重現性好。
為實現上述目的,本發明具體技術方案如下:
一種芹菜籽提取物,所述芹菜籽提取物的製備方法如下:
a.取芹菜乾燥種子,粉碎,加入體積分數為95%的乙醇水溶液回流提取1-2次,每次加入乙醇水溶液為芹菜乾燥種子2-4倍體積量,回流時間為0.5-1.5h;收集並合併提取液,減壓濃縮至無醇,得稠浸膏;
b.將步驟a所得的稠浸膏混懸於芹菜乾燥種子0.5-1倍體積的水中,然後用萃取試劑萃取2-4次,每次加入萃取試劑量為稠浸膏0.2-0.4倍體積量,萃取完畢後合併有機相,乾燥,減壓濃縮,得芹菜籽提取物;
其中,所述萃取試劑選自:乙酸乙酯、二氯甲烷、石油醚、正己烷中的一種或幾種。
優選地,所述製備方法還包括如下精製方法:
c.將粗提物以0.2-0.5g/ml的濃度溶於乙酸乙酯中,上矽膠層析柱;
d.梯度洗脫:洗脫流量為7-10ml/min,先用石油醚洗脫8-10個柱體積,除去流分;再用體積比為7:1的石油醚和二氯甲烷混合液洗脫10-12個柱體積,收集流分;再用體積比為9:4:1的石油醚、二氯甲烷和乙酸乙酯的混合液洗脫3-5個柱體積,除去流分;再用體積比為5:7:3的石油醚、二氯甲烷和乙酸乙酯的混合液洗脫15-20個柱體積,收集流分,將收集的流分合併,減壓濃縮,即得精製芹 菜籽提取物。
本發明所提供的芹菜籽提取物,在降低尿酸方面具有非常好的效果,有利於對高尿酸血症的治療和人腎臟的保護。
另一方面,提供了一種芹菜籽提取物的製備方法,所述製備方法具體步驟如下:
a.取芹菜乾燥種子,粉碎,加入體積分數為95%的乙醇水溶液回流提取1-2次,每次加入乙醇水溶液為芹菜乾燥種子2-4倍體積量,回流時間為0.5-1.5h;收集並合併提取液,減壓濃縮至無醇,得稠浸膏;
b.將步驟a所得的稠浸膏混懸於芹菜乾燥種子0.5-1倍體積的水中,然後用萃取試劑萃取2-4次,每次加入萃取試劑量為稠浸膏0.2-0.4倍體積量,萃取完畢後合併有機相,乾燥,減壓濃縮,得粗提物;
其中,所述萃取試劑選自:乙酸乙酯(EA)、二氯甲烷(DCM)、石油醚(PE)或正己烷(Hex)中的一種或幾種;優選地為質量比為1:1-1:4的乙酸乙酯和正己烷的混合液,進一步優選,乙酸乙酯和正己烷的質量比為1:2;
c.將粗提物以0.2-0.5g/ml的濃度溶於乙酸乙酯中,上矽膠層析柱;
d.梯度洗脫:洗脫流量為7-10ml/min,優選為8ml/min;先用石油醚洗脫8-10個柱體積,除去流分;再用體積比為7:1的石油醚和二氯甲烷混合液洗脫10-12個柱體積,收集流分;再用體積比為9:4:1的石油醚、二氯甲烷和乙酸乙酯的混合液洗脫3-5個柱體積,除去流分;再用體積比為5:7:3的石油醚、二氯甲烷和乙酸乙酯的混合液洗脫15-20個柱體積,收集流分,將收集的流分合併,減壓濃縮, 即得所述芹菜籽提取物。
進一步地,為了提高產物收率,在回流提取步驟設有超聲波輔助,所述超聲波頻率為60-80KHz。
本發明所提供的芹菜籽提取物的製備方法,經過大量實驗、合理的統籌和對比總結而出,具有工藝簡單、提取次數少、藥物產率高、條件溫和等優點;所述純化精製步驟合理,純化產率較高,經過該純化步驟後所得的芹菜籽提取物中包含的活性成分較現有技術提高12-15%,可適於工業化生產。
另一方面,本發明還提供了芹菜籽提取物與藥學上可接受的輔料製成的軟膠囊劑,所述軟膠囊包括軟膠囊填充物和囊材,所述軟膠囊填充物包括如下重量份的原料:芹菜籽提取物10-25份、稀釋劑20-35份、崩解劑3-6份、粘合劑1-2份。
優選地,所述稀釋劑為重量份數比為2:3的N-十二烷胺木糖甙和麻油的混合物;所述崩解劑為重量份數比為1:2:2的交聯聚維酮、月桂醇硫酸鈉和月桂醯肌氨酸的混合物。
進一步優選地,所述囊材主要由如下重量份數的原料製備而成,明膠10、醋酸纖維素酞酸酯1.2、出芽短梗孢糖0.8、水10、二氧化鈦2.8、半乳糖1.9。
本發明所提供的軟膠囊劑,各輔料與芹菜在提取物之間無反應,且能提高膠囊劑內芹菜籽提取物的生物利用度,充分發揮膠囊劑的療效,且含量均勻度高;經過嚴格篩選輔料的種類和工藝參數,選取了上述原料製備形成的囊材,與芹菜籽提取物相配合,解決了藥物遇溼熱不穩定的問題,進一步保證膠囊劑的穩定性,使芹菜籽提取物的穩定性進一步增加。
另外,本發明還提供芹菜籽提取物在製備降低尿酸的藥物中的應用。
本發明所述的芹菜籽提取物,在降低尿酸方面具有非常好的效果,有利於對高尿酸血症的治療和人腎臟的保護;此外,本發明所提供的芹菜籽提取物的製備方法,經過大量實驗、合理的統籌和對比總結而出,具有工藝簡單、提取次數少、藥物產率高、條件溫和等優點,為芹菜籽提取物的可工業化生產提供了較優的選擇;本發明將芹菜籽提取物與輔料製備成軟膠囊劑,不但提高了患者的攜帶和使用的方便性,且優化輔料配方,提高芹菜籽提取物的生物利用度,增強芹菜籽提取物及軟膠囊的穩定性;使膠囊的貯存條件變得更加溫和。
附圖說明
圖1回流時間對產率的影響圖;
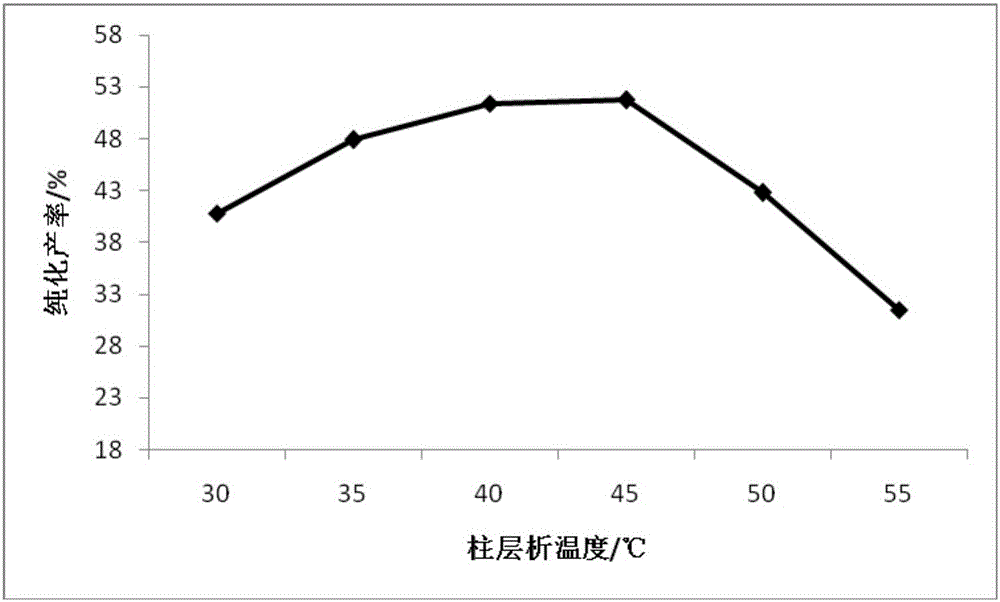
圖2柱層析溫度對柱層析產率的影響圖。
具體實施方式
實施例1
一種芹菜籽提取物,由下述步驟製備而得:
a.取芹菜乾燥種子,粉碎,加入2倍體積量的體積分數為95%的乙醇水溶液回流提取1.5h;收集提取液,減壓濃縮至無醇,得稠浸膏;
b.將步驟a所得的稠浸膏混懸於原料1倍體積的水中,然後用體積比為3:1的石油醚和乙酸乙酯的混合液萃取2次,每次加入萃取試劑量為原料0.2倍體積量,萃取完畢後合併有機相,乾燥,減壓濃縮,得芹菜籽提取物;
實施例2
一種芹菜籽提取物,由下述步驟製備而得:
a.取芹菜乾燥種子,粉碎,加入體積分數為95%的乙醇水溶液回流提取2次,每次加入乙醇水溶液為2.5倍體積量,回流時間為0.5h,收集並合併提取液,減壓濃縮至無醇,得稠浸膏;
b.將步驟a所得的稠浸膏混懸於原料0.5倍體積的水中,然後乙酸乙酯或二氯甲烷萃取4次,每次加入萃取試劑量為原料0.4倍體積量,萃取完畢後合併有機相,乾燥,減壓濃縮,得粗提物;
c.將粗提物以0.2g/ml的濃度溶於乙酸乙酯中,上矽膠層析柱;
d.梯度洗脫:洗脫流量為7ml/min,先用石油醚洗脫10個柱體積,除去流分;再用體積比為7:1的石油醚和二氯甲烷混合液洗脫12個柱體積,收集流分;再用體積比為9:4:1的石油醚、二氯甲烷和乙酸乙酯的混合液洗脫3個柱體積,除去流分;再用體積比為5:7:3的石油醚、二氯甲烷和乙酸乙酯的混合液洗脫15個柱體積,收集流分,將收集的流分合併,減壓濃縮,即得芹菜籽提取物。
實施例3
一種製備芹菜籽提取物的製備方法,所述製備方法步驟如下:
a.提取:取芹菜乾燥種子,粉碎,加入4倍體積量的體積分數為95%的乙醇水溶液回流提取1h,同時進行超聲波輔助;收集提取液,減壓濃縮至無醇,得稠浸膏;
b.萃取:將步驟a所得的稠浸膏混懸於原料0.9倍體積的水中,然後用質量比為1:2的乙酸乙酯和正己烷的混合溶液萃取3次,每次加入萃取試劑量為原料0.3倍體積量,萃取完畢後合併有機相,乾燥,減壓濃縮即得所述芹菜籽提取物;
c.將粗提物以0.5g/ml的濃度溶於乙酸乙酯中,上矽膠層析柱;
d.梯度洗脫:洗脫流量為10ml/min,先用石油醚洗脫8個柱體積,除去流分;再用體積比為7:1的石油醚和二氯甲烷混合液洗脫10個柱體積,收集流分;再用體積比為9:4:1的石油醚、二氯甲烷和乙酸乙酯的混合液洗脫5個柱體積,除去流分;再用體積比為5:7:3的石油醚、二氯甲烷和乙酸乙酯的混合液洗脫20個柱體積,收集流分,將收集的流分合併,減壓濃縮,即得芹菜籽提取物。
實施例4
一種製備芹菜籽提取物的製備方法,所述製備方法步驟如下:
a.提取:取芹菜乾燥種子,粉碎,加入4倍體積量的體積分數為95%的乙醇水溶液回流提取1h,同時進行超聲波輔助;收集提取液,減壓濃縮至無醇,得稠浸膏;
b.萃取:將步驟a所得的稠浸膏混懸於原料0.9倍體積的水中,然後用質量比為1:2的乙酸乙酯和正己烷的混合溶液萃取3次,每次加入萃取試劑量為原料0.3倍體積量,萃取完畢後合併有機相,乾燥,減壓濃縮即得所述芹菜籽提取物;
c.將粗提物以0.5g/ml的濃度溶於乙酸乙酯中,上矽膠層析柱;
d.梯度洗脫:洗脫流量為8ml/min,先用石油醚洗脫9個柱體積,除去流分;再用體積比為7:1的石油醚和二氯甲烷混合液洗脫11個柱體積,收集流分;再用體積比為9:4:1的石油醚、二氯甲烷和乙酸乙酯的混合液洗脫4個柱體積,除去流分;再用體積比為5:7:3的石油醚、二氯甲烷和乙酸乙酯的混合液洗脫17個柱體積,收集流分,將收集的流分合併,減壓濃縮,即得芹菜籽提取物。
實施例5軟膠囊劑
軟膠囊填充物:
囊材:
製備方法:
1)將明膠、水、半乳糖和醋酸纖維素酞酸酯常規混合併加熱熔融成膠液後,加入二氧化鈦和出芽短梗孢糖混合均勻後,過膠體磨後壓製成膠皮待用;
2)將實施例2所製備的芹菜籽提取物、N-十二烷胺木糖甙、麻油和三分之二的交聯聚維酮、月桂醇硫酸鈉和月桂醯肌氨酸混合物混合均勻後,粉碎成微粉待用;將聚維酮溶於75%體積分數的乙醇水溶液中形成溶液,將微粉溶於溶液中混合均勻,然後製成溼丸,將溼丸與剩餘交聯聚維酮、月桂醇硫酸鈉和月桂醯肌氨酸混合物混合均勻,乾燥後得微丸;
3)將微丸與步驟1)所得的膠皮壓制,即得軟膠囊劑。
實施例6軟膠囊劑
軟膠囊填充物:
囊材:
製備方法:按照實施例4所述的製備方法進行製備。
實施例7軟膠囊劑
軟膠囊填充物:
囊材:
製備方法:按實施例4所述的方法進行製備。
對照實施例1軟膠囊劑
軟膠囊填充物:
囊材:
製備方法:
1)將明膠、水和半乳糖常規混合併加熱熔融成膠液後,加入二氧化鈦混合均勻後,過膠體磨後壓製成膠皮待用;
2)將實施例2所製備的芹菜籽提取物、N-十二烷胺木糖甙、麻油和三分之二的交聯聚維酮、月桂醇硫酸鈉和月桂醯肌氨酸混合物混合均勻 後,粉碎成微粉待用;將聚維酮溶於75%體積分數的乙醇水溶液中形成溶液,將微粉溶於溶液中混合均勻,然後製成溼丸,將溼丸與剩餘交聯聚維酮、月桂醇硫酸鈉和月桂醯肌氨酸混合物混合均勻,乾燥後得微丸;
3)將微丸與步驟1)所得的膠皮壓制,即得軟膠囊劑。
對照實施例2軟膠囊劑
軟膠囊填充物:
囊材:
製備方法:
1)將明膠、水和甘油常規混合併加熱熔融成膠液後,加入二氧化鈦混合均勻後,過膠體磨後壓製成膠皮待用;
2)將實施例2所製備的芹菜籽提取物、山梨醇和海藻酸混合均勻後,粉碎成微粉,將甲基纖維素溶於75%體積分數的乙醇水溶液中形成溶液,將微粉溶於溶液中混合均勻,然後製成溼丸,將溼丸與羧甲基纖素鈉混合均勻,乾燥後得微丸;
3)將微丸與步驟1)所得的膠皮壓制,即得軟膠囊劑。
試驗1芹菜籽提取物降高尿酸血症的藥效研究
1實驗方法
(1)芹菜籽提取物對正常小鼠血清尿酸的影響:ICR小鼠72隻,SPF級,雌雄各半,體重18.2~22.9g,按性別、體重隨機分為6組,分別為空白對照組、別嘌醇片組(39mg/kg)、中國專利CN 100569241中公開的芹菜籽乙酸乙酯萃取物作為陽性對照組(3.3g芹菜籽/kg)、芹菜籽提取物低、中、高劑量組(3.3、9.9、29.7g芹菜籽/kg),每組12隻動物。各組小鼠按20mL/kg灌胃給予相應劑量的藥液,空白對照組灌胃給予等體積花生油,1次/日,連續14天。末次給藥前禁食不禁水12h,末次給藥後1h,各組小鼠眼眶靜脈叢採血,檢測血清尿酸水平。
(2)芹菜籽提取物對氧嗪酸鉀鹽所致小鼠高尿酸血症模型的影響:ICR小鼠70隻,SPF級,雄性,體重24.1~27.9g,按體重隨機分為7組,分別為正常對照組、模型對照組、別嘌醇片組(39mg/kg)、中國專利CN100569241中公開的芹菜籽乙酸乙酯萃取物作為陽性對照組(9.9g/kg),芹菜籽提取物低、中、高劑量組(3.3、9.9、29.7g/kg),每組10隻動物。各組小鼠按20mL/kg灌胃給予相應劑量的藥液,正常對照組灌胃給予等體積蒸餾水,模型對照組灌胃給予等體積花生油,1次/日,連續7天。末次給藥前禁食不禁水12h,給藥前1h,除正常對照組外,其餘各組小鼠腹腔注射液氧嗪酸鉀鹽300mg/kg,各組小鼠分別於造模前及末次給藥1h後,眼眶靜脈叢採血,檢測血清尿酸水平,結果見表1。
(3)芹菜籽提取物對腺嘌呤和乙胺丁醇所致大鼠高尿酸血症模型的影響:SD大鼠70隻,SPF級,雄性,體重198.4~228.4g,按體重隨機分為正常對照組、模型對照組、別嘌醇片組(27mg/kg)、中國專利CN100569241中公開的芹菜籽乙酸乙酯萃取物作為陽性對照組(5.1g/kg),芹菜籽提取物低、中、高劑量組(1.7、5.1、15.3g/kg), 每組10隻動物。各組大鼠按10mL/kg灌胃給予相應劑量的藥液,正常對照組灌胃給予等體積蒸餾水,模型對照組灌胃給予等體積花生油,1次/日,連續17天。除正常對照組外,其餘各組大鼠均於給藥第10天上午開始灌胃腺嘌呤(300mg/kg)和乙胺丁醇(250mg/kg),複製大鼠高尿酸血症模型,下午按10mL/kg灌胃給予相應藥液。末次給藥前禁食不禁水12h,末次給藥後1h,各組大鼠眼眶靜脈叢採血,檢測血清尿酸水平,結果見表2。
2實驗結果
表1芹菜籽提取物對氧嗪酸鉀鹽所致小鼠高尿酸血症模型的影響
註:與陽性對照組相比Pa<0.05,Pb<0.01,與別嘌醇片組相比Pc<0.05.
表2芹菜籽提取物對腺嘌呤和乙胺丁醇所致大鼠高尿酸血症模型的影響
註:與陽性對照組相比Pa<0.05,Pb<0.01,與別嘌醇片組相比Pc<0.05.
(1)芹菜籽提取物對正常小鼠血清尿酸的影響:小鼠連續14天灌胃給予不同劑量的芹菜籽提取物(3.3、9.9、29.7g/kg),其中低劑量芹菜籽提取物就能顯著降低正常小鼠血清尿酸水平。
(2)芹菜籽提取物對氧嗪酸鉀鹽所致小鼠高尿酸血症模型的影響:連續給藥7天,小鼠採用腹腔注射氧嗪酸鉀複製高尿酸血症模型,造模後小鼠血清UA顯著升高;芹菜籽提取物低、中、高劑量(3.3、9.9、29.7g/kg)均能顯著降低小鼠造模後血清UA水平,且造模後低、中、高劑量均能顯著減小造模後小鼠血清UA升高程度,低劑量組與陽性對照組相比具有差異性,中劑量組與高劑量組與陽性對照組相比具有顯著差異性,高劑量組與現有別嘌醇片相比效果更優。
(3)芹菜籽提取物對腺嘌呤和乙胺丁醇所致大鼠高尿酸血症模型的影響:大鼠採用連續7天灌胃給予腺嘌呤加乙胺丁醇複製高尿酸血症模型,造模後大鼠血清UA顯著升高,芹菜籽提取物低、中、高劑量(1.7、5.1、15.3g/kg)均能顯著降低模型大鼠血清尿素氮BUN水平、血清肌酸CRE水平和血清UA水平,與陽性對照組相比具有顯著差異。
由上述試驗結果可知,芹菜籽提取物對高尿酸血症有顯著預防及治療作用,並對腎臟具有一定的保護作用。實驗過程中,小鼠給藥均無死亡,且其他器官無異常,毒性較微。
試驗2芹菜籽提取物的最佳提取條件試驗研究
取20kg芹菜籽,使用實施例3所述的方法進行提取,在保證其他實驗條件不變的情況下,分別改變提取試劑、回流時間或柱層析溫度等單因素,考察提取的收率變化,實驗結果見表3、圖1和圖2。
表3不同提取試劑對產率的影響
由上述實驗結果可知,EA/Hex為最佳的提取試劑,生藥產率可達9.2%,純EA作為提取試劑,粗產物量較高,但雜質較多,純化後總產率相對於EA/Hex作為提取試劑稍差。
表4乙酸乙酯和正己烷不同比例對產率的影響
由上述實驗結果可知,隨著正己烷的含量的減少,產率逐漸增加,當正己烷/乙酸乙酯=1:2時產率達到最高,正己烷含量進一步增加,產率下降。
由圖1可知,回流0.5h產率較低,回流1h之後隨著時間的延長,產率不再增加,考慮到節約成本的原則,可選擇回流1h為最佳回流時間;由圖2可知,本發明所述的提取方法中,過柱純化產率較高,保證其他條件不變的情況下,單獨改變過柱溫度,考察到隨著溫度的升高,過柱產率增大,到40℃時為最佳,溫度進一步升高後至50-55℃後,產率下降,矽膠對產品的吸附性增大。
綜合的,本發明所述的芹菜籽提取物的製備方法,提取次數少、提取條件溫和、方法簡單和純化效率高等優點,且大大提高了天然藥物的生藥提取產率,最高可達9.3%,為工業化生產提供了有效途徑。
試驗3軟膠囊劑穩定性試驗研究
3.1加速試驗
取實施例5、實施例7、對照實施例1和對照實施例2所述的軟膠囊劑,在恆溫40℃±2℃下,相對溼度為75%±5%的恆溼條件下放置6個月,在試驗期間1個月、2個月、3個月、6個月末分別取樣一次,按中國藥典中的規定,檢測膠囊劑的性狀、含芹菜素的標示量(%),加速試驗結果見表5;
表5本發明的樣品及對照品的加速試驗結果
從表中可看出本發明的軟膠囊劑,實施例7在高溫高溼的環境下,放置6個月後,沒有破裂和裂痕,且含有芹菜素的標示量未發生明顯的變化;實施例7與實施例5的區別僅在於囊材原料的重量配比 不同,實施例5的穩定性稍差,含有芹菜素的標示量下降6%左右;實施例7與對照實施例的區別在於囊材原料不同,對照實施例所述的芹菜籽提取物軟膠囊高溫高溼環境下放置2-3個月後,表面粗糙,且含芹菜素的標示量顯著下降;由此可知,本發明的軟膠囊劑穩定性顯著提高。
3.2長期試驗
取實施例5、實施例7、對照實施例1和對照實施例2所述的軟膠囊劑,在溫度25℃±2℃下,相對溼度為60%±10%的條件下放置24個月,每3個月取樣一次,分別於0個月、3個月、6個月、9個月、12個月、18個月、24個月取樣,檢測膠囊劑的性狀、含芹菜素的標示量(%),長期試驗結果見表6;
表6本發明的樣品和對照品的長期試驗結果
從表中可看出本發明的軟膠囊劑,長時間放置,該軟膠囊劑的性狀符合標準、含有芹菜素的量未發生明顯的變化;而對照實施例軟膠囊劑長時間放置放置9-12個月後,該膠囊劑的表面出現斑點,並發生破裂現象;並且含丹芹菜素的量顯著下降;表明本發明的軟膠囊劑與對照軟膠囊劑相比,長時間放置性質穩定。
