一種檢測日本乙型腦炎病毒的核酸組合、試劑盒及其應用的製作方法
2023-10-06 03:32:14 2
本發明涉及日本乙型腦炎病毒檢測技術領域,具體而言,涉及一種檢測日本乙型腦炎病毒的核酸組合、試劑盒及其應用。
背景技術:
乙型腦炎是一種可通過蚊蟲媒介傳播的人畜共患傳染病,其由乙型腦炎病毒(Japanese encephalitis virus,JEV)引起。JEV屬於蟲媒病毒黃病毒科黃病毒屬。豬是乙腦病毒的主要感染動物之一,可與蚊蟲形成循環傳播模式。感染該病毒可導致妊娠母豬流產和死胎,公豬單側或兩側性睪丸腫大。此病毒主要造成母豬繁殖障礙,給養豬業的持續高產發展造成巨大的經濟損失。
目前核酸方面的檢測方法主要為傳統PCR、螢光定量PCR以及核酸雜交技術等。定量或者半定量的PCR方法已經有許多的研究報導,往往也顯示出不錯的效果。但是,在感染早期,病毒感染量較低時,這些方法的檢測靈敏度低、檢出率低,不能提供及時準確的診斷結果。
技術實現要素:
本發明的第一目的在於提供一種檢測日本乙型腦炎病毒的核酸組合,該核酸組合包括檢測日本乙型腦炎病毒的引物和探針,利用微滴數字PCR技術檢測出待測樣本中低含量的日本乙型腦炎病毒,特異性強。
本發明的第二目的在於提供上述檢測日本乙型腦炎病毒的核酸組合在檢測日本乙型腦炎病毒中的應用,提高檢測的靈敏性和特異性。
本發明的第三目的在於提供一種檢測日本乙型腦炎病毒的試劑盒,該試劑包括上述核酸組合,該試劑盒可用於檢測低日本乙型腦炎病毒含量的待測樣本,其具有靈敏性好、特異性強、檢測速度快、操作方便等特點。
本發明解決其技術問題是採用以下技術方案來實現的。
一種檢測日本乙型腦炎病毒的核酸組合,其包括引物對和與引物對相對應的探針,引物對包括鹼基序列如SEQ ID NO.1所示的第一義務和如SEQ ID NO.2所示的第二引物,探針的鹼基序列如SEQ ID NO.3所示,探針的5』端標記有螢光報告基團,螢光報告基團選自HEX、FAM或VIC中的任意一種,探針的3』端標記有淬滅基團,淬滅基團為BHQ或TAMRA。
上述的檢測日本乙型腦炎病毒的核酸組合在檢測日本乙型腦炎病毒中的應用。
一種檢測日本乙型腦炎病毒的試劑盒,其包括上述的檢測日本乙型腦炎病毒的核酸組合。
本發明實施例提供的一種檢測日本乙型腦炎病毒的核酸組合、試劑盒及其應用的有益效果是:
本發明的檢測日本乙型腦炎病毒的核酸組合,根據日本乙型腦炎病毒全基因組的保守序列進行設計,該核酸組合包括鹼基序列如SEQ ID NO.1所示的第一引物、如SEQ ID NO.1所示的第二引物以及鹼基序列如SEQ ID NO.3所示的探針。該核酸組合用於日本乙型腦炎病毒的檢測具有很好的特異性。將該核酸組合製備成檢測日本乙型腦炎病毒的試劑盒或者用於微滴數字PCR平臺上檢測日本乙型腦炎病毒,可實現對低日本乙型腦炎病毒含量的樣本進行檢測,具有靈敏性高、特異性強、檢出率高等特點。
附圖說明
為了更清楚地說明本發明實施例的技術方案,下面將對實施例中所需要使用的附圖作簡單地介紹,應當理解,以下附圖僅示出了本發明的某些實施例,因此不應被看作是對範圍的限定,對於本領域普通技術人員來講,在不付出創造性勞動的前提下,還可以根據這些附圖獲得其他相關的附圖。
圖1為本發明實施例7中不同退火溫度的擴增圖;
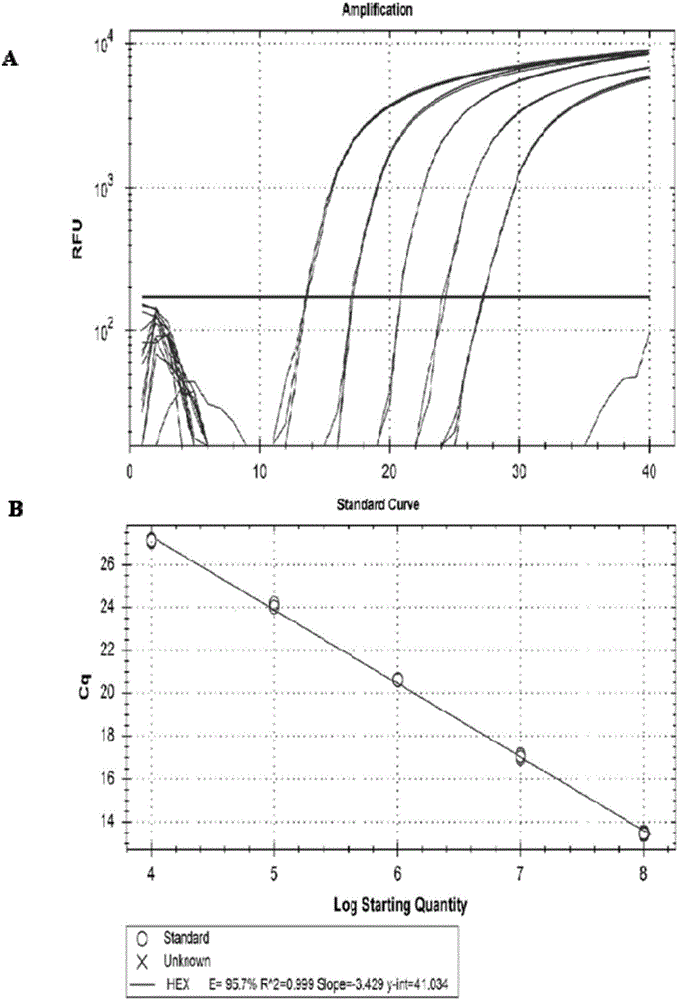
圖2為本發明實施例8中qPCR的標準曲線圖;
圖3為本發明實施例8中qPCR的特異性驗證結果圖;
圖4為本發明實施例8中ddPCR的特異性驗證結果圖;
圖5為本發明實施例9中靈敏性驗證結果圖。
具體實施方式
為使本發明實施例的目的、技術方案和優點更加清楚,下面將對本發明實施例中的技術方案進行清楚、完整地描述。實施例中未註明具體條件者,按照常規條件或製造商建議的條件進行。所用試劑或儀器未註明生產廠商者,均為可以通過市售購買獲得的常規產品。
下面對本發明實施例的一種檢測日本乙型腦炎病毒的核酸組合、試劑盒及其應用進行具體說明。
微滴數字PCR(Droplet digital PCR,ddPCR)是近年來發展起來的快速、準確、可實現DNA絕對定量的PCR方法。其原理是通過把稀釋到一定濃度的DNA分子分布在一定數目的微滴中,使大部分微滴中的DNA分子數目為1或0,然後通過PCR擴增和螢光信號的累計讀取陽性微滴數目,再根據泊松分布計算出(現有的微滴數字PCR儀器基本上都自動相應軟體可自動計算出DNA分子數)樣本中的DNA分子數。該方法無需內參基因無需製備標準曲線,在微量核酸待測樣本的檢測中顯示出很好的檢測效果。
乙型腦炎是一種可通過蚊蟲媒介傳播的人畜共患傳染病,具有有明顯的季節性及區域性。乙型腦炎主要流行於東亞、南亞和太平洋地區,每年因日本乙型腦炎病毒感染而死亡的易感人群在亞洲各國均有大量報導,對全球公共衛生安全造成一定威脅。同時,豬作為日本乙型腦炎病毒主要的易感動物,感染該病毒後使得母豬繁殖障礙,對我國養豬業的持續增產造成巨大危害。因此,建立一種高度靈敏,能在早期檢測極微病毒量的日本乙型腦炎病毒ddPCR檢測技術,不僅對該病的鑑別診斷和預防控制提供支撐,也為我國公共衛生安全和人畜共患病實時監控提供技術參考。
基於此,發明人根據日本乙型腦炎病毒的全基因組的保守序列設計出了可用於ddPCR平臺的檢測日本乙型腦炎病毒的核酸組合,其包括引物對和與引物對相對應的探針,引物對包括鹼基序列分別如SEQ ID NO.1-2所示的引物,探針的鹼基序列如SEQ ID NO.3所示,探針的5』端標記有螢光報告基團,選自HEX、FAM或VIC中的任意一種,探針的3』端標記有淬滅基團BHQ或TAMRA。
具體地,引物對包括SEQ ID NO.1所示的第一引物即上遊引物和如SEQ ID NO.2所示的第二引物即下遊引物,上遊引物的鹼基序列如SEQ ID NO.1所示,下遊引物的鹼基序列如SEQ ID NO.2所示。
通過上述核酸組合,可實現對日本乙型腦炎病毒的檢測,其具很好的特異性。
本發明提供了檢測日本乙型腦炎病毒的試劑盒,其包括上述任一種的核酸組合。
該試劑盒可用於在ddPCR平臺上檢測待測樣本中是否含有日本乙型腦炎病毒,該試劑盒在ddPCR平臺上的運用,與現有技術的檢測方法相比,尤其適用於對低日本乙型腦炎病毒含量的待測樣本的檢測,具有靈敏性好、特異性強、檢出率高的特點。
優選地,本發明提供的檢測日本乙型腦炎病毒的試劑盒還可以包括在進行ddPCR時配套的PCR反應緩衝液、dNTP、Taq DNA聚合酶中的一種或多種等成分。
本發明提供了上述的任意一種檢測日本乙型腦炎病毒的核酸組合在檢測日本乙型腦炎病毒中的應用。該檢測日本乙型腦炎病毒的核酸組合其不僅可在ddPCR平臺進行應用,還可以通過螢光定量PCR、普通PCR等方式來實現對檢測日本乙型腦炎病毒的檢測,只要採用本發明提供的核酸組合用於檢測日本乙型腦炎病毒即屬於本發明的保護範圍。
將本發明提供的檢測日本乙型腦炎病毒的核酸組合應用於日本乙型腦炎病毒的檢測包括以下操作步驟:
(1)配製PCR反應體系
往PCR體系中加入上述的引物對和與引物對相對應的探針,以進行PCR,實現對待測樣本中日本乙型腦炎病毒的高靈敏性檢測。其中,PCR體系包括PCR反應混合液和待測樣本的DNA模板。PCR反應混合液可通過市面購買,也可自行配製,PCR反應混合液主要包括PCR反應緩衝液、dNTP、Taq DNA聚合酶等成分。
優選地,引物對在PCR體系中的終濃度分別為0.88-0.92μM。更優選地,引物對在PCR體系中的終濃度分別為0.9μM。
優選地,探針在PCR體系中的終濃度為0.23-0.27μM。更優選地,引物對在PCR體系中的終濃度為0.25μM。
(2)微滴生成
將PCR體系與微滴生成油混合形成微滴,並進行微滴數字PCR。
優選地,微滴生成油與PCR體系的體積比為6.8-7.2:2。更優選地,微滴生成油與PCR體系的體積比為7:2。
優選地,微滴生成後,對其進行封閉處理,封閉處理的程序為:溫度178-182℃,時間8-12s;更優選地,封閉處理程序為:溫度180℃,時間10s。封閉處理即是對反應容器進行封閉,防止在反應過程中液體蒸發。
當然,本發明在其他的實施例中,也可以採用將PCR反應體系分散到ddPCR反應晶片上的方式形成微滴,並不限於採用微滴生成油包裹的方式。
(3)在預設條件進行微滴數字PCR反應
優選地,進行微滴數字PCR的預設條件為:95℃預變性10min;94℃變性30s,50-60℃退火1min,40個循環;98℃10min,4℃停止反應。
(4)檢測
在微滴分析儀器上檢測相應的螢光信號,得到檢測結果。
綜上,本發明提供的檢測日本乙型腦炎病毒的核酸組合及其應用、試劑盒以及方法具有很高的靈敏性和很強的特異性,能夠有效地對低日本乙型腦炎病毒含量的待測樣本進行檢測,檢出率高,克服了現有檢測方法中對低日本乙型腦炎病毒含量的待測樣本的檢測靈敏度不高的缺陷,為日本乙型腦炎病毒的檢測提供了更多的科學依據和支撐。
以下結合實施例對本發明的特徵和性能作進一步的詳細描述。
實施例1
本實施例提供了檢測日本乙型腦炎病毒的核酸組合,其包括引物對和探針。該引物對和探針根據日本乙型腦炎病毒全基因組的保守序列進行設計得到,可用於檢測出待測樣本中是否含有日本乙型腦炎病毒。
具體地,引物對的上遊引物為:
5』-TGGACCACAACACTTGGAACAT-3』(其鹼基序列如SEQ ID NO.1所示)。
引物對的下遊引物為:
5』-CACAGTCGTCTCCGCTGATC-3』(其鹼基序列如SEQ ID NO.2所示)。
探針為:
HEX-5』-CTTTGAGAATGGAGAGGAGAGAGTGA-3』-BHQ(其鹼基序列如SEQ ID NO.3所示)。
綜上,本實施例提供的核酸組合可通過採用微滴數字PCR技術,檢測出待測樣本中是否含有日本乙型腦炎病毒,實現對日本乙型腦炎病毒的快速檢測,提高檢測的靈敏度。
應當理解的是,在其他的實施例中,本發明提供核酸組合中的探針的5』端標記的螢光報告基團可以是FAM或VIC,3』端的淬滅基團可以是TAMRA。
實施例2
本實施例提供了檢測日本乙型腦炎病毒的試劑盒,該試劑盒包括實施例1提供的核酸組合。該試劑盒可用於在微滴數字PCR平臺上檢測待測樣本中是否含有日本乙型腦炎病毒。本實施例提供的試劑盒具有良好的靈敏性和特異性,能夠檢測出樣本中的極微量的病毒。
應當理解的是,在其他的實施例中,本發明提供的檢測日本乙型腦炎病毒的試劑盒還可以包括在進行微滴數字PCR時配套的PCR反應緩衝液、dNTP、Taq DNA聚合酶中的一種或多種等成分。
實施例3
本實施例提供了應用上述核酸組合檢測日本乙型腦炎病毒的方法,具體如下。
1.配製ddPCR反應體系20μL:ddPCR緩衝液10μL,上、下遊引物終濃度各為0.9μM,探針終濃度為0.25μM,待測樣本的DNA模板2μL,雙蒸H2O補足至20μL。
上、下遊引物以及探針的鹼基序列同實施例1。
2.生成微滴:採用微滴生成油包裹ddPCR反應體系方式形成微滴,微滴生成油與ddPCR反應體系的體積比7:2。在本實施例中,將PCR反應體系20μL加入微滴生成卡中間一排,微滴生成油(droplet generation oil)70μL加入微滴生成卡最底一排,覆蓋專用膠墊後置入微滴生成儀(QX100微滴式數字PCR系統、美國伯樂公司),自動生成微滴。
3.封閉ddPCR體系:吸取生成的微滴40μL加入96孔反應板內,用預熱好的熱封儀(PX1PCR熱封儀、美國伯樂公司)對96孔反應板進行封膜,封膜程序為:溫度180℃,時間10s。
4.按如下ddPCR反應條件進行反應:95℃預變性10min;94℃變性30s,60℃退火1min,40個循環;98℃10min,4℃停止反應。
5.檢測:在微滴分析儀(QX100微滴式數字PCR系統、美國伯樂公司)的HEX通道檢測HEX螢光信號。根據螢光信號值,檢測出待測樣本中的日本乙型腦炎病毒的濃度。
實施例4
本實施例提供了應用上述核酸組合檢測日本乙型腦炎病毒的方法,其與實施例3中提供的方法大致相同,其區別在於:本實施例提供的檢測日本乙型腦炎病毒的方法的ddPCR反應體系中上、下遊引物終濃度各為0.92μM;ddPCR反應體系中探針終濃度為0.23μM;微滴生成油與ddPCR反應體系的體積比為6.8:2;封膜程序為:溫度182℃,時間8s。
實施例5
本實施例提供了應用上述核酸組合檢測日本乙型腦炎病毒的方法,其與實施例3中提供的方法大致相同,其區別在於:本實施例提供的檢測日本乙型腦炎病毒的方法的ddPCR反應體系中上、下遊引物終濃度各為0.88μM;ddPCR反應體系中探針終濃度為0.27μM;微滴生成油與ddPCR反應體系的體積比為7.2:2;封膜程序為:溫度178℃,時間12s。
實施例6
本實施例提供了應用上述核酸組合檢測日本乙型腦炎病毒的方法,其與實施例3中提供的方法大致相同,其區別在於:本實施例提供的檢測日本乙型腦炎病毒的方法的ddPCR反應體系中上、下遊引物終濃度各為0.9μM;ddPCR反應體系中探針終濃度為0.25μM;微滴生成油與ddPCR反應體系的體積比為7:2;封膜程序為:溫度178℃,時間8s。
實施例7
本實施例提供了應用上述核酸組合對日本乙型腦炎病毒進行ddPCR擴增的擴增退火溫度的優化。
本實施例中採用實施例3中的方法分別在60℃、59.2℃、58℃、56℃、54℃、52℃、50℃的退火溫度下進行PCR擴增,比較不同溫度下的擴增效率。結果如圖1所示。
由圖1(1-8分別代表:退火溫度分別為60℃、59.2℃、58℃、56℃、54℃、52℃、50℃、陰性對照)可知,退火溫度在60℃、59.2℃、58℃、56℃、54℃、52℃、50℃下均能擴增,並且擴增效率差異不明顯,陰性對照沒有螢光信號。
實施例8
對實施例1提供的檢測日本乙型腦炎病毒的核酸組合進行特異性驗證。
1利用qPCR方法檢測上述核酸組合的擴增效率:
以濃度依次為104copies/μL、105copies/μL、106copies/μL、107copies/μL、108copies/μL的PMD-19T-JEV重組質粒為模板,用qPCR方法進行擴增,繪製標準曲線。
(JEV cDNA質粒模板PMD-19T-JEV的製備方法可參考:利用JEV特異性引物對病毒核酸RNA進行RT-PCR擴增,擴增產物通過1%瓊脂糖凝膠電泳分析,對擴增片段進行純化回收,純化後的DNA與載體PMD-19T在16℃連接過夜,並轉化至感受態細胞DH5a中,在含100ng/mL的氨苄青黴素的營養瓊脂培養基上37℃培養16-24h,篩選陽性克隆子進行測序鑑定。按照質粒提取試劑盒(天根生化科技有限公司)說明書提取PMD-19T-JEV重組質粒,利用超微量核酸蛋白測定儀(Nanodrop 2000)測定重組質粒濃度,置於-70℃保存備用。)
1.1配製qPCR反應體系20μL:2×qPCR反衝液10μL,上遊引物和下遊引物終濃度各為0.4μM,探針終濃度為0.6μM,待測樣本的DNA模板2μL,雙蒸水H2O補足20μL。
上、下遊引物以及探針的鹼基序列同實施例1。
1.2按如下qPCR反應條件進行反應:94℃預變性3min;94℃變性10s,58℃退火30s,72℃30s(收集螢光信號),40個循環。結果如圖2所示。
由圖2(圖2-A為qPCR的擴增曲線,圖2-B為qPCR的標準曲線)可知,日本乙型腦炎病毒qPCR的擴增效率E=95.7%,標準曲線的相關係數R2=0.999,標準曲線線性關係良好。
2利用qPCR方法驗證上述核酸組合的特異性:分別以豬日本乙型腦炎病毒(JEV,SA14-14-2株)疫苗、豬偽狂犬病毒(PRV,Bartha-K61,HB-98株)疫苗、豬圓環病毒2型(PCV2,LG,ZJ/C株)疫苗、豬瘟病毒(CSFV,兔化弱毒株)疫苗、豬繁殖與呼吸症候群病毒(PRRSV,R98、CH-1a、CH-1R株)疫苗、高致病性豬繁殖與呼吸症候群病毒(HP-PRRSV,JXA1-R、HUN4株)疫苗為待測樣本,檢測上述核酸組合的特異性。
2.1配製qPCR反應體系20μL:2×qPCR反衝液10μL,上遊引物和下遊引物終濃度各為0.4μM,探針終濃度為0.6μM,標準品(JEV cDNA質粒模板)2μL,雙蒸水H2O補足20μL。
2.2按如下qPCR反應條件進行反應:94℃預變性3min;94℃變性10s,58℃退火30s,72℃30s(收集螢光信號),40個循環。結果如圖3所示和表1所示。
由圖3和表1可知,以PRV、PCV2、CSFV、PRRSV、HP-PRRSV的DNA/cDNA為模板的反應孔中均沒有檢測出螢光信號,而以JEV cDNA質粒為模板的反應孔中檢測到螢光信號。由此表明,以JEV cDNA質粒為模板的反應孔中有擴增,上述核酸組合對日本乙型腦炎病毒具有很好的特異性。
3利用ddPCR方法檢測上述核酸組合的特異性:分別以豬日本乙型腦炎病毒(JEV,SA14-14-2株)疫苗、豬偽狂犬病毒(PRV,Bartha-K61,HB-98株)疫苗、豬圓環病毒2型(PCV2,LG,ZJ/C株)疫苗、豬瘟病毒(CSFV,兔化弱毒株)疫苗、豬繁殖與呼吸症候群病毒(PRRSV,R98、CH-1a、CH-1R株)疫苗、高致病性豬繁殖與呼吸症候群病毒(HP-PRRSV,JXA1-R、HUN4株)疫苗為待測樣本,檢測上述核酸組合的特異性。
3.1配製ddPCR反應體系20μL:ddPCR緩衝液10μL,上、下遊引物終濃度各為0.9μM,探針終濃度為0.25μM,待測樣本的DNA模板2μL,雙蒸H2O補足至20μL。
上、下遊引物以及探針的鹼基序列同實施例1。
3.2生成微滴:採用微滴生成油包裹ddPCR反應體系方式形成微滴,微滴生成油與ddPCR反應體系的體積比7:2。在本實施例中,將PCR反應體系20μL加入微滴生成卡中間一排,微滴生成油70μL加入微滴生成卡最底一排,覆蓋專用膠墊後置入微滴生成儀(QX100微滴式數字PCR系統、美國伯樂公司),自動生成微滴。
3.3封閉ddPCR體系:吸取生成的微滴40μL加入96孔反應板內,用預熱好的熱封儀(PX1PCR熱封儀、美國伯樂公司)對96孔反應板進行封膜,封膜程序為:溫度180℃,時間10s。
3.4按如下ddPCR反應條件進行反應:95℃預變性10min;94℃變性30s,60℃退火1min,40個循環;98℃10min,4℃停止反應。
3.5檢測:在微滴分析儀(QX100微滴式數字PCR系統、美國伯樂公司)的HEX通道檢測HEX螢光信號。根據螢光信號值,檢測出待測樣本中的日本乙型腦炎病毒的濃度。結果如圖4所示和表1所示。
由圖4和表1可知,以PRV、PCV2、CSFV、PRRSV、HP-PRRSV的DNA/cDNA為模板的反應孔中均沒有檢測出螢光信號,而以JEV cDNA質粒為模板的反應孔中檢測到螢光信號。由此表明,以JEV cDNA質粒為模板的反應孔中有擴增,在ddPCR檢測平臺上,上述核酸組合對日本乙型腦炎病毒具有很好的特異性。
利用qPCR和ddPCR分別檢測JEV、PRV、PCV2、CSFV、PRRSV、HP-PRRSV的結果如表1所示。
表1特異性檢測結果
註:「+」表示檢測到螢光信號,「-」表示未檢測到螢光信號。
綜上,本發明提供的檢測日本乙型腦炎病毒的核酸組合以及試劑盒對日本乙型腦炎病毒的檢測具有很好的特異性。
實施例9
本實施例提供了應用上述核酸組合檢測日本乙型腦炎病毒的靈敏性的驗證。
本實施中主要通過將檢測日本乙型腦炎病毒的qPCR方法與ddPCR方法進行對比,以評價上述核酸組合在兩種方法中檢測日本乙型腦炎病毒的靈敏性。以終濃度為105copies/μL、104copies/μL、103copies/μL、102copies/μL、101copies/μL、100copies/μL、10-1copies/μL的PMD-19T-JEV重組質粒為模板,分別以qPCR和ddPCR兩種方法進行PCR擴增。具體地:
1 qPCR方法按照如下步驟進行:
1.1配製qPCR反應體系20μL:2×qPCR緩衝液10μL,上遊引物和下遊引物終濃度各0.4μM,探針終濃度為0.6μM,PMD-19T-JEV重組質粒2μL,雙蒸水H2O補足20μL。
上、下遊引物以及探針的鹼基序列同實施例1。
1.2按如下qPCR反應條件進行反應:94℃預變性3min;94℃變性10s,58℃退火30s,72℃30s(收集螢光信號),40個循環。結果如圖5-A所示。
2 ddPCR方法按照如下步驟進行:
2.1配製ddPCR反應體系20μL:ddPCR緩衝液10μL,上、下遊引物終濃度各為0.9μM,探針終濃度為0.25μM,PMD-19T-JEV重組質粒2μL,雙蒸H2O補足至20μL。
上、下遊引物以及探針的鹼基序列同實施例1。
2.2生成微滴:採用微滴生成油包裹ddPCR反應體系方式形成微滴,微滴生成油與ddPCR反應體系的體積比7:2。在本實施例中,將PCR反應體系20μL加入微滴生成卡中間一排,微滴生成油70μL加入微滴生成卡最底一排,覆蓋專用膠墊後置入微滴生成儀(QX100微滴式數字PCR系統、美國伯樂公司),自動生成微滴。
2.3封閉ddPCR體系:吸取生成的微滴40μL加入96孔反應板內,用預熱好的熱封儀(PX1PCR熱封儀、美國伯樂公司)對96孔反應板進行封膜,封膜程序為:溫度180℃,時間10s。
2.4按如下ddPCR反應條件進行反應:95℃預變性10min;94℃變性30s,60℃退火1min,40個循環;98℃10min,4℃停止反應。
2.5檢測:在微滴分析儀(QX100微滴式數字PCR系統、美國伯樂公司)的HEX通道檢測HEX螢光信號。根據螢光信號值,檢測出待測樣本中的日本乙型腦炎病毒的濃度。結果如圖5-B所示。
由圖5(圖5-A為qPCR的靈敏性驗證結果;圖5-B為ddPCR的靈敏性驗證結果,其中1-7中分別代表擴增模板拷貝數分別為105copies/μL、104copies/μL、103copies/μL、102copies/μL、101copies/μL、100copies/μL、10-1copies/μL。)可知,qPCR的最低檢出濃度為102copies/μL,ddPCR的最低檢出濃度為100copies/μL。由此說明ddPCR檢測方法的最低檢出濃度比qPCR高出兩個數量級。進一步說明,本發明中提供的檢測日本乙型腦炎病毒的核酸組合應用於ddPCR檢測方法對日本乙型腦炎病毒的檢測具有很高的靈敏性。
實施例10
本實施例中提供了檢測日本乙型腦炎病毒的核酸組合分別結合qPCR和ddPCR檢測平臺檢測實際樣本。
qPCR的檢測方法同實施例8;
ddPCR的檢測方法同實施例8;
對57份疑似患病豬的樣品進行ddPCR檢測,同時用qPCR對樣品進行平行檢測,並對兩者的檢測結果進行比較。57份樣品中包括:31份內臟樣品、18份精液樣品、6份流產胎樣品、2份腦組織樣品。檢測結果如表2所示。
表2.樣品信息及檢測結果
註:SAU:Sichuan Agricultural University(四川農業大學);陽性總檢出率=(檢出陽性樣品總數/57)×100%。
由表2可知,在57份實際樣品中,qPCR檢出陽性樣品總數為23個,陽性檢出率為40.4%;ddPCR檢出陽性樣品總數為31個,陽性檢出率為54.4%。ddPCR的陽性檢出率高於qPCR的陽性檢出率,由此表明:本發明提供的核酸組合可應用於qPCR和ddPCR檢測平臺,實現對日本乙型腦炎病毒的檢測,並且ddPCR可以彌補qPCR的不足,可對螢光定量PCR檢測結果可疑的樣品進行進一步確證。
綜上所述,本發明提供的檢測日本乙型腦炎病毒的核酸組合,根據日本乙型腦炎病毒全基因組的保守序列進行設計,該核酸組合包括鹼基序列分別如SEQ ID NO.1-2所示的引物對和鹼基序列如SEQ ID NO.3所示的探針。該核酸組合用於日本乙型腦炎病毒的檢測具有很好的特異性。將還核酸組合製備成檢測日本乙型腦炎病毒的試劑盒或者用於微滴數字PCR平臺上檢測日本乙型腦炎病毒,可實現對低日本乙型腦炎病毒含量的樣本進行檢測,具有靈敏性高、特異性強、檢出率高等特點。
以上所描述的實施例是本發明一部分實施例,而不是全部的實施例。本發明的實施例的詳細描述並非旨在限制要求保護的本發明的範圍,而是僅僅表示本發明的選定實施例。基於本發明中的實施例,本領域普通技術人員在沒有作出創造性勞動前提下所獲得的所有其他實施例,都屬於本發明保護的範圍。
SEQUENCE LISTING
四川出入境檢驗檢疫局檢驗檢疫技術中心 、成都大學
一種檢測日本乙型腦炎病毒的核酸組合、試劑盒及其應用
3
PatentIn version 3.5
1
22
DNA
人工序列
1
tggaccacaa cacttggaac at 22
2
20
DNA
人工序列
2
cacagtcgtc tccgctgatc 20
3
26
DNA
人工序列
3
ctttgagaat ggagaggaga gagtga 26
