A型3,6‑二碘‑N‑苯基咔唑的晶體結構及其製備方法與流程
2023-06-10 01:49:31 2
本發明屬於光電材料、精細化工領域,主要涉及一種雙碘代咔唑衍生物的晶體結構研究。
背景技術:
在過去的二十年裡,研究螢光元件的科學家和工程師們在合成相關的咔唑螢光材料與設計最佳螢光結構方面取得了很多可喜的成果。一些基於咔唑的有機分子和聚合化合物都擁有極好的空穴傳輸能力、薄膜成型性質和熱學性質,這些優良性質皆有助於咔唑及其衍生物應用於有機電致發光元件和光伏電池的開發中(于濤等. 咔唑衍生物在有機電致發光材料中的研究進展[J]. 化工新型材料. 2009, 37(5):6-8)。例如,在OLED燈的開發過程中,科學家們集中精力尋找更多擁有良好熱學性質、強光性和優良的空穴傳輸能力的材料。咔唑在有機光致發光、電致發光以及非線性光學元件等領域都有極大的應用性,特別是咔唑衍生物被廣泛的應用為空穴傳輸層材料(李猛,呂宏飛,李淑輝等. 3-溴-9-苯基咔唑的合成[J]. 黑龍江科學. 2012, 3(1):26-31)。
正如上所述,儘管這類咔唑化合物具有良好的光學性質,但是其晶體結構研究報導比較少。尤其是雙碘代咔唑衍生物的晶體結構研究仍然未見文獻報導。這類雙碘代咔唑是合成其它更優良的光電材料中間體。本發明旨在研究這種雙碘代咔唑衍生物的晶體結構。
技術實現要素:
本發明提供一種3,6-二碘-N-苯基咔唑的晶體結構及其製備方法。這個雙碘代咔唑衍生物由於碘原子很活潑,為以後合成其他含咔唑的單體或聚合物的設計和構築提供了更多可能。
本發明所要解決的技術問題通過以下技術方案予以實現:一種A型3,6-二碘-N-苯基咔唑晶體結構的製備方法如下:將9-苯基咔唑(0.2433 g, 0.1 mmol)、碘化鉀(0.6640 g, 4.0 mmol)和碘酸鉀(0.4277 g, 2.0 mmol)與50ml冰醋酸室溫下混合。加熱至135℃,回流18小時後。反應液自然冷卻至室溫。抽濾,用50ml 10%硫代硫酸鈉溶液和30ml蒸餾水洗滌沉澱。稱取0.1克的3,6-二碘-N-苯基咔唑,溶解在5毫升氯仿中,過濾,靜置3天後,得到一種無色塊狀晶體。其晶體結構屬於單斜晶系,P21空間群,晶胞參數為
。
本發明的有益效果:結合了咔唑類化合物的優點,這種雙碘代咔唑化合物很容易與含炔基、硼酸基芳香化合物進行反應,為以後構築其他含咔唑類的單體或聚合物提供了更多可能性。而所得的化合物中咔唑環具有螢光性能的芳香環,為光學材料提供了一個可能。
附圖說明
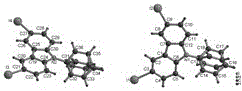
圖1、本發明的A型3,6-二碘-N-苯基咔唑的晶體結構圖。
圖2、本發明的A型3,6-二碘-N-苯基咔唑的一維鏈圖。
圖3、本發明的A型3,6-二碘-N-苯基咔唑的二維圖。
圖4、本發明的A型3,6-二碘-N-苯基咔唑的堆積圖。
圖5、本發明的A型3,6-二碘-N-苯基咔唑的紫外可見光譜圖。
圖6、本發明的A型3,6-二碘-N-苯基咔唑的紅外光譜圖。
具體實施方式
下面結合實施例對本發明進行詳細的說明,實施例僅是本發明的優選實施方式,不是對本發明的限定。
實施例 3,6-二碘-N-苯基咔唑化合物的製備。
將9-苯基咔唑(0.2433 g, 0.1 mmol)、碘化鉀(0.6640 g, 4.0 mmol)和碘酸鉀(0.4277 g, 2.0 mmol)與50ml冰醋酸室溫下混合。加熱至135℃,回流18小時後。反應液自然冷卻至室溫。抽濾,用50ml 10%硫代硫酸鈉溶液和30ml蒸餾水洗滌沉澱。稱取0.1克的3,6-二碘-N-苯基咔唑,溶解在5毫升氯仿中,過濾,靜置3天後,得到一種無色塊狀晶體。
然後將上述3,6-二碘-N-苯基咔唑化合物進行結構表徵。
該3,6-二碘-N-苯基咔唑化合物通過單晶結構衍射,並在計算機上用SHELXTL程序包完成結構確定和精修。化合物3,6-二碘-N-苯基咔唑的晶體學參數見表1。
表1 3,6-二碘-N-苯基咔唑的晶胞參數。
由圖1可知,X-射線衍射分析表明,化合物1以手性空間群P21的結晶。在不對稱單元中,存在著兩個獨立的3,6-二碘-N-苯基咔唑的分子。晶體結構表明,第一個3,6-二碘-N-苯基咔唑分子中,在咔唑的3位和6位分別連接著一個碘原子,其鍵長分別是2.124(9)和2.054(10)Å。而在第二個3,6-二碘-N-苯基咔唑分子中,C-I鍵的長度為2.043(9)和2.120(9)Å。N-苯基基團和五員環之間的二面角是52.6o和47.4o。其平均二面角50o,這是比第一個分子的二面角要高得多。
圖2表示沿晶胞b軸的一維鏈。在相鄰兩個化合物之間,分子間靠π∙∙∙π作用力與C-H∙∙∙π作用力相互連接成一維鏈。這些作用力來自於咔唑環之間,比如:Cg(1)∙∙∙Cg(3)a3.847(7)Å; Cg(2)∙∙∙Cg(1)a 3.900(7)Å; Cg(2)∙∙∙Cg(3)a 3.727(6)Å; Cg(3)∙∙∙Cg(1)b3.848(7)Å; Cg(3)∙∙∙Cg(2)b 3.728(6)Å; Cg(6)∙∙∙Cg(7)c 3.890(6)Å; Cg(6)∙∙∙Cg(8)d3.877(6) Å; Cg(7)∙∙∙Cg(6)d 3.889(6) Å; Cg(7)∙∙∙Cg(8)d 3.761(6) Å; Cg(8)∙∙∙Cg(6)a 3.876(6) Å; Cg(8)∙∙∙Cg(7)a 3.761(6) Å。這裡的a、b 和c分別表示如下的對稱碼:x,-1+y,z; x,1+y,z;x,-1+y,z和 x,1+y,z。另外,芳香環Cg(1)是由這些原子構成N(1)-C(6)-C(1)-C(7)-C(12); Cg(2) 由 C(1)-C(2)-C(3)-C(4)-C(5)-C(6)組成; Cg(3) 是由C(7)-C(8)-C(9)-C(10)-C(11)-C(12)原子構成; 芳香環Cg(6) 由N(2)-C(24)-C(19)-C(25)-C(30)原子構成; 芳香環Cg(7) 由C(19)-C(20)-C(21)-C(22)-C(23)-C(24)組成; Cg(8) 是由這些原子構成 C(25)-C(26)-C(27)-C(28)-C(29)-C(30)。除此以外,苯基芳香環上的氫與苯基芳香環存在著超分子作用力,例如:C(15)-H(15)∙∙∙Cg(7)a 153o, 3.661(17)Å; C(18')-H(18')∙∙∙Cg(4)b 135o,3.663(16)Å; C(33)-H(33)∙∙∙Cg(2)c 141o, 3.669(17)Å; C(35)-H(35)∙∙∙Cg(3)d 152o,3.693(15)Å。這裡的a、b和c分別表示對稱碼為:1-x,1/2+y,1-z;x,1+y,z;1-x,-1/2+y,1-z和-x,-1/2+y,1-z。芳香環Cg(2)、 Cg(3) 、Cg(4)和Cg(7)分別由下列原子構成:C(1)-C(2)-C(3)-C(4)-C(5)-C(6); C(7)-C(8)-C(9)-C(10)-C(11)-C(12); C(13)-C(14)-C(15)-C(16)-C(17)-C(18); C(19)-C(20)-C(21)-C(22)-C(23)-C(24)。
圖3表示沿ab面的二維層。通過分子間通過π∙∙∙π作用力與C-H∙∙∙π作用力將多個一維鏈擴展成二維層。
圖4表示化合物的堆積圖。上述的二維層堆積成一個三維超分子結構。
圖5表示3,6-二碘-N-苯基咔唑的紫外可見光譜圖。如圖5所示,發現在264-377 nm區域存在明顯的吸收峰。研究發現,化合物1的最大吸收峰位於在359 nm處。
圖6表示3,6-二碘-N-苯基咔唑的紅外光譜圖。由紅外譜圖可知,在3134 cm-1處,可分為芳香C-H鍵(νC-H)。芳香環上的C = C伸縮振動通常發生在1400-1625 cm-1範圍內。五個峰分別位於1595,1500,1463,1427和1400 cm-1,這可能歸因於咔唑環的C = C骨架伸縮振動。一般來說,芳香環上的C-H鍵的彎曲振動一般落在1000-1300 cm-1區域。正如我們所預料的那樣,幾個峰位於1278-1014 cm-1範圍內,表明苯環的存在。譜帶落在1014-630 cm-1區域,從而表示C-H面外和芳香體系的平面變形振動。在565和563 cm-1處的強峰是芳環中碘的特徵振動峰。
以上所述實施例僅表達了本發明的實施方式,其描述較為具體和詳細,但並不能因此而理解為對本發明專利範圍的限制,但凡採用等同替換或等效變換的形式所獲得的技術方案,均應落在本發明的保護範圍之內。
