聚乙二醇化7‑脫氫膽固醇衍生物的製作方法
2023-05-24 22:32:02 2
本發明涉及聚乙二醇化7-脫氫膽固醇衍生物(Pegylated 7-dehydrocholesterol derivatives)。更特別地,本發明涉及聚乙二醇化7-脫氫膽固醇衍生物,其具有得到改善的穩定性和溶解度並在體內經過水解而提供維生素D,且還涉及用於減少皺紋和抗老化的含有所述聚乙二醇化7-脫氫膽固醇衍生物的組合物。
背景技術:
維生素D具有兩種類型,維生素D2(鈣化醇)和維生素D3(膽鈣化醇,化合物B),這兩種物質在肝臟和腎臟進行代謝而轉化成它們的活性形態(骨化三醇,化合物C)。7-脫氫膽固醇(7-DHC,化合物A)為維生素D3的維生素原形態,經過陽光照射會被轉化成維生素D3。
通常,維生素D3促進鈣吸收以強化骨密度,因此它被用作骨質疏鬆症的治療劑及用於老年人或居住在難以獲得充足日照的北半球居民的補充劑。
已知,作為維生素D的前體的所述7-脫氫膽固醇具有強效的皮膚抗老化和抗氧化活性,且具有防紫外線的效果,因此被用作功能性化妝品的原材料【參見韓國專利申請公開號2001-0002281】。此外,美國專利申請公開號2013-0017234公開了,7-脫氫膽固醇由於能使參與骨骼形成中的Col-1、ALP、OSX、OC、BMP-2和IL-5因子進行表達而具有用於治療關節炎的可能性。此外,韓國專利號10-0568600通過臨床試驗公開了7-脫氫膽固醇具有優異的毛髮保護效果。
因此我們期待,通過在皮膚外層上持續提供7-脫氫膽固醇,可增加膽鈣化醇的生成,以預防骨質疏鬆症及預防以異常皮膚的皮屑為特點的牛皮癬和如特應性皮炎的皮膚疾病,同時還能提供隔離紫外線吸收及抗老化的效果。
然而,7-脫氫膽固醇在除皮膚以外的區域上極不穩定,且因光照而被轉化成各種物質,這些物質儘管幾乎沒有副作用卻難以轉化成維生素D3。此外,在除皮膚之外區域上,7-脫氫膽固醇會被轉化成焦骨化醇(pyrocalciferol)或光甾醇(lumisterol)和異光甾醇(isopyrocalciferol),使得活性降低。
為了克服上述問題,美國專利號5,342,833公開了具有新特性的新型膽鈣化醇,即活性維生素D衍生物,用於治療皮膚疾病和牛皮癬。此外,美國專利號5,747,478公開了通過利用氧化鎂和檸檬酸鈉來穩定活化的膽鈣化醇。
然而,對7-脫氫膽固醇的穩定化的研究停滯不前,究其原因,在於7-脫氫膽固醇受紫外線和溫度的影響而易於轉化成其他物質,且存在與空氣中的氧氣反應而發生結構變性。
此外,如上所述,現有的專利僅僅公開了7-脫氫膽固醇的製藥穩定性或展示作為活性形態的膽鈣化醇的研究,但並沒有涉及7-脫氫膽固醇的合成穩定性的公開。
技術實現要素:
技術問題
本發明人為了克服上述的7-脫氫膽固醇對化學製品、紫外線、溫度的不穩定性及與空氣接觸時的不穩定性且在水中具有極低的溶解度等問題,經過研究發現,7-脫氫膽固醇與聚乙二醇的偶聯物(conjugation)可以提高在有機溶劑或水溶液中的溶解度,且可以提升在皮膚內向細胞傳遞的效果,且其特性的改善可以促進功效的提高,從而增強7-脫氫膽固醇的溶解度和在長期保存中的穩定性。
因此,本發明的一個目的在於,提供具有改善的溶解度和穩定性的聚乙二醇化7-脫氫膽固醇衍生物。
本發明的另一目的在於,提供用於減少皺紋及抗老化的組合物,該組合物包含所述聚乙二醇化7-脫氫膽固醇衍生物。
技術方案
本發明涉及以下化學式(I)的聚乙二醇化7-脫氫膽固醇衍生物:
其中,R為氫或C1-C6烷基,
G為-XCOCH2(CH2)mCO-、-XCH2(CH2)mCO-、-XCONHCYCO-、-XCOCYNHCO(CH2)mCH2CO-或–XCH2(CH2)mCONHCYCO-,
X為O、NH或S,
Y為氫、C1-C6烷基、(CH2)m′CH2NHCO(CH2)mCH2(OCH2CH2)nOR、(CH2)m′CH2NHCOCH2(CH2)mCO(OCH2CH2)nOR或(CH2)m′CH2NHCOCH2(CH2)mCO-DHC,
n為1-700之間的整數,優選為3-200之間的整數,且
m和m′分別獨立地為1-3之間的整數,優選為1。
這裡使用的術語「C1-C6烷基」是指具有1-6個碳原子的直鏈或支鏈的碳氫化合物,包括甲基、乙基、正丙基、異丙基、正丁基、正丁基、仲丁基、叔丁基、正戊基、正己基等,不限於此。
在本發明的一個實施例中,所述聚乙二醇化7-脫氫膽固醇衍生物可以為以下化學式(1A)的化合物:
其中,R為氫或C1-C6烷基,
X為O或NH,
n為1-700之間的整數,優選為3-200之間的整數,且
m為1-3之間的整數,優選為1。
在本發明的一個實施例中,所述聚乙二醇化7-脫氫膽固醇衍生物可以為以下化學式(1B)的化合物:
其中,R為氫或C1-C6烷基,
n為1-700之間的整數,優選為3-200之間的整數,且
m為1-3之間的整數,優選為1。
在本發明的一個實施例中,所述聚乙二醇化7-脫氫膽固醇衍生物可以為以下化學式(2A)的化合物:
其中,R為氫或C1-C6烷基,
X為O或NH,
n為1-700之間的整數,優選為3-200之間的整數,且
Y1為C1-C6烷基。
在本發明的一個實施例中,所述聚乙二醇化7-脫氫膽固醇衍生物可以為以下化學式(2B)的化合物:
其中,R為氫或C1-C6烷基,
X為O或NH,
n為1-700之間的整數,優選為3-200之間的整數,
m為1-3之間的整數,優選為1,且
Y1為C1-C6烷基。
在本發明的一個實施例中,所述聚乙二醇化7-脫氫膽固醇衍生物可以為以下化學式(2C)的化合物:
其中,R為氫或C1-C6烷基,
n為1-700之間的整數,優選為3-200之間的整數,
m為1-3之間的整數,優選為1,且
Y1為C1-C6烷基。
在本發明的一個實施例中,所述聚乙二醇化7-脫氫膽固醇衍生物可以為以下化學式(2D)的化合物:
其中,R為氫或C1-C6烷基,
X為O或NH,
n為1-700之間的整數,優選為3-200之間的整數,且
m和m′分別獨立地為1-3之間的整數,優選為1。
在本發明的一個實施例中,所述聚乙二醇化7-脫氫膽固醇衍生物可以為以下化學式(2E)的化合物:
其中,R為氫或C1-C6烷基,
X為O或NH,
n為1-700之間的整數,優選為3-200之間的整數,且
m和m′分別獨立地為1-3之間的整數,優選為1。
在本發明的一個實施例中,所述聚乙二醇化7-脫氫膽固醇衍生物可以為以下化學式(2F)的化合物:
其中,R為氫或C1-C6烷基,
X為O或NH,
n為1-700之間的整數,優選為3-200之間的整數,且
m和m′分別獨立地為1-3之間的整數,優選為1。
在本發明的一個實施例中,所述聚乙二醇化7-脫氫膽固醇衍生物可以為以下化學式(2G)的化合物:
其中,R為氫或C1-C6烷基,
X為O或NH,
n為1-700之間的整數,優選為3-200之間的整數,且
m和m′分別獨立地為1-3之間的整數,優選為1。
本發明的聚乙二醇化7-脫氫膽固醇衍生物可通過以下反應式1-5中所示的方法製備而成。所述反應式的方法僅僅用於說明用於本發明中的具代表性的方法,而反應式中的單元操作順序、試劑和反應條件可以作適應性改變。
【反應式1】
其中,R、X、n和m與上述化學式(I)中的定義一致。
根據反應式1,化學式(4)的化合物和化學式(5)的化合物可分別經過與化學式(7a)的化合物或化學式(6)的化合物進行縮合反應,而獲得化學式(1A)的聚乙二醇化7-脫氫膽固醇衍生物。此外,化學式(4)的化合物可經過與化學式(7b)的化合物進行縮合反應,而獲得化學式(1B)的聚乙二醇化7-脫氫膽固醇衍生物。
化學式(5)的化合物和化學式(7a)的化合物可分別通過化學式(4)的化合物或化學式(6)的化合物與酸酐進行反應而製成,且化學式(7b)的化合物可根據已知方法使用X為O的化學式(6)的化合物作為起始物質進行製備,或可商購獲得【請見:J.M.Harris et.al,Advanced Drug Delivery Reviews,2002,54,459-476】。
此外,化學式(6)的化合物可商購獲得或可通過已知方法進行製備【請見:andler and Karo,Polymer Synthesis,Academic Press,New York,Vol.3,pages 138-161】。
【反應式2】
其中,R、X、n和m與上述化學式(I)中的定義一致。
Zb和Zc分別為保護基團,且
Y1為氫、C1-C6烷基或胺基酸殘基。
根據反應式2,化學式(6)的化合物可被活化而獲得化學式(8)的化合物,化學式(8)的化合物經過與化學式(9)的化合物進行反應而獲得化學式(10)的聚乙二醇衍生物。此外,化學式(10)的化合物可經過與化學式(4)的化合物進行縮合反應而獲得化學式(2A)的聚乙二醇化7-脫氫膽固醇衍生物。
此外,化學式(6)的化合物可經過與化學式(12)的化合物進行縮合反應而獲得化學式(13)的化合物。然後,化學式(13)的化合物經過去保護而獲得化學式(14)的化合物,且化學式(14)的化合物可經過與化學式(5)的化合物進行縮合反應而獲得化學式(2B)的聚乙二醇化7-脫氫膽固醇衍生物。
進一步,在某些情況下,可有選擇地使用具有保護基團的化合物,如化學式(11)的化合物,當Y1為胺基酸殘基時,其可以被保護基團取代或未被取代。
【反應式3】
其中,R、n和m與上述化學式(I)中的定義一致。
L為滷素、琥珀醯亞胺或咪唑,且
Y1為氫、C1-C6烷基或胺基酸殘基。
根據反應式3,化學式(7b)的化合物可被活化而獲得化學式(15b)的化合物,化學式(15b)的化合物經過與化學式(9)的化合物進行反應而獲得化學式(16)的聚乙二醇衍生物。化學式(16)的化合物可經過與化學式(4)的化合物進行縮合反應而獲得化學式(2C)的聚乙二醇化7-脫氫膽固醇衍生物。
【反應式4】
其中,R、X、n、m和m′與上述化學式(I)中的定義一致。
L為滷素、琥珀醯亞胺或咪唑,且
Za和Zb分別為保護基團。
根據反應式4,化學式(6)的化合物可經過與被保護基團取代或未被取代的化學式(17)的化合物進行反應而獲得化學式(18)的化合物。化學式(18)的化合物可經過去保護而獲得化學式(19)的化合物,化學式(19)的化合物可經過與化學式(7b)的化合物進行反應而獲得作為側鏈式聚乙二醇衍生物的化學式(20)的化合物。化學式(20)的化合物可經過去保護而獲得化學式(21)的化合物,化學式(21)的化合物可經過與化學式(5)的化合物進行縮合反應而獲得化學式(2D)的聚乙二醇化7-脫氫膽固醇衍生物。
【反應式5】
其中,R、X、n、m和m′與上述化學式(I)中的定義一致,且
Za為保護基團。
根據反應式5,化學式(8)的化合物可經過與被保護基團取代或未被取代的化學式(22)的化合物進行反應而獲得化學式(23)的化合物。化學式(23)的化合物可經過去保護而獲得化學式(24)的化合物,化學式(24)的化合物經過與化學式(15b)的化合物進行反應而獲得化學式(25b)的化合物。化學式(25b)的化合物可經過與化學式(4)的化合物進行縮合反應而獲得化學式(2E)的聚乙二醇化7-脫氫膽固醇衍生物。
此外,化學式(24)的化合物可經過與通過活化化學式(7a)的化合物而獲得的化學式(15a)的化合物進行反應,而獲得化學式(25a)的化合物,且化學式(25a)的化合物可經過與化學式(4)的化合物進行縮合反應,而獲得化學式(2F)的聚乙二醇化7-脫氫膽固醇衍生物。
【反應式6】
其中,R、X、n、m和m′與上述化學式(I)中的定義一致,且
Za為保護基團。
根據反應式6,化學式(8)的化合物可經過與被保護基團取代或未被取代的化學式(22)的化合物進行反應,而獲得化學式(23)的化合物,且化學式(23)的化合物可經過與化學式(4)的化合物進行縮合反應,而獲得化學式(26)的化合物,化學式(26)的化合物可經過去保護而獲得化學式(27)的化合物。化學式(27)的化合物可經過與化學式(5)的化合物進行縮合反應,而獲得化學式(2G)的聚乙二醇化7-脫氫膽固醇衍生物。
在所述反應式中,所述縮合反應可優選地在存在縮合劑和有機胺催化劑的溶劑內進行。
所述縮合劑的例子可包括N,N,N',N'-四甲基-(苯並三唑-1-基)-uronium四氟硼酸鹽(TBTU)、N-(3-二甲基氨基丙基)-N'-乙基-碳二亞胺(EDC)、N,N'-二異丙基(DIC)和N,N'-二環己基碳(DCC),但不限於此。
此外,所述有機胺催化劑的例子可包括異丙基乙胺(DIPEA)和4-二甲氨基吡啶(DMAP),但不限於此。
所述溶劑的例子可包括無水有機溶劑,例如選自二氯甲烷、苯、甲苯、四氫呋喃和乙醚中的至少一種,但不限於此。此外,可將水或緩衝液用作所述溶劑,或與水混溶的有機溶劑,如可將乙腈、二甲基甲醯胺等與水一起混合使用。
上述反應可在冷卻或加熱溫度下進行。
同時,所述保護基團的例子可包括Boc、Fmoc、CBz、tBuCO、Trt、Me、Et等,但不限於此。
此外,所述去保護反應可在存在酸或鹼的有機溶劑內進行。所述有機溶劑可包括四氫呋喃(THF)、二氯甲烷(DCM)、甲醇、二甲基甲醯胺(DMF)等,但不限於此。此外,所述酸或鹼的例子可包括三氟乙酸(TFA)、鹽酸、硫酸、乙酸、哌啶、氫氧化鈉等,但不限於此。
在反應式3和5中,如果必要,所述被活化的離去基團的取代反應可以在無水有機溶劑內,通過與有機胺催化劑,與亞硫醯氯、草醯氯、N-羥基琥珀醯亞胺、羰二咪唑等進行反應來實施。
本發明的化學式(I)的聚乙二醇化7-脫氫膽固醇衍生物,與7-脫氫膽固醇相比,在水溶液內的溶解度得到提高,且對光和熱的穩定性得到意想不到的改善。
因此,本發明的化學式(I)的聚乙二醇化7-脫氫膽固醇衍生物可在體內水解而起到用於供應維生素D的前體、7-脫氫膽固醇的來源的作用,從而可被有效地用在用於減少皺紋和抗老化的化妝品組合物、藥物組合物和功能食品中。
本發明還涉及用於減少皺紋和抗老化的化妝品組合物,該組合物包含化學式(I)的聚乙二醇化7-脫氫膽固醇衍生物。
本發明的化妝品組合物可包含約0.0001-10wt%,優選為0.01-1wt%量的作為活性成分的化學式(I)的聚乙二醇化7-脫氫膽固醇衍生物。所述活性成分的量可根據使用目的而定。
除了化學式(I)的聚乙二醇化7-脫氫膽固醇衍生物之外,所述本發明的化妝品組合物還可包含本領域常用的化妝品成分,例如,如抗氧化劑、穩定劑、增溶劑、維生素、色素和香料的常用佐劑,以及載體。
本發明的化妝品組合物可被製成本領域常用的任何劑型,例如,溶液、懸浮液、乳液、膏劑、凝膠、霜劑、粉末、噴霧劑等。
在所述化妝品組合物被製成膏劑、霜劑或凝膠的情況下,所述載體的例子包括動物油、植物油、蠟、石蠟、澱粉、黃芪膠、纖維素衍生物、聚乙二醇、矽、膨潤土、二氧化矽、滑石、氧化鋅等。
在所述化妝品組合物被製成粉末或噴霧劑的情況下,所述載體的例子包括乳糖、滑石粉、矽石、氫氧化鋁、矽酸鈣、聚醯胺粉末等。特別地,當所述劑型為噴霧劑時,所述化妝品組合物可進一步包含氯氟烴、丙烷/丁烷或二甲醚的推進劑。
在所述化妝品組合物被製成溶液或乳液的情況下,所述載體的例子包括溶劑、增溶劑和乳化劑,如水、乙醇、異丙醇、碳酸乙酯、乙酸乙酯、苄醇、苯甲酸苄酯、丙二醇、1,3-丁基二醇油、甘油脂肪酸酯、聚乙二醇、山梨糖醇脂肪酸酯等。
在所述化妝品組合物被製成懸浮液的情況下,所述載體的例子包括如水、乙醇和丙二醇的液體稀釋劑,如乙氧基化異硬脂醇、聚氧乙烯山梨糖醇酯和聚氧乙烯山梨糖醇酯的懸浮劑,微晶纖維素,鋁金屬氫氧化物,膨潤土,瓊脂,西黃蓍等。
本發明的化妝品組合物可應用於化妝品,如化妝水、乳液、霜、精華液、面膜、粉底、彩妝、防曬霜、兩用粉餅、散粉、壓縮粉底、底妝、遮瑕妝、眼影、唇膏、唇彩、修唇膏和眉筆。
本發明進一步涉及用於減少皺紋和抗老化的藥物組合物,該組合物包含所述化學式(I)的聚乙二醇化7-脫氫膽固醇衍生物。
本發明的藥物組合物可通過口服(如,通過口部或吸入服用)或腸胃外(如,注射給藥、透皮吸收給藥、直腸給藥)途徑進行給藥,且所述注射可以為靜脈注射、皮下注射、肌內注射和腹腔注射。本發明的藥物組合物可被製成片劑、膠囊劑、顆粒劑、細字幕(fine subtilae)、粉劑、舌下表、栓劑、軟膏、注射劑、乳劑、懸浮液、糖漿、噴霧劑等。本發明的藥物組合物的這些各類劑型可根據已知方法通過使用本領域常用的藥學上可接受的載體進行製備。所述藥學上可接受的載體的例子可包括賦形劑、粘合劑、崩解劑、潤滑劑、防腐劑、抗氧劑、等滲劑、緩衝劑、包衣劑、甜味劑、增溶劑、鹼、分散劑、潤溼劑、懸浮劑、穩定劑、著色劑等。
儘管根據劑型的種類會有所不同,本發明的藥物組合物包含約0.1-10wt%,優選為0.1-1wt%的量的化學式(I)的聚乙二醇化7-脫氫膽固醇衍生物。
本發明的藥物組合物的具體劑量可根據待治療的包括人在內的哺乳動物的分類、體重、性別、疾病的嚴重程度、醫囑等來確定。優選地,基於受試者體重60公斤,用於口服的每日劑量可以在5-60μg的範圍內。所述總的每日劑量可以根據疾病的嚴重程度、醫囑和其他條件進行一次給藥或分幾次給藥。
此外,本發明涉及用於減少皺紋和抗老化的功能食品,該功能食品包含所述化學式(I)的聚乙二醇化7-脫氫膽固醇衍生物。
本發明的功能食品的種類不受特別限制。例如,所述功能食品可以為口服劑型,如粉末、顆粒劑、片劑、膠囊劑、懸浮液、乳液、糖漿,或者所述功能食品可被添加到如糖果、餅乾、口香糖、冰淇淋、麵條、麵包、飲料的通常食品內。
本發明的功能食品可以根據其形式通過常用方法進行製備,且所述功能食品可適當地包含可被接受為食品材料的載體,例如,填充劑、增量劑、粘合劑、潤溼劑、崩解劑、甜味劑、調味劑、防腐劑、表面活性劑、潤滑劑、賦形劑等。
儘管根據所述功能食品的種類會有所不同,所述功能食品可包含約0.0001-10wt%,優選為0.1-1wt%的量的化學式(I)的聚乙二醇化7-脫氫膽固醇衍生物。
有益效果
本發明的聚乙二醇化7-脫氫膽固醇衍生物具有得到改善的穩定性和水中溶解度,且表現出減少的毒性。
因此,本發明的聚乙二醇化7-脫氫膽固醇衍生物可有效地用作用於減少皺紋和抗老化的化妝品組合物、藥物組合物和功能食品中供應維生素D的良好來源。
此外,本發明的聚乙二醇化7-脫氫膽固醇衍生物可被各種體內酶轉化成活性維生素D,從而能持續地提供如抗氧化、減少皺紋和美白的生物活性。
附圖說明
圖1為展示了實施例1的化合物(MP350DHC)和作為對比化合物的7-脫氫膽固醇(DHC)在恆溫40℃下的熱穩定性的圖。
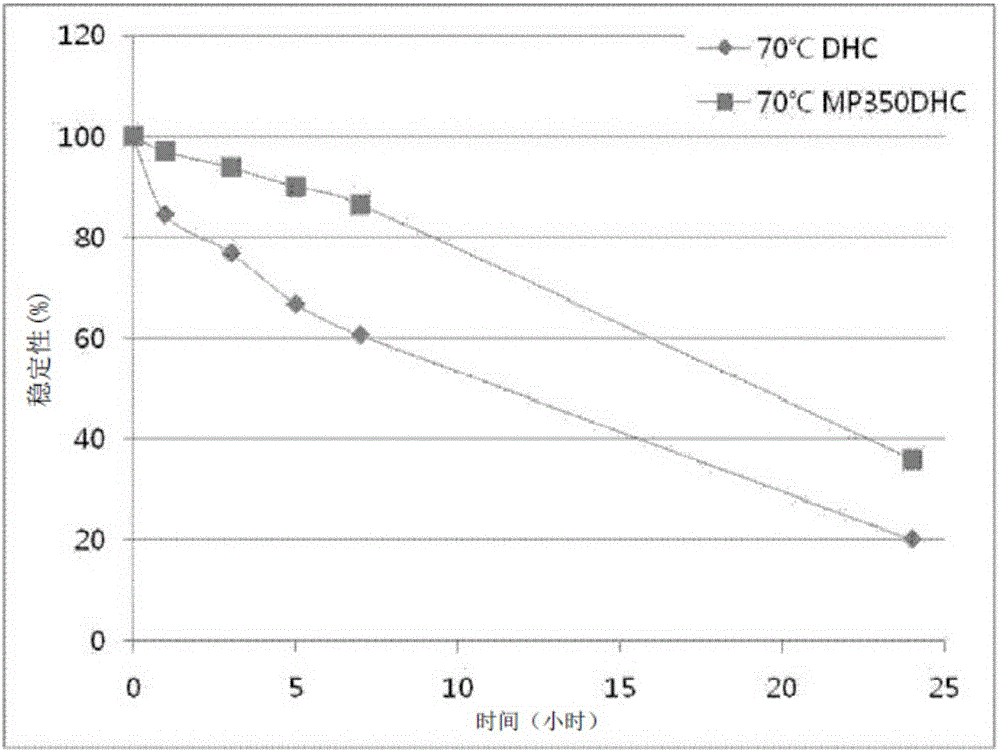
圖2為展示了實施例1的化合物(MP350DHC)和作為對比化合物的7-脫氫膽固醇(DHC)在恆溫70℃下的熱穩定性的圖。
圖3為展示了實施例1的化合物(MP350DHC)和作為對比化合物的7-脫氫膽固醇(DHC)的光穩定性的圖。
具體實施方式
通過以下實施例,進一步說明本發明,但不會限制本發明的範圍。
實施例1:mPEG350-S-DHC酯的製備(化學式(1A)的化合物,其中R為甲基,X為O,n為7.25(平均值),且m為1)
實施例1-1:7-脫氫膽固醇琥珀酸酯的製備(化合式(5)的化合物,其中m為1)
在120ml二氯甲烷內溶解化學式(4)的7-脫氫膽固醇(DHC)(6.45g,16.8mmol),其中加入三乙胺(3.39g,33.5mmol)和4-二甲氨基吡啶(0.82g,6.7mmol)而獲得溶液。其中,加入琥珀酸酐(化合式(3)的化合物,其中m為1)(3.35g,33.5mmol),然後在室溫下攪拌12小時。所述反應溶液依次用3.5%HCl水溶液、飽和碳酸氫鈉水溶液和飽和氯化鈉水溶液進行清洗。然後,使所述有機相經過無水硫酸鎂乾燥,過濾,減壓濃縮。將殘留物用矽膠柱層析(乙酸乙酯:己烷=1:2)進行提純,而獲得7.2g目標化合物。
1H NMR 400MHz(CDCl3)δ5.59(dd,1H),5.41(dd,1H),4.75(m,1H),2.72(dt,2H),2.64(dt,2H),2.52(d,1H),2.39(t,1H),2.18-1.85(m,6H),1.82-1.50(m,6H),1.48-0.93(m,11H),0.97(s,6H),0.90(d,3H),0.89(d,3H)0.64(s,3H)。
實施例1-2:mPEG350-S-DHC酯的製備(化學式(1A)的化合物,其中R為甲基,X為O,n為7.25(平均值),且m為1)
在10ml二氯甲烷內溶解實施例1-1的7-脫氫膽固醇琥珀酸酯(化學式(5)的化合物,其中m為1)(1.1g,2.30mmol)和mPEG350-OH(化學式(6)的化合物,其中R為甲基,n為7.25(平均值),且X為O)(0.8g,2.30mmol),向其中加入4-二甲氨基吡啶(0.42g,3.44mmol)。其中,緩緩加入N-(3-二甲基氨基丙基)-N'-乙基-碳二亞胺(0.88g,4.59mmol),然後在室溫下攪拌12小時。所述反應溶液依次用1.0N的HCl水溶液、飽和碳酸氫鈉水溶液和飽和氯化鈉水溶液進行清洗。然後,使所述有機相經過無水硫酸鎂乾燥,過濾,減壓濃縮,並真空乾燥,而獲得1.77g目標化合物。
1H NMR 400MHz(CDCl3)δ5.59(dd,1H),5.40(dd,1H),4.74(m,1H),4.27(t,2H),3.72(t,2H),3.67(PEG backbone),3.57(t,2H),3.40(s,3H),2.67(dt,2H),2.62(dt,2H),2.52(d,1H),2.38(t,1H),2.12-1.89(m,6H),1.75-1.53(m,6H),1.43-0.95(m,11H),0.97(s,6H),0.90(d,3H),0.88(d,3H)0.64(s,3H)。
實施例2:mPEG2K-S-DHC酯的製備(化學式(1A)的化合物,其中R為甲基,X為O,n為44.3(平均值),且m為1)
除了使用實施例1-1的7-脫氫膽固醇琥珀酸酯(82.8mg,0.22mmol)、mPEG2K-OH(化學式(6)的化合物,其中R為甲基,n為44.3(平均值),且X為O)(452mg,0.22mmol)、5ml二氯甲烷、4-二甲氨基吡啶(65.7mg,0.54mmol)和N-(3-二甲基氨基丙基)-N'-乙基-碳二亞胺(123.8mg,0.65mmol)之外,重複進行實施例1-2的過程,而獲得462mg目標化合物。
1H NMR 400MHz(CDCl3)δ5.57(m,1H),5.40(m,1H),4.72(m,1H),4.25(t,2H),3.83-3.45(PEG backbone),3.38(s,3H),2.70-2.56(m,5H),2.48(dt,1H),2.38(dt,1H),2.12-1.89(m,6H),1.75-1.53(m,6H),1.43-0.95(m,11H),0.95(s,6H),0.88(d,3H),0.84(d,3H)0.62(s,3H)。
實施例3:mTrEG-S-DHC酯的製備(化學式(1A)的化合物,其中R為甲基,X為O,n為3,且m為1)
在8ml二氯甲烷內溶解化學式(4)的7-脫氫膽固醇(0.54g,1.40mmol)和甲氧基三乙二醇琥珀酸酯(化學式(7a)的化合物,其中R為甲基,n為3,X為O,且m為1;mTrEG-琥珀酸)(0.37g,1.40mmol),向其中加入4-二甲氨基吡啶(0.26g,2.11mmol)。其中,緩緩加入N-(3-二甲基氨基丙基)-N'-乙基-碳二亞胺(0.67g,3.51mmol),然後在室溫下攪拌12小時。所述反應溶液依次用1.0N的HCl水溶液、飽和碳酸氫鈉水溶液和飽和氯化鈉水溶液進行清洗。然後,使所述有機相經過無水硫酸鎂乾燥,過濾,減壓濃縮,並真空乾燥,而獲得0.69g目標化合物。
1H NMR 400MHz(CDCl3)δ5.58(dd,1H),5.40(dd,1H),4.74(m,1H),4.28(t,2H),3.72(t,2H),3.68(m,6H),3.59(t,2H),3.40(s,3H),2.65(m,4H),2.52(dd,1H),2.39(t,1H),2.12-1.89(m,6H),1.75-1.53(m,6H),1.43-0.95(m,11H),0.97(s,6H),0.90(d,3H),0.88(d,3H)0.64(s,3H)。
實施例4:mPEG350-S-DHC醯胺的製備(化學式(1A)的化合物,其中R為甲基,X為NH,n為7.25(平均值),且m為1)
在6ml二氯甲烷內溶解實施例1-1中獲得的7-脫氫膽固醇琥珀酸酯(346.2mg,0.714mmol)和mPEG350-NH2(化學式(6)的化合物,其中R為甲基,n為7.25(平均值),且X為NH;平均分子量為350)(250mg,0.714mmol),向其中加入4-二甲氨基吡啶(87.3mg,0.714mmol)。其中,緩緩加入N-(3-二甲基氨基丙基)-N'-乙基-碳二亞胺(410.8g,2.14mmol),然後在室溫下攪拌12小時。所述反應溶液依次用1.0N的HCl水溶液、飽和碳酸氫鈉水溶液和飽和氯化鈉水溶液進行清洗。然後,使所述有機相經過無水硫酸鎂乾燥,過濾,減壓濃縮,並真空乾燥,而獲得508mg目標化合物。
1H NMR 400MHz(CDCl3)δ6.35(s,1H),5.57(dd,1H),5.39(dd,1H),4.72(m,1H),3.66(PEG back-bone),3.47(t,2H),3.39(s,3H),2.65(dt,2H),2.48(d,1H),2.37(t,1H),2.08-1.89(m,6H),1.74-1.50(m,6H),1.42-0.96(m,11H),0.96(s,6H),0.88(d,3H),0.87(s,3H),0.63(s,3H)。
實施例5:mPEG2K-P-DHC的製備(化學式(1B)的化合物,其中R為甲基,X為NH,n為44.3(平均值),且m為1)
在100ml二氯甲烷內溶解化學式(4)的7-脫氫膽固醇(0.32g,0.84mmol)和mPEG2K-丙酸(化學式(7b)的化合物,其中R為甲基,n為44.3(平均值),且m為1;平均分子量為2,000)(1.68g,0.84mmol),向其中加入4-二甲氨基吡啶(0.154g,1.26mmol)。其中,緩緩加入N-(3-二甲基氨基丙基)-N'-乙基-碳二亞胺(0.322g,1.68mmol),然後在室溫下攪拌12小時。所述反應溶液依次用1.0N的HCl水溶液、飽和碳酸氫鈉水溶液和飽和氯化鈉水溶液進行清洗。然後,使所述有機相經過無水硫酸鎂乾燥,過濾,減壓濃縮,並真空乾燥,而獲得1.57g目標化合物。
1H NMR 400MHz(CDCl3)δ5.58(m,1H),5.40(m,1H),4.74(m,1H),3.84-3.47(PEG backbone),3.39(s,3H),2.67(dt,2H),2.60(dt,2H),2.52(d,1H),2.38(t,1H),2.12-1.89(m,6H),1.75-1.53(m,6H),1.43-0.95(m,11H),0.96(s,6H),0.89(d,3H),0.87(d,3H)0.63(s,3H)。
實施例6:mPEG2K-O-A-DHC的製備(化學式(2A)的化合物,其中R為甲基,X為O,n為44.3(平均值),且Y1為甲基)
實施例6-1:mPEG2K-NPC的製備(化學式(8)的化合物,其中R為甲基,X為O,n為44.3(平均值))
在120ml二氯甲烷內溶解乾燥的mPEG2K-OH(化學式(6)的化合物,其中R為甲基,n為44.3(平均值),且X為O)(30g,14.9mmol)而獲得溶液,向其中加入4-硝基苯基氯甲酸酯(12g,59.7mmol)和吡啶(5.9ml,74.6mmol),然後在室溫下攪拌20小時。所述反應溶液依次用150ml的1.0N HCl水溶液和150ml飽和氯化鈉水溶液進行清洗。然後,使所述有機相經過無水硫酸鎂乾燥,過濾和減壓濃縮。所得混合物在二乙醚內進行沉澱,而獲得33.5g的白色固體目標化合物。
實施例6-2:mPEG2K-Ala-OH的製備(化學式(10)的化合物,其中R為甲基,X為O,n為44.3(平均值),且Y1為甲基)
在100ml乙腈和60ml蒸餾水內溶解實施例6-1中獲得的mPEG2K-NPC(16g,7.2mmol),而獲得溶液。其中,加入H-Ala-OH(化學式(9)的化合物,其中Y1為甲基)(1.9g,21.7mmol)、二異丙基乙胺(1.5ml,21.7mmol),然後在室溫下攪拌8小時。所述反應溶液用300ml二氯甲烷進行提取後,依次用300ml的1.0N HCl水溶液和300ml飽和氯化鈉水溶液進行清洗。然後,使所述有機相經過無水硫酸鎂乾燥,過濾和減壓濃縮。所得混合物在二乙醚內進行沉澱,而獲得白色固體目標化合物(18.8g,36.4mmol)。
實施例6-3:mPEG2K-O-A-DHC的製備(化學式(2A)的化合物,其中R為甲基,X為O,n為44.3(平均值),且Y1為甲基)
在100ml二氯甲烷內溶解化學式(4)的7-脫氫膽固醇(0.2g,0.48mmol)和實施例6-2中獲得的mPEG2K-Ala-OH(0.10g,0.23mmol),向其中加入4-二甲氨基吡啶(0.14g,1.14mmol)。其中,緩緩加入N-(3-二甲基氨基丙基)-N'-乙基-碳二亞胺(0.2g,1.14mmol),然後在室溫下攪拌12小時。所述反應溶液依次用1.0N的HCl水溶液、飽和碳酸氫鈉水溶液和飽和氯化鈉水溶液進行清洗。然後,使所述有機相經過無水硫酸鎂乾燥,過濾,減壓濃縮,並真空乾燥,而獲得1.06g目標化合物。
1H NMR 400MHz(CDCl3)δ5.59(dd,1H),5.44(dd,1H),5.41(bs,1H),4.36(q,1H),4.22(t,2H),3.83(t,2H),3.77-3.52(PEG back-bone),3.48(t,2H),3.39(s,3H),2.80(dt,2H),2.55(d,2H),2.41(d,2H),2.19-1.77(m,6H),1.74-1.52(m,6H),1.43-1.08(m,11H),0.96(s,6H),0.89(d,3H),0.88(d,3H),0.63(s,3H)。
實施例7:mPEG2K-NH-A-DHC的製備(化學式(2B)的化合物,其中R為甲基,n為44.3(平均值),X為NH,Y1為甲基,且m為1)
實施例7-1:mPEG2K-NH-Ala-Fmoc的製備(化學式(13)的化合物,其中R為甲基,n為44.3(平均值),X為NH,Y1為甲基,且Zb為Fmoc)
在二甲基甲醯胺(DMF)內溶解mPEG2K-NH2(化學式(6)的化合物,其中R為甲基,n為44.3,且X為NH)(280mg,0.14mmol)、HOBt(94.6mg,0.70mmol)、二異丙基乙胺(90.5mg,0.70mmol)並攪拌10分鐘,獲得溶液。其中,加入通過混合Fmoc-Ala-OH(化學式(12)的化合物,其中Zb為Fmoc,Y1為甲基)(218.0mg,0.70mmol)和PyBOP(364.5mg,0.70mmol)並攪拌該混合物10分鐘而獲得的溶液,然後在室溫下攪拌5小時。所述反應溶液依次用150ml的1.0N HCl水溶液和150ml飽和氯化鈉水溶液進行清洗。然後,使所述有機相經過無水硫酸鎂乾燥,過濾和減壓濃縮。所得混合物在二乙醚進行沉澱,而獲得301.1mg的白色固體目標化合物。
實施例7-2:mPEG2K-NH-Ala-H的製備(化學式(14)的化合物,其中R為甲基,n為44.3(平均值),X為NH,且Y1為甲基)
在6ml含有25%哌啶的DMF溶液內溶解實施例7-1中獲得的mPEG2K-NH-Ala-Fmoc(300mg,0.13mmol),然後在室溫下攪拌3小時。所述反應溶液在100ml二乙醚內進行沉澱,而獲得0.26mg的白色固體目標化合物。
實施例7-3:mPEG2K-NH-A-DHC的製備(化學式(2B)的化合物,其中R為甲基,n為44.3(平均值),X為NH,Y1為甲基,且m為1)
在5ml二氯甲烷內溶解實施例1-1獲得的7-脫氫膽固醇琥珀酸酯(120mg,0.24mmol)和mPEG2K-NH-Ala-H(250mg,0.12mmol),向其中加入4-二甲氨基吡啶(17.7mg,0.14mmol)。其中,緩緩加入N-(3-二甲基氨基丙基)-N'-乙基-碳二亞胺(69.5mg,0.36mmol),然後在室溫下攪拌12小時。所述反應溶液依次用1.0N的HCl水溶液、飽和碳酸氫鈉水溶液和飽和氯化鈉水溶液進行清洗。然後,使所述有機相經過無水硫酸鎂乾燥,過濾,減壓濃縮,並真空乾燥,而獲得283mg目標化合物。
1H NMR 400MHz(CDCl3)δ5.59(dd,1H),5.44(m,3H),4.33(q,1H),4.23(m,1H),3.66(PEG backbone),3.48(t,2H),3.39(s,3H),2.72(dt,2H),2.64(dt,2H),2.52(d,1H),2.48(d,3H),2.39(t,1H),2.18-1.85(m,6H),1.82-1.50(m,6H),1.48-0.93(m,11H),0.97(s,6H),0.90(d,3H),0.89(d,3H)0.64(s,3H)。
實施例8:mPEG2K-P-Ala-DHC的製備(化學式(2C)的化合物,其中R為甲基,n為44.3(平均值),m為1,且Y1為甲基)
實施例8-1:mPEG2K-P-NHS的製備(化學式(15b)的化合物,其中R為甲基,n為44.3(平均值),m為1,且L為琥珀醯亞胺)
在7ml二氯甲烷內溶解mPEG-PA(化學式(7b)的化合物,其中R為甲基,n為44.3(平均值),且m為1)(1g,0.476mmol)。其中,加入N-羥基琥珀醯亞胺(0.27g,2.38mmol)、1-乙基-3-(3-二甲基氨基丙基)碳二亞胺(0.45g,2.38mmol)、二甲氨基吡啶(0.18g,1.198mmol),然後在室溫下攪拌5小時。所述反應溶液用100ml二氯甲烷進行提取後,依次用100ml的1.0N HCl水溶液和100ml飽和碳酸氫鈉水溶液和100ml飽和氯化鈉水溶液進行清洗。然後,使所述有機相經過無水硫酸鎂乾燥,過濾和減壓濃縮。使所得混合物在二乙醚進行沉澱,而獲得0.94g的白色固體目標化合物。
實施例8-2:mPEG2K-P-Ala-OH的製備(化學式(16)的化合物,其中R為甲基,n為44.3(平均值),m為1,且Y1為甲基)
在5ml二氯甲烷內溶解實施例8-1中獲得的mPEG2K-P-NHS(450mg,0.21mmol)而獲得溶液。將該溶液緩緩加入到在2.5ml二氯甲烷和2.5ml二甲基甲醯胺內溶解H-Ala-OH(92.4mg,1.04mmol)和三乙胺(115.5mg,1.14mmol)的溶液中,然後在室溫下攪拌3小時。所述反應溶液依次用1.0N HCl水溶液、飽和碳酸氫鈉水溶液和飽和氯化鈉水溶液進行清洗。然後,使所述有機相經過無水硫酸鎂乾燥,過濾,減壓濃縮,並真空乾燥,而獲得478mg目標化合物。
實施例8-3:mPEG2K-P-Ala-DHC的製備(化學式(2C)的化合物,其中R為甲基,n為44.3(平均值),m為1,且Y1為甲基)
在10ml二氯甲烷內溶解化學式(4)的7-脫氫膽固醇(90.4mg,0.24mmol)和實施例8-2中獲得的mPEG2K-P-Ala-OH(420mg,0.19mmol),向其中加入4-二甲氨基吡啶(35.9mg,0.29mmol)。其中,緩緩加入N-(3-二甲基氨基丙基)-N'-乙基-碳二亞胺(93.9mg,0.49mmol),然後在室溫下攪拌12小時。所述反應溶液依次用1.0N的HCl水溶液、飽和碳酸氫鈉水溶液和飽和氯化鈉水溶液進行清洗。然後,使所述有機相經過無水硫酸鎂乾燥,過濾,減壓濃縮,並真空乾燥,而獲得457mg目標化合物。
1H NMR 400MHz(CDCl3)δ5.59(dd,1H),5.44(m,3H),4.26(q,1H),4.23(m,1H),3.66(PEG backbone),3.39(s,3H),2.60(t,2H),2.52(d,1H),2.39(t,1H),2.18-1.85(m,6H),1.82-1.50(m,6H),1.50(d,3H),1.48-0.93(m,11H),0.97(s,6H),0.90(d,3H),0.89(d,3H)0.64(s,3H)。
實施例9:α-mPEG2K-NH-γ-mPEG2K-P-Dab-DHC的製備(化學式(2D)的化合物,其中R為甲基,n為44.3(平均值),X為NH,m和m′分別為1)
實施例9-1:α-mPEG2K-NH-Dab(tBoc)-Fmoc的製備(化學式(18)的化合物,其中R為甲基,n為44.3(平均值),X為NH,m′為1,Za為tBoc的保護基團,且Zb為Fmoc的保護基團)
除了使用mPEG2K-NH2(400mg,0.20mmol)、HOBt(135.2mg,1.00mmol)、二異丙基乙胺(129.3mg,1.00mmol)、Fmoc-Dab(tBoc)-OH(化學式(17)的化合物,其中m′為1,Za為tBoc的保護基團,且Zb為Fmoc的保護基團)(264.4mg,0.60mmol)、PyBOP(520.6mg,1.00mmol)和40ml的DMF之外,重複進行實施例7-1的過程,而獲得473mg的白色固體目標化合物。
實施例9-2:α-mPEG2K-NH-Dab-Fmoc的製備(化學式(19)的化合物,其中R為甲基,n為44.3(平均值),X為NH,m′為1,且Zb為Fmoc的保護基團)
在5ml二氯甲烷內溶解實施例9-1中獲得的α-mPEG2K-NH-Dab(tBoc)-Fmoc(450mg,0.47mmol)而獲得溶液。其中,加入5ml三氟乙酸,然後在室溫下攪拌3小時。所述反應溶液中加入50ml二氯甲烷後,依次用50ml飽和碳酸氫鈉水溶液和50ml飽和氯化鈉水溶液進行清洗。然後,使所述有機相經過無水硫酸鎂乾燥,過濾和減壓濃縮。使所得混合物在二乙醚進行沉澱,而獲得428mg的白色固體目標化合物。
實施例9-3:α-mPEG2K-NH-γ-mPEG2K-P-Dab-Fmoc的製備(化學式(20)的化合物,其中R為甲基,n為44.3(平均值),X為NH,m和m′分別為1,且Zb為Fmoc的保護基團)
在8ml二氯甲烷內溶解實施例9-2中獲得的α-mPEG2K-NH-Dab-Fmoc(420mg,0.18mmol),其中加入mPEG2K-PA(374.9mg,0.18mmol)、4-二甲氨基吡啶(33.2mg,0.27mmol)。其中,緩緩加入N-(3-二甲基氨基丙基)-N'-乙基-碳二亞胺(69.4mg,0.36mmol),然後在室溫下攪拌12小時。所述反應溶液依次用1.0N的HCl水溶液、飽和碳酸氫鈉水溶液和飽和氯化鈉水溶液進行清洗。然後,使所述有機相經過無水硫酸鎂乾燥,過濾,減壓濃縮,並真空乾燥,而獲得750mg目標化合物。
實施例9-4:α-mPEG2K-NH-γ-mPEG2K-P-Dab-H的製備(化學式(21)的化合物,其中R為甲基,n為44.3(平均值),X為NH,且m和m′分別為1)
在14ml含有25%哌啶的DMF溶液內溶解實施例9-3中獲得的α-mPEG2K-NH-γ-mPEG2K-P-Dab-Fmoc(700mg,0.16mmol),然後在室溫下攪拌3小時。使所述反應溶液在100ml二乙醚內進行沉澱,而獲得651mg的白色固體目標化合物。
實施例9-5:α-mPEG2K-NH-γ-mPEG2K-P-Dab-DHC的製備(化學式(2D)的化合物,其中R為甲基,n為44.3(平均值),X為NH,且m和m′分別為1)
除了在10ml二氯甲烷內溶解實施例1-1中獲得的7-脫氫膽固醇琥珀酸酯(64.2mg,0.13mmol)和實施例9-4中獲得的α-mPEG2K-NH-γ-mPEG2K-P-Dab-H(550mg,0.13mmol),向其中加入4-二甲氨基吡啶(24.3mg,0.20mmol),然後使用N-(3-二甲基氨基丙基)-N'-乙基-碳二亞胺(50.8mg,0.26mmol)之外,重複進行實施例7-3的過程,而獲得587mg目標化合物。
1H NMR 400MHz(CDCl3)δ5.74(m,2H),5.59(d,1H),5.44(m,2H),4.35(m,1H),4.23(m,3H),3.84-3.66(PEG back-bone),3.57(m,6H),3.48(t,2H),3.39(s,6H),2.72(dt,2H),2.64(dt,2H),2.62(t,2H),2.53-2.39(m,4H),2.20-1.52(m,16H),1.41-1.06(m,11H),0.96(s,6H),0.89(d,3H),0.88(d,3H),0.63(s,3H)。
實施例10:α-mPEG2K-γ-mPEG2K-P-Dab-DHC的製備(化學式(2E)的化合物,其中R為甲基,n為44.3(平均值),X為O,m和m′分別為1)
實施例10-1:mPEG2K-Dab(tBoc)-OH的製備(化學式(23)的化合物,其中R為甲基,n為44.3(平均值),X為O,m′為1,且Za為tBoc)
除了使用將實施例6-1中獲得的mPEG2K-NPC(2g,0.91mmol)溶解於15ml乙腈和10ml蒸餾水中而獲得的溶液、H-Dab(tBoc)-OH(化學式(22)的化合物,其中m′為1,Za為tBoc)(0.59g,2.72mmol)和二異丙基乙胺(0.46ml,2.72mmol)之外,重複進行實施例6-2的過程,而獲得1.67g目標化合物。
實施例10-2:mPEG2K-Dab-OH的製備(化學式(24)的化合物,其中R為甲基,n為44.3(平均值),X為O,且m′為1)
除了在10ml二氯甲烷中溶解實施例10-1中獲得的mPEG2K-Dab(tBoc)-OH(1g,0.47mmol)並在其中加入三氟乙酸(10ml,0.13mmol)之外,重複進行實施例9-2的過程,而獲得0.76g目標化合物。
實施例10-3:α-mPEG2K-γ-mPEG2K-P-Dab-OH的製備(化學式(25b)的化合物,其中R為甲基,n為44.3(平均值),X為O,且m和m′分別為1)
在5ml二氯甲烷內溶解實施例10-2中獲得的mPEG2K-Dab-OH(0.34g,0.16mmol)和實施例8-1中獲得的mPEG2K-P-NHS(0.35g,0.16mmol),而獲得溶液。其中,加入87μl三乙胺,然後在室溫下攪拌12小時。所述反應溶液中加入100ml二氯甲烷後,依次用100ml的1.0N HCl水溶液和100ml飽和氯化鈉水溶液進行清洗。然後,使所述有機相經過無水硫酸鎂乾燥,過濾和減壓濃縮。使所得混合物在二乙醚進行沉澱,而獲得0.54g的白色固體目標化合物。
實施例10-4:α-mPEG2K-γ-mPEG2K-P-Dab-DHC的製備(化學式(2E)的化合物,其中R為甲基,n為44.3(平均值),X為O,且m和m′分別為1)
在50ml二氯甲烷內溶解化學式(4)的7-脫氫膽固醇(38.0mg,0.098mmol)和實施例10-3中獲得的α-mPEG2K-γ-mPEG2K-P-Dab-OH(0.10g,0.049mmol),向其中加入4-二甲氨基吡啶(6.0mg,0.247mmol)。其中,緩緩加入N-(3-二甲基氨基丙基)-N'-乙基-碳二亞胺(95mg,0.494mmol),然後在室溫下攪拌12小時。所述反應溶液依次用1.0N的HCl水溶液、飽和碳酸氫鈉水溶液和飽和氯化鈉水溶液進行清洗。然後,使所述有機相經過無水硫酸鎂乾燥,過濾,減壓濃縮,並真空乾燥,而獲得0.48g目標化合物。
1H NMR 400MHz(CDCl3)δ6.85(bs,1H),5.74(m,1H),5.59(d,1H),5.32(d,1H),4.35(m,1H),4.23(m,3H),3.84-3.66(PEG back-bone),3.49(t,2H),3.39(s,6H),2.53-2.39(m,4H),2.20-1.52(m,8H),1.41-1.06(m,11H),0.96(s,6H),0.89(d,3H),0.88(d,3H),0.63(s,3H)。
實施例11:α-mPEG5K-γ-mPEG5K-S-Dab-DHC的製備(化學式(2F)的化合物,其中R為甲基,n為113.0(平均值),X為O,m和m′分別為1)
實施例11-1:mPEG5K-S-NHS的製備(化學式(15a)的化合物,其中R為甲基,n為113.0(平均值),X為O,m為1,且L為NHS)
除了使用mPEG5K-SA(化學式(7a)的化合物,其中R為甲基,n為113.0(平均值),X為O,且m為1)(1.0g,0.20mmol)、N-羥基琥珀醯亞胺(0.16g,1.4mmol)、二甲氨基吡啶(73mg,0.6mmol)、1-乙基-3-(3-二甲基氨基丙基)碳二亞胺(0.27g,1.4mmol)和7ml二氯甲烷之外,重複進行實施例8-1的過程,而獲得0.93g的白色固體目標化合物。
實施例11-2:mPEG5K-Dab(tBoc)-OH的製備(化學式(23)的化合物,其中R為甲基,n為113.0(平均值),X為O,m′為1,且Za為tBoc)
除了在10ml乙腈和10ml蒸餾水中溶解mPEG5K-NPC(2g,0.384mmol)並在其中加入H-Dab(tBoc)-OH(0.17g,0.768mmol)和二異丙基乙胺(0.2ml,1.15mmol)之外,重複進行實施例10-1的過程,而獲得1.7g目標化合物。
實施例11-3:mPEG5K-Dab-OH的製備(化學式(24)的化合物,其中R為甲基,n為113.0(平均值),X為O,且m′為1)
除了使用實施例11-2中獲得的mPEG5K-Dab(tBoc)-OH(1.3g,0.254mmol)、13ml三氟乙酸和13ml二氯甲烷之外,重複進行實施例9-2的過程,而獲得1.2g目標化合物。
實施例11-4:α-mPEG5K-γ-mPEG5K-S-Dab-OH的製備(化學式(25a)的化合物,其中R為甲基,n為113.0(平均值),X為O,且m和m′分別為1)
在15ml二氯甲烷內溶解實施例11-3中獲得的mPEG5K-Dab-OH(0.79g,0.15mmol)和實施例11-1中獲得的mPEG5K-S-NHS(0.8g,0.15mmol),而獲得溶液。其中,加入0.1ml三乙胺,然後在室溫下攪拌12小時。所述反應溶液中加入50ml二氯甲烷後,依次用50ml的1.0N HCl水溶液和50ml飽和氯化鈉水溶液進行清洗。然後,使所述有機相經過無水硫酸鎂乾燥,過濾和減壓濃縮。使所得混合物在二乙醚進行沉澱,而獲得1.35g的白色固體目標化合物。
實施例11-5:α-mPEG5K-γ-mPEG5K-S-Dab-DHC的製備(化學式(2F)的化合物,其中R為甲基,n為113.0(平均值),X為O,且m和m′分別為1)
在10ml二氯甲烷內溶解化學式(4)的7-脫氫膽固醇(38.0mg,0.098mmol)和實施例11-4中獲得的α-mPEG5K-γ-mPEG5K-S-Dab-OH(0.5g,0.049mmol),向其中加入4-二甲氨基吡啶(6.0mg,0.247mmol)。其中,緩緩加入N-(3-二甲基氨基丙基)-N'-乙基-碳二亞胺(95mg,0.494mmol),然後在室溫下攪拌12小時。所述反應溶液依次用1.0N的HCl水溶液、飽和碳酸氫鈉水溶液和飽和氯化鈉水溶液進行清洗。然後,使所述有機相經過無水硫酸鎂乾燥,過濾,減壓濃縮,並真空乾燥,而獲得0.49g目標化合物。
1H NMR 400MHz(CDCl3)δ6.79(bs,1H),5.69(m,1H),5.53(d,1H),5.30(d,1H),4.29(m,1H),4.17(m,3H),3.91-3.50(PEG backbone),3.45(t,4H),3.34(t,4H),3.34(s,6H),2.55-2.48(m,8H),2.1-1.62(m,14H),1.42-1.14(m,11H),0.95(s,6H),0.84(d,3H),0.82(d,3H),0.59(s,3H)。
實施例12:α-mPEG350-γ-DHC-Dab-DHC的製備(化學式(2G)的化合物,其中R為甲基,n為7.25(平均值),X為O,m和m′分別為1)
實施例12-1:mPEG350-NPC的製備(化學式(8)的化合物,其中R為甲基,X為O,且n為7.25(平均值))
在200ml二氯甲烷內溶解乾燥的mPEG350-OH(化學式(6)的化合物,其中R為甲基,n為7.25(平均值),且X為O)((15g,42.86mmol)而獲得溶液。其中,加入4-硝基苯基氯甲酸酯(12g,64.29mmol)和吡啶(5.0ml,64.29mmol),然後在室溫下攪拌16小時。所述反應溶液依次用150ml的1.0N HCl水溶液和150ml飽和氯化鈉水溶液進行清洗。然後,使所述有機相經過無水硫酸鎂乾燥,過濾和減壓濃縮。所得混合物用甲醇和二氯甲烷經過矽膠柱層析獲得18.8g的白色固體目標化合物。
實施例12-2:α-mPEG350-Dab(tBoc)-OH的製備(化學式(23)的化合物,其中R為甲基,X為O,n為7.25(平均值),m′為1,且Za為tBoc的保護基團)
除了使用使用將實施例12-1中獲得的mPEG350-NPC(1.0g,1.94mmol)溶解於20ml乙腈和20ml蒸餾水中而獲得的溶液和二異丙基乙胺(0.50g,3.88mmol)且使所得混合物經過矽膠柱層析之外,重複進行實施例6-2的過程,而獲得0.98g目標化合物。
實施例12-3:α-mPEG350-Dab(tBoc)-DHC的製備(化學式(26)的化合物,其中R為甲基,X為O,n為7.25(平均值),m′為1,且Za為tBoc的保護基團)
除了在10ml二氯甲烷內溶解化學式(4)的7-脫氫膽固醇(582.6mg,0.098mmol)和實施例12-2中獲得的α-mPEG350-Dab(tBoc)-OH(900mg,1.51mmol),其中加入4-二甲氨基吡啶(208.2mg,1.70mmol)並使用N-(3-二甲基氨基丙基)-N'-乙基-碳二亞胺(435.5mg,2.27mmol),然後使所得混合物經過矽膠柱層析之外,重複進行實施例6-3的過程,而獲得1.23g目標化合物。
實施例12-4:α-mPEG350-Dab-DHC的製備(化學式(27)的化合物,其中R為甲基,X為O,n為7.25(平均值),且m′為1)
除了加入將實施例12-3中獲得的α-mPEG350-Dab(tBoc)-DHC(250mg,0.26mmol)溶解於2.5ml二氯甲烷內而獲得的溶液和2.5ml三氟乙酸,並使所得混合物經過矽膠柱層析之外,重複進行實施例9-2的過程,而獲得194mg目標化合物。
實施例12-5:α-mPEG350-γ-DHC-Dab-DHC的製備(化學式(2G)的化合物,其中R為甲基,n為7.25(平均值),X為O,且m和m′分別為1)
除了在5ml二氯甲烷內溶解實施例1-1中獲得的7-脫氫膽固醇琥珀酸酯(56.3mg,0.12mmol)和實施例12-4中獲得的α-mPEG350-Dab-DHC(100mg,0.12mmol),其中加入4-二甲氨基吡啶(21.3mg,0.17mmol),然後使用N-(3-二甲基氨基丙基)-N'-乙基-碳二亞胺(44.5mg,0.23mmol)之外,重複進行實施例7-3的過程,而獲得141mg目標化合物。
1H NMR 400MHz(CDCl3)δ6.85(bs,1H),5.74(m,1H),5.59(d,2H),5.44(m,2H),4.35(t,2H),4.33(m,2H),4.22(m,1H),3.84-3.66(PEG back-bone),3.39(s,3H),2.72(dt,2H),2.64(dt,2H),2.53-2.39(m,6H),2.23-1.51(m,14H),1.41-1.06(m,22H),0.97(s,12H),0.88(d,6H),0.87(d,6H),0.63(s,6H)。
表1展示了在實施例1-12中獲得的本發明的聚乙二醇化7-脫氫膽固醇衍生物的化學結構。
【表1】
實驗實施例1:溶解度測試
在100ml蒸餾水中分別溶解100mg的實施例1和5的化合物及作為對比材料的7-脫氫膽固醇,然後在室溫下攪拌1小時。重複該過程,直到各化合物達到飽和,過濾那些沒有溶解的部分,而分別製備飽和水溶液。
然後,將所述飽和水溶液放入稱重空容器(A)內,進行稱重(B)。然後,所述容器內的飽和水溶液經過減壓濃縮和真空乾燥後,進行稱重(C)。根據以下方程式1,計算各溶液的溶解度,將其結果顯示於表2中。
【方程式1】
【表2】
從表2中可確認,與7-脫氫膽固醇相比,實施例1和5的聚乙二醇化7-脫氫膽固醇衍生物具有意想不到的優異的水中溶解度。
實驗實施例2:熱穩定性測試
將實施例1的化合物以10mM的濃度溶解於二甲基亞碸內,以製備溶液。作為對比材料,將7-脫氫膽固醇以10mM的濃度溶解於二甲基亞碸和甲醇(9:1)的混合液內,而製備另一溶液。將製備的溶液分成每組量為1.5ml的測試溶液,分別避光保存在恆溫40℃和70℃下。待經過一定時間後,將每組測試溶液用甲醇稀釋,而製備1mM的樣品。在以下條件下,分別用高效液相色譜法(HPLC)分析所述樣品。其結果在圖1和圖2中展示。
檢測儀:Agilent HPLC 1260
柱:C18(150×4.6mm/5um)
洗脫液:乙腈:甲醇=6:4
柱的溫度;30℃
解析度(%)=[Ctx/Ct0]×100(%)
Ct0=實施例1的溶液在0時的峰面積
Ctx=實施例1的溶液在X時的峰面積。
從圖1和圖2中可確定,與7-脫氫膽固醇相比,實施例1的聚乙二醇化7-脫氫膽固醇衍生物具有優異的熱穩定性。
實驗實施例3:光穩定性測試
將實施例1的化合物溶解於二甲基亞碸內,而製備實施例1的化合物的濃度為10mM的溶液。作為對比材料,將7-脫氫膽固醇溶解於二甲基亞碸和甲醇(9:1)的混合液內,而製備7-脫氫膽固醇的濃度為10mM的另一溶液。將製備的溶液分成小組而置於板孔內,每組150μl,然後曝光在紫外線(中波,315nm,寬度:12cm)。待經過一定時間後,將每組測試溶液用甲醇稀釋,而製備1mM的樣品。在以下條件下,分別用高效液相色譜法(HPLC)分析所述樣品。其結果在圖3中展示。
檢測儀:Agilent HPLC 1260
柱:C18(150×4.6mm/5um)
洗脫液:乙腈:甲醇=6:4
柱的溫度;30℃
解析度(%)=[Ctx/Ct0]×100(%)
Ct0=實施例1的溶液在0時的峰面積
Ctx=實施例1的溶液在X時的峰面積。
從圖3中可確定,實施例1的聚乙二醇化7-脫氫膽固醇衍生物與7-脫氫膽固醇相比具有優異的光穩定性。
